TUGAS KHUSUS
PRAKTEK KERJA PROFESI
FARMASI INDUSTRI
DI
LEMBAGA FARMASI ANGKATAN UDARA
Drs. ROOSTYAN EFFENDIE, Apt
BANDUNG
Disusun oleh
:
ZULFIKAR, S.Farm
073202111
FAKULTAS FARMASI
UNIVERSITAS SUMATERA UTARA
MEDAN
DI
LEMBAGA FARMASI ANGKATAN UDARA
Drs. ROOSTYAN EFFENDIE, Apt
BANDUNG
Disusun oleh
:
ZULFIKAR, S.Farm
073202111
FAKULTAS FARMASI
UNIVERSITAS SUMATERA UTARA
MEDAN
Lembar Pengesahan
LAPORAN PRAKTEK KERJA PROFESI
FARMASI INDUSTRI
Di
LEMBAGA FARMASI ANGKATAN UDARA
Drs. ROOSTYAN EFFENDIE, Apt
BANDUNG
Laporan ini disusun untuk melengkapi salah satu syarat untuk memperoleh gelar
apoteker pada Fakultas Farmasi Universitas Sumatera Utara Medan
Disusun oleh
:
ZULFIKAR,
S.Farm 073202111
LEMBAGA FARMASI ANGKATAN UDARA
Drs.ROOSTYAN EFFENDIE, Apt
BANDUNG
Pembimbing,
Drs. Akmal, M.Si., Apt
Mayor Kes NRP 527570
Mengetahui,
Kepala Lembaga Farmasi Angkatan Udara
Fakultas Farmasi
Drs. Roostyan Effendie, Apt Universitas Sumatera Utara
Dekan,
Puji syukur kehadirat Tuhan YME atas berkat dan rahmat-Nya kepada kita
sehingga kegiatan dan penyusunan laporan Praktek Kerja Lapangan di Lembaga
Farmasi Angkatan Udara Bandung, dapat berjalan dengan baik dan lancar.
Praktek Kerja Lapangan ini untuk memenuhi salah satu syarat guna mencapai
gelar Apoteker di Fakultas Farmasi Universitas Sumatera Utara. Praktek Kerja
Lapangan ini dilaksanakan untuk meningkatkan pemahaman tentang aspek industri
farmasi bagi mahasiswa profesi apoteker sehingga setelah lulus dan menjadi apoteker
mempunyai kompetensi yang mampu bersaing di dunia kerja.
Kami menyadari bahwa pelaksanaan Praktek Kerja Lapangan sampai
penyusunan laporan ini dapat terlaksana dengan lancar berkat kerjasama, bantuan,
pengarahan dan dukungan dari berbagai pihak, baik secara langsung maupun tidak
langsung. Oleh karena itu, pada kesempatan ini kami ingin menyampaikan terima
kasih kepada:
1. Kolonel Kes Drs. Purwanto Budi T., M.M selaku Kepala Lembaga Farmasi
Angkatan Udara Roostyan Effendie Bandung, yang telah memberikan kesempatan
kepada kami untuk melakukan Praktek Kerja Profesi Apoteker.
2. Bapak Prof. Dr. Sumadio Hadisahputra, Apt selaku Dekan Fakultas Farmasi USU
dan Bapak Drs. Wiryanto, M.Si., Apt. selaku Koordinator Program Pendidikan
Profesi Apoteker Fakultas Farmasi USU Medan yang telah memberikan fasilitas
dan saran kepada penulis.
3. Mayor Kes Drs. Akmal, M.Si., Apt., selaku pembimbing dari Lembaga Farmasi
Angkatan Udara Roostyan Effendie, Bandung.
5. Bapak Drs. Daniel Azali, Apt., selaku pembimbing yang dengan tulus, sabar dan
penuh perhatian telah membimbing dan mengarahkan penulis selama melakukan
latihan kerja profesi hingga selesainya penulisan laporan ini.
6. Segenap apoteker, staff dan karyawan Lembaga Farmasi Angkatan Udara yang
telah banyak memberikan bimbingan, dan masukan selama Pelatihan Program
Kerja Profesi Apoteker (PPKPA) di Lembaga Farmasi Angkatan Udara.
7. Segenap dosen, karyawan dan pengelola Program Profesi Apoteker Fakultas
Farmasi Universitas Sumatera Utara.
8. Orangtua serta saudara kami tercinta atas dukungan dan doa yang telah diberikan
kepada kami. Rekan-rekan Mahasiswa Program Profesi Apoteker Universitas
Sumatera Utara.
9. Semua pihak yang tidak dapat kami sebutkan satu per satu atas bantuan dan
dukungan yang diberikan, baik secara langsung maupun tidak.
Semoga Tuhan Yang Maha Esa akan selalu memberkati dan membalas semua
bantuan yang telah diberikan kepada kami. Kami sadar bahwa Laporan PKL ini masih
jauh dari sempurna dikarenakan keterbatasan pengetahuan dan pengalaman dari kami.
Oleh karena itu kami sangat mengharapkan adanya kritik dan saran yang membangun
dari semua pihak. Dengan segala kerendahan hati , semoga laporan PKL ini dapat
bermanfaat bagi Almamater dan mahasiswa seprofesi serta sejawat
Bandung, Februari 2008
Halaman
JUDUL ... i
LEMBAR PENGESAHAN ... ii
KATA PENGANTAR... iii
DAFTAR ISI ... iv
DAFTAR LAMPIRAN ... vi
BAB I PENDAHULUAN ... 1
1.1. Latar belakang ... 1
1.2. Tujuan Latihan Kerja Profesi ... 3
BAB II TINJAUAN PUSTAKA ... 4
2.1. Sistem Manajemen Mutu ... 4
2.2. Sumber Daya Manusia ... 5
2.3. Bangunan ... 6
2.4. Peralatan ... 9
2.5. Sanitasi dan Higiene ... 10
2.6. Produksi... 11
2.7. Pengawasan Mutu ... 12
2.8. Inspeksi Diri ... 13
2.9 Penanganan Keluhan Terhadap Obat, Penarikan Kembali Obat dan Obat
Kembalian ... 14
2.9.1. Keluhan dan Laporan ... 14
2.9.2. Penarikan Kembali Obat Jadi... 15
2.9.3. Obat Kembalian ... 15
2.10 Dokumentasi... 17
BAB III TINJAUAN UMUM LEMBAGA FARMASI ANGKATAN UDARA
18
3.1. Sejarah dan Perkembangan Lembaga Farmasi Ankatan Udara
Roostyan Effendie... 18
3.2. Kedudukan, Tugas, dan Kewajiban Lafiau ... 21
3.3. Visi, Misi, Dan Sasaran... 21
3.3.1 Visi dari LAFIAU adalah ... 21
anggaran dan masa depan adalah ...
22
3.4. Profil Lafiau... 22
3.4.1 Sumber Daya Manusia ... 22
3.4.2 Susunan Organisasi ... 23
3.4.2.1 Kalafiau... 23
3.4.2.2 Sekretaris Lafiau (Sesla) ... 24
3.4.2.3 Pelayanan dan Pegurusan Kas/Keuangan (Pekas)... 25
3.4.2.4
Bagian
Produksi... 25
3.4.2.5 Bagian Gudang Pusat Farmasi (Gupusfi) ... 26
3.4.2.6 Bagian Pengujian dan Pengembangan... 28
3.4.2.7
Bagian
Penunjangan ... 30
3.5. Lokasi gedung dan Sarana... 30
3.5.1 Lokasi Gedung ... 30
3.5.2 Sarana produksi... 30
3.5.3 Sarana gudang ... 32
BAB IV KEGIATAN LEMBAGA FARMASI ... 33
4.1. Perencanaan dan Pengadaan Perbekalan Kesehatan... 34
4.2. Unit Pergudangan ... 34
4.3. Gudang transit (Gutrans) ... 34
4.4. Gudang bahan jadi dan bahan baku (Guhanjabaku) ... 34
4.5. Gudang Peralatan Kesehatan (Gupalkes)... 35
4.6. Gudang penyaluran (Gulur)... 35
4.6.1
Penerimaan... 37
4.6.2
Penyimpanan... 38
4.6.3
Distribusi... 39
4.6.3.1 Rutin... 40
4.6.3.2 Non rutin ... 40
4.6.4
Penghapusan ... 41
4.6.5
Pelaporan ... 41
4.7. Unit Produksi Lembaga Farmasi Angkatan Udara ... 42
4.7.1 Tata Letak dan Klasifikasi Ruang Produksi ... 42
4.7.2
Produksi
Obat... 43
4.7.7
Pengawasan
Mutu ... 50
4.7.8 Sanitasi
dan Higiene ... 50
4.8. Produk ... 52
BAB V KEGIATAN KERJA PRAKTEK PROFESI APOTEKER
DILEMBAGA FARMASI ANGKATAN UDARA... 53
5.1. Bagian Pengujian dan Pengembangan (Ujibang) ... 53
5.1.1 Pengenalan Bagian Pengujian dan Pengembangan (Ujibang) ... 53
5.1.2 Pengembangan Formula Granul Effervescent ... 54
5.2. Bagian Gudang Pusat Farmasi... 54
5.3. Bagian Produksi... 56
5.3.1
Produksi
Non-betalaktam ... 56
5.3.2
Produksi
Betalaktam... 64
BAB VI PEMBAHASAN ... 66
6.1. Personalia ... 67
6.2. Banguanan dan Fasilitas... 68
6.3. Peralatan ... 71
6.4. Sanitasi dan Higiene ... 71
6.5 Penanganan Terhadap Hasil Pengamatan Keluhan dan Penarikan
Kembali Obat yang Beredar ...
73
6.6 Bagian Produksi... 73
6.7 Bagian Pengawasan Mutu ... 74
6.8 Dokumentasi... 75
BAB VII. KESIMPULAN DAN SARAN ... 76
7.1 Kesimpulan... 76
7.2 Saran ... 77
DAFTAR LAMPIRAN
Halaman
Lampiran 1 Struktur Organisasi Lafiau ... 80
Lampiran 2 Struktur Jabatan Lafiau ... 81
Lampiran 3 Denah Bangunan LAFIAU ... 82
Lampiran 4 Daerah Ruang Produksi Sediaan Beta Laktam... 83
Lampiran 5 Denah Ruang Produksi Sediaan Non Beta Laktam ... 84
Lampiran 6 Alur Kegiatan Produksi Tablet ... 85
Lampiran 7 Alur Kegiatan Pembuatan Tablet Salut Gula... 86
Lampiran 8 Alur Kegiatan Produksi Kapsul ... 87
Lampiran 9 Alur Kegiatan Produksi Sirup... 88
Lampiran 10 Alur Kegiatan Produksi Salep... 89
Lampiran 11 Pengelolahan Limbah Cair ... 90
Lampiran 12 Alur Proses Penerimaan Obat Jadi dari Produksi ... 91
Lampiran 13 Alur Proses Pengeluaran Obat Jadi dan Alkes oleh Lafiau
Bandung... 92
Lampiran 14 Alur Alokasi Materil Kesehatan... 93
Lampiran 15 Alur Alokasi Proses Pengadaan dan Penerimaan Barang... 94
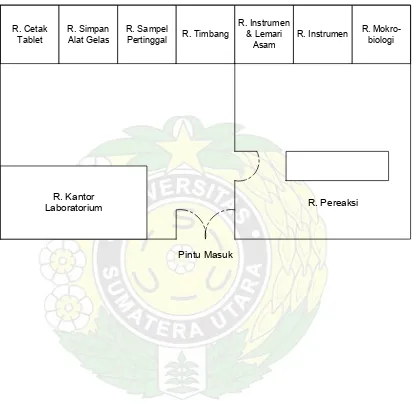
Lampiran 16 Denah Ruang Labolatorium ... 95
PENDAHULUAN
1.1 Latar Belakang
Pembangunan kesehatan merupakan salah satu bagian dari pembangunan
nasional. Tujuan pembangunan kesehatan adalah tercapainya kemampuan untuk
hidup sehat bagi setiap penduduk agar dapat mewujudkan derajat kesehatan yang
optimal, baik secara jasmani, rohani dan sosial sebagai salah satu unsur
kesejahteraan umum.
Dalam usaha mencapai tujuan pembangunan kesehatan dilakukan upaya
kesehatan dan salah satu sarana dalam melaksanakan upaya kesehatan adalah
industri farmasi. Industri farmasi merupakan salah satu tempat dimana apoteker
melakukan pekerjaan kefarmasiaan terutama menyangkut pengadaan,
pengendalian mutu sediaan farmasi, penyimpanan, pendistribusian dan
pengembangan obat.
2
memenuhi persyaratan sesuai dengan tujuan penggunaan saat sampai ditangan
konsumen.
Sasaran utama industri farmasi adalah memproduksi obat jadi dengan
mengutamakan keamanan, keefektifan, kualitas dan harga yang terjangkau oleh
masyarakat. Untuk menghasilkan obat jadi yang memenuhi persyaratan yang telah
ditetapkan sesuai dengan tujuan penggunaannya, maka setiap industri farmasi
harus menerapkan Cara Pembuatan Obat yang Baik (CPOB), sedangkan harga
yang ekonomis dapat diperoleh dengan perbaikan efisiensi dan produktifitas.
1.2 Tujuan Praktek Kerja Lapangan
BAB II
TINJAUAN PUSTAKA
Industri farmasi diwajibkan menerapkan Cara Pembuatan Obat yang Baik
(CPOB). Hal ini didasarkan oleh Keputusan Menteri Kesehatan RI.
No.43/MENKES/SK/II/1988 tentang CPOB dan Keputusan Direktur Jenderal
Pengawasan Obat dan Makanan DepKes RI. No.04510/A/SK/XII/1989 tentang
Petunjuk Operasional Penerapan CPOB.
Cara Pembuatan Obat yang Baik menyangkut seluruh aspek produksi dan
pengendalian mutu yang bertujuan untuk menjamin bahwa produk obat yang
dibuat senantiasa memenuhi persyaratan mutu yang telah ditentukan sesuai tujuan
penggunaannya.
Pengawasan menyeluruh pada pembuatan obat sangat penting untuk
menjamin bahwa konsumen menerima obat yang bermutu tinggi. Tidak cukup
bila obat jadi hanya sekedar lolos dari serangkaian pengujian, tetapi sangat
penting bahwa mutu obat harus dibentuk dalam produk obat tersebut. Semua obat
hendaknya dibuat dalam kondisi yang dikendalikan dan dipantau. CPOB meliputi
beberapa hal pokok yang menjadi perhatian utama antara lain:
2.1 Sistem Manajemen Mutu
Dalam ketentuan umum, ada beberapa landasan yang penting untuk
diperhatikan, yaitu :
a. Pengawasan menyeluruh pada proses pembuatan obat untuk menjamin
bahwa konsumen menerima obat yang bermutu tinggi.
b. Mutu obat tergantung pada bahan awal, proses pembuatan dan
pengawasan mutu, bangunan, peralatan yang digunakan dan personalia.
c. Untuk menjamin mutu suatu obat jadi tidak boleh hanya mengandalkan
pada suatu pengujian tertentu saja, melainkan semua obat hendaknya
dibuat dalam kondisi terkendali dan terpadu dengan cermat.
CPOB merupakan pedoman yang dibuat untuk memastikan agar sifat dan
mutu obat yang dihasilkan sesuai dengan syarat bahwa standar mutu obat yang
telah ditentukan tetap tercapai.
2.2 Sumber Daya Manusia
Jumlah sumber daya manusia pada tiap tingkatan harus memadai dan
memiliki pengetahuan, keterampilan serta kemampuan sesuai dengan tugasnya.
Setiap karyawan juga harus memiliki kesehatan mental dan fisik yang baik,
sehingga mampu melaksanakan tugasnya secara profesional, memiliki sikap dan
kesadaran yang tinggi untuk mewujudkan CPOB.
6
Penanggung jawab produksi maupun penanggung jawab mutu hendaklah
seorang apoteker yang cakap, terlatih dan memiliki pengalaman praktis yang
memadai di bidang industri farmasi, sehingga memungkinkan pelaksanaan
tugasnya secara profesional. Untuk menunjang dan membantu tugasnya dapat
ditunjuk tenaga yang terampil dalam jumlah yang sesuai untuk melaksanakan
supervisi langsung dibagian produksi dan pengawasan mutu. Selain itu tersedia
juga tenaga yang terlatih secara teknis dalam jumlah yang memadai untuk
melaksanakan kegiatan produksi dan pengawasan mutu sesuai dengan prosedur
dan spesifikasi yang telah ditentukan.
Seluruh karyawan yang terlibat langsung dalam kegiatan pembuatan obat
diberikan pelatihan oleh tenaga yang kompeten mengenai tugasnya sesuai dengan
CPOB. Latihan dilakukan secara berkesinambungan dengan frekuensi yang
memadai serta menurut program yang tertulis yang telah disetujui penanggung
jawab produksi dan penanggung jawab pengawasan mutu.
2.3 Bangunan
Bangunan untuk pembuatan obat sebaiknya memiliki ukuran, rancangan,
kontruksi serta letak yang memadai agar memudahkan pelaksanaan kerja,
pembersihan dan pemeliharaan yang baik. Tiap sarana kerja hendaknya memadai
sehingga resiko terjadinya kekeliruan dan pencemaran silang dapat dicegah sedini
mungkin.
umum bagi karyawan. Rancang bangun dan penataan gedung harus memenuhi
persyaratan:
1. Mencegah resiko tercampurnya obat atau komponen obat yang berbeda.
2. Kegiatan pengolahan bahan bagi produk bukan obat dipisahkan dari
ruang produksi obat.
3. Ruang terpisah untuk membersihkan alat yang dapat
dipindah-pindahkan dan ruang untuk menyimpan bahan pembersih.
4. Kamar ganti pakaian berhubungan langsung dengan daerah produksi
tetapi letaknya terpisah.
5. Toilet tidak terbuka langsung ke daerah produksi dan dilengkapi
dengan ventilasi yang baik.
Lokasi bangunan hendaklah sedemikian rupa sehingga dapat mencegah
pencemaran lingkungan disekelilingnya seperti pencemaran udara, tanah dan air
maupun terhadap kegiatan di sekitarnya.
Permukaan bagian dalam ruangan seperti dinding, lantai dan langit-langit
sebaiknya licin, bebas keretakan dan sambungan terbuka serta mudah dibersihkan
dan didesinfeksi. Lantai di daerah pengolahan harus dibuat dari bahan kedap air,
permukaan rata dan memiliki permukaan yang mudah dicuci. Sudut-sudut antar
dinding, lantai dan langit-langit harus berbentuk lengkungan.
8
Bangunan harus mendapatkan penerangan yang cukup dan mempunyai
ventilasi dengan fasilitas pengendali udara termasuk pengaturan suhu dan
kelembaban untuk kegiatan dalam bangunan. Disamping itu tersedianya tenaga
listrik yang memadai akan menjamin kelancaran fungsi peralatan produksi dan
laboratorium.
Pintu yang menghubungkan ruangan produksi dan lingkungan luar seperti
pintu bahaya kebakaran hendaklah selalu ditutup rapat untuk mencegah masuknya
cemaran. Seluruh bangunan termasuk daerah produksi, laboratorium, gedung dan
koridor serta daerah sekeliling gudang hendaknya dirawat agar senantiasa bersih
dan rapi. Daerah penyimpanan barang harus cukup luas, terang serta tertata rapi
untuk memungkinkan penyimpanan bahan produk dalam keadaan bersih dan
teratur.
Untuk menjamin mutu obat dan kelangsungan produksi, maka penentuan
rancang bangun dan penataan gedung hendaklah dipertimbangkan kesesuaiannya
dengan kegiatan-kegiatan lain. Sehubungan dengan itu, maka daerah produksi
dibagi atas empat kelas:
dibuktikan dan divalidasi. Aliran udara searah berkecepatan lebih rendah
dapat digunakan pada isolator tertutup dan kotak bersarung tangan.
Kelas B : untuk pembuatan dan pengisian secara aseptik, kelas ini adalah
lingkungan latar belakang untuk zona kelas A.
Kelas C dan D : area bersih untuk melakukan tahap pembuatan produk
steril dengan tingkat resiko lebih rendah.
2.4 Peralatan
Peralatan yang digunakan dalam produksi obat sebaiknya memiliki
rancang bangun dan kontruksi yang tepat, ukuran yamg memadai serta
ditempatkan dengan tepat. Hal ini dimaksudkan agar tiap produk obat terjamin
keseragamannya dari tiap batch serta memudahkan pembersihan dan
perawatannya.
Permukaan peralatan yang bersentuhan dengan bahan baku, produk antara,
produk ruahan atau obat jadi tidak boleh bereaksi yang dapat mengubah identitas
mutu dan kemurniannya dari batas yang telah ditetapkan. Peralatan tidak boleh
menimbulkan akibat yang merugikan terhadap produk dan sebaiknya dapat
dibersihkan dengan mudah, baik bagian dalam maupun bagian luar. Bahan yang
diperlukan untuk tujuan khusus misalnya pelumas tidak boleh bersentuhan
langsung dengan bahan yang diolah.
10
Peralatan hendaknya dirawat menurut jadwal yang tepat agar tetap
berfungsi baik dan dapat mencegah terjadinya pencemaran yang dapat mengubah
identitas, mutu atau kemurnian produk. Prosedur-prosedur tertulis untuk
perawatan peralatan hendaknya dibuat dan digunakan.
2.5 Sanitasi dan Higiene
Ruang lingkup sanitasi dan higiene meliputi personalia, bangunan,
peralatan dan perlengkapan, bahan produksi serta wadahnya dan setiap hal yang
dapat menjadi sumber pencemaran produk. Sumber pencemaran dapat dihilangkan
melalui suatu program sanitasi dan higiene yang menyeluruh dan terpadu.
Semua karyawan yang berhubungan dengan pembuatan obat harus
memiliki kesehatan yang baik dan menggunakan pelindung badan dan penutup
rambut yang sesuai dengan tugas yang dilakukan, sehingga produk yang
dihasilkan dapat terhindar dari pencemaran oleh personal. Karena itu harus
dilakukan higiene perseorangan yang baik, khususnya pada saat penerimaan
karyawan baru.
Gedung yang digunakan untuk pembuatan obat harus dirancang dan
dibangun dengan tepat untuk memudahkan pelaksanaan sanitasi yang baik.
Disamping itu tersedia pula toilet dalam jumlah yang cukup dengan ventilasi yang
baik dan tempat cuci bagi karyawan yang letaknya mudah dicapai di daerah kerja,
serta fasilitas yang memadai untuk penyimpanan pakaian karyawan.
2.6 Produksi
Produksi harus dilaksanakan mengikuti prosedur yang telah ditetapkan
sehingga menjamin obat yang dihasilkan sesuai dengan spesifikasi yang telah
ditentukan.
Untuk bahan baku yang baru datang harus dikarantina sampai disetujui
dan diluluskan untuk digunakan oleh penanggung jawab pengawasan mutu.
Semua bahan awal yang tidak memenuhi persyaratan ditandai dengan jelas,
disimpan secara terpisah dan secepatnya dikembalikan ke supplier atau
dimusnahkan. Pencemaran kimiawi atau mikroba terhadap suatu obat yang dapat
merugikan kesehatan, mengurangi daya terapeutik atau mempengaruhi kualitas
suatu produk, tidak dapat diterima. Perhatian khusus harus diberikan pada
masalah pencemaran silang.
Suatu sistem yang menjabarkan cara penomoran batch dan lot secara rinci
diperlukan untuk memastikan bahwa produk dapat dikenali dari nomor lot atau
batch tertentu.
Setiap penimbangan atau pengukuran hendaknya dilakukan pembuktian
kebenaran, ketepatan identitas, dan jumlah bahan yang ditimbang dan diukur oleh
dua petugas secara terpisah. Bahan baku, produk antara, dan produk ruahan
hendaknya diperiksa ulang kebenarannya dan ditandatangani oleh supervisor
produksi sebelum diserahkan ke bagian produksi.
12
menghindari campur aduk antara produk. Tiap mesin hendaknya ditempatkan
dalam ruangan terpisah.
Terjadinya kesalahan dalam pengemasan dapat diperkecil dengan
pemakaian label gulungan, pemberian kode batch langsung pada jalur
pemasangan label, penggunaan alat pembacaan label, dan penghitung label
elektronik. Label dan barang cetak yang lain dirancang sedemikian rupa sehingga
memiliki tanda yang berbeda jelas terhadap produk yang berlainan. Disamping
pemeriksaan visual selama pengemasan berlangsung juga dilakukan pemeriksaan
secara terpisah oleh bagian pengawasan mutu setelah pengemasan. Produk yang
bentuk dan warnanya sama atau hampir sama tidak boleh dikemas pada jalur yang
berdampingan, kecuali ada pemisah secara fisik. Pada setiap jalur pengemasan,
nama dan nomor batch produk yang sedang dikemas hendaknya dapat terlihat
jelas.
Produk antara atau produk ruahan dapat diolah ulang asalkan bahan
tersebut layak untuk diolah ulang dengan prosedur tertentu yang disahkan, serta
hasilnya masih memenuhi persyaratan spesifikasi yang ditentukan.
Produk antara, produk ruahan, dan obat jadi hendaknya dikarantina sambil
menunggu hasil pemeriksaan dan keputusan dari bagian pengawasan mutu.
2.7 Pengawasan Mutu
Pengawasan mutu merupakan bagian yang penting dari CPOB agar tiap
obat yang dibuat memenuhi persyaratan mutu yang sesuai dengan tujuan
penggunaannya.
antara, produk ruahan, dan produk jadi. Disamping itu juga dilakukan program uji
stabilitas, pemantauan lingkungan kerja, validasi, dokumentasi suatu batch,
program penyimpanan contoh dan penyusunan serta sertifikasi yang berlaku dari
tiap bahan dan produk termasuk metode pengujiannya.
Bagian pengawasan mutu hendaknya memberikan bantuan yang
diperlukan atau mengambil bagian dalam pelaksanaan validasi berkala oleh
bagian lain, khususnya bagian produksi untuk menjamin bahwa tiap produk yang
dihasilkan selalu memenuhi spesifikasi yang telah ditetapkan.
2.8 Inspeksi Diri
Inspeksi diri bertujuan untuk melakukan penilaian apakah seluruh aspek
produksi dan pengendalian mutu selalu memenuhi CPOB. Program inspeksi diri
dirancang untuk mencari kelemahan dalam pelaksanaan CPOB dan untuk
menetapkan tindakan perbaikannya. Inspeksi diri harus dilakukan secara teratur
dan dibuat prosedur serta pencatatannya. Tindakan perbaikan yang disarankan
sebaiknya dilaksanakan. Untuk pelaksanaan inspeksi diri ditunjuk tim yang
mampu menilai secara objektif pelaksanaan CPOB.
Hal-hal yang diinspeksi meliputi karyawan, bangunan termasuk fasilitas
untuk karyawan, penyimpanan bahan awal dan obat jadi, peralatan, produksi,
pengawasan mutu, dokumentasi, serta pemeliharaan gedung dan peralatan.
14
2.9 Penanganan Keluhan Terhadap Obat, Penarikan Kembali Obat dan
Obat Kembalian
2.9.1. Keluhan dan Laporan
Keluhan dan laporan dapat menyangkut kualitas, efek samping yang
merugikan dan masalah medis lainnya. Keluhan dan laporan ditangani secara:
1. Hendaklah dibuat catatan tertulis mengenai semua keluhan dan laporan
yang diterima.
2. Keluhan dan laporan hendaklah ditangani oleh bagian yang bersangkutan
sesuai dengan jenis keluhan dan laporan yang diterima.
3. Terhadap tiap keluhan dan laporan dilakukan penelitian dan evaluasi
secara seksama, termasuk meninjau seluruh informasi yang masuk tentang
pemeriksaan atau pengujian terhadap contoh yang diterima. Bila perlu
dilakukan pemeriksaan terhadap contoh pertinggal batch yang
bersangkutan dan meneliti kembali semua data serta dokumentasi yang
berkaitan.
Tindak lanjut terhadap keluhan dan laporan:
1. Tindakan perbaikan yang diperlukan termasuk penarikan kembali batch
obat jadi atau seluruh obat jadi yang bersangkutan dan tindak lanjut
lainnya yang sesuai.
2.9.2. Penarikan Kembali Obat Jadi
Penarikan kembali obat jadi dapat berupa penarikan kembali satu atau
beberapa batch atau seluruh obat jadi tertentu dari semua mata rantai distribusi.
Penarikan kembali dilakukan apabila ditemukan adanya produk yang tidak
memenuhi persyaratan kualitas atau atas dasar pertimbangan adanya efek samping
yang tidak diperhitungkan yang merugikan kesehatan.
Penarikan kembali dapat dilakukan atas prakarsa produsen sendiri atau
instruksi instansi pemerintah yang berwenang. Keputusan untuk melakukan
penarikan kembali obat jadi adalah tanggung jawab apoteker penanggung jawab
pabrik dan pimpinan perusahaan. Penarikan kembali obat jadi dapat pula sekaligus
merupakan penghentian pembuatan obat jadi yang bersangkutan.
Pelaksanaan penarikan kembali obat jadi:
1. Tindakan penarikan kembali dilakukan segera setelah diketahui adanya
obat jadi yang tidak memenuhi persyaratan atau mempunyai efek samping
yang tidak diperhitungkan sebelumnya dan membahayakan kesehatan.
2. Obat jadi yang mempunyai resiko besar terhadap kesehatan selain tindakan
penarikan hendaklah segera diambil tindakan khusus agar obat yang
bersangkutan dikenakan embargo untuk tidak digunakan. Dalam hal ini
penarikan dilakukan sampai ke tingkat konsumen.
Sistem dokumentasi pabrik dapat mendukung pelaksanaan penarikan
kembali dan embargo secara efektif, cepat, dan tuntas.
2.9.3. Obat Kembalian
16
atau sebab lain mengenai kondisi obat, wadah, atau kemasan sehingga
menimbulkan keraguan akan keamanan, identitas, kualitas, dan kuantitas obat jadi
yang bersangkutan.
Pabrik hendaklah membuat prosedur untuk menahan, menyelidiki, dan
menganalisa obat yang dikembalikan, serta menetapkan apakah obat tersebut
dapat diproses kembali atau harus dimusnahkan. Terhadap obat kembalian
dilakukan evaluasi yang seksama untuk menentukan apakah obat jadi yang
bersangkutan dapat diolah kembali atau dimusnahkan.
Obat kembalian digolongkan sebagai berikut:
1. Obat kembalian yang masih memenuhi spesifikasi dan masih dapat
digunakan.
2. Obat kembalian yang masih dapat diolah ulang.
3. Obat kembalian yang tidak dapat diolah ulang.
Prosedur penanganan obat kembalian dibuat dengan memperhatikan
hal-hal berikut:
1. Jumlah dan identifikasi obat kembalian harus dicatat.
2. Obat kembalian yang diterima hendaklah dikarantina.
3. Terhadap obat kembalian dilakukan penelitian dan pemeriksaan oleh
bagian pengawasan mutu untuk menentukan tindak lanjut.
4. Keputusan untuk melakukan pengolahan obat kembalian hendaklah
dilakukan oleh pimpinan perusahaan atas dasar pertimbangan yang
seksama dan proses pengolahan harus diawasi secara ketat.
pencegahan pencemaran lingkungan dan mencegah kemungkinan jatuhnya obat
tersebut ke tangan orang yang tidak berwenang.
2.10 Dokumentasi
Dokumentasi pembuatan obat merupakan bagian dari sistem informasi
yang meliputi spesifikasi, prosedur, metode dan instruksi, catatan dan laporan,
serta jenis laporan lain yang ditentukan dalam perencanaan, pelaksanaan, dan
evaluasi seluruh rangkaian pembuatan obat.
Dokumentasi sangat penting untuk memastikan bahwa setiap petugas
mendapat instruksi secara terinci dan jelas mengenai bidang tugas yang harus
dilaksanakannya, sehingga memperkecil resiko terjadinya kekeliruan yang
biasanya timbul karena hanya mengandalkan komunikasi lisan.
BAB III
TINJAUAN UMUM LEMBAGA FARMASI
ANGKATAN UDARA
3.1. Sejarah dan Perkembangan Lembaga Farmasi Angkatan Udara
Roostyan Effendie
Perjalanan sejarah di mulai ketika di Pangkalan Udara belum mempunyai
satuan kesehatan, anggota AURI mendapatkan perawatan dan pengobatan di
poliklinik dan Rumah Sakit Angkatan Darat RI (ADRI). Untuk mengurangi
ketergantungan terhadap DKAD, maka pimpinan berusaha mencukupi kebutuhan
obat dan Alkes secara mandiri dengan mendirikan Apotek di Pangkalan Udara
ANDIR yang di pimpin oleh Lmu I Badris Nuch dan di Cililitan dipimpin oleh
Ramelan. Keberadaan Apotik tersebut mendorong Pimpinan untuk mendirikan
Depot obat guna mendukung Pelayanan Kesehatan dan Kegiatan Operasional
AURI. Periode Tahun 1951 sampai dengan !963 DOP di Pimpin oleh Lmu I Amir
Andjilin. Kiprahnya disamping tugas rutin juga turut serta mengirimkan personel
dan logistik dalam operasi Trikora.
Berdasarkan keputusan Panglima Angkatan Udara No. 5 tanggal 5 februari
1968, Puskalkes di kembangkan menjadi dua unit satuan yang masing-masing
berdiri sendiri yaitu Pusalkes dan Pusprodkes. Puskalkes bertugas melaksanakan
penerimaan, penyimpanan, penyaluran alat kesehatan, obat-obatan, bahan baku
dan embalage. Dipimpin oleh Mayor Far Drs. Soekarsono, Apt, di lanjutkan oleh
Mayor Dk Drs. Poedjiadi Soemodimedjo dan kemudian oleh Mayor Far Drs.
Amin Mustofa, Apt.
Pusprodkes bertugas melaksanakan produksi obat dengan bahan baku dan
embalage dari Puspalkes di Pimpin oleh Kapten Far Drs. Beatus Gunawan, Apt, di
lanjutkan oleh Mayor Far Drs Sartono, Apt, kemudian nama Pusprodkes berubah
menjadai Lembaga Farmasi Angkatan Udara (Lafiau). Pada tahun 1981 dan 1982
Lafiau di percaya melaksanakan pemeriksaan terhadap ransum tempur ABRI
dalam rangka Latgab dan HUT ABRI.
20
Saat ini Lafiau di pimpin oleh Kolonel Kes Drs Purwanto Budi.Apt. yang
dalam pengambilan kebijakannya tetap berpedoman pada kebijakan para
pendahulunya. Dengan selesainya pembangunan fasilitas produksi sefalosporin
berikut sarana penunjangnya, maka dilakukan pemenuhan persyaratan sertifikat
CPOB produk tersebut. Mengeluarkan tiga dari empat sertifikat CPOB yang
diajukan yaitu : sediaan tablet, kapsul dan syrup kering. Satu sertifikat CPOB
yang masih tertunda adalah untuk injeksi kering. Hal ini di sebabkan persyaratan
yang terus berkembang dan semakin ketat, sehingga perlu di lakukan pembenahan
fasilitas dan sarana penunjangnya.
Dalam mengemban peran Farmasi Militer di harapkan Lafiau tidak hanya
berorientasi kepada produk hanya, tetapi juga pada pelayanan kefarmasian
(Pharmaceutical Care), yang langsung menjangkau personel Angkatan Udara.
Dalam mengemban peran mencerdaskan bangsa, Lafiau aktif membimbing
mahasiswa praktek kerja dan tugas akhir di Lembaga ini, serta ikut menyusun
kurikulum dan mengirim personelnya sebagai dosen pada pendidikan D3 Farmasi
di Poltekkes Ciumbeleuit Bandung.
3.2. Kedudukan, Tugas, dan Kewajiban Lafiau
Lafiau adalah pelaksana teknis yang berkedudukan di bawah Dinas
Kesehatan Angkatan Udara (Diskesau). Lafiau bertugas membina kemampuan
dan pelaksanaan produksi obat jadi, pembekalan dan pengawasan kualitas dan
persyaratan teknis kefarmasian untuk melaksanakan dukungan dan pelayanan
kesehatan bagi anggota Angkatan Udara pada khususnya dan ABRI pada
umumnya. Dalam rangka melaksanakan tugasnya, Lafiau mempunyai kewajiban
sebagai berikut:
1. melaksanakan kegiatan produksi obat serta pengendalian mutu dari bekal
kesehatan Angkatan Udara,
2. melaksanakan penerimaan, penyimpanan, penyaluran, dan penghapusan bekal
kesehatan berdasarkan kebijaksanaan Diskesau,
3. melaksanakan pengawasan atas kualitas dan persyaratan teknis kefarmasian
bekal kesehatan dengan cara pengujian dan percobaan serta penelitian,
4. melaksanakan penelitian dan pengembangan di bidang farmasi.
3.3. Visi, Misi, Dan Sasaran
3.3.1 Visi dari Lafiau adalah :
Terpenuhinya obat berkualitas bagi anggota Angkatan Udara dan
keluarganya, berperan serta dalam pemenuhan kebutuhan obat nasional,
terlaksananya pembekalan matkes tepat waktu, tepat jumlah, tepat sasaran dan
aman serta tegaknya sistem manajemen mutu dalam kinerjanya.
3.3.2 Misi dari Lafiau adalah :
22
b. Melaksanakan pembekalan matkes mulai dari penerimaan, penyimpanan,
penyaluran, pencacahan dan penghapusan berdasarkan kebijaksanaan
Diskesau.
c. Melaksanakan pengawasan dan pemastian mutu matkes sesuai dengan
persyaratan teknis kefarmasian.
d. Melaksanakan penelitian dan pengembangan serta pendidikan dan pelatihan
dengan mengedepankan profesionalitas, efisien, efektif dan modern.
3.3.3 Sasaran yang hendak dicapai oleh Lafiau di tahun-tahun anggaran dan
masa depan adalah :
a) Mengajukan sertifikat CPOB untuk sediaan obat injeksi kering golongan
sefalosporin.
b) Menyiapkan produksi obat antibiotik golongan sefalosporin.
c) Melaksanakan revisi Vademicum Lafiau.
d) Melaksanakan kerjasama dengan berbagai instansi/lembaga farmasi
pemerintah dan swasta.
3.4. Profil Lafiau
3.4.1 Sumber Daya Manusia
Personel yang ada saat ini belum mencukupi jumlah yang diharapkan
karena ada beberapa personel yang merangkap tugas tetapi pada unit Produksi dan
unit Ujibang tidak terjadi perangkapan jabatan. Jumlah personel yang ada
sekarang sudah mampu menjalankan setiap tugas yang ada.
3.4.2 Susunan Organisasi
Organisasi di Lafiau tersusun dari tiga eselon, yaitu eselon pimpinan,
eselon pembantu pimpinan / staf dan eselon pelaksana. Eselon pimpinan yaitu
Kepala Lembaga Farmasi Angakatan Udara (Kalafiau) dan eselon pembantu
pimpinan/staf adalah Sektretaris Lembaga (Sesla), sedangkan eselon pelaksana
meliputi Kepala Bagian Produksi (Kabag Prod), Kepala Gudang Pusat Farmasi
(Kaguspusfi), Kepala Bagian Pengujian dan Pengembangan (Kabag Ujibang) dan
Kepala Bagian Penunjangan (Kabag Jang).
Pembagian tugas dan tanggung jawab dari masing-masing bagian adalah
sebagai berikut :
3.4.2.1 Kalafiau
Kalafiau adalah pelaksana teknis Diskesau yang bertanggung jawab
kepada Kadiskesau dalam hal pembinaan kemampuan dan pelaksanaan produksi
farmasi yang diperlukan oleh Angkatan Udara, perbekalan kesehatan yang
diperlukan bagi pelaksana dukungan dan pelayanan kesehatan Angkatan Udara
serta pengawas atas kualitas dan persyaratan teknis kefarmasian bekal kesehatan
Angkatan Udara. Kalafiau mempunyai tugas dan kewajiban sebagai berikut:
i.
melaksanakan bimbingan dan petunjuk teknis kegiatan produksi serta
24
ii. melaksanakan penerimaan, penyimpanan, penyaluran, dan penghapusan bekal
kesehatan berdasarkan kebijaksanaan Diskesau,
iii. melaksanakan pengawasan obat-obatan Angkatan Udara,
iv. melaksanakan pengawasan atas kualitas dan persyaratan teknis kefarmasian
bekal kesehatan dengan cara pengujian dan percobaan serta penelitian kualitas
kefarmasian,
v. melaksanakan penelitian dan pengembangan bidang farmasi.
3.4.2.2 Sekretaris Lafiau (Sesla)
Sekretaris Lafiau (Sesla) adalah pembantu staf Kalafiau dalam
menyelenggarakan perencanaan dan pengendalian pentahapan pelaksanaan
kegiatan produksi, perbekalan, serta program dan dukungan kegiatan Lafiau, yang
dalam pelaksanaannya dibantu oleh Bagian Program dan Anggaran, kepala
Pembina Profesi (Kabinprof), Kepala Tata Usaha dan Urusan Dalam (Kataud).
Sesla mempunyai tugas dan tanggung jawab sebagai berikut:
i.
menyusun dan menyiapkan kebijaksanaan dan perencanaan pentahapan
pelaksanaan dan kegiatan administrasi produksi dan perbekalan, pengendalian
produksi, dan pembekalan serta pembinaan personil,
ii. menyusun dan menyiapkan kebijaksanaan dan perencanaan pentahapan
pelaksanaan kegiatan program kerja dan anggaran, pengelolaan data kegiatan
serta mengembangkan dukungan materiil dan fasilitas,
3.4.2.3 Pelayanan dan Pegurusan Kas/Keuangan (Pekas)
Pekas adalah staf pembantu dan pelaksanan Kalafiau dalam bidang
pelayanan dan pengurusan keuangan. Pekas memiliki tugas dan kewajiban sebagai
berikut:
i.
menyelenggarakan penerimaan dan penyimpanan uang di kas dan di bank
serta pembayaran pada pihak ketiga atas dasar pengujian dokumen tagihan
yang sah,
ii. menyelenggarakan pengujian kualitatif dan kuantitatif atas segala dokumen
sebelum dilakukan pembayaran tagihan atau penerimaan uang,
iii. mengawasi, mengendalikan, mengevaluasi pelaksanaan pengurusan dan
pelayanan keuangan,
iv. mengadakan kerja sama dengan staf dan satuan yang ada di lingkungan Lafiau
untuk kepentingan tugasnya.
3.4.2.4 Bagian Produksi
Bagian produksi Lafiau adalah pembantu pelaksana Kalafiau
melaksanakan produksi bekal kesehatan. Bagian produksi dipimpin oleh Kepala
Bagian Produksi (Kabagprod) yang bertanggungjawab langsung kepada Kalafiau.
Kegiatan yang dilakukan bagian produksi dalam rangka menjalankan tugasnya
adalah :
i.
melaksanakan penerimaan dan penyimpanan bahan baku, bahan penolong dan
embalage dalam rangka persiapan proses produksi,
ii. menyiapkan alat pembantu produksi yang diperlukan dalam kegiatan produksi,
iii. menyiapkan bahan baku dan bahan penolong untuk proses selanjutnya,
26
v. melaksanakan kegiatan produksi sesuai kebijaksanaan Diskesau berdasarkan
surat perintah pelaksanaan produksi yang dikeluarkan oleh Kalafiau.
Bagian produksi dalam melaksanakan tugasnya dibantu oleh:
i.
Unit produksi tablet yang bertugas melaksanakan produk obat jadi dalam
bentuk tablet.
ii.
Unit produksi kapsul yang bertugas melaksanakan produksi obat jadi
dalam bentuk kapsul.
iii.
Unit produksi khusus yang bertugas melaksanakan produksi khusus,
seperti sirup, salep, cairan, antiseptik, tetes, dan lain-lain.
3.4.2.5 Bagian Gudang Pusat Farmasi (Gupusfi)
Gudang Pusat Farmasi dipimpin oleh Kaguspusfi yang
bertanggungjawab kepada Kalafiau. Kaguspusfi bertugas melaksanakan
penerimaan, penyimpanan, pemeliharaan, penyaluran serta penghapusan bekal
kesehatan. Dalam rangka pelaksanaan tugasnya Kaguspusfi melaksanakan
kegiatannya sebagai berikut:
a. Menerima, menyimpan, memelihara, menyalurkan bekal kesehatan sesuai
dengan ketentuan dan perintah Kadiskesau selaku ordonatur materiil
kesehatan
b. Mengajukan barang-barang yang akan dihapuskan sesuai ketentuan yang
berlaku
c. Melaksanakan pertanggungjawaban bekal kesehatan melalui laporan yang
berkala
Kaguspusfi dalam melaksanakan tugasnya dibantu oleh :
1). Kepala Unit Gudang Transit (Ka Unit Gutrans), unit ini bertugas menerima
alat kesehatan (alkes) dan perbekalan kesehatan (bekkes) dari hasil
pengadaan Dinas Pengadaan Angkatan Udara (Disadaau) dan obat jadi
dari bagian produksi Lafiau, bersama komite penerimaan barang
melaksanakan pemeriksaan terhadap alkes dan bekkes yang diterima dari
hasil pengadaan Disadaau dan obat jadi dari bagian produksi Lafiau,
menuangkan hasil pemeriksaan dalam berita acara pemeriksaan,
mengembalikan alkes dan bekkes yang tidak memenuhi persyaratan pada
kontrak jual beli kepada rekanan yang mengirimkan alkes dan bekkes,
mengirimkan hasil alkes dan bekkes serta bahan baku yang diterima dan
memenuhi syarat ke gudang Palkes dan Guhanjabaku.
2). Kepala unit gudang penyaluran dan pengemasan (Ka Unit Gulur), bertugas
melaksanakan pengemasan/penyiapan barang yang akan dikirim
berdasarkan Surat Perintah Kadiskesau selaku ordonatur materiil
kesehatan, mengusahakan angkutan darat dan udara melalui seksi
Angkatan Udara untuk mendukung kegiatan penyaluran, serta
melaksanakan kegiatan penyaluran barang pada satuan kerja dengan
kelengkapan administrasi melalui sarana yang tersedia.
28
pengkartuan serta penyimpanan dokumen yang berkaitan dengan
penerimaan dan pengeluaran barang.
4). Kepala unit gudang obat jadi, bahan baku,
embalage
(Ka Unit
guhanjabaku), bertugas menerima obat jadi, bahan baku,
embalage
dari
unit gudang transit sesuai dengan berita acara yang telah disahkan oleh
ordonatur, menyimpan, merawat/memelihara dan mengeluarkan barang
(obat jadi, bahan baku,
embalage).
sesuai dengan ketentuan dan peraturan yang berlaku, serta melaksanakan
administrasi pergudangan terhadap obat jadi, bahan baku,
embalage
yang
disimpan melalui pembukuan, pengkartuan dan penyimpanan dokumen
yang berkaitan dengan penerimaan dan pengeluaran barang.
3.4.2.6 Bagian Pengujian dan Pengembangan
Bagian Pengujian dan Pengembangan (Ujibang) adalah pembantu
pelaksana Kalafiau yang bertugas melaksanakan pengujian dan percobaan atas
kualitas bekal kesehatan, melaksanakan penelitian dan pengembangan untuk
meningkatkan hasil produksi obat jadi dan menyelenggarakan perencanaan serta
pelaksanaan pendidikan dan latihan. Bagian Uji Bang dipimpin oleh Kepala
Bagian Ujibang yang bertanggungjawab kepada Kalafiau.
Dalam pelaksanaan tugasnya Kabag Pengujian dan Pengembangan
melaksanakan kegiatan antara lain:
i. Pengujian terhadap bekal kesehatan berdasarkan persyaratan dan ketentuan
kefarmasian yang berlaku
iii. Melaksanakan penelitian dan pengembangan di bidang kefarmasian terutama
yang menghasilkan formula-formula baru dalam rangka meningkatkan hasil
produksi
iv. Pemantauan langsung dan tidak langsung bekal kesehatan yang disimpan baik
di gudang Lafiau maupun gudang satker (satuan kerja) kesehatan di
masing-masing pangkalan Angkatan Udara
v. Melaksanakan perencanaan dan penyelenggaraan pendidikan dan latihan
Kabag Pengujian dan Pengembangan dibantu oleh :
1). Kepala Unit Pengujian dan Percobaan (Ka Unit Uji Coba) yang bertugas
melaksanakan percobaan-percobaan dalam rangka perbaikan dan
pengembangan formula obat jadi yang sudah ada, melaksanakan
“In
Process Control”
dalam setiap tahap produksi, melaksanakan pengujian
terhadap kualitas obat jadi yang dihasilkan oleh Unit Produksi Lafiau,
melaksanakan pemantauan terhadap kualitas bekkes (bekal kesehatan)
yang disimpan di Unit gudang Lafiau dan di satker (satuan kerja)
kesehatan Angkatan Udara.
30
“retain sample” sebagai contoh pertinggal obat jadi yang diproduksi
Lafiau.
3). Kepala Unit Pendidikan dan Latihan (Ka Unit Diklat) yang bertugas
membuat perencanaan serta melaksanakan penyelenggaraan pendidikan
dan latihan.
3.4.2.7 Bagian Penunjangan
Bagian penunjangan adalah pembantu pelaksana Kalafiau yang dipimpin
oleh Kepala Bagian Penunjangan yang bertanggungjawab kepada Kalafiau.
Bagian Penunjangan bertugas mendukung kelancaran operasional Lafiau. Dalam
pelaksanaan tugasnya Bagian Penunjangan dibantu oleh :
1) Kepala Unit Penunjangan Material (Ka Unit Jangmat) bertugas mendukung
kelancaran operasional produksi dan pembekalan serta pengujian dan
pengembangan
2)
Kepala Unit Fasilitas dan Material (Ka Unit Harfasmat) bertugas
merencanakan dan menyelenggarakan pemeliharaan terhadap fasilitas dan
material dalam rangka mendukung kelancaran operasional Lafiau.
3.5. Lokasi gedung dan Sarana
3.5.1 Lokasi Gedung
Lembaga farmasi Angkatan Udara Roostyan Effendie berlokasi di Jl.
Nurtanio Utara Komplek Lapangan Udara Husein Sastranegara Bandung tepat di
belakang gedung Poliklinik dan gedung Pertemuan Graha Antariksa.
3.5.2 Sarana produksi
Lafiau memiliki tiga gedung yang terpisah, satu gedung sefalosporin, gedung beta
laktam yang digunakan untuk memproduksi antibiotik beta laktam dan gedung
non beta laktam. Semua ruangan produksi terpisah sesuai jenis produksinya, hal
ini untuk menghindari adanya kontaminasi silang antara produk beta laktam
dengan produk non beta laktam. Pada ruang produksi non beta laktam dirancang
berurutan sesuai dengan urutan proses produksi. Ruang produksi terdiri dari
gudang produksi, tempat ganti pakaian, laundry, penimbangan, granulasi,
pengeringan granul, pencetakan tablet, pengisian kapsul, produksi kapsul,
produksi salep, produksi sirup,
stripping,
ruang antara, ruang produk ruahan serta
ruang pencucian alat dan ruang kemas. Pada ruang produksi beta laktam
susunannya hampir sama dengan ruang produksi non beta laktam, namun pada
ruang antara sudah dilengkapi dengan
air shower
untuk membersihkan
partikel-partikel yang menempel pada baju khusus yang dikenakan personel.
Bagian dalam ruang produksi Lafiau baik dinding maupun lantai dibuat
licin dan tanpa sudut , hal ini ditujukan untuk mempermudah pembersihan. Lantai
bagian produksi dilapisi dengan epoksi sehingga lebih tahan goresan dan tidak
cepat terkelupas, kondisi seperti ini harus terus dijaga agar mutu produk tetap
terjamin.
32
3.5.3 Sarana gudang
KEGIATAN LEMBAGA FARMASI
4.1 Perencanaan dan Pengadaan Perbekalan Kesehatan
Pengadaan perbekalan kesehatan yang mengacu kepada Program Kerja.
Dinas Kesehatan Angkatan Udara (Diskesau) dan Pusat Kesehatan Angkatan
Udara (Puskesau), diajukan oleh Kalafiau kepada Kepala Dinas Kesehatan
Angkatan Udara (Kadiskesau) dengan pertimbangan seperti rencana produksi satu
tahun anggaran, persediaan perbekalan kesehatan dan kebutuhan satuan kerja.
Usulan dari Kalafiau akan dipertimbangkan dan dievaluasi lebih lanjut sesuai
dengan kebijaksanaan dan anggaran dari Diskesau.
Setelah melalui proses evaluasi, usulan pengadaan perbekalan Angkatan
Udara (Disadaau) oleh Diskesau. Disadaau akan mengadakan tender untuk
mencari rekanan yang dapat memenuhi barang-barang yang diusulkan. Rekanan
yang dicari harus memenuhi kualifikasi tertentu dan diutamakan
penanggungjawab rekanan tersebut adalah seorang militer untuk memudahkan
semua urusan. Setelah pemenang tender ditentukan, maka dilaksanakan
pengadaan barang oleh rekanan menurut kontrak jual beli. Kontrak jual beli
tersebut dapat digunakan untuk mengirimkan perbekalan farmasi.
4.2 Unit Pergudangan
Gupusfi atau Gudang Pusat Farmasi merupakan pembantu pelaksana
Kalafiau yang bertugas menerima, menyimpan, memelihara dan mengeluarkan
serta menghapus perbekalan kesehatan yang ada di Lafiau. Gupusfi dipimpin oleh
34
dibantu oleh unit gudang transit, unit gudang obat jadi dan bahan baku, unit
gudang peralatan kesehatan dan unit gudang penyaluran. Bangunan gudang terdiri
dari empat unit gedung, denah gudang dapat dilihat pada lampiran
4.3 Gudang transit (Gutrans)
Bekal kesehatan yang dikirim dari rekanan ke Lafiau akan diterima di
gudang transit untuk dikarantina menunggu pemeriksaan dari panitia penerimaan
barang selesai. Untuk bahan baku atau obat jadi yang diberi label kuning
(karantina) menandakan bahwa obat jadi atau bahan baku tersebut masih dalam uji
pemeriksaan laboratorium Ujibang.
4.4 Gudang bahan jadi dan bahan baku (Guhanjabaku)
Penyusunan barang digudang menggunakan sistem
First In First Out
(FIFO) dengan memperhatikan waktu masuknya barang dan tanggal
kadaluarsanya sehingga memungkinkan barang yang masuk lebih awal akan
dikeluarkan terlebih dahulu. Sehingga dapat dicegah rusaknya barang akibat
penyimpanan terlalu lama. Sedangkan untuk barang-barang yang waktu
kadaluarsanya singkat disusun menggunakan sistem
First Expired First Out
(FEFO).
4.5 Gudang Peralatan Kesehatan (Gupalkes)
Gupalkes di Lafiau merupakan salah satu gudang yang kedudukannya
berada di bawah bagian pergudangan Lafiau. Kegiatan penyimpanan dan
pengendalian peralatan kesehatan merupakan kelanjutan dari kegiatan penerimaan
peralatan kesehatan. Tujuan penyimpanan dan pengendalian peralatan kesehatan
ini adalah untuk memelihara mutu, menghindari penggunaan yang tidak
bertanggung jawab, menjaga kelangsungan persediaan, memudahkan pencarian
dan pengawasan serta menjaga keseimbangan antara persediaan dan penggunaan
peralatan kesehatan. Bekkes yang termasuk dalam kategori peralatan kesehatan
adalah barang, instrumen atau alat yang digunakan dalam pemeliharaan dan
peralatan kesehatan, diagnosa, penyembuhan dan pencegahan penyakit, kelainan
badan atau gejala yang terjadi pada manusia, dan tidak termasuk dalam golongan
obat.
4.6 Gudang penyaluran (Gulur)
Pengeluaran barang dari Gupalkes atau Guhanjabaku dan
embalage
dilakukan di Gulur setelah ada SPPB dari Kadiskesau kepada Kalafiau yang
36
oleh Satker. Bentuk 051 haruslah dipisahkan untuk setiap Satker dan dibuat
rangkap delapan untuk arsip Gupalkes, arsip Guhanjabaku dan
embalage
, arsip
Gulur, arsip Suburminbekkes sebelum bekkes dikirim, arsip Matfaskesau sebelum
bekkes dikirim, dan 3 rangkap dikirim bersama dengan bekkes dengan rincian
yaitu setelah ditandatangani penerima 1 rangkap arsip penerima, 1 rangkap dikirm
ke Matfaskesau sebagi bukti bekkes telah diterima, dan 1 rangkap dikirim kembali
ke Suburminbekkes Lafiau sebagai bukti bekkes telah diterima. Berdasarkan
bentuk 051, barang dikeluarkan dari Guhanjabaku dan
embalage
, serta Gupalkes
sebelum dikirim ke Satker akan disimpan di Gulur. Di Gulur ini barang akan
dikemas dan didistribusikan untuk Satker di seluruh Indonesia. Untuk Satker di
Pulau Jawa pengirimannya dapat menggunakan jasa angkutan darat sedangkan
untuk Satker di luar Pulau Jawa pengirimannya menggunakan armada udara milik
Angkatan Udara.
Kalafiau dapat mengeluarkan SPPB kepada Ka Unit Pergudangan setelah
menerima SPL dan bentuk 051 dari Kadiskesau. SPL mempunyai 2 jenis yaitu
Log A untuk obat-obatan dan Log B untuk peralatan kesehatan.
Tahap-tahap penyaluran Material Kesehatan :
i) Material Kesehatan diturunkan dari rak penyimpanan dan dicek sesuai
bentuk 40501 menyangkut jumlah dan nomor kodefikasinya.
ii) Material Kesehatan tersebut dikirimkan ke Gudang penyaluran oleh
petugas gudang penyimpanan dan diserahterimakan dengan petugas
gudang penyaluran sambil mengecek kembali jumlah dan nomor
iii) Material Kesehatan beserta daftar koli dimasukkan ke dalam kantong
plastk dan disegel, kemudian dimasukkan dalam dus ditutup, dilakban dan
diberi plat ezer. Material Kesehatan siap dikirim ke tempat tujuan melalui
darat dan udara.
4.6.1
Penerimaan
Anggota KPB berasal dari unit gudang, unit produksi dan unit litbang.
Panitia ini bertanggungjawab kepada Kadiskesau dan dibentuk setahun sekali.
Perbekalan kesehatan yang dikirimkan ke Lafiau diterima oleh Panitia Penerimaan
Barang (PPB). Semua barang yang diterima oleh Lafiau harus diperiksa, dan
selama menunggu pemeriksaan, barang-barang tersebut diletakkan dalam gudang
transit. Gudang transit merupakan gudang penerimaan barang sebelum diperiksa
dan berfungsi sebagai gudang karantina. Sebelum diuji barang diberi label
berwarna kuning atau label “karantina”, yang berisi: nama barang, jumlah, nomor
batch
/ nomor order, tanggal diterima, unit penerimaan, dan tanda tangan
penerima. Semua barang tersebut akan diperiksa oleh Komite Penerimaan Barang
(KPB). KPB anggotanya ditunjuk oleh Kalafiau dan diangkat oleh Kadiskesau.
38
ditandatangani oleh PPB, Kepala Gudang dan diketahui oleh Kalafiau. Barang
yang diterima lolos uji/memenuhi kriteria, diberi label “Diluluskan” yang
berwarna hijau, label tersebut berisi: nama barang, tanggal diterima, jumlah,
pembuat/penyalur, nomor
batch
asal, dan data yang diisi oleh petugas unit uji
coba. Data tersebut berisi tanggal uji, nomor lot, tanda tangan, dan tanggal
berlaku. Barang tersebut akan disimpan di gudang sesuai dengan spesifikasinya.
Barang yang berupa obat jadi, bahan baku dan
embalage
akan disimpan di gudang
alat kesehatan.
Barang yang tidak memenuhi kriteria diberi label “Ditolak” berwarna
merah, berisi nama barang, jumlah, nomor
batch
/nomor order, tanggal diterima,
dan tanda tangan unit uji coba. Barang yang ditolak akan ditempatkan tersendiri
dan unit uji coba akan membuat surat penolakkan kepada pemasok dengan
menyebutkan alasan penolakkan. Contoh berita acara penerimaan barang dan
label dapat dilihat pada lampiran
4.6.2
Penyimpanan
Penyimpanan mencakup kegiatan penyusunan, pengawetan, dan
pengadministrasian materiil secara tertib dan teratur sesuai dengan sifat fisika,
kimia, dan biologi dari bekal kesehatan tersebut sesuai dengan ketentuan yang
berlaku di lingkungan pergudangan. Sasaran penyimpanan adalah materiil dapat
disimpan dan dipelihara dengan baik sehingga memudahkan dalam pemeliharaan,
pengawasan yang baik secara fisik maupun administratif.
Penyimpanan barang menggunakan sistem FIFO (
First In First Out)
kodifikasi meliputi jenis barang, alfabetis, sehingga memudahkan dalam
pengambilan dan menghindari kekeliruan pengambilan barang.
Barang yang mudah terbakar disimpan di gudang tahan api yang
letaknya terpisah dari gudang bahan baku/obat jadi/embalage. Penyimpanan
bahan baku berdasarkan perbedaan konsistensi, bahan padat dan kering terpisah
dari bahan cair. Peralatan kesehatan (palkes) disimpan di gudang Palkes berdasar
urutan barang yang akan disalurkan ke satker di seluruh Indonesia.
Obat jadi golongan narkotika disimpan di lemari khusus yang dilengkapi
kunci sesuai dengan peraturan perundang-undangan yang berlaku. Obat jadi dan
bahan baku yang memelukan suhu kelembaban terkendali seperti cairan infus dan
cangkang kapsul, disimpan di ruang khusus yang dilengkapi dengan AC.
Beberapa obat injeksi yang memerlukan suhu penyimpanan yang rendah disimpan
di lamari es.
4.6.3
Distribusi
Distribusi bekal kesehatan keseluruh jajaran satker kesehatan Angkatan
Udara diseluruh Indonesia dilakukan oleh bagian Gupusfi yang meliputi rumah
sakit, seksi kesehatan, Lakespra dan Lakesgilut. Dasar dalam penyaluran
perbekalan farmasi adalah surat perintah logistik (SPL) dalam bentuk 051 oleh
Kadiskesau kepada Kalafiau yang kemudian dikeluarkan Surat Perintah
Pengeluaran Barang (SPPB). Sedangkan administrasinya dilakukan oleh bagian
Minbekkes untuk diteruskan ke bagian produksi dan pergudangan. Bentuk 051
40
satker, 1 lembar sebagai arsip,1 lembar dikirim lagi ke Minbekkes dan 1 lembar
dikirim ke Diskesau. Kegiatan pengeluaran barang terbagi dalam 2 kegiatan yaitu:
4.6.3.1 Rutin
Pendistribusian rutin dilakukan alokasi kebutuhan 6 bulan sekali. Satker
mengajukan kebutuhan dan sisa persediaan ke Diskesau, Diskesau lalu akan
menunjuk Matfaskes untuk mengeluarkan rencana surat perintah logistik
(RSPL) ke Minbekkes. Minbekkes akan mencocokkan dengan kartu stok dan
melaporkan ke Diskesau, sebagai acuan SPL. Dengan SPL, Kalafiau
mengeluarkan surat perintah pengeluaran (SPPB) ke gudang. Penyaluran
barang dari gudang dari gudang penyaluran menggunakan jalur darat dan
udara. Penyaluran dilakukan pada : semester I pada bulan Januari dan
semester II pada bulan Juni.
4.6.3.2 Non rutin
Pengeluaran non rutin (Suplisi) adalah pengeluaran barang yang dilakukan
mendadak, diluar SPL seperti bencana alam, bakti sosial, dan operasi militer.
Pengeluaran suplisi dilakukan dengan menggunakan bon sementara yang
disetujui oleh Kalafiau kepada unit pergudangan.
Pengeluaran bahan baku berdasarkan atas Surat Perintah Produksi (SPP) dari
Kalafiau, ke bagian produksi, dan mengajukan permintaan bahan baku ke
Diskesau. Diskesau akan mengeluarkan SPL bahan baku produksi dan
4.6.4
Penghapusan
Penghapusan materiil kesehatan adalah usaha untuk membebaskan
bendaharawan materiil dari tuntutan pertanggungjawaban materiil yang berkaitan
dengan administrasi perbendaharaan berdasarkan ketentuan yang berlaku serta
memanfaatkan materiil tersebut dalam bentuk lain.
Materiil kesehatan yang akan dihapuskan harus memenuhi kriteria:
barang yang dinyatakan tercela; rusak/tidak dapat diperbaiki lagi, rusak atau
masih dapat diperbaiki namun tidak ekonomis, berbahaya jika disimpan lama,
kadaluarsa, berlebih, tidak dapat digunakan karena alasan tertentu. Sedangkan
barang yang dinyatakan sah untuk dihapuskan, apabila: telah dikeluarkan surat
keputusan penghapusan, telah diterbitkan surat perintah pelaksanaan
penghapusan, berita acara penghapusan yang ditandatangani panitia
bendaharawan dan ordonatur, telah dikeluarkan dari buku inventaris
/perbendaharaan.
4.6.5
Pelaporan
barang-42
barang yang mendekati ED. Laporan satu bulanan berisi : kode, nama, satuan,
jumlah (baik/rusak), tanggal kadaluarsa, sedangkan laporan triwulan berisi :
nomor, tujuan, harga (alkes/obat), jumlah, tanggal SPL, No.Reg., jumlah item,
jumlah berat, jumlah isi dan keterangan. Laporan ini juga berguna untuk
mengontrol jumlah barang dan keperluan atau alokasi setiap semester.
Stok
opname dilakukan tiap akhir semester.
Perbekalan kesehatan yang diterima dari Diskesau atau Puskes Angkatan
Udara maupun hasil produksi Lafiau selanjutnya di simpan di gudang untuk di
alokasikan ke satker-satker AU seluruh Indonesia.
4.7 Unit Produksi Lembaga Farmasi Angkatan Udara
4.7.1
Tata Letak dan Klasifikasi Ruang Produksi
Gedung produksi Lafiau terdiri dari dua bagian, yaitu bagian produksi
obat beta laktam dan non beta laktam. Ruang-ruang produksi terpisah satu sama
lain sesuai dengan jenis produksi. Hal ini bertujuan untuk menghindari
kontaminasi antara produk yang satu dengan produk yang lain. Ruangan
dirancang berurutan sesuai dengan urutan proses produksi. Denah ruang produksi
beta laktam dan non beta laktam dapat dilihat pada bagian lampiran.
Berdasarkan tingkat kebersihan ruangan, ruang produksi Lafiau dibagi
menjadi dua kelas, yaitu:
1)
Black area (daerah hitam/kelas IV)
Daerah ini meliputi kamar ganti pakaian, toilet, kamar mandi, ruang
2)
Grey area (daerah abu-abu/kelas III)
Daerah ini meliputi ruang pengolahan dan pengemasan obat non steril, ruang
timbang, pembuatan dan pencampuran sirup dan salep/krim, ruang
pencampuran, pembuatan granul, pencetakan tablet, pengisian kapsul, ruang
in
process control, penyalutan,
stripping, dan ruang penyimpanan obat setengah
jadi. Pakaian yang digunakan di daerah ini adalah pakaian khusus produksi
yang terbuat dari bahan dengan serat yang tidak mudah lepas dan dilengkapi
dengan sarung tangan, penutup kepala, serta penutup hidung dan mulut.
4.7.2
Produksi Obat
Produksi di Lafiau dilakukan berdasarkan adanya Surat Perintah
Produksi (SPP) yang dilakukan oleh Kadiskesau kepada Kalafiau kemudian
Kalafiau mengeluarkan SP3 kepada Kabagprod dan pelaksanaannya dilakukan
oleh Kaunit (Kepala Unit) berdasarkan Surat Perintah Kerja.
1. Sub Unit Produksi Tablet
Unit produksi tablet bertanggung jawab dalam memproduksi tablet dan kaplet
baik antibiotik maupun non antibiotik. Kegiatan produksi tablet yang
dilakukan dimulai dengan penimbangan bahan baku yang dinyatakan telah
memenuhi syarat oleh unit uji coba.
Bahan baku tersebut meliputi : bahan aktif, fase dalam dan fase luar,
selanjutnya dilakukan pencampuran bahan aktif dan fase dalam. Sebelum
digranulasi, diperiksa dulu oleh unit uji coba untuk mengetahui apakah
pencampuran sudah homogen. Granul yang diperoleh dari proses granulasi
basah dikeringkan, dilakukan pengujian kadar air oleh unit uji coba. Granul
44
dan mengalami proses
“coating” untuk tablet salut sebelum dikemas. Setelah
proses pencetakan, tablet diperiksa secara fisik (bentuk, bau, warna,
keseragaman bobot, ukuran, kekerasan, kerapuhan, waktu hancur, dan
disolusi) dan secara kimia.
Metode yang banyak dipakai untuk produksi tablet non beta laktam adalah
granulasi basah, selain itu metode cetak langsung juga dilakukan. Untuk
produksi tablet beta laktam, metode yang dipakai adalah granulasi kering dan
cetak langsung.
Jika tablet yang dicetak telah memenuhi persyaratan, maka produksi tablet
dapat terus berjalan dan jika tidak memenuhi persyaratan, maka produksi
dihentikan. Sisa sampel di simpan untuk sampel pertinggal. Hasil pengujian
selama proses dan akhir akan dibuat catatan pengujian kemudian dikirimkan
ke Kabagprod (Kepala Bagian Produksi).
Produk-produk yang diproduksi oleh unit produksi tablet Lafiau antara lain
tablet Ampisilin 500mg, Amokisilin 500mg, Antalgin 500mg, Antiflu, Asetilet
81mg, Aupirin 200mg, Baktrim AU, CTM, Deksametason 0,5mg,
Dekstometorphan HBr, Energic C, INH Plus 100mg, Lactas Calcicus 500mg,
Magtacida HCl 400mg, Paracetamol 500mg, Prednison, Vitamin B1, Vitamin
B6, Vitamin B12, Vitamin B kompleks, Vitamin C. Alur produksi tablet dapat
dilihat pada bagian lampiran.
2. Sub Unit Produksi Kapsul
Unit produksi kapsul bertanggungjawab dalam memproduksi kapsul, tablet
atau kaplet antibiotik dan non antibiotik serta sirup kering antibiotik. Kegiatan
dicampurkan. Selanjutnya dilakukan pengisian kapsul lalu dikemas. Pada
setiap tahap mulai dari tahap pencampuran sampai tahap pengemasan
dilakukan pengemasan mutu oleh unit uji coba
Produk-produk kapsul yang diproduksi oleh unit produksi kapsul Lafiau
antara lain Afostan 250mg, Amoxicillin 250mg, Aurobion, Chloramphenicol
250mg, Tetrasiklin 250mg. Alur produksi kapsul dapat dilihat pada bagian
lampiran.
3. Sub Unit Produksi Khusus
Unit produksi khusus Lafiau memproduksi sediaan cair baik untuk pemakaian
dalam maupun pemakaian luar, sediaan semisolid (salep/krim), dan
pengolahan air demineralisata.
Proses produksi sirup
Produksi sirup dimulai dengan penimbangan bahan baku meliputi bahan
aktif, bahan pembantu dan bahan sirup simpleks. Bahan aktif dan bahan
pembantu dilarutkan, sementara sirup simpleks disaring, larutan bahan
aktif dan sirup simpleks dicampur, larutan hasil pencampuran diuji kadar,
viskositas, pH dan berat jenisnya oleh unit uji coba. Bila kadarnya tidak
sesuai maka dilakukan penambahan aktif atau dilakukan pengenceran. Jika
kadarnya sudah sesuai maka dilakukan penyaringan. Larutan jernih hasil
penyaringan diisi ke dalam botol yang sudah dicuci. Botol yang telah diisi
larutan disortir dan diberi etiket.
Proses produksi salep
46
dicampur dengan bahan aktif, hasil pencampuran diuji kadar, homogenitas
dan konsistensi oleh unit uji coba. Setelah hasil pengujian dilakukan
pengisian dan penutupan tube, penyortiran dan pemberian etiket.
Proses produksi krim
Proses pembuatan krim dimulai dengan penimbangan bahan baku, basis
dilebur dan dicampur dengan bahan penolong sebelum membeku dan diuji
homogenitasnya selanjutnya basis dicampur dalam bahan aktif. Setelah itu
dilakukan pengujian kembali yang meliputi homogenitas, kadar dan
konsistensi. Setelah hasil pengujian memenuhi syarat maka dilakukan
penutupan tube dan pengemasan.
Proses pembuatan aqua demineralisata (aqua DM)
Lafiau mendapatkan air demineralisata dengan cara memproduksi dan
mengolahnya sendiri. Sumber air yang digunakan untuk membuat aqua
DM berasal dari sumur artesis. Dalam mencukupi kebutuhan aqua DM
untuk proses produksi dan pemeriksaan laboratorium maka dilakukan
proses pengolahan air. Air artesis disaring terlebih dahulu dan dialirkan ke
”Multi Sorb”
yang merupakan penyaringan zat secara mekanik termasuk
dapat menyaring besi, kemudian air dialirkan ke penukar ion positif dan
penukar ion negatif. Setelah itu air dididihkan dan dapat digunakan untuk
proses produksi. Reaksi yang terjadi adalah resin, sebagi contoh Mg
2+sebagai kation dan SO
42-sebagai anion. Proses reaksinya adalah sebagai
berikut :
Kation Mg
2++ Resin Mg-Resin + 2H
+-Aqua DM berasal dari air bersih yang diproses lebih lanjut dengan
menggunakan resin penukar ion (ion menjadi lebih sedikit). Parameter
mutu air yang dapat diperiksa disini adalah kejarnihan, bau, rasa, warna,
pH serta kandungan ion. Air yang telah diolah harus jernih, tidak berbau,
tidak berasa dan tidak berwarna serta pH sekitar 6-7. Air yang telah diolah
selanjutnya dididihkan jika langsung dipakai dalam proses produksi.
4.7.3
Produk Unit Produksi Khusus
Obat-obatan yang diproduksi oleh unit produksi khusus, adalah sebagai
berikut : Sirup DMP , Salep Terra-cord, Sirup
Difenhidramin-Exp, Salep Tetrasiklin, Sirup Prometazin, Krim prometazin, Tetes telinga
Klorampenikol, Sirup Deflugen, Larutan antiseptik Lafiodin dan Salep
Klorampenikol
Jenis produk yang diproduksi oleh unit produksi khusus Lafiau adalah :
a.
Cairan : Deflugen, Diphenhidramin DMP, Diphenhidramin Exp,
Paracetamol, Prometazin, Hawk 2000 (minuman kesehatan), Lafiodin,
Rivanol (untuk pemakaian luar).
b.
Salep/krim : Chloramphenicol, Prometazin, Terracort, Tetrasiklin dan
Chloramfecort.
c.
Tetes telinga : Chloramphenicol tetes.
4.7.4 Unit Pemeriksaan
In Process Control
dan Pengujian Obat Jadi
48
a
Sediaan Tablet
Pemeriksaan tablet pada saat IPC dilakukan terhadap granul meliputi
pemeriksaan kadar air dan zat aktifnya. Setelah proses pencetakan, tablet
diperiksa secara fisik (bentuk, bau, warna, keseragaman bobot, ukuran,
kekerasan, kerapuhan, waktu hancur, disolusi) dan secara kimia (pemeriksaan
kadar zat berkhasiat secara kuantitatif).
b
Sediaan Kapsul
Pemeriksaan pada saat IPC dilakukan setelah pencampuran bahan aktif dan
bahan tambahan meliputi pemeriksaan kadar zat aktifnya. Kapsul diperiksa
secara fisik (keseragaman bobot, waktu hancur, disolusi) dan secara kimia
(pemeriksaan kadar zat aktif secara kuantitatif).
Selama proses pengisian ke dalam kapsul, beberapa sampel diambil untuk
dilakukan pengujian keseragaman bobot setiap 15 menit sekali. Jika ada
penyimpangan selama pengisian kapsul, maka proses dihentikan dan
diperbaiki. Pengujian yang dilakukan terhadap obat ja