Lampiran 1.Data pengamatan susut bobot (%)
Kombinasi Ulangan Total Rataan
I II
P1L1 1,18 1,37 2,55 1,276
P1L2 1,31 1,25 2,56 1,279
P1L3 1,51 1,44 2,95 1,477
P2L1 1,41 1,49 2,90 1,450
P2L2 1,04 1,01 2,05 1,026
P2L3 1,01 1,08 2,10 1,048
P3L1 0,68 0,63 1,30 0,651
P3L2 0,98 0,96 1,94 0,968
P3L3 1,60 1,62 3,22 1,610
P4L1 0,67 0,60 1,28 0,638
P4L2 1,08 0,92 2,00 0,998
P4L3 1,32 1,23 2,54 1,271
P5L1 0,66 0,62 1,28 0,641
P5L2 0,99 0,96 1,96 0,979
P5L3 1,28 1,23 2,50 1,252
Total - - 33,13 -
Rataan - - - 1,104
Tabel sidik ragam susut bobot (%)
SK db JK KT F.Hit F 0,05 F 0,01
Perlakuan 14 2,6340 0,1881 54,69 ** 3,48 4,38 P 4 0,6177 0,1544 44,89 ** 3,25 4,46 P-lin 1 0,5744 0,5744 166,97 ** 4,54 8,68 P-kuad 1 0,0400 0,0400 11,61 ** 4,54 8,68 P-kub 1 0,0004 0,0004 0,11 tn 4,54 8,68 P-kuar 1 0,0029 0,0029 0,86 tn 4,54 8,68 L 2 0,8475 0,4238 123,17 ** 3,68 6,36 L-lin 1 0,8031 0,8031 233,44 ** 4,54 8,68 L-kuad 1 0,0444 0,0444 12,90 ** 4,54 8,68 PxL 8 1,1687 0,1461 42,46 ** 2,64 4,00
Galat 15 0,0516 0,0034 - - - -
Total 29 2,6856 - - - -
Lampiran 2. Data pengamatan total asam (%)
Kombinasi Ulangan Total Rataan
I II
P1L1 0,61 0,56 1,17 0,585
P1L2 0,59 0,50 1,09 0,546
P1L3 0,45 0,48 0,93 0,464
P2L1 0,58 0,56 1,14 0,571
P2L2 0,59 0,56 1,15 0,576
P2L3 0,47 0,51 0,98 0,492
P3L1 0,64 0,67 1,31 0,655
P3L2 0,61 0,59 1,20 0,601
P3L3 0,55 0,59 1,14 0,569
P4L1 0,69 0,66 1,35 0,675
P4L2 0,61 0,64 1,25 0,625
P4L3 0,57 0,51 1,08 0,540
P5L1 0,75 0,75 1,49 0,747
P5L2 0,67 0,64 1,31 0,653
P5L3 0,50 0,49 0,99 0,494
Total - - 17,58 -
Rataan - - - 0,586
Tabel sidik ragam total asam (%)
SK db JK KT F hit F 0,05 F 0,01
Perlakuan 14 0,1629 0,0116 14,67 ** 3,48 4,38
P 4 0,0469 0,0117 14,80 ** 3,25 4,46
P-lin 1 0,0426 0,0426 53,70 ** 4,54 8,68 P-kuad 1 0,0011 0,0011 1,39 tn 4,54 8,68 P-kub 1 0,0007 0,0007 0,87 tn 4,54 8,68 P-kuart 1 0,0026 0,0026 3,24 tn 4,54 8,68
L 2 0,0938 0,0469 59,17 ** 3,68 6,36
L-lin 1 0,0908 0,0908 114,59 ** 4,54 8,68 L-kuad 1 0,0030 0,0030 3,76 tn 4,54 8,68
PxL 8 0,0221 0,0028 3,49 * 2,64 4,00
Galat 15 0,0119 0,0008 - - - -
Total 29 0,1748 - - - - -
Lampiran 3. Data pengamatan kadar vitamin C (mg/100 g) Kombinasi
Ulangan
Total Rataan
I II
P1L1 20,24 18,48 38,72 19,36
P1L2 17,60 16,72 34,32 17,16
P1L3 14,96 14,08 29,04 14,52
P2L1 18,48 19,36 37,84 18,92
P2L2 19,36 17,60 36,96 18,48
P2L3 16,72 15,84 32,56 16,28
P3L1 24,64 23,76 48,40 24,20
P3L2 21,12 18,48 39,60 19,80
P3L3 17,60 19,36 36,96 18,48
P4L1 24,64 26,40 51,04 25,52
P4L2 19,36 20,24 39,60 19,80
P4L3 17,60 18,48 36,08 18,04
P5L1 24,64 25,52 50,16 25,08
P5L2 21,12 22,88 44,00 22,00
P5L3 17,60 17,60 35,20 17,60
Total - - 590,48 -
Rataan - - - 19,683
Tabel sidik ragam kadar vitamin C (mg/100 g)
SK db JK KT F hit F 0,05 F 0,01
Perlakuan 14 288,4382 20,6027 21,57 ** 3,48 4,38 P 4 103,3566 25,8391 27,05 ** 3,25 4,46 P-lin 1 91,0694 91,0694 95,35 ** 4,54 8,68 P-kuad 1 5,3102 5,3102 5,56 * 4,54 8,68 P-kub 1 2,1812 2,1812 2,28 tn 4,54 8,68 P-kuart 1 4,7957 4,7957 5,02 * 4,54 8,68 L 2 159,4231 79,7116 83,46 ** 3,68 6,36 L-lin 1 158,5971 158,5971 166,05 ** 4,54 8,68 L-kuad 1 0,8260 0,8260 0,86 tn 4,54 8,68
PxL 8 25,6585 3,2073 3,36 * 2,64 4,00
Galat 15 14,3264 0,9551 - - - -
Total 29 - - - - - -
Lampiran 4. Data pengamatan total soluble solid (oBrix) Kombinasi
Ulangan
Total Rataan
I II
P1L1 5,92 6,38 12,31 6,153
P1L2 7,95 7,45 15,40 7,699
P1L3 9,58 8,80 18,38 9,190
P2L1 7,54 7,16 14,70 7,351
P2L2 7,96 7,12 15,08 7,539
P2L3 8,38 8,00 16,38 8,189
P3L1 7,48 7,15 14,63 7,317
P3L2 7,53 7,14 14,67 7,337
P3L3 8,78 9,55 18,33 9,167
P4L1 8,00 7,92 15,92 7,958
P4L2 8,33 7,47 15,80 7,900
P4L3 8,80 8,30 17,10 8,549
P5L1 7,48 7,97 15,44 7,721
P5L2 8,75 9,10 17,86 8,929
P5L3 9,15 9,17 18,32 9,160
Total - - 240,32 -
Rataan - - - 8,011
Tabel sidik ragam total soluble solid (oBrix)
SK db JK KT F hit F 0,05
F 0,01 Perlakuan 14 20,9088 1,4935 10,45 ** 3,48 4,38
P 4 3,4892 0,8723 6,10 ** 3,25 4,46
P-lin 1 3,1398 3,1398 2,21 tn 4,54 8,68 P-kuad 1 0,3166 0,3166 2,21 tn 4,54 8,68 P-kub 1 0,0008 0,0008 0,01 tn 4,54 8,68 P-kuart 1 0,0320 0,0320 0,22 tn 4,54 8,68 L 2 12,2838 6,1419 42,96 ** 3,68 6,36 L-lin 1 12,0311 12,0311 84,16 ** 4,54 8,68 L-kuad 1 0,2528 0,2528 1,77 tn 4,54 8,68 PxL 8 5,1357 0,6420 4,49 ** 2,64 4,00
Galat 15 2,1444 0,1430 - - - -
Total 29 23,0532 - - - - -
Lampiran 5. Data pengamatan kadar tanin (%) Kombinasi
Ulangan
Total Rataan
I II
P1L1 0,34 0,34 0,69 0,344
P1L2 0,31 0,29 0,60 0,299
P1L3 0,31 0,28 0,59 0,293
P2L1 0,37 0,34 0,71 0,356
P2L2 0,34 0,31 0,66 0,328
P2L3 0,25 0,34 0,59 0,294
P3L1 0,33 0,32 0,65 0,323
P3L2 0,37 0,34 0,72 0,360
P3L3 0,38 0,32 0,69 0,347
P4L1 0,35 0,31 0,66 0,329
P4L2 0,31 0,34 0,65 0,327
P4L3 0,32 0,29 0,60 0,302
P5L1 0,28 0,31 0,59 0,297
P5L2 0,35 0,31 0,65 0,327
P5L3 0,32 0,29 0,60 0,301
Total - - 9,65 -
Rataan - - - 0,322
Tabel sidik ragam kadar tanin (%)
SK db JK KT F hit F 0,05 F 0,01
Perlakuan 14 0,0146 0,0010 1,52 tn 3,48 4,38 P 4 0,0045 0,0011 1,65 tn 3,25 4,46 P-lin 1 0,0001 0,0001 0,17 tn 4,54 8,68 P-kuad 1 0,0035 0,0035 5,09 ** 4,54 8,68 P-kub 1 0,0001 0,0001 0,08 tn 4,54 8,68 P-kuart 1 0,0009 0,0009 1,26 tn 4,54 8,68 L 2 0,0030 0,0015 2,20 tn 3,68 6,36 L-lin 1 0,0024 0,0024 3,52 tn 4,54 8,68 L-kuad 1 0,0006 0,0006 0,88 tn 4,54 8,68 PxL 8 0,0071 0,0009 1,28 tn 2,64 4,00
Galat 15 0,0103 0,0007 - - - -
Total 29 0,0103 - - - - -
Lampiran 6. Data pengamatan total mikroba (log CFU/g)
Kombinasi Ulangan Total Rataan
I II
P1L1 5,00 4,99 9,99 4,996
P1L2 5,01 5,04 10,05 5,023
P1L3 5,20 5,29 10,49 5,243
P2L1 4,85 4,91 9,76 4,879
P2L2 4,99 4,98 9,97 4,984
P2L3 5,00 5,07 10,07 5,036
P3L1 4,91 4,85 9,75 4,877
P3L2 4,87 4,82 9,69 4,844
P3L3 5,11 5,20 10,31 5,156
P4L1 4,98 4,86 9,84 4,921
P4L2 4,83 4,74 9,57 4,786
P4L3 5,29 4,99 10,28 5,138
P5L1 4,20 4,79 9,00 4,498
P5L2 4,76 4,86 9,62 4,810
P5L3 5,26 5,03 10,30 5,148
Total - - 148,68 -
Rataan - - - 4,956
Tabel sidik ragam total mikroba (log CFU/g)
SK db JK KT F hit F 0,05 F 0,01
Perlakuan 14 0,9827 0,0702 3,84 * 3,48 4,38
P 4 0,2175 0,0544 2,97 tn 3,25 4,46
P-lin 1 0,1849 0,1849 10,12 ** 4,54 8,68 P-kuad 1 0,0002 0,0002 0,01 tn 4,54 8,68 P-kub 1 0,0323 0,0323 1,77 tn 4,54 8,68 P-kuart 1 10-7 10-7 4x10-5 tn 4,54 8,68
L 2 0,5472 0,2736 14,97 ** 3,68 6,36
L-lin 1 0,4812 0,4812 26,33 ** 4,54 8,68 L-kuad 1 0,0660 0,0660 3,61 tn 4,54 8,68
PxL 8 0,2180 0,0273 1,49 tn 2,64 4,00
Galat 15 0,2742 0,0183 - - - -
Total 29 1,2569 - - - - -
Lampiran 7. Data pengamatan organoleptik warna, rasa, aroma (hedonik) Kombinasi
Ulangan
Total Rataan
I II
P1L1 4,00 3,20 7,20 3,600
P1L2 3,47 2,87 6,33 3,167
P1L3 1,13 1,67 2,80 1,400
P2L1 3,07 3,20 6,27 3,133
P2L2 2,53 2,53 5,07 2,533
P2L3 1,67 1,87 3,53 1,767
P3L1 3,67 3,47 7,13 3,567
P3L2 2,80 2,80 5,60 2,800
P3L3 1,60 1,87 3,47 1,733
P4L1 3,00 3,00 6,00 3,000
P4L2 3,33 2,86 6,19 3,095
P4L3 1,80 1,73 3,53 1,767
P5L1 3,07 2,67 5,73 2,867
P5L2 3,07 2,67 5,73 2,867
P5L3 1,80 2,00 3,80 1,900
Total - - 78,39 -
Rataan - - - 2,61
Tabel sidik ragam organoleptik warna, rasa, aroma (hedonik)
SK db JK KT F hit F 0,05 F 0,01
Perlakuan 14 14,3988 1,0285 15,09 ** 3,48 4,38
P 4 0,2553 0,0638 0,94 tn 3,25 4,46
P-lin 1 0,0271 0,0271 0,40 tn 4,54 8,68 P-kuad 1 0,0005 0,0005 0,01 tn 4,54 8,68 P-kub 1 0,1289 0,1289 1,89 tn 4,54 8,68 P-kuart 1 0,0987 0,0987 1,45 tn 4,54 8,68 L 2 12,7227 6,3613 93,34 ** 3,68 6,36 L-lin 1 11,5520 11,5520 169,51 ** 4,54 8,68 L-kuad 1 1,1707 1,1707 17,18 ** 4,54 8,68
PxL 8 1,4208 0,1776 2,61 tn 2,64 4,00
Galat 15 1,0223 0,0682 - - - -
Total 29 15,4210 - - - - -
Lampiran 8. Data pengamatan organoleptik tekstur (skor) Kombinasi
Ulangan
Total Rataan
I II
P1L1 3,60 3,27 6,87 3,433
P1L2 2,67 2,67 5,33 2,667
P1L3 1,87 1,73 3,60 1,800
P2L1 3,13 3,60 6,73 3,367
P2L2 2,47 2,47 4,93 2,467
P2L3 2,13 2,47 4,60 2,300
P3L1 3,27 3,73 7,00 3,500
P3L2 2,93 2,93 5,87 2,933
P3L3 2,20 1,87 4,07 2,033
P4L1 3,07 3,60 6,67 3,333
P4L2 3,00 3,00 6,00 3,000
P4L3 2,20 2,27 4,47 2,233
P5L1 4,00 3,40 7,40 3,700
P5L2 3,47 3,00 6,47 3,233
P5L3 1,73 1,80 3,53 1,767
Total - - 83,53 -
Rataan - - - 2,784
Tabel sidik ragam organoleptik tekstur (skor)
SK db JK KT F hit F 0,05 F 0,01
Perlakuan 14 11,8083 0,8434 15,26 ** 3,48 4,38
P 4 0,2883 0,0721 1,30 tn 3,25 4,46
P-lin 1 0,2756 0,2756 4,99 * 4,54 8,68 P-kuad 1 0,0089 0,0089 0,16 tn 4,54 8,68 P-kub 1 0,0003 0,0003 0,01 tn 4,54 8,68 P-kuart 1 0,0034 0,0034 0,06 tn 4,54 8,68 L 2 10,4536 5,2268 94,59 ** 3,68 6,36 L-lin 1 10,3680 10,3680 187,62 ** 4,54 8,68 L-kuad 1 0,0856 0,0856 1,55 tn 4,54 8,68 PxL 8 1,0664 0,1333 2,41 tn 2,64 4,00
Galat 15 0,8289 0,0553 - - - -
Total 29 12,6372 - - - - -
Lampiran 9. Data pengamatan buah salak kontrol
Kandungan KL1 KL2
Susut Bobot (%) 0,991 1,373
Total Padatan Terlarut (oBrix) 8,344 12,312
Kadar Vitamin C (mg/100g) 16,280 15,400
Total Asam (%) 0,732 0,563
Kadar Tanin (%) 0,367 0,342
Total Mikroba 6,732 8,919
Organoleptik Warna, Aroma, Rasa (Hedonik) 3,067 3,000
Organoleptik Tekstur (Skor) 3,333 2,667
Keterangan: K = Kontrol
Lampiran 10. Kandungan buah salak segar
Kandungan Jumlah
Total Padatan Terlarut (oBrix) 7,728
Kadar Vitamin C (mg/100g) 26,840
Total Asam (%) 0,624
Lampiran 11. Gambar buah salak terolah minimal yang dilapisi pelapis edibel
P1L1 P2L1 P3L1
P4L1 P5L1 P1L2
P5L2 P1L3 P1L3
DAFTAR PUSTAKA
Ahmad, U., Yulianingsih, dan M. Lintang. 2010. Aplikasi film edibel dan kemasan atmosfir termodifikasi untuk meningkatkan umur simpan buah salak terolah minimal. Jurnal Ilmu Pertanian Indonesia. 15(3):163-171. Anarsis, W. 1999. Agribisnis Komoditas Salak. Bumi Aksara, Jakarta.
Antara, N. S. 2007. Proses mínimum untuk meningkatkan nilai tambah produk hortikultura. Seminar Nasional Peningkatan Keuntungan Ritel Produk Hortikultura Segar Melalui Praktek Penanganan Pascapanen dan Keamanan Pangan yang Baik. Universitas Udayana.
AOAC, 1984. Official Method of Analysis of AOAC International. The Association of The Official Analytical Chemists 11th Edition, Academic Press, Washington DC.
Awwaly, K. U. A, A. Manab, dan E. Wahyuni. 2010. Pembuatan edible film protein whey : kajian rasio protein dan gliserol terhadap sifat fisik dan kimia. Jurnal Ilmu dan Teknologi Hasil Ternak. 5(1) : 45-56.
Badan Pusat Statisik. 2014. Produksi tanaman pangan. (10 Juni 2015).
Baldwin, E. 2003. Coatings and Other Supplemental Treatments to Maintain Vegetable Quality. Di dalam : Bart. J. A. dan Brecht J. K.,editor. Postharvest Physiology and Pathology of Vegetables : Second Edition. Marcel Dekker Inc, Quebec.
Bangun, M. K. 1991. Rancangan Percobaan untuk Menganalisis Data. Bagian Biometri. Fakultas Pertanian USU, Medan.
Corbo, R.M., M.A.D. Nobile, dan M. Sinigaglia. 2006. A novel approach for calculating shelf life of minimally processed vegetables. International Journal of Food Microbiology.106 : 69-73.
Crisosto, C.H., D. Garner, J. Doyle, dan K. R. Day. 1993. Relationship between fruit respiration, bruising susceptibility and temperature in sweet cherries. Di dalam : Helmiyesi, R. B. Hastuti, dan E. Prihastanti. 2008. Pengaruh lama penyimpanan terhadap kadar gula dan vitamin C pada buah jeruk siam (Citrus nobilis var. microcarpa). Buletin Anatomi dan Fisiologi. 16(2).
Departemen Kesehatan Republik Indonesia, 1996. Daftar Komposisi Bahan Makanan. Bhratara Aksara, Jakarta.
Desrosier, N. W. 2008. Teknologi Pengawetan Pangan. Penerjemah : M. Muljohardjo. Edisi Ketiga. UI-Press, Jakarta.
Estiasih, T. dan K. Ahmadi. 2009. Teknologi Pengolahan Pangan. Bumi Aksara, Jakarta.
Fardiaz, S. 1992. Mikrobiologi Pangan I. Gramedia, Jakarta.
Helmiyesi, R. B. Hastuti, dan E. Prihastanti. 2008. Pengaruh lama penyimpanan terhadap kadar gula dan vitamin C pada buah jeruk siam (Citrus nobilis
var. microcarpa). Buletin Anatomi dan Fisiologi. 16(2).
Hong, S. I. dan D. Kim. 2004. The effect of packaging treatment on the storage quality of minimally processed bunched onions. International Journal of Food Science and Technology. 39 : 1033-1041.
Huri, D. dan F. C. Nisa. 2014. Pengaruh konsentrasi gliserol dan ekstrak ampas kulit apel terhadap karakteristik fisik dan kimia edible film. Jurnal Pangan Agroindustri. 2(4) : 29-40.
Indriyanti, D. Indrarti, dan E. Rahimi. 2006. Pengaruh carboxy methyl cellulose (CMC) dan gliserol terhadap sifat mekanik lapisan tipis komposit bakterial selulosa. Jurnal Sains Materi Indonesia. 8 (1) : 40-44.
Islam, A. A., S. Wijana, dan I. A. Dewi. 2014. Pengaruh konsentrasi bubuk cincau hitam dan pati tapioka terhadap kualitas edible coating dari cincau hitam (Mesona Palustris) pada sosis. Jurnal Skripsi Universitas Brwijaya.
Juanda, D. dan B. Cahyono. 2000. Ubi Jalar. Kanisius, Yogyakarta.
Kamal, N. 2010. Pengaruh bahan aditif CMC (carboxyl methyl cellulose) terhadap beberapa parameter pada larutan sukrosa. Jurnal Teknologi. 1(17) : 78-85.
Kusnandar, F. 2010. Kimia Pangan. Dian Rakyat, Jakarta.
Lin, D, Y. Zhao, 2007. Innovations in the Development and Application of Edible Coatings for Fresh and Minimally Processed Fruits and Vegetables. Comprehensive Reviews in Food Science and Food Safety. 6 : 60 - 77. Mais, A. 2008. Utilization of sweet potato starch, flour and fibre in bread and
Manurung, V. H., G. S. S. Djarkasi, T. M. Langi, dan L. E. Lalujan. 2014. Analisis sifat fisik dan kimia buah salak Pangu (Salacca zalacca) dengan pelilinan selama penyimpanan. Jurnal UNSRAT.
Mardiana, K. 2008. Pemanfaatan gel lidah buaya sebagai edible coating buah belimbing manis (Averrhoa carambola L.). Skripsi. IPB. Bogor.
Masruroh, H., A. F. Fauzi, D. Anggryani, dan V. Paramita. 2013. Pengaruh penambahan xhantan gum dalam aplikasi teknologi edible coating aloe vera untuk mempertahankan mutu tomat (Solanum lycopersicum) menggunakan metode spray. Prosiding SNST ke-4. Fakultas Teknik Universitas Wahid Hasyim.
Miskiyah, Widaningrum, dan C. Winarti. 2011. Aplikasi edible coating berbasis pati sagu dengan penambahan vitamin C pada paprika : preferensi konsumen dan mutu mikrobiologi. Jurnal Hortikultura. 21 (1) : 68-76. Nasution, I. S., Yusmanizar, dan K. Melianda. 2012. Pengaruh penggunaan
lapisan edibel (edible coating), kalsium klorida, dan kemasan plastik terhadap mutu nanas (Ananas comosus Merr.) terolah minimal. Jurnal Teknologi dan Industri Pertanian. 4 (2) : 21-26.
Noerhartati, E., T. Rahayuningsih, dan N. V. Feriyani. 2010. Pembuatan selai salak (Salacca edulis reinw) : kajian dari penambahan natrium benzoat dan gula yang tepat terhadap mutu selai salak selama penyimpanan. Jurnal Universitas Wijaya Kusuma, Surabaya.
Novita, M., Satriana, Martunis, S. Rohaya, dan E. Hasmarita. 2012. Pengaruh pelapisan kitosan terhadap sifat fisik dan kimia tomat segar (Lycopersicum pyriforme) pada berbagai tingkat kematangan. Jurnal Teknologi dan Industri Pertanian. 4 (3) : 1-8.
Nunes, M. C. D. dan J. P. Emond. 2003. Storage Temperature. Di dalam : Bart, J. A. dan Brecht J. K., editor. Postharvest Physiology and Pathology of Vegetables : Second Edition. Marcel Dekker Inc, Quebec.
Ohlsson, T., Gothenburg dan Bengstsson. 2002. Minimally Processing Technologies in the Food Industry. CRC Press, Boca Ratton, Florida. Pantastico, E.R. B. 1993. Fisiologi Pascapanen. Penerjemah : Komeriyani. UGM
Press, Yogyakarta.
Pardede, E. 2009. Buah dan sayur olahan secara minimalis.Visi. 17 (3) : 245-254. Ragaert, P., W. Verbekeh, F. Devlieghere, dan J. Debevere. 2004. Consumer
Rahmawati, I. S., E. D. Hastuti, dan S. Darmanti. 2011. Pengaruh perlakuan konsentrasi kalsium klorida (CaCl2) dan lama penyimpanan terhadap kadar
asam askorbat buah tomat (Lycopersicum esculentum Mill.). Buletin Anatomi dan Fisiologi. 19 (1) : 62-70.
Ranganna, S. 1978. Hand of Analysis and Quality Control for Fruit and Vegetable Product, 2nd ed. Mc.Graw-Hill Publishing Coimpany Limited, New Delhi.
Ristek. 2009. Salak (Salacca edulis).
(09 April 2015).
Robinson dan N. A. Eskin. 1991. Oxidative Enzym in Food. Elsevier, New York. Rokhati, N., A. Prasetyaningrum, D. Ikhsan, dan T. D. Kusworo. 2015.
Peningkatan mutu simpan buah dengan coating komposit tapioka-kitosan. Prosiding Seminar Nasional Teknik Kimia Kejuangan Pengembangan Teknologi Kimia untuk Pengolahan Sumber Daya Alam Indonesia.
Rudito, 2005. Perlakuan komposisi gelatin dan asam sitrat dalam edible coating yang mengandung gliserol pada penyimpanan tomat. Jurnal Teknologi Pertanian. 6 (1) : 1-6.
Santosa, B. dan Wirawan. 2014. Chemistry changes in minimally process snake fruit variety pondoh during storage in room temperature which coating used edible coating from starch of jackfruit seed. International Journal of Science and Technology. 3 (3) : 15-18.
Santoso, B., G. Priyanto, dan R. H. Purnomo. 2007. Sifat fisik dan kimia edibel film berantioksidan dan aplikasinya sebagai pengemas primer lempok durian. Jurnal Agribisnis dan Industri Pertanian. 6 (1) : 77-82.
Santoso, B., D. Saputra, dan R. Pambayun. 2004. Kajian teknologi edible coating dari pati dan aplikasinya untuk pengemas primer lempok durian. Jurnal Teknologi dan Industri Pangan. 15(3) : 239-244.
Setyaningsih, D., A. Apriyantono, dan M. P. Puspitasari. 2010. Analisis Sensori untuk Industri Pangan dan Agro. IPB-Press, Bogor.
Smith, A. C., K. W. Waldron, N. Maness, dan P. P. Veazie. 2003. Vegetable Texture : Measurement and Structural Implications. Di dalam : Bart, J. A. dan Brecht J. K., editor. Postharvest Physiology and Pathology of Vegetables : Second Edition. Marcel Dekker Inc, Quebec.
Steel, R.G.D. dan Torrie, J. H. 1960. Principles and Procedures of Statistics. McGraw-Hill, New York.
Suharyono dan M. Kurniadi. 2010. Efek sinar ultraviolet dan lama simpan terhadap karakteristik sari buah tomat. Agritech. 30(1) : 25 - 31.
Swinkels, 1985. Sources of Starch, Its Chemistry and Physics. Marcel Dekker, Inc., New York.
Syamal, M. M. 1990. Biochemical Composition of Tomato Fruits During Storage. Di dalam : Bart. J. A. dan Brecht J. K., editor. 2003. Postharvest Physiology and Pathology of Vegetables : Second Edition. Marcel Dekker Inc, Quebec.
Tannenbaum, S.R. 1976. Di dalam : Rudito, 2005. Perlakuan komposisi gelatin dan asam sitrat dalam edible coating yang mengandung gliserol pada penyimpanan tomat. Jurnal Teknologi Pertanian. 6 (1) : 1-6.
Wilss, R. H. H., T. H. Lee, D. Graham, W. B. McGlason, dan E. G. Hall. 1981. Post Harvest, An Introducing to the Physiology and Handling of Fruits and Vegetables. New South Wales University Press, Kensington.
Winarno, F. G. 2008. Kimia Pangan dan Gizi. Mbrio Press, Bogor.
Winarti, C., Miskiyah, dan Widaningrum. 2012. Teknologi produksi dan aplikasi pengemas edibel antimikroba berbasis pati. Jurnal Litbang Pertanian. 31(3) : 85-93.
BAHAN DAN METODE PENELITIAN
Waktu dan Tempat Penelitian
Penelitian ini dilaksanakan pada bulan Juli 2015 di Laboratorium Analisa Kimia Bahan Pangan Program Studi Ilmu dan Teknologi Pangan Fakultas Pertanian Universitas Sumatera Utara.
Bahan Penelitian
Bahan yang digunakan adalah buah salak Padangsidimpuan (Salacca sumatrana) yang diperoleh dari petani salak di Parsalakan Padangsidimpuan dan pati ubi jalar ungu varietas Ayamurasaki.
Reagensia
Bahan kimia yang digunakan adalah NaOH 0,1 N, Iodium 0,1 N, larutan phenolptalein 1%, larutan pati 1%, akuades, gliserol, asam askorbat, asam sitrat, CMC (carboxyl methyl cellulose), PCA (Plate Count Agar), dan alkohol.
Alat
Peralatan yang digunakan adalah pisau, blender, kain saring, piring, oven, timbangan, ayakan 80 mesh, loyang, tirisan, baskom, hot plate, magnet stirrer,
handrefraktometer, fruit hardness tester, lemari pendingin, pipet tetes, styrofoam,
Metode Penelitian (Bangun, 1991).
Penelitian ini dilakukan dengan menggunakan Rancangan Acak Lengkap (RAL) yang terdiri dari dua faktor, yaitu (Bangun, 1991) :
Faktor I : Konsentrasi pati ubi jalar ungu (P) yang terdiri dari 5 taraf yaitu : P1 = 2% (b/b)
P2 = 3% (b/b)
P3 = 4% (b/b)
P4= 5% (b/b)
P5 = 6% (b/b)
Faktor II : Lama penyimpanan (L) yang terdiri dari 3 taraf yaitu : L1 = 2 hari
L2 = 4 hari
L3 = 6 hari
Banyaknya kombinasi perlakuan atau Treatment Combination (Tc) adalah 5x3 = 15, maka jumlah ulangan (n) minimum adalah sebagai berikut :
Tc (n-1) ≥ 15 15 (n-1) ≥ 15
15n ≥ 30
n ≥ 2
Untuk ketelitian dalam penelitian ini dilakukan ulangan sebanyak 2 kali.
Model Rancangan
Penelitian ini dilakukan dengan model Rancangan Acak Lengkap (RAL) faktor dengan model:
Dimana :
Ŷijk : Hasil pengamatan dari faktor P pada taraf ke-i dan faktor L pada taraf ke-j dalam ulangan ke-k
µ : Efek nilai tengah
αi : Efek faktor P pada taraf ke-i
βj : Efek faktor L pada taraf ke-j
(αβ)ij : Efek interaksi faktor P pada taraf ke-i dan faktor L pada taraf ke-j
εijk : Efek galat dari faktor P pada taraf ke-i dan faktor L pada taraf ke-j
dalam ulangan ke-k.
Apabila diperoleh hasil yang berbeda nyata dan sangat nyata maka uji dilanjutkan dengan uji beda rataan dengan menggunakan uji DMRT (Duncan Multiple Range Test).
Pelaksanaan Penelitian Ekstraksi pati ubi jalar
Ubi jalar ungu disortasi dan dicuci bersih. Ubi jalar dikupas lalu dipotong-potong kemudian dihancurkan dengan blender dengan penambahan air 1:3 sampai menjadi bubur. Selanjutnya disaring dengan kain saring sehingga diperoleh filtrat I. Ampas yang diperoleh ditambah air dengan perbandingan 1:1 dan disaring kembali sehingga diperoleh filtrat II.
diblender dan diayak menggunakan ayakan 80 mesh. Skema pembuatan ubi jalar ungu ditampilkan pada Gambar 1.
Penyiapan salak terolah minimal
Buah salak Padangsidimpuan disortasi dan tidak ada cacat fisik. Buah dikupas dan dipisahkan anakan, kulit ari dibuang. Dicuci dengan air bersih dan ditiriskan. Buah salak dicelupkan ke dalam larutan asam askorbat 100 ppm dan asam sitrat 150 ppm selama 30 detik dan ditiriskan selama 10 detik. Skema penyiapan salak terolah minimal ditampilkan pada Gambar 2.
Pembuatan pelapis edibel
Dilarutkan pati ubi jalar sesuai perlakuan (2% b/b; 3% b/b; 4% b/b; 5% b/b; 6% b/b) dalam 500 ml akuades, dipanaskan diatas hot plate diaduk selama 5 menit hingga homogen. Kemudian ditambahkan CMC 1% dan gliserol 1% sedikit demi sedikit dan diaduk hingga homogen. Dipanaskan sampai suhu 70oC sambil diaduk selama 15 menit. Didinginkan sampai suhu 30oC dan ditambah asam askorbat sebanyak 1%. Skema pembuatan larutan edibel ditampilkan pada Gambar 3.
Aplikasi pelapis edibelpada buah salak terolah minimal
dan ditutup dengan plastik wrapping dan disimpan dalam lemari pendingin suhu 10-15oC selama 2, 4, dan 6 hari.
Pengamatan dan Pengukuran Data
Penentuan susut bobot (Steel dan Torrie, 1960)
Pengukuran susut bobot dilakukan dengan cara menimbang bahan sebelum penyimpanan dan sesudah penyimpanan. Kemudian dilakukan perhitungan sebagai berikut :
Susut Bobot (%) = x 100 %
X = berat bahan sebelum penyimpanan Y = berat bahan setelah penyimpanan
Penentuan kadar vitamin C (Ranganna, 1978)
Sampel dihaluskan kemudian ditimbang sebanyak 10 g dimasukkan ke dalam beaker glass dan ditambahkan akuades sebanyak 100 ml. Diaduk hingga merata kemudian disaring dengan kertas saring. Filtrat diambil sebanyak 10 ml lalu ditambahkan larutan pati 1% lalu dititrasi dengan larutan iodium 0,01 N. Titrasi dianggap selesai setelah timbul warna biru.
Kadar vitamin C = (mg/100g bahan) FP = Faktor pengencer
Penentuan total asam (Ranganna, 1978)
Sampel dihaluskan kemudian ditimbang sebanyak 5 g ke dalam beaker glass dan ditambahkan akuades sampai volume 100 ml. Diaduk hingga merata dan disaring dengan kertas saring. Diambil filtratnya sebanyak 10 ml dan dimasukkan
X – Y X
ke dalam Erlenmeyer lalu ditambahkan indikator phenolptalein 1% sebanyak 2-3 tetes. Kemudian dititrasi dengan menggunakan NaOH 0,1 N. Titrasi dihentikan setelah timbul warna merah jambu yang stabil.
Total Asam (%) = x 100%
Asam dominan = asam malat (berat massa = 134, valensi = 2)
Penentuan total soluble solid (TSS) (AOAC, 1984)
Penentuan total soluble solid (TSS) dilakukan dengan menggunakan
handrefractometer. Buah salak dihaluskan terlebih dahulu. Dimasukkan salak yang telah dihaluskan sebanyak 5 g ke dalam beaker glass dan ditambahkan 20 ml akuades. Diambil setetes larutan dan diletakkan pada lensa. Lalu dilihat batas terang dan gelap. Angka yang tertera pada batas tersebut merupakan nilai total padatan terlarut. Dihitung total padatan terlarut dengan rumus :
Total padatan terlarut (oBrix) = angka handrefractometer x faktor pengencer
Penentuan kadar tanin (Sudarmadji, 1989)
Penentuan kadar tanin dilakukan dengan menimbang 1,5 g bahan, kemudian dimasukkan ke dalam Erlenmeyer 100 ml lalu ditambahkan akuades 50 ml, dipanaskan pada suhu 50oC selama 30 menit. Setelah dingin larutan disaring ke dalam labu ukur 250 ml, lalu ditambahkan dengan akuades sampai tanda garis. Dari larutan tersebut diambil 25 ml dimasukkan ke dalam Erlenmeyer dan ditambahkan 20 ml larutan indigocarmin kemudian dititrasi dengan larutan KMnO4 0,1 N sampai berubah warna menjadi kuning emas.
Penetapan blanko dilakukan dengan memasukkan 20 ml larutan indigocarmin ke dalam Erlenmeyer dan ditambahkan akuades 25 ml lalu dititrasi
sampai berwarna kuning emas. Kadar tanin dihitung dengan rumus sebagai berikut:
% Tanin = x 100%
A = volume titrasi tanin (ml) B = volume titrasi blanko (ml) 10 = faktor pengenceran 1 ml KMnO4 = 0,00416 g tanin
Pengujian total mikroba (Fardiaz, 1992)
Bahan diambil sebanyak 1 g dan dimasukkan ke dalam tabung reaksi kemudian ditambahkan akuades 9 ml dan diaduk sampai merata. Hasil pengenceran ini diambil dengan pipet volume sebanyak 1 ml kemudian ditambahkan akuades 9 ml. Pengenceran ini dilakukan sampai 1000 kali (103).
Dari hasil pengenceran pada tabung reaksi yang terakhir diambil sebanyak 1 ml dan diratakan pada medium agar PCA (ditimbang 7 g PCA, ditambahkan akuades 250 ml dan kemudian disterilisasikan dalam autoclave pada suhu 121oC selama 15 menit). PCA yang telah disiapkan di atas cawan petri, selanjutnya diinkubasi selama 24 jam pada suhu 32 oC dengan posisi terbalik. Jumlah koloni yang ada dihitung dengan colony counter.
Total koloni = Jumlah koloni x 1 ��
FP = faktor pengencer
Uji organoleptik warna, rasa, dan aroma (Setyaningsih, dkk., 2010)
Uji organoleptik warna, rasa, dan tekstur dilakukan oleh panelis sebanyak 15 orang. Pengujian dilakukan secara inderawi (organoleptik) yang ditentukan
berdasarkan skala numerik. Uji organoleptik untuk menentukan tingkat kesukaan warna, rasa, dan tekstur dilakukan berdasarkan skala numerik pada Tabel 3.
Tabel 3. Skala uji hedonik warna, rasa, dan tekstur
Skala hedonik Skala numerik
Sangat suka 5
Suka 4
Agak suka 3
Tidak suka 2
Sangat tidak suka 1
Organoleptik tekstur (Setyaningsih, dkk., 2010)
Uji organoleptik skor tekstur dilakukan oleh panelis sebanyak 15 orang. Pengujian dilakukan secara inderawi (organoleptik) yang ditentukan berdasarkan skala numerik. Uji organoleptik untuk menentukan tingkat kekerasan dilakukan berdasarkan skala numerik pada Tabel 4.
Tabel 4. Skala organoleptik tekstur (skor)
Skor tekstur Keterangan
5 Sangat keras
4 Keras
3 Agak keras
2 Tidak keras
Gambar 1. Skema pembuatan pati ubi jalar ungu Disortasi, dikupas dan dicuci
Dipotong-potong dan diblender dengan penambahan air 1:3
Disaring dengan kain saring
Diendapkan selama 30 menit
Diambil endapan pati dan dikeringkan di oven dengan suhu 50 oC selama 12 jam
Penghalusan dengan blender
Pengayakan menggunakan ayakan 80 mesh Digabung dan diendapkan selama 12 jam
Dibuang bagian larutan dan ditambah air 1:1
Filtrat I Ampas
Ditambah air 1:1 dan disaring dengan kain saring
Filtrat II
Gambar 2. Skema penyiapan salak terolah minimal Disortasi dan dikupas
Dicuci dengan air bersih Ditiriskan dengan tirisan
Pencelupan dalam larutan asam askorbat 100 ppm dan asam sitrat 150 ppm selama
30 detik
Penirisan dengan tirisan selama 10 detik Dipisahkan anakan dan kulit ari dibuang
Gambar 3. Skema pembuatan larutan pelapis edibel Penambahan CMC 1% dan gliserol 1%
Pemanasan sampai suhu 70 oC selama 15 menit
Pendinginan hingga suhu 30 oC Pati + 500 ml akuades
Penambahan asam askorbat 1% Konsentrasi
pati (P) P1 = 2% b/b
P2 = 3% b/b
P3 = 4% b/b
P4 = 5% b/b
P5 = 6% b/b
Pemanasan dan homogenisasi 5 menit
Gambar 4. Skema aplikasi pelapis edibel pada salak terolah minimal Pencelupan dalam larutan pelapis edibel selama
15 detik dan ditiriskan selama 2 menit
Pencelupan dalam larutan pelapis edibel selama 10 detik dan ditiriskan selama 2 menit
Pengemasan di dalam styrofoam dan ditutup dengan plastik wrapping
Penyimpanan pada suhu 10-15oC
- Susut bobot (%)
- Kadar vitamin C (mg/100 g) - Total asam (%)
- Total soluble solid (oBrix) - Kadar tanin
- Total mikroba
- Nilai organoleptik : warna, rasa, dan aroma (hedonik) - Nilai organoleptik tekstur
(skor) Lama
Penyimpanan (L)
L1 = 2 hari
L2 = 4 hari
L3 = 6 hari
Konsentrasi pati dalam larutan edibel (P)
P1 = 2% b/b
P2 = 3% b/b
P3 = 4% b/b
P4 = 5% b/b
P5 = 6% b/b
Analisa
HASIL DAN PEMBAHASAN
Pengaruh Konsentrasi Pati terhadap Parameter yang Diamati
Hasil penelitian yang dilakukan menunjukkan bahwa konsentrasi pati memberikan pengaruh terhadap susut bobot, total asam, kadar vitamin C, total soluble solid, kadar tanin, total mikroba, organoleptik warna, aroma, rasa, dan tekstur seperti yang terlihat pada Tabel 5.
Tabel 5. Pengaruh konsentrasi pati terhadap parameter mutu salak terolah minimal yang diamati
Parameter mutu
Pengaruh konsentrasi pati (P) P1
(2%)
P2
(3%)
P3
(4%)
P4
(5%)
P5
(6%)
Susut bobot (%) 1,344 1,175 1,077 0,969 0,957
Total asam (%) 0,531 0,546 0,608 0,613 0,631
Kadar vitamin C (mg/100 g) 17,013 17,893 20,827 21,120 21,560
Total soluble solid (oBrix) 7,681 7,693 7,940 8,136 8,603
Kadar tanin (%) 0,312 0,326 0,343 0,319 0,308
Total mikroba (CFU/g) 6,262 5,900 5,877 5,845 5,457 Organoleptik warna, rasa,
aroma(hedonik) 2,722 2,478 2,700 2,621 2,544
Organoleptik tekstur (skor) 2,633 2,711 2,822 2,856 2,900 Tabel 5 menunjukkan susut bobot tertinggi pada perlakuan P1 yaitu
1,344%dan terendah pada P2 yaitu 0,957%. Total asam tertinggi pada perlakuan
P5 yaitu 0,631% dan terendah pada P1 yaitu 0,531%. Kadar vitamin C tertinggi
pada perlakuan P5 yaitu 21,560 mg/100 g dan terendah pada P1 yaitu
17,013 mg/100 g. Total soluble solid tertinggi pada perlakuan P5 yaitu 8,603 oBrix
dan terendah pada P1 yaitu 7,681 oBrix.
Kadar tanin tertinggi pada perlakuan P3 0,343%dan terendah pada P5 yaitu
0,308%. Total mikroba tertinggi pada perlakuan P1 yaitu 6,262 CFU/g dan
terendah pada P5 yaitu 5,457 CFU/g. Nilai organoleptik warna, rasa, aroma
organoleptik tekstur tertinggi pada perlakuan P5 yaitu 2,900dan terendah pada P1
yaitu 2,633.
Pengaruh Lama Penyimpanan terhadap Parameter yang Diamati
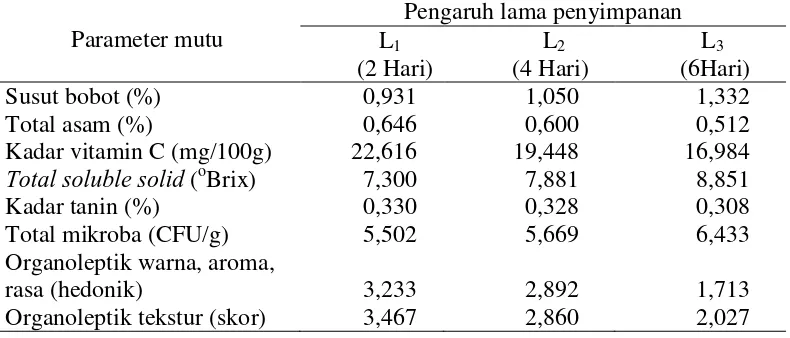
[image:30.595.116.511.321.490.2]Hasil penelitian yang dilakukan menunjukkan bahwa lama penyimpanan memberikan pengaruh terhadap susut bobot, total asam, kadar vitamin C, total soluble solid, kadar tanin, total mikroba, organoleptik warna, aroma, rasa, dan tekstur seperti yang terlihat pada Tabel 6.
Tabel 6. Pengaruh lama penyimpanan terhadap parameter mutu salak terolah minimal yang diamati
Parameter mutu
Pengaruh lama penyimpanan L1
(2 Hari)
L2
(4 Hari)
L3
(6Hari)
Susut bobot (%) 0,931 1,050 1,332
Total asam (%) 0,646 0,600 0,512
Kadar vitamin C (mg/100g) 22,616 19,448 16,984
Total soluble solid (oBrix) 7,300 7,881 8,851
Kadar tanin (%) 0,330 0,328 0,308
Total mikroba (CFU/g) 5,502 5,669 6,433
Organoleptik warna, aroma,
rasa (hedonik) 3,233 2,892 1,713
Organoleptik tekstur (skor) 3,467 2,860 2,027 Tabel 6 menunjukkan susut bobot tertinggi pada perlakuan L3 yaitu
1,332%dan terendah pada L1 yaitu 0,931%. Total asam tertinggi pada perlakuan
L1 yaitu 0,646% dan terendah pada L3 yaitu 0,512%. Kadar vitamin C tertinggi
pada perlakuan L1 yaitu 22,616 mg/100 g dan terendah pada L3 yaitu
16,984 mg/100 g. Total soluble solid tertinggi pada perlakuan L3 yaitu
8,851 oBrix dan terendah pada L1 yaitu 7,300 oBrix.
Kadar tanin tertinggi pada perlakuan L1 0,330% dan terendah L3 yaitu
0,308%. Total mikroba tertinggi pada perlakuan L3 yaitu 6,433 CFU/g dan
pada perlakuan L1 yaitu 3,233 dan terendah L3 1,713. Nilai organoleptik tekstur
tertinggi pada perlakuan L1 yaitu 3,467dan terendah L3 yaitu 2,027.
Susut Bobot (%)
Pengaruh konsentrasi pati terhadap susut bobot (%)
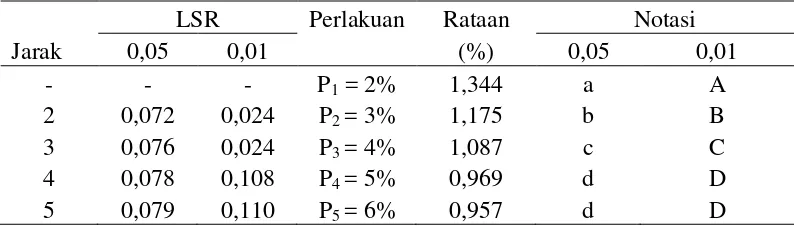
[image:31.595.113.510.333.446.2]Daftar analisis sidik ragam (Lampiran 1) menunjukkan bahwa konsentrasi pati berbeda sangat nyata (P<0,01) terhadap susut bobot (%) buah salak terolah minimal. Hasil uji LSR pengaruh konsentrasi pati terhadap susut bobot dapat dilihat pada Tabel 7.
Tabel 7. Uji LSR efek utama pengaruh konsentrasi pati terhadap susut bobot (%) Jarak
LSR Perlakuan Rataan Notasi
0,05 0,01 (%) 0,05 0,01
- - - P1 = 2% 1,344 a A
2 0,072 0,024 P2 = 3% 1,175 b B
3 0,076 0,024 P3 = 4% 1,087 c C
4 0,078 0,108 P4 = 5% 0,969 d D
5 0,079 0,110 P5 = 6% 0,957 d D
Keterangan : Notasi huruf yang berbeda menunjukkan pengaruh berbeda nyata pada taraf 5% (huruf kecil) dan berbeda sangat nyata pada taraf 1% (huruf besar).
Tabel 7 menunjukkan bahwa perlakuan P1 berbeda sangat nyata dengan
P2, P3, P4, dan P5. Perlakuan P2 berbeda sangat nyata dengan P3, P4 , dan P5.
Perlakuan P3 berbeda sangat nyata dengan P4, dan P5.Perlakuan P4 berbeda tidak
nyata dengan P5. Susut bobot tertinggi pada perlakuan P1 yaitu 1,344% dan
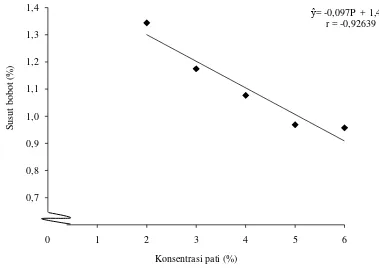
terendah pada perlakuan P5 yaitu 0,957%. Hubungan konsentrasi pati dengan susut
bobot dapat dilihat pada Gambar 5.
transpirasi pada buah akan terhambat sehingga akan mengurangi terjadinya dehidrasi dan penyusutan buah (Zhao, 2007).
Gambar 5. Hubungan konsentrasi pati dengan susut bobot
Pengaruh lama penyimpanan terhadap susut bobot (%)
[image:32.595.109.514.593.667.2]Hasil analisis sidik ragam (Lampiran 1) menunjukkan bahwa lama penyimpanan berbeda sangat nyata (P<0,01) terhadap susut bobot. Hasil uji LSR pengaruh konsentrasi pati terhadap susut bobot dapat dilihat pada Tabel 8.
Tabel 8. Uji LSR efek utama pengaruh lama penyimpanan terhadap susut bobot (%) Jarak
LSR Perlakuan
Rataan (%)
Notasi
0,05 0,01 0,05 0,01
- - - L1 = 2 hari 0,931 c C
2 0,056 0,077 L2 = 4 hari 0,105 b B
3 0,059 0,081 L3 = 6 hari 1,332 a A
Keterangan : Notasi huruf yang berbeda menunjukkan pengaruh berbeda nyata pada taraf 5% (huruf kecil) dan berbeda sangat nyata pada taraf 1% (huruf besar).
Tabel 8 menunjukkan bahwa masing-masing perlakuan berbeda sangat nyata dengan perlakuan lainnya. Susut bobot tertinggi pada perlakuan L3 yaitu
ŷ= -0,097P + 1,495 r = -0,92639
0,6 0,7 0,8 0,9 1,0 1,1 1,2 1,3 1,4
0 1 2 3 4 5 6
S
u
su
t
bobot
(
%
)
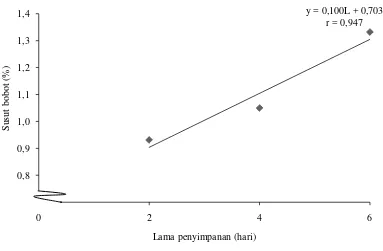
1,332% dan terendah pada L1 yaitu 0,931%. Hubungan lama penyimpanan
[image:33.595.117.500.140.391.2]dengan susut bobot dapat dilihat pada Gambar 6.
Gambar 6. Hubungan lama penyimpanan dengan susut bobot
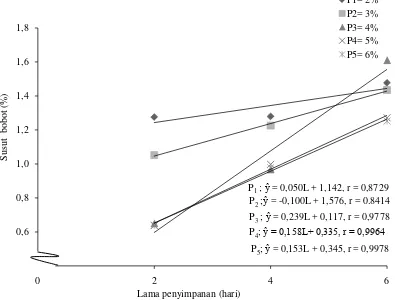
Gambar 6 menunjukkan bahwa semakin lama penyimpanan maka susut bobot salak terolah minimal semakin tinggi. Transpirasi akan terjadi selama penyimpanan buah yang mengakibatkan kehilangan air, penurunan mutu dan menimbulkan kerusakan(Novita, dkk., 2012).
Pengaruh interaksi konsentrasi pati dan lama penyimpanan terhadap susut bobot (%)
Daftar analisis sidik ragam (Lampiran 1) menunjukkan bahwa interaksi konsentrasi pati dan lama penyimpanan berbeda sangat nyata (P<0,01) terhadap susut bobot salak terolah minimal. Hasil uji LSR pengaruh interaksi konsentrasi pati dan lama penyimpanan terhadap susut bobot dapat dilihat pada Tabel 9.
y = 0,100L + 0,703 r = 0,947
0,7 0,8 0,9 1,0 1,1 1,2 1,3 1,4
0 2 4 6
S
u
su
t
bobot
(
%
)
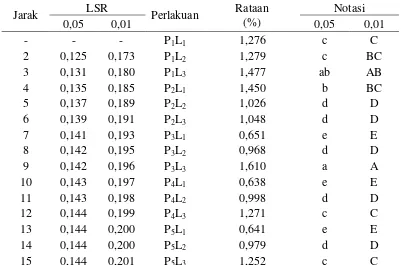
Tabel 9. Uji LSR pengaruh interaksi konsentrasi pati dan lama penyimpanan terhadap susut bobot salak (%)
Jarak LSR Perlakuan Rataan
(%)
Notasi
0,05 0,01 0,05 0,01
- - - P1L1 1,276 c C
2 0,125 0,173 P1L2 1,279 c BC
3 0,131 0,180 P1L3 1,477 ab AB
4 0,135 0,185 P2L1 1,450 b BC
5 0,137 0,189 P2L2 1,026 d D
6 0,139 0,191 P2L3 1,048 d D
7 0,141 0,193 P3L1 0,651 e E
8 0,142 0,195 P3L2 0,968 d D
9 0,142 0,196 P3L3 1,610 a A
10 0,143 0,197 P4L1 0,638 e E
11 0,143 0,198 P4L2 0,998 d D
12 0,144 0,199 P4L3 1,271 c C
13 0,144 0,200 P5L1 0,641 e E
14 0,144 0,200 P5L2 0,979 d D
15 0,144 0,201 P5L3 1,252 c C
Keterangan : Notasi huruf yang berbeda menunjukkan pengaruh berbeda nyata pada taraf 5% (huruf kecil) dan berbeda sangat nyata pada taraf 1% (huruf besar).
Tabel 9 menunjukkan bahwa interaksi perlakuan antara konsentrasi pati dan lama penyimpanan terhadap susut bobot berpengaruh sangat nyata. Susut bobot terendah diperoleh pada interaksi P4L1 (konsentrasi pati 5% dan lama
penyimpanan 2 hari) yaitu 0,638% dan tertinggi diperoleh pada interaksi P3L3
(konsentrasi pati 4% dan lama penyimpanan 6 hari) yaitu 1, 610%.
akan terjadi selama penyimpanan buah yang mengakibatkan kehilangan air, penurunan mutu dan menimbulkan kerusakan(Novita, dkk., 2012).
Gambar 7. Hubungan interaksi konsentrasi pati dan lama penyimpanan dengan susut bobot (%)
Total Asam
Pengaruh konsentrasi pati terhadap total asam (%)
[image:35.595.113.510.698.749.2]Daftar analisis ragam (Lampiran 2) menunjukkan bahwa konsentrasi pati berbeda sangat nyata (P<0,01) terhadap total asam buah salak terolah minimal. Hasil uji LSR pengaruh konsentrasi pati terhadap total asam dapat dilihat pada Tabel 10.
Tabel 10. Uji LSR efek utama pengaruh konsentrasi pati terhadap total asam (%)
Jarak LSR Perlakuan Rataan
(%)
Notasi
0,05 0,01 0,05 0,01
- - - P1 = 2% 0,531 b B
P1; ŷ= 0,050L + 1,142, r = 0,8729 P2;ŷ= -0,100L + 1,576, r = 0.8414 P3; ŷ= 0,239L + 0,117, r = 0,9778 P4; ŷ = 0,158L+ 0,335, r = 0,9964
P5; ŷ = 0,153L + 0,345, r = 0,9978 0,4 0,6 0,8 1,0 1,2 1,4 1,6 1,8
0 2 4 6
S u su t bobot ( % )
Lama penyimpanan (hari)
2 0,035 0,048 P2 = 3% 0,546 b B
3 0,036 0,050 P3 = 4% 0,608 a A
4 0,037 0,052 P4 = 5% 0,613 a A
5 0,038 0,053 P5 = 6% 0,631 a A
[image:36.595.115.509.84.149.2]Keterangan : Notasi huruf yang berbeda menunjukkan pengaruh berbeda nyata pada taraf 5% (huruf kecil) dan berbeda sangat nyata pada taraf 1% (huruf besar).
Tabel 10 menunjukkan bahwa perlakuan P1 berbeda tidak nyata dengan P2
dan berbeda sangat nyata dengan P3, P4, dan P5. Perlakuan P2 berbeda sangat
nyata dengan P3, P4, dan P5. Perlakuan P3 berbeda tidak nyata dengan P4 dan P5.
Perlakuan P4 berbeda tidak nyata dengan P5. Hubungan konsentrasi pati dengan
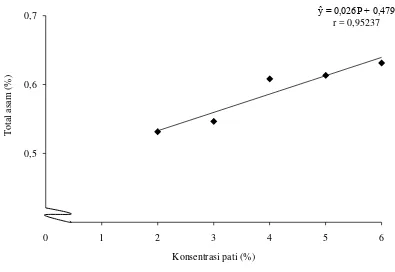
[image:36.595.117.512.331.603.2]total asam dapat dilihat pada Gambar 8.
Gambar 8. Hubungan konsentrasi pati dengan total asam
Gambar 8 menunjukkan bahwa semakin tinggi konsentrasi pati maka total asam akan semakin besar. Hal ini dikarenakan terjadinya penurunan laju respirasi sehingga perombakan asam menjadi gula akan terhambat. Menurut Winarti, dkk (2012) pelapis edibel dari polisakarida dapat berperan sebagai membran
ŷ = 0,026P + 0,479 r = 0,95237
0,4 0,5 0,6 0,7
0 1 2 3 4 5 6
T
o
tal
as
am
(
%
)
permeabel yang selektif terhadap pertukaran gas CO2 dan O2 sehingga laju
respirasi akan menurun. Menurut Nunes dan Emond (2003) karbohidrat dan asam organik merupakan komponen yang berperan penting dalam metabolisme produk hortikultura terutama untuk proses respirasi. Peningkatan laju respirasi akan mengakibatkan terjadinya perombakan karbohidrat dan asam organik menjadi glukosa.
Pengaruh lama penyimpanan terhadap total asam (%)
[image:37.595.115.515.419.496.2]Daftar analisis sidik ragam (Lampiran 2) menunjukkan bahwa lama penyimpanan berbeda sangat nyata (P<0,01) terhadap total asam salak terolah minimal. Hasil uji LSR pengaruh konsentrasi pati terhadap total asam dapat dilihat pada Tabel 11.
Tabel 11. Uji LSR efek utama pengaruh lama penyimpanan terhadap total asam (%)
Jarak LSR Perlakuan Rataan
(%)
Notasi
0,05 0,01 0,05 0,01
- - - L1 = 2 hari 0,647 a A
2 0,027 0,037 L2 = 4 hari 0,600 b B
3 0,028 0,039 L3 = 6 hari 0,512 c C
Keterangan : Notasi huruf yang berbeda menunjukkan pengaruh berbeda nyata pada taraf 5% (huruf kecil) dan berbeda sangat nyata pada taraf 1% (huruf besar).
Tabel 11 menunjukkan bahwa masing-masing perlakuan berbeda sangat nyata dengan perlakuan lainnya. Total asam tertinggi terdapat pada perlakuan L1 yaitu 0,647% dan terendah pada perlakuan L3 yaitu 0,512%. Hubungan lama
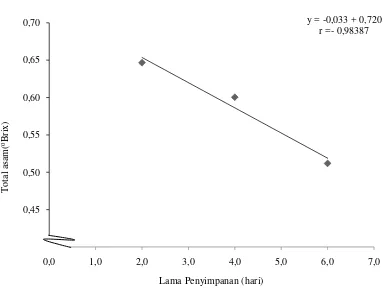
Gambar 9. Hubungan lama penyimpanan dengan total asam
Gambar 9 menunjukkan bahwa semakin lama penyimpanan maka total asam akan semakin menurun. Selama penyimpanan buah dapat terjadi penurunan total asam jika buah telah lewat matang karena asam dikonversi menjadi gula sehingga total padatan terlarut akan meningkat (Wills, dkk., 2007).
Pengaruh interaksi konsentrasi pati dan lama penyimpanan terhadap total asam (%)
Daftar analisis sidik ragam (Lampiran 2) menunjukkan bahwa interaksi konsentrasi pati dan lama penyimpanan berbeda nyata (P<0,05) terhadap total asam salak terolah minimal. Hasil uji LSR pengaruh interaksi konsentrasi pati dan lama penyimpanan terhadap total asam dapat dilihat pada Tabel 12.
y = -0,033 + 0,720 r =- 0,98387
0,40 0,45 0,50 0,55 0,60 0,65 0,70
0,0 1,0 2,0 3,0 4,0 5,0 6,0 7,0
T
o
tal
as
am
(
oB
ri
x
)
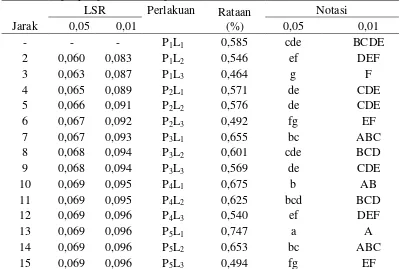
Tabel 12. Uji LSR efek utama pengaruh interaksi konsentrasi pati dan lama penyimpanan terhadap total asam (%)
Jarak
LSR Perlakuan Rataan (%)
Notasi
0,05 0,01 0,05 0,01
- - - P1L1 0,585 cde BCDE
2 0,060 0,083 P1L2 0,546 ef DEF
3 0,063 0,087 P1L3 0,464 g F
4 0,065 0,089 P2L1 0,571 de CDE
5 0,066 0,091 P2L2 0,576 de CDE
6 0,067 0,092 P2L3 0,492 fg EF
7 0,067 0,093 P3L1 0,655 bc ABC
8 0,068 0,094 P3L2 0,601 cde BCD
9 0,068 0,094 P3L3 0,569 de CDE
10 0,069 0,095 P4L1 0,675 b AB
11 0,069 0,095 P4L2 0,625 bcd BCD
12 0,069 0,096 P4L3 0,540 ef DEF
13 0,069 0,096 P5L1 0,747 a A
14 0,069 0,096 P5L2 0,653 bc ABC
15 0,069 0,096 P5L3 0,494 fg EF
Keterangan : Notasi huruf yang berbeda menunjukkan pengaruh berbeda nyata pada taraf 5% (huruf kecil) dan berbeda sangat nyata pada taraf 1% (huruf besar)
Tabel 12 menunjukkan bahwa interaksi konsentrasi pati dan lama penyimpanan berbeda nyata terhadap total asam salak terolah minimal. Total asam terendah diperoleh pada interaksi P1L3 (konsentrasi pati 2% dan lama
penyimpanan 6 hari) yaitu 0,464% sedangkan total asam tertinggi diperoleh pada interaksi P5L1 (konsentrasi pati 6% dan lama penyimpanan 2 hari) yaitu 0,747%.
Gambar 10. Hubungan interaksi konsentrasi pati dan lama penyimpanan dengan total asam
Gambar 10 menunjukkan bahwa semakin rendah konsentrasi pati dan semakin lama penyimpanan maka total asam semakin menurun. Hal ini terjadi karena pelapisan salak dengan pelapis edibel akan menurunkan laju respirasi dan kandungan asam dapat dipertahankan. Pelapisan buah dengan polisakarida akan menurunkan laju respirasi karena polisakarida berperan sebagai membran yang mengatur pertukaran gas CO2 dan O2 (Winarti, dkk., 2011). Selama penyimpanan
buah akan terjadi aktivitas metabolik seperti respirasi dan transpirasi yang menyebabkan asam dikonversi menjadi gula sehingga kandungan asam pada bahan akan menurun (Rahmawati, 2011).
Kadar Vitamin C (mg/100 g)
Pengaruh konsentrasi pati terhadap kadar vitamin C (mg/100 g)
Daftar analisis ragam (Lampiran 3) menunjukkan bahwa konsentrasi pati berbeda sangat nyata (P<0,01) terhadap kadar vitamin C (mg/100 g) salak terolah
P1; ŷ = -0,030L+ 0,652, r = -0,97787 P2; ŷ= -0,019L + 0,625, r = -0,83726 P3; ŷ = -0,021L + 0,693, r= -0,99843 P4; ŷ = -0,033L + 0,748, r = -0,98843
P5; ŷ = -0,063L + 0,884, r = -0,98894 0,40
0,45 0,50 0,55 0,60 0,65 0,70 0,75
0 2 4 6
T
o
tal
as
am
(
%
)
Lama penyimpanan (hari)
minimal. Hasil uji LSR pengaruh konsentrasi pati terhadap kadar vitamin C dapat dilihat pada Tabel 13.
Tabel 13. Uji LSR efek utama pengaruh konsentrasi pati terhadap kadar vitamin C (mg/100 g)
Jarak LSR Perlakuan Rataan
(mg/100g)
Notasi
0,05 0,01 0,05 0,01
- - - P1 = 2% 17,013 b C
2 2,201 3,049 P2 = 3% 17,893 b BC
3 2,310 3,195 P3 = 4% 20,827 a AB
4 2,376 3,290 P4 = 5% 21,120 a AB
5 2,420 3,349 P5 = 6% 21,560 a A
Keterangan : Notasi huruf yang berbeda menunjukkan pengaruh berbeda nyata pada taraf 5% (huruf kecil) dan berbeda sangat nyata pada taraf 1% (huruf besar).
Tabel 13 menunjukkan bahwa perlakuan P1 berbeda nyata dengan P2,
berbeda sangat nyata dengan P3,P4, dan P5. Perlakuan P2 berbeda nyata dengan P3
danP4, berbeda sangat nyata dengan P5. Perlakuan P3 berbeda tidak nyata dengan
P4, berbeda nyata dengan P5. Perlakuan P4 berbeda nyata dengan P5.Hubungan
[image:41.595.122.513.455.713.2]konsentrasi pati dengan kadar vitamin C dapat dilihat pada Gambar 11.
Gambar 11. Hubungan konsentrasi pati dengan kadar vitamin C
ŷ = 1,232P + 14,75 r = 0,9386
15 16 17 18 19 20 21 22
0 1 2 3 4 5 6
K ad ar vi ta m in C ( m g/ 1 0 0 g)
Semakin tinggi konsentrasi pati maka kadar vitamin C salak terolah minimal semakin meningkat. Peningkatan kadar vitamin C terjadi karena salak yang dilapisi dengan pelapis yang lebih tebal lebih sedikit kehilangan air sehingga
akan mempertahankan kadar vitamin C buah.
Menurut Baldwin (2003) pelapisan buah atau sayur dengan pelapis edibel
dapat mencegah penguapan air. Winarno (2008) menyatakan bahwa asam
askorbat merupakan vitamin yang larut air yang berbentuk sebagai asam
L-askorbat dan asam L-dehidroaskorbat.
Pengaruh lama penyimpanan terhadap kadar vitamin C
Daftar analisis sidik ragam (Lampiran 3) menunjukkan bahwa lama penyimpanan berbeda sangat nyata (P<0,01) terhadap kadar vitamin C salak terolah minimal. Hasil uji LSR pengaruh konsentrasi pati terhadap kadar vitamin C dapat dilihat pada Tabel 14.
Tabel 14. Uji LSR efek utama pengaruh lama penyimpanan terhadap kadar vitamin C (mg/100 g)
Jarak
LSR Perlakuan Rataan
(mg/100 g)
Notasi
0,05 0,01 0,05 0,01
- - - L1 = 2 hari 22,616 a A
2 0,930 1,289 L2 = 4 hari 19,448 b B
3 0,977 1,351 L3 = 6 hari 16,984 c C
Keterangan : Notasi huruf yang berbeda menunjukkan pengaruh berbeda nyata pada taraf 5% (huruf kecil) dan berbeda sangat nyata pada taraf 1% (huruf besar).
Tabel 14 menunjukkan bahwa masing-masing perlakuan berbeda sangat nyata dengan perlakuan lainnya. Kadar vitamin C tertinggi pada perlakuan L1
yaitu 22,616 mg/100 g dan terendah pada L3 yaitu 16,984 mg/100 g. Hubungan
Gambar 12. Hubungan lama penyimpanan dengan kadar vitamin C
Gambar 12 menunjukkan bahwa semakin lama penyimpanan maka kadar vitamin C semakin menurun karena selama penyimpanan terjadi degradasi vitamin C yang dipengaruhi suhu, cahaya maupun udara. Vitamin C pada bahan pangan akan semakin menurun bersamaan dengan kenaikan suhu dan semakin lamanya penyimpanan (Nunes dan Emond, 2003).
Pengaruh interaksi konsentrasi pati dan lama penyimpanan terhadap kadar vitamin C (mg/100 g)
[image:43.595.114.511.708.757.2]Daftar analisis sidik ragam (Lampiran 3) menunjukkan bahwa interaksi konsentrasi pati dan lama penyimpanan memberikan pengaruh berbeda nyata (P<0,01) terhadap kadar vitamin C salak terolah minimal. Hasil uji LSR pengaruh interaksi konsentrasi pati dan lama penyimpanan terhadap kadar vitamin C dapat dilihat pada Tabel 15.
Tabel 15. Uji LSR pengaruh interaksi konsentrasi pati dan lama penyimpanan terhadap kadar vitamin C (mg/100g)
Jarak LSR Perlakuan Rataan
(mg/100g)
Notasi
0,05 0,01 0,05 0,01
- - - P1L1 19,360 de CDE
ŷ= -1,408L + 25,31 r = -0,997
15 16 17 18 19 20 21 22 23
0 2 4 6
K ad ar vi ta m in C ( m g/ 1 0 0 g)
2 2,083 2,880 P1L2 17,160 ef DEF
3 2,184 3,003 P1L3 14,520 g F
4 2,246 3,084 P2L1 18,920 de CDE
5 2,289 3,142 P2L2 18,480 def DE
6 2,319 3,186 P2L3 16,280 fg EF
7 2,342 3,220 P3L1 24,200 ab AB
8 2,359 3,248 P3L2 19,800 de CD
9 2,372 3,271 P3L3 18,480 def DE
10 2,381 3,289 P4L1 25,520 a A
11 2,389 3305 P4L2 19,800 cd CD
12 2,394 3,319 P4L3 18,040 def DE
13 2,399 3,331 P5L1 25,080 a AB
14 2,402 3,341 P5L2 22,000 bc BC
15 2,403 3,349 P5L3 17,600 def DEF
[image:44.595.124.504.80.307.2]Keterangan : Notasi huruf yang berbeda menunjukkan pengaruh berbeda nyata pada taraf 5% (huruf kecil) dan berbeda sangat nyata pada taraf 1% (huruf besar).
Tabel 15 menunjukkan bahwa interaksi perlakuan konsentrasi pati dan lama penyimpanan berbeda nyata terhadap kadar vitamin C salak terolah minimal. Kadar vitamin C tertinggi diperoleh pada interaksi P4L1 (konsentrasi pati 5% dan
lama penyimpanan 2 hari) yaitu 25,520 mg/100 g sedangkan yang terendah diperoleh pada interaksi P1L3 (konsentrasi pati 2% dan lama penyimpanan 6 hari)
Gambar 13. Hubungan interaksi konsentrasi pati dan lama penyimpanan dengan kadar vitamin C
Pelapisan buah dengan polisakarida akan menurunkan laju respirasi dan mencegah oksidasi. Penurunan oksigen menghambat terjadinya degradasi asam askorbat menjadi asam dehidroaskorbat dan H2O2. Peningkatan H2O2 akan
mempercepat kerusakan asam askorbat karena terjadi autooksidasi (Tannenbaum 1976 dalam Rudito, 2005). Selama pertumbuhan dan perkembangan buah kandungan asam askorbat meningkat dan mencapai maksimal kemudian selama pematangan dan senesensi akan menurun.
Total soluble solid (oBrix)
Pengaruh konsentrasi pati terhadap total soluble solid (oBrix)
Daftar analisis ragam (Lampiran 4) menunjukkan bahwa konsentrasi pati memberikan pengaruh berbeda sangat nyata (P<0,01) terhadap total soluble solid
buah salak terolah minimal. Hasil uji LSR pengaruh konsentrasi pati terhadap
total soluble solid dapat dilihat pada Tabel 16.
P1; ŷ = -1,21L + 21,85, r = - 0,9985 P2' ŷ= -0,66L + 20,53,r = - 0,9333 P3; ŷ= -1,43L + 26,54, r = -0,9545 P4; ŷ= -1,87L + 28,6, r = -0,9560 P5; ŷ= -1,87L + 29,04, r = -0,9945 10 12 14 16 18 20 22 24 26
0 2 4 6
K ad ar vi ta m in C ( m g/ 1 0 0 g)
Lama penyimpanan (hari)
Tabel 16. Uji LSR efek utama pengaruh konsentrasi pati terhadap total soluble solid (oBrix)
Jarak LSR Perlakuan Rataan Notasi
0,05 0,01 (oBrix) 0,05 0,01
- - - P1 = 2% 7,681 b B
2 0,465 0,644 P2 = 3% 7,693 b B
3 0,488 0,675 P3 = 4% 7,940 b AB
4 0,502 0,695 P4 = 5% 8,136 ab AB
5 0,511 0,707 P5 = 6% 8,603 a A
Keterangan : Notasi huruf yang berbeda menunjukkan pengaruh berbeda nyata pada taraf 5% (huruf kecil) dan berbeda sangat nyata pada taraf 1% (huruf besar).
Tabel 16 menunjukkan bahwa perlakuan P1 berbeda tidak nyata dengan P2,
berbeda nyata dengan P3 dan P4, dan berbeda sangat nyata dengan P5. Perlakuan
P2 berbeda nyata dengan P3 dan P4, berbeda sangat nyata dengan P5. Perlakuan P3
berbeda tidak nyata dengan P4, berbeda nyata dengan P5. Perlakuan P4 berbeda
nyata dengan P5. Hubungan konsentrasi pati dengan total soluble solid dapat
[image:46.595.164.435.440.646.2]dilihat pada Gambar 14.
Gambar 14. Hubungan konsentrasi pati dengan total soluble solid
Gambar 14 menunjukkan bahwa semakin tinggi konsentrasi pati maka semakin tinggi total soluble solid. Hal ini karena aplikasi pelapis edibel akan menurunkan laju respirasi pada buah yang mengakibatkan total soluble solid
ŷ = 0,228P + 7,095 r = 0,9482
7,0 7,4 7,8 8,2 8,6 9,0
0 1 2 3 4 5 6
T ot al s ol ubl e s ol id ( oB ri x)
meningkat. Crisosto, dkk (1993) dalam Helmiyesi, dkk (2008) menyatakan bahwa respirasi akan mengakibatkan penurunan komponen total padatan terlarut
karena komponen tersebut digunakan sebagai substrat dalam proses respirasi.
Berdasarkan hasil penelitian Santoso dan Wirawan (2015) pelapis edibeldari pati biji nangka dengan konsentrasi 3% dapat mencegah penurunan gula reduksi buah salak selama penyimpanan.
Pengaruh lama penyimpanan terhadap total soluble solid (oBrix)
[image:47.595.113.509.431.512.2]Daftar analisis ragam (Lampiran 4) menunjukkan bahwa lama penyimpanan berbeda sangat nyata (P<0,01) terhadap total soluble solid salak terolah minimal. Hasil uji LSR pengaruh lama penyimpanan terhadap total soluble solid dapat dilihat pada Tabel 17.
Tabel 17. Uji LSR efek utama pengaruh lama penyimpanan terhadap total soluble solid (oBrix)
Jarak LSR Perlakuan Rataan
(oBrix)
Notasi
0,05 0,01 0,05 0,01
- - - L1 = 2 hari 7,300 c C
2 0,360 0,499 L2 = 4 hari 7,881 b B
3 0,378 0,523 L3 = 6 hari 8,851 a A
Keterangan : Notasi huruf yang berbeda menunjukkan pengaruh berbeda nyata pada taraf 5% (huruf kecil) dan berbeda sangat nyata pada taraf 1% (huruf besar).
Tabel 17 menunjukkan bahwa masing-masing perlakuan berbeda sangat nyata dengan perlakuan lainnya. Total soluble solid tertinggi terdapat pada perlakuan L3 yaitu 8,851 oBrix dan terendah pada L1 yaitu 7,300 oBrix. Hubungan
Gambar 15. Hubungan lama penyimpanan dengan total soluble solid
Total soluble solid meningkat karena terjadi pembentukan gula-gula reduksi yang sesuai dengan pernyataan Wills, dkk (2007) bahwa selama penyimpanan buah zat pati dihidrolisis menjadi sukrosa yang kemudian menjadi gula reduksi dan digunakan untuk respirasi.
Pengaruh interaksi konsentrasi pati dan lama penyimpanan terhadap total soluble solid (oBrix)
Daftar analisis sidik ragam (Lampiran 4) menunjukkan bahwa interaksi konsentrasi pati dan lama penyimpanan berbeda sangat nyata (P<0,01) terhadap
total soluble solid salak terolah minimal. Hasil uji LSR pengaruh interaksi konsentrasi pati dan lama penyimpanan terhadap total soluble solid dapat dilihat pada Tabel 18.
Tabel 18 menunjukkan bahwa interaksi konsentrasi pati dan lama penyimpanan memberikan pengaruh sangat nyata terhadap total soluble solid
salak terolah minimal. Total soluble solid terendah diperoleh pada P1L1
(konsentrasi pati 2% dan lama penyimpanan 2 hari) yaitu 6,153 oBrix sedangkan y = 0,387L + 6,459
r = 0,9894
6,6 7,0 7,4 7,8 8,2 8,6 9,0
0 2 4 6
T
ot
al
s
ol
ubl
e s
ol
id
(o
B
ri
x
)
yang tertinggi P1L3 (konsentrasi pati 2% dan lama penyimpanan 6 hari) yaitu
[image:49.595.109.513.171.439.2]9,190 oBrix.
Tabel 18. Uji LSR efek utama pengaruh interaksi konsentrasi pati dan lama penyimpanan terhadap total soluble solid (oBrix)
Jarak LSR Perlakuan Rataan
(oBrix)
Notasi
0,05 0,01 0,05 0,01
- - - P1L1 6,153 e D
2 0,806 1,114 P1L2 7,699 cd BC
3 0,845 1,162 P1L3 9,190 a A
4 0,869 1,193 P2L1 7,351 def C
5 0,885 1,216 P2L2 7,539 def C
6 0,897 1,233 P2L3 8,189 bc ABC
7 0,906 1,246 P3L1 7,317 def C
8 0,912 1,257 P3L2 7,370 def C
9 0,918 1,265 P3L3 9,167 a A
10 0,921 1,273 P4L1 7,958 cd ABC
11 0,924 1,279 P4L2 7,900 cd ABC
12 0,926 1,284 P4L3 8,549 abc ABC
13 0,928 1,289 P5L1 7,721 cd BC
14 0,929 1,292 P5L2 8,929 ab AB
15 0,930 1,296 P5L3 9,160 a A
Keterangan : Notasi huruf yang berbeda menunjukkan pengaruh berbeda nyata pada taraf 5% (huruf kecil) dan berbeda sangat nyata pada taraf 1% (huruf besar).
Gambar 16. Hubungan interaksi konsentrasi pati dan lama penyimpanan dengan total soluble solid
Total soluble solid meningkat selama penyimpanan karena terjadi pembentukan gula-gula reduksi sesuai dengan pernyataan Wills, dkk (2007) bahwa selama penyimpanan buah zat pati dihidrolisis menjadi sukrosa yang kemudian menjadi gula reduksi dan digunakan untuk respirasi.
Kadar Tanin (%)
Pengaruh konsentrasi pati terhadap kadar tanin (%)
Daftar analisis sidik ragam (Lampiran 5) menunjukkan bahwa konsentrasi pati berbeda tidak nyata (P>0,05) terhadap kadar tanin buah salak yang diperoleh, sehingga pengujian LSR tidak dilanjutkan.
Pengaruh lama penyimpanan terhadap kadar tanin (%)
Daftar analisis sidik ragam (Lampiran 5) menunjukkan bahwa lama penyimpanan berbeda tidak nyata (P>0,05) terhadap kadar tanin buah salak yang diperoleh, sehingga pengujian LSR tidak dilanjutkan.
P1; ŷ= 0,759L + 4,643, r = 0,9995 P2; ŷ= 0,209L + 6,854, r = 0,9529 P3; ŷ= 0,462L+ 6,089, r = 0,8706 P4; ŷ= 0,147 L+ 7,544, r = 0,8222 P5; ŷ= 0,359L + 7,164, r =0,9306 5,2 5,8 6,4 7,0 7,6 8,2 8,8 9,4
0 2 4 6
T o ta l S o lu b le S o lid ( o B rix )
Lama Penyimpanan (hari)
Pengaruh interaksi konsentrasi dan lama penyimpanan terhadap kadar tanin (%)
Daftar analisis sidik ragam (Lampiran 5) menunjukkan bahwa interaksi konsentrasi pati dan lama penyimpanan berbeda tidak nyata (P>0,05) terhadap kadar tanin buah salak yang diperoleh, sehingga pengujian LSR tidak dilanjutkan.
Total Mikroba (CFU/g)
Pengaruh konsentrasi pati terhadap total mikroba (CFU/g)
Daftar analisis sidik ragam (Lampiran 6) menunjukkan bahwa konsentrasi pati berbeda tidak nyata (P>0,05) terhadap total mikroba buah salak terolah minimal yang diperoleh, sehingga pengujian LSR tidak dilanjutkan.
Pengaruh lama penyimpanan terhadap total mikroba (CFU/g)
Daftar analisis ragam (Lampiran 6) menunjukkan bahwa lama penyimpanan berbeda sangat nyata (P<0,01) terhadap total mikroba buah salak terolah minimal. Hasil uji LSR pengaruh konsentrasi pati terhadap susut bobot dapat dilihat pada Tabel 19.
Tabel 19. Uji LSR efek utama pengaruh lama penyimpanan terhadap total mikroba (CFU/g)
Jarak LSR Perlakuan Rataan
(CFU/g)
Notasi
0,05 0,01 0,05 0,01
- - - L1 = 2 hari 5,502 b B
2 0,386 0,535 L2 = 4 hari 5,669 b B
3 0,405 0,560 L3 = 6 hari 6,433 a A
Keterangan : Notasi huruf yang berbeda menunjukkan pengaruh berbeda nyata pada taraf 5% (huruf kecil) dan berbeda sangat nyata pada taraf 1% (huruf besar).
Tabel 19 menunjukkan perlakuan P1 berbeda tidak nyata dengan perlakuan
P2, berbeda sangat nyata dengan P3. Perlakuan P2 berbeda sangat nyata dengan P3.
L1 yaitu 5,502 CFU/g. Hubungan lama penyimpanan dengan total mikroba dapat
[image:52.595.158.413.152.361.2]dilihat pada Gambar 17.
Gambar 17. Hubungan lama penyimpanan dengan total mikroba
Gambar 17 menunjukkan bahwa semakin lama penyimpanan maka total mikroba semakin meningkat. Mikroba pada bahan pangan dapat tumbuh dan berkembang jika kondisi lingkungannya mendukung dan tersedia nutrisi selama penyimpanan (Suharyono dan Kurniadi, 2010).
Pengaruh interaksi konsentrasi pati dan lama penyimpanan terhadap total mikroba (CFU/g)
Daftar analisis sidik ragam (Lampiran 6) menunjukkan bahwa interaksi konsentrasi pati dan lama penyimpanan memberikan pengaruh berbeda tidak nyata (P>0,05) terhadap total mikroba salak terolah minimal yang diperoleh, sehingga pengujian LSR tidak dilanjutkan.
ŷ= 0,232L + 4,937
r = 0,9375
5,0 5,2 5,4 5,6 5,8 6,0 6,2 6,4 6,6
0 2 4 6
T
o
ta
l m
ik
ro
b
a
(C
F
U
/m
l)
Organoleptik Warna, Rasa, dan Aroma (hedonik)
Pengaruh konsentrasi pati terhadap organoleptik warna, rasa, dan aroma (hedonik)
Daftar analisis sidik ragam (Lampiran 7) menunjukkan bahwa konsentrasi pati berbeda tidak nyata (P>0,05) terhadap organoleptik warna, rasa, dan aroma yang diperoleh, sehingga pengujian LSR tidak dilanjutkan.
Pengaruh lama penyimpanan terhadap organoleptik warna, rasa, dan aroma (hedonik)
Daftar analisis ragam (Lampiran 7) menunjukkan bahwa lama penyimpanan berbeda sangat nyata (P<0,01) terhadap organoleptik warna, rasa, dan aroma buah salak terolah minimal. Hasil uji LSR pengaruh lama penyimpanan terhadap organoleptik warna, rasa, dan aroma dapat dilihat pada Tabel 20.
Tabel 20. Uji LSR efek utama pengaruh lama penyimpanan terhadap organoleptik warna, rasa, dan aroma (hedonik)
Jarak LSR Perlakuan Rataan Notasi
0,05 0,01 0,05 0,01
- - - L1 = 2 hari 3,233 a A
2 0,248 0,344 L2 = 4 hari 2,892 b A
3 0,261 0,361 L3 = 6 hari 1,713 c B Keterangan : Notasi huruf yang berbeda menunjukkan pengaruh berbeda nyata pada taraf 5%
(huruf kecil) dan berbeda sangat nyata pada taraf 1% (huruf besar).
Tabel 20 menunjukkan bahwa perlakuan P1 berbeda tidak nyata dengan P2,
berbeda sangat nyata dengan P3. Perlakuan P2 berbeda sangat nyata dengan P3.
Nilai organoleptik warna, rasa, dan aroma tertinggi terdapat pada perlakuan L1
yaitu 3,233 dan terendah pada L3 yaitu 1,71. Hubungan lama penyimpanan dengan
skor tekstur dapat dilihat pada Gambar 18.
penyimpanan terjadi perubahan pada karakteristik sensori buah sesuai dengan pernyataan Helmiyesi, dkk (2008) bahwa selama penyimpanan buah dapat terjadi perubahan warna, tekstur, rasa dan bau karena masih terjadi proses respirasi, transpirasi dan penuaan sehingga akan mengakibatkan perubahan berbagai kandungan produk.
Gambar 18. Hubungan lama penyimpanan dengan organoleptik warna, rasa, dan aroma
Pengaruh interaksi konsentrasi pati dan lama penyimpanan terhadap organoleptik warna, aroma, dan rasa (hedonik)
Daftar analisis sidik ragam (Lampiran 7) menunjukkan bahwa interaksi konsentrasi pati dan lama penyimpanan berbeda tidak nyata (P>0,05) terhadap organoleptik warna, aroma, rasa buah salak yang diperoleh, sehingga pengujian LSR tidak dilanjutkan.
ŷ= -0,38L + 4,133
r = -0,9528
1,0 1,5 2,0 2,5 3,0 3,5
0 2 4 6
O rg an o lep ti k w ar n a, ar o m a, r as a (h ed o n ik )
Skor Tekstur (numerik)
Pengaruh konsentrasi pati terhadap skor tekstur (numerik)
Daftar analisis sidik ragam (Lampiran 8) menunjukkan bahwa konsentrasi pati berbeda tidak nyata (P>0,05) terhadap skor tekstur yang diperoleh, sehingga pengujian LSR tidak dilanjutkan.
Pengaruh lama penyimpanan terhadap skor tekstur (numerik)
Daftar analisis sidik ragam (Lampiran 8) menunjukkan bahwa lama penyimpanan berbeda sangat nyata (P<0,01) terhadap skor tekstur (numerik) buah salak terolah minimal. Hasil uji LSR pengaruh lama penyimpanan terhadap skor tekstur dapat dilihat pada Tabel 21.
Tabel 21. Uji LSR efek utama pengaruh lama penyimpanan terhadap skor tekstur (numerik)
Jarak LSR Perlakuan Rataan Notasi
0,05 0,01 0,05 0,01
- - - L1 = 2 hari 3,467 a A
2 0,224 0,310 L2 = 4 hari 2,860 b B
3 0,235 0,325 L3 = 6 hari 2,027 c C
Keterangan : Notasi huruf yang berbeda menunjukkan pengaruh berbeda nyata pada taraf 5% (huruf kecil) dan berbeda sangat nyata pada taraf 1% (huruf besar).
Tabel 21 menunjukkan bahwa masing-masing perlakuan berbeda sangat nyata dengan perlakuan lainnya. Hubungan lama penyimpanan dengan skor tekstur dapat dilihat pada Gambar 19.
Gambar 19. Hubungan lama penyimpanan dengan skor tekstur
Pengaruh interaksi konsentrasi pati dan lama penyimpanan terhadap skor tekstur (numerik)
Daftar analisis sidik ragam (Lampiran 8) menunjukkan bahwa interaksi konsentrasi pati dan lama penyimpanan berbeda tidak nyata (P>0,05) terhadap tekstur buah salak yang diperoleh, sehingga pengujian LSR tidak dilanjutkan.
ŷ= -0,36L + 4,224
r = -0,9954
1,5 2,0 2,5 3,0 3,5
0 2 4 6
O
rga
no
le
p
ti
k t
eks
tur
(
S
ko
r)
KESIMPULAN
Kesimpulan
Dari hasil penelitian menunjukkan pengaruh konsentrasi pati dan lama penyimpanan terhadap parameter yang diamati dapat disimpulkan sebagai berikut: 1. Konsentrasi pati ubi jalar memberikan pengaruh berbeda sangat nyata
(P<0,01) terhadap susut bobot, total asam, kadar vitamin C, total soluble solid
dan memberikan pengaruh tidak nyata (P>0,05) terhadap kadar tanin, total mikro