SELULOSA MIKROFIBRIL DARI BATANG PISANG
SEBAGAI BAHAN BAKU FILM PLASTIK
EKA PRETTY FEBRIYANI
DEPARTEMEN KIMIA
FAKULTAS MATEMATIKA DAN ILMU PENGETAHUAN ALAM INSTITUT PERTANIAN BOGOR
PERNYATAAN MENGENAI SKRIPSI DAN SUMBER
INFORMASI SERTA PELIMPAHAN HAK CIPTA
Dengan ini saya menyatakan bahwa skripsi berjudul Selulosa Mikrofibril dari Batang Pisang sebagai Bahan Baku Film Plastik adalah benar karya saya dengan arahan komisi pembimbing dan belum diajukan dalam bentuk apa pun kepada perguruan tinggi mana pun. Sumber informasi yang berasal dari karya yang diterbitkan dari penulis lain telah disebutkan dalam teks yang dicantumkan dalam Daftar Pustaka di bagian akhir skripsi ini.
Dengan ini saya melimpahkan hak cipta dari karya tulis saya kepada Institut Pertanian Bogor.
Bogor, Agustus 2014
Eka Pretty Febriyani
ABSTRAK
EKA PRETTY FEBRIYANI. Selulosa Mikrofibril dari Batang Pisang sebagai Bahan Baku Film Plastik. Dibimbing oleh BETTY MARITA SOEBRATA dan SRI MULIJANI.
Batang pisang merupakan limbah lignoselulosa yang kandungan selulosanya bisa diisolasi dan dimanfaatkan sebagai bahan baku pembuatan film plastik. Selulosa berhasil diisolasi menggunakan metode kimia mekanik dan didapatkan selulosa mikrofibril dengan ukuran partikel 920 nm. Analisis gugus fungsi menggunakan spektroskopi inframerah membuktikan bahwa hasil isolasi adalah benar selulosa. Selulosa mikrofibril hasil isolasi dicampurkan dengan pati jagung dan gliserol sebagai pemlastis. Ragam pati jagung yang digunakan adalah 1.5, 1.75, 2.0, dan 3.0 g. Selulosa mikrofibril dan gliserol yang ditambahkan pada tiap ragam adalah 2.5 dan 1 g. Film plastik dengan jumlah pati 1.5 g menghasilkan nilai kuat tarik paling tinggiyaitu 13 MPa dan memiliki nilai permeabilitas uap air paling rendah, yaitu 2.3 ng m m-2 s-1 Pa-1. Film plastik yang mengandung pati 3.0 g memiliki elongasi paling tinggi, yaitu 11%. Mikrograf elektron parayan menunjukkan distribusi campuran film telah homogen.
Kata kunci: film plastik, selulosa mikrofibril, sifat fisik-mekanik, permeabilitas uap
ABSTRACT
EKA PRETTY FEBRIYANI. Microfibrillated Cellulose of Banana Stem as Plastic Film Material. Supervised by BETTY MARITA SOEBRATA and SRI MULIJANI.
Banana stem is a waste that contain lignoselulose from which cellulose can be isolated and used as raw material for plastic film. Cellulose was sucessfully isolated by mechanical chemical method giving 920 nm microfibrils. Functional group analysis by infrared spectroscopy proved that the isolated material was cellulose. The isolated microfibrils was mixed with corn starch and glicerol as plastisizer. Corn starch was added at various composition, i.e. 1.5, 1.75, 2.0, and 3.0 g. The microfibrillated cellulose and glicerol added into corn starch were 2.5 and 1 g, respectively. The plastic film with 1.5 g corn starch showed the highest tensile strength1 of 3 MPa and the lowest water vapor permeability 2.3 ng m m-2 s-1 Pa-1. The plastic film with 3 g corn starch gave the highest elongation rate of 11%. The scanning electron micrograph showed that the film component distribution was homogeneous.
SELULOSA MIKROFIBRIL DARI BATANG PISANG
SEBAGAI BAHAN BAKU FILM PLASTIK
EKA PRETTY FEBRIYANI
Skripsi
sebagai salah satu syarat untuk memperoleh gelar Sarjana Sains pada
Program Studi Kimia
DEPARTEMEN KIMIA
FAKULTAS MATEMATIKA DAN ILMU PENGETAHUAN ALAM INSTITUT PERTANIAN BOGOR
Judul Skripsi : Selulosa Mikrofibril dari Batang Pisang Sebagai Bahan Baku Film Plastik
Nama : Eka Pretty Febriyani
NIM : G44090015
Disetujui oleh
Betty Marita Soebrata, SSi, MSi Pembimbing I
Dr Sri Mulijani, MS Pembimbing II
Diketahui oleh
Prof Dr Dra Purwantiningsih Sugita, MS Ketua Departemen
ii
PRAKATA
Puji dan syukur penulis ucapkan kepada Tuhan Yang Maha Esa atas berkat-Nya sehingga penulis dapat melaksanakan Penelitian yang dilakukan sejak bulan Desember 2014, serta dapat menyelesaikan karya ilmiah hasil penelitian tersebut dengan judul Selulosa Mikrofibril dari Batang Pisang Sebagai Bahan Baku Film Plastik.
Terima kasih penulis ucapkan kepada Ibu Betty Marita Soebrata, S.Si, M.Si selaku pembimbing pertama dan Ibu Dr. Sri Mulijani, MS selaku pembimbing kedua. Ucapan terima kasih juga penulis sampaikan staf Laboratorium Kimia Fisik, staf Laboratorium Kimia Anorganik, staf Laboratorium Terpadu, serta staf Komisi Pendidikan Departemen Kimia, yang telah membantu selama penelitian berlangsung hingga ditulisnya karya ilmiah ini. Ungkapan terimakasih juga ditujukan kepada ayah Subowo Husen dan ibu Aplonia Elteningsih, Alvian Ariwibowo, keluarga besar, Saima, Sefri, Noni, serta teman-teman seperjuangan Kimia 46 atas segala doa dan dukungannya.
Semoga karya ilmiah ini bermanfaat.
Bogor, Agustus 2014
iv
DAFTAR ISI
DAFTAR TABEL v
DAFTAR GAMBAR v
DAFTAR LAMPIRAN v
PENDAHULUAN 1
Latar Belakang 1
Waktu dan Tempat 2
BAHAN DAN METODE 2
Alat dan Bahan 2
Metode 2
HASIL DAN PEMBAHASAN 5
Kadar air dan Kadar Abu 5
Selulosa Hasil Isolasi 6
Pembuatan Film dan Ketebalan 9
Sifat Mekanik 10
Sifat permeabilitas 11
Elektron pemayan (Scanning Electron Microscope/SEM) 12
SIMPULAN DAN SARAN 13
DAFTAR PUSTAKA 14
DAFTAR TABEL
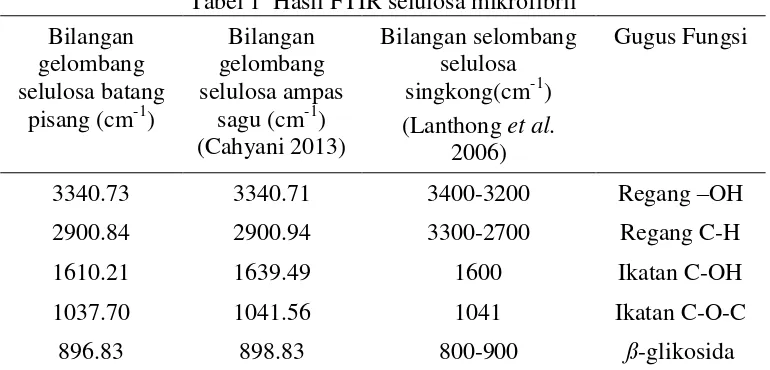
1 Hasil FTIR selulosa mikrofibril 8
2 Pengukuran ketebalan film 9
DAFTAR GAMBAR
1 Grafik hubungan antara ukuran pertikel dengan distribusi number sampel 6
2 Susunan selulosa di dalam sel tanaman 7
3 Spektrum FTIR selulosa mikro fibril hasil isolasi dari pelepah batang pisang 8 4 Hasil FTIR pelepah batang pisang penelitian Elanthikkal (2010) 9
5 Hasil pengukuran kuat tarik film 10
6 Hasil pengukuran % elongasi film 11
7 Permeabilitas uap air film 12
8 Mikrograf elektron pemayaran film plastik perbesaran 7500. (a) pati 1.5 g,
(b) pati 1.75 g, (c) pati 2.0 g, (d) pati 3.0 g. 13
9 Mikrograf elektron pemayaran dari permukaan komposit pada penelitian
Chang et al. (2010) 13
DAFTAR LAMPIRAN
1 Bagan alir penelitian 16
2 Pengukuran kadar air tepung batang pisang 17
3 Pengukuran kadar tepung batang pisang 17
4 Hasil pengukuran ketebalan plastik biodegradasi 18
5 Hasil pengukuran kuat tarik dan elongasi komposit 18
6 Perubahan bobot cawan petri 19
7 Data WVTR (g/menit cm2) 19
8 Permeabilitas uap air (g mm cm-2 menit-1 Pa-1) 20
Latar Belakang
Pisang (Musa spp.) adalah salah satu komoditas buah asli Indonesia. Tanaman tropis dan subtropis ini termasuk famili Musaceae. Tahun 2012 produksi pisang mencapai 6.071.043 ton. Produksi tersebut sebagian besar dipanen dari kebun rakyat seluas 269.000 ha (BPS 2013). Di samping memiliki nilai gizi yang tinggi untuk dikonsumsi secara langsung, pisang juga dikenal luas dalam dunia industri makanan. Bagian batang, daun, kulit buah dan akar merupakan limbah lignoselulosa yang dihasilkan oleh tanaman ini. Limbah lignoselulosa adalah limbah hasil pertanian yang mengandung serat selulosa, hemiselulosa dan lignin (Richana dan Suarni 2004). Secara tradisional limbah tanaman pisang sudah banyak dimanfaatkan. Daun pisang biasa dimanfaatkan sebagai media pembungkus makanan matang, sedangkan bagian akar, batang dan kulit pada umumnya dijadikan makanan untuk ternak. Dalam industri batang pisang telah dimanfaatkan untuk dijadikan bioetanol, papan serat, kertas, pupuk, dan media peredam suara (Zulferiyenni et al. 2009).
Kandungan selulosa pada batang pisang mencapai 40-65% (Zulferiyenni et al. 2009). Selulosa merupakan polisakarida penyusun serat pada dinding sel tanaman dengan struktur kimia berupa rantai yang tidak bercabang dan tersusun atas satuan β-D-gluko-piranosa melalui ikatan glikosida (ß-1,4). Sifat alami selulosa murni adalah kristalin, kaku dan tidak larut air. Isolasi selulosa dari berbagai sumber nabati telah dikembangkan oleh para peneliti, diantaranya isolasi selulosa dari ampas sagu (Nurpagi 2013, Cahyani 2013), limbah mahkota nanas (Susana 2011) dan isolasi selulosa dari tongkol jagung (Evandani 2012).Selulosa hasil isolasi memiliki ikatan yang lebih kuat dibandingkan selulosa alami yang ada pada tanaman. Selulosa hasil isolasi yang dicampurkan dengan pati dan pemlastis dapat menghasilkanfilm plastik.
2
Sifat unggul dari film plastik yang dihasilkan dari campuran pati dan selulosa adalah cepat terurai sehingga aman bagi lingkungan, tetapi karena berasal dari polimer alam maka secara fisik bersifat rapuh. Untuk itu perlu ditambahkan pemlastis. Pemlastis adalah bahan organik dengan bobot molekul rendah yang dapat meningkatkan fleksibiltas dan ekstensibilitas polimer (Julianti 2006). Menurut Winarno (1992) gliserol (C3H8O3) adalah senyawa alkohol polihidrat dengan 3 buah gugus hidroksil dalam satu molekul atau disebut alkohol trivalen. Gliserol mempunyai sifat mudah larutair atau hidrofilik dan mampu meningkatkan viskositas larutan(Krisna 2011). Gliserol merupakan salah satu pemlastisyang banyak digunakan karena cukup efektif mengurangi ikatan hidrogen internal sehingga akan meningkatkan jarak intermolekuler dan tidak mudah menguap saat proses pemanasan karena titik didih gliserol mencapai 204 °C.
Tujuan dari penelitian ini adalah mengisolasi selulosa dari batang pisang dengan menggunakan metode kimia mekanik, selanjutnya selulosa dicampurkan dengan pati jagung dan gliserol sebagai pemlastis untuk mendapatkan film plastik yang memiliki sifat mekanik dan permeabilitas uap air yang baik. Berbeda dari penelitian Chang et al. (2010) yang menggunakan selulosa sebagai variabel bergeraknya, pada penelitian ini variabel bergeraknya adalah pati pada pembuatan film.
Waktu dan Tempat
Penelitian ini dilaksanakan pada bulan Desember 2013-Mei 2014 di Laboratorium Kimia Fisik dan Lingkungan Departemen Kimia dan Laboratorium Terpadu Institut Pertanian Bogor.
BAHAN DAN METODE
Alat dan Bahan
Alat-alat yang digunakan pada penelitian ini, yaitu oven, alat-alat gelas, timbangan analitik, pH Universal, elektron pemayaran (Scanning electron microscope/SEM) tipe JSM-5000-JEOL JSM 5310 LV, spektroskopi inframerah (Fourier transform Infrared Spectroscopy/FTIR) tipe IR-Prestige 21, Particle Size Analyzer (PSA), cawan petri, blender, sonikasi, sentrifiusa.
Bahan–bahan yang digunakan pada penelitian ini, yaitu pelepah batang pisang batu (Musa brachycarpa), NaOH, HCl, NaOCl, pati jagung, dan gliserol.
Metode
Preparasi Batang Pisang (Susana 2011)
Kadar air (AOAC 2007)
Cawan porselin dikeringkan terlebih dahulu di dalam oven selama 30 menit pada suhu 100-105 ˚C, kemudian didinginkan di dalam desikator selama 30 menit dan ditimbang hingga diperoleh bobot konstan (A). Sebanyak 2 gram sampel tepung batang pisang ditimbang dan diletakkan dalam cawan yang telah dikeringkan (B). Cawan yang berisi sampel dipanaskan di dalam oven pada suhu 105-110 ˚C selama 3-4 jam. Setelah selesai, cawan tersebut didinginkan di dalam desikator selama 30 menit kemudian ditimbang lagi (C). Tahap ini diulangi hingga diperoleh bobot konstan. Kadar air dapat dihitung menggunakan rumus sebagai berikut:
Kadar air (%) =B-C
B-A×100% Keterangan:
A = Bobot cawan kosong (gram)
B = Bobot cawan + sampel sebelum dikeringkan (gram) C = Bobot cawan + sampel setelah dikeringkan (gram)
Kadar abu (AOAC 2007)
Cawan porselin dikeringkan terlebih dahulu di dalam oven selama 30 menit pada suhu 100-105 ˚C, kemudian didinginkan di dalam desikator selama 30 menit dan ditimbang hingga diperoleh bobot konstan. Sampel tepung batang pisang sebanyak 2 gram ditimbang dan diletakkan di dalam cawan yang sudah dikeringkan. Cawan beserta sampel dibakar menggunakan bunsen hingga tidak berasap selama ± 20 menit dan dilanjutkan dengan pengabuan di dalam tanur pada suhu 600 ˚C sampai pengabuan sempurna. Sampel yang telah diabukan didinginkan di dalam desikator dan ditimbang. Kadar abu dihitung menggunakan rumus sebagai berikut:
Kadar abu (%) =C-A
B-A×100% Keterangan:
A = Bobot cawan kosong (gram) B = Bobot cawan + sampel (gram) C = Bobot cawan + abu (gram)
Isolasi Selulosa Mikrofibril
Isolasi selulosa dilakukan melalui empat tahap perlakuan. Tahap pertama adalah perlakuan basa dengan menggunakan NaOH disertai pemanasan. Tahap ini bertujuan untuk menghidrolisis hemiselulosa dan depolimerisasi lignin pada tepung batang pisang menjadi komponen gula dan fenolik yang larut air (Cherian
4
Tahap ketiga adalah perlakuan dengan asam menggunakan HCl 3% disertai pemanasan pada suhu 60 °C selama 1 jam. Perlakuan dengan HCl ini bertujuan untuk menguraikan fibril-fibril selulosa yang masih saling berikatan dalam bentuk mikrofibril selulosa. Tahap keempat adalah sonikasi dengan menggunakan ultrasonik selama 1 jam. Tahap ini bertujuan untuk mengurai fibril-fibril selulosa menjadi berukuran nano. Sampel yang masih dalam bentuk suspensi di sentrifugasi pada 5000 rpm selama 45 menit dengan tujuan mengambil filtrat (selulosa miktofibril). Selulosa hasil isolasi dikeringkan dalam oven bersuhu 30-40 °C sampai kering dan siap digunakan untuk bahan baku pembuatan film plastik.
Spektroskopi inframerah (Fourier Transform Infrared Spectroscopy/FTIR)
Film ditempatkan di dalam sel holder kemudian dilakukan analisis pada bilangan gelombang 4000-500 cm-1. Hasil analisis gugus fungsi dengan FTIR berupa spektrogram hubungan antara bilangan gelombang dan persentase transmisi puncak yang mendeskripsikan gugus fungsi.
Particle Size Analyzer (PSA)
Sampel dalam bentuk suspensidiletakkan di atas permukaan wadah dengan pipet sebanyak 1 tetes. Sampel diukur menggunakan Zeta Sizer Nano Particle Analyzer.
Pembuatan film plastik (Chang et al. 2010)
Selulosa (2.50 g) dan gliserol (1.00 g) didispersikan ke dalam akuades (50 mL), kemudian disonikasi selama 45 menit. Penambahan pati jagung disertai pemanasan padasuhu 90 °C dan pengadukan dengan pengaduk magnet selama 50 menit. Pati jagung sebagai pengisi ditambahkan dengan variasi bobot (1.50, 1.75, 2.00, 3.00 g). Campuran dicetak di atas kaca dan dikeringkan di dalam oven pada suhu 40 °C.
Ketebalan film (Bae et al. 2007)
Ketebalan film diukur menggunakan mikrometer mekanik di 10 posisi acak pada masing-masing spesimen film dengan akurasi ±1 μm.
Kuat tarik dan elongasi (ASTM D 882 – 02)
Kuat tarik dan elongasi diukur menggunakan alat uji tarik berdasarkan ASTM D 882-02. Film yang telah dikeringkan dipotong dengan ukuran panjang 7 cm dan lebar 2 cm. Kemudian, film dijepitkan pada alat uji tarik dengan kecepatan konstan. Data yang dihasilkan dicetak di atas kertas. Perhitungan besarnya kuat tarik dan persentase elongasi menggunakan persamaan di bawah ini.
Kuat tarik (MPa)=Gaya tarik saat putus (N) Luas area (mm2)
Laju transmisi uap air diukur dengan menggunakan metode cawan berdasarkan ASTM E 96-95. Sebanyak 30 mL akuades dimasukkan ke dalam cawan petri. Kemudian cawan petri ditutup dengan alumunium foil yang telah dilubangi. Luas lubang pada alumunium sebesar 10% dari luas cawan. Film dilekatkan di atas lubang menggunakan epoxy. Batas ketinggian permukaan air dalam cawan dan film sebesar 6 mm. Cawan dipanaskan di dalam oven pada suhu 37±0.5˚C dan RH 81% selama 5–6 jam dan diukur hilangnya massa air setiap jamnya. Laju transmisi uap air dihitung menggunakan persamaan di bawah ini.
Laju transmisi uap air (WVTR)=masa air yang hilang waktu×luas
Permeabilitas uap air (WVP)= WVTR x l S x (R1-R2)
Keterangan:
S = Tekanan udara jenuh pada suhu 37 ˚C (63.63199 Pa) R1 = Kelembaban udara di dalam cawan petri (100%) R2 = Kelembaban udara pada suhu 37 ˚C (81%) l = ketebalan film (mm)
Elektron parayan (Scanning Electron Microscope/SEM)
Film plastik yang dihasilkan diamati dengan elektron parayan untuk dianalisis karakteristik mikrostrukturalnya.
HASIL DAN PEMBAHASAN
Kadar air dan Kadar Abu
6
Selulosa Hasil Isolasi
Ukuran partikel selulosa yang berhasil diisolasi pada penelitian ini ditentukan menggunakan instrumen PSA. Mode analisis yang digunakan adalah
commulant. Mode ini menghasilkan sebaran ukuran berdasarkan jumlah (size dispersion by number). Ukuran partikel selulosa hasil isolasi berada di rentang 269.22 sampai 9778.96 nm dengan rerata sebesar 920.96 nm. Sampel selulosa yang berada dalam akuades dipengaruhi oleh gaya gravitasi, sehingga mudah mengendap. Proses pengendapan ini sangat menyulitkan pengukuran karena partikel yang seharusnya melakukan gerakan Brown akanmengendap di dasar wadah ukur. Grafik hubungan antara ukuran partikel dengan sebaran jumlah disajikan pada Gambar 1.
Gambar 1Grafik hubungan antara ukuran partikel dengan sebaran jumlah sampel
Metode yang digunakan pada penelitian ini adalah kimia mekanik. Perlakuan kimia yang dikenakan pada tepung batang pisang adalah perlakuan basa, pemucatan, dan hidrolisis asam, sedangkan perlakuan mekaniknya dengan menggunakan instrumen ultrasonik. Sampel yang berbentuk tepung ketika diberi perlakuan basa akan menghasilkan suatu pulp berwarna coklat kehitaman. warna ini akan memudar dengan proses pencucian yang intensif. Warna coklat kehitaman pada pulp disebabkan oleh terbentuknya komponen gula dan zat fenolik akibat terlarutnya lignin dan hemiselulosa yang membungkus struktur selulosa. Gambar 2 mengilustrasikan letak selulosa di dalam susunan komponen dinding sel tanaman.
tidak dapat kembali. Hal inilah yang mengakibatkan terbentuknya struktur selulosa II yang memiliki ikatan hidrogen lebih kuat (Achmadi 1990).
Gambar 2 Susunan selulosa di dalam sel tanaman
Tahapan pemucatan menggunakan larutan NaOCl 5% menghasilkan perubahan warna pada sampel menjadi putih kekuningan. Warna kekuningan yang dibawa oleh sampel disebabkan ion Cl- yang berlebih dan ion ini bisa dihilangkan dengan proses pencucian. Sampel dicuci bersih sampai warnanya berubah menjadi putih bersih. Hidrolisis asam menggunakan HCl 3% dan pemanasan pada suhu 60 °C. Pada tahap ini fibril-fibril selulosa diuraikan menjadi ukuran yang lebih kecil. Proses penguraian ini terlihat dari bentuk sampel yang semula menggumpal menjadi butiran-butiran di dalam akuades. Dalam larutan, HCl dapat mengion menjadi H+ dan Clˉ. Ion H+ dapat memecah glikosida pada selulosa dan hemiselulosa sehingga akan membentuk monomer gula sederhana. Monomer gula yang dihasilkan masih dalam bentuk radikal bebas, namun dengan adanya gugus -OH dari air akan menstabilkan radikal bebas dan membentuk gugus glukosa. Hidrolisis dengan HCl menghasilkan rendemen yang lebih tinggi dibandingkan dengan H2SO4. Hal ini disebabkan karena larutan H2SO4 dapat menyebabkan terjadinya reaksi esterifikasi selulosa (Adel et al. 2011). Proses sonikasi menyebabkan ukuran fibril-fibril partikel selulosa yang telah dikenakan perlakuan kimia semakin kecil.
8
Tabel 1 Hasil FTIR selulosa mikrofibril Bilangan
2900.84 2900.94 3300-2700 Regang C-H
1610.21 1639.49 1600 Ikatan C-OH
1037.70 1041.56 1041 Ikatan C-O-C
896.83 898.83 800-900 ß-glikosida
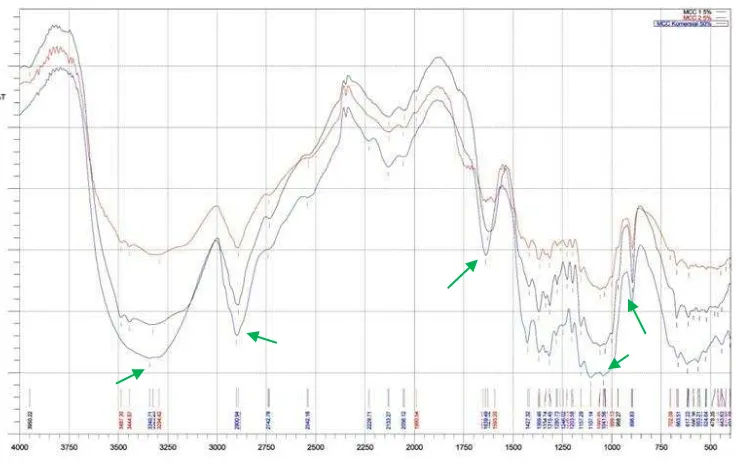
Sebagai pembanding,Gambar 4 menunjukan spektrum FTIR selulosa dari ampas sagu (Cahyani 2013) yang juga menunjukan puncak pada panjang gelombang yang hampir sama. Berdasarkan analisis bilangan gelombang yang dihasilkan oleh sampel pelepah batang pisang membuktikan bahwa isolat yang didapatkan adalah selulosa. Hanya saja ukuran partikel dari selulosa belum semuanya berukuran nano.
Gambar 3Spektrum FTIR selulosa mikrofibril hasil isolasi dari pelepah batang pisang
Gambar 4Hasil FTIR ampas sagu (Cahyani 2013)
Film Plastik dan Ketebalan
Campuran larutan (selulosa, pati, gliserol dan akuades) yang telah dibuat, dicetak di atas plat kaca yang diberi pembatas berupa pita perekat sebanyak 5 lapisan. Ketebalan film sangat mempengaruhi sifat mekanik film dan menunjukkan kehomogenan komponen penyusun film. Film yang homogen akan memiliki ketebalan yang seragam pada sepuluh titik pengukuran. Tabel 2 menunjukan hasil rata-rata dari pengukuran ketebalan film dan Lampiran 4 menyajikan data ketebalan dari 10 titik pengukuran. Film D dengan penambahan 3.00 gram pati memiliki ketebalan paling tinggi, yaitu 0.123 mm sedangkan film B dengan penambahan pati 1.75 gram memiliki ketebalan paling tipis yaitu 0.088 mm. Ketebalan film yang dihasilkan meningkat bersamaan dengan jumlah pati yang ditambahkan pada campuran. Sampel B dengan jumlah pati yang lebih banyak dari sampel A memiliki ketebalan film yang lebih rendah disebabkan proses pembentukan gelatinisasi yang tidak sempurna karena suhu pemanasan yang tidak stabil.
10
(Corradini et al.2007). Pada saat proses termoplastisasi, air akan masuk ke dalam pati jagung dan bahan pemlastis akan membentuk ikatan hidrogen dengan pati sehingga terjadi reaksi antara gugus hidroksil dengan molekul pati yang akan membuat pati menjadi lebih plastis dan tebal (Kalambur et al. 2006). Secara fisik lembaran film D memiliki permukaan yang paling halus dan lentur.
Sifat Mekanik
Sifat mekanik film meliputi kekuatan tarik dan persentase perpanjangan tarik (elongasi). Menurut Stevans (2007) kuat tarik merupakan ukuran besarnya beban atau gaya yang dapat ditahan sebelum suatu sampel rusak atau putus, sedangkan elongasi adalah perubahan panjang sampel yang diakibatkan gaya yang diberikan. Perbedaan mendasar pada selulosa mikrofiber dan campuran pati-gliserol adalah sifat selulosa yang kristalin, sedangkan campuran pati-pati-gliserol bersifat amorf. Hal inilah yang menyebabkan kelemahan proses pencampuran selulosa dengan campuran pati-gliserol dan mempengaruhi kekuatan mekanik film yang dihasilkan. Gambar 5 menyajikan hasil uji kuat tarik sampel.
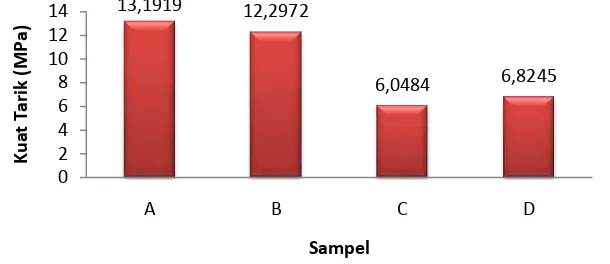
Gambar 5Hasil pengukuran kuat tarik film
Sampel A yang memiliki komposisi pati 1.50 gram menghasilkan kuat tarik paling tinggi. Semakin besar komposisi pati kuat tarik yang dihasilkansemakin kecil. Hal ini berkaitan dengan molekul-molekul campuran pati-gliserol yang masuk ke antara struktur rantai selulosa yang teratur sehingga terjadi interaksi tarik menarik antar molekul yang cukup besar dan menghasilkan molekul yang amorf serta menyebabkan susunan molekul selulosa menjadi terganggu dan tidak teratur (Permatasari 2010). Semakin besar interaksi yang terjadi maka susunan molekul selulosa pun akan semakin tidak teratur. Hal ini yang menyebabkan kuat tarik sampel menjadi semakin kecil dengan penambahan pati. Sampel C dengan penambahan pati 2.00 gram memiliki nilai kuat tarik yang lebih rendah dibandingkan dengan sampel D dengan penambahan pati 3.00 gram. Hal ini bisa disebabkan karena faktor penyimpanan yang kurang baik, sehingga film plastik yang bersifat higroskopisakan menyerap uap air dari udara dan menurunkan kekuatan tariknya.
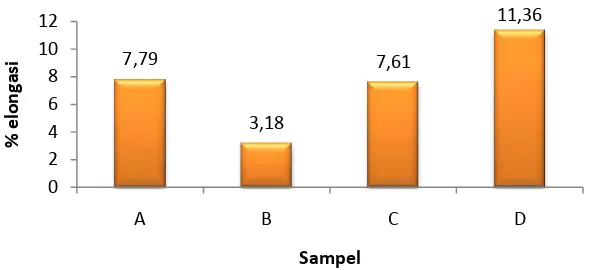
Perpanjangan putus (elongasi) menentukan sifat elastis film. Berdasarkan Gambar 6 persen elongasi sampel A sampai D berturut-turut adalah 7.79, 3.18, 7.61, dan 11.36%. Besar kecilnya nilai elongasi berkaitan dengan jumlah pati dan
dapat membentuk gel dan gliserol sebagai pemlastis maka semakin banyak komposisi kedua bahan ini akan menghasilkan film dengan elastisitas tinggi. Pada penelitian ini, jumlah gliserol yang ditambahkan pada tiap komposisi sampel sama sehingga gliserol tidak dapat digunakan sebagai parameter pembanding.
Gambar 6Hasil pengukuran % elongasi film
Sampel B memiliki nilai elongasi terkecil (3.18%) sedangkan sampel D memiliki nilai elongasi tertinggi (11.36%). Nilai elongasi sampel D sesuai teori yang menyatakan bahwa banyaknya pati yang ditambahkan akan meningkatkan elastisitas (Purba 2013), sedangkan sampel B yang seharusnya lebih tinggi nilai elongasinya dibandingkan dengan sampel A (7.79%),menunjukan kondisi sebaliknya. Hal ini bisa disebabkan pati yang ditambahkan belum semuanya mengalami glatinisasi (proses pembentukan gel) akibat dari suhu pemanasan yang tidak stabil sehingga elastisitas yang dihasilkan oleh film menjadi berkurang. Hasil pengukuran kuat tarik dan elongasi disajikan secara lengkap pada Lampiran 5.
Sifat permeabilitas uap air
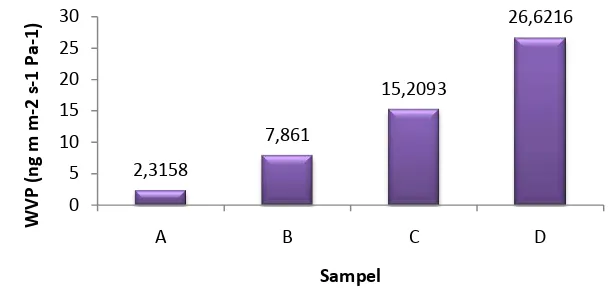
Sifat permeabilitas uap air (Water Vapor Permeability/WVP) film plastik sangat penting untuk diketahui terutama untuk film yang diaplikasikan sebagai bahan pengemas makanan. Film plastik yang baik digunakan sebagai bahan pengemas adalah film yang memiliki permeabilitas uap air yang rendah, karena pergerakan uap air antar lapisan film yang rendah akan menurunkan pergerakan uap air antara lingkungan dengan produk, sehingga kemungkinan produk untuk rusak akibat kelebihan kandungan airnya makin kecil. Hasil penelitian menunjukkan bahwa film plastik yang memiliki nilai permeabilitas uap air yang paling rendah adalah film dengan komposisi pati sebanyak 1.50 g (sampel A), yaitu 2.3158 ng m m-2 s-1 Pa-1.
Gambar 7menunjukan kenaikan nilai permeabilitas uap air seiring dengan kenaikan jumlah pati yang ditambahkan di dalam campuran sampel. Hal ini berkaitan dengan struktur pati yang bercabang dan strukturselulosa yang teratur. Martins et al. (2012) menyatakan bahwa semakin banyak komponen teratur dalam penyusun film, maka nilai permeabilitasnya juga semakin rendah. Sehingga
12
semakin banyak pati di dalam campuran, maka uap air yang lewat pun akan semakin mudah.
Gambar 7Permeabilitas uap air film
Hal ini dibuktikan dengan sampel D yang memiliki nilai permeabilitas sekitar 26.6216 ng m m-2 s-1 Pa-1, sehingga film plastik yang kandungan selulosanya tinggi lebih sulit untuk dilalui air, karena uap air cenderung untuk tertahan pada permukaan film. Nilai permeabilitas tersebut dipengaruhi oleh suhu, kelembaban udara (RH), ketebalan film, dan jumlah pemlastis yang digunakan. Hasil pengukuran permeabilitas uap air disajikan pada Lampiran 9.
Elektron Parayan (Scanning Electron Microscope/SEM)
Gambar 8 Mikrograf elektron pemayaran film plastik perbesaran 7500. (a) pati 1.5 g, (b) pati 1.75 g, (c) pati 2.0 g, (d) pati 3.0 g.
Gambar 9 Mikrograf elektron pemayaran dari permukaan komposit pada penelitian Chang et al. (2010)
SIMPULAN
Selulosa mikrofibril berhasil diisolasi dari pelepah batang pisang melalui metode kimia mekanik dengan ukuran partikel selulosa yang didapatkan ± 920.96 nm. Film plastik dengan variasi penambahan pati 1.5 g menghasilkan nilai kuat tarik dan permeabilitas paling baik yaitu 13.1919 Mpa dan 2.3158 ng m m-2s-1Pa-1. Nilai elongasi paling tinggi ditunjukkan oleh film plastik dengan penambahan pati 3.0 g,yaitu 11.36%. Mikrograf SEM menunjukan distribusi campuran selulosa dan pati-gliserol yang homogen.
SARAN
Perlu dilakukan analisis penentuan kadar selulosa, hemiselulosa, dan lignin dari sampel pelepah batang pisang yang digunakan. Optimisasi proses gelatinisasi yang terjadi pada pati-gliserol juga perlu dilakukan agar proses distribusi struktur selulosa semakin baik dan film yang dihasilkan memiliki sifat mekanik yang lebih
14
baik, serta perlu dilakukan analisis dengan menggunakan istrumen XRD untuk mengetahui tipe selulosa (fibril atau kristalin) yang didapatkan.
DAFTAR PUSTAKA
Achmadi SS. 1990. Kimia Kayu. Bogor(ID): IPB Press.
Adel AM, Abd El-Wahab ZH, Ibrahim A A, Al-Shemy, MT. 2011.Characterization of microcrystalline mellulose prepared from lignocellulosic materials. Part II: physicochemical properties. Carbohydrate Polymers 83:676-687.
Bae Ho J, Cha Dong S, Whiteside William S, Park Hyun J. 2007. Film and pharmaceutical hard capsule formation properties of mungbean, waterchestnut, and sweet potao starches. Food Chem 106:96–105.
Cahyani N. 2013. Sifat fisikokimia, termal, dan spektroskopi mikrokristalin selulosa serabut ampas sagu [skripsi]. Bogor (ID): Institut Pertanian Bogor. Chang PR, Jian R, Zheng P, Yu J, Ma X. 2013. Preparation and properties of glycerol plasticized-starch (GPS)/cellulose nanoparticle (CN) composites.
Journal of Carbohydrate Polymers. 79(2010): 301-305. doi:10.1016/j.carbpol.2009.08.007.
Cherian BM, Pothan LA, Chung TN, Mennig G, Kottaisamy M, Thomas S. 2008. A novel method for synthesis of cellulose nanofibril whiskers from banana fibers and characterization. Food Chem 56: 5617-5627. doi: 10.1021/jf8003674. Epub 2008 Jun 21
Corradini E, A.J.F Carvalho, A.A.D Curvelo, L.H.C Mattoso. 2007. Preparation and Characterization of Thermoplastic Starch/Zein Blends. Mat Res 10(3):1-5.doi: 10.1590/S1516-14392007000300002.
Evandani N. 2012. Sintesis nanoselulosa dari tongkol jagung dengan perlakuan hidrolisis kimia dan homogenisasi [skripsi]. Bogor (ID): Institut Pertanian Bogor.
Hattaka A.2001. Degradation of Lignin. Journal Bioplymer 1: 129-145.
Kalambur S, Rizvi SSH. 2006. An Overview of Starch-Based Plastic Blends From Reactive Extrusion. J Plast Film Sheet 22:39-58.
Krisna D. 2011. Pengaruh regelatinasi dan modifikasi hidrotermal terhadap sifat fisik pada pembuatan edible film dari pati kacang merah (vigna angularis sp.) [tesis]. Semarang (ID): Universitas Diponegoro.
Lanthong P, Nuisin R, Kiatkamjornwong S. 2006. Graft copolymerization, characterization, and degradation of cassava starch-g-acrylamide/itaconic acid superabsorbents. Carbohydrate Polymers 66: 229-245.
Mali, S., M.V.E. Grossmann, M.A. Garcia, M.N. Martino dan N.E. Zaritzky. 2005. Mechanical and Thermal properties of yam starch films. J. Food Hydrocolloid. 19:157-164.
10.1016/j.foodhyd.2012.03.004
Nurpagi EM. 2013. Kemurnian selulosa serabut ampas sagu pada berbagai perlakuan isolasi [skripsi]. Bogor (ID): Institut Pertanian Bogor
.
Permatasari NA. 2010. Produksi plastik komposit dari campuran tapioka-onggok termoplastis dengan compatibilized polietilen [skripsi]. Bogor (ID): Institut Pertanian Bogor.
Purba S. 2013.Film edibel berbahan dasar karaginan dengan penambahan tepung porang (Amorphophallus Onchophyllus) dan selulosa[skripsi]. Bogor (ID): Institut Pertanian Bogor.
Richana N, Suarni. 2004. Teknologi Pengolahan Jagung. Balai Besar Pengembangan dan Penelitian Pascapanen Bogor.
Stevens MP. 2007.Kimia Polimer. IisSopyan, penerjemah. Jakarta (ID): PT Pradnya Paramita.Terjemahandari: Polymer Chemistry
Susana. 2011. Ekstraksi selulosa limbah mahkota nanas. Jurnal Vokasi. 7(1): 87-94.
Winarno FG. 1992. Kimia PangandanGizi. Jakarta: Gramedia.
16
LAMPIRAN
Lampiran 1Bagan alir penelitian
Penepungan sampel batang pisang
Isolasi Selulosa
Pembuatan Film Plastik Kadar air dan abu tepung batang pisang
PSA
FTIR
SEM Permeabilitas
uap air Kuat tarik
dan elongasi Ketebalan
Sampel
Kadar air % = Bobot cawan dan sampel-bobot kering oven
Bobot cawan dan sampel-bobot cawan kosongx 100 %
= 32.7631 gram-32.4890 gram
32.7631 gram-30.7561 gramx 100 % = 13.6%
Kerata kadar air % =13.6+13.5+13.2
3 =13.43 %
Lampiran 3Pengukuran kadar tepung batang pisang
Sampel Bobot cawan
Kadar abu % = Bobot kering tanur-bobot cawan kosong
Bobot cawan dan sampel-bobot cawan kosongx 100 %
=35.4806 gram-35.3667 gram
37.3711 gram-35.3667 gramx 100 % = 9.98 %
Rerata kadar abu % =5.68+5.68+5.37
18
Lampiran 4Hasil pengukuran ketebalan plastik biodegradasi
Ulangan A B C D
Rerata ketebalan komposit (mm)=ketebalan film plastik Banyaknya ulangan
=0.11 + 0.10 + 0.11 + 0.10 + 0.11 + 0.11 + 0.11 + 0.10 + 0.11 + 0.11 10
= 0.107 mm
Lampiran 5Hasil pengukuran kuat tarik dan elongasi komposit
Sampel
Kuat tarik (MPa)=Gaya tarik saat putus
Luas area =
28.4026 � 20 mm х 0.107 mm
Panjang awal film
=6.4555 mm
70 mm x 100% = 9.22%
Lampiran 6Perubahan bobot cawan petri Waktu
(menit)
A B C D
Bobot (g) Kehilangan
bobot (g) Bobot (g)
Kehilangan
bobot (g) Bobot (g)
Kehilangan
bobot (g) Bobot (g)
Kehilangan bobot (g)
0 73.8571 - 74.0600 - 72.9284 - 73.9094 -
60 73.7889 0.0682 73.8925 0.1675 72.7524 0.1760 73.3785 0.5309
120 73.7506 0.1065 73.6874 0.3726 72.3721 0.5563 72.9870 0.9224
180 73.7291 0.1280 73.4517 0.6083 72.0891 0.8393 72.4211 1.4883
240 73.6849 0.1722 73.3157 0.7443 71.9055 1.0229 72.1393 1.7701
300 73.6682 0.1889 73.2823 0.7777 71.8060 1.1224 72.0211 1.8883
Lampiran 7Data WVTR (g/menit cm2)
Waktu (menit) Film plastik (g/menit cm2)
A B C D
60 0.000284 0.000698 0.000734 0.00221
120 0.000221 0.000776 0.00116 0.00192
180 0.000178 0.000845 0.00116 0.00207
240 0.000179 0.000775 0.00106 0.00184
20
Contoh perhitungan:
WVTR (g /menit cm2)= berat air yang hilang waktu x luas film edibel
Penulis dilahirkan di Sumba Timur pada tanggal 05 Februari 1991 dari ayah Subowo Husen dan ibu Aplonia Elteningsih Marumata. Penulis merupakan putri pertama dari tiga bersaudara. Tahun 2009 penulis lulus dari SMA Negeri 1 Waingapu dan pada tahun yang sama lulus seleksi masuk departemen Kimia IPB melalui jalur Undangan Seleksi Masuk IPB (USMI).