Lampiran 1. Sampel Tablet A, Tablet G, dan Tablet I
Gambar 1. Tablet A
F
Lampiran 1. (Lanjutan)
Lampiran 2. Komposisi Tablet A, Tablet G, dan Tablet I Daftar Spesifikasi Sampel
1. Tablet A
Nama Sampel : ASMADEX®
Nomor Registrasi : DTL 9205002310 A1 Expire Date : Januari 2019
Komposisi : Theophylline ... 130 mg Ephedrine HCl ... 10 mg
2. Tablet G
Nama Sampel : GRAFASMA®
Nomor Registrasi : DTL 9231102410 A1 Expire Date : September 2017
Komposisi : Theophylline ... 130 mg Ephedrine HCl ... 10 mg
3. Tablet I
Nama Sampel : IFASMA®
Nomor Registrasi : DKL 7609203410 A1 Expire Date : September 2017
Lampiran 3. Gambar Alat-Alat Pengukuran Kadar Campuran Teofilin dan Efedrin HCl
Gambar 4. Spektrofotometer UV-Visible (Shimadzu UV 1800)
Lampiran 3. (Lanjutan)
Lampiran 4. Perhitungan Pembuatan HCl 0,1 N
HCl 37% (v/v) setara dengan HCl 12 N
V1 x N1 = V2 x N2
V1 x 12 N = 1000 ml x 0,1 N
V1 =
1000 ml
Lampiran 5. Bagan Alir Pembuatan Larutan Induk Baku dan Serapan Maksimum Teofilin
ditimbang sebanyak 50 mg
dimasukkan ke dalam labu tentukur 50 ml
dilarutkan dan dicukupkan dengan pelarut HCl 0,1 N sampai garis tanda
dipipet 2,5 ml
dimasukkan ke dalam labu tentukur 50 ml dicukupkan dengan pelarut HCl 0,1 N sampai garis tanda
dipipet 4,05 ml
dimasukkan ke dalam labu tentukur 25 ml dicukupkan dengan pelarut HCl 0,1 N sampai garis tanda
diukur serapan pada panjang gelombang 200-400 nm
Baku Teofilin
LIB II Teofilin (50 μg/ml)
Teofilin (8,1 μg/ml)
Panjang Gelombang Teofilin = 270,40 nm
Lampiran 6. Bagan Alir Pembuatan Larutan Induk Baku dan Serapan Maksimum Efedrin HCl
ditimbang sebanyak 53 mg
dimasukkan ke dalam labu tentukur 50 ml dilarutkan dan dicukupkan dengan pelarut HCl 0,1 N sampai garis tanda
dipipet 8,5 ml
dimasukkan kedalam labu tentukur 25 ml dicukupkan dengan pelarut HCl 0,1 N sampai garis tanda
diukur serapan pada panjang gelombang 200-400 nm
Baku Efedrin HCl
LIB I Efedrin HCl (1060 μg/ml)
Efedrin HCl (360,4 μg/ml)
Lampiran 7. Bagan Alir Penentuan Panjang Gelombang Analisis Teofilin dan Efedrin HCl
Efedrin HCl (360,4 μg/ml) Teofilin (8,1 μg/ml)
diukur serapan dari masing-masing teofilin dan efedrin HCl pada panjang gelombang 200 - 400 nm
ditumpang-tindihkan spektrum serapan dari masing-masing komponen
ditentukan panjang gelombang analisis dalam rentang 215-300 nm
dipilih panjang gelombang berdasarkan panjang gelombang maksimum teofilin dan efedrin HCl
Lampiran 8. Bagan Alir Pembuatan dan Pengukuran Larutan Standar Teofilin
dipipet masing-masing sebanyak 2 ml, 3 ml, 4 ml, 5 ml, dan 6 ml
dimasukkan masing-masing ke dalam labu tentukur 25 ml
dicukupkan dengan pelarut HCl 0,1 N Larutan Standar Teofilin
(4 µg/ml, 6 µg/ml, 8 µg/ml, 10 µg/ml, dan 12 µg/ml)
Data Kalibrasi Teofilin LIB II Teofilin (50 μg/ml)
Lampiran 9. Bagan Alir Pembuatan dan Pengukuran Larutan Standar Efedrin HCl
dipipet masing-masing sebanyak 4 ml, 6 ml, 8,5 ml, 10 ml, dan 12 ml
dimasukkan masing-masing ke dalam labu tentukur 25ml
dicukupkan dengan pelarut HCl 0,1 N Larutan Standar Efedrin HCl
(169,6 µg/ml; 254,4 µg/ml; 360,4 µg/ml; 424 µg/ml; dan 508,8 µg/ml)
Data Kalibrasi Efedrin HCl LIB I Efedrin HCl (1060 μg/ml)
Lampiran 10. Bagan Alir Pembuatan Larutan Baku Campuran Teofilin dan Efedrin HCl
Kedua larutan dicampurkan ke dalam labu tentukur 25 ml dan dicukupkan dengan pelarut HCl 0,1 N
Larutan diukur pada panjang gelombang 200-400 nm
Lakukan pengulangan sebanyak 6 kali
Efedrin HCl = 12 mg Teofilin = 10 mg
Dimasukkan ke dalam labu tentukur 25 ml Dilarutkan dan dicukupkan dengan pelarut HCl 0,1 N Larutan Teofilin
(400 µg/ml)
Dimasukkan ke dalam labu tentukur 25 ml Dilarutkan dan dicukupkan dengan pelarut HCl 0,1 N Larutan Efedrin HCl
(480 µg/ml)
Diambil 0,5 ml Diambil 18,85 ml
Lampiran 11. Bagan Alir Penentuan Kadar Teofilin dan Efedrin HCl dalam Tablet A
ditimbang (berat 20 tablet = 7516 mg)
digerus dalam lumpang sampai halus dan homogen
ditimbang setara 10 mg teofilin (penimbangan dilakukan sebanyak 6 kali pengulangan)
dihitung kesetaraan efedrin HCl yang terkandung di dalamnya
dimasukkan ke dalam labu tentukur 100 ml dilarutkan dengan pelarut HCl 0,1 N
dihomogenkan dengan sonikator selama 15 menit dicukupkan dengan pelarut HCl 0,1 N sampai garis tanda
dikocok sampai homogen disaring larutan
dibuang ± 10 ml filtrat pertama ditampung filtrat selanjutnya dipipet sebanyak 1,7 ml
dimasukkan ke dalam labu tentukur 25 ml
dipipet 5 ml (metode adisi standar)
dimasukkan ke dalam labu tentukur 25 ml dicukupkan campuran dengan pelarut HCl 0,1 N diukur pada empat panjang gelombang yang telah ditentukan (270,4 nm; 262,8 nm; 256,8 nm; dan 251,2 nm)
dihitung Larutan Efedrin HCl
(1000 μg/ml)
Kadar 20 tablet
Serbuk
Lampiran 12. Bagan Alir Penentuan Kadar Teofilin dan Efedrin HCl dalam Tablet G
ditimbang (berat 20 tablet = 4244 mg)
digerus dalam lumpang sampai halus dan homogen
ditimbang setara 10 mg teofilin (penimbangan dilakukan sebanyak 6 kali pengulangan)
dihitung kesetaraan efedrin HCl yang terkandung didalamnya
dimasukkan ke dalam labu tentukur 100 ml dilarutkan dengan pelarut HCl 0,1 N
dihomogenkan dengan sonikator selama 15 menit dicukupkan dengan pelarut HCl 0,1 N sampai garis tanda
dikocok sampai homogen disaring larutan
dibuang ± 10 ml filtrat pertama ditampung filtrat selanjutnya dipipet sebanyak 1,5 ml
dimasukkan ke dalam labu tentukur 25 ml
dipipet 5 ml (metode adisi standar)
dimasukkan ke dalam labu tentukur 25 ml dicukupkan campuran dengan pelarut HCl 0,1 N diukur pada empat panjang gelombang yang telah ditentukan (270,4 nm; 262,8 nm; 256,8 nm; dan 251,2 nm)
dihitung Larutan Efedrin HCl
(1000 μg/ml)
Kadar 20 tablet
Serbuk
Lampiran 13. Bagan Alir Penentuan Kadar Teofilin dan Efedrin HCl dalam Tablet I
ditimbang (berat 20 tablet = 6626 mg)
digerus dalam lumpang sampai halus dan homogen
ditimbang setara 10 mg teofilin (penimbangan dilakukan sebanyak 6 kali pengulangan)
dihitung kesetaraan efedrin HCl yang terkandung didalamnya
dimasukkan ke dalam labu tentukur 100 ml dilarutkan dengan pelarut HCl 0,1 N
dihomogenkan dengan sonikator selama 15 menit dicukupkan dengan pelarut HCl 0,1 N sampai garis tanda
dikocok sampai homogen disaring larutan
dibuang ± 10 ml filtrat pertama ditampung filtrat selanjutnya dipipet sebanyak 1,7 ml
dimasukkan ke dalam labu tentukur 25 ml
dipipet 5 ml (metode adisi standar)
dimasukkan ke dalam labu tentukur 25 ml dicukupkan campuran dengan pelarut HCl 0,1 N diukur pada empat panjang gelombang yang telah ditentukan (270,4 nm; 262,8 nm; 256,8 nm; dan 251,2 nm)
dihitung Larutan Efedrin HCl
(1000 μg/ml)
Kadar 20 tablet
Serbuk
Lampiran 14. Perhitungan Kadar Teoritis dari Campuran Baku Teofilin dan Efedrin HCl
Pengulangan 1 Kadar Teofilin:
Teofilin = 10 mg
25 ml = 400 µg/ml
V1 x C1 = V2 x C2
V1 x 400 µg/ml = 25 ml x 8,01 µg/ml
V1 = 0,5 ml
Kadar Efedrin HCl:
Efedrin HCl =12 mg
25 ml = 480 µg/ml
V1 x C1 = V2 x C2
V1 x 480 µg/ml = 25 ml x 361,92 µg/ml
V1 = 18,85 ml
Pengulangan 2 Kadar Teofilin:
Teofilin = 11 mg
25 ml = 440 µg/ml
V1 x C1 = V2 x C2
V1 x 440 µg/ml = 25 ml x 8,01 µg/ml
V1 = 0,45 ml
Kadar Efedrin HCl:
Efedrin HCl =13 mg
25 ml = 520 µg/ml
V1 x C1 = V2 x C2
V1 x 520 µg/ml = 25 ml x 361,92 µg/ml
V1 = 17,4 ml
Pengulangan 3 Kadar Teofilin:
Teofilin = 13 mg
25 ml = 520 µg/ml
V1 x C1 = V2 x C2
V1 x 520 µg/ml = 25 ml x 8,01 µg/ml
Lampiran 14. (Lanjutan) Kadar Efedrin HCl:
Efedrin HCl =12 mg
25 ml = 480 µg/ml
V1 x C1 = V2 x C2
V1 x 480 µg/ml = 25 ml x 361,92 µg/ml
V1 = 18,85 ml
Pengulangan 4 Kadar Teofilin:
Teofilin = 13 mg
25 ml = 520 µg/ml
V1 x C1 = V2 x C2
V1 x 520 µg/ml = 25 ml x 8,01 µg/ml
V1 = 0,4 ml
Kadar Efedrin HCl:
Efedrin HCl =13 mg
25 ml = 520 µg/ml
V1 x C1 = V2 x C2
V1 x 520 µg/ml = 25 ml x 361,92 µg/ml
V1 = 17,4 ml
Pengulangan 5 Kadar Teofilin:
Teofilin = 13 mg
25 ml = 520 µg/ml
V1 x C1 = V2 x C2
V1 x 520 µg/ml = 25 ml x 8,01 µg/ml
V1 = 0,4 ml
Kadar Efedrin HCl:
Efedrin HCl =14 mg
25 ml = 560 µg/ml
V1 x C1 = V2 x C2
V1 x 560 µg/ml = 25 ml x 361,92 µg/ml
Lampiran 14. (Lanjutan) Pengulangan 6
Kadar Teofilin:
Teofilin =13 mg
25 ml = 520 µg/ml
V1 x C1 = V2 x C2
V1 x 520 µg/ml = 25 ml x 8,01 µg/ml
V1 = 0,4 ml
Kadar Efedrin HCl:
Efedrin HCl =14 mg
25 ml = 560 µg/ml
V1 x C1 = V2 x C2
V1 x 560 µg/ml = 25 ml x 361,92 µg/ml
Lampiran 15. Data Penimbangan dan Serapan dalam Tablet Tabel 15.1 Data Penimbangan dan Serapan dalam Tablet A
Pengulangan Penimbangan (gram)
Serapan pada Panjang Gelombang
270,40 nm 262,80 nm 256,80 nm 251,20 nm
1 0,0290 0,342 0,485 0,471 0,343
2 0,0290 0,342 0,485 0,471 0,343
3 0,0300 0,345 0,475 0,471 0,349
4 0,0300 0,347 0,480 0,470 0,352
5 0,0300 0,345 0,475 0,471 0,349
6 0,0300 0,345 0,475 0,471 0,349
Tabel 15.2 Data Penimbangan dan Serapan dalam Tablet G Pengulangan Penimbangan
(gram)
Serapan pada Panjang Gelombang
270,40 nm 262,80 nm 256,80 nm 251,20 nm
1 0,0180 0,350 0,544 0,536 0,381
2 0,0180 0,350 0,545 0,533 0,384
3 0,0180 0,350 0,545 0,533 0,384
4 0,0210 0,350 0,545 0,533 0,384
5 0,0210 0,350 0,545 0,533 0,384
6 0,0220 0,353 0,551 0,535 0,385
Tabel 15.3 Data Penimbangan dan Serapan dalam Tablet I Pengulangan Penimbangan
(gram)
Serapan pada Panjang Gelombang
270,40 nm 262,80 nm 256,80 nm 251,20 nm
1 0,0260 0,319 0,485 0,488 0,371
2 0,0260 0,318 0,477 0,488 0,371
3 0,0027 0,319 0,485 0,488 0,371
4 0,0027 0,320 0,493 0,488 0,371
5 0,0028 0,319 0,485 0,488 0,371
Lampiran 16. Contoh Perhitungan Kadar Teoritis dari Teofilin dan Efedrin HCl dalam Tablet A
Komposisi tablet A = Teofilin ... 130 mg Efedrin HCl ... 10 mg Berat 20 tablet A = 7516 mg
Berat setara teofilin adalah 10 mg (pemilihan 10 mg adalah agar tahap pengenceran tidak banyak sehingga dapat mengurangi kesalahan pengerjaan), jadi penimbangan berat serbuk tablet A yang mengandung kesetaraan 10 mg teofilin adalah:
Berat serbuk tablet A = berat setara teofilin x berat 20 tablet A kandungan teofilin dalam 20 tablet
= 10 mg x 7516 mg 130 mg x 20 tablet
= 28,91 mg
Dalam 28,91 mg serbuk tablet A mengandung kesetaraan teofilin sebesar 10 mg. Berat serbuk tablet A yang ditimbang adalah 29 mg, jadi berat setara teofilin yang seharusnya adalah:
Berat serbuk tablet A = berat setara teofilin x berat 20 tablet A kandungan teofilin dalam 20 tablet
29 mg = berat setara teofilin x 7516 mg 130 mg x 20 tablet
Berat setara teofilin = 10,0319 mg
Konsentrasi teofilin dan efedrin HCl dalam 29 mg serbuk tablet A yang dimasukkan ke labu tentukur 100 ml adalah:
Teofilin = 10,0319 mg x 1000 100 ml
= 100,319 µg/ml
Efedrin HCl: Kandungan teofilin dalam tablet A = Konsentrasi teofilin Kandungan efedrin HCl dalam tablet A Konsentrasi efedrin HCl
Lampiran 16. (Lanjutan)
Selanjutnya dilakukan pengenceran terhadap teofilin menjadi konsentrasi yang diinginkan (rentang konsentrasi teofilin = 4-12 µg/ml) dan konsentrasi yang saya pilih adalah 7 µg/ml.
V1 x C1 = V2 x C2
V1 x 100,319 µg/ml = 25 ml x 7 µg/ml
V1 = 1,74 ml ≈ 1,75 ml
Konsentrasi teofilin dan efedrin HCl dalam 1,75 ml adalah: Teofilin:
V1 x C1 = V2 x C2
1,75 ml x 100,319 µg/ml = 25 ml x C2
C2 = 7,0223 µg/ml
Efedrin HCl:
V1 x C1 = V2 x C2
1,75 ml x 7,7169 µg/ml = 25 ml x C2
C2 = 0,5402 µg/ml
Karena konsentrasi efedrin HCl tidak dalam rentang 169,6-508,8 µg/ml, jadi perlu dilakukan metode adisi standar terhadap efedrin HCl sebesar:
Efedrin HCl = 137,5 mg x 1000 = 1375 µg/ml 100 ml
V1 x C1 = V2 x C2
5 ml x 1375 µg/ml = 25 ml x C2
C2 = 275 µg/ml
Konsentrasi teoritis teofilin dan efedrin HCl:
• Teofilin = 7,0223 µg/ml
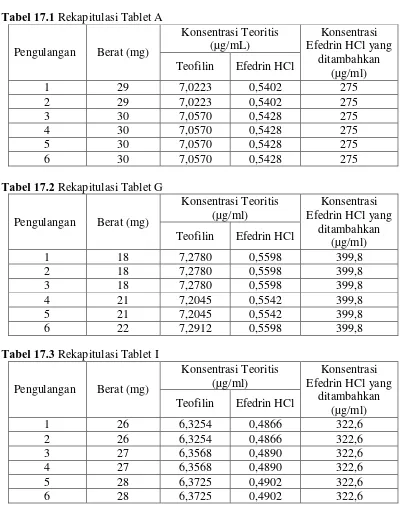
Lampiran 17. Rekapitulasi Kadar Teoritis dari Teofilin dan Efedrin HCl dalam Tablet
Tabel 17.1 Rekapitulasi Tablet A Pengulangan Berat (mg)
Konsentrasi Teoritis (µg/mL)
Konsentrasi Efedrin HCl yang
ditambahkan (µg/ml) Teofilin Efedrin HCl
1 29 7,0223 0,5402 275
2 29 7,0223 0,5402 275
3 30 7,0570 0,5428 275
4 30 7,0570 0,5428 275
5 30 7,0570 0,5428 275
6 30 7,0570 0,5428 275
Tabel 17.2 Rekapitulasi Tablet G Pengulangan Berat (mg)
Konsentrasi Teoritis (µg/ml)
Konsentrasi Efedrin HCl yang
ditambahkan (µg/ml) Teofilin Efedrin HCl
1 18 7,2780 0,5598 399,8
2 18 7,2780 0,5598 399,8
3 18 7,2780 0,5598 399,8
4 21 7,2045 0,5542 399,8
5 21 7,2045 0,5542 399,8
6 22 7,2912 0,5598 399,8
Tabel 17.3 Rekapitulasi Tablet I Pengulangan Berat (mg)
Konsentrasi Teoritis (µg/ml)
Konsentrasi Efedrin HCl yang
ditambahkan (µg/ml) Teofilin Efedrin HCl
1 26 6,3254 0,4866 322,6
2 26 6,3254 0,4866 322,6
3 27 6,3568 0,4890 322,6
4 27 6,3568 0,4890 322,6
5 28 6,3725 0,4902 322,6
6 28 6,3725 0,4902 322,6
Keterangan:
Lampiran 18. Perhitungan Kadar Teofilin dan Efedrin HCl dalam Tablet A dengan Operasi Matriks
Pengulangan 1
��1
�2�=
-⎝ ⎜ ⎛
�0.0437 0.0419 0.0314 0.02020.0001 0.0007 0.0009 0.0007� �
0.0437 0.0001 0.0419 0.0314 0.0007 0.0009 0.0202 0.0007 � 1 ⎠ ⎟ ⎞ −1
X �0.0437 0.0419 0.0314 0.0202 0.0001 0.0007 0.0009 0.0007� �
0.342 0.485 0.471 0.343
�
��1
�2� = � 7.11918 275,517� Pengulangan 2
��1
�2�=
-⎝ ⎜
⎛�0.0437 0.0419 0.0314 0.0202 0.0001 0.0007 0.0009 0.0007� �
0.0437 0.0001 0.0419 0.0314 0.0007 0.0009 0.0202 0.0007 � 1 ⎠ ⎟ ⎞ −1
X �0.0437 0.0419 0.0314 0.0202 0.0001 0.0007 0.0009 0.0007� �
0.342 0.485 0.471 0.343
�
��1
�2� = � 7.11918 275.517� Pengulangan 3
��1
�2�=
-⎝ ⎜ ⎛
�0.0437 0.0419 0.0314 0.02020.0001 0.0007 0.0009 0.0007� �
0.0437 0.0001 0.0419 0.0314 0.0007 0.0009 0.0202 0.0007 � 1 ⎠ ⎟ ⎞ −1
X �0.0437 0.0419 0.0314 0.0202 0.0001 0.0007 0.0009 0.0007� �
0.345 0.475 0.471 0.349
�
��1
�2� = � 7.08606 275.528� Pengulangan 4
��1
�2�=
-⎝ ⎜ ⎛
�0.0437 0.0419 0.0314 0.02020.0001 0.0007 0.0009 0.0007� �
0.0437 0.0001 0.0419 0.0314 0.0007 0.0009 0.0202 0.0007 � 1 ⎠ ⎟ ⎞ −1
X �0.0437 0.0419 0.0314 0.0202 0.0001 0.0007 0.0009 0.0007� �
0.347 0.480 0.470 0.352
�
��1
�2� = � 7.15063 275.521� Pengulangan 5
��1
�2�=
-⎝ ⎜ ⎛
�0.0437 0.0419 0.0314 0.02020.0001 0.0007 0.0009 0.0007� �
0.0437 0.0001 0.0419 0.0314 0.0007 0.0009 0.0202 0.0007 � 1 ⎠ ⎟ ⎞ −1
X �0.0437 0.0419 0.0314 0.0202 0.0001 0.0007 0.0009 0.0007� �
0.345 0.475 0.471 0.349
�
��1
�2� = � 7.08606 275.528� Pengulangan 6
��1
�2�=
-⎝ ⎜ ⎛
�0.0437 0.0419 0.0314 0.02020.0001 0.0007 0.0009 0.0007� �
0.0437 0.0001 0.0419 0.0314 0.0007 0.0009 0.0202 0.0007 � 1 ⎠ ⎟ ⎞ −1
X �0.0437 0.0419 0.0314 0.0202 0.0001 0.0007 0.0009 0.0007� �
0.345 0.475
0.471 0.349
�
��1
�2� = � 7.08606 275.528� Keterangan:
C1 = Konsentrasi Teofilin
Lampiran 19. Perhitungan Kadar Akurasi dari Hasil Matriks Teofilin dan Efedrin HCl dalam Tablet A
Pengulangan 1
Teofilin = 7,11918 µg/ml
7,0223 µg/ml x 99,69 % = 101,07% Efedrin HCl = (275,517−275)µg/ml
0,5402 µg/ml x 99,60 % = 95,32% Pengulangan 2
Teofilin = 7,11918 µg/ml
7,0223 µg/ml x 99,69 % = 101,07% Efedrin HCl = (275,517−275)µg/ml
0,5402 µg/ml x 99,60 % = 95,32% Pengulangan 3
Teofilin = 7,08606 µg/ml
7,0570 µg/ml x 99,69 % = 100,10% Efedrin HCl = (275,528−275)µg/ml
0,5428 µg/ml x 99,60 % = 96,88% Pengulangan 4
Teofilin = 7,15063 µg/ml
7,0570 µg/ml x 99,69 % = 101,01% Efedrin HCl = (275,521−275)µg/ml
0,5428 µg/ml x 99,60 % = 95,60% Pengulangan 5
Teofilin = 7,08606 µg/ml
7,0570 µg/ml x 99,69 % = 100,10% Efedrin HCl = (275,528−275)µg/ml
0,5428 µg/ml x 99,60 % = 96,88% Pengulangan 6
Teofilin = 7,08606 µg/ml
7,0570 µg/ml x 99,69 % = 100,10% Efedrin HCl = (275,528−275)µg/ml
Lampiran 20. Perhitungan Statistik Kadar Teofilin dan Efedrin HCl dalam Tablet A
1. Kadar Teofilin
No.
(X)
Kadar Akurasi dari Hasil Matriks (%)
X - X (X - X)2
1. 101,07 0,49 0,2401
2. 101,07 0,49 0,2401
3. 100,10 -0,48 0,2304
4. 101,01 0,43 0,1849
5. 100,10 -0,48 0,2304
6. 100,10 -0,48 0,2304
X = 100,58 Σ (X - X)2= 1,3563
SD =
�
∑��−��2
�−1 =
�
1,3563
6−1 =
�
1,3563
5 = 0,5208
Uji statistik pada taraf kepercayaan 95% maka nilai α = 0,05 ; dk = n-1 = 6-1 = 5 Diperoleh ttabel = (1 – ½ α); dk
= (1 – 0,025); 5 = 0,975; 5 = 2,5706
Dasar penerimaan data jika t hitung≤ t tabel.
t hitung =
X−X
SD /√n
t hitung 1 =
�
�−�
�� √�⁄
�
=
�
0,49
0,5208⁄√6
�
= 2,3048 (Data diterima)t hitung 2 =
�
�−�
�� √�⁄
�
=
�
0,49
0,5208⁄√6
�
= 2,3048 (Data diterima)t hitung 3 =
�
�−�
�� √�⁄
�
=
�
−0,48
Lampiran 20. (Lanjutan)
t hitung 4 =
�
�−�
�� √�⁄
�
=
�
0,43
0,5208⁄√6
�
= 2,0226 (Data diterima)t hitung 5 =
�
�−�
�� √�⁄
�
=
�
−0,48
0,5208⁄√6
�
= 2,2578 (Data diterima)t hitung 6 =
�
�−�
�� √�⁄
�
=
�
−0,48
0,5208⁄√6
�
= 2,2578 (Data diterima)Semua data diterima, maka kadar teofilin sebenarnya untuk α = 0,05; dk =5 adalah:
μ = �� ± ttabel x
�� √�
= (100,58 ± 2,5706 x 0,5208 √6 ) = (100,58 ± 0,55) %
2. Kadar Efedrin HCl
No.
(X)
Kadar Akurasi dari Hasil Matriks (%)
X - X (X - X)2
1. 95,32 -0,83 0,6889
2. 95,32 -0,83 0,6889
3. 96,88 0,73 0,5329
4. 95,60 -0,55 0,3025
5. 96,88 0,73 0,5329
6. 96,88 0,73 0,5329
X = 96,15 Σ (X - X)2= 3,279
SD =
�
∑��−��2
�−1 =
�
3,2796−1 =
�
3,279
5 = 0,8098
Uji statistik pada taraf kepercayaan 95% maka nilai α = 0,05 ; dk = n-1 = 6-1 = 5 Diperoleh ttabel = (1 – ½ α); dk
Lampiran 20. (Lanjutan)
= 0,975; 5 = 2,5706
Dasar penerimaan data jika t hitung≤ t tabel.
t hitung =
X−X
SD /√n
t hitung 1 =
�
�−�
�� √�⁄
�
=
�
−0,83
0,8098⁄√6
�
= 2,4498 (Data diterima)t hitung 2 =
�
�−�
�� √�⁄
�
=
�
−0,83
0,8098⁄√6
�
= 2,4498 (Data diterima)t hitung 3 =
�
�−�
�� √�⁄
�
=
�
0,73
0,8098⁄√6
�
= 2,1547 (Data diterima)t hitung 4 =
�
�−�
�� √�⁄
�
=
�
−0,55
0,8098⁄√6
�
= 1,6234 (Data diterima)t hitung 5 =
�
�−�
�� √�⁄
�
=
�
0,73
0,8098⁄√6
�
= 2,1547 (Data diterima)t hitung 6 =
�
�−�
�� √�⁄
�
=
�
0,73
0,8098⁄√6
�
= 2,1547 (Data diterima)Semua data diterima, maka kadar teofilin sebenarnya untuk α = 0,05; dk =5 adalah:
μ = �� ± ttabel x
�� √�
Lampiran 21. Perhitungan %KV (Koefisien Variasi) Teofilin dan Efedrin HCl dalam Tablet A
%KV = ��
� x 100%
%KV Teofilin = 0,5208
100,58 X 100% = 0,5178 % %KV Efedrin HCl = 0,8098
Lampiran 22. Data Perhitungan Kadar Teofilin dan Efedrin HCl dalam Tablet G dengan Operasi Matriks
Pengulangan 1
��1
�2�=
-⎝ ⎜ ⎛
�0.0437 0.0419 0.0314 0.02020.0001 0.0007 0.0009 0.0007� �
0.0437 0.0001 0.0419 0.0314 0.0007 0.0009 0.0202 0.0007 � 1 ⎠ ⎟ ⎞ −1
X �0.0437 0.0419 0.0314 0.0202 0.0001 0.0007 0.0009 0.0007� �
0.350 0.544 0.536 0.381
�
��1
�2� = � 7.2563 340,354� Pengulangan 2
��1
�2�=
-⎝ ⎜
⎛�0.0437 0.0419 0.0314 0.0202 0.0001 0.0007 0.0009 0.0007� �
0.0437 0.0001 0.0419 0.0314 0.0007 0.0009 0.0202 0.0007 � 1 ⎠ ⎟ ⎞ −1
X �0.0437 0.0419 0.0314 0.0202 0.0001 0.0007 0.0009 0.0007� �
0.350 0.545 0.533 0.384
�
��1
�2� = � 7.25851 340 ,349� Pengulangan 3
��1
�2�=
-⎝ ⎜ ⎛
�0.0437 0.0419 0.0314 0.02020.0001 0.0007 0.0009 0.0007� �
0.0437 0.0001 0.0419 0.0314 0.0007 0.0009 0.0202 0.0007 � 1 ⎠ ⎟ ⎞ −1
X �0.0437 0.0419 0.0314 0.0202 0.0001 0.0007 0.0009 0.0007� �
0.350 0.545 0.533 0.384
�
��1
�2� = � 7.25851 340 ,349� Pengulangan 4
��1
�2�=
-⎝ ⎜
⎛�0.0437 0.0419 0.0314 0.0202 0.0001 0.0007 0.0009 0.0007� �
0.0437 0.0001 0.0419 0.0314 0.0007 0.0009 0.0202 0.0007 � 1 ⎠ ⎟ ⎞ −1
X �0.0437 0.0419 0.0314 0.0202 0.0001 0.0007 0.0009 0.0007� �
0.350 0.545 0.533 0.384
�
��1
�2� = � 7.25851 340 ,349� Pengulangan 5
��1
�2�=
-⎝ ⎜ ⎛
�0.0437 0.0419 0.0314 0.02020.0001 0.0007 0.0009 0.0007� �
0.0437 0.0001 0.0419 0.0314 0.0007 0.0009 0.0202 0.0007 � 1 ⎠ ⎟ ⎞ −1
X �0.0437 0.0419 0.0314 0.0202 0.0001 0.0007 0.0009 0.0007� �
0.350 0.545 0.533 0.384
�
��1
�2� = � 7.25851 340 ,349� Pengulangan 6
��1
�2�=
-⎝ ⎜ ⎛
�0.0437 0.0419 0.0314 0.02020.0001 0.0007 0.0009 0.0007� �
0.0437 0.0001 0.0419 0.0314 0.0007 0.0009 0.0202 0.0007 � 1 ⎠ ⎟ ⎞ −1
X �0.0437 0.0419 0.0314 0.0202 0.0001 0.0007 0.0009 0.0007� �
0.353 0.551 0.535 0.385
�
��1
�2� = � 7.35056 340,346� Keterangan:
C1 = Konsentrasi Teofilin
Lampiran 23. Perhitungan Kadar Akurasi dari Hasil Matriks Teofilin dan Efedrin HCl dalam Tablet G
Pengulangan 1
Teofilin = 7,2563 µg/ml
7,2780 µg/ml x 99,69 % = 99,39% Efedrin HCl = (340,354−339,8)µg/ml
0,5598 µg/ml x 99,60 % = 98,67% Pengulangan 2
Teofilin = 7,25851 µg/ml
7,2780 µg/ml x 99,69 % = 99,42% Efedrin HCl = (340,349−339,8)µg/ml
0,5598 µg/ml x 99,60 % = 97,62% Pengulangan 3
Teofilin = 7,25851 µg/ml
7,2780 µg/ml x 99,69 % = 99,42% Efedrin HCl = (340,349−339,8)µg/ml
0,5598 µg/ml x 99,60 % = 97,62% Pengulangan 4
Teofilin = 7,25851 µg/ml
7,2045 µg/ml x 99,69 % = 100,44% Efedrin HCl = (340,349−339,8)µg/ml
0,5542 µg/ml x 99,60 % = 98,60% Pengulangan 5
Teofilin = 7,25851 µg/ml
7,2045 µg/ml x 99,69 % = 100,44% Efedrin HCl = (340,349−339,8)µg/ml
0,5542 µg/ml x 99,60 % = 98,60% Pengulangan 6
Teofilin = 7,35056 µg/ml
7,2912 µg/ml x 99,69 % = 100,50% Efedrin HCl = (340,346−339,8)µg/ml
Lampiran 24. Perhitungan Statistik Kadar Teofilin dan Efedrin HCl dalam Tablet G
1. Kadar Teofilin
No.
(X)
Kadar Akurasi dari Hasil Matriks (%)
X - X (X - X)2
1. 99,39 -0,54 0,2916
2. 99,42 -0,51 0,2601
3. 99,42 -0,51 0,2601
4. 100,44 0,51 0,2601
5. 100,44 0,51 0,2601
6. 100,50 0,57 0,3249
X = 99,93 Σ (X - X)2= 1,6569
SD =
�
∑��−��2
�−1 =
�
1,6569
6−1 =
�
1,6569
5 = 0,5757
Uji statistik pada taraf kepercayaan 95% maka nilai α = 0,05 ; dk = n-1 = 6-1 = 5 Diperoleh ttabel = (1 – ½ α); dk
= (1 – 0,025); 5 = 0,975; 5 = 2,5706
Dasar penerimaan data jika t hitung≤ t tabel.
t hitung =
X−X
SD /√n
t hitung 1 =
�
�−�
�� √�⁄
�
=
�
−0,54
0,5757⁄√6
�
= 2,2979 (Data diterima)t hitung 2 =
�
�−�
�� √�⁄
�
=
�
−0,51
0,5757⁄√6
�
= 2,1702 (Data diterima)t hitung 3 =
�
�−�
�� √�⁄
�
=
�
−0,51
Lampiran 24. (Lanjutan)
t hitung 4 =
�
�−�
�� √�⁄
�
=
�
0,51
0,5757⁄√6
�
= 2,1702 (Data diterima)t hitung 5 =
�
�−�
�� √�⁄
�
=
�
0,51
0,5757⁄√6
�
= 2,1702 (Data diterima)t hitung 6 =
�
�−�
�� √�⁄
�
=
�
0,57
0,5757⁄√6
�
= 2,4255 (Data diterima)Semua data diterima, maka kadar teofilin sebenarnya untuk α = 0,05; dk =5 adalah:
μ = �� ± ttabel x
�� √�
= (99,93 ± 2,5706 x 0,5756 √6 ) = (99,93 ± 0,60) %
2. Kadar Efedrin HCl
No.
(X)
Kadar Akurasi dari Hasil Matriks (%)
X - X (X - X)2
1. 98,67 0,55 0,3025
2. 97,62 -0,50 0,2500
3. 97,62 -0,50 0,2500
4. 98,60 0,48 0,2352
5. 98,60 0,48 0,2352
6. 97,64 -0,48 0,2352
X = 98,12 Σ (X - X)2= 1,5081
SD =
�
∑�X−X�2
n−1 =
�
1,5081
6−1 =
�
1,5081
5 = 0,5492
Uji statistik pada taraf kepercayaan 95% maka nilai α = 0,05 ; dk = n-1 = 6-1 = 5 Diperoleh ttabel = (1 – ½ α); dk
Lampiran 24. (Lanjutan)
= 0,975; 5 = 2,5706
Dasar penerimaan data jika t hitung≤ t tabel.
t hitung =
X−X
SD /√n
t hitung 1 =
�
�−�
�� √�⁄
�
=
�
0,55
0,5492⁄√6
�
= 2,4532 (Data diterima)t hitung 2 =
�
�−�
�� √�⁄
�
=
�
−0,50
0,5492⁄√6
�
= 2,2301 (Data diterima)t hitung 3 =
�
�−�
�� √�⁄
�
=
�
−0,50
0,5492⁄√6
�
= 2,2301 (Data diterima)t hitung 4 =
�
�−�
�� √�⁄
�
=
�
0,48
0,5492⁄√6
�
= 2,1409 (Data diterima)t hitung 5 =
�
�−�
�� √�⁄
�
=
�
0,48
0,5492⁄√6
�
= 2,1409 (Data diterima)t hitung 6 =
�
�−�
�� √�⁄
�
=
�
−0,48
0,5492⁄√6
�
= 2,1409 (Data diterima)Semua data diterima, maka kadar efedrin HCl sebenarnya untuk α = 0,05; dk =5 adalah:
μ = �� ± ttabel x
�� √�
Lampiran 25. Perhitungan %KV (Koefisien Variasi) Teofilin dan Efedrin HCl dalam Tablet G
%KV = ��
� x 100%
%KV Teofilin = 0,5757
99,93 X 100% = 0,5761% %KV Efedrin HCl = 0,5492
Lampiran 26. Data Perhitungan Kadar Teofilin dan Efedrin HCl dalam Tablet I dengan Operasi Matriks
Pengulangan 1
��1
�2�=
-⎝ ⎜ ⎛
�0.0437 0.0419 0.0314 0.02020.0001 0.0007 0.0009 0.0007� �
0.0437 0.0001 0.0419 0.0314 0.0007 0.0009 0.0202 0.0007 � 1 ⎠ ⎟ ⎞ −1
X �0.0437 0.0419 0.0314 0.0202 0.0001 0.0007 0.0009 0.0007� �
0.319 0.485 0.488 0.371
�
��1
�2� = � 6,42212 323 ,098� Pengulangan 2
��1
�2�=
-⎝ ⎜
⎛�0.0437 0.0419 0.0314 0.0202 0.0001 0.0007 0.0009 0.0007� �
0.0437 0.0001 0.0419 0.0314 0.0007 0.0009 0.0202 0.0007 � 1 ⎠ ⎟ ⎞ −1
X �0.0437 0.0419 0.0314 0.0202 0.0001 0.0007 0.0009 0.0007� �
0.318 0.477 0.488 0.371
�
��1
�2� = � 6,34724 323 ,097� Pengulangan 3
��1
�2�=
-⎝ ⎜ ⎛
�0.0437 0.0419 0.0314 0.02020.0001 0.0007 0.0009 0.0007� �
0.0437 0.0001 0.0419 0.0314 0.0007 0.0009 0.0202 0.0007 � 1 ⎠ ⎟ ⎞ −1
X �0.0437 0.0419 0.0314 0.0202 0.0001 0.0007 0.0009 0.0007� �
0.319 0.485 0.488
0.371
�
��1
�2� = � 6,42212 323 ,098� Pengulangan 4
��1
�2�=
-⎝ ⎜
⎛�0.0437 0.0419 0.0314 0.0202 0.0001 0.0007 0.0009 0.0007� �
0.0437 0.0001 0.0419 0.0314 0.0007 0.0009 0.0202 0.0007 � 1 ⎠ ⎟ ⎞ −1
X �0.0437 0.0419 0.0314 0.0202 0.0001 0.0007 0.0009 0.0007� �
0.320 0.493 0.488 0.371
�
��1
�2� = � 6,49699 323,099� Pengulangan 5
��1
�2�=
-⎝ ⎜ ⎛
�0.0437 0.0419 0.0314 0.02020.0001 0.0007 0.0009 0.0007� �
0.0437 0.0001 0.0419 0.0314 0.0007 0.0009 0.0202 0.0007 � 1 ⎠ ⎟ ⎞ −1
X �0.0437 0.0419 0.0314 0.0202 0.0001 0.0007 0.0009 0.0007� �
0.319 0.485 0.488 0.371
�
��1
�2� = � 6,42212 323 ,098� Pengulangan 6
��1
�2�=
-⎝ ⎜ ⎛
�0.0437 0.0419 0.0314 0.02020.0001 0.0007 0.0009 0.0007� �
0.0437 0.0001 0.0419 0.0314 0.0007 0.0009 0.0202 0.0007 � 1 ⎠ ⎟ ⎞ −1
X �0.0437 0.0419 0.0314 0.0202 0.0001 0.0007 0.0009 0.0007� �
0.320 0.493 0.488 0.371
�
��1
�2� = � 6,49699 323,099� Keterangan:
C1 = Konsentrasi Teofilin
Lampiran 27. Perhitungan Kadar Akurasi dari Hasil Matriks Teofilin dan Efedrin HCl dalam Tablet I
Pengulangan 1
Teofilin = 6,42212 µg/ml
6,3254 µg/ml x 99,69 % = 101,21% Efedrin HCl = (323,098−322,6)µg/ml
0,4866 µg/ml x 99,60 % = 101,93% Pengulangan 2
Teofilin = 6,34724 µg/ml
6,3254 µg/ml x 99,69 % = 100,03% Efedrin HCl = (323,097−322,6)µg/ml
0,4866 µg/ml x 99,60 % = 101,73% Pengulangan 3
Teofilin = 6,42212 µg/ml
6,3568 µg/ml x 99,69 % = 100,71% Efedrin HCl = (323,098−322,6)µg/ml
0,4890 µg/ml x 99,60 % = 101,43% Pengulangan 4
Teofilin = 6,49699 µg/ml
6,3568 µg/ml x 99,69 % = 101,89% Efedrin HCl = (323,099−322,6)µg/ml
0,4890 µg/ml x 99,60 % = 101,64% Pengulangan 5
Teofilin = 6,42212 µg/ml
6,3725 µg/ml x 99,69 % = 100,47% Efedrin HCl = (323,098−322,6)µg/ml
0,4902 µg/ml x 99,60 % = 101,18% Pengulangan 6
Teofilin = 6,49699 µg/ml
6,3725 µg/ml x 99,69 % = 101,64% Efedrin HCl = (323,099−322,6)µg/ml
Lampiran 28. Perhitungan Statistik Kadar Teofilin dan Efedrin HCl dalam Tablet I
1. Kadar Teofilin
No.
(X)
Kadar Akurasi dari Hasil Matriks (%)
X - X (X - X)2
1. 101,21 0,22 0.0484
2. 100,03 -0,96 0.9216
3. 100,71 -0,28 0.0784
4. 101,89 0,90 0.8100
5. 100,47 -0,52 0.2704
6. 101,64 0,65 0.4225
X = 100,99 Σ (X - X)2= 2,5513
SD =
�
∑��−��2
�−1 =
�
2,5513
6−1 =
�
2,5513
5 = 0,7143
Uji statistik pada taraf kepercayaan 95% maka nilai α = 0,05 ; dk = n-1 = 6-1 = 5 Diperoleh ttabel = (1 – ½ α); dk
= (1 – 0,025); 5 = 0,975; 5 = 2,5706
Dasar penerimaan data jika t hitung≤ t tabel.
t hitung =
X−X
SD /√n
t hitung 1 =
�
�−�
�� √�⁄
�
=
�
0,22
0,7143⁄√6
�
= 0,7545 (Data diterima)t hitung 2 =
�
�−�
�� √�⁄
�
=
�
−0,96
0,7143⁄√6
�
= 3,2922 (Data ditolak)t hitung 3 =
�
�−�
�� √�⁄
�
=
�
−0,28
Lampiran 28. (Lanjutan)
t hitung 4 =
�
�−�
�� √�⁄
�
=
�
0,90
0,7143⁄√6
�
= 3,0864 (Data ditolak)t hitung 5 =
�
�−�
�� √�⁄
�
=
�
−0,52
0,7143⁄√6
�
= 2,2291 (Data diterima)t hitung 6 =
�
�−�
�� √�⁄
�
=
�
0,65
0,7143⁄√6
�
= 1,7833 (Data diterima)Data 2 dan 4 ditolak karena nilai t hitung≥ t tabel, maka data yang dipakai adalah
data nomor 1,3,5, dan 6.
No.
(X) Kadar Akurasi
dari hasil
matriks (%) X - X (X - X)
2
1. 101,21 0,20 0,0400
3. 100,71 -0,30 0,0900
5. 101,64 0,63 0,3969
6. 100,47 -0,54 0,2916
X = 101,01 Σ (X - X)2= 0,8185
SD =
�
∑��−��2
�−1 =
�
0,8185
4−1 =
�
0,8185
3 = 0,5223
Uji statistik pada taraf kepercayaan 95% maka nilai α = 0,05 ; dk = 4-1 = 4-1 = 3 Diperoleh ttabel= (1 – ½ α); dk
= (1 – 0,025); 3 = 0,975; 3 = 3,1824
Dasar penerimaan data jika t hitung≤ t tabel.
t hitung =
X−X
SD /√n
t hitung 1 =
�
�−�
�� √�⁄
�
=
�
0,20
Lampiran 28. (Lanjutan)
t hitung 3 =
�
�−�
�� √�⁄
�
=
�
−0,30
0,5223⁄√4
�
= 1,1490 (Data diterima)t hitung 5 =
�
�−�
�� √�⁄
�
=
�
0,63
0,5223⁄√4
�
= 2,4129 (Data diterima)t hitung 6 =
�
�−�
�� √�⁄
�
=
�
−0,54
0,5223⁄√4
�
= 2,0682 (Data diterima)Semua data diterima, maka kadar teofilin sebenarnya adalah:
μ = �� ± ttabel x ��
√�
= 101,01 ± 3,1824x 0,5223
√4
= (101,01 ± 0,83)%
2. Kadar Efedrin HCl
No.
(X)
Kadar Akurasi dari Hasil Matriks (%)
X - X (X - X)2
1. 101,93 0,38 0,1444
2. 101,73 0,18 0,0324
3. 101,43 -0,12 0,0144
4. 101,64 0,09 0,0081
5. 101,18 -0,37 0,1369
6. 101,39 -0,16 0,0256
X = 101,55 Σ (X - X)2= 0,3618
SD =
�
∑�X−X�2
n−1 =
�
0,3618
6−1 =
�
0,3618
5 = 0,2690
Uji statistik pada taraf kepercayaan 95% maka nilai α = 0,05 ; dk = n-1 = 6-1 = 5 Diperoleh ttabel = (1 – ½ α); dk
Lampiran 28. (Lanjutan)
= 2,5706
Dasar penerimaan data jika t hitung≤ t tabel.
t hitung =
X−X
SD /√n
t hitung 1 =
�
�−�
�� √�⁄
�
=
�
0,38
0,2690⁄√6
�
= 3,4608 (Data ditolak)t hitung 2 =
�
�−�
�� √�⁄
�
=
�
0,18
0,2690⁄√6
�
= 1,6393 (Data diterima)t hitung 3 =
�
�−�
�� √�⁄
�
=
�
−0,12
0,2690⁄√6
�
= 1,0929 (Data diterima)t hitung 4 =
�
�−�
�� √�⁄
�
=
�
0,09
0,2690⁄√6
�
= 0,8197 (Data diterima)t hitung 5 =
�
�−�
�� √�⁄
�
=
�
−0,37
0,2690⁄√6
�
= 3,3698 (Data ditolak)t hitung 6 =
�
�−�
�� √�⁄
�
=
�
−0,16
0,2690⁄√6
�
= 1,4572 (Data diterima)Data 1 dan 4 ditolak karena nilai t hitung≥ t tabel, maka data yang dipakai adalah
data nomor 2,3,4, dan 6.
No.
(X) Kadar Akurasi
dari hasil
matriks (%) X - X (X - X)
2
2. 101,73 0,18 0,0324
3. 101,43 -0,12 0,0144
4. 101,64 -0,09 0,0081
6. 101,39 0,16 0,0256
Lampiran 28. (Lanjutan)
SD =
�
∑�X−X�2
n−1 =
�
0,0805
4−1 =
�
0,0805
3 = 0,1638
Uji statistik pada taraf kepercayaan 95% maka nilai α = 0,05 ; dk = 4-1 = 4-1 = 3 Diperoleh ttabel= (1 – ½ α); dk
= (1 – 0,025); 3 = 0,975; 3 = 3,1824
Dasar penerimaan data jika t hitung≤ t tabel.
t hitung =
X−X
SD /√n
t hitung 1 =
�
�−�
�� √�⁄
�
=
�
0,18
0,1638⁄√4
�
= 2,1978 (Data diterima)t hitung 3 =
�
�−�
�� √�⁄
�
=
�
−0,12
0,1638⁄√4
�
= 1,4652 (Data diterima)t hitung 5 =
�
�−�
�� √�⁄
�
=
�
−0,09
0,1638⁄√4
�
= 1,0989 (Data diterima)t hitung 6 =
�
�−�
�� √�⁄
�
=
�
0,16
0,1638⁄√4
�
= 1,9536 (Data diterima)Semua data diterima, maka kadar efedrin HCl sebenarnya adalah:
μ = �� ± ttabel x ��
√�
= 101,55 ± 3,1824x 0,1638
√4
Lampiran 29. Perhitungan %KV (Koefisien Variasi) Teofilin dan Efedrin HCl dalam Tablet I
%KV = ��
� x 100%
%KV Teofilin = 0,5223
101,01 X 100% = 0,5171% %KV Efedrin HCl = 0,1638
Lampiran 30. Spektrum Serapan dari Larutan Baku Campuran Teofilin dan Efedrin HCl
[image:43.595.116.511.489.719.2]Gambar 7. Pengulangan 1
Gambar 8. Pengulangan 2
Gambar 9. Pengulangan 3
nm .
200.00 250.00 300.00 350.00 400.00
Ab
s.
1.000
0.800
0.600
0.400
0.200
Lampiran 30. (Lanjutan)
[image:44.595.118.512.449.688.2]Gambar 10. Pengulangan 4
Gambar 11. Pengulangan 5
Gambar 12. Pengulangan 6
nm .
200.00 250.00 300.00 350.00 400.00
Ab
s.
1.000
0.800
0.600
0.400
0.200
Lampiran 31. Spektrum Serapan dari Sampel Teofilin dan Efedrin HCl dalam Tablet A
[image:45.595.122.508.521.727.2]Gambar 13. Pengulangan 1
Gambar 14. Pengulangan 2
Gambar 15. Pengulangan 3
nm .
200.00 250.00 300.00 350.00 400.00
Ab
s.
1.250
1.000
0.500
Lampiran 31. (Lanjutan)
[image:46.595.121.511.491.703.2]Gambar 16. Pengulangan 4
Gambar 17. Pengulangan 5
Gambar 18. Pengulangan 6
nm .
200.00 250.00 300.00 350.00 400.00
Ab
s.
1.250
1.000
0.500
Lampiran 32. Spektrum Serapan dari Sampel Teofilin dan Efedrin HCl dalam Tablet G
Gambar 19. Pengulangan 1
[image:47.595.124.509.530.723.2]Gambar 20. Pengulangan 2
Gambar 21. Pengulangan 3
nm .
200.00 250.00 300.00 350.00 400.00
Ab
s.
0.700
0.600
0.400
0.200
Lampiran 32. (Lanjutan)
[image:48.595.121.508.497.702.2]Gambar 22. Pengulangan 4
Gambar 23. Pengulangan 5
Gambar 24. Pengulangan 6
nm .
200.00 250.00 300.00 350.00 400.00
Ab
s.
0.700
0.600
0.400
0.200
Lampiran 33. Spektrum Serapan dari Sampel Teofilin dan Efedrin HCl dalam Tablet I
[image:49.595.121.513.487.711.2]Gambar 25. Pengulangan 1
Gambar 26. Pengulangan 2
Gambar 27. Pengulangan 3 nm .
200.00 250.00 300.00 350.00 400.00
Ab
s.
0.900
0.800
0.600
0.400
0.200
Lampiran 33. (Lanjutan)
Gambar 28. Pengulangan 4
[image:50.595.124.510.524.716.2]Gambar 29. Pengulangan 5
Gambar 30. Pengulangan 6
nm .
200.00 250.00 300.00 350.00 400.00
Ab
s.
0.900
0.800
0.600
0.400
0.200
DAFTAR PUSTAKA
Andrianto, Y.C. (2009). Validasi Metode Penetapan Kadar Campuran Parasetamol dan Ibuprofen Secara Spektrofotometri UV dengan Aplikasi Metode Panjang Gelombang Berganda. Skripsi. Yogyakarta: Fakultas Farmasi Universitas Sanata Dharma. Halaman 1-3, 23-26.
Bliesner, D.M. (2006). Validating Chromatographic Methods: A Practical Guide. New Jersey: John Wiley and Sons, Inc. Halaman 1.
Budiarto, E. (2004). Metodologi Penelitian Kedokteran: Sebuah Pengantar. Cetakan Pertama. Jakarta: Penerbit Buku Kedokteran EGC. Halaman 46. Day, R.A., dan Underwood, A.L. (1986). Quantitative Analysis. Edisi Kelima.
Penerjemah: Pudjaatmaka, A.H. (2002). Analisis Kimia Kuantitatif. Edisi Kelima. Jakarta: Penerbit Erlangga. Halaman 413-415.
Ditjen POM. (1979). Farmakope Indonesia. Edisi Ketiga. Jakarta: Departemen Kesehatan RI. Halaman 53.
Ditjen BKAK. (2014). Farmakope Indonesia. Edisi Kelima. Jakarta: Kementerian Kesehatan RI. Halaman 57, 363, 1250-1251.
Ermer, J., dan McB., J.H.M. (2005). Method Validation in Pharmaceutical Analysis: A Guide to Best Practice. Weinheim: Wiley-VCH. Halaman 63, 80, 86.
Gandjar, I.G., dan Rohman, A. (2012). Analisis Obat secara Spektrofotometri dan Kromatografi. Cetakan Pertama. Yogyakarta: Pustaka Pelajar. Halaman 466-467.
Harmita. (2004). Petunjuk Pelaksanaan Validasi Metode dan Cara Perhitungannya. Majalah Ilmu Kefarmasian. 1(3): 117-135.
Huber, L. (2007). Validation and Qualification in Analytical Laboratories. Edisi Kedua. New York: Informa Healthcare USA, Inc. Halaman 125-126. Khopkar, S.M. (1985). Basic Concepts of Analytical Chemistry. Penerjemah:
Saptorahardjo, A., dan Nurhadi, A. (1990). Konsep Dasar Kimia Analitik. Jakarta: UI-Press. Halaman 215.
Moffat, A.C., Osselton, M.D., dan Widdop, B. (2005). Clarke’s Analysis of Drugs and Poisons. Edisi Ketiga. London: Pharmaceutical Press. Halaman 351, 517.
Mulja, M., dan Suharman. (1995). Analisis Instrumental. Surabaya: Airlangga University Press. Halaman 35 dan 52.
Munson, J.W. (1984). Pharmaceutical Analysis: Modern Methods. Part B. Penerjemah: Harjana. (1991). Analisis Farmasi: Metode Modern. Parwa B. Surabaya: Airlangga University Press. Halaman 334 dan 385.
Owen, T. (1996). Fundamentals of UV-Visible Spectroscopy. Germany: Hewlett-Packard. Halaman 48.
Pratiwi, P. (2011). Optimasi Fase Gerak Metanol-Air dan Laju Alir pada Penetapan Kadar Campuran Teofilin dan Efedrin HCl Dalam Tablet dengan Metode Kromatografi Cair Kinerja Tinggi (KCKT). Skripsi. Medan: Fakultas Farmasi Universitas Sumatera Utara. Halaman 20.
Rohman, A. (2007). Kimia Farmasi Analisis. Cetakan Pertama. Yogyakarta: Pustaka Pelajar. Halaman 224-233, 240-243, 254-255, 261-262.
Satiadarma, K., Mulja, H.M., Tjahjono, D.H., dan Kartasasmita, R.E. (2004). Asas Pengembangan Prosedur Analisis. Edisi Pertama. Surabaya: Airlangga University Press. Halaman 46-47, 88-91, 97.
Sentuerk, Z., Erk, N., Oezkan, S.A., Akay, C., dan Cevheroglu, S. (2002). Determination of Theophylline and Ephedrine HCl in Tablets by Ratio-Spectra Derivative Spectrophotometry and LC. Journal of Pharmaceutical and Biomedical Analysis. 29: 291-298.
Sudjana. (2005). Metode Statistika. Bandung: Penerbit Tarsito. Halaman 93, 145, 201, 225.
Sweetman, S.C. (2009). Martindale: The Complete Drug Reference. Edisi Ketiga Puluh Enam. London: Pharmaceutical Press. Halaman 418.
Tan, T.H., dan Rahardja, K. (2007). Obat-Obat Penting Kasiat, Penggunaan, dan Efek-Efek Sampingnya. Edisi Keenam. Jakarta: PT. Elex Media Komputindo. Halaman 646, 651.
Tarigan, T.O. (2015). Penetapan Kadar Campuran Teofilin dan Efedrin Hidroklorida dalam Sediaan Tablet dengan Metode Spektrofotometri Derivatif. Skripsi. Medan: Fakultas Farmasi Universitas Sumatera Utara. Halaman 30-47.
BAB III
METODE PENELITIAN
3.1 Jenis Penelitian
Penelitian ini termasuk jenis penelitian eksperimental dengan menggunakan metode yang dikembangkan dari metode spektrofotometri secara multikomponen dan adanya percobaan bereksperimen dalam menentukan panjang gelombang yang akan digunakan terhadap penetapan kadar campuran teofilin dan efedrin hidroklorida yang terkandung dalam tiga sediaan tablet merek dagang.
3.2 Tempat dan Waktu Penelitian
Penelitian ini dilakukan pada bulan Desember 2015 sampai dengan Februari 2016 di Laboratorium Farmasi Fisik Fakultas Farmasi Universitas Sumatera Utara.
3.3 Alat
Alat-alat yang digunakan dalam penelitian ini adalah spektrofotometer UV-Visible, Personal Computer (PC) yang dilengkapi dengan software UV Probe
2.42 (UV-1800 Shimadzu), neraca analitik (Ohaus), sonikator (Branson 1510), kuvet, kertas saring, lumpang dan alu, bola karet, spatula, alat gelas dan alat-alat lainnya yang diperlukan dalam penyiapan sampel. Gambar beberapa alat-alat di atas dapat dilihat pada Lampiran 3 halaman 49.
3.4 Bahan
97), tablet Asmadex® (PT Dexa Medica) yang kemudian pada penelitian ini disebut tablet A, tablet Grafasma® (PT Graha Farma) yang kemudian pada penelitian ini disebut tablet G, dan tablet Ifasma® (PT Ifars) yang kemudian pada penelitian ini disebut tablet I.
3.5 Pengambilan Sampel
Metode pengambilan sampel dilakukan cara sampling purposif yang dikenal juga sebagai sampel pertimbangan, dimana sampel ditentukan atas dasar pertimbangan bahwa sampel yang diambil dapat mewakili populasi (Budiarto, 2004). Sampel yang digunakan yaitu tablet A, tablet G, dan tablet I yang mengandung teofilin 130 mg dan efedrin HCl 10 mg. Gambar sediaan dan daftar spesifikasi sediaan tablet masing-masing dapat dilihat pada Lampiran 1 dan 2 halaman 46 dan 48.
3.6 Prosedur Penelitian 3.6.1 Pembuatan Pelarut
Diencerkan 8,3 ml HCl 37% (v/v) dengan 1 Liter akuades (Ditjen POM RI,
1979). Perhitungan pembuatan pereaksi dapat dilihat pada Lampiran 4 halaman 51. 3.6.2 Pembuatan Larutan Induk Baku
3.6.2.1 Pembuatan Larutan Induk Baku Teofilin
dengan HCl 0,1 N sampai garis tanda sehingga diperoleh larutan dengan konsentrasi 50 μg/ml (LIB II). Bagan alir prosedur penelitian dapat dilihat pada Lampiran 5 halaman 52.
3.6.2.2 Pembuatan Larutan Induk Baku Efedrin HCl
Ditimbang dengan seksama 50 mg baku pembanding efedrin HCl BPFI, kemudian dimasukkan ke dalam labu tentukur 50 ml, dilarutkan dengan HCl 0,1 N hingga larut, dan dicukupkan volume dengan HCl 0,1 N sampai garis tanda sehingga didapatkan larutan dengan konsentrasi 1000 μg/ml (LIB I). Bagan alir prosedur penelitian dapat dilihat pada Lampiran 6 halaman 53.
3.6.3 Pembuatan Spektrum Serapan Maksimum
3.6.3.1 Pembuatan Spektrum Serapan Maksimum Teofilin
Diambil sebanyak 4,05 ml dari LIB II teofilin (konsentrasi = 50 μg/ml), kemudian dimasukkan ke dalam labu tentukur 25 ml. Selanjutnya larutan diencerkan dengan pelarut HCl 0,1 N sampai garis tanda, lalu dikocok sampai homogen untuk memperoleh larutan teofilin dengan konsentrasi 8,1 μg/ml. Diukur serapannya pada panjang gelombang 200-400 nm. Bagan alir prosedur penelitian dapat dilihat pada Lampiran 5 halaman 52.
3.6.3.2 Pembuatan Spektrum Serapan Maksimum Efedrin HCl
3.6.4 Penentuan Panjang Gelombang Analisis dari Tumpang Tindih Spektrum
Dibuat larutan teofilin dengan konsentrasi 8,1 μg/ml dan larutan efedrin HCl dengan konsentrasi 361,92 μg/ml. Kemudian kedua larutan ini diukur serapannya masing-masing pada panjang gelombang 200–400 nm. Selanjutnya spektrum serapan dari masing-masing komponen ditumpang-tindihkan, pembacaan spektrum ini dilakukan pada rentang panjang gelombang antara teofilin dan efedrin HCl bertumpang tindih secara keseluruhan. Kemudian dipilih titik panjang gelombang yang akan digunakan, pemilihan panjang gelombang diambil dari spektrum serapan maksimum masing-masing komponen. Bagan alir prosedur penelitian dapat dilihat pada Lampuran 7 halaman 54.
3.6.5 Penentuan Serapan pada Empat Panjang Gelombang 3.6.5.1 Pembuatan Larutan Standar Teofilin
Larutan standar dibuat dalam 5 labu tentukur 25 ml yang memiliki konsentrasi masing-masing 3,73 μg/ml; 5,60 μg/ml; 8,10 μg/ml; 9,33 μg/ml; dan 11,19 μg/ml, dengan cara mengencerkan sebanyak 1,86 ml; 2,80 ml; 4,05 ml; 4,66 ml; dan 5,59 ml secara berurutan dari LIB II teofilin (konsentrasi = 50 μg/ml) menggunakan pelarut HCl 0,1 N. Bagan alir prosedur penelitian dapat dilihat pada Lampiran 8 halaman 55.
3.6.5.2 Pembuatan Larutan Standar Efedrin HCl
μg/ml) menggunakan pelarut HCl 0,1 N. Bagan alir prosedur penelitian dapat dilihat pada Lampiran 9 halaman 56.
3.6.5.3 Penentuan Serapan Larutan Standar
Larutan standar teofilin dan efedrin HCl yang telah dibuat, diukur absorbansinya pada empat panjang gelombang yang telah ditentukan. Nilai serapan kedua senyawa ditentukan dengan menggunakan persamaan regresi yang dioperasikan pada data konsentrasi dan absorbansi masing-masing komponen pada setiap panjang gelombang pengukuran.
Dari persamaan regresi yang diperoleh : y = ax + b Keterangan:
y = Harga serapan (A)
a = Koefisien regresi yang menunjukkan nilai serapan x = Konsentrasi (µg/ml)
b = Konstanta
3.6.6 Penentuan Spektrum Serapan Campuran Baku Teofilin dan Efedrin HCl
3.6.7 Penentuan Kadar Teofilin dan Efedrin HCl dalam Tablet A, Tablet G, dan Tablet I
Ditimbang 20 tablet merek dagang yang mengandung teofilin 130 mg dan efedrin HCl 10 mg, kemudian digerus dalam lumpang sampai halus dan homogen. Selanjutnya ditimbang seksama sejumlah serbuk setara dengan 10 mg teofilin (penimbangan serbuk dilakukan sebanyak 6 kali pengulangan), dihitung kesetaraan efedrin HCl yang terkandung di dalamnya. Selanjutnya dimasukkan ke dalam labu tentukur 100 ml dan dilarutkan dengan HCl 0,1 N (dihomogenkan dengan sonikator selama 15 menit), kemudian dicukupkan dengan HCl 0,1 N sampai garis tanda, dikocok sampai homogen. Larutan tersebut kemudian disaring, lebih kurang 10 ml filtrat pertama dibuang. Filtrat selanjutnya ditampung dan dipipet sebanyak 1,7 ml dan dimasukkan ke dalam labu tentukur 25 ml.
Kemudian ditambahkan 5 ml dari larutan efedrin HCl (konsentrasi = 1000 μg/ml) dan dimasukkan ke dalam labu tentukur 25 ml yang di dalamnya terdapat 1,7 ml filtrat. Campuran tersebut dicukupkan dengan HCl 0,1 N sampai garis tanda sehingga diperoleh larutan yang di dalamnya terdapat teofilin dengan konsentrasi 7 μg/ml dan efedrin HCl dengan konsentrasi 360 μg/ml. Diukur serapan pada empat panjang gelombang yang telah ditentukan. Bagan alir prosedur penelitian penentuan kadar teofilin dan efedrin HCl dalam tablet A, tablet G, dan tablet I masing-masing dapat dilihat pada Lampiran 11 halaman 58, Lampiran 12 halaman 59, dan Lampiran 13 halaman 60.
metode tersebut, kadar yang diperoleh dinyatakan sebagai rasio antara hasil yang diperoleh dengan hasil yang sebenarnya:
% Kadar Sampel = CA − CB
CC
x
100 %Keterangan:
CA = Konsentrasi perolehan sampel setelah penambahan bahan baku
CC = Konsentrasi teoritis sampel sebelum penambahan bahan baku
CB = Konsentrasi baku yang ditambahkan
3.6.8 Perhitungan Kadar Teofilin dan Efedrin HCl dalam Campuran
Perhitungan kadar masing-masing komponen dalam campuran dilakukan atas dasar serapan campuran (Ac) dan serapan tiap komponen pada multi panjang gelombang yang telah diketahui dari hasil pengukuran dengan menggunakan persamaan matriks:
[c] = [[a] x [a1]]-1 x [a] x Ac] Keterangan:
[c] = Kadar komponen dari campuran
[a] = Matriks serapan senyawa penyusun campuran
[a1] = Matriks perubahan bentuk serapan senyawa penyusun campuran
[[a] X [a1]]-1 = Invers matriks dikali transpose matriks serapan senyawa penyusun campuran
[Ac] = Matriks nilai serapan sampel 3.6.9 Analisis Hasil
Analisis hasil dilakukan untuk mengetahui validitas metode yang digunakan dalam penelitian, berikut parameter yang diukur:
a. Akurasi
Akurasi dari hasil matriks diperoleh dengan rumus: Akurasi dari hasil matriks = Kadar perolehan matriks
Kadar teoritis x % Kadar sertifikat analisis
b. Presisi
Penentuan presisi berdasarkan nilai koefisian variasi (KV) atau Coefficient of variation (CV). Jika KV lebih kecil dari 2% maka dinilai
mempunyai presisi yang baik (Andrianto, 2009). Koefisien variasi (KV) diperoleh dengan rumus:
KV = Standar deviasi kadar hasil
Harga rerata kadar hasil x 100%
c. Analisis Data Penetapan Kadar Secara Statistik
Data perhitungan kadar teofilin dan efedrin HCl dianalisis secara statistik dengan menggunakan uji ttabel distribusi t dapat dilihat pada Lampiran 29
halaman 84 dan Lampiran 30 halaman 85. Rumus yang digunakan adalah:
SD =
�
∑�X−X� 2n−1
Untuk mencari thitung digunakan rumus:
thitung = X−X SD /√n
Data diterima jika thitung < ttabel pada interval kepercayaan 95% dengan
nilai α = 0,05. Keterangan:
SD = Standard deviation / simpangan baku Xi = Kadar dalam satu perlakuan
−
X = Kadar rata-rata dalam satu sampel
n = Jumlah pengulangan
Menurut Sudjana (2005), untuk menghitung kadar teofilin dan efedrin HCl sebenarnya dalam sampel secara statistik dapat digunakan rumus:
μ = X� ± ttabel x SD √n
Keterangan:
SD = Standard deviation / simpangan baku
−
X = Kadar rata-rata dalam satu sampel
n = Jumlah pengulangan
BAB IV
HASIL DAN PEMBAHASAN
4.1 Hasil Penentuan Spektrum Serapan Maksimum
Berdasarkan hasil penelitian, diperoleh panjang gelombang maksimum
teofilin (konsentrasi = 8,1 μg/ml) pada 270,40 nm dan untuk efedrin HCl
(konsentrasi = 360,4 μg/ml) pada 262,80 nm; 256,80 nm; dan 251,20 nm.
Spektrum serapan maksimum teofilin dan efedrin HCl masing-masing dapat dilihat pada Gambar 4.1 dan Gambar 4.2, sedangkan tumpang tindih spektrum serapan teofilin dan efedrin HCl dapat dilihat pada Gambar 4.3.
Gambar 4.1 Spektrum Serapan Maksimum Teofilin (8,1 μg/ml)
Spektrum Serapan Maksimum Efedrin HCl (360,4 μg/ml)
nm .
200.00 250.00 300.00 350.00 400.00
Ab
s.
2.500
2.000
1.500
1.000
0.500
0.000
262,80 nm 256,80 nm
[image:67.595.119.506.538.736.2]Gambar 4.3 Tumpang Tindih Spektrum Serapan Maksimum Teofilin (8,1 µg/ml) dan Efedrin HCl (360,4 µg/ml)
Penentuan spektrum serapan maksimum teofilin dan efedrin HCl dilakukan pada panjang gelombang 200-400 nm. Panjang gelombang maksimum untuk teofilin dalam suasana asam (A11 = 536a) terletak pada 270 nm, sedangkan
untuk efedrin HCl dalam suasana asam (A11 = 12a) terletak pada 263 nm, 257 nm,
dan 251 nm (Moffat, dkk., 2011).
Berdasarkan teori dengan hasil yang diperoleh, perbedaan panjang gelombang maksimum masing-masing teofilin dan efedrin HCl tidak kurang dan tidak lebih dari 2 nm. Dalam hal ini, panjang gelombang maksimum masing-masing komponen telah memenuhi syarat (Moffat, dkk., 2005). Spektrum serapan maksimum teofilin dan efedrin HCl dapat dilihat pada Gambar 4.4.
Gambar 4.4 Spektrum Serapan Maksimum Teofilin (a) dan Efedrin HCl (b) (Moffat, dkk., 2011)
nm .
200.00 250.00 300.00 350.00 400.00
Ab
s.
2.500
2.000
1.500
1.000
0.500
4.2 Hasil Penentuan Panjang Gelombang Analisis
[image:69.595.117.505.147.358.2]Tumpang tindih spektrum serapan maksimum teofilin (8,1 µg/ml) dan efedrin HCl (360,4 µg/ml) pada skala yang diatur dapat dilihat pada Gambar 4.5.
Gambar 4.5 Tumpang Tindih Spektrum Serapan Maksimum Teofilin (8,1 µg/ml) dan Efedrin HCl (360,4 µg/ml) pada Skala yang Diatur
Dari Gambar 4.5 dapat dilihat bahwa hasil tumpang tindih spektrum serapan dibuat dengan menggabungkan kedua serapan dari teofilin (konsentrasi 8,1 µg/ml) dan efedrin HCl (konsentrasi 360,4 µg/ml). Pembacaan spektrum serapan ini dilakukan pada panjang gelombang 215-300 nm, karena pada panjang gelombang ini teofilin dan efedrin HCl tumpang tindih secara keseluruhan.
Metode spektrofotometri secara multikomponen dalam menetapkan kadar campuran teofilin dan efedrin HCl, hanya dapat menggunakan dua panjang gelombang maksimum dari masing-masing komponen, yakni 270,40 nm dari teofilin dan 256,80 nm dari efedrin HCl. Sedangkan dua panjang gelombang lain dari efedrin HCl yakni 262,80 nm dan 251,20 nm tidak dapat digunakan karena metode spektrofotometri secara multikomponen hanya menggunakan dua panjang gelombang maksimum dalam perhitungan matriks.
nm .
200.00 250.00 300.00 320.00
Ab
s.
0.500
0.400
0.300
0.200
0.100
Berbeda dengan metode spektrofotometri secara panjang gelombang berganda, metode ini dapat menetapkan kadar campuran yang terdapat lebih dari dua panjang gelombang dari masing-masing komponen dengan syarat panjang gelombang yang diambil merupakan panjang gelombang maksimum (Rohman, 2007). Syarat lainnya bahwa masing-masing komponen masih memiliki serapan pada panjang gelombang yang ditentukan (Andrianto, 2009).
[image:70.595.116.507.413.617.2]Pada penelitian ini, dipilih empat titik panjang gelombang dalam penetapan kadar teofilin dan efedrin HCl dalam tablet. Pemilihan empat panjang gelombang ini berdasarkan jumlah panjang gelombang maksimum antara teofilin dan efedrin HCl, yakni 270,40 nm dari teofilin; 262,80 nm; 256,80 nm; dan 251,20 nm dari efedrin HCl. Empat titik panjang gelombang analisis yang akan digunakan dalam penetapan kadar dalam tablet dapat dilihat pada Gambar 4.6.
Gambar 4.6 Empat Titik Panjang Gelombang yang akan Digunakan dalam Penetapan Kadar Teofilin dan Efedrin HCl dalam Tablet
Berdasarkan Gambar 4.6, dapat diketahui apakah empat panjang gelombang yang ditentukan memenuhi syarat lainnya bahwa masing-masing komponen masih memiliki serapan pada panjang gelombang yang ditentukan. Pada panjang gelombang 270,40 nm, efedrin HCl masih memberikan serapan dan
nm .
200.00 250.00 300.00 320.00
Ab
s.
0.500
0.400
0.300
0.200
0.100
0.000
270,40 nm 262,80 nm
256,80 nm
merupakan serapan maksimum dari teofilin. Pada panjang gelombang 251,20 nm; 256,80 nm; dan 262,80 nm; teofilin sudah memberikan serapan dan ketiga panjang gelombang tersebut merupakan serapan maksimum dari efedrin HCl. Jadi, keempat panjang gelombang tersebut dapat digunakan untuk menetapkan kadar teofilin dan efedrin HCl dalam tablet.
4.3 Hasil Perbandingan Spektrum Serapan Campuran Teofilin dan Efedrin HCl Sebelum Penambahan Baku dengan Sesudah Penambahan Baku
Spektrum campuran teofilin dan efedrin HCl sebelum penambahan baku dengan sesudah penambahan baku dapat dilihat Gambar 4.6 dan Gambar 4.7.
Gambar 4.7 Spektrum Serapan Campuran Teofilin dan Efedrin HCl (Sebelum Metode Adisi Standar)
Gambar 4.8 Spektrum Serapan Campuran Teofilin dan Efedrin HCl (Sesudah Metode Adisi Standar)
nm .
200.00 250.00 300.00 350.00 400.00
Ab
s.
1.000
0.800
0.600
0.400
0.200
[image:71.595.121.517.518.710.2]Dari Gambar 4.7 dan Gambar 4.8 dapat dilihat bahwa adanya perbedaan spektrum sebelum penambahan baku dengan sesudah penambahan baku. Sebelum penambahan baku, spektrum yang terlihat hanya teofilin sedangkan efedrin HCl tidak terlihat dan tidak dapat dilakukan penetapan kadar efedrin HCl karena konsentrasinya di dalam campuran kecil atau hampir tidak ada.
Oleh karena itu, diperlukan metode adisi standar terhadap efedrin HCl agar konsentrasi efedrin HCl dapat meningkat dan absorbansinya turut meningkat. Menurut Harmita (2004), dalam metode adisi (penambahan bahan baku), sejumlah sampel yang dianalisis ditambah analit dengan kadar biasanya 98% sampai 102% dari kadar analit yang diperkirakan, dicampur dan dianalisis kembali. Selisih kedua hasil dibandingkan dengan kadar yang sebenarnya.
4.4 Hasil Perbandingan Spektrum Serapan Campuran Baku Teofilin dan Efedrin HCl dengan Spektrum Tablet A, Tablet G, dan Tablet I
Spektrum serapan campuran teofilin dan efedrin HCl antara campuran baku dengan campuran yang terdapat dalam tablet A, tablet G, dan tablet I dapat dilihat Gambar 4.9, Gambar 4.10, Gambar 4.11 dan Gambar 4.12.
Gambar 4.9 Spektrum Serapan Campuran Baku Teofilin dan Efedrin HCl
nm .
200.00 250.00 300.00 350.00 400.00
Ab
s.
1.000
0.800
0.600
0.400
0.200
[image:72.595.115.508.514.715.2]Gambar 4.10 Spektrum Serapan Teofilin dan Efedrin HCl pada Tablet A
Gambar 4.11 Spektrum Serapan Teofilin dan Efedrin HCl pada Tablet G
Gambar 4.12 Spektrum Serapan Teofilin dan Efedrin HCl pada Tablet I
nm .
200.00 250.00 300.00 350.00 400.00
Ab
s.
0.700
0.600
0.400
0.200
Berdasarkan Gambar 4.9, Gambar 4.10, Gambar 4.11, dan Gambar 4.12 dapat dilihat bahwa spektrum serapan campuran teofilin dan efedrin HCl pada tablet A, tablet G, dan tablet I memberikan spektrum serapan yang serupa dengan campuran baku teofilin dan efedrin HCl.
Perhitungan kadar teoritis dari campuran baku teofilin dan efedrin HCl dapat dilihat pada Lampiran 14 halaman 61 dan spektrum serapan dari larutan baku yang dibuat sebanyak 6 kali dapat dilihat pada Lampiran 30 halaman 88. Contoh perhitungan kadar teoritis dari teofilin dan efedrin HCl dalam tablet A dapat dilihat pada Lampiran 16 halaman 65 dan rekapitulasi kadar teoritis dari teofilin dan efedrin HCl dalam tablet A, tablet G, dan tablet I dapat dilihat pada Lampiran 17 halaman 67. Spektrum serapan dalam tablet A yang dibuat sebanyak 6 kali dapat dilihat pada Lampiran 31 halaman 90. Spektrum serapan dalam tablet G yang dibuat sebanyak 6 kali dapat dilihat pada Lampiran 32 halaman 92. Spektrum serapan dalam tablet I yang dibuat sebanyak 6 kali dapat dilihat pada Lampiran 33 halaman 94.
4.5 Hasil Penentuan Serapan pada Empat Panjang Gelombang
Tabel 4.1 Data Perhitungan Serapan Teofilin C
(µg/ml)
λ1 = 270,40 nm λ2 = 262,80 nm λ3 = 256,80 nm λ4 = 251,20 nm
A A11 A A12 A A13 A A14
0 0
0,0437 0 0,0419 0 0,0314 0 0,0202
4 0,175 0,169 0,124 0,08
6 0,263 0,25 0,188 0,121
8 0,349 0,334 0,255 0,161
10 0,433 0,42 0,315 0,203
12 0,528 0,503 0,374 0,242
a = 0,0437 a = 0,0419 a = 0,0314 a = 0,0202 b = -0,0003 b = 0 b = 0,0001 b = -0,0004 r = 0,99992 r = 0,99998 r = 0,99986 r = 0,99997 Keterangan:
a = Koefisien regresi yang menunjukkan nilai serapan b = Konstanta
r = Koefisien korelasi
Tabel 4.2 Data Perhitungan Serapan Efedrin HCl C
(µg/ml)
λ1 = 270,40 nm λ2 = 262,80 nm λ3 = 256,80 nm λ4 = 251,20 nm
A A11 A A12 A A13 A A14
0 0
0,0001 0 0,0007