AKIBAT PROSES PENGOLAHAN
JATU RUKMI MULYANINGTYAS
DEPARTEMEN TEKNOLOGI HASIL PERAIRAN
FAKULTAS PERIKANAN DAN ILMU KELAUTAN
INSTITUT PERTANIAN BOGOR
BOGOR
Lemak dan Kolesterol pada Daging Remis (Corbicula javanica) Akibat Proses Pengolahan. Dibimbing oleh ELLA SALAMAH dan SRI PURWANINGSIH.
Kerang merupakan salah satu komoditas perairan yang mempunyai kandungan gizi tinggi seperti mineral, vitamin, asam amino dan protein. Salah satu kandungan gizi yang tinggi pada kerang adalah asam lemak tak jenuh jamak yaitu omega-3 yang mempunyai turunan eicosapentaenoic acid (EPA) dan docosahexaenoic acid (DHA). Salah satu jenis kerang yang mengandung kedua asam lemak ini adalah remis (Corbicula javanica). Pada umumnya remis dikonsumsi oleh masyarakat setelah melalui proses pengolahan. Pengolahan dengan panas umumnya memberikan pengaruh terhadap kandungan gizi, oleh sebab itu perlu dilakukan penelitian tentang pengaruh pengolahan terhadap kandungan asam lemak dan kolesterol pada remis.
Tujuan dari penelitian ini adalah untuk menentukan rendemen dan komposisi proksimat (kadar air, abu, lemak dan protein), mengetahui kandungan asam lemak dan kolesterol daging remis segar dan setelah proses pengolahan (pengukusan, perebusan dan perebusan dalam air garam), serta menentukan metode pengolahan yang memberikan penurunan asam lemak paling sedikit.
Tahap awal penelitian ini adalah melakukan identifikasi, pengukuran dan penimbangan bobot serta perhitungan rendemen. Penelitian pendahuluan dilakukan untuk mengetahui waktu pengolahan terbaik dari setiap jenis perlakuan (pengukusan, perebusan dan perebusan dalam air garam) dan menentukan konsentrasi garam terbaik pada perlakuan perebusan dalam air garam. Pada tahap penelitian utama, sampel remis yang telah dilakukan proses pengolahan (pengukusan pada suhu 100 0C selama 12-15 menit, perebusan 100 0C selama 7-10 menit dan perebusan dalam air garam dengan konsentrasi 1,5 % pada suhu 100 0C selama 7-10 menit) kemudian dilakukan analisis proksimat, analisis asam lemak dan analisis kolesterol.
AKIBAT PROSES PENGOLAHAN
JATU RUKMI MULYANIGTYAS
C34070020
Skripsi
Sebagai salah satu syarat untuk memperoleh gelar sarjana Perikanan pada Departemen Teknologi Hasil Perairan
DEPARTEMEN TEKNOLOGI HASIL PERAIRAN
FAKULTAS PERIKANAN DAN ILMU KELAUTAN
INSTITUT PERTANIAN BOGOR
BOGOR
Nama : Jatu Rukmi Mulyaningtyas NRP : C34070020
Departemen : Teknologi Hasil Perairan
Menyetujui: Pembimbing 1
Dra. Ella Salamah, M.Si NIP. 19530629 198803 2 001
Pembimbing 2
Dr. Ir. Sri Purwaningsih, M.Si NIP. 19650713 199002 2 001
Mengetahui:
Ketua Departemen Teknologi Hasil Perairan
Dr. Ir. Ruddy Suwandi, MS., MPhil. NIP: 19580511 198503 1 002
Dengan ini saya menyatakan bahwa skripsi dengan judul “Perubahan
Kandungan Asam Lemak dan Kolestrol pada Daging Remis
(Corbicula javanica) Akibat Proses Pengolahan “ adalah benar karya saya sendiri dengan arahan dari komisi pembimbing dan belum diajukan dalam bentuk apapun kepada perguruan tinggi manapun. Sumber informasi yang berasal atau dikutip dari karya yang diterbitkan penulis lain telah disebutkan dalam teks dan dicantumkan dalam daftar pustaka di bagian akhir skripsi ini.
Bogor, Agustus 2011
Puji syukur penulis panjatkan kepada Tuhan Yang Maha Esa karena berkat rahmat dan karunia-Nya, penulis dapat menyelesaikan skripsi yang berjudul
“Perubahan Kandungan Asam Lemak dan Kolesterol pada Daging Remis (Corbicula javanica) Akibat Proses Pengolahan”. Penulisan skripsi ini
dilaksanakan sebagai salah satu syarat untuk menyelesaikan pendidikan di Departemen Teknologi Hasil Perairan, Fakultas Perikanan dan Ilmu Kelautan,
Institut Pertanian Bogor.
Penulis ingin mengucapkan terima kasih kepada semua pihak yang telah memberikan bantuan dan dorongan selama penelitian ini, diantaranya:
1 Dra. Ella Salamah, M.Si dan Dr. Sri Purwaningsih, M.Si selaku dosen pembimbing atas segala saran arahan, perbaikan dan motivasi serta semua ilmu yang telah diberikan.
2 Dr. Ir. Ruddy Suwandi, MS., MPhil selaku Ketua Departemen Teknologi Hasil Perairan, Fakultas Perikanan dan Ilmu Kelautan, Institut Pertanian Bogor dan sebagai dosen penguji atas arahan dan perbaikan yang telah diberikan.
3 Dr. Ir. Agoes Mardiono Jacoeb, Dipl. Biol selaku Ketua Program Studi Departemen Teknologi Hasil Perairan.
4 Ayahanda dan Ibunda tercinta atas segala doa dan apapun yang telah diberikan kepada penulis yang tak terhitung banyaknya.
5 Teman-teman THP 44, 45, dan 46 yang selalu memberikan bantuan tenaga, fikiran, motivasi dan doa untuk membatu penulis dari penelitian hingga penyelesaian skripsi imi.
Penulis menyadari bahwa di dalam skripsi ini masih terdapat banyak kekurangan, oleh sebab itu kritik dan saran yang bersifat membangun dari semua pihak sangat diharapkan.
Bogor , Agustus 2011
Penulis merupakan anak pertama dari dua bersaudara yang dilahirkan di Malang pada tanggal 28 Januari 1989 dari ayah Abdulloh Zaini dan ibu Suryani Kushariyanti.
Jenjang pendidikan penulis dimulai tahun 1995-2001 di SDN Lesanpuro 6, penulis melanjutkan ke jenjang SMP yaitu tahun 2001-2004 di SMPN 5 Malang dan melanjutkan ke SMAN 1 Malang pada tahun 2004-2007 dan pada tahun 2007 masuk IPB melalui jalur Undangan Seleksi Masuk IPB. Penulis memilih Departemen Teknologi Hasil Perairan, Fakultas Perikanan dan Ilmu Kelautan.
Penulis pernah mengikuti beberapa organisasi diantaranya sebagai pengurus Himpunan Mahasiswa Hasil Perikanan sebagai anggota Divisi Kewirausahaan pada tahun 2008/2009 dan sebagai anggota Divisi Sosial Kemasyarakatan tahun 2009/2010. Penulis juga pernah menjadi asisten
praktikum mata kuliah Teknologi Pengolahan Tradisional Hasil Perairan pada tahun 2010/2011.
Sebagai salah satu syarat memperoleh gelar Sarjana Perikanan pada Fakultas Perikanan dan Ilmu Kelautan, penulis melakukan penelitian dengan judul Perubahan Kandungan Asam Lemak dan Kolesterol pada Daging Remis
DAFTAR GAMBAR ... viii
DAFTAR TABEL ... ix
DAFTAR LAMPIRAN ... x
1 PENDAHULUAN ... 1
1.1 Latar belakang ... 1
1.2 Tujuan ... 2
2 TINJAUAN PUSTAKA ... 3
2.1 Deskripsi dan Klasifikasi Remis (Corbicula javanica) ... 3
2.2 Komposisi Kimia Remis (Corbicula javanica) ... 4
2.3 Lemak ... 5
2.4 Asam Lemak ... 6
2.4.1 Autooksidasi lemak ... 7
2.4.2 Fungsi asam lemak ... 8
2.5 Kolesterol ... 9
2.6 Pengaruh Pengolahan terhadap Nilai Gizi ... 11
2.7 Kromatografi Gas ... 12
3 METODOLOGI ... 15
3.1 Waktu dan Tempat Penelitian ... 15
3.2 Bahan dan Alat ... 15
3.3 Metode Penelitian ... 15
3.3.1 Pengambilan dan preparasi sampel... 16
3.3.2 Metode Pengolahan ... 17
3.3.3 Analisis proksimat ... 17
3.3.4 Analisis asam lemak ... 20
3.3.5 Analisis kolesterol ... 22
3.3.6 Rancangan percobaan dan analisis data ... 23
4 HASIL DAN PEMBAHASAN ... 26
4.1 Ukuran dan Bobot Remis (Corbicula javanica) ... 26
4.2 Rendemen Remis (Corbicula javanica) ... 27
4.3 Penetapan Waktu Pengolahan dan Konsentrasi Garam ... 28
4.4 Komposisi Proksimat Remis ... 29
vii
5.1 Kesimpulan ... 49
5.2 Saran ... 49
DAFTAR PUSTAKA ... 50
Nomor Halaman
1 Remis (Corbicula javanica) ... 3
2 Struktur kimia lemak berdasarkan jumlah asam lemak ... 6
3 Skema autooksidasi pada asam lemak tak jenuh... 7
4 Struktur EPA dan DHA ... 8
5 Struktur kimia kolesterol ... 9
6 Alat kromatografi gas ... 13
7 Diagram alir metode penelitian ... 16
8 Kromatografi gas dan rekorder ... 21
9 Rendemen remis segar ... 27
10 Histogram nilai rata-rata parameter rasa remis ... 29
11 Histogram kadar air remis ... 31
12 Histogram kadar abu remis ... 32
13 Histogram kadar protein remis ... 34
14 Hisogram kadar lemak remis ... 35
15 Histogram kandungan asam palmitat ... 38
16 Histogram kandungan asam oleat ... 39
17 Histogram kandungan asam linoleat ... 41
18 Histogram kandungan asam linolenat ... 42
19 Histogram kandungan asam arakidonat ... 43
20 Histogram kandungan EPA (Eicosapentaenoic acid) ... 44
21 Histogram kandungan DHA (Docosahexaenoic acid) ... 45
Nomor Halaman
1 Kandungan gizi kerang-kerangan ... 5
2 Ukuran dan bobot remis (Corbicula javanica) ... 26
3 Hasil analisis proksimat remis (Corbicula javanica) ... 30
Nomor Halaman
1 Data panjang, lebar, tinggi dan berat remis... 56
2 Lembar penilaian (score sheet) uji hedonik parameter rasa ... 57
3 Hasil uji hedonik parameter rasa remis ... 58
4 Hasil uji Kruskal Wallis parameter rasa remis ... 58
5 Hasil uji Multiple Comparison parameter rasa remis ... 59
6 Analisis kadar air remis ... 59
7 Analisis kadar abu remis ... 59
8 Analisis kadar protein remis... 60
9 Analisis kadar lemak remis ... 60
10 Grafik uji kenormalan galat proksimat ... 61
11 Analisis ragam kadar air remis ... 63
12 Uji Duncan kadar air ... 63
13 Analisis ragam kadar abu remis ... 63
14 Uji Duncan kadar abu... 63
15 Analisis ragam kadar protein remis... 64
16 Uji Duncan kadar protein ... 64
17 Analisis ragam kadar lemak remis ... 64
18 Uji Duncan kadar lemak... 64
19 Contoh perhitungan asam lemak ... 65
20 Kromatogram standar asam lemak ke-1 ... 66
21 Kromatogram standar asam lemak ke-2 ... 66
22 Kromatogram asam lemak remis segar ... 67
23 Kromatogram asam lemak remis kukus ... 67
24 Kromatogram asam lemak remis rebus ... 68
25 Kromatogram asam lemak remis rebus dalam air garam ... 68
26 Grafik uji kenormalan galat asam lemak ... 69
27 Analisis ragam kandungan asam palmitat ... 72
28 Uji Duncan kandungan asam palmitat ... 72
32 Uji Duncan kandungan asam linoleat ... 73
33 Analisis ragam kandungan asam linolenat ... 73
34 Uji Duncan kandungan asam linolenat ... 73
35 Analisis ragam kandungan asam arakidonat ... 73
36 Uji Duncan kandungan asam arakidonat... 73
37 Analisis ragam kandungan EPA (Eicosapentaenoic acid)... 74
38 Uji Duncan kandungan EPA (Eicosapentaenoic acid) ... 74
39 Analisis ragam kandungan DHA (Docosapentaenoic acid) ... 74
40 Uji Duncan kandungan DHA (Docosapentaenoic acid) ... 74
41 Kurva standar pengujian kolesterol ... 75
42 Hasil uji kolesterol remis ... 75
43 Grafik uji kenormalan galat kolesterol ... 76
44 Analisis ragam kolesterol ... 76
1.1 Latar Belakang
Indonesia sebagai negara kepulauan memiliki keanekaragaman sumberdaya perairan yang sangat melimpah. Wilayah perairan yang sangat luas mampu menyediakan berbagai jenis ikan, karang, rumput laut dan kerang-kerangan. Salah satu sumberdaya yang belum dimanfaatkan secara optimal adalah kerang-kerangan.
Kerang memiliki kandungan gizi yang tinggi, yaitu protein, asam amino, asam lemak, vitamin dan mineral. Salah satu kandungan gizi yang terdapat pada kerang-kerangan adalah asam lemak. Asam lemak merupakan asam organik berantai panjang yang mempunyai gugus karboksil (COOH) di salah satu ujungnya dan gugus metil (CH3) di ujung lainnya (Almatsier 2006). Asam lemak dibedakan menjadi asam lemak jenuh dan tidak jenuh. Asam lemak tidak jenuh contohnya adalah linoleat (omega-6) dan linolenat (omega-3) yang mempunyai peranan penting dalam perkembangan otak. Asam linolenat memiliki turunan Eicosapentaenoic Acid (EPA) dan Docosahexaenoic Acid (DHA) yang dibutuhkan oleh tubuh manusia karena memiliki beberapa manfaat untuk mencerdaskan otak, membantu masa pertumbuhan dan menurunkan kadar trigliserida. Asam lemak tak jenuh (EPA dan DHA) pada berbagai jenis kerang tergolong tinggi. Menurut Imre dan Sahgk (1997) kerang jenis Mytilus galloprovincialis mengandung EPA 0,124 mg/100 g dan DHA 0,169 mg/100 g.
Adanya pengaruh yang terjadi pada proses pengolahan terhadap penurunan komponen gizi, sehingga perlu dilakukan penelitian mengenai pengaruh metode pengolahan (pengukusan, perebusan dan perebusan dalam air garam) terhadap penurunan kandungan asam lemak dan kolesterol pada remis.
1.2 Tujuan
Tujuan dilakukannya penelitian ini adalah :
1) Menentukan rendemen dan komposisi proksimat (air, protein, abu dan lemak) daging remis segar dan setelah proses pengolahan.
2) Menganalisis pengaruh pengolahan (pengukusan, perebusan dan perebusan dalam air garam) pada kandungan asam lemak dan kolesterol remis
2.1 Deskripsi dan Klasifikasi Remis (Corbicula javanica)
Remis (Corbicula javanica) adalah kerang yang hidup di dasar perairan. Remis mempunyai cangkang yang kuat dan simetris, bentuk cangkang agak bundar atau memanjang. Permukaan periostrakum agak licin, bagian dalam bewarna putih dan bagian luar bewarna abu-abu kecoklatan dan hidup dengan membenamkan diri dalam substrat. Lebar cangkang dapat mencapai 3-4 cm. Remis (Corbicula javanica) termasuk mollusca yang hidup di air tawar (sungai, danau dan sawah) yang airnya mengalir. Bila air tidak mengalir remis akan mati (Darmawanti 2004). Contoh remis dapat dilihat pada Gambar 1. Klasifikasi remis menurut Jutting (1953) adalah sebagai berikut:
Filum : Mollusca Kelas : Pelecypoda Sub kelas : Lamiliabranchia Ordo : Veneroida
Sub ordo : Eulamellibranchia Famili : Corbiculidae Genus : Corbicula
Spesies : Corbicula javanica
Gambar 1 Remis (Corbicula javanica) (Darmawanti 2004)
besar karena selain berfungsi sebagai alat pernafasan juga berfungsi sebagai pengumpul makanan. Massa visceral pada tubuh kerang merupakan kumpulan organ-organ bagian dalam, seperti insang, perut, gonad, anus dan organ penting lainnya (Suwignyo et al.2005).
Kerang melakukan reproduksinya dengan cara menghasilkan sel telur untuk kerang betina dan kerang jantan menghasilkan spermanya yang kemudian akan terbawa aliran air menuju kerang betina. Fertilisasi terjadi di dalam cangkang kerang betina. Hasil pembuahan yang berbentuk larva disebut glochidium. Perkembangan embrio di dalam insang berlangsung beberapa hari sampai beberapa minggu (Shan 1999). Glochidia yang lepas memiliki keping cangkang dan sehelai benang yang menempel pada ikan-ikan sebagai parasit yang akan mengambil makanan dengan cara mengabsorbsi cairan tubuh inang. Glochidia memiliki ukuran sekitar 60 sampai 400 mikron. Lamanya hidup sebagai parasit tergantung dari spesies kerang dan mutu air sekitarnya (Neves 2002).
Mekanisme makan remis, yaitu dengan cara memompakan air ke dalam tubuhnya dengan gerakan cilia dan menyaring partikel mikroskopis. Partikel-partikel ini dilewatkan melalui insang dan akhirnya memasuki perut. Proses ini menyebabkan terkumpulnya plankton, bakteri, senyawa kimia dan partikel-partikel kecil lainnya di dalam saluran pencernaan kerang (Broom 1985).
2.2 Komposisi Kimia Remis (Corbicula javanica)
Kerang merupakan makanan sumber protein hewani dengan kategori complete protein, karena mengandung asam amino esensial yang lengkap sehingga mudah diserap tubuh. Kerang juga merupakan makanan sumber vitamin larut lemak dan air serta sumber utama mineral yang dibutuhkan tubuh seperti
iodium, besi, seng, selenium, kalsium, fosfor, kalium dan fluor (Suwignyo et al. 2005).
kelamin, umur, musim, dan habitat. Kandungan gizi kerang secara umum dapat dilihat pada Tabel 1.
Tabel 1 Kandungan gizi kerang-kerangan
Komponen Jumlah
Abu (%) 1,3 - 2,0
Air (%) 78
Lemak (%) 0,4 – 2,4
Protein (%) 7,1 – 16,7
Karbohidrat (%) 2,3 – 4,9
2Kalsium (mg) 133 Fosfor (mg) 170 Sumber : Dore (1991)
2.3 Lemak
Lemak merupakan senyawa organik yang tidak larut dalam air tetapi dapat diekstraksi dengan pelarut non polar. Senyawa organik ini terdapat dalam semua sel dan berfungsi sebagai sumber energi, komponen struktur sel, sebagai simpanan bahan bakar metabolik, sebagai komponen pelindung dinding sel, dan juga sebagai komponen pelindung kulit vertebrata (Girindra 1987). Ditinjau dari sudut nutrisi, lemak merupakan sumber kalori penting disamping berperan sebagai pelarut berbagai vitamin (Ketaren 1986).
Gambar 2 Struktur kimia lemak berdasarkan jumlah asam lemak (Ketaren 1986)
Lemak berfungsi sebagai penghasil asam lemak esensial (essensial fatty acid = EFA). Asam lemak esensial merupakan asam lemak yang
tidak dapat dibentuk tubuh dan harus tersedia dari luar (berasal dari makanan). Jenis asam lemak esensial yang memegang peranan penting bagi tubuh adalah oleat, linoleat dan linolenat. Ketiganya mengandung ikatan rangkap (dua atau lebih) termasuk ke dalam kelompok asam lemak tak jenuh jamak (polyunsaturated fatty acid = PUFA) (Suharjo dan Kusharto 1987).
2.4 Asam Lemak
Asam lemak merupakan senyawa pembangun berbagai lipid, termasuk lipid sederhana, fosfogliserida, glikolipid, stingolipid, ester kolesterol, lilin dan lain-lain, dan telah diisolasi lebih dari 70 macam asam lemak dari berbagai sel dan jaringan berupa rantai hidrokarbon dengan ujungnya berupa gugus hidroksil. Asam lemak memiliki gugus karboksil tunggal dan ujung hidrokarbon nonpolar yang panjang, yang menyebabkan hampir semua lipid bersifat tidak larut dalam air dan tampak berminyak atau berlemak (Lehninger 1990).
lemak tidak jenuh tunggal (monounsaturated fatty acid /MUFA). Asam lemak yang mengandung dua atau lebih ikatan rangkap disebut asam lemak tak jenuh jamak (polyunsaturated fatty acid/PUFA) (Ackman 1994).
Keberadaan letak ikatan rangkap dalam struktur kimiawi asam lemak mengakibatkan adanya perbedaan konfigurasi, bila ikatan rangkapnya terletak pada sisi yang sama dengan gugus hidrogen maka disebut sebagai konfigurasi cis, sedangkan bila ikatan rangkapnya terletak di sisi yang berlawanan maka disebut sebagai konfigurasi trans. Asam lemak konfigurasi trans dapat memberikan resiko terjadinya penyakit jantung koroner. Asam lemak tak jenuh jamak yang ideal adalah asam lemak yang berkonfigurasi cis, biasanya yang berasal dari alam, seperti asam lemak omega-3 cis yang berasal dari ikan (Hidajat 2003).
2.4.1 Autooksidasi asam lemak
Lemak pada daging remis akan mengalami beberapa perubahan setelah remis mati. Kerusakan lemak di dalam bahan pangan dapat terjadi selama proses pengolahan. Ketengikan adalah indikator dari kerusakan lemak dan minyak. Ketengikan dihasilkan oleh autooksidasi asam lemak tidak jenuh yang menimbulkan bau dan flavor yang tidak menyenangkan dan membuat makanan menjadi tidak enak. Skema autooksidasi asam lemak tidak jenuh dapat dilihat pada Gambar 3.
Oksigen yang dihasilkan mengandung radikal bebas lalu bereaksi dengan molekul asam lemak dan membentuk hidroperoksida serta asam lemak radikal yang lain, kemudian siklus ini terjadi berulang kali (Connel 1979). Hidroperoksida yang terbentuk sangat tidak stabil dan mudah pecah menjadi senyawa rantai karbon yang lebih pendek berupa beberapa asam lemak, aldehid dan keton yang mudah menguap (volatile) dan potensial bersifat toksik (Almatsier 2006).
2.4.2 Fungsi asam lemak
Asam lemak memiliki fungsi yang penting bagi tubuh, asam lemak esensial digunakan untuk menjaga bagian-bagian struktural dari membran sel dan untuk membuat bahan-bahan seperti hormon (hormonlike) yang disebut eikosanoid. Eikosanoid membantu mengatur tekanan darah, proses pembekuan darah, lemak dalam darah dan respon imun terhadap luka dan infeksi (Thoha 2004).
Asam lemak Omega-3 merupakan asam lemak esensial yang memiliki ikatan rangkap pada atom C urutan ke-3 jika dihitung dari gugus C(metil). Asam lemak yang merupakan kelompok Omega-3, contohnya α-linolenic acid/ALA, docosahexaenoic acid /DHA dan eicosapentaenoic acid/EPA. Struktur kimia dari EPA dan DHA dapat dilihat pada Gambar 4.
Gambar 4 Struktur EPA dan DHA (Tan 2008)
Asam linolenat merupakan asam lemak esensial, karena dibutuhkan tubuh namun tubuh tidak dapat mensintesisnya. Turunan dari asam linolenat adalah EPA dan DHA. Ikan dapat mengubah asam linolenat menjadi EPA dan DHA, sejalan dengan hal tersebut perubahan asam linolenat menjadi EPA dan DHA terjadi pada manusia namun tidak efisien (Almatsier 2006).
pertumbuhan, karena tidak dapat disintesa dari asam lemak lain. Omega-3 mempunyai fungsi khususnya dalam jaringan syaraf, retina mata, mempengaruhi otot jantung dan memproduksi substansi yang mengontrol respon imun. Fungsi asam lemak esensial yang terdapat dalam tubuh sebagai fosfolipid menurut Muchtadi et al.(1993) adalah sebagai berikut:
1) memelihara integritas dan fungsi membran seluler dan subseluler 2) mengatur metabolisme kolesterol
3) merupakan prekursor dari senyawa yang memiliki fungsi pengatur fisiologis dalam tubuh
4) dibutuhkan untuk aksi piridoksin (Vitamin B6) dan asam pantotenat; dan 5) dibutuhkan untuk pertumbuhan dan perkembangan bayi.
2.5 Kolesterol
Kolesterol adalah sterol yang paling dikenal oleh masyarakat. Kolesterol di dalam tubuh mempunyai fungsi ganda, yaitu di satu sisi diperlukan dan di sisi lain dapat membahayakan bergantung berapa banyak terdapat di dalam tubuh dan di bagian mana. Kolesterol merupakan komponen membran struktural sel dan komponen sel otak maupun syaraf. Dalam hati kolesterol disintesis dan disimpan. Kadar tinggi terdapat pada hati dan jaringan kelenjar. Pembentukan asam empedu, asam folat, dan progesteron memerlukan kolesterol. Kolesterol dalam tubuh dapat diperoleh dari sintesis dalam hati dengan bahan utama karbohidrat, protein, lemak. Banyak sedikitnya sintesis tergantung jumlah kebutuhan dan jumlah kolesterol dari makanan (Achadi 2007). Struktur kimia kolesterol disajikan pada Gambar 5.
Kolesterol dapat membahayakan tubuh apabila terdapat dalam jumlah terlalu banyak di dalam darah yang dapat membentuk endapan pada dinding pembuluh darah sehingga menyebabkan penyempitan yang dinamakan arterosklerosis. Bila penyempitan terjadi pada pembuluh darah jantung dapat menyebabkan penyakit jantung koroner dan bila pada pembuluh darah otak penyakit serebrovaskuler. Menurut Colpo (2005) ada dua jenis lipoprotein yang membawa kolesterol dalam darah, yaitu:
1) Kolesterol Low Density Lipoprotein (LDL)
Jenis kolesterol ini berbahaya sehingga sering disebut juga sebagai kolesterol jahat. Kolesterol LDL menyebabkan pengendapan kolesterol dalam arteri.
Kolesterol LDL merupakan faktor risiko utama penyakit jantung koroner sekaligus target utama dalam pengobatan.
2) Kolesterol High Density Lipoprotein (HDL)
Kolesterol ini tidak berbahaya. Kolesterol HDL sering disebut kolesterol baik karena dapat membuang kelebihan kolesterol jahat di pembuluh darah arteri kembali ke hati, untuk diproses dan dibuang. HDL mencegah kolesterol mengendap di arteri dan melindungi pembuluh darah dari proses arterosklerosis.
Komoditas kerang memiliki kandungan kolesterol yang rendah dibandingkan dengan udang, yaitu sebesar 20,2 mg/100 gram sedangkan pada udang sebesar 109,3 mg/100 gram. Kadar kolesterol yang rendah komoditas ini dapat dijadikan sebagai bahan pangan untuk diet yang dapat mencegah penyakit jantung koroner (Imre & Saghk 1997).
Kolesterol mempunyai peranan penting untuk mengatur fungsi tubuh. Kolesterol juga penting sebagai bahan dasar untuk biosintesis asam empedu (vital untuk pencernaan dan penyerapan lemak), biosintesis hormon laki-laki dan
perempuan (progesteron dan esterogen) serta hormon steroid yang lain (Okuzumi dan Fujii 2000). Kolesterol menjalankan 3 fungsi utama menurut
Freeman dan Junge (2005) yaitu:
1) Kolesterol membentuk selubung luar sel
3) Kolesterol memungkinkan tubuh membentuk vitamin D dan hormon-hormon penting dalam tubuh.
2.6 Pengaruh Pengolahan terhadap Nilai Gizi
Pemanasan merupakan suatu perlakuan suhu tinggi yang diberikan pada suatu bahan pangan yang bertujuan untuk mengurangi populasi mikroorganisme atau membunuhnya yang ada di dalam bahan pangan. Perlakuan-perlakuan pemanasan biasanya dikombinasikan dengan perlakuan lainnya untuk mencegah rekontaminasi oleh mikroorganisme (Tamrin dan Prayitno 2008).
Pada umumnya setelah proses pengolahan bahan pangan, akan terjadi kerusakan lemak yang terkandung di dalamnya. Tingkat kerusakannya sangat bervariasi tergantung suhu yang digunakan serta lamanya waktu proses pengolahan. Makin tinggi suhu yang digunakan, maka kerusakan lemak akan semakin intens. Asam lemak esensial terisomerisasi ketika dipanaskan dalam larutan alkali dan sensitif terhadap sinar, suhu dan oksigen. Proses oksidasi lemak dapat menyebabkan inaktivasi fungsi biologisnya dan bahkan dapat bersifat toksik. Suatu penelitian telah membuktikan bahwa produk volatil hasil oksidasi asam lemak babi bersifat toksik terhadap tikus percobaan.
Pengukusan merupakan proses pemanasan yang sering diterapkan pada sistem jaringan sebelum pembekuan, pengeringan atau pengalengan. Pengukusan sebelum pengeringan terutama bertujuan untuk menginaktifkan enzim yang akan menyebabkan perubahan warna, cita rasa atau nilai gizi yang tidak dikehendaki selama penyimpanan. Tujuan dilakukannya pengukusan adalah untuk mengurangi kadar air dalam bahan baku, sehingga tekstur bahan menjadi kompak. Dalam pengukusan diterapkan suhu tinggi dan penambahan air sehingga menyebabkan gelatinisasi (Sartika 2009).
Perebusan adalah cara memasak makanan dalam cairan yang sedang
mendidih (100 ˚C) (Widyati 2001). Perebusan dipakai dalam pengolahan makanan, sayuran atau bahan bertepung. Temperatur yang tinggi akan mengeraskan (membuat liat) protein daging, ikan, dan telur. Air yang mendidih dengan cepat akan mengurai kehalusan makanan (delicated food) (Widyati 2001). Bahan pangan yang dimasak dengan menggunakan air akan meningkatkan daya kelarutan. Pemanasan dapat mengurangi daya tarik-menarik antara molekul-molekul air dan akan memberikan cukup energi pada molekul-molekul-molekul-molekul air tersebut sehingga dapat mengatasi daya tarik-menarik antar molekul dalam bahan pangan tersebut, karena itu daya kelarutan pada bahan yang melibatkan ikatan hidrogen, akan meningkat dengan meningkatnya suhu (Winarno 2008).
2.7 Kromatografi Gas
Analisis asam lemak dalam suatu bahan pangan dapat diuji dengan Gas Chromatography (GC). Kromatografi gas adalah teknik yang digunakan untuk memisahkan campuran berdasarkan sifat volatilitas masing-masing komponennya. Pemisahan ini terjadi karena adanya interaksi antara komponen sampel dengan fasa gerak dan fase diam pada kromatografi gas. Komponen volatil tersebut akan dibawa oleh fasa gerak (carier) yang berupa gas yang bersifat inert seperti gas helium dan nitrogen. Fasa diam pada kromatografi gas berfungsi untuk mempartisikan komponen yang dipisahkan berdasarkan interaksinya dengan fasa diam. Fasa diam pada kromatografi gas dapat berupa padatan, yang disebut dengan kromatografi gas padat (Gas Solid Chromatography/ GSC) atau padatan yang dilapis dengan cairan yang disebut (Gas Liquid Chropmatography/GLC) (Herawati et al.,2011).
Senyawa yang tidak stabil secara termal ataupun tidak mudah menguap, dapat juga dianalisis dengan kromatografi gas dengan cara mengubahnya menjadi turunan-turunannya yang lebih mudah menguap dan stabil, misalnya: asam lemak, dapat diubah menjadi ester metilik atau metil ester melalui esterifikasi dengan BF3 dalam pelarut metanol. Alkohol, sterol dan senyawa hidroksi dapat diasetilasi, misalkan dengan asam asetat anhidrida dan piridin (Khopkar 1983). Alat kromatografi gas dapat dilihat pada Gambar 6.
Gambar 6 Alat kromatografi gas
Menurut Mcnair dan Bonelli (1988) kromatografi gas dalam analisis pangan memilki berbagai keuntungan, antara lain:
1) Kecepatan
Seluruh analisis dapat diselesaikan dalam waktu 23 menit. Penggunaan gas sebagai fasa gerak mempunyai keuntungan, yaitu cepat tercapainya kesetimbangan antara fasa gerak dan fasa diam, dan dapat digunakan kecepatan gas pembawa yang tinggi.
2) Resolusi (daya pisah)
didih yang hampir sama. Hal ini dikarenakan kromatografi gas menggunakan fase cair yang selektif.
3) Analisis kualitatif
Waktu retensi atau waktu tambat adalah waktu sejak penyuntikan sampai maksimum puncak. Waktu tambat tersebut dapat dipersingkat dengan menggunakan aliran yang tepat dan mengendalikan suhu.
4) Kepekaan
Kromatografi gas memiliki kepekaan yang tinggi. Keuntungan tambahan dari kepekaan yang tinggi ini adalah sampel yang diperlukan hanya sedikit untuk menganalisis secara lengkap.
5) Kesederhanaan
Kromatografi gas mudah dijalankan dan mudah dipahami. Penafsiran data yang diperoleh biasanya cepat dan langsung serta mudah. Penerapan kromatografi gas pada bidang industri antara lain meliputi: obat-obatan dan farmasi, lingkungan hidup, industri minyak, kimia klinik, pestisida dan residunya serta pangan. Di bidang pangan, kromatografi gas digunakan untuk menetapkan kadar antioksidan dan bahan pengawet makanan serta untuk menganalisis sari buah, keju, aroma makanan, minyak, produk susu dan lain-lain.
3.1 Waktu dan Tempat Penelitian
Penelitian ini dilaksanakan pada bulan Februari sampai April 2011 bertempat di Laboratorium Karakteristik dan Penanganan Hasil Perairan (preparasi sampel); Laboratorium Formulasi dan Diversifikasi Hasil Perairan
(proses perlakuan pengolahan) dan Laboratorium Biokimia Hasil Perairan (analisis proksimat), Departemen Teknologi Hasil Perairan, Fakultas Perikanan
dan Ilmu Kelautan, Intitut Pertanian Bogor. Laboratorium Terpadu Baranang Siang (Analisis asam lemak), Laboratorium Terpadu Fakultas Peternakan (Analisis kolesterol).
3.2 Bahan dan Alat
Bahan baku yang digunakan dalam penelitian ini adalah remis (Corbicula javanica) yang diperoleh dari perairan situ Gede. Bahan-bahan yang digunakan dalam penelitian ini antara lain: akuades, HCl, NaOH, katalis selenium, H2SO4, H3BO3, pelarut heksana, larutan standar, larutan NaOH 0,5 N dalam metanol, larutan BF3 16 %, larutan NaCl jenuh, isooktan, Na2SO4 anhidrat, etanol, petroleum benzena, alkohol, acetic anhidrid, H2SO4 dan kloroform.
Alat-alat yang digunakan pada penelitian ini antara lain meja preparasi, pisau, timbangan kue dan timbangan analitik, cawan porselen, oven, desikator, tanur, tabung reaksi, gelas erlenmeyer, tabung soxhlet, tabung Kjeldahl, destilator, buret, kromatografi gas Shimadzu GC 2010, penangas air, tabung bertutup teflon, neraca analitik, pipet mikro, tabung sentrifuge, sentrifuge 4000 rpm, vortex dan spektrofotometer dengan panjang gelombang 420 nm.
3.3 Metode Penelitian
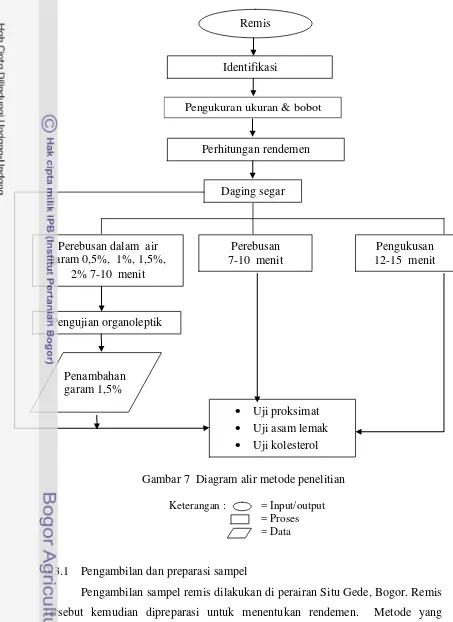
Gambar 7 Diagram alir metode penelitian
Keterangan : = Input/output
= Proses = Data
3.3.1 Pengambilan dan preparasi sampel
Pengambilan sampel remis dilakukan di perairan Situ Gede, Bogor. Remis tersebut kemudian dipreparasi untuk menentukan rendemen. Metode yang digunakan untuk perhitungan rendemen ini berdasarkan persentase bobot bagian
Remis
Perhitungan rendemen Identifikasi
Perebusan dalam air garam 0,5%, 1%, 1,5%,
2% 7-10 menit
Pengujian organoleptik
Pengukuran ukuran & bobot
Uji proksimat
Uji asam lemak
Uji kolesterol Penambahan
garam 1,5%
Perebusan 7-10 menit
tubuh remis dari bobot remis awal. Perumusan matematika rendemen adalah sebagai berikut:
Rendemen % =Bobot contoh (g)
Bobot total (g) � 100%
3.3.2 Metode Pengolahan
Penelitian ini menggunakan 3 metode pengolahan yaitu pengukusan, perebusan dan perebusan dalam air garam. Penelitian pendahuluan sebelumnya telah dilakukan untuk menentukan lamanya waktu perebusan dan pengukusan yang paling baik. Remis yang dikukus akan matang pada suhu 100 0C selama 12-15 menit, sedangkan yang direbus akan matang pada suhu 100 0C selama 7-10 menit. Pada perlakuan perebusan dalam air garam dilakukan uji organoleptik untuk mengetahui konsentrasi garam terbaik. Konsentrasi garam yang akan diuji hedonik (uji kesukaan) parameter rasa yaitu 0,5 %, 1%, 1,5 % dan 2 % (b/v).
Tahapan uji hedonik (SNI 2346-2011) yaitu sampel disajikan dengan memberikan kode nomor secara acak dan panelis sebanyak 30 orang akan memberikan penilaian tingkat kesukaan terhadap rasa dari remis. Uji skala hedonik dilakukan berdasarkan tingkat kesukaan panelis dalam 9 skala kesukaan (1= amat sangat suka, 2=sangat tidak suka, 3=tidak suka, 4=agak tidak suka, 5=netral, 6=agak suka, 7=suka, 8=sangat suka, 9=amat sangat suka) (Lampiran 2). 3.3.3 Analisis proksimat
Analisis proksimat merupakan suatu analisis yang dilakukan untuk mengetahui komposisi kimia yang ada pada suatu bahan. Analisis proksimat terhadap remis meliputi : analisis kadar air, abu, protein, dan lemak.
1) Analisis kadar air (AOAC 2005)
sampel tersebut dimasukkan ke dalam oven suhu 102 0C-105 0C selama 5-6 jam. Cawan tersebut dimasukkan ke dalam desikator dan dibiarkan sampai dingin (30 menit) kemudian ditimbang.
Perhitungan kadar air pada daging remis:
% Kadar air = B−C
B−A � 100%
Keterangan : A = Berat cawan kosong (gram)
B = Berat cawan yang diisi dengan sampel (gram)
C = Berat cawan dengan sampel yang sudah dikeringkan (gram) 2) Analisis kadar abu (AOAC 2005)
Prinsip dari analisis kadar abu yaitu untuk mengetahui jumlah abu yang terdapat pada suatu bahan terkait dengan mineral dari bahan yang dianalisis. Cawan abu porselen dibersihkan dan dikeringkan di dalam oven bersuhu sekitar 105 0C selama 30 menit. Cawan abu porselen tersebut dimasukkan ke dalam cawan abu porselen. Selanjutnya dibakar di atas kompor listrik sampai tidak berasap dan dimasukkan ke dalam tanur pengabuan dengan suhu 600 0C selama 7 jam. Cawan dimasukkan di dalam desikator sampai dingin dan kemudian ditimbang.
Perhitungan kadar abu pada daging remis:
% Kadar abu = C−A
B−A � 100%
Keterangan : A = Berat cawan kosong (gram)
B = Berat cawan dengan daging remis (gram)
C = Berat cawan dengan daging remis setelah dikeringkan (gram) 3) Analisis kadar protein (AOAC 1995)
Prinsip dari analisis protein, yaitu untuk mengetahui kandungan protein kasar (crude protein ) pada suatu bahan. Tahap-tahap yang dilakukan dalam analisis protein terdiri dari tiga tahap, yaitu destruksi, destilasi, dan titrasi.
1) Tahap destruksi
ditambahkan 10 ml H2SO4. Tabung yang berisi larutan tersebut dimasukkan ke dalam alat pemanas dengan suhu 400 0C. Proses destruksi dilakukan sampai larutan menjadi bening.
2) Tahap destilasi
Hasil destruksi diencerkan dengan akuades hingga 100 ml dengan labu takar. Air dipanaskan sampai mendidih di heater rangkaian alat destilator. Asam borat sebanyak 25 ml dimasukkan ke dalam erlenmeyer. Erlenmeyer tersebut kemudian dipasang pada tempatnya (di tempat pengeluaran sampel NaOH). Hasil destruksi (larutan sampel) dipipet sebanyak 10 ml juga dimasukkan ke dalam desikator. Setelah itu, larutan NaOH 50 % sebanyak 10 ml juga dimasukkan ke dalam destilator. Setelah larutan di dalam erlenmeyer yang berisi asam borat berubah warna menjadi biru kehitaman atau hijau toska, erlenmeyer diangkat dan dilakukan proses titrasi.
3) Tahap Titrasi
Titrasi dilakukan dengan menggunakan HCl 0,0947 N sampai terjadi perubahan warna menjadi warna (warna asam borat semula). Kadar protein dihitung dengan rumus sebagai berikut:
% Nitrogen = ml HCl sampel−ml HCl blanko x N HCl x 14
mg daging remis x 100%
% Kadar protein = % Nitrogen x faktor konversi(6,25) 4) Analisis kadar lemak (AOAC 2005)
105 0C, setelah itu labu didinginkan dalam desikator sampai beratnya konstan (W3).
Perhitungan kadar lemak pada daging remis:
% Kadar Lemak = W3−W2
W1 � 100%
Keterangan : W1 = Berat sampel remis (gram)
W2 = Berat labu lemak tanpa lemak (gram) W3 = Berat labu lemak dengan lemak (gram) 3.3.4 Analisis asam lemak (AOAC 1999)
Metode analisis yang digunakan memiliki prinsip mengubah asam lemak menjadi turunannya, yaitu metil ester sehingga dapat terdeteksi oleh alat kromatografi. Gas chromatography (GC) memiliki prinsip kerja pemisahan antara gas dan lapisan tipis cairan berdasarkan perbedaan jenis bahan (Fardiaz 1989). Jenis alat kromatografi gas yang digunakan dalam penelitian ini adalah Shimadzu GC 2010. Hasil analisis akan terekam dalam suatu lembaran yang terhubung dengan rekorder dan ditunjukkan melalui beberapa puncak pada waktu retensi tertentu sesuai dengan karakter masing-masing asam lemak. Sebelum melakukan injeksi metil ester, terlebih dahulu lemak diekstraksi dari bahan lalu dilakukan metilasi sehingga terbentuk metil ester dari masing-masing asam lemak yang didapat.
a) Ekstraksi asam lemak
Tahap pertama dilakukan ekstraksi soxhlet untuk memperoleh asam lemak,dan ditimbang sebanyak 20-30 mg lemak dalam bentuk minyak.
b) Pembentukan metil ester (metilasi)
berisi 0,1 gram Na2SO4 anhidrat dan dibiarkan 15 menit. Larutan disaring dengan mikrofilter untuk memisahkan fase cairnya sebelum diinjeksikan ke dalam kromatografi gas. Sebanyak 1 μl sampel diijeksikan ke dalam Gas Chromatography. Asam lemak yang ada dalam metil ester akan diidentifikasi oleh flame ionization detector (FID) atau detector ionisasi nyala dan respon yang ada akan tercatat melalui kromatogram (peak).
c) Identifikasi dengan kromatografi gas
Identifikasi asam lemak dilakukan dengan menginjeksikan metil ester pada alat kromatografi gas dengan kondisi sebagai berikut: jenis alat kromatografi gas yang digunakan adalah Shimadzu GC 2010, gas yang digunakan sebagai fase bergerak adalah gas nitrogen dengan aliran bertekanan 20 ml/menit dan sebagai gas pembakar adalah hidrogen dengan aliran bertekanan 30 ml/menit dan oksigen dengan aliran 200-300 ml/menit, kolom yang digunakan adalah kolom kapiler (capillary column) yang panjangnya 60 cm dan diameter dalam 0,25 mm dengan tebal lapisan film 0,25 µm. Temperatur terpogram yang digunakan adalah suhu 125 0C yang dipertahankan 515 menit, kemudian suhu dinaikkan hingga suhu akhir 225 0C yang dipertahankan 20 menit, suhu injektor 220 0C dan suhu detektor 230 0C. Alat kromatografi gas yang digunakan dalam analisis dapat dilihat pada Gambar 8.
(a) (b)
Kondisi alat GC pada saat analisis sebagai berikut :
a) Jenis Kolom : Cyanopropil methyl sil (capillary column) b) Panjang kolom : 60 cm
c) Diameter dalam : 0,25 mm d) Tebal lapisan film : 0,25 µm e) Laju alir N2 : 20 ml/menit f) Laju alir H2 : 30 ml/menit g) Laju alir udara : 200-250 ml/menit h) Suhu injektor : 220 0C
i) Suhu detektor : 230 0C j) Suhu terpogram : 125 - 225 0C d) Perhitungan jumlah asam lemak
Prinsip analisis komposisi asam lemak dengan kromatografi gas adalah dengan mengubah komponen asam lemak pada lemak/minyak menjadi senyawa volatil metil ester lemak yang akan dideteksi oleh detektor ionisasi nyala api dalam bentuk respon berupa peak kromatogram. Jenis dan jumlah asam lemak yang ada pada contoh dapat diidentifikasi dengan membandingkan peak kromatogram contoh dengan peak kromatogram asam lemak standar yang telah diketahui jenis dan konsentrasinya, kemudian dihitung kadar asam lemaknya. Pada pengujian asam lemak digunakan metode eksternal standar dimana contoh dan standar dilakukan secara terpisah, tidak ada penambahan larutan standar ke dalam contoh. Kadar asam lemak sampel dengan metode eksternal standar dapat dihitung sebagai berikut:
3.3.5 Analisis kolesterol dengan spektrofotometer
sampai homogen. Pengaduk dibilas dengan 2 ml larutan alkohol : petroleum benzena ( 3:1) kemudian disentrifuge 4000 rpm selama 10 menit.
Supernatan dituang ke dalam beaker glass 100 ml dan diuapkan di penangas air. Residu dilarutkan dengan kloroform sedikit demi sedikit sambil dituangkan ke dalam tabung berskala (sampai volume 5 ml) dan ditambahkan 2 ml acetic anhidrid ditambahkan juga 0,2 ml H2SO4 pekat atau 2 tetes. Selanjutnya dihomogenkan dengan vortex dan dibiarkan di tempat gelap selama 15 menit. Lalu dibaca absorbansinya menggunakan spektrofotemeter pada panjang gelombang 420 nm yang ditunjukkan dengan warna hijau tua.
Kadar kolesterol dalam sampel dihitung dengan rumus :
Kadar Kolesterol = Absorbansi contoh Absorbansi standar x
Konsentrasi standar bobot contoh
3.3.6 Rancangan percobaan dan analisis data 1) Analisis data uji hedonik
Konsentrasi garam untuk proses perebusan dalam air garam ditentukan dengan menggunakan uji hedonik. Data hasil uji hedonik dianalisis menggunakan Kruskal Wallis distribusi uji Chi Square. Apabila nilai x2 hitung > x2 tabel maka tolak Ho (perbedaan konsentrasi garam tidak memberikan pengaruh nyata terhadap parameter rasa remis). Prosedur pengujian Kruskal Wallis menggunakan rumus sebagai berikut (Steel dan Torrie 1993):
(1) H = 12
Keterangan ni = banyaknya pengamatan tiap perlakuan atau jumlah panelis N = banyaknya data
Ri = jumlah rata-rata tiap perlakuan ke-i
T = banyaknya pengamatan yang seri dalam tiap ulangan H’ = H terkoreksi
Apabila hasil uji Chi Square menunjukkan di antara perlakuan tersebut memberikan pengaruh nyata terhadap rasa remis maka pengujian dilanjutkan
dengan uji Multiple Comparison dengan rumus sebagai berikut
R’i = rata-rata rangking perlakuan ke-i R’j = rata-rata rangking perlakuan ke-j N = banyaknya data
K = banyaknya perlakuan ni = jumlah data perlakuan ke-i nj = jumlah dat perlakuan ke-j
2) Rancangan percobaan kandungan proksimat, asam lemak dan kolesterol Rancangan percobaan yang digunakan untuk menguji pengaruh metode pengolahan terhadap komposisi proksimat, kandungan asam lemak dan kolesterol adalah rancangan acak lengkap (RAL) dengan satu faktor dan 4 taraf (sampel segar, pengukusan, perebusan dan perebusan dalam air garam). Data dianalisis dengan ANOVA (Analysis Of Variant) menggunakan uji F, sebelum dilakukan uji F terlebih dahulu di uji kenormalan data.
Uji kenormalan data menggunakan uji Kolmogrov Simirnov (Steel dan Torrie 1993). Kurva normal yang dihasilkan pada uji Kolmogrov Simirnov disertakan dengan nilai rata dan standar deviasi (simpangan baku). Nilai rata-rata menggambarkan posisi kurva sumbu X, sedangkan standar deviasi menggambarkan sebaran varian. Koefisien keragaman dengan nilai dibawah 50 % (median) dinyatakan cukup baik karena dapat membuktikan pada tingkat 95 %.
Suatu data dapat menyebar normal pada : x ‒ z α/2√��
<
�
<
x + z α/2√σn (Walpole 1992) Koefisien keragaman = σ
Keterangan: x = rata-rata z = 1,96
µ = (1-α) 100 %
� = simpangan baku n = banyak data
Model rancangan analisis ANOVA (Analysis Of Variant) atau uji F adalah sebagai berikut (Steel dan Torrie 1993):
Yij = μ + τi + εij Keterangan :
Yij = Nilai pengamatan pada taraf ke-i dan ulangan ke-j (j=1,2) μ = Nilai tengah atau rataan umum pengamatan
τi = Pengaruh metode pengolahan pada taraf ke-i (i=1,2,3) εij = Galat atau sisa pengamatan taraf ke-i dengan ulangan ke-j
Hipotesa terhadap data hasil uji komposisi proksimat pada berbagai metode pengolahan adalah sebagai berikut:
H0 = Metode pengolahan tidak memberikan pengaruh terhadap komposisi proksimat. H1 = Metode pengolahan memberikan pengaruh terhadap komposisi proksimat.
Hipotesa terhadap data hasil analisis asam lemak pada berbagai metode pengolahan adalah sebagai berikut:
H0 = Metode pengolahan tidak memberikan pengaruh terhadap asam lemak. H1 = Metode pengolahan memberikan pengaruh terhadap asam lemak.
Hipotesa terhadap data hasil analisis kolesterol pada berbagai metode pengolahan adalah sebagai berikut:
H0 = Metode pengolahan tidak memberikan pengaruh terhadap kolesterol. H1 = Metode pengolahan memberikan pengaruh terhadap kolesterol.
Jika uji F pada ANOVA memberikan pengaruh yang berbeda terhadap komposisi kimia, asam lemak dan kolesterol maka dilanjutkan dengan uji Duncan, dengan rumus sebagai berikut:
Duncan = tα/2; dbs 2� � Keterangan :
4.1 Ukuran dan Bobot Remis (Corbicula javanica)
Remis yang digunakan dalam penelitian ini diperoleh dari Situ Gede, Bogor. Remis memiliki cangkang yang kuat dan simetris dimana bentuk cangkang agak bundar atau memanjang. Permukaan periostrakum agak licin, bagian dalam bewarna putih dan bagian luar bewarna abu-abu kecoklatan. Pengukuran terhadap ukuran dan penimbangan bobot remis diperoleh dari 30 sampel yang diambil secara acak (Lampiran 1). Hasil pengukuran terhadap ukuran dan bobot remis dapat dilihat pada Tabel 2.
Tabel 2 Ukuran dan bobot remis (Corbicula javanica)
No Parameter Satuan Nilai
1 Panjang cm 2,07 ± 0,36
2 Lebar cm 1,67 ± 0,28
3 Tebal cm 0,99 ± 0,29
4 Berat gram 2,70 ± 0,34
Keterangan : Menggunakan sampel 30 ekor remis
Tabel 2 menunjukkan bahwa rata-rata panjang remis (Corbicula javanica) adalah 2,07 cm, rata-rata lebar sebesar 1,67 cm, rata-rata tebal sebesar 0,99 cm dan rata-rata berat adalah sebesar 2,70 gram. Menurut Metusalach (2007), pertumbuhan suatu biota dipengaruhi faktor eksternal dan internal. Faktor eksternal yaitu habitat, musim, suhu perairan, jenis makanan yang tersedia dan faktor lingkunan lainnya, sedangkan faktor internalnya yaitu umur, ukuran, jenis kelamin, kebiasaan makan dan faktor biologis lainnya.
4.2 Rendemen Remis (Corbicula javanica)
Rendemen merupakan suatu parameter yang paling penting untuk mengetahui nilai ekonomis dan efektifitas suatu produk atau bahan. Hasil penelitian menunjukkan bahwa rendemen tertinggi pada remis terdapat pada cangkang remis yaitu sebesar 60,74 %, sedangkan rendemen jeroan remis sebesar 21,61 % dan rendemen daging remis sebesar 17,65 %. Diagram pie pengukuran rendemen remis dapat dilihat pada Gambar 9.
Gambar 9 Rendemen remis segar
Remis memiliki nilai rendemen tertinggi yaitu pada cangkang. Hal ini disebabkan sebagian besar tubuh kerang-kerangan adalah berupa cangkang yang membungkus organ dalam dari kerang itu sendiri.
Remis adalah hewan yang bersifat filter feeder, sifat inilah yang menyebabkan nilai rendemen jeroan lebih besar daripada rendemen daging. Partikel makanan maupun partikel lain dapat mengendap di dalam tubuh remis, terutama di saluran pencernaan dan bagian jeroan ketika remis mengambil makanannya (Turgeon 1988).
Hasil penelitian menunjukkan bahwa rendemen remis yang telah diberikan beberapa perlakuan pengolahan yaitu pengukusan, perebusan, dan perebusan dalam air garam mengalami penyusutan rendemen. Rendemen remis setelah proses pengukusan adalah sebesar 62,20 %, setelah proses perebusan sebesar
Cangkang Jeroan Daging 21,61 %
17,65 %
53,60 % sedangkan rendemen setelah proses perebusan dalam air garam adalah sebesar 66,05 %.
Metode pengolahan baik pengukusan, perebusan dan perebusan garam bertujuan untuk mempertahankan mutu remis yang diinginkan, perbaikan cita rasa dan tekstur, nilai gizi dan daya cerna. Pada waktu proses pengolahan berlangsung, terjadi pengurangan kadar air pada daging remis. Bersamaan dengan keluarnya air dari remis, komponen zat gizi lain juga berkurang yaitu protein, lemak, vitamin dan mineral. Hal inilah yang menyebabkan terjadinya penurunan nilai rendemen setelah dilakukan pengolahan.
Penyusutan rendemen setelah dilakukan beberapa proses pengolahan ini disebabkan pengolahan dengan panas menyebabkan kandungan air yang terdapat pada cangkang, daging dan jeroan menguap sehingga terjadi pengurangan berat,
selain itu daging mengalami pengerutan karena panas (Thamrin dan Prayitno 2008). Faktor-faktor yang menyebabkan suatu bahan
kehilangan berat selama proses pengolahan berlangsung adalah lama pengolahan, suhu yang digunakan, luas permukaan bahan yang diolah, jenis bahan dan tingkat kerusakan pada bahan sebelum bahan tersebut diolah (Connel 1979).
4.3 Penetapan waktu pemasakan dan konsentrasi garam
Metode pengolahan yang digunakan dalam penelitian ini adalah pengukusan, perebusan dan perebusan dalam air garam. Penentuan lamanya proses pengukusan dan perebusan harus ditentukan terlebih dahulu untuk memperoleh waktu pengolahan terbaik hingga remis matang. Remis (Corbicula javanica) yang direbus akan matang pada suhu 100 0C selama 7-10 menit, sedangkan untuk proses pengukusan remis akan matang pada suhu 70 – 100 0C selama 12-15 menit.
proses perebusan dengan berbagai konsentrasi garam dapat dilihat pada Gambar 10.
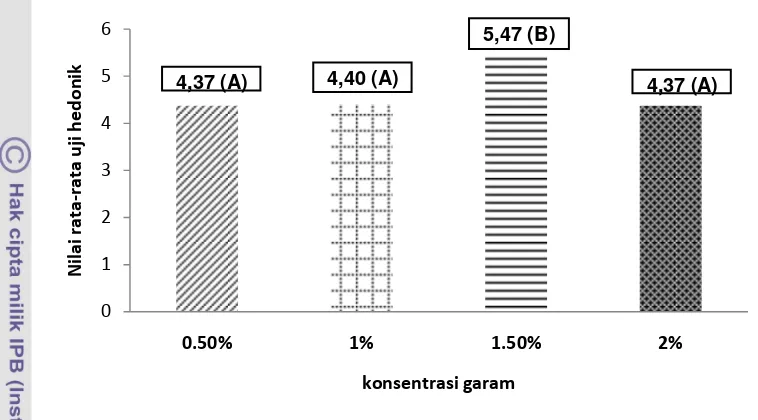
Gambar 10 Histogram nilai rata-rata parameter rasa remis; angka-angka yang diikuti huruf yang berbeda menunjukkan beda nyata (p<0,05).
Berdasarkan Gambar 10 nilai uji hedonik terhadap rasa remis menunjukkan bahwa nilai rata-rata tertinggi yaitu 5,47 yang dicapai oleh konsentrasi garam 1,5 %. Hasil uji Kruskal Wallis (Lampiran 4) pada tingkat kepercayaan 95 % menunjukkan bahwa konsentrasi garam yang berbeda memberikan pengaruh terhadap rasa remis. Hasil uji Multiple Comparison (Lampiran 5) diketahui bahwa konsentrasi garam 1,5 % memberikan pengaruh yang berbeda terhadap konsentrasi garam 0,5 %, konsentrasi garam 1 % dan konsentrasi garam 2 %. Berdasarkan hasil yang diperoleh, maka diketahui bahwa konsentrasi garam 1,5 % adalah formulasi yang terbaik untuk perlakuan perebusan garam.
4.4 Komposisi Proksimat Remis
Analisis mengenai komposisi kimia suatu bahan pangan sangat penting dilakukan untuk memperoleh informasi mengenai kandungan gizi yang terdapat di dalam bahan pangan tersebut. Komposisi kimia yang terdapat dalam remis dipengaruhi oleh beberapa faktor, diantaranya musim, ukuran, tahap kedewasaan, suhu lingkungan dan ketersediaan bahan makanan (Sudhakar et al. 2009).
Kandungan gizi dalam suatu produk adalah parameter yang penting bagi konsumen dalam mempertimbangkan pemilihan makanan yang akan dikonsumsinya. Salah satu cara untuk mengetahui kandungan gizi secara kasar adalah dengan analisis proksimat yang meliputi kadar air, abu, protein, lemak dan karbohidrat by difference. Hasil analisis proksimat remis disajikan pada Tabel 3.
Tabel 3 Hasil analisis proksimat remis (Corbicula javanica) Komposisi kimia
rata-Remis Rebus Remis Rebus garam Kadar air (bb) 85,38a 80,90b 81,05b 78,17b Kadar abu (bk) 5,83b 4,14a 4,16a 8,69c Kadar protein (bk) 67,34c 39,51b 42,27b 31,31a Kadar lemak (bk) 4,99c 3,09b 2,83b 1,98a Keterangan: angka-angka yang diikuti huruf yang beda pada baris yang sama menunjukkan beda nyata (p<0,05).
Tabel 3 menunjukkan komposisi kimia remis segar dan setelah diberikan perlakuan pengolahan. Data didapatkan melalui uji kenormalan galat dengan menggunakan metode Kolmogrov simirnov. Berdasarkan uji Kolmogrov simirnov (Lampiran 10), semua perlakuan menghasilkan galat yang menyebar normal sehingga dapat dilakukan analisis ragam dan jika F hitung > F tabel maka dilanjutkan dengan uji Duncan. Uji Duncan bertujuan untuk mengetahui pengaruh beberapa metode pengolahan terhadap komposisi proksimat remis. (a) Kadar air
Air merupakan bahan yang sangat penting bagi kehidupan manusia dan fungsinya tidak pernah dapat digantikan oleh senyawa lain. Air juga merupakan komponen penting dalam bahan makanan karena air dapat mempengaruhi penampakan, tekstur, serta cita rasa makanan (Winarno 2008). Kadar air remis segar dari hasil penelitian ini adalah sebesar 85,38 % (bb), nilai ini lebih tinggi dibandingkan dengan penelitian Prasastyane (2009), yang menyatakan bahwa kadar air kijing sebesar 81,54%.
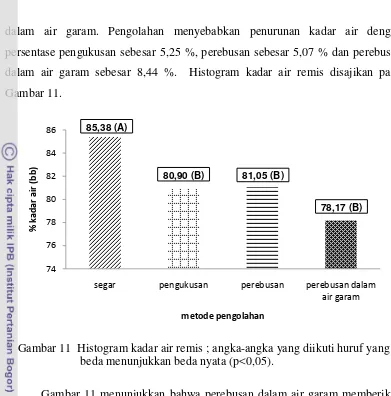
dalam air garam. Pengolahan menyebabkan penurunan kadar air dengan persentase pengukusan sebesar 5,25 %, perebusan sebesar 5,07 % dan perebusan dalam air garam sebesar 8,44 %. Histogram kadar air remis disajikan pada Gambar 11.
Gambar 11 Histogram kadar air remis ; angka-angka yang diikuti huruf yang beda menunjukkan beda nyata (p<0,05).
Gambar 11 menunjukkan bahwa perebusan dalam air garam memberikan penurunan yang paling besar terhadap kadar air, hal ini sesuai dengan penelitian Sukarsa et al. (1996) tentang pengaruh konsentrasi gula dan garam terhadap mutu jambal roti yang menyatakan bahwa garam mempunyai sifat sebagai penarik air dari jaringan sehingga perebusan dalam air garam dapat menurunkan kadar air suatu bahan.
Pemanasan adalah metode pengolahan yang menyebabkan kehilangan air cukup tinggi pada daging. Penurunan kadar air setelah remis mengalami pengolahan terkait dengan sifat air yang mudah menguap apabila dipanaskan, hal ini didukung oleh penelitian Jacoeb et al. (2008) tentang perubahan komposisi kimia dan vitamin daging udang ronggeng (Harpiosquilla raphidea) akibat perebusan yang menyatakan bahwa pengolahan dengan panas pada suhu 100 0C mengakibatkan protein akan terkoagulasi dan air dari dalam daging akan keluar, hal inilah yang menyebabkam kadar air setelah pengolahan mengalami penurunan.
segar pengukusan perebusan perebusan dalam
(b) Kadar abu
Abu merupakan residu anorganik dari proses pembakaran atau oksidasi komponen organik bahan pangan. Kadar abu dari suatu bahan pangan menunjukkan total mineral yang terkandung dalam bahan pangan tersebut. Kadar abu total adalah bagian dari analisis proksimat yang digunakan untuk (Anadara granosa) yaitu sebesar 2,24 % (bb).
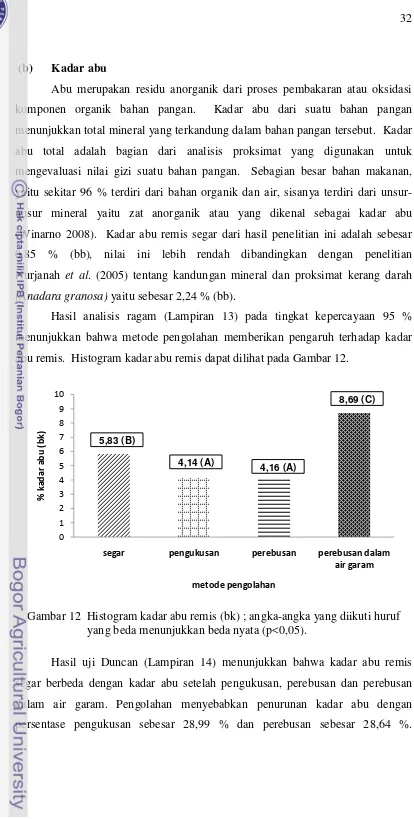
Hasil analisis ragam (Lampiran 13) pada tingkat kepercayaan 95 % menunjukkan bahwa metode pengolahan memberikan pengaruh terhadap kadar abu remis. Histogram kadar abu remis dapat dilihat pada Gambar 12.
Gambar 12 Histogram kadar abu remis (bk) ; angka-angka yang diikuti huruf yang beda menunjukkan beda nyata (p<0,05).
Hasil uji Duncan (Lampiran 14) menunjukkan bahwa kadar abu remis segar berbeda dengan kadar abu setelah pengukusan, perebusan dan perebusan dalam air garam. Pengolahan menyebabkan penurunan kadar abu dengan persentase pengukusan sebesar 28,99 % dan perebusan sebesar 28,64 %.
segar pengukusan perebusan perebusan dalam
Pengolahan dengan panas mengakibatkan kehilangan beberapa zat gizi terutama zat-zat yang labil seperti mineral. Mineral bersifat mantap dan tidak rusak karena pengolahan, namun pengolahan dapat menyebabkan penyusutan mineral pada bahan pangan tidak lebih dari 3 %. (Harris dan Karmas 1989).
Perlakuan perebusan dalam air garam mengalami peningkatan nilai kadar abu, hal ini disebabkan garam mengandung mineral seperti Mg, Na, Ca dan Fe sehingga terjadi akumulasi mineral dalam bahan yang menyebabkan kadar abunya mengalami peningkatan. Akumulasi mineral ini disebabkan terjadinya peristiwa osmosis karena adanya garam. Hal ini didukung oleh penelitian Desniar et al. (2009) tentang pengaruh konsentrasi garam terhadap mutu peda ikan kembung (Rastrelliger kanagurta) yang menyatakan bahwa semakin tinggi konsentrasi garam yang digunakan maka kadar abunya semakin mengalami peningkatan.
Manusia memerlukan berbagai jenis mineral untuk metabolisme terutama sebagai kofaktor dalam aktifitas-aktifitas enzim. Keseimbangan ion-ion mineral di dalam cairan tubuh diperlukan untuk pengaturan pekerjaan enzim, pemeliharaan keseimbangan asam-basa, membantu transfer ikatan-ikatan penting melalui membran sel dan pemeliharaan kepekaan otot dan saraf terhadap rangsangan (Almatsier 2006).
(c) Kadar protein
Protein merupakan suatu zat makanan yang amat penting bagi tubuh, karena zat ini disamping berfungsi sebagai bahan bakar dalam tubuh juga berfungsi sebagai zat pembangun dan pengatur. Protein adalah sumber asam-asam amino yang mengandung unsur-unsur C, H, O, dan N yang tidak dimiliki oleh lemak atau karbohidrat (Winarno 2008). Kandungan protein remis segar yang diperoleh dari hasil penelitian ini adalah sebesar 9,85 % (bb). Nilai ini lebih tinggi dibandingkan dengan penelitian Soekandarsi et al. (2009) pada kerang jenis semele sp yaitu sebesar 7,82 %.
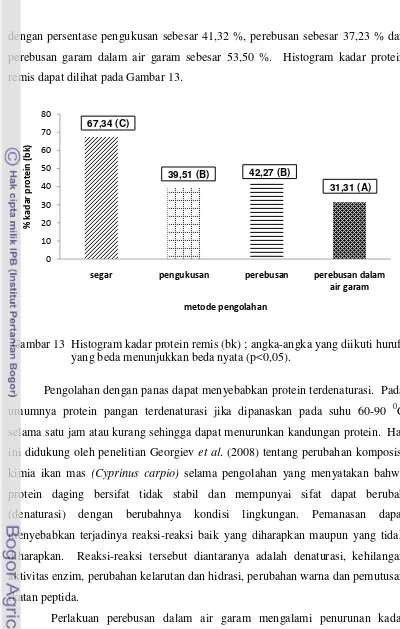
dengan persentase pengukusan sebesar 41,32 %, perebusan sebesar 37,23 % dan perebusan garam dalam air garam sebesar 53,50 %. Histogram kadar protein remis dapat dilihat pada Gambar 13.
Gambar 13 Histogram kadar protein remis (bk) ; angka-angka yang diikuti huruf yang beda menunjukkan beda nyata (p<0,05).
Pengolahan dengan panas dapat menyebabkan protein terdenaturasi. Pada umumnya protein pangan terdenaturasi jika dipanaskan pada suhu 60-90 0C selama satu jam atau kurang sehingga dapat menurunkan kandungan protein. Hal ini didukung oleh penelitian Georgiev et al. (2008) tentang perubahan komposisi kimia ikan mas (Cyprinus carpio) selama pengolahan yang menyatakan bahwa protein daging bersifat tidak stabil dan mempunyai sifat dapat berubah (denaturasi) dengan berubahnya kondisi lingkungan. Pemanasan dapat menyebabkan terjadinya reaksi-reaksi baik yang diharapkan maupun yang tidak diharapkan. Reaksi-reaksi tersebut diantaranya adalah denaturasi, kehilangan aktivitas enzim, perubahan kelarutan dan hidrasi, perubahan warna dan pemutusan ikatan peptida.
Perlakuan perebusan dalam air garam mengalami penurunan kadar protein yang lebih besar dibandingkan perlakuan yang lainnya. Hal ini disebabkan protein-protein dapat larut pada garam sehingga kadar proteinnya menurun. Hal ini didukung oleh penelitian Desniar et al. (2009) yang menyatakan bahwa
segar pengukusan perebusan perebusan dalam
penurunan kadar protein terjadi karena garam mempunyai sifat higroskopis dan mengabsorpsi air dari jaringan daging. Garam merupakan elektrolit kuat yang dapat melarutkan protein, sehingga mampu memecah ikatan molekul air dalam air dan dapat mengubah sifat alami protein.
(d) Kadar lemak
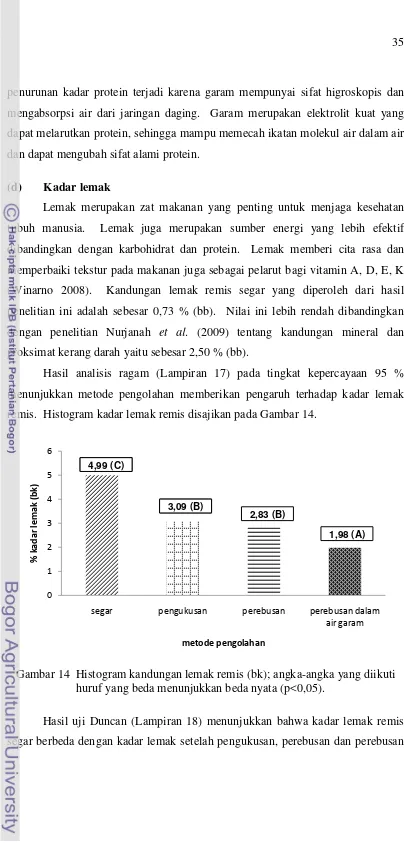
Lemak merupakan zat makanan yang penting untuk menjaga kesehatan tubuh manusia. Lemak juga merupakan sumber energi yang lebih efektif dibandingkan dengan karbohidrat dan protein. Lemak memberi cita rasa dan memperbaiki tekstur pada makanan juga sebagai pelarut bagi vitamin A, D, E, K (Winarno 2008). Kandungan lemak remis segar yang diperoleh dari hasil penelitian ini adalah sebesar 0,73 % (bb). Nilai ini lebih rendah dibandingkan dengan penelitian Nurjanah et al. (2009) tentang kandungan mineral dan proksimat kerang darah yaitu sebesar 2,50 % (bb).
Hasil analisis ragam (Lampiran 17) pada tingkat kepercayaan 95 % menunjukkan metode pengolahan memberikan pengaruh terhadap kadar lemak remis. Histogram kadar lemak remis disajikan pada Gambar 14.
Gambar 14 Histogram kandungan lemak remis (bk); angka-angka yang diikuti huruf yang beda menunjukkan beda nyata (p<0,05).
Hasil uji Duncan (Lampiran 18) menunjukkan bahwa kadar lemak remis segar berbeda dengan kadar lemak setelah pengukusan, perebusan dan perebusan
0
segar pengukusan perebusan perebusan dalam
dalam air garam. Pengolahan menyebabkan penurunan kadar lemak dengan persentase pengukusan sebesar 38,08 %, perebusan sebesar 43,29 % dan perebusan dalam air garam sebesar 60,33 %. Proses pengolahan dengan panas dapat menyebabkan lemak yang terdapat pada remis mencair bahkan menguap
(volatil) menjadi komponen lain. Hal ini didukung oleh penelitian Prabandari et al. (2005) tentang pengaruh waktu perebusan dari dua jenis udang
yang berbeda yang menyatakan bahwa lemak akan mencair menjadi senyawa volatil seperti aldehid, keton, alkohol, asam dan hidrokarbon yang akan menguap saat pemanasan.
Pemanasan akan mempercepat gerakan-gerakan molekul lemak, sehingga jarak antara molekul lemak menjadi besar dan akan mempermudah proses pengeluaran lemak (Winarno 1997). Proses tersebut dipengaruhi oleh suhu pengolahan dan lama pemanasan (Gurr 1992).
4.5 Kandungan Asam Lemak Remis
Asam lemak merupakan komponen rantai panjang yang menyusun lipid. Asam lemak adalah asam organik berantai panjang yang mempunyai atom karbon 4-24, memiliki gugus karboksil tunggal dan ujung hidrokarbon nonpolar yang panjang yang menyebabkan hampir semua lipid bersifat tidak larut dalam air dan tampak berminyak atau berlemak. Analisis asam lemak pada remis menunjukkan bahwa kandungan asam lemak pada remis tersebut tergolong dalam asam lemak jenuh (saturated fatty acid/ SAFA), asam lemak tidak jenuh tunggal (monounsaturated fatty acid/ MUFA), dan asam lemak tak jenuh jamak (polyunsaturated fatty acid/ PUFA).
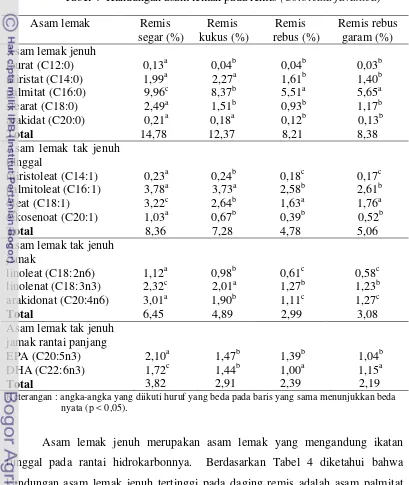
Asam lemak yang terkandung di dalam remis terdiri dari asam lemak jenuh, asam lemak tak jenuh tunggal, asam lemak tak jenuh jamak dan asam lemak tak jenuh jamak rantai panjang. Asam lemak jenuh yang paling tinggi pada remis adalah asam palmitat, asam lemak tak jenuh tunggal yang paling tinggi adalah asam palmitoleat, asam lemak tak jenuh jamak yang paling tinggi adalah asam arakidonat dan asam lemak tak jenuh jamak rantai panjang yang paling tinggi adalah EPA (Eicosapentaenoic acid).
6,45 % dan asam lemak tak jenuh jamak rantai panjang sebesar 3,82 %. Metode pengolahan baik pengukusan, perebusan dan perebusan dalam air garam menyebabkan terjadinya penurunan kandungan asam lemak. Kandungan asam lemak pada remis disajikan pada Tabel 4.
Tabel 4 Kandungan asam lemak pada remis (Corbicula javanica) Asam lemak Remis
Keterangan : angka-angka yang diikuti huruf yang beda pada baris yang sama menunjukkan beda nyata (p < 0,05).
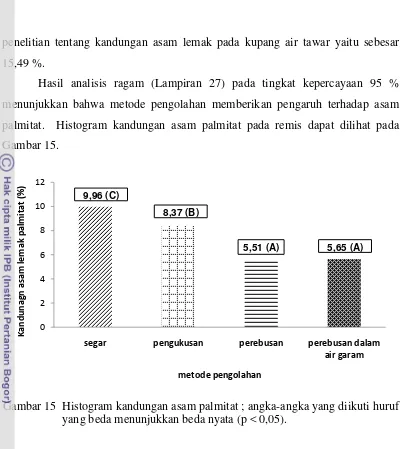
penelitian tentang kandungan asam lemak pada kupang air tawar yaitu sebesar 15,49 %.
Hasil analisis ragam (Lampiran 27) pada tingkat kepercayaan 95 % menunjukkan bahwa metode pengolahan memberikan pengaruh terhadap asam palmitat. Histogram kandungan asam palmitat pada remis dapat dilihat pada Gambar 15.
Gambar 15 Histogram kandungan asam palmitat ; angka-angka yang diikuti huruf yang beda menunjukkan bedanyata (p < 0,05).
Hasil uji Duncan (Lampiran 28) menunjukkan bahwa kandungan asam palmitat remis segar berbeda dengan kandungan asam palmitat remis setelah perebusan, pengukusan dan perebusan garam. Gambar 15 menunjukkan bahwa terjadi penurunan kandungan asam palmitat setelah pengolahan dengan persentase pengukusan sebesar 15,96 %, perebusan sebesar 44,68 % dan perebusan dalam air garam sebesar 43,27 %. Proses pemanasan dapat menyebabkan berubahnya komponen asam lemak menjadi senyawa-senyawa yang volatil seperti aldehid, keton, asam dan hidrokarbon. Senyawa-senyawa ini akan menguap ketika diberikan perlakuan panas sehingga kandungan asam lemaknya mengalami penurunan. Hal ini sesuai dengan penelitian Gumilar et al. (2009) tentang pengaruh pemanasan terhadap asam lemak minyak bekatul yang menyatakan
0
segar pengukusan perebusan perebusan dalam
bahwa terjadi penurunan asam lemak pada minyak bekatul setelah diberikan perlakuan panas pada suhu 100 0C.
Asam palmitat sering ditemukan dalam daging sapi, mentega, keju dan minyak sawit. Menurut French et al. (2002) dalam penelitiannya tentang dampak asam palmitat terhadap kolesterol dalam diet asam lemak menyatakan bahwa asam palmitat dapat meningkatkan kandungan kolesterol apabila tidak melakukan diet yang seimbang dalam mengkonsumsinya.
Asam lemak tak jenuh tunggal yang paling dominan adalah asam palmitoleat dan asam oleat yaitu sebesar 3,78 % dan 3,22 %. Asam oleat adalah asam lemak esensial yang diperlukan oleh tubuh, biasanya asam oleat ini sering dikenal dengan omega-9. Kandungan asam oleat pada remis sedikit lebih rendah dibandingkan dengan penelitian Prasastyane (2009) tentang asam lemak dan kolesterol pada kijing (Pilsbryoconcha exilis) yaitu 3,48 %. Histogram kandungan asam oleat disajikan pada Gambar 16.
Gambar 16 Histogram kandungan asam oleat ; angka-angka yang diikuti huruf yang beda menunjukkan beda nyata (p < 0,05).
Hasil analisis ragam (Lampiran 29) pada tingkat kepercayaan 95 % menunjukkan bahwa metode pengolahan memberikan pengaruh terhadap asam oleat. Berdasarkan Gambar 16 diketahui bahwa hasil uji Duncan (Lampiran 30)
0
segar pengukusan perebusan perebusan dalam
menunjukkan bahwa kandungan asam oleat remis segar berbeda dengan asam oleat setelah pengukusan, perebusan dan perebusan dalam air garam. Pengolahan menyebabkan terjadinya penurunan asam oleat dengan persentase pengukusan sebesar 18,01 %, perebusan sebesar 49,38 % dan perebusan dalam air garam sebesar 45,34 %. Proses pengolahan dapat menyebabkan terjadinya kerusakan lemak yang dapat menurunkan mutu dan nilai gizi suatu bahan pangan. Kerusakan ini menyebabkan bahan pangan berlemak mempunyai bau dan rasa yang tidak enak. Hal ini didukung oleh penelitian Dolezal et al. (2009) tentang perubahan asam lemak akibat oksidasi selama pemanasan dengan microwave pada cincangan daging ikan bahwa kerusakan asam lemak disebabkan adanya proses oksidasi yang menghasilkan asam lemak bebas yang merupakan sumber bau tengik pada produk.
Asam oleat merupakan asam lemak yang dapat ditemukan hampir di seluruh bahan makanan, baik hewan maupun tumbuhan. Asam oleat merupakan asam lemak esensial. Fungsi asam oleat di dalam tubuh adalah sebagai sumber energi, sebagai zat antioksidan untuk menghambat kanker, menurunkan kadar kolesterol dan media pelarut vitamin A, D, E, K. Kekurangan asam oleat dapat menyebabkan terjadinya gangguan pada penglihatan, menurunya daya ingat serta gangguan pertumbuhan sel otak pada janin dan bayi (Peddyawati 2008).
Asam linoleat adalah asam tidak jenuh ikatan majemuk yang esensial untuk tubuh. Kandungan asam linoleat pada remis segar dalam penelitian ini lebih tinggi dibandingkan penelitian Prasastyane (2009) yang melakukan penelitian tentang kandungan asam lemak pada kijing yaitu sebesar 0,32 %.