SEKOLAH PASCASARJANA INSTITUT PERTANIAN BOGOR
BOGOR 2013
SINTESIS NANOPARTIKEL EKSTRAK SIRIH MERAH
(
Piper crocatum
) DAN KAJIAN SISTEM PENGANTARANNYA
PERNYATAAN MENGENAI TESIS DAN
SUMBER INFORMASI SERTA PELIMPAHAN HAK CIPTA*
Dengan ini saya menyatakan bahwa tesis berjudul Sintesis Nanopartikel Ekstrak Sirih Merah (Piper Crocatum) dan Kajian Sistem Pengantarannya adalah benar karya saya dengan arahan dari komisi pembimbing dan belum diajukan dalam bentuk apa pun kepada perguruan tinggi mana pun. Sumber informasi yang berasal atau dikutip dari karya yang diterbitkan maupun tidak diterbitkan dari penulis lain telah disebutkan dalam teks dan dicantumkan dalam Daftar Pustaka di bagian akhir tesis ini.
Dengan ini saya melimpahkan hak cipta dari karya tulis saya kepada Institut Pertanian Bogor.
Bogor, Agustus 2013
Kun Tanti Dewandari
RINGKASAN
KUN TANTI DEWANDARI. Sintesis nanopartikel ekstrak sirih merah (Piper crocatum) dan Kajian Sistem Pengantarannya. Dibimbing oleh SEDARNAWATI YASNI dan SRI YULIANI.
Sirih merah merupakan salah satu tanaman obat yang dapat dimanfaatkan sebagai minuman fungsional, karena mengandung senyawa fitokimia dari golongan alkaloid, flavonoid, dan tanin yang berkhasiat sebagai antihiperglikemik dan antioksidan. Rasa ekstrak daun sirih merah yang pahit dan rendahnya bioavailabilitas bahan aktif suatu ekstrak tanaman merupakan kendala yang perlu dicarikan solusinya.
Upaya meningkatkan bioavailabilitas dapat dilakukan dalam bentuk nanopartikel, karena bentuk nanopartikel akan memperluas permukaan sehingga aktivitasnyapun akan meningkat. Tujuan utama dalam merancang partikel nano sebagai suatu sistem pengantaran senyawa aktif adalah untuk (1) mengontrol ukuran partikel, sifat permukaan dan pelepasan agen farmakologi aktif untuk mencapai target senyawa pada tingkat optimal; (2) meningkatkan stabilitas senyawa; dan (3) mengontrol sifat pelepasan senyawa aktif. Penelitian ini merupakan salah satu alternatif untuk diversifikasi produk pangan fungsional berbasis sirih merah guna meningkatkan efektivitas penggunaan daun sirih merah serta biovaibilitasnya. Peluang pengembangan teknologi nano melalui teknik enkapsulasi formula ekstrak berbasis sirih merah dalam matrik nano diharapkan dapat meningkatkan sifat fungsionalnya, agar penggunaannya sebagai fitofarmaka menjadi lebih optimal.
Penelitian diawali dengan ekstraksi senyawa aktif sirih merah menggunakan metode maserasi dan refluks. Pada ekstrak yang diperoleh dilakukan uji fitokimia dan analisis yang meliputi rendemen, kapasitas antioksidan, total fenol,
concentration providing 50% inhibition (IC50) dan analisis komponen volatil senyawa aktif. Tahap kedua adalah sintesis nanopartikel menggunakan metode gelasi ionik dengan 4 konsentrasi kitosan yaitu 0,1%, 0,2%, 1% dan 2%. Pada masing-masing konsentrasi ditentukan ukuran partikel dengan menggunakan
Particle Size Analyzer (PSA), pengujian aktivitas fungsionalnya dan pengukuran kestabilannya. Tahapan ketiga adalah pengeringan semprot untuk mendapatkan nanopartikel dalam bentuk bubuk dengan bahan pengisi maltodekstrin (M) dan kombinasi antara maltodekstrin dan isolat protein kedelai (MISP). Tahapan keempat adalah pengkajian sistem pengantaran produk enkapsulasi berdasarkan uji disolusi dan uji bioaccessibility.
dan kestabilan yang baik ditunjukkan oleh nilai zeta potensial sebesar 32.75±2.11 mV.
Pengeringan semprot yang dilakukan terhadap konsentrasi ekstrak terpilih menggunakan bahan pengisi maltodekstrin dan isolat protein kedelai menunjukkan bahwa bahan pengisi kombinasi isolat protein kedelai 20% dan maltodekstrin 80% memberikan hasil yang baik, nilai aktivitas antioksidan lebih tinggi dibanding perlakuan bahan pengisi maltodekstrin 100% (M), walaupun terjadi peningkatan ukuran partikel hingga menjadi 8266,9 ± 1134,9 nm, Dari hasil foto Scanning Electron Microscopy, morfologi nanopartikel menyerupai bentuk bola dengan permukaan kasar dan berkerut. Hasil uji stabilitas pada beberapa pH selama 7 hari penyimpanan menunjukkan bahwa kerusakan senyawa fenol pada pH tinggi (6, 7 dan 8) lebih banyak dibandingkan pada pH rendah (2, 3 dan 4).
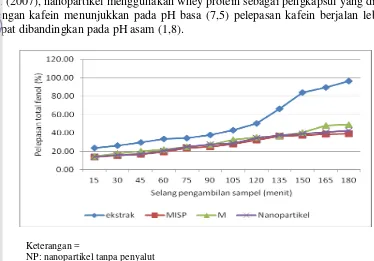
Hasil pengujian bioavailabilitas dengan metode disolusi menunjukkan bahwa pelepasan senyawa fenol pada medium basa berjalan lebih cepat dibandingkan pada medium asam. Pada medium basa pelepasan maksimal terjadi pada menit ke 180 untuk sampel nanopartikel dan MISP, sedangkan pada medium asam, pelepasan terbesar pada sampel ekstrak sebesar 96,51% diikuti oleh sampel maltodekstrin 49%, sampel nanopartikel 42,78% dan sampel MISP 39%. Hasil pengujian bioacessibility menunjukkan bahwa kandungan total fenol masih dapat ditemukan di dalam lambung, tetapi tidak semua dapat digunakan hingga ke dalam usus karena sebagian terbuang dan masuk ke dalam kolon. Semua sampel yang diujikan mempunyai potensi sebagai inhibitor enzim alfa glukosidase dengan nilai penghambatan ekstrak, nanopartikel, M, MISP dan acarbose berturut-turut 83,44±0,494 %; 28,21±1,124 %; 16,49±0,330 %; 15,36±0,202% dan 65,76±2,362%.
Nanopartikel sirih merah dapat digunakan sebagai salah satu alternatif produk nutraseutikal yang lebih tahan pada kondisi asam. Pelepasan senyawa fenol terkendali pada kondisi asam, sedangkan pada kondisi basa terlepas lebih cepat. Formula nanopartikel kitosan konsentrasi 0,2% yang dikeringkan dengan bahan pengisi maltodekstrin 80% dan isolat protein kedelai 20% memberikan sifat fungsional yang baik serta tahan terhadap kondisi asam.
SUMMARY
KUN TANTI DEWANDARI. Synthesis of Nanoparticles of Extracts of Red Betel (Piper Crocatum) and Its Delivery System . Supervised by Sedarnawati Yasni and Sri Yuliani
Red betel plant is one of medicinal plants that can be used as an ingredient of functional drinks, because it contains phytochemical compounds such as alkaloids, flavonoids, and tannins having antihyperglycemic and antioxidant properties. Bitter flavors of red betel leaf extract and its low bioavailability are a problem.
To improve the bioavailability can be done in the nanoparticles, because the surface of the nanoparticles will expand so the activity will increase. The main goals in designing nanoparticles as a delivery system for the active compound is (1) to control the particle size, surface properties and release of active compounds to achieve a target compounds at optimum levels, (2) increase the stability of the compound, and (3 ) to control the release of active compounds. This study provides diversification product of red betel-based functional food to increase its effectiveness and bioavailability. Development of nanoencapsulation of extracts of red betel is expected to improve its functional properties.
The first stage of this study is extraction of active compounds of red betel using maceration and reflux method. The extract was analysed for its phytochemical compounds, yield, antioxidant capacity, total phenol, concentration providing 50% inhibition (IC50) and the profile of volatile components. The second stage is the synthesis of nanoparticles using ionic gelation method with four concentration of chitosan (0.1%, 0.2%, 1% and 2%) with 10% extract. At this stage, product characterization includes particle size, functional activities and stability are measured. The third stage is encapsulation using spray drying with two different encapsulants, i.e.maltodextrin (M) and a combination of maltodextrin and soy protein isolate (MISP). The fourth stage is examining delivery system by using dissolution technique and bioaccessibility assay.
observed at free extract (96.51%) followed by maltodextrin capsule powder (49%), nanoparticle solution (42.78%). Bioacessibility analysis show that phenolic content was found in the stomach, with some part was wasted. All samples had alpha-glucosidase inhibitor properties (83.44 ± 0.494%, 28.21 ± 1.124%, 16.49 ± 0.330%; 15.36 ± 0.202% and 65.76 ± 2.362%) for nanoparticle solution, maltodextrin capsule powder, MISP capsule powder and acarbose, respectively.
Red betel nanoparticles can be used as an alternative nutraceuticals products that are more resistant to acidic conditions. The release of phenolic compounds in acidic conditions can be controlled, but under alkaline conditions more faster than in acidic concentration. The best formula is encapsulate with maltodextrin 80% and soy protein isolate 20% and contains nanoparticle of 0.2% chitosan provide good functional properties. Nanoparticle powder with maltodextrin 80% and soy protein isolate 20% provide good functional properties and resistant to acidic conditions.
© Hak Cipta Milik IPB, Tahun 2013
Hak Cipta Dilindungi Undang-Undang
Dilarang mengutip sebagian atau seluruh karya tulis ini tanpa mencantumkan atau menyebutkan sumbernya. Pengutipan hanya untuk kepentingan pendidikan, penelitian, penulisan karya ilmiah, penyusunan laporan, penulisan kritik, atau tinjauan suatu masalah; dan pengutipan tersebut tidak merugikan kepentingan IPB
Tesis
sebagai salah satu syarat untuk memperoleh gelar Magister Sains
pada
Program Studi Ilmu Pangan
SEKOLAH PASCASARJANA INSTITUT PERTANIAN BOGOR
BOGOR 2013
SINTESIS NANOPARTIKEL EKSTRAK SIRIH MERAH
(
Piper crocatum
) DAN KAJIAN SISTEM PENGANTARANNYA
Judul Tesis : Sintesis Nanopartikel Ekstrak Sirih Merah (Piper Crocatum) dan Kajian Sistem Pengantarannya
Nama : Kun Tanti Dewandari
NIM : F251100111
Disetujui oleh Komisi Pembimbing
Prof Dr Ir Sedarnawati Yasni, MAgr Ketua
Dr Ir Sri Yuliani, MT Anggota
Diketahui oleh
Ketua Program Studi Ilmu Pangan
Dr Ir Ratih Dewanti-Hariyadi, MSc
Dekan Sekolah Pascasarjana
Dr Ir Dahrul Syah, MScAgr
Tanggal Ujian: 20 Mei 2013
PRAKATA
Puji dan syukur penulis panjatkan kepada Tuhan atas segala berkat dan karunia-Nya sehingga karya ilmiah ini berhasil diselesaikan. Tema yang dipilih dalam penelitian yang dilaksanakan sejak bulan Juni 2012 ini mengenai sirih merah dan kajian sistem pengantarannya dengan judul Sintesis Nanopartikel Ekstrak Sirih Merah (Piper Crocatum) dan Kajian Sistem Pengantarannya. Tesis ini merupakan hasil penelitian yang didanai oleh Proyek KKP3T (Kerjasama Kemitraan Penelitian Pertanian dengan Perguruan Tinggi) tahun anggaran 2012.
Terima kasih penulis ucapkan kepada Ibu Prof.Dr.Ir. Sedarnawati Yasni, MAgr selaku ketua komisi pembimbing dan Ibu Dr. Ir. Sri Yuliani, MT selaku anggota komisi pembimbing yang telah meluangkan waktu untuk membimbing penulis selama melakukan penelitian dan memberikan kritik serta saran selama penyusunan tesis ini. Penulis juga mengucapkan terima kasih kepada Ibu Dr.Ir. Didah Nur Faridah yang telah bersedia menjadi penguji luar pada ujian tesis dan memberikan saran-saran untuk perbaikan tesis.
Penghargaan dan terima kasih penulis sampaikan kepada Badan Litbang Pertanian yang telah memberi beasiswa belajar, Bapak Ir. Rudy Tjahjohutomo, MT selaku kepala balai, bapak dan ibu peneliti di Balai Besar Litbang Pascapanen Pertanian, yang tidak dapat disebut satu persatu yang telah memberikan dorongan moril selama penulis melaksanakan tugas belajar. Ucapan terima kasih ditujukan juga kepada laboran dan teknisi di Balai Besar Litbang Pascapanen Pertanian : Citra, Idris, Ibu Dini, Ibu Pia, Mas Tri, Dwi, Mas Yudi yang telah membantu selama pelaksaan penelitian. Penulis juga mengucapkan terima kasih kepada laboran dan teknisi laboratorium Ilmu dan Teknologi Pangan IPB.
Ungkapan terima kasih ditujukan pula kepada teman-teman IPN 2010, Komang, Pipit, Ratna, Tika, Ame, Mbak Maria, Mbak Rara, Sadek, Pak Cecep, Umi, Mbak Farah dan yang lainnya yang tidak dapat disebut satu persatu yang bersedia membantu dan berbagi suka duka selama kuliah dan penelitian.
Terakhir, terima kasih tak terhingga kepada suami tercinta Diner Y.E Saragih, SP, MSE dan anakku tersayang Theresia Ayuditha Saragih atas hilangnya waktu dan kebersamaan serta doa dan kasih sayangnya. Kepada bapak ibu tercinta, Bapak KRT.Prodjoharjono, SH dan Ibu Sumijati, SIP atas doa, kasih sayang, perhatian yang tak ternilai. Kepada mbak Anik, mbak Nuning, mas Bowo dan mas Anto atas segala doa dan kasih sayangnya.
Semoga karya ilmiah ini bermanfaat.
DAFTAR ISI
DAFTAR ISI xi
DAFTAR TABEL xii
DAFTAR GAMBAR xii
DAFTAR LAMPIRAN xii
1 PENDAHULUAN 1
Dasar Pertimbangan 3
Tujuan Penelitian 3
Manfaat Penelitian 3
2 TINJAUAN PUSTAKA 3
Sirih Merah 3
Nanopartikel kitosan 4
Nanoteknologi pada produk pangan 5
Bioaccessibility 6
3. METODE PENELITIAN 7
Tempat dan Waktu Penelitian 7
Bahan dan Alat 7
Metode 8
4. HASIL DAN PEMBAHASAN 12
Ekstraksi Sirih Merah 12 Rendemen, Kapasitas Antioksidan dan Total fenol Ekstrak 14 Analisis Komponen Volatil Ekstrak Sirih Merah 15
Sintesis Nanopartikel 16 Stabilitas Nanopartikel 19 Sifat Fungsional Nanopartikel 20 Pengeringan Semprot (Spray Drying) Nanopartikel Ekstrak Sirih Merah 21 Stabilitas pada Penyimpanan 22 Kapasitas Antioksidan serta Total Fenol 24 Struktur mikrokapsul 25 Uji disolusi in vitro pada medium asam dan basa 26 Uji bioaccessibility secara in vitro 28 Penghambatan enzim α-glukosidase 30
5 SIMPULAN DAN SARAN 31 Simpulan 31
Saran 32
DAFTAR PUSTAKA 33
DAFTAR TABEL
1. Uji fitokimia ekstrak sirih merah 13
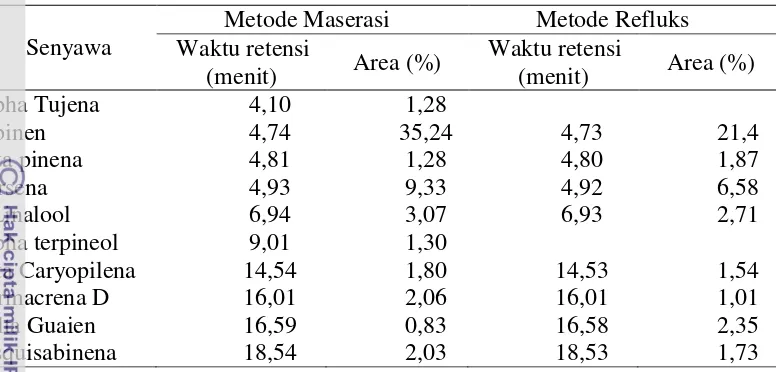
2. Data rendemen, kapasitas antioksidan dan total fenol ekstrak sirih merah 14 3. Profil senyawa volatil ekstrak sirih merah yang teridentifikasi dengan
GC-MS 16
4. Ukuran nanokitosan sirih merah pada berbagai konsentrasi 18
5. Hasil analisis sifat fungsional nanopartikel 20
6. Konsentrasi total fenol pada pH asam selama penyimpanan 7 hari 23 7. Konsentrasi total fenol pada pH basa selama penyimpanan 7 hari 23
8. Hasil pengujian sifat fungsional 24
9. Penghambatan enzim α-glukosidase 31
DAFTAR GAMBAR
1. Interaksi kitosan dengan TPP (a) deprotonasi, (b) ikatan silang ionik 17
2. Sampel nanokitosan sirih merah 18
3. Bubuk nanopartikel (A) kombinasi 80% maltodekstrin,20% Isolat Protein
Kedelai dan (B) Maltodekstin 100% 22
4. Struktur nanopartikel hasil foto SEM 25
5. Hubungan waktu terhadap pelepasan total fenol pada medium basa 26
6. Hubungan waktu terhadap pelepasan total fenol pada medium asam 27
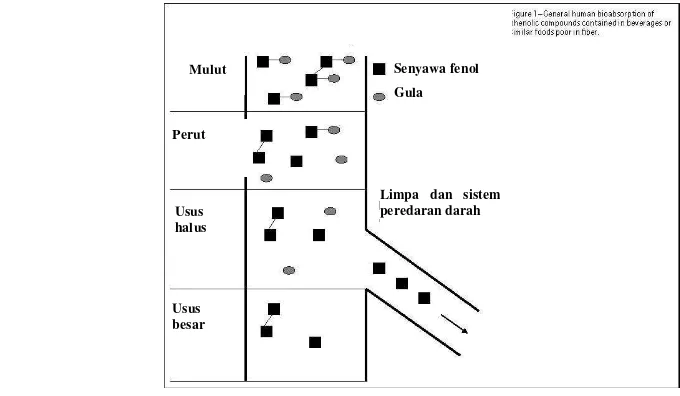
7. Skema penyerapan senyawa fenol dalam tubuh 29 8. Hasil uji bioaccessibility nanopartikel sirih merah 29
DAFTAR LAMPIRAN
1. Skema penelitian 40 2. Analisa dengan GC-MS 413. Prosedur Analisa 43 4. Uji anova total fenol, IC50 dan kapasitas antioksidan nanopartikel 45 5. Uji anova indeks polidispersitas, ukuran partikel dan zeta potensial 47 6. Uji statistik pengaruh perlakuan terhadap pH selama penyimpanan 49
7. Uji statistik rendemen dan sifat fungsional ekstrak 50
8. Hasil uji ukuran nanopartikel dengan PSA 51
1
PENDAHULUAN
Indonesia memiliki kekayaan sumberdaya hayati terbesar kedua setelah Brazil dengan lebih dari 30.000 spesies tanaman, walaupun hanya sekitar 300 spesies tanaman yang terdaftar pada Badan Pengawasan Obat dan Makanan (BPOM) yang telah digunakan untuk bahan obat tradisonal (jamu) oleh industri obat tradisional (Depkes 2007). Menurut laporan BPS (2004) sejumlah 7.000 spesies merupakan tanaman obat, dan 4.500 spesies diantaranya berada di Pulau Jawa. Tanaman obat dan rempah asli Indonesia menjadi salah satu keunggulan komparatif bagi daya saing Indonesia, khususnya untuk mengembangkan produk pangan fungsional, karena senyawa fitokimia yang terkandung di dalam tanaman obat dan rempah asli Indonesia memiliki khasiat tertentu yang bermanfaat untuk menjaga kesehatan tubuh.
Pengembangan produk pangan fungsional berbahan dasar tanaman obat dan rempah asli Indonesia yang memiliki aktivitas antihiperglikemik sangat diperlukan untuk menunjang upaya pemerintah mengurangi peningkatan jumlah penderita diabetes. Indonesia menduduki peringkat keempat sebagai negara dengan penderita diabetes mellitus terbanyak di dunia setelah Amerika Serikat, Cina dan India. Penderita diabetes saat ini berjumlah 13,7 juta orang, dan dapat meningkat menjadi 20,1 juta pada 2030 (Antara 2011). Hal ini menunjukkan adanya peningkatan jumlah penyandang diabetes sebanyak 2-3 kali lipat pada tahun 2030. Diabetes melitus adalah penyakit kronis yang terjadi sebagai akibat dari ketidakmampuan pankreas untuk memproduksi insulin yang cukup atau tubuh tidak mampu menggunakan insulin yang diproduksinya dengan efektif.
Salah satu tanaman obat Indonesia yang potensial yang diketahui memiliki aktivitas antihiperglikemik adalah daun sirih merah (P. crocatum). Sirih merah merupakan salah satu tanaman obat yang mengandung senyawa fitokimia dari golongan alkaloid, flavonoid, dan tanin yang berkhasiat sebagai antihiperglikemik dan antioksidan. Dari penelitian Batubara (2011), komponen utama dalam sirih merah adalah monoterpen dan sesquiterpen yang dapat meningkatkan aktivitas monofenolase dan difenolase pada enzim tirosinase. Pemberian air rebusan sirih merah dosis 20 g/kg BB pada tikus jantan galur Sprague dawley dapat menurunkan kadar glukosa darah dengan cara memperbaiki kelenjar eksokrin pankreas tikus yang rusak akibat aloksan (Safithri et al. 2006). Penelitian lain menunjukkan bahwa ekstrak etanol daun sirih merah dapat menghambat oksidasi asam lemak dengan daya hambat terbesar 80,40% pada konsentrasi 200 ppm dan sebagai radical scavenger dengan nilai IC50 85,82 ppm (Alfarabi et al. 2010).
Saat ini, kecenderungan penggunaan tanaman herbal untuk pengobatan terus meningkat. Berdasarkan hasil Riset Kesehatan Dasar (Riskesdas) 2010, hampir separuh orang Indonesia mengkonsumsi jamu (obat herbal). Data dari Departemen Kesehatan (2010) menyatakan bahwa sebanyak 49,53 persen penduduk Indonesia berusia 45 tahun ke atas mengkonsumsi jamu. Oleh karena itu, daun sirih merah berpotensi untuk dikembangkan menjadi produk pangan fungsional. Umumnya masyarakat dengan mudah mengkonsumsi air rebusan daun sirih merah, tetapi karena rasanya yang pahit hanya kalangan tua (usia 50 th ke atas) yang menyukai.
2
rasa yang kurang disukai, hanya sedikit senyawa polifenol yang terdapat dalam sistem pencernaan, karena waktu tinggal di dalam lambung tidak cukup lama, permeabilitas serta kelarutan dalam usus yang rendah. Selain itu, senyawa polifenol tidak stabil pada proses pengolahan pangan dan penyimpanan (suhu, oksigen dan cahaya) atau dalam saluran pencernaan (pH, enzim) merupakan faktor pembatas bagi aktivitas maupun manfaat polifenol bagi kesehatan. Salah satu teknologi yang mulai banyak digunakan, adalah teknologi nano karena dalam bentuk partikel nano luas permukaan meningkat, dan aktivitas senyawa aktif akan meningkat juga. Nanoenkapsulasi menunjukkan partikel dengan diameter dari 1 hingga 1000nm (Fang 2010). Tujuan utama dalam merancang partikel nano sebagai suatu sistem pengantaran senyawa aktif adalah (1) mengontrol ukuran partikel, sifat permukaan dan pelepasan agen farmakologi aktif dalam rangka mencapai tindakan situs-spesifik senyawa pada tingkat optimal; (2) meningkatkan stabilitas senyawa ; dan (3) memiliki sifat pelepasan terkontrol.
Keuntungan menggunakan partikel nano sebagai sistem pengantaran senyawa aktif meliputi hal-hal berikut: (1) ukuran partikel dan karakteristik permukaan partikel nano dapat dengan mudah dimanipulasi, (2) partikel nano dapat mengontrol dan mempertahankan pelepasan senyawa aktif selama transportasi sehingga mengurangi efek samping, (3) pelepasan senyawa aktif terkontrol dan karakteristik partikel degradasi dapat dengan mudah dipengaruhi oleh pilihan konstituen matriks. Kandungan senyawa aktif dapat dimasukkan ke dalam sistem tanpa reaksi kimia, hal ini merupakan faktor penting untuk menjaga aktivitas senyawa (Hirano S et al 1990 ).
Aplikasi nanoteknologi di bidang pangan cenderung semakin meningkat, karena keunggulannya dalam meningkatkan bioavailabilitas senyawa aktif, pengendalian pelepasan senyawa aktif serta memperbaiki sifat sensori. Dalam ukuran nano, partikel senyawa aktif lebih mudah diabsorpsi oleh dinding usus halus sehingga meningkatkan bioavailabilitasnya. Absorpsi senyawa aktif meningkat karena kelarutan partikel meningkat akibat dari luas permukaan partikel yang lebih besar. Dalam ukuran nano, partikel juga memiliki waktu tinggal yang lebih panjang karena terjerap dalam lapisan mukosa usus.
Penerapan teknologi nano dimaksudkan untuk meningkatkan kemampuan aktivitas fungsional dan bioavailabilitas dari senyawa-senyawa fitokimia daun sirih merah. Mengacu kepada beberapa hasil penelitian nano partikel
nutraceutical, seperti propolis, teh hijau maupun curcuma yang menunjukkan bahwa bioavailabilitas dan sifat fungsional lainnya meningkat secara signifikan dalam bentuk nanopartikel.
3 Dasar Pertimbangan
1. Peningkatan jumlah penderita diabetes mellitus merupakan tantangan dan peluang bagi pengembangan tanaman biofarmaka terutama dalam bentuk pangan fungsional berbasis sirih merah sebagai alternatif pengobatan alami. 2. Tanaman sirih merah sudah lama dikenal dan dimanfaatkan oleh sebagian
besar masyarakat Indonesia sebagai obat tradisional antihiperglikemik secara empirik.
3. Pemanfaatan daun sirih merah yang banyak dihasilkan di Indonesia sebagai bahan alami yang memiliki senyawa antioksidan dan khasiat antihiperglikemik akan meningkatkan nilai tambah tanaman sirih merah dan penghasilan masyarakat
4. Penerapan teknologi nanoenkapsulasi dapat meningkatkan aktivitas, kestabilan, keamanan, serta sifat fungsional ekstrak daun sirih merah.
Tujuan Penelitian
1. Mengkaji kondisi proses ekstraksi daun sirih merah
2. Mengembangkan formulasi nanopartikel ekstrak sirih merah dengan teknik gelasi ionik
3. Mengkaji karakteristik fisik dan sifat fungsional nanopartikel ekstrak sirih merah
4. Mengkaji sistem pengantaran nanopartikel formula terpilih secara in vitro Manfaat Penelitian
Hasil penelitian ini diharapkan dapat memberikan manfaat untuk memperluas pemanfaatan daun sirih merah sebagai alternatif bahan alami pencegahan/pengobatan penyakit diabetes
2
TINJAUAN PUSTAKA
Sirih Merah (Piper crocatum)
Tanaman sirih merah termasuk dalam famili Piperaceae, tumbuh merambat dengan bentuk daun menyerupai hati dan bertangkai. Sirih merah (Piper crocatum) adalah salah satu tanaman obat potensial yang sejak lama telah diketahui memiliki berbagai khasiat untuk menyembuhkan berbagai jenis penyakit.
4
daun sirih merah memiliki manfaat yang sangat luas sebagai bahan obat diantaranya bersifat antikanker, desinfektan dan anti jamur.
Pada awalnya sirih merah merupakan tanaman hias tetapi akhirnya melihat potensinya yang besar mulai banyak dikembangkan sebagai biofarmaka. Konsentrasi ekstrak etanol 30% daun sirih merah sebanyak 0, 1000, dan 200000 ppm memiliki aktivitas sebagai inhibitor enzim glukosa oksidase sebesar 0,1421,
0.2255, dan 12.4452 μmol/mL.menit (Agustanti 2008), suspensi ekstrak etanol
sirih merah dapat menurunkan kadar glukosa darah tikus putih jantan (rattus norvegicus l.) galur wistar hingga 67,45% dengan dosis 105mg/kg berat badan (Robianto. 2009). Selain itu, ekstrak etanolik daun sirih merah (Piper crocatum) pada konsentrasi 7,8125-500 μg/mL dapat menghambat proliferasi sel kanker dengan nilai IC50 123,18 μg/mL sehingga berpotensi sebagai antikanker (Yulianti 2010). Ekstrak methanol daun sirih merah dapat menghambat proliferasi sel kanker payudara (T47D) (Wicaksono 2009). Penelitian terhadap ekstrak etanol daun sirih menunjukkan bahwa ekstrak tersebut memiliki aktivitas antioksidasi, yaitu dapat menghambat oksidasi asam lemak dengan daya hambat terbesar 80,40% pada konsentrasi 200 ppm dan sebagai radical scavenger dengan nilai IC50 85,82 ppm (Alfarabi et al 2010).
Nanopartikel kitosan
Nanopartikel merupakan salah satu jenis modifikasi bentuk kitosan, tergantung metode yang digunakan. Pembuatan nanopartikel kitosan dapat dilakukan dalam berbagai cara diantaranya (1) Nanopartikel kitosan dengan basis taut silang kovalen (modifikasi kitosan taut silang dengan glutaraldehid), (2) berbasis taut silang ionik (metode gelasi ionik dengan natrium tripolifosfat), (3) pembuatan dengan metode desolvasi, (4) metode emulsion-droplet coalescence, (5) metode reverse micellar dan (6) metode self-assembly melalui modifikasi kimia (metode grafting menggunakan polietilen glikol).
Beberapa hasil penelitian penggunaan nanopartikel menyatakan nanopartikel kitosan dapat meningkatkan efisiensi protein Bovine Serum Albumin
5 (Harris et al. 2011). Nanopartikel kitosan terisi ekstrak katekin dari teh telah berhasil dilakukan dan menunjukkan aktivitas antioksidan yang cukup tinggi (Tang et al. 2013).
Nanopartikel dengan metode gelasi ionik banyak dikembangkan. Gelasi ionik merupakan sifat interaksi gel kitosan dengan polianion khusus. Proses ini membentuk taut silang inter dan intra dalam rantai polimer yang dimediasi oleh polianion. Salah satu polianion yang sangat banyak digunakan sebagai senyawa taut silang adalah natrium tripolifosfat. Natrium tripolifosfat (STPP) seringkali dibandingkan dengan glutaraldehid sebagai pentaut silang kitosan karena penggunaan keduanya sangat banyak. STPP lebih menguntungkan penggunaannya sebagai pentaut silang kitosan dalam pembentukan sistem pengantar obat daripada glutaraldehid, karena metode modifikasi kitosan menggunakan agen taut silang glutaraldehid berbahaya bagi kesehatan manusia bila digunakan sebagai sistem pengantar obat secara oral terutama karena glutaraldehid memiliki efek toksik yang tinggi (Hritcu et al. 2009). Penelitian Yu-Hsin Lin et al. (2008) menyatakan bahwa digunakannya natrium tripolifosfat sebagai salah satu pasangan ion kitosan, akan membentuk nanopartikel menjadi lebih stabil dan memiliki penembusan membran yang lebih baik. Pada nanopartikel sambung silang multi ion, tripolifosfat berperan sebagai salah satu komponen anion multivalent yang akan membentuk ikatan sambung silang dengan kitosan yang bersifat kationik.
Nanoteknologi pada produk pangan
Menurut National Nanotechnology Initiative (2006),nanoteknologi dipahami sebagai ilmu yang mempelajari karakterisasi dan manipulasi bahan biologi dan mikrobiologi yang berukuran lebih kecil dari 100 nanometer, termasuk juga fenomena unik dan sifat fungsional baru yang akan timbul. Beberapa sistem pangan dan pertanian dapat memanfaatkan nanotekologi untuk meningkatkan ketahanan pangan, mengembangkan alat baru di bidang biologi molekular dan seluler, bahan baru untuk deteksi patogen, dan delivery system bahan pangan fungsional. Dewasa ini, nanoteknologi dalam bidang pangan difokuskan pada pengembangan bahan pengemas baru, nutraceutical, dan bahan antimikroba serta pengawetan dan penyimpanan bahan pangan
Keuntungan menggunakan nanopartikel sebagai sistem pengantaran obat/senyawa aktif dapat dijelaskan sebagai berikut:
a. Ukuran partikel dan karakteristik permukaan nanopartikel dapat dengan mudah dimanipulasi sehingga dapat tepat menuju sasaran bagian tubuh yang akan diterapi
b. Dapat mengontrol dan mempertahankan pelepasan obat selama transportasi dan di lokasi target
c. Pengontrolan pelepasan partikel dan karakteristik degradasi partikel degradasi dipengaruhi oleh matrik pembawa. Pemasukan obat ke dalam sistem tubuh tanpa melewati reaksi kimia sehingga dapat mencegah kerusakan obat (Hirano et al. 1990).
6
kesehatan, kosmetik, agrokimia, dan pangan. Sistem pengantaran (delivery system) harus memenuhi sejumlah persyaratan agar fungsinya terpenuhi. Pertama, dapat berfungsi sebagai kendaraan yang membawa bahan fungsional ke tempat yang dituju (site of action). Kedua, sistem tersebut harus mampu melindungi bahan fungsional dari kerusakan kimia atau biologi selama pengolahan, penyimpanan dan penggunaan. Dengan kata lain, sistem pengangkutan dapat menjaga bahan fungsional tetap berada dalam keadaan aktifnya. Ketiga, sistem tersebut harus dapat mengakomodasi pelepasan bahan fungsional secara terkendali (controlled realese) atau memiliki kondisi tertentu yang memicu pelepasan (pH, kekuatan ionik atau suhu). Keempat, delivery system harus sesuai dengan komponen lain dalam sistem, misalnya kompatibel dengan sifat fisikokimia dan atribut kualitatif (penampakan, tekstur, rasa dan masa simpan) produk akhir (Weiss et al. 2006). Selain itu, sebagian besar senyawa bioaktif bersifat lipofilik dan menunjukkan kelarutan yang rendah. Kelarutan yang rendah, mengakibatkan penyerapan yang rendah pada sistem pencernaan dan ketersediaannya yang rendah dalam tubuh. Pada industri pangan, hal ini akan mengurangi ketersediaan senyawa aktif untuk dienkapsulasi, menjaga dari kerusakan dan pelepasan senyawa aktif dalam pengembangan pangan fungsional.
Nanoenkapsulasi didefinisikan sebagai suatu teknologi untuk mengemas suatu zat yang mengacu pada pengemasan bioaktif pada skala nano, teknik pembuatannya meliputi nanokomposit, nanoemulsifikasi dan nanostrukturisasi (Quintanilla et al. 2009). Fungsionalitas produk akhir (termasuk pelepasan bahan inti) dapat dipertahankan selama penyimpanan. Dalam bidang rekayasa pangan, perlindungan senyawa bioaktif seperti vitamin, antioksidan, protein, lemak, dan karbohidrat dapat dicapai dengan menggunakan nanoenkapsulasi untuk menghasilkan pangan fungsional dengan fungsi dan kestabilan yang optimal (Quintanilla et al. 2009). Selain itu, nanoenkapsulasi efisien untuk mengatasi berbagai hambatan seperti kehilangan fungsionalitas selama pemrosesan atau penyimpanan, ketidakcocokan antara inti dan bahan dinding (pelapis), menutupi rasa dan bau tidak enak, kerusakan tekstur, dan kehilangan aktivitas enzim.
Sistem pengantaran senyawa bioaktif diartikan sebagai senyawa bioaktif yang diletakkan di dalam zat pembawa untuk mengatur laju pelepasan zat bioaktif. Zat pembawa nano (nanocarriers) dapat melindungi senyawa bioaktif dari lingkungan yang kurang kondusif. Zat pembawa nano memiliki luas permukaan yang dapat meningkatkan kelarutan, bioavailabilitas, dan memperbaiki target pelepasan bahan pangan yang dienkapsulasi, bila dibandingkan dengan zat pembawa ukuran mikro (Ahmed et al. 2012).
Aplikasi nanoteknologi dalam bidang pangan menunjukkan peningkatan, karena teknologi nano dapat meningkatkan bioavailabilitas bahan aktif, mengendalikan pelepasan bahan aktif, dan memperbaiki sifat sensori.
Bioaccessibility
Bioaccessibility dapat diartikan sebagai pelepasan senyawa dari matriks makanan ke dalam cairan pencernaan dalam saluran pencernaan. Bioaccessibility
7 antioksidan) yang telah melalui membran sel dan tersedia untuk digunakan dalam sel.
Pencernaan merupakan proses fisiologis yang memungkinkan ekstraksi makronutrien (misalnya karbohidrat, protein), bahan penyusun (misalnya monosakarida, asam amino), mikronutrien (vitamin dan mineral, seperti Zn, Fe dan Na) dan fitokimia (misalnya polifenol) dari matriks makanan, untuk penyerapan yang berlanjut. Tiga langkah prosedur simulasi proses pencernaan dalam mulut, perut dan usus kecil, merupakan bagian paling mungkin untuk menentukan bioaccessibility. Saluran usus besar tidak diperhitungkan, karena dalam pencernaan makanan secara in vivo penyerapan senyawa terutama terdapat pada usus kecil (Alishahi et al. 2011). Hasil yang diperoleh pada metode in vitro
didasarkan pada pembentukan produk pencernaan yang larut atau terdialisis (dialyzable). Nilai fraksi yang bioaccessible merupakan konsentrasi elemen yang larut dalam media pencernaan. Prosedur in vitro melibatkan simulasi lambung dan kondisi pencernaan usus yang dilakukan di laboratorium. Sebagai percobaan yang dilakukan di bawah kondisi pencernaan, disebut pula dengan istilah 'simulasi', hasilnya mungkin tidak akurat seperti yang diperoleh dalam studi in vivo.
Enzim yang berbeda biasanya ditambahkan secara berurutan untuk mensimulasikan tahapan yang berbeda dari proses pencernaan. Sebagai contoh, banyak model in vitro didasarkan pada inkubasi berturut-turut dengan pepsin untuk mensimulasikan perut dan kemudian pankreatin untuk mensimulasikan usus kecil. Komposisi enzim dari cairan pencernaan tertentu dapat disimulasikan dengan mencampurkan bersama-sama dalam jumlah yang tepat dari enzim murni. Juga harus dicatat bahwa enzim sering membutuhkan komponen tambahan dalam cairan pencernaan agar berjalan secara efisien, misalnya, lipase pankreas membutuhkan keberadaan kalsium dan garam empedu (Liang et al. 2012).
3 METODE PENELITIAN
Tempat dan Waktu Penelitian
Penelitian ini dilaksanakan sejak bulan April 2012 hingga Oktober 2012 bertempat di Laboratorium Kimia Pangan dan Laboratorium Biokimia, Departemen Ilmu dan Teknologi Pangan, Fakultas Teknologi Pertanian, Institut Pertanian Bogor, Laboratorium Pusat Teknologi Farmasi BPPT Serpong, Balai Inkubator BPPT Serpong, Pusat Teknologi Bahan dan Industri BATAN Serpong serta Laboratorium Balai Besar Penelitian dan Pengembangan Pascapanen Pertanian Bogor.
Bahan dan Alat
8
Peralatan yang digunakan adalah peralatan ekstraksi, peralatan sintesis nanopartikel meliputi stirrer bar, magnetic stirrer dan hot plate, syringe, sentrifuse, ultra turrax homogenizer serta instrument untuk analisis meliputi Gas Chromatography (Agilent 7890A USA), Particle Size Analyzer (DelsaNano C Beckman Coulter USA) dan Scanning Electron Microscopy (SEM-EDS JEOL-JSM 6510 AL, Jepang) serta peralatan gelas.
Metode
Pelaksanaan penelitian secara umum dapat dibagi menjadi beberapa tahapan. Tahap pertama adalah ekstraksi sirih merah menggunakan pelarut etanol 96%. Tahap kedua adalah sintesis nanopartikel terisi ekstrak sirih merah serta karakterisasi fisik dan sifat fungsional yang dilanjutkan dengan proses enkapsulasi dan karakterisasi enkapsulat. Tahap ketiga adalah uji stabilitas serta uji pelepasan senyawa fenol dan bioacessibility secara in vitro. Pelaksanaan penelitian secara rinci dapat disimak pada Lampiran 1 dan dapat dijelaskan sebagai berikut : Ekstraksi sirih merah
Ekstraksi daun sirih merah dilakukan untuk mendapatkan ekstrak yang akan digunakan sebagai bahan aktif dalam sintesis nanopartikel. Ekstraksi dilakukan dengan metode maserasi (metode dingin) dan refluks (metode panas) menggunakan etanol 96%. Pada metode maserasi, bahan baku sebanyak 50 gram yang telah kering digiling dengan ukuran partikel 50 mesh, selanjutnya direndam menggunakan pelarut etanol 96% dengan perbandingan bahan dan pelarut 1:4. Selama perendaman dilakukan pengadukan menggunakan shaker selama 6 jam, kemudian didiamkan hingga 24 jam. Setelah itu dilakukan penyaringan untuk mendapatkan filtrat. Filtrat yang diperoleh kemudian dievaporasi menggunakan
rotary evaporator hingga diperoleh ekstrak pekat. Pada metode refluks, pelarut panas akan mengekstrasi senyawa volatil sebagai senyawa murni dan kemudian terdinginkan dalam kondensor dan masuk ke dalam wadah penampung. Proses ini berlangsung secara berkesinambungan sampai penyaringan sempurna selama 3 jam, dengan suhu 45oC. Filtrat yang diperoleh dari masing-masing metode ekstraksi dikumpulkan dan dievaporasi menggunakan rotary evaporator pada suhu 40-50oC sampai dihasilkan ekstrak kental dengan total padatan terlarut 30o brix. Pada ekstrak yang diperoleh kemudian dilakukan uji fitokimia sebagai skrining awal dan dilanjutkan dengan identifikasi komponen aktif menggunakan GC-MS (Lampiran 2). Selanjutnya dilakukan penghitungan rendemen serta pengukuran total fenol, kapasitas antioksidan dan IC50. Pada tahapan ini, ekstrak terpilih berdasarkan rendemen, sifat fisik, sifat kimia, sifat fungsional serta analisis secara visual meliputi bau dan warna yang kemudian digunakan untuk sintesis nanopartikel.
Sintesis nanopartikel terisi ekstrak sirih merah (Alishahi et al., 2011)
9 larutan kitosan dan ekstrak. Konsentrasi kitosan dibuat dengan beberapa konsentrasi yaitu 0,1%, 0,2%, 1% dan 2%. Pembuatan larutan kitosan dengan konsentrasi 0,1% dilakukan dengan cara melarutkan 0,1g kitosan ke dalam asam asetat 0,1% (b/v), demikian pula dengan konsentrasi 0,2%, 1% dan 2%. Pencampuran dilakukan dengan cara diaduk selama 24 jam agar campuran larut sempurna, kemudian disaring dengan kertas Whatman no 40. Larutan STPP 0,2% dibuat dengan mencampurkan 0,2 g natrium tripolifosfat ke dalam 100ml air suling dan diaduk selama 2 jam.
Pada sintesis nanopartikel, ekstrak sirih merah ditimbang sebanyak 30g larutan kitosan, lalu diaduk dengan magnetic stirrer pada kecepatan 350 rpm sampai homogen. Penambahan larutan STPP dilakukan sebanyak 6 g dengan cara setetes demi tetes hingga habis dan dibiarkan selama 15 menit. Setelah pencampuran sempurna, ditambahkan ekstrak sirih merah sebanyak 1 g dengan cara setetes demi tetes menggunakan syringe. Larutan campuran diaduk kembali hingga ekstrak tercampur sempurna dan pengadukan dilanjutkan selama 15 menit untuk mendapatkan larutan yang homogen. Dari masing-masing konsentrasi dilakukan karakterisasi fisik meliputi ukuran partikel, kestabilan, indeks polidispersitas serta sifat fungsional (aktivitas antioksidan, IC50, total fenol). Pemilihan nanopartikel terbaik berdasarkan ukuran dengan rentang nilai terkecil, kestabilan serta indeks polidispersitas yang menunjukkan keseragaman ukuran partikel. Selain itu juga dipertimbangkan sifat fungsionalnya meliputi aktivitas antioksidan, IC50 serta total fenol.
Karakterisasi nanopartikel
Karakterisasi nanopartikel dilakukan terhadap sifat fisik dan sifat fungsional nanopartikel. Karakterisasi sifat fisik nanopartikel meliputi ukuran, indeks polidispersitas dan kestabilan (zeta potensial). Karakterisasi sifat fungsional meliputi aktivitas antioksidan, total fenol dan IC50. Penentuan ukuran nanopartikel dan indeks polidispersitas dilakukan dengan Particle Size Analyzer (PSA) Delsa Nano C Beckman Coulter, yang pada alat ini menggunakan metode dynamic light scattering. Sampel nanopartikel dimasukkan ke dalam kuvet, kemudian dilakukan pengukuran dengan menentukan intensitas, volume maupun number distribusi. Enkapsulasi nanopartikel ekstrak sirih merah dan karakterisasi (Desai dan Park 2005)
10
aktivitas antioksidan, total fenol, IC 50 serta uji kestabilan dalam beberapa pH yang dilakukan selama 7 hari penyimpanan dalam suhu ruang.
Proses rekonstitusi
Pada sampel yang telah dilakukan pengeringan semprot, dilakukan rekonstitusi untuk mendapatkan kembali nanopartikel dalam bentuk cairan. Rekonstitusi dilakukan dengan penambahan akuades sejumlah tertentu sehingga dihasilkan kembali larutan dengan kandungan total padatan terlarut sebesar 20% atau sama dengan kondisi sebelum dilakukan pengeringan. Setelah itu dilakukan pengujian kembali terhadap ukuran dan diameter partikel yang terbentuk.
Struktur partikel enkapsulat
Pengukuran struktur partikel dilakukan dengan menggunakan Scanning Electron Microscopy (SEM-EDS JEOL-JSM 6510 AL), dengan tujuan untuk mengetahui bentuk struktur dan morfologi nanopartikel yang diperoleh. SEM adalah mikroskop yang menggunakan hamburan elektron dalam membentuk bayangan sehingga sampel dapat diobservasi dan dikarakterisasi pada skala mikrometer. Sebelum dilakukan analisa, sampel dengan ukuran 2 mm diberi lapisan emas menggunakan alat gold sputter coater pada kondisi vakum. Sampel tersebut ditempatkan pada mikroskop SEM dan diamati pada voltase akselerasi 20 KV. Gambar yang diperoleh kemudian direkam dan dicetak.
Stabilitas nanopartikel dalam berbagai pH (Tsai et al., 2011)
Pengujian stabilitas nanopartikel dilakukan untuk mengetahui kestabilan nanopartikel pada berbagai pH (2-8) selama penyimpanan 7 hari pada suhu ruang (28oC). Pengaturan pH dengan menggunakan buffer fosfat dan buffer klorida. Buffer fosfat dibuat dengan menambahkan Na2HPO4 sebanyak 0,89 g dan NaH2PO4.sebanyak 0,69 g untuk membuat 100 ml larutan. Buffer khlorida dibuat dengan mencampur 0,2M KCl dan 0,2M HCl hingga 200 ml . Nanopartikel disimpan di dalam botol plastik sebanyak 30 ml. Pengujian kestabilan dilakukan dengan mengukur kandungan total fenol yang terlepas ke dalam medium penyimpanan. Pengujian kandungan total fenol dilakukan menggunakan Folin-Ciocalteau dengan persiapan ekstraksi senyawa fenol mengunakan metanol dilanjutkan sonikasi selama 20 menit. Semakin banyak total fenol yang terdeteksi dalam medium penyimpanan menunjukkan kestabilan yang rendah karena bahan penyalut tidak dapat melindungi senyawa aktif.
Uji pelepasan senyawa fenol dan bioaccessibility secara in vitro
Pengujian pelepasan senyawa fenol (in vitro release) (Departemen Kesehatan 1995)
11 pada suhu (37±0,5)oC. Konsentrasi senyawa aktif dalam larutan aliquot setiap 15 menit diambil dan diukur kandungan total fenolnya menggunakan spektofotometer UV pada panjang gelombang 750nm. Medium asam dibuat dengan mencampurkan 0,2M HCl dan 0,2M KCl dilarutkan dalam aquadest. Medium basa dibuat dengan mencampurkan 0,89 g Na2HPO4 dan 0,69 NaH2PO4 Uji Bioacessibility (simulasi pencernaan secara in vitro) (Liang et al. 2012)
Simulasi pencernaan dilakukan pada fase gastric (lambung) dan fase small intestine (usus kecil). Pada tahap awal dibuat larutan yang menyerupai kondisi di lambung, dengan mengatur pH larutan melalui penambahan HCl 4 N agar didapatkan pH 2. Selanjutnya larutan sampel sebanyak 2,5 ml ditambah dengan 20 ml larutan kondisi lambung diinkubasi di penangas air bergoyang selama 2 jam pada 37oC. Setelah 1 jam diinkubasi, diambil cuplikan dari fraksi sampel, kemudian diukur total fenolnya (fraksi lambung). Sisa larutan dimasukkan ke dalam tabung sentrifuse yang berisi 20 ml NaHCO3 0,1 M, kemudian ditambahkan larutan yang terdiri dari campuran pankreatin dan ox bile hingga pH 7,5. Larutan campuran diinkubasi kembali dalam penangas air bergoyang pada suhu 37oC selama 2 jam, diasamkan hingga pH 2 dan disentrifuse. Fraksi yang terpisah kemudian diuji kandungan total fenolnya, baik fraksi supernatan (fraksi bagian atas/digesta) maupun fraksi pelet (fraksi bagian bawah/dialisat). Fraksi di atas sebagai fraksi yang terserap sedangkan fraksi di bawah sebagai fraksi yang masuk ke dalam kolon. Pengukuran total fenol dilakukan pada fraksi lambung, fraksi digesta dan fraksi dialisat menggunakan spektrofotometer UV pada panjang gelombang 750nm.
Analisis Penghambatan Aktivitas Enzim Alfa Glukosidase (Matsumoto et al. 2002)
Enzim alfa glukosidase adalah enzim golongan hidrolase yang berfungsi mengkatalisis reaksi akhir dari proses penyerapan karbohidrat di usus. Enzi mini
mengkatalisis hidrolisis ikatan α-1,4 sehingga menghasilkan α-D-glukosa.
Terhambatnya kerja enzim α-glukosidase menyebabkan berkurangnya glukosa yang diserap oleh usus sehingga berkurangnya sumber glukosa yang masuk ke dalam aliran darah. Hal ini mampu membantu menurunkan keadaan hiperglikemia sehingga penderita diabetes dapat mengatur kadar glukosa darahnya. Prosedur analisa data dilihat pada Lampiran 3.
Analisis Statistik
Seluruh data yang diperoleh dilakukan analisis perhitungan nilai rata-rata dan standar deviasi serta ANOVA (Analysis of Varianc
e) pada tingkat kepercayaan 95% (taraf α 0,05). Nilai P<0,05 menunjukkan
12
4 HASIL DAN PEMBAHASAN
Ekstraksi Sirih Merah
Ekstraksi sirih merah dilakukan dengan metode maserasi (ekstraksi cara dingin) dan refluks (ekstraksi cara panas) menggunakan pelarut etanol 96% yang merupakan pelarut polar. Dasar pertimbangan pemilihan kedua metode adalah untuk mengetahui pengaruh penggunaan panas pada proses ekstraksi terhadap kandungan senyawa aktif ekstrak. Kedua metode dibandingkan berdasarkan rendemen serta sifat kimia untuk mendapatkan proses ekstraksi optimum yang akan digunakan pada tahap selanjutnya. Pemilihan pelarut didasarkan pada senyawa yang diharapkan akan terekstrak, apakah bersifat polar, semi polar atau non polar. Ekstraksi dilakukan berdasarkan prinsip kepolaran, yaitu pelarut polar akan melarutkan senyawa polar, pelarut semi polar akan melarutkan senyawa semi polar dan pelarut non polar akan melarutkan senyawa non polar. Berdasarkan tingkat kepolaran dapat digunakan berbagi macam pelarut, misalnya hexane untuk non polar, etil asetat semi polar dan metanol untuk polar (Marlina 2008). Penggunaan pelarut untuk aplikasi pada bahan pangan perlu mempertimbangkan toksisitas (Prasad et al. 2009). Daun sirih merah mengandung senyawa polar, terutama flavonoid, alkaloid dan tanin. Senyawa polar banyak mengandung gugus OH, oleh karena itu, penggunaan etanol merupakan pelarut yang tepat untuk mengekstrak senyawa aktif pada daun sirih merah. Selain etanol, pelarut lain yang dapat digunakan untuk mengekstrak senyawa polar adalah metanol dan aseton, namun tingkat toksisitasnya lebih tinggi dibandingkan dengan etanol (Harborne 1987, Prasad et al. 2009). Selain penggunaan pelarut yang tepat, faktor lain yang perlu diperhatikan adalah pengecilan ukuran bahan agar mempermudah proses ekstraksi. Pada penelitian ini, daun sirih merah yang akan digunakan dicuci terlebih dahulu, kemudian dikeringkan pada suhu 40-50oC, digiling hingga didapatkan bubuk berukuran 50 mesh. Proses penggilingan bertujuan untuk meningkatkan peluang terlarutnya senyawa-senyawa yang ingin diekstrak dengan etanol karena rusaknya dinding dan membran sel akan memudahkan etanol berinteraksi dengan senyawa-senyawa yang ingin diekstrak.
Maserasi adalah ekstraksi senyawa aktif dengan cara merendam jaringan atau organ tumbuhan di dalam suatu larutan yang tepat untuk mendapatkan senyawa yang diinginkan (Marlina 2008). Metode maserasi memiliki keuntungan, yaitu cara pengerjaannya yang lebih mudah, alat-alat yang digunakan sederhana, dan cocok untuk bahan yang tidak tahan pemanasan. Perbandingan yang digunakan antara bahan dan pelarut adalah 1 : 4 kemudian dishaker selama 6 jam dengan kecepatan 131 rpm, lalu sampel didiamkan selama 24 jam, kemudian larutan sampel disaring menggunakan kertas saring dan diambil filtratnya.
13 selama 3 jam pada suhu 45oC. Filtrat yang diperoleh dari masing-masing metode ekstraksi, dievaporasi menggunakan rotary evaporator dengan suhu 40-50oC sampai dihasilkan ekstrak kental dengan total padatan terlarut 30o brix.
Pada ekstrak yang diperoleh dilakukan uji fitokimia (Suratmo 2008) sebagai skrining awal untuk analisis yang akan dijadikan dasar prosedur tahap selanjutnya. Uji fitokimia dilakukan untuk menentukan kandungan golongan senyawa aktif dari ekstrak tumbuhan, meliputi uji polifenol, saponin, tanin dan flavonoid (Tabel 1).
Tabel 1 Uji fitokimia ekstrak sirih merah
Parameter Metode Ekstraksi
Keterangan : +/positif : senyawa teridentfikasi , -/negatif : senyawa tidak teridentifikasi
Hasil uji fitokimia menunjukkan bahwa ekstrak sirih merah baik dengan metode maserasi maupun refluks mengandung polifenol, tanin dan flavonoid. Pada ekstrak dengan metode maserasi warna merah pada uji polifenol lebih pekat dibandingkan dengan metode refluks, begitu juga dengan warna merah pada uji flavonoid secara visual terlihat lebih pekat.
Skrining total fenol dan tanin menggunakan pereaksi dengan memanfaatkan sifat tanin yang bereaksi dengan protein menghasilkan kopolimer yang tidak larut air. Reaksinya menjadi lebih sensitif dengan penambahan NaCl untuk meningkatkan salting out dari kompleks protein-tanin (Gobalakrishnan et al. 2013). Adanya total fenol ditunjukkan dengan timbulnya warna merah pada sampel, sedangkan adanya tanin pada ekstrak sirih merah menunjukkan perubahan warna dari kuning menjadi hijau kehitaman dengan penambahan FeCl3. Ekstrak sirih merah yang positif mengandung flanovoid ditandai dengan terbentuknya warna merah jingga hingga hijau setelah dilakukan penambahan HCl pekat. Terbentuknya warna merah menunjukkan adanya flavon, warna jingga menunjukkan adanya flavanol dan warna hijau menunjukkan adanya aglikon. Flavonoid-o-glikosida memiliki molekul gula, yang diketahui memiliki gugus hidroksil sehingga akan mudah larut dalam pelarut dengan kepolaran tinggi. Semakin banyak gugus monosakarida yang berikatan dengan senyawa flavonoid (ikatan glikosida) maka akan semakin bersifat polar karena semakin bertambahnya gugus hidroksil.
Rendemen, Kapasitas Antioksidan dan Total Fenol Ekstrak
14
100%. Rendemen yang diperoleh dari proses ekstraksi maserasi dan refluks berturut-turut adalah 7,2 ±0,25% dan 9,8±0,35% (Tabel 2).
Tabel 2 Data rendemen, kapasitas antioksidan dan total fenol ekstrak sirih merah
Parameter Metode Ekstraksi
Maserasi Refluks
Rendemen (%) 7,2 ± 0,25a 9,8 ± 0,35b
Kapasitas antioksidan (AAEµg/ml) 10892,86 ± 6,06a 9971,43 ± 6,06b
IC50 (AAEµg/ml) 46,51 ± 0.05a 49,57 ± 0,27b
Total fenol (mg/100gr) 2388,37 ± 0,3a 2257,22 ± 0,9a
Keterangan :
Data merupakan rerata dari 3 kali ulangan (rata-rata ± SD)
Huruf yang sama pada baris yang sama menunjukkan tidak berbeda nyata pada P < 0,5 (uji selang berganda Duncan)
Rendemen pada metode maserasi lebih rendah dibandingkan dengan metode refluks. Pemanasan pada metode refluks dapat meningkatkan jumlah rendemen oleoresin karena suhu yang dibutuhkan oleh suatu pelarut untuk mencapai titik didihnya dapat melarutkan komponen oleoresin yang tidak terekstrak dengan perlakuan tanpa pemanasan. Pemanasan yang lama dapat menyebabkan sejumlah komponen oleoresin rusak dan menguap, sehingga jumlahnya lebih rendah dibandingkan dengan tanpa pemanasan. Selain itu salah satu antioksidan yaitu flavonoid, merupakan golongan senyawa fenol yang memiliki sistem aromatik terkonjugasi yang mudah rusak pada suhu tinggi. Panas menyebabkan terjadi degradasi dinding sel sehingga semakin memudahkan keluarnya fenol, dan pemanasan berfungsi pula untuk inaktivasi enzim polifenol oksidase sehingga kerusakan fenol semakin kecil, dan stabilitas fenol terjaga (Susanti 2008). Penelitian Prasad et al. (2009) menunjukkan bahwa ekstraksi dengan etanol memberikan rendemen yang lebih tinggi dibanding dengan air dan etil asetat. Begitu juga ekstraksi oleoresin kayu manis dengan etanol memiliki rendemen yang lebih tinggi dibandingkan dengan metanol maupun air, dan minyak atsiri dapat teresktrak lebih tinggi dengan pelarut etanol (Solehuddin 2001). Etanol memiliki polaritas 0,68 sedangkan air >0,73. Peran polaritas pelarut dalam mengekstrak oleoresin sangat besar karena sebagian besar komponen oleoresin bersifat polar. Oleh karena itu, ekstraksi dengan konsentrasi etanol yang tinggi dapat mengekstrak lebih banyak senyawa aktif pada sirih merah dibandingkan etanol dengan konsentrasi lebih rendah.
Hasil pengukuran kapasitas antioksidan ekstrak sirih merah dengan metode maserasi dan refluks berturut-turut adalah sebesar 10892,86 ± 6,06 AAEµg/ml dan 9971,43 ± 6,06 AAEµg/ml yang setara dengan nilai IC50 sebesar 46,51µg/ml dan 49,57 µg/ml. Hal ini menunjukkan bahwa metode maserasi memberikan nilai kapasitas antioksidan dan total fenol yang lebih tinggi, karena metode maserasi tidak menggunakan panas sehingga senyawa fenolik tidak mengalami kerusakan. Dari hasil analisa statistik menunjukkan bahwa kapasitas antioksidan kedua metode berbeda nyata, sedangkan nilai IC 50 tidak berbeda nyata.
15 protein, lemak dengan cara melengkapi kekurangan elektron yang dimiliki radikal bebas sehingga senyawa stabil dan mencegah pembentukan rantai radikal bebas. Pengukuran kapasitas antioksidan bertujuan untuk mengetahui kemampuan ekstrak menahan reaksi oksidasi yang tergantung dari banyaknya komponen antioksidan dan komponen prooksidan. Kapasitas antioksidan diukur dengan standar asam askorbat. Kapasitas antioksidan pada penelitian ini berbanding lurus dengan total fenol, karena senyawa antioksidan alami pada tumbuhan umumnya adalah senyawa fenolik yang termasuk ke dalam golongan flavonoid. Oleh karena itu, kandungan total fenol dapat dijadikan sebagai dasar atau indikasi awal pendugaan besarnya kapasitas antioksidan suatu bahan (Prasad et al. 2009).
Hasil analisis total fenol dan kapasitas antioksidan menunjukkan metode maserasi lebih baik dibandingkan dengan metode refluks sehingga pada tahap selanjutnya ekstraksi dilakukan dengan menggunakan metode maserasi. Selain itu, maserasi lebih efisien dalam penggunaan energi, cara pengerjaan lebih mudah serta alat yang digunakan sederhana.
Analisis Komponen Volatil Ekstrak Sirih Merah
Komponen volatil dalam bahan pangan sangat penting untuk diketahui. Senyawa volatil sebagian besar tedapat dalam minyak atsiri. Minyak atsiri adalah kelompok senyawa berbau, larut dalam alkohol, terdiri dari campuran eter, aldehid, keton dan terpen. Komponen bahan aktif suatu bahan pangan banyak terdapat di dalam minyak atsiri. Pada penelitian ini, ekstrak yang diperoleh merupakan oleoresin yang didalamnya terdapat resin dan minyak yang diekstrak menggunakan pelarut etanol yang bersifat polar. Senyawa fungsional yang penting pada ekstrak sirih merah adalah golongan fenol dan terpen. Pengukuran senyawa volatil dengan GC-MS diperlukan sebagai data pendukung yang menujukkan kandungan senyawa aktif dalam ekstrak sirih merah. Hasil kromatogram dengan GC-MS ekstrak sirih merah dapat dilihat pada Tabel 3.
16
Komponen monoterpena dan sesquiterpena minyak atsiri sirih merah memiliki kemampuan untuk meningkatkan aktivitas enzim monofenolase dan difenolase tirosinase, sedangkan pada penelitian Suratmo (2008) yang melakukan ekstraksi daun sirih merah menggunakan beberapa pelarut menunjukkan bahwa senyawa yang terekstrak meliputi senyawa fenol, flavonoid dan alkaloid yang berpotensi sebagai senyawa antioksidan. Dari pengujian dengan menggunakan GC-MS, ekstrak sirih merah berpotensi sebagai antioksidan dengan terdeteksinya senyawa yang merupakan golongan monoterpen.
Sintesis Nanopartikel
Nanopartikel ekstrak sirih merah disintesis dengan modifikasi fisik menggunakan metode gelasi ionik dengan bantuan magnetic stirrer dan memanfaatkan sodium tripolifosfat (STPP) untuk membentuk ikatan silang ionik dengan molekul kitosan sehingga dapat digunakan sebagai bahan penjerap (Mi et al. 1999). Penggunaan TPP untuk mencampurkan polimer kitosan dengan polianion sodium tripolifosfat yang menghasilkan interaksi antara muatan positif pada gugus amino kitosan dengan muatan negatif tripolifosfat (Chattopadhyay and Inamdar 2010).
Kitosan dengan pKa 6,5 merupakan polikationik, ketika dilarutkan dalam asam, amin bebas akan terprotonasi menghasilkan –NH+. Natrium tripolifosfat (Na5P3O10) larut dalam air hingga diperoleh ion hidroksil dan ion tripolifosfat yang akan bergabung dengan struktur kitosan. Derajat taut silang kitosan dengan natrium tripolifosfat dipengaruhi oleh keberadaan sisi kationik dan senyawa anionik sehingga pH dari natrium tripolifosfat memiliki peran penting selama proses taut silang.
-17 P3O105-. Reaksi sambung silang secara ionik terjadi antara ion -P3O105- dari tripolifosfat dengan ion -NH3+ dari kitosan, sedangkan reaksi antara ion -OH- dari tripolifosfat dengan ion -NH3+ dari kitosan terjadi secara deprotonasi (Ko et al. 2002; Bhumkar dan Pokharkar 2006) (Gambar 1).
Sintesis nanopartikel dipengaruhi oleh beberapa faktor, diantaranya komposisi material dan metode yang digunakan. Komposisi material yang sesuai akan menghasilkan nanopartikel dengan ukuran kecil dan morfologi seragam. Nanopartikel akan terbentuk pada komposisi tertentu antara kitosan dan TPP. Metode pembuatan nanopartikel juga sangat mempengaruhi terbentuknya ukuran dan keseragaman partikel selain komposisi material. Semakin banyak terjadi ikatan silang antara kitosan dengan STPP akan meningkatkan jumlah pori yang terbentuk sehingga semakin banyak zat aktif yang akan terjerap.
Hasil pengujian terhadap ukuran dan distribusi nanopartikel pada beberapa konsentrasi kitosan (0,1%, 0,2%,1% dan 2%) dengan menggunakan PSA dapat dilihat pada Tabel 4. Data lengkap dapat dilihat pada Lampiran 7. Tabel 4 menunjukkan bahwa semakin tinggi konsentrasi kitosan yang ditambahkan terjadi peningkatan ukuran partikel karena akan terjadi penggumpalan (aglomerasi) pada molekul kitosan (Wahyono 2010). Semakin besar konsentrasi kitosan dengan jumlah STPP yang tetap juga akan memperbesar ukuran nanopartikel karena adanya kecenderungan untuk beraglomerasi. Pada konsentrasi yang tinggi, partikel-partikel yang terbentuk dari reaksi antara kitosan dan TPP sangat banyak dan padat, sehingga bergerombol membentuk agregat menjadi partikel berukuran mikro (Mardliyati et al. 2012). Konsentrasi 0,2% memberikan ukuran partikel yang paling kecil, sedangkan pada konsentrasi 0,1% tidak terdeteksi adanya partikel. Hal ini kemungkinan karena konsentrasi yang terlalu kecil atau karena terlarut sempurna sehingga tidak terdeteksi adanya partikel. Meningkatnya ukuran partikel serta kecenderungan partikel untuk beragregasi dipengaruhi juga oleh rasio kitosan dengan TPP serta kondisi pH. Pada konsentrasi kitosan 1% dan 2% terjadi peningkatan ukuran partikel
18
dikarenakan jumlah kitosan yang tinggi sehingga pada saat pencampuran dengan STPP ukuran partikel menjadi lebih besar. Pada konsentrasi 2% partikel yang terbentuk berukuran mikro, karena tingginya penambahan kitosan sehingga rasio antara STPP dan kitosan menjadi semakin besar sehingga meningkatkan ukuran partikel yang terbentuk (Mardliyati et al. 2012).
Dari hasil uji statistik tidak terdapat perbedaan yang nyata antara konsentrasi kitosan 0,2% dan 1%, tetapi dengan pertimbangan ukuran yang lebih kecil serta efisiensi proses, maka konsentrasi kitosan 0,2% yang dipilih untuk proses enkapsulasi menggunakan spray dryer. Dari penampakan secara visual menunjukkan bahwa semakin besar konsentrasi kitosan semakin keruh penampakan larutan (Gambar 3). Semakin tinggi konsentrasi kitosan maka terjadi peningkatan ukuran partikel yang ditandai dengan terjadinya peningkatan kekeruhan.
Tabel 4. Ukuran nanokitosan sirih merah pada beberapa konsentrasi Konsentrasi
Keterangan : data merupakan rerata dari 3 ulangan (rata-rata ± SD) ttd = tidak terdeteksi
Huruf yang sama pada kolom yang sama menunjukkan tidak berbeda nyata pada P < 0,5 (uji selang berganda Duncan)
Analisis dengan Particle Size Analyzer (PSA) dapat menentukan nilai indeks polidispersitas (IP) yang menunjukkan distribusi ukuran partikel. Semakin kecil nilai indeks polidispersitas menunjukkan distribusi ukuran droplet semakin sempit, yang berarti ukuran diameter droplet semakin homogen (Yuan et al. 2008). Nilai IP yang lebih kecil dari 0,3 mendekati angka 0 menunjukkan sampel uji memiliki distribusi sempit dan menunjukkan formula nanopartikel yang seragam (Yen et al. 2008). Indeks polidispersitas lebih besar dari 0,5
Gambar 2. Sampel nanokitosan sirih merah
19 menunjukkan heterogenitas yang tinggi (Avadi et al. 2010). Dari keempat konsentrasi yang diuji, semua konsentrasi memiliki nilai IP kurang 0,3 sehingga dapat dikatakan masih seragam dan semua masih dalam kisaran rentang ukuran nanopartikel (Patel et al. 2009).
Stabilitas Nanopartikel
Stabilitas nanopartikel dinyatakan dengan menggunakan zeta potensial. Zeta potensial adalah muatan pada permukaan partikel yang dapat mempengaruhi kestabilan partikel di dalam larutan dengan gaya elektrostatik diantara partikel atau dapat dikatakan merupakan ukuran kekuatan tolak menolak antar partikel (Qi
et al. 2004). Sebagian besar sistem koloid dalam air distabilkan oleh gaya tolak eletrostatik, semakin besar gaya tolak menolak maka semakin kecil kemungkinan partikel untuk bergabung dan membentuk agregat.
Pada pengukuran zeta potensial dapat diketahui ada tidaknya kecenderungan partikel saling beraglomerasi sehingga akan memperbesar ukuran partikel atau sebaliknya. Selain ukuran partikel, nilai zeta potensial juga sangat penting pada saat merancang suatu partikel yang bersifat pengiriman terkendali (Konecsni et al. 2012). Semakin tinggi nilai zeta potensial, kemampuan mencegah terjadinya flokulasi (peristiwa penggabungan koloid dari yang kecil menjadi besar) semakin baik. Koloid dengan nilai zeta potensial tinggi diatas 30 mV adalah elektrik stabil, sedangkan koloid dengan nilai potensial rendah cenderung akan mengental flokulasi. Suatu partikel dinyatakan stabil bila memiliki nilai zeta potensial di atas |30mV| (Mardliyati et al. 2012). Penelitian Mohanraj dan Chen (2006) menyatakan , bahwa nanopartikel dengan nilai zeta potensial lebih dari +/- 30 mV telah terbukti stabil dalam suspensi untuk mencegah agregasi.
Dari hasil pengukuran menunjukkan bahwa konsentrasi 0,2% dan 1% memiliki rentang nilai yang menunjukkan kestabilan dibanding konsentrasi 0,1% dan 2% (Tabel 4 dan Lampiran 5). Pada konsentrasi 0,1% nanopartikel tidak terbentuk dan cenderung tidak stabil, pada konsentrasi kitosan 2% mengalami kecenderungan berflokulasi karena jumlah kitosan yang lebih banyak dan menjadi tidak stabil (Fan et al. 2012) Konsentrasi kitosan dapat mempengaruhi zeta potensial nanopartikel. Konsentrasi kitosan yang tinggi menyebabkan NH3 ternetralkan pada permukaan sehingga mengakibatkan kekuatan elektrostatik antara partikel lebih kuat dan menjadi tidak stabil (Li et al. 2012). Pada konsentrasi rendah dengan berat molekul rendah, nanopartikel lebih stabil karena kecenderungan untuk membentuk partikel yang kecil karena rantai kitosan yang lebih pendek sehingga lebih mudah untuk membentuk komplek kitosan dan TPP yang lebih rapat.
20
Sifat fungsional nanopartikel
Nanopartikel dengan beberapa konsentrasi diuji sifat fungsional meliputi kapasitas antioksidan, total fenol dan IC50. Pengujian ini diperlukan untuk mengetahui apakah terjadi perubahan sifat fungsional selama proses sintesis nanopartikel. Kapasitas antioksidan merupakan kemampuan suatu senyawa antioksidan dalam menghambat paparan radikal bebas. Kapasitas antioksidan juga dapat diartikan sebagai kemampuan suatu bahan pangan untuk menahan reaksi oksidasi tergantung dari banyaknya komponen antioksidan dan komponen prooksidan yang dikandungnya. Pengukuran kapasitas antioksidan dilakukan menggunakan metode DPPH dengan prinsip reaksi reduksi dan oksidasi antara DPPH dan senyawa antioksidan. Semakin banyak radikal DPPH yang tereduksi, akan menunjukkan semakin besar nilai kapasitas antioksidan dan penghitungan didasarkan pada jumlah asam askorbat sebagai standar.
Hasil pengujian kapasitas antioksidan menunjukkan bahwa diantara konsentrasi yang lain, nanopartikel dengan perlakuan konsentrasi 0,2% memberikan nilai yang tertinggi, yaitu sebesar 560,00±5,65 ppm. Tingginya nilai aktivitas antioksidan pada konsentrasi 0,2% karena ukuran partikel yang kecil akan meningkatkan sifat mukoadhesiv dan permeabilitas sehingga ketersediaannya di dalam tubuh meningkat. Selain itu, nilai total fenol juga paling tinggi karena ukuran partikel yang sangat kecil sehingga senyawa fenol yang terjerap lebih banyak dibandingkan perlakuan lain yang ukuran partikelnya lebih besar. Dengan semakin meningkatnya jumlah antioksidan maka semakin banyak radikal DPPH yang tereduksi. Secara umum, aktivitas antioksidan suatu senyawa berkaitan dengan kandungan total fenol karena antioksidan alami pada tumbuhan umumnya adalah senyawa fenolik termasuk di dalamnya golongan flavonoid. Hal ini sejalan dengan nilai total fenol yang tinggi. Penelitian Meenakshi et al. (2009) menyatakan adanya hubungan antara total fenol dan aktivitas antioksidan dimana jika didalam suatu bahan memiliki konsentrasi senyawa fenol yang tinggi maka aktivitas antioksidan dalam bahan tersebut juga tinggi.
Nilai IC50 juga sangat berhubungan dengan nilai total fenol. Semakin tinggi kandungan total fenol menunjukkan nilai IC50 yang semakin rendah. Golongan senyawa polifenolik yang berupa golongan flavonoid, turunan asam sinamat, tokoferol bersifat multifungsional dan dapat beraksi sebagai pereduksi, penangkap radikal bebas, pengkelat logam dan peredam terbentuknya singlet oksigen (Meenakshi et al. 2009).
Tabel 5. Hasil analisis sifat fungsional nanopartikel Konsentrasi
Keterangan : Penambahan ekstrak sebesar 10%
data merupakan rerata dari 3 ulangan (rata-rata±SD)
21 Pengeringan semprot (spray drying) nanopartikel ekstrak sirih merah
Pengeringan semprot banyak digunakan untuk sampel yang mengandung partikel yang larut dalam air, memiliki sifat kristalinitas dan mudah berdifusi. Selain itu, sampel yang dikeringkan dengan pengering semprot harus mampu bertahan terhadap panas (Patel et al. 2009).
Penggunaan bahan pengkapsul yang berbeda bertujuan untuk mendapatkan nanopartikel dengan sistem pengeluaran senyawa aktif terkontrol, terutama penggunaan protein. Maltodekstrin merupakan salah satu bahan yang banyak digunakan untuk enkapsulasi senyawa polifenol. Ekstrak etanol wortel hitam yang mengandung antosianin tinggi dikeringkan dengan menggunakan maltodekstrin sebagai bahan pembawa dan pengkapsul (Ersus 2007). Maltodekstrin memiliki kelarutan yang tinggi di dalam air, bersifat membentuk film, berikatan dengan flavor dan lemak, serta dapat mengurangi permeabilitas terhadap oksigen (Richana et al. 2007).
Selain maltodekstrin, bahan pengkapsul nanopartikel dari protein juga dapat digunakan, karena sifatnya yang unik diantaranya membentuk gel yang memungkinkan sebagai bahan yang ideal untuk enkapsulasi senyawa aktif. Protein merupakan salah satu bahan yang sangat potensial digunakan sebagai enkapsulan serta pembawa senyawa aktif dan obat, dan dapat mengoptimalkan pengantaran yang spesifik dan sesuai target (Gunasekaran et al. 2006). Pengkapsulan dengan protein dapat juga digunakan untuk bahan-bahan nutrasetikal yang sensitif di dalam saluran pencernaan. Protein dapat digunakan bersama-sama dengan bahan lain seperti beta-laktoglobulin yang mengkapsul kitosan nanopartikel (ukuran 100nm) dengan gelasi ionik dan sodium tripolifosfat. Selain itu, protein juga akan melindungi senyawa-senyawa yang sensitif terhadap kondisi di dalam saluran pencernaan (Chen et al. 2006). Menurut Zhang et al. (2012), protein merupakan salah satu bahan dengan sifat fungsional yang unik, diantaranya kemampuan untuk membentuk gel dan emulsi dan kemampuan dalam sistem pengantaran tersebut untuk senyawa aktif yang bersifat lipofilik maupun hidrofilik. Selain dapat berikatan dengan beberapa jenis senyawa aktif karena struktur ikatan polipeptida yang dapat melindungi senyawa aktif. Isolat protein kedelai digunakan sebagai bahan pengkapsul karena ketersediaannya yang melimpah, murah dan merupakan bahan yang dapat didaur ulang (Tapal and Purnima 2012).