FORMULASI PATCH NATRIUM DIKLOFENAK
BERBASIS POLIMER HIDROKSI PROPIL METIL
SELULOSA (HPMC) SEBAGAI SEDIAAN LOKAL
PENANGANAN INFLAMASI PADA PENYAKIT
PERIODONTAL
SKRIPSI
HISSI FITRIYAH
109102000006
PROGRAM STUDI FARMASI
FAKULTAS KEDOKTERAN DAN ILMU KESEHATAN
UNIVERSITAS ISLAM NEGERI SYARIF HIDAYATULLAH
UIN SYARIF HIDAYATULLAH JAKARTA
FORMULASI PATCH NATRIUM DIKLOFENAK
BERBASIS POLIMER HIDROKSI PROPIL METIL
SELULOSA (HPMC) SEBAGAI SEDIAAN LOKAL
PENANGANAN INFLAMASI PADA PENYAKIT
PERIODONTAL
SKRIPSI
Diajukan sebagai salah satu syarat memperoleh gelar Sarjana Farmasi
HISSI FITRIYAH
109102000006
PROGRAM STUDI FARMASI
FAKULTAS KEDOKTERAN DAN ILMU KESEHATAN
UNIVERSITAS ISLAM NEGERI SYARIF HIDAYATULLAH
v
Nama : Hissi Fitriyah
Program Studi : Farmasi
Judul : Formulasi Patch Natrium Diklofenak Berbasis Polimer Hidroksi Propil Metil Selulosa (HPMC) Sebagai Sediaan Lokal Penanganan Inflamasi pada Penyakit Periodontal.
Telah dibuat sediaan mukoadhesif patch yang mengandung natrium diklofenak sebagai sediaan lokal penanganan inflamasi pada penyakit periodontal. Penelitian ini bertujuan untuk memformulasi dan mengkarakterisasi sifat-sifat dari patch
natrium diklofenak yang berbasis polimer hidroksi propil metil selulosa (HPMC). Patch dibuat dalam 3 formula A1, A2 dan A3 dengan memvariasikan konsentrasi larutan HPMC sebanyak 1%, 1,5% dan 2%. Patch dibuat dengan metode solvent casting. Patch yang telah dibuat menunjukkan bahwa ketiga patch dapat melekat dipermukaan membran gusi lebih dari 7 jam. Persen kumulatif difusi natrium diklofenak pada jam ke-enam dari patch A1, A2 dan A3 berturut-turut 34%, 21% dan 24%. Lapisan backing yang dibentuk dari etil selulosa diketahui dapat menahan difusi natrium sebesar 97,5%. Dari hasil tersebut dapat disimpulkan bahwa patch yang terbaik ditunjukkan oleh formula A1.
vi
Name : Hissi Fitriyah
Program Study : Pharmacy
Title : Formulation of Diclofenac Sodium Patch Based Hydroxy Propyl Methyl Cellulose (HPMC) as Local Administration for The Inflammatory Treatment in Periodontal Disease.
Mucoadhesive patches containing diclofenak sodium have been made as local administration for the inflamatory treatment in periodontal deasease. The objectives of this research were to formulate and to study characteristic of the resulting diclofenac sodium patch based hydroxy propyl methyl cellulose (HPMC). Patches were formulated in three formulas termed A1, A2 and A3 by varying the concentration of hidroxy propyl methyl celullose (HPMC) solution in the formula as much as 1%, 1,5% and 2%. Patches were prepared by solvent casting methode. In vitro residence time showed that all formulas patch can be attachted on the mucosa gingival bovine more than 7 hours. Cumulatif diffusion of diclofenak sodium at sixth hours from A1, A2 and A3 respectively were 34%, 21% and 24%. Backing layer formed from ethyl cellulose can inhibit diffusion of diclofenac sodium as much as 97,5%. From these result, the best diclofenac sodium patch showed by A1.
vii Alhamdulillahirabbil`alamiin, segala puji dan syukur penulis panjatkan kehadirat Allah SWT yang telah melimpahkan rahmat dan ridho-Nya sehingga penulis dapat menyelesaikan penyusunan skripsi ini hingga selesai. Penulisan
skripsi yang berjudul “Formulasi Patch Natrium Diklofenak Berbasis Polimer Hidroksi Propil Metil Selulosa (HPMC) Sebagai Sediaan Lokal Penanganan
Inflamasi pada Penyakit Periodontal” bertujuan untuk memenuhi persyaratan guna
memperoleh gelar Sarjana Farmasi pada Fakultas Kedokteran dan Ilmu Kesehatan Universitas Islam Negeri Syarif Hidayatullah Jakarta.
Pada kesempatan ini penulis menyadari bahwa, tanpa bantuan dan bimbingan dari berbagai pihak, dari masa perkuliahan sampai pada penyusunan skripsi ini, sangatlah sulit bagi saya untuk menyelesaikan skripsi ini. Oleh karena itu saya mengucapkan terima kasih dan penghargaan sebesar-besarnya kepada :
1. Yuni Anggraeni, M.Farm., Apt dan Sabrina, M.Farm., Apt., selaku dosen pembimbing yang telah banyak memberikan bimbingan, waktu, tenaga, saran dan dukungan dalam penelitian ini.
2. Prof. Dr. (hc) dr. M. K. Tadjudin, Sp. And., selaku Dekan Fakultas Kedokteran dan Ilmu Kesehatan Universitas Islam Negeri Syarif Hidayatullah Jakarta.
3. Drs. Umar Mansur, M.Sc., Apt selaku ketua Program Studi Farmasi Fakultas Kedokteran dan Ilmu Kesehatan Universitas Islam Negeri Syarif Hidayatullah Jakarta.
4. Seluruh dosen di Program Studi Farmasi Fakultas Kedokteran dan Ilmu Kesehatan Universitas Islam Negeri Syarif Hidayatullah Jakarta.
5. Kedua orang tua dan keluarga yang telah memberikan semangat, doa dan dukungan baik moral maupun material hingga terwujudnya skripsi ini.
6. Fanny Putu Saputra atas segala pengertian, semangat dan bantuannya.
viii penelitian.
9. Teman teman seperjuangan farmasi angkatan 2009 atas kebersamaan kita. 10.Serta pihak-pihak lain yang tidak dapat disebutkan satu persatu, yang telah
memberikan dukungan hingga terwujudnya skripsi ini.
Penulis menyadari bahwa skripsi ini masih jauh dari sempurna, namun penulis berharap semoga hasil penelitian ini dapat bermanfaat bagi perkembangan ilmu pengetahuan pada umumnya dan ilmu Farmasi pada khususnya. Amin.
Jakarta, Juli 2013
x Halaman
HALAMAN JUDUL ... i
HALAMAN PERNYATAAN ORISINALITAS ... ii
HALAMAN PERSETUJUAN PEMBIMBING ... iii
HALAMAN PENGESAHAN ... iv
ABSTRAK ... v
ABSTRACT ... vi
KATA PENGANTAR ... vii
HALAMAN PERSETUJUAN PUBLIKASI KARYA ILMIAH ... ix
DAFTAR ISI ... x
2. 6 Hidroxypropyl Methylcellulose (HPMC) ... 20
xi
3.4.5.6.Uji Waktu Tinggal ... 29
3.4.5.7.Uji Kemampuan Penentrasi Zat aktif ... 29
3.4.5.8.Uji Kebocoran Backing ... 30
BAB 4 HASIL DAN PEMBAHASAN 4. 1 Karakteristik Cairan Polimer ... 31
4. 2 Karakteristik Fisikokimia Patch ... 32
4. 3 pH Permukaan Patch ... 37
4. 4 Waktu Tinggal Patch pada Permukaan Gusi Sapi ... 38
4. 5 Derajat Pengembangan ... 39
4. 6 Kemampuan Penentrasi Natrium Diklofenak ... 41
4. 7 Kebocoran Backing Membran ... 45
BAB 5 KESIMPULAN DAN SARAN 5. 1Kesimpulan ... 47
5. 2Saran ... 47
xii Halaman
Tabel 2.1 Komposisi dan Keberadaan Keratin di Mukosa Mulut ... 11
Tabel 3.1 Formula Patch Natrium Diklofenak ... 26
Tabel 4.1 Viskositas Larutan Polimer ... 31
Tabel 4.2 Uji Pelipatan Patch ... 34
Tabel 4.3 Sifat Fisikokimia Patch ... 35
Tabel 4.4 pH Permukaan Masing-masing Formula Patch ... 37
Tabel 4.5 Waktu Tinggal Patch pada Permukaan Membran Gusi Sapi 38
Tabel 4.6 Derajat Pengembangan Patch ... 39
Tabel 4.7 Persentase Kumulatif Difusi Zat Aktif ... 41
Tabel 4.8 Jumlah Kumulatif Zat Aktif Yang Terdifusi ... 41
Tabel 4.9 Analisis Statistik Kruskal-Wallis Test dari Data Persentase Difusi Natrium Diklofenak ... 43
Tabel 4.10 Statistik Persentase Difusi Natrium Diklofenak ... 43
Tabel 4.11 Fluks Natrium Diklofenak dari Masing-masing Formula .... 44
Tabel 4.12 Pengolahan Data Fluks Secara Statistik Menggunakan ANOVA ... 45
Tabel 4.13 Statistik Fluks Natrium Diklofenak ... 45
xiii Halaman
Gambar 2.1. Struktur Kimia Natrium Diklofenak ... 7
Gambar 2.2. Area Rongga Mulut ... 9
Gambar 2.3. Lapisan Mukosa Mulut ... 10
Gambar 2.4. Tahap Proses Mukoadhesi ... 13
Gambar 2.5 Struktur Formula HPMC ... 20
Gambar 2.6. Struktur Formula Etil Selulosa ... 22
Gambar 3.1. Skema dari Franz Diffusion ... 30
Gambar 4.1. Patch dari Masing-masing Formula ... 32
Gambar 4.2. Organoleptis Patch ... 33
Gambar 4.3. Penampakan Mikroskopis Patch ... 35
Gambar 4.4. Grafik Keragaman Bobot ... 36
Gambar 4.5. Grafik Ketebalan Patch ... 37
Gambar 4.6. Grafik Pengembangan Patch ... 40
Gambar 4.7. Grafik Persentase Difusi Zat Aktif Melalui Membran Gusi Sapi dari Masing-masing Formula ... 42
Gambar 4.8. Grafik Jumlah Difusi Zat Aktif Melalui Membran Gusi Sapi dari Masing-masing Formula ... 42
xiv Halaman
Gambar 2.1 Struktur Kimia Natrium Diklofenak ... 7
Gambar 2.2 Area Rongga Mulut ... 9
Gambar 2.3 Lapisan Mukosa Mulut ... 10
Gambar 2.4 Tahap Proses Mukoadhesi ... 13
Gambar 2.5 Struktur Formula HPMC ... 20
Gambar 2.6 Struktur Formula Etil Selulosa ... 22
Gambar 3.1 Skema dari Franz Diffusion ... 30
Gambar 4.1 Patch dari Masing-masing Formula ... 32
Gambar 4.2 Organoleptis Patch ... 33
Gambar 4.3 Penampakan Mikroskopis Patch ... 35
Gambar 4.4 Grafik Keragaman Bobot ... 36
Gambar 4.5 Grafik Ketebalan Patch ... 36
Gambar 4.6 Grafik Pengembangan Patch ... 40
Gambar 4.7 Grafik Persentase Difusi Zat Aktif Melalui Membran Gusi Sapi dari Masing-masing Formula ... 42
Gambar 4.8 Grafik Jumlah Difusi Zat Aktif Melalui Membran Gusi Sapi dari Masing-masing Formula ... 42
1 UIN Syarif Hidayatullah PENDAHULUAN
1. 1 Latar Belakang
Diklofenak termasuk salah satu obat non-steroid anti-inflamasi drug
(NSAID) yang banyak digunakan untuk menangani nyeri dan inflamasi, diklofenak juga digunakan untuk mengatasi nyeri dan inflamasi pada penyakit periodontal. Penelitian mengungkapkan bahwa terdapat hubungan antara produksi prostaglandin lokal dan metabolit lainnya dari asam arakidonat dengan terjadinya resorpsi tulang alveolar pada penyakit periodontal. Penelitian telah menemukan bahwa senyawa yang dapat menghambat produksi prostaglandin seperti obat golongan non steroidal anti-inflamasi drug
(NSAID), dapat mempengaruhi tahap kehilangan tulang pada penyakit periodontal (Mohammed et al., 2009).
Hampir semua obat golongan NSAID memiliki kecenderungan memiliki efek samping terhadap lambung dan duodenum (Wongso, 1996). Penyebab kematian yang sering akibat dari pemakaian NSAID adalah perdarahan lambung terutama pada pasien usia lanjut (Wongso, 1996). Pemakaian diklofenak selama kehamilan juga tidak dianjurkan (Wilmana dan Sulistia, 2007). Berdasarkan pedoman pelayanan farmasi untuk ibu hamil dan menyusui yang dikeluarkan oleh Depkes RI natrium diklofenak digolongkan pada katagori B dan D untuk wanita hamil dengan usia kehamilan di trimester ketiga dan menjelang kelahiran. Semua obat anti radang non-steroid (NSAID) dapat mengurangi peradangan dengan menghambat sintesis prostaglandin sampai derajat tertentu. Karena prostaglandin memainkan peran yang sangat besar pada perkembangan janin, penghambatan ini menyebabkan berbagai efek pada ibu, janin dan neonatus (Rubin, 1999).
UIN Syarif Hidayatullah
ideal harus dapat dengan cepat melekat dan memiliki kekuatan melekat yang optimum, tidak mengganggu proses berbicara, makan dan minum, harus dapat memberikan pelepasan obat yang searah menuju lapisan mukosa, tidak menyebabkan infeksi sekunder seperti karies gigi dan harus memiliki ketahanan yang baik akibat adanya pembilasan saliva (Izhar & John, 2012).
Patch terdiri dari dua lapisan, dimana lapisan utama mengandung polimer yang adhesif dilapisi dengan lapisan backing yang impermeable (Koyi dan Arsyad, 2013). Polimer mukoadhesif yang ideal memiliki karakteristik tidak toksik dan dapat diabsorpsi pada saluran cerna, tidak menimbulkan iritasi, cocok jika digunakan setiap hari dan polimer tidak menjadi penghalang untuk pelepasan obat (Vimal et al., 2010). Kelompok polimer yang memiliki sifat mukoadhesif antara lain adalah kelompok polimer hidrofilik. Beberapa kelompok polimer hidrofilik dari polisakarida dan turunannnya seperti hidroksi propil metil selulosa (HPMC) telah digunakan dalam penghantaran mukoadhesif (Roy et al., 2009). Berdasarkan penelitian yang dilakukan oleh Doshi et al., (2011), formulasi film dengan polimer hidroksi propil metil selulosa (HPMC) memiliki sifat bioadhesi yang maksimum dibandingkan dengan film yang mengandung polimer polivinil alkohol (PVA) dan film yang mengandung kombinasi PVA serta polivinil pirolidon (PVP). Selain itu dari penelitian yang dilakukan oleh Lalatendu tahun 2004 menunjukkan bahwa patch Salbutamol sulfat yang mengandung konsentrasi polimer HPMC sebanyak 1,5% memiliki waktu tinggal yang lebih lama, yaitu selama 2,9 ± 0,55 jam jika dibandingkan dengan
patch yang mengandung konsentrasi PVA 10% dengan waktu tinggal 2,20 ± 0,98 jam.
Lapisan backing dibentuk dari polimer yang bersifat impermeable
UIN Syarif Hidayatullah
menghasilkan film yang tidak larut dalam air. Film yang terbentuk memiliki kekuatan tarik yang tinggi dan memberikan aliran zat aktif yang searah dengan sangat baik (Rowe, Paul and Marian, 2009). Etil selulosa telah digunakan sebagai backing membran pada formulasi sediaan bukal film yang mengandung zat aktif Carvedilol. Pada Penelitian tersebut sebagai backing
membran digunakan larutan dengan konsentrasi etil selulosa sebanyak 10 % (w/v) (Viram et al., 2010).
Berdasarkan uraian di atas, maka dalam penelitian ini akan dibuat suatu sediaan lokal yang berupa mukoadhesif patch. Patch yang akan dibuat merupakan patch yang terdiri dari dua lapisan. Lapisan utama yang mengandung zat aktif dalam matriks polimer HPMC dengan penambahan lapisan backing yang terbentuk dari polimer etil selulosa. Selain memformulasikan dalam penelitian ini juga akan dilakukan evaluasi terhadap sifat fisikokimia patch, waktu tinggal patch pada membran gusi sapi dan difusi natrium diklofenak secara in vitro dengan menggunakan Franz diffusion cell.
1. 2. Perumusan Masalah
a. Bagaimana sifat adhesivitas patch yang mengandung polimer HPMC pada membran mukosa gusi?
b. Bagaimana kemampuan difusi natrium diklofenak dari sediaan patch? c. Bagaimana kemampuan polimer etil selulosa (EC) dalam mencegah
difusi zat aktif ke saliva? 1. 3 Hipotesis
a. Lapisan yang terbentuk dari polimer hidroksi propil metil selulosa (HPMC) yang mengandung zat aktif dapat melekat pada lapisan mukosa gusi.
b. Lapisan yang terbentuk dari polimer etil selulosa (EC) dapat menjadi
UIN Syarif Hidayatullah
1. 4 Tujuan
Adapun tujuan dalam penelitian ini adalah untuk memformulasi dan mengkarakterisasi sifat-sifat dari patch natrium diklofenak yang berbasis polimer hidroksi propil metil selulosa (HPMC).
1. 5 Manfaat
5 UIN Syarif Hidayatullah TINJAUAN PUSTAKA
2. 1 Penyakit Periodontal
Jaringan periodontal merupakan bagian dari struktur gigi yang tersusun atas bagian jaringan gigi lunak dan keras (terdiri dari gingiva, sementum, ligamen periodontal) serta tulang alveolar yang berfungsi sebagai penyangga gigi (Houwink et al., 1993).
Kelainan periodontal disebabkan oleh adanya plak pada gigi yang disebabkan oleh adanya bakteri. Penyebab lainnya penyakit periodontal adalah adanya variasi yang luas dari penyakit pada mukosa mulut yang terkadang berdampak pada gingiva (Cawson & Odell, 2002).
Terdapat beberapa tahapan yang penting pada proses terjadinya penyakit periodontal. Yang pertama adalah adanya mekanisme pertahanan yang membentuk inflamasi pada gusi akibat paparan dari plak gigi. Proses peradangan tersebut dikenal dengan gingivitis. Tahap selanjutnya adalah terjadinya kerusakan periodontal, yang menyebabkan hilangnya jaringan penyangga. Apabila kerusakan tersebut tidak ditanggulangi maka tahap selanjutnya adalah hilangnya tulang mandibula, yang mengakibatkan tidak dapat dihindarinya ekstraksi elemen gigi. Klasifikasi penyakit periodontal dibagi atas dua golongan yaitu gingivitis dan periodontitis (Houwink et al., 1993).
Gingivitis merupakan suatu peradangan pada periodonsium, yang terbatas pada daerah gingiva dan dianggap reversibel. Gingivitis dianggap sebagai pertahanan terhadap paparan bakteri yang menyebabkan plak pada gigi. Plak yang terdeposit pada daerah gingiva diakibatkan oleh buruknya kebersihan mulut serta tidak efektifnya proses membersihkan gigi. Proses inflamasi pada peradangan gingiva pada awalnya terjadi di daerah sulkus gingiva dan bagian yang terletak dibawah gingiva (Houwink et al., 1993).
UIN Syarif Hidayatullah
menyikat gigi atau terkadang terjadi perdarahan spontan atau tanpa sebab. Oleh sekelompok besar masyarakat gingiva yang berdarah masih dapat dianggap sebagai proses yang normal dan tidak mengahawatirkan (Houwink et al., 1993). Gejala lainnya adalah terdapatnya perubahan warna pada gingiva. Warna gingiva berubah dengan meningkatnya peradangan, perubahan terjadi dari warna merah muda ke merah tua sampai ungu. Perubahan tersebut diakibatkan oleh adanya dilatasi pembuluh darah dan perubahan pada dinding pembuluh darah yang mengarah pada pengurangan kecepatan aliran darah serta adanya lebih banyak darah pada daerah yang meradang (Houwink et al., 1993). Pembengkakan bentuk gingiva diakibatkan dinding pembuluh darah menjadi lebih permeabel, maka terjadi perubahan keseimbangan osmotik darah dan jaringan interstisial. Perubahan bentuk gingiva terjadi pada stadium lebih lanjut yang diakibatkan oleh pembentukan jaringan granulasi, yang mengandung banyak fibroblas, pembuluh darah dan sedikit serabut kolagen. Pada gingivitis juga terkadang disertai dengan rasa nyeri (Houwink et al., 1993). Gingiva yang mengalami peradangan dapat kehilangan fungsinya, peradangan yang menyebabkan epitel menjadi lebih permeabel dan tidak dapat lagi menjadi penghalang (barier) terhadap pengaruh zat asing yang berasal dari rongga mulut (Houwink et al., 1993).
Periodontitis merupakan proses peradangan di dalam periodonsium dimana sudah ada yang hilang dari bagian-bagian yang menghubungkan serat antara elemen gigi dan jaringan sekelilingnya, pada periodontitis juga dapat mengebabkan hilangnya tulang alveolar (Houwink et al., 1993). Periodontitis merupakan salah satu penyebab utama lepasnya gigi pada dewasa dan merupakan penyebab utama lepasnya gigi pada lanjut usia. Periodontitis terjadi jika gingivitis menyebar ke struktur penyangga gigi (Cawson & Odell, 2002).
UIN Syarif Hidayatullah
tidak enak (kadang-kadang disertai dengan pemebentukan nanah) (Houwink et al., 1993).
2. 2 Natrium Diklofenak
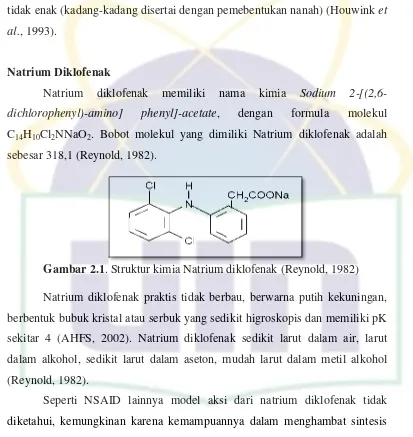
Natrium diklofenak memiliki nama kimia Sodium 2-[(2,6-dichlorophenyl)-amino] phenyl]-acetate, dengan formula molekul C14H10Cl2NNaO2. Bobot molekul yang dimiliki Natrium diklofenak adalah
sebesar 318,1 (Reynold, 1982).
Gambar 2.1. Struktur kimia Natrium diklofenak (Reynold, 1982)
Natrium diklofenak praktis tidak berbau, berwarna putih kekuningan, berbentuk bubuk kristal atau serbuk yang sedikit higroskopis dan memiliki pK sekitar 4 (AHFS, 2002). Natrium diklofenak sedikit larut dalam air, larut dalam alkohol, sedikit larut dalam aseton, mudah larut dalam metil alkohol (Reynold, 1982).
Seperti NSAID lainnya model aksi dari natrium diklofenak tidak diketahui, kemungkinan karena kemampuannya dalam menghambat sintesis prostaglandin yang berhubungan dengan efek anti-inflamasi (Reynold, 1982). Diklofenak menghambat sintesis prostaglandin di jaringan, dengan menghambat COX1 dan COX2 (AHFS, 2002).
UIN Syarif Hidayatullah
Diklofenak merupakan turunan asam fenilasetat, diklofenak merupakan golongan analgesik non-narkotik (NSAID). Yang paling banyak digunakan adalah garam natriumnya. Garam natrium diklofenak digunakan untuk penangnan nyeri dan inflamasi di beberapa kondisi, seperti nyeri sendi, rhematoid arthritis, osteoarthritis, natrium diklofenak juga digunakan dalam penanganan nyeri seperti nyeri pada ginjal, gout akut, dysmenorrhoea dan migren (Reynold, 1982).
Dosis lazim Natrium diklofenak yang diberikan secara oral dan rektal sebesar 75 hingga 150 mg sehari. Dalam penanganan nyeri akibat terkilir, 1 plaster yang mengandung 1% natrium diklofenak dan diaplikasikan 1 kali dalam sehari dalam 3 hari sedangkan untuk epiconylitis 1 plaster 2 kali dalam sehari selama 14 hari (Reynold, 1982).
Efek samping yang banyak dilaporkan dari penggunaan diklofenak adalah efek terhadap saluran cerna. Reaksi yang terjadi antara lain nyeri lambung, mual, muntah dan diare. Kadang-kadang dapat menyebabkan juga tukak lambung (peptic ulcer) dan perdarahan pada saluran cerna dapat terjadi. Diklofenak dapat menjadi penyebab tukak lambung kronik, small bowel perforation dan pseudomembranous colitis. Kerusakan ginjal dan hati dapat terjadi pada pasien yang mengkonsumsi diklofenak. Hepatotoksik akibat penggunaan diklofenak dapat diketahui setelah pemberian selama 6 bulan (Reynold, 1982).
UIN Syarif Hidayatullah
kelainan hemostatik, peningkatan insiden perdarahan intrakranial, penutupan prematur duktus arteriosus dan hipertensi paru persisten (Rubin, 1999).
2. 3 Anatomi Mukosa Rongga Mulut
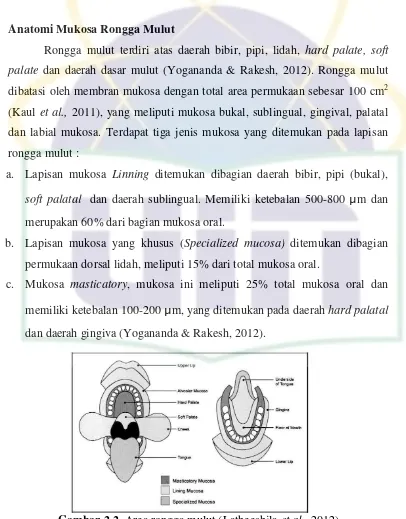
Rongga mulut terdiri atas daerah bibir, pipi, lidah, hard palate, soft palate dan daerah dasar mulut (Yogananda & Rakesh, 2012). Rongga mulut dibatasi oleh membran mukosa dengan total area permukaan sebesar 100 cm2 (Kaul et al., 2011), yang meliputi mukosa bukal, sublingual, gingival, palatal dan labial mukosa. Terdapat tiga jenis mukosa yang ditemukan pada lapisan rongga mulut :
a. Lapisan mukosa Linning ditemukan dibagian daerah bibir, pipi (bukal),
soft palatal dan daerah sublingual. Memiliki ketebalan 500-800 µm dan merupakan 60% dari bagian mukosa oral.
b. Lapisan mukosa yang khusus (Specialized mucosa) ditemukan dibagian permukaan dorsal lidah, meliputi 15% dari total mukosa oral.
c. Mukosa masticatory, mukosa ini meliputi 25% total mukosa oral dan memiliki ketebalan 100-200 µm, yang ditemukan pada daerah hard palatal
dan daerah gingiva (Yogananda & Rakesh, 2012).
Gambar 2.2. Area rongga mulut (Latheeshjla et al., 2012)
UIN Syarif Hidayatullah
Gambar 2.3. Lapisan mukosa mulut (Bhardwaj et al., 2012) Sel epitel, sebagai lapisan pelindung untuk jaringan di bawahnya, dibagi menjadi (a) permukaan non-keratin yang terdapat pada daerah di lapisan mukosa langit-langit lunak, permukaan ventral lidah, dasar mulut, mukosa alveolar, vestibula, bibir dan pipi, dan (b) epitel keratin yang ditemukan di daerah langit-langit keras dan di bagian yang tidak fleksibel dari rongga mulut. Sel-sel epitel, berasal dari sel-sel basal, matang berubah bentuk dan bertambah besar saat bergerak menuju permukaan (Kaul et al., 2012).
Keratin merupakan protein yang berbentuk non filamen dengan ukuran molekul 40 – 70 kDa. Jaringan yang mengandung keratin dan jaringan yang tidak berkeratin meliputi 50% dan 30% dari total luas area di mulut. Perbedaan diantara epitel yang mengandung keratin dan epitel yang tidak mengandung keratin adalah perbedaan ukuran dari keratin. Epitel yang tidak mengandung keratin mengandung protein dengan bobot molekul rendah dibandingkan dengan keratin yang menyusun epitel berkeratin.
UIN Syarif Hidayatullah
Tabel 2.1. Komposisi dan Keberadaan Keratin di Mukosa Mulut
Jaringan Keberadaan keratin Komposisi
Bukal mukosa Non Keratin Sedikit netral, tetapi mengandung lipid polar, terutama kolesterol sulfat dan glukosiceramida
Mukosa Sublingual Non Kerain
Mukosa gusi Keratin Lemak netral seperti
ceramida
Palatal Keratin
Mukus merupakan sekret yang bening dan lengket yang membentuk lapisan tipis, yang berupa lapisan gel yang melekat pada permukaan epitel. Pada manusia ketebalan dari lapisan mukus ini bervariasi antara 50-450 µm. Lapisan mukosa yang terbentuk oleh mukus yang disekresikan oleh lapisan sel goblet atau oleh kelenjar eksokrin khusus dengan mukus sel acini. Komposisi tepat dari lapisan mukus bervariasi tergantung pada spesies, lokasi anatominya serta patofisiologi bagiannya. Secara umum komposisi mukus terdiri dari air dengan konsentrasi 95%, glikoprotein dan lipid sebesar 0,5 – 5%, garam mineral 0,5 – 1% dan protein bebas sebanyak 0,5-1% (Yogananda & Rakesh, 2012). Pada pH fisiologis, lapisan mukus mengandung muatan negatif dikarenakan adanya residu asam sialic dan sulfat dan muatan dengan bobot jenis yang tinggi disebabkan oleh adanya muatan negatif yang berperan pada sifat bioadhesi. Lapisan mukus memiliki beberapa fungsi. Fungsi primer dari lapisan mukus antara lain :
1) Mukus menjadi pelindung karena sifat hidrofobiknya
2) Lapisan mukus berperan sebagai penghalang (barier) dalam proses absorpsi obat dan zat lainnya
3) Mukosa memiliki sifat melekat yang kuat dan dengan kuat terikat pada lapisan permukaan epitel sebagai lapisan gel
UIN Syarif Hidayatullah
2. 4 Mukoadhesif
Adhesi (pelekatan) didefinisikan sebagai keadaaan suatu permukaan yang berikatan bersama melalui daya antarmuka, yang dapat terjadi akibat daya valensi atau aksi saling mengikat atau bahkan keduanya (Kumar et al.,
2011). Istilah bioadhesi digunakan untuk mendeskripsikan pelekatan antara 2 bahan yang salah satunya merupakan bahan biologis. Dalam sistem penghantaran bioadhesif merujuk kepada pelekatan antara bahan pembantu dalam formulasi dengan jaringan biologis. Istilah mukoadhesif menunjukkan adanya pelekatan polimer pada permukaan mukosa (Roy et al., 2009). Sistem penghantaran obat dengan mukoadhesif memanfaatkan polimer yang larut dalam air serta dapat melekat. Oleh karena itu dapat digunakan untuk menetapkan sasaran obat pada suatu daerah tertentu di tubuh untuk periode waktu yang lebih lama (Kumar et al., 2011).
Agar adhesi (pelekatan) dapat terjadi molekul harus dapat melekat pada suatu permukaan dengan ikatan tertentu. Ikatan yang dapat terjadi antara lain adalah ikatan ionik, ikatan kovalen, ikatan hidrogen, ikatan Vander Wall, ikatan hidrofobik, ikatan yang membentuk jembatan disulfida, daya hidrasi, daya elektrostatik dan daya sterik (Kumar et al., 2011).
UIN Syarif Hidayatullah
Gambar 2.4. Tahap proses mukoadhesi (Kaul et al., 2011)
Karena mekanisme mukoadhesif itu termasuk rumit, maka proses mukoadhesif tidak dapat dijelaskan oleh satu teori saja (Kaul et al., 2011). Terdapat berbagai teori mengenai adhesi (pelekatan) yang digunakan untuk menjelaskan proses mukoadhesif. Teori teori tersebut antara lain :
1.Teori adsorpsi
Teori ini menjelaskan, setelah terjadi kontak antara dua permukaan, bahan akan melekat disebabkan adanya daya permukaan. Ada dua jenis ikatan kimia yang berperan. Yang pertama adalah ikatan kovalen yang tidak diinginkan dalam proses bioadhesi karena ikatan tersebut memiliki daya lekat yang kuat yang dapat menghasilkan ikatan yang permanen. Ikatan yang kedua adalah ikatan kimia yang memiliki gaya tarik menarik yang berbeda, meliputi gaya elektrostatik, gaya Vander Wall, ikatan hidrogen dan ikatan hidrofobik (Kumar et al., 2011).
2.Teori difusi
Berdasarkan teori ini, rantai polimer dengan mukus akan bercampur dengan kedalaman yang cukup untuk membentuk suatu ikatan semi-permanen. Kedalaman penetrasi keduanya tergantung pada koefisien difusi dan lamanya waktu kontak. Koefisien difusi tergantung pada bobot jenis antara cross-links (Kumar et al., 2011).
3.Teori elektronik
UIN Syarif Hidayatullah
bioadhesif. Transfer elektron terjadi antara dua buah pembentukan lapisan ganda dari muatan elektron pada permukaan (Kumar et al., 2011).
4.Teori mekanik
Berdasarkan teori ini, pelakatan muncul akibat saling mengikat dari suatu cairan pelekat ke bagian yang tidak teratur pada permukaan kasar pada substrat. Difusi tersebut akan membentuk suatu ikatan bersama pada struktur yang memberikan peningkatan pelekatan (Kumar et al., 2011). 5.Teori pembasahan (Wetting teori)
Teori ini menjelaskan bahwa kemampuan melekat dan kontak dari suatu bahan dijelaskan oleh kemampuan suatu cairan atau pasta tersebar dalam sistem biologis. Selain itu teori pembasahan juga menyatakan jika sudut kontak cairan pada permukaan substrat lebih rendah, maka ada afinitas yang lebih besar bagi cairan ke permukaan substrat. Jika dua permukaan substrat tersebut berkontak satu sama lain dengan adanya cairan, cairan dapat bertindak sebagai perekat antara permukaan substrat (Kumar et al.,
2011).
Berdasarkan teori-teori tersebut, proses bioadhesi secara luas dapat diklasifikasikan menjadi dua katagori. Katagori pertama yaitu proses kimia yang meliputi teori elektronik dan teori adsopsi, katagori kedua adalah proses fisika yang meliputi teori pembasahan dan teori difusi (Roy et al., 2009).
Terdapat beberapa faktor yang mempengaruhi kekuatan mukoadhesi, antara lain polimer, lingkungan yang mempengaruhi dan perubahan fisiologis (Vimal et al., 2010).
1. Polimer dan faktor yang mempengaruhinya meliputi bobot molekul polimer, konsentrasi polimer aktif, fleksibilitas dari rantai polimer serta konformasi ruang dari polimer (Vimal et al., 2010).
UIN Syarif Hidayatullah
dapat meningkat dengan meningkatnya bobot molekul dari suatu polimer (Vimal et al., 2010).
b. Konsentrasi polimer yang digunakan juga mempengaruhi sifat bioadhesif dari suatu bahan. Terdapat konsentrasi optimum dari penggunaan polimer bioadhesif untuk menghasilkan sifat bioadhesi yang maksimal. Dalam sistem dengan konsentrasi polimer yang tinggi, yang melampaui batas optimal, kekuatan adhesinya akan berkurang secara signifikan dikarenakan molekul yang tergulung menjadi terpisah dari medium sehingga rantai yang tersedia untuk saling berpenetrasi menjadi terbatas (Vimal et al., 2010).
c. Sifat fleksibilitas dari rantai polimer. Sifat fleksibilitas sangat diperlukan dalam proses saling berpenetrasi serta membentuk gulungan. Polimer yang larut dalam air membentuk ikatan silang, gerakan dari masing-masing rantai polimer berkurang dan menurunkan lengan efektif yang dapat berpenetrasi ke dalam lapisan mukus, sehingga dapat mengurangi kekuatan bioadhesifnya (Vimal
et al., 2010).
d. Selain bobot molekul dan panjang rantai dari polimer, konformasi ruang dari polimer juga penting. Walaupun memuliki bobot molekul yang besar contohnya dextran (BM 19.500.000) memiliki kekuatan adhesif yang sama dengan polietilen glikol (PEG) dengan bobot molekul 200.000. Konformasi heliks dari dextran dapat melindungi gugus aktif yang bertanggung jawab terhadap sifat adhesinya, tidak seperti dextran, PEG memiliki konformasi linier (Vimal et al., 2010). 2. Faktor lainnya adalah faktor lingkungan, seperti tempat pelekatan, pH,
waktu kontak serta derajat pengembangan (Vimal et al., 2010).
UIN Syarif Hidayatullah
mukoadhesif walaupun polimer tersebut tidak memiliki interaksi yang menarik dengan mukus (Vimal et al., 2010).
b. pH dapat mempengaruhi muatan di permukaan mukus, seperti yang telah diketahui beberapa polimer bioadhesi terionisasi pada lapisan tersebut. Mukus akan memiliki perbedaan muatan tergantung pada pH karena adanya pemisahan dari gugus fungsi pada karbohidrat dan asam amino dari rantai polipeptida (Vimal et al., 2010).
c. Waktu kontak antara materi bioadhesi dan lapisan mukosa menentukan derajat pengembangan dan saling penetrasi dari rantai bioadhesif. Selain itu, kekuatan bioadhesi meningkat dengan peningkatan waktu kontak awal (Vimal et al., 2010).
d. Derajat pengembangan, tergantung pada konsentrasi polimer, konsentrasi ion serta keberadaan air (Vimal et al., 2010).
3. Perubahan fisiologis yang terdiri dari perubahan mucin serta suatu penyakit. a. Perubahan mucin secara normal sangat penting karena dua alasan. Yang
pertama, perubahan mucin mengharapkan batasan pelekatan dari bahan mukoadhesif pada lapisan mukus. Walaupun kekuatan adhesi yang besar dari bahan bioadhesi, bahan tersebut dapat terlepas akibat perubahan mucin. Alasan yang kedua, perubahan mucin menghasilkan senyawa antara yang larut dalam molekul mucin. Molekul tersebut berinteraksi dengan bahan mukoadhesi sebelum memberi kesempatan untuk berinteraksi dengan lapisan mukosa. Perubahan mucin
bergantung pada faktor lain seperti makanan (Vimal et al., 2010). b. Fisikokimia dari mukus dipengaruhi oleh berbagai kondisi yang
diakibatkan suatu penyakit, seperti flu, tukak lambung, infeksi bakteri dan jamur pada saluran reproduksi wanita (Vimal et al., 2010).
UIN Syarif Hidayatullah
optimal yang memungkinkan untuk saling adsorpsi dan saling berpenetrasi antara polimer dan mukus (Vimal et al., 2010).
Polimer mukoadhesif yang melekat pada permukaan epitel mucin
secara luas dapat dibagi menjadi 3 kelas, yaitu :
a. Polimer yang menjadi lengket ketika berkontak dengan air dan memperlihatkan sifat bioadhesivitasnya.
b. Polimer yang melekat secara tidak spesifik, melalui interaksi non kovalen terutama ikatan elektrostatik (seperti, ikatan hidrogen dan ikatan hidrofobik).
c. Polimer yang berikatan secara spesifik dengan reseptor di permukaan (Vimal et al., 2010).
Polimer mukoadhesif yang ideal memiliki karakteristik berikut ini (Vimal et al., 2010) :
a. Polimer dan produk degradasinya harus tidak toksik dan dapat diabsorpsi pada saluran cerna.
b. Tidak iritasi terhadap membran mukosa.
c. Membentuk ikatan yang non kovalen dengan sel epitel permukaan mucin. d. Cepat melekat di jaringan dan memiliki lokasi yang spesifik.
e. Polimer tidak rusak dalam penyimpanan selama waktu tertentu. f. Harganya tidak mahal.
g. Cocok jika digunakan setiap hari dan polimer tidak menjadi penghalang untuk pelepasan obat (Vimal et al., 2010).
2. 5 Patch
UIN Syarif Hidayatullah
dibandingkan dengan sediaan gel atau salep (Shravan et al., 2012). Tipe patch
ada 2 jenis antara lain : 1. Tipe matriks
Patch dengan tipe matriks dirancang agar zat aktif, polimer dan bahan tambahan lainnya dicampur bersama.
2. Tipe reservoir
Patch dengan tipe ini dirancang dalam sistem reservoir yang mengandung lubang untuk zat aktif dan bahan tambahan lainnya agar terpisah dari lapisan adhesif. Backing yang impermeable digunakan untuk mengontrol arah pelepasan zat aktif (Shravan et al., 2012).
Patch terdiri dari beberapa komponen antara lain : 1. Bahan aktif.
Obat yang mengalami first pass effect serta obat bagi pasien dengan kondisi khusus merupakan kandidat terbaik untuk dibuat dalam sediaan
patch. Zat aktif dapat ditambahkan sebesar 5-25% w/w dari bobot total polimer (Yogananda & Rakesh, 2012).
2. Polimer (lapisan adhesif)
Polimer mukoadhesif digunakan untuk menghantarkan zat aktif ke tempat spesifik dan untuk mengoptimalkan penghantaran obat dikarenakan adanya kontak yang lebih lama. Polimer pada lapisan ini akan berkontak dengan mukosa yang merupakan faktor penting dalam keberhasilan penghantaran obat (Yogananda & Rakesh, 2012).
3. Lapisan Backing
Polimer yang bersifat impermeable dengan air dapat digunakan untuk membentuk lapisan backing pada patch. Lapisan backing ini harus memiliki fleksibilitas yang baik, kakuatan tarik yang tinggi serta permeasi air melewati lapisan ini harus rendah. Fungsi utama dari lapisan backing
UIN Syarif Hidayatullah
4. Plasticizer
Merupakan komponen yang digunakan untuk membentuk film tipis yang halus dan fleksibel dari satu jenis polimer atau campuran polimer. Konsentrasi polimer yang digunakan secara umum berkisar antara 0-20% w/w dari bobot kering polimer. Plasticizer dapat mencegah film pecah, mudah sobek dan mengelupas (Yogananda & Rakesh, 2012).
5. Peningkat Penetrasi
Merupakan senyawa yang dapat membantu meningkatkan penetrasi zat aktif. Bahan yang digunakan harus tidak toksik, inert, tidak menimbulakan iritasi dan tidak menyebabkan alergi (Yogananda & Rakesh, 2012).
Terdapat beberapa metode yang digunakan dalam proses pembuatan mukoadhesif patch, antara lain metode solvent casting, hot melt extruction dan
direct milling (Shravan et al., 2012). 1. Solvent Casting
Film oral lebih sering dibuat dengan metode solvent casting, komponen yang larut dalam pelarut dilarutkan untuk menghasilkan larutan kental yang jernih. Zat aktif dan komponen lainnya dilarutkan dalam sejumlah kecil pelarutnya dan dikombinasikan menjadi larutan bulk. Campuran ini ditambahkan kedalam larutan kental. Udara yang terperangkap dipindahkan dengan vakum. Larutan yang dihasilkan dicetak sebagai film dan dibiarkan mengering, kemudian dipotong-potong menjadi lembaran dengan ukuran yang diinginkan.
2. Hot Melt Extrusion
Hot Melt Extrusion (HME) umum digunakan untuk membuat granul, tablet
UIN Syarif Hidayatullah
minimum, kontrol parameter operasi yang baik, dapat untuk operasi berkelanjutan dan scale up.
3. Direct milling
Dalam metode ini, proses pembuatan dilakukan tanpa menggunakan pelarut. Obat dan bahan tambahan lainnya secara mekanik dicampur dengan menggunakan direct milling atau kneading, biasanya tanpa menggunakan larutan sedikitpun. Setelah dicampur, hasilnya digulung di
release liner hingga mencapai ketebalan yang diinginkkan. Kemudian dilapisi dengan lapisan backing.
2. 6 Hidroksi Propil Metil Selulosa
Hidroksi propil metil selulosa atau dengan nama lain Benecel MHPC; E464; Hidroksi propil metil selulosa; hypermellose; hypromellosum; Methocel;
methyl cellulose propylene glycol ether; methyl hydroxypropylcellulose;
Metolose; MHPC; Pharmacoat; Tylopur; Tylose MO. Merupakan polimer dengan karakteristik bentuk berupa serbuk granul atau berserat dengan warna putih kecoklatan (krem) dengan tidak memiliki rasa dan bau (Rowe, Paul and Marian, 2009).
Keterangan : R adalah H, CH3 atau CH3CH(OH)CH2
Gambar 2.5 Struktur HPMC (Rowe, Paul and Marian, 2009).
UIN Syarif Hidayatullah
konsentrasi 2% dalam larutan air memiliki pH sebesar 5,0–8,0 (Rowe, Paul and Marian, 2009).
HPMC tidak bercampur dengan beberapa zat pengoksidasi kuat. HPMC merupakan polimer nonionik, sehingga tidak membentuk kompleks dengan garam logam atau ion organik dan membentuk endapan yang tidak terlarut. Larutan HPMC stabil pada pH 3-11 (Rowe, Paul and Marian, 2009).
HPMC digunakan sebagai bahan bioadhesif, pembentuk film, zat penyalut, zat pengontrol pelepasan obat, agen pendispersi, peningkat disolusi, emulgator, stabilizer emulsi, zat peningkat viskositas, pengikat, mukoadhesif dan agen peningkat kelarutan (Rowe, Paul and Marian, 2009).
UIN Syarif Hidayatullah
2. 7 Etil Selulosa (EC)
Etil selulosa merupakan selulosa hasil reaksi antara etil klorida dengan alkali selulosa. Etil selulosa mmemiliki nama kimia Cellulose ethyl ether
[9004-57-3], selain itu Etil selulosa juga memiliki sinomin antara lain
Aquacoat ECD; Aqualon; Ashacel; E462; Ethocel; ethylcellulosum; Surelease. Etil selulosa berfungsi sebagai agen penyalut (coating agent), perasa, pengisi tablet, pengikat tablet dan peningkat viskositas (Rowe, Paul and Marian, 2009).
Gambar 2.6. Struktur Formula Etil selulosa (Rowe, Paul and Marian, 2009)
Etil selulosa berupa bubuk putih, bebas mengalir dan tidak berasa. Etil selulosa praktis tidak larut dalam gliserin, propilen glikol dan air. Etil selulosa yang mengandung kurang dari 46,5% gugus etoksi mudah larut dalam kloroform, metil asetat dan tetrahidrofuran serta campuran hidrokarbon aromatik dengan etanol (95%). Etil selulosa yang mengandung tidak kurang dari 46,5% gugus etoksi mudah larut dalam kloroform, etanol (95%), etil asetat, metanol dan toluen (Rowe, Paul and Marian, 2009). Etil selulosa tidak mengembang dan tidak larut dalam air dikarenakan etil selulosa memiliki kepadatan dan porositas yang merupakan kunci utama dalam pelepasan obat dari bahan yang tidak larut air. Walaupun etil selulosa tidak larut dalam air, etil selulosa dapat menyerap air, dikarenakan ikatan hidrogen antara atom oksigen dan gugus etil pada etil selulosa. Etil selulosa memiliki bobot jenis 0,4 g/cm3 (Rowe, Paul and Marian, 2009).
UIN Syarif Hidayatullah
Viskositas etil selulosa yang diukur pada suhu 250C dengan menggunakan 5% etil selulosa yang dilarutkan dalam campuran 80% toluen dengan 20% etanol (w/w), memiliki viskositas yang berbeda antara 7-100 mPa (7-100 cP) (Rowe, Paul and Marian, 2009).
Etil selulosa yang dilarutkan dalam pelarut organik atau campuran pelarut organik digunakan untuk menghasilkan film yang tidak larut dalam air. Etil selulosa dengan viskositas yang tinggi dapat menghasilkan film yang kuat dan tahan lama. Film etil selulosa dapat dimodifikasi untuk merubah kelarutannya dengan penambahan Hypermellose atau plasticizer (Rowe, Paul and Marian, 2009).
Etil selulosa juga digunakan sebagai backing membran dalam sediaan bukal patch. Membran yang terbentuk memiliki kekuatan tarik yang tinggi dan memberikan aliran zat aktif yang searah dengan sangat baik (Rowe, Paul and Marian, 2009). Etil selulosa telah digunakan sebagai backing membran pada formulasi sediaan bukal film yang mengandung zat aktif Carvedilol. Pada Penelitian tersebut sebagai backing membran digunakan larutan etil selulosa sebanyak 10 % (w/v) yang dilarutkan dalam etanol dan ditambahkan propilen glikol sebagai plasticizer (Viram et al., 2010).
24 UIN Syarif Hidayatullah 3. 1 Alur Penelitian
Evaluasi viskositas
Pembuatan larutan pembentuk patch
Larutan HPMC 1%, 1,5% dan 2%
Pembuatan lapisan HPMC yang mengandung Na diklofenak
Evaluasi Fisik Keragaman Bobot Keseragaman Kandungan Keragaman Ketebalan Organoleptis
Derajat
Pengembangan pH Permukaan
Uji Waktu
Tinggal
Uji kebocoran
backing
Uji Kemampuan
Difusi Zat Aktif
Kesimpulan Pembahasan Analisis Data
Pembuatan lapisan backing
Pembuatan patch bilayer
Larutan etil selulosa
UIN Syarif Hidayatullah
3. 2 Tempat dan Waktu Penelitian
Laboratorium Penelitian 2, Laboratorium Penelitian 1 Prodi Farmasi Fakultas Kedokteran dan Ilmu Kesehatan UIN Syarif Hidayatullah Jakarta, Laboratorium Kesehatan Lingkungan (Kesling) Prodi Kesehatan Masyarakat Fakultas Kedokteran dan Ilmu Kesehatan UIN Syarif Hidayatullah Jakarta. Penelitian berlangsung 5 bulan, dari bulan Maret 2013 hingga Juli 2013.
3. 3 Alat dan Bahan 3. 3.1 Alat
Timbangan analitik (AND GH-202), viskotester HAAKE 6R, pengaduk magnetik (WIGGEn HAUSER), mikrometer digital (Mitutoyo, Jepang), cetakan film, mikroskop optik (Olympus IX 71, Jepang), disintegrator (Electrolab ED-2L), desikator, oven (Eyela NDO- 400, Jepang), cutter,
gunting, Franz diffusion cell, spuit, vial, spektrofotometer Uv Visible (Hitachi U-2910) dan alat-alat gelas yang sering dipakai di laboratorium. 3. 3.2 Bahan
Na Diklofenak (PT. Indofarma), Hidroksi propil metil selulosa 50 cPs (ShinEtsu, Japan), etil selulosa N100 (Hercules), aquades, gliserin (Brataco, Indonesia), Propilen glikol (Brataco, Indonesia), Etanol 70%, Etanol 95% (Mallincrkrodt, USA), Kloroform (Merck, Indonesia), Natrium hidroksida (Merck, Indonesia), kalium dihidrogen fosfat (Merck, Indonesia), mukosa gingival sapi, cyanoacrylate adhesive, silika, kertas saring dan pH indikator (Merck, Indonesia).
3. 4 Prosedur Kerja 3. 4.1 Formula Patch
Melalui perhitungan, maka tiap 20 gram formula mengandung komponen-komponen seperti yang ada dalam tabel 3.1.
a. Preparasi lapisan HPMC
UIN Syarif Hidayatullah
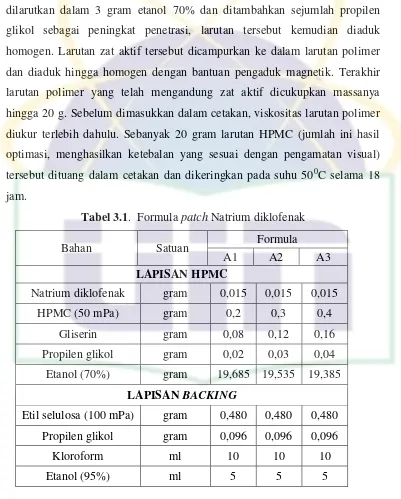
diaduk homogen kembali. Dalam beker terpisah, natrium diklofenak dilarutkan dalam 3 gram etanol 70% dan ditambahkan sejumlah propilen glikol sebagai peningkat penetrasi, larutan tersebut kemudian diaduk homogen. Larutan zat aktif tersebut dicampurkan ke dalam larutan polimer dan diaduk hingga homogen dengan bantuan pengaduk magnetik. Terakhir larutan polimer yang telah mengandung zat aktif dicukupkan massanya hingga 20 g. Sebelum dimasukkan dalam cetakan, viskositas larutan polimer diukur terlebih dahulu. Sebanyak 20 gram larutan HPMC (jumlah ini hasil optimasi, menghasilkan ketebalan yang sesuai dengan pengamatan visual) tersebut dituang dalam cetakan dan dikeringkan pada suhu 500C selama 18 jam.
Tabel 3.1. Formula patch Natrium diklofenak
Bahan Satuan Formula
A1 A2 A3
LAPISAN HPMC
Natrium diklofenak gram 0,015 0,015 0,015
HPMC (50 mPa) gram 0,2 0,3 0,4 Propilen glikol gram 0,096 0,096 0,096
Kloroform ml 10 10 10
Etanol (95%) ml 5 5 5
b. Preparasi Pacth
UIN Syarif Hidayatullah
dalam cetakan yang telah mengandung lapisan HPMC. Kemudian dikeringkan selama 8 jam dalam suhu 400C. Setelah semua lapisan patch
kering, patch dipisahkan dari cetakan. Patch dipotong dengan ukuran 8 x 20 mm2.
3. 4.2 Pembuatan Larutan Buffer Fosfat pH 6,8
Dibuat dengan mencampur sebanyak 250 ml larutan kalium dihidrogen fosfat 0,2 M dengan 112 ml NaOH 0,2 M kemudian dicukupkan volumenya dengan air bebas karbondioksida hingga volumenya 1000 ml.
3. 4.3 Pembuatan Kurva Kalibrasi
a. Penentuan Panjang Gelombang Maksimum (λmaks)
Dilakukan scanning panjang gelombang dari larutan standar natrium diklofenak menggunakan spektrofotometer UV-Visibel dengan panjang gelombang 200-300 nm.
b. Pembuatan Larutan Standar Na Diklofenak
Ditimbang secara akurat 5 mg Na diklofenak kemudian dilarutkan dalam 50 ml buffer fosfat pH 6,8 sehingga diperoleh larutan induk standar sebesar 100 µg/ml. Dari larutan induk tersebut diambil sebanyak 200, 400, 600, 800 dan 1000 µl kemudian dicukupkan volumenya hingga 10 ml, sehingga dihasilkan larutan dengan konsentrasi 2, 4, 6, 8 dan 10 ppm. Masing-masing larutan standar natrium diklofenak diambil dan diukur absorbansi larutan tersebut dengan panjang gelombang 275,5 nm (sesuai hasil scanning sebelumnya).
3. 4.4 Evaluasi Cairan Polimer
UIN Syarif Hidayatullah
3. 4.5 Evaluasi Patch
3.4.5.1. Organoleptis (Balasubramanian et al., 2012)
Meliputi pengamatan secara mikroskopis dan makroskopis terhadap dari fisik
patch yang dibuat. Meliputi pengamatan warna patch dan tekstur permukaan
patch.
3.4.5.2. Evaluasi Fisik
a. Keragaman bobot (Yogananda & Rakesh, 2012)
Pengujian terhadap keragaman bobot patch dilakukan dengan menimbang 10 buah patch dengan ukuran 8 x 20 mm2 secara acak dari setiap batch kemudian dihitung massa rata-ratanya dan dibandingkan dengan massa patch
satu per satu kemudian dihitung simpangan bakunya.
b. Keseragaman kandungan (Doshi, 2011 dan Yogananda & Rakesh, 2012) Diambil patch dari masing-masing formula dengan ukuran 8 x 20 mm2 kemudian dilarutkan dalam 42,5 ml buffer fosfat pH 6,8 dan diaduk dengan menggunakan magnetik stirer selama 2 jam. Larutan tersebut kemudian ditambahkan 7,5 ml etanol 96% dan dilakukan pengadukan kembali hingga 4 jam. Larutan kemudian disaring dan dianalisis dengan menggunakan spektrofotometer Uv-Vis dengan panjang gelombang 275,5 nm. Dengan blangko yang mengandung patch tanpa zat aktif yang telah dilarutkan dalam campuran buffer fosfat pH 6,8 dan etanol 96% dengan perbandingan 85:15. c. Keragaman ketebalan (Yogananda & Rakesh, 2012)
Ketebalan patch diukur dengan mikrometer di tiga titik pada masing-masing
patch, dan kemudian dihitung rata-rata ketebalannya. Ketebalan patch
dinyatakan dalam satuan mikrometer (µm).
3.4.5.3. Uji Pelipatan (Bindu et al., 2010)
UIN Syarif Hidayatullah
3.4.5.3. Pengukuran pH Permukaan (Yogananda & Rakesh, 2012)
Diambil patch secara acak, patch dimasukkan ke dalam wadah yang telah berisi 0,5 ml aquades (pH 6) selama 120 menit dalam temperatur ruang dan pH permukaan patch diukur dengan menggunakan pH indikator.
3.4.5.4. Uji Pengembangan (Swelling studies) (Yogananda & Rakesh, 2012)
Pengembangan patch diukur dengan menempatkan patch dari masing-masing formula dengan ukuran 1 x 2 cm2 ke dalam beaker glass yang mengandung 20 ml larutan buffer fosfat pH 6,8. Bobot patch ditimbang setiap 5 menit, sebelum ditimbang patch dikeringkan terlebih dahulu dengan tissue.
Penimbangan dilakukan hingga menit ke 30. Derajat pengembangan dihitung dengan menggunakan persamaan :
Keterangan : w1 = bobot sebelum (gram), w2 = bobot setelah berkontak dengan larutan buffer (gram).
3.4.5.6. Uji Waktu Tinggal ( in vitro residence time) (Chinna Reddy et al., 2011) Uji waktu tinggal patch dengan menggunakan modifikasi disintegrator USP. Menggunakan 800 ml larutan buffer fosfat pH 6,8 yang dipertahankan suhunya pada 370C sebagai larutan medium. Mukosa dari gusi sapi segar disiapkan dan direkatkan di atas permukaan kaca dengan bantuan perekat (cyanoacrylate adhesive). Sebelum patch diletakkan di atas mukosa, lapisan mukosa terlebih dahulu dibasahi dengan 50 µl larutan buffer fosfat pH 6,8 dan patch diletakkan di permukaan mukosa dengan sedikit ditekan. Kaca tersebut dimasukkan ke dalam alat disintegrator. Amati waktu yang diperlukan hingga patch terlepas dari permukaan mukosa gusi.
3.4.5.7. Uji Kemampuan Penetrasi Zat Aktif (Koyi dan Arshad, 2012)
Menggunakan Franz diffusion cell pada suhu 370C ± 0,20C. Mukosa gusi sapi segar diletakkan di antara kompartemen donor dan reseptor. Patch
diletakkan dengan bagian inti menghadap ke arah mukosa. Kompartemen % Derajat pengembangan =
UIN Syarif Hidayatullah
reseptor diisi dengan larutan buffer fosfat pH 6,8 dan diaduk secara konstan dengan kecepatan sedang. Pada interval menit ke 0, 15, 30, 45, 60, 90, 120, 180, 240, 300 dan 360 diambil 1 ml larutan buffer dari kompartemen reseptor dan ditambahkan juga sejumlah larutan buffer dengan volume yang sama. Larutan tersebut diencerkan dengan buffer yang sama kemudian dilakukan analisis dengan menggunakan spektrofotometer dengan panjang gelombang 275,5 nm.
Gambar 3.1. Skema dari Franz Diffusion Cell (Koyi dan Arshad, 2012)
3.4.5.7. Uji Kebocoran Backing
31 UIN Syarif Hidayatullah HASIL DAN PEMBAHASAN
4. 1 Karakteristik Cairan Polimer
Polimer utama yang digunakan dalam penelitian ini adalah HPMC, proses pembentukan larutan polimer dilakukan dengan melarutkan HPMC dengan berbagai konsentrasi sesuai formula ke dalam etanol 70%. Pemilihan etanol 70% disebabkan polimer HPMC praktis tidak larut dalam etanol 96% tetapi dapat larut dalam campuran air dan alkohol (Rowe, Paul and Marian, 2009). Penggunaan etanol sebagai pelarut dalam pembuatan larutan polimer HPMC sebagai larutan pembentuk film juga telah dilakukan pada formulasi film natrium diklofenak sebagai sediaan mukoadhesif bukal (Balasubramanian et al., 2012).
Pengamatan secara visual terhadap organoleptis cairan polimer pembentuk lapisan HPMC menunjukkan bahwa semua larutan polimer dengan konsentrasi yang berbeda memiliki kesamaan warna, semua formula memberikan warna larutan yang jernih. Selain dari pengamatan visual, dilakukan juga pengamatan pengaruh perbedaan konsentrasi polimer dari ketiga formula terhadap viskositas larutan. Larutan polimer yang dibentuk memiliki perbedaan viskositas. Hasil pengukuran viskositas larutan polimer tersebut dapat dilihat pada tabel 4.1.
Tabel 4.1. Viskositas larutan polimer Formula Viskositas (cPs)
A1 30
A2 44
A3 60
UIN Syarif Hidayatullah
4. 2 Karakteristik Fisikokimia Patch
Patch yang dibuat terdiri dari dua lapisan, lapisan utama merupakan lapisan yang mengandung polimer adhesif dan natrium diklofenak sedangkan lapisan kedua adalah lapisan backing yang berfungsi untuk menahan difusi natrium diklofenak ke saliva serta untuk memberikan arah difusi zat aktif yang searah. Patch dibuat dengan metode solven casting, metode ini memiliki kelebihan pengerjaannya mudah dilakukan. Beberapa penelitian sebelumnya yang memformulasikan patch untuk sediaan oral juga menggunakan metode solven casting, beberapa penelitian tersebut diataranya penelitian yang dilakukan oleh Balasubramanian et al., tahun 2012 yang memformulasikan sediaan film bukal dengan zat aktif natrium diklofenak.
Secara visual patch dengan formula A1, A2, A3 dan blangko memiliki bentuk yang penampilan yang serupa. Semua patch berwarna jernih. Seperti yang dilihat pada gambar 4.1.
A1
A2
A3
UIN Syarif Hidayatullah
Patch yang terbentuk tidak terlihat adanya pemisahan antara lapisan adhesif yang mengandung polimer HPMC dengan lapisan backing yang mengandung polimer etil selulosa. Pada proses pembentukan patch bilayer
lapisan HPMC yang telah terbentuk ditambahkan larutan polimer etil selulosa. Penggabungan ini tidak menyebabkan adanya perubahan bentuk dari lapisan HPMC. Proses pengeringan dilakukan pada suhu 400C selama 8 jam. Pada percobaan pendahuluan pemanasan dilakukan hingga lapisan etil selulosa kering yaitu membutuhkan waktu selama 6 jam, tetapi lapisan kedua polimer tersebut tidak saling bersatu. Hal tersebut dapat dilihat pada gambar 4.2 yang menunjukkan penampakan patch secara mikroskopis dengan perbesaran 100 kali.
A B
Gambar 4.2. Organoleptis patch. A = patch bilayer yang dikeringkan selama 6 jam (mengalami pemisahan). B = Patch bilayer yang dikeringkan selama 8 jam (tidak mengalami pemisahan).
Patch yang terbentuk agak kaku, terutama pada lapisan baking. Untuk mengetahui hal tersebut dilakukan uji pelipatan pada patch, patch
dilipat pada lokasi yang sama hingga patch robek. Hasil uji pelipatan jika diambil rata-ratanya menunjukkan bahwa lapisan backing memiliki ketahanan terhadap pelipatan hingga lipatan ke-25, sedangkan lapisan HPMC tidak mengalami kerusakan hingga pelipatan ke-300. Penambahan gliserin sebagai plasticizer sebanyak 40% untuk lapisan HPMC mampu membentuk lapisan polimer yang tidak mudah sobek. Hasil uji pelipatan dapat dilihat pada tabel 4.2.
UIN Syarif Hidayatullah
Tabel 4.2. Uji pelipatan patch
Formula Lapisan HPMC Lapisan Backing
A1 > 300 22
A2 > 300 25
A3 > 300 27
Untuk memastikan sediaan patch yang terbentuk memiliki organoleptis yang serupa dilakukan pengamatan organoleptis secara mikroskopis. Pengamatan secara mikroskopis juga bertujuan untuk mengetahui apakah natrium diklofenak dalam sediaan tersebut tidak mengalami rekristalisasi. Hasil pengamatan secara mikroskopis menunjukkan bahwa patch yang mengandung natrium diklofenak sebagai zat aktif dengan
patch yang tidak mengandung zat aktif memiliki penampak yang sama di bawah mikroskop. Hasil pengamatan di bawah lensa mikroskop dengan perbesaran 100x menunjukkan bahwa natrium diklofenak yang telah dilarutkan terlebih dahulu dalam etanol dan kemudian ditambahkan pada larutan yang telah mengandung polimer dan plasticizer yang kemudian dilakukan proses pengeringan tidak mengalami rekristalisasi. Natrium diklofenak pada masing-masing formula terdispersi secara molekuler dalam larutan polimer HPMC sehingga hasil pengamatan secara mikroskopis tidak menunjukkan adanya partikel dari natrium diklofenak. Hasil pengamatan secara mikroskopis tersebut dapat dilihat pada gambar. 4.3.
UIN Syarif Hidayatullah
A1
A2
A3
Blangko
Na diklofenak
Gambar 4.3. Penampakan mikroskopis patch. Kiri = gambar mikroskopis bagian permukaan patch. Kanan = gambar mikroskopis penampang melintang.
Tabel 4.3. Sifat fisikokimia patch
Formula Bobot (mg) Ketebalan
(µm)
Kandungan Zat Aktif (µg)
A1 10 ± 1 70 ± 1 814 ± 17
A2 17 ± 0 102 ± 1 851 ± 11
UIN Syarif Hidayatullah
Dari hasil pengamatan diketahui bahwa patch yang dihasilkan memiliki bobot dan ketebalan yang cukup seragam yang dilihat dari simpangan baku yang diperoleh. Peningkatan jumlah polimer pada formula secara langsung menyebabkan peningkatan bobot dan ketebalan patch yang dibentuk. Bobot patch paling rendah diperoleh dari bobot formula A1 dengan konsentrasi larutan polimer HPMC terendah yaitu 1%, sedangkan bobot
patch terberat adalah patch dengan formula A3 yang mengandung konsentrasi larutan polimer HPMC terbanyak yaitu 2%.
Gambar 4.4. Grafik keragaman bobot
Begitu juga ketebalannya, ketebalan maksimal dihasilkan patch
dengan konsentrasi larutan polimer terbesar yaitu 2% sedangkan patch
dengan ketebalan minimal dihasilkan oleh formula A1 yang mengandung konsentrasi larutan polimer terendah yaitu 1%.
UIN Syarif Hidayatullah
Hal ini sesuai dengan beberapa penelitian sebelumnya seperti yang telah dilakukan oleh Hamabindu tahun 2012. Dari penelitiannya diketahui bahwa peningkatan konsentrasi polimer HPMC pada formulasi patch yang mengandung Cyproheptadine Hydrochloride menunjukkan adanya peningkatan bobot dan ketebalan dari patch yang terbentuk (Himabindu, 2012). Adanya keseragaman bobot dan ketebalan pada patch yang dibuat diharapkan memberikan distribusi zat aktif yang seragam, karena zat aktif yang ditambahkan pada proses preparasi patch sudah dalam bentuk terdispersi secara molekuler dalam etanol, sehingga keseragaman distribusi zat aktif pada sediaan dipengaruhi oleh ketebalan patch. Pengujian kandungan zat aktif dalam sediaan menunjukkan bahwa jumlah zat aktif dalam sediaan patch yang dibuat sekitar 800-851 µg. Pengujian kandungan zat aktif menggunakan medium campuran antara buffer posfat pH 6,8 – etanol 96% dengan perbandingan 85:15. Penggunaan campuran etanol ini bertujuan untuk meningkatkan kelarutan natrium diklofenak dalam medium air, karena natrium diklofenak memiliki karakteristik agak sukar larut dalam air. Sebelum dilakukan pengujian kandungan natrium diklofenak dalam sediaan patch yang berukuran 8 x 20 mm2 dilakukan pengujian terhadap perolehan kembali dari natrium diklofenak dalam 1 cetakan. Hasil perolehan kembali diketahui sebesar 91,148 %.
4.3 pH Permukaan Patch
Tabel 4.4. pH permukaan masing-masing formula patch
UIN Syarif Hidayatullah
diharapkan tidak menimbulkan iritasi pada permukaan mukosa gusi sebab pH permukaan sediaan patch berada pada range pH saliva yaitu 5,6-7 (Kaul, Verma, Rawat & Saini, 2011).
4.4 Waktu Tinggal Patch pada Permukaan Gusi Sapi
Pengujian waktu tinggal patch menggunakan membran gusi sapi segar yang diambil dari rumah pemotongan hewan. Pengujian dilakukan menggunakan modifikasi disintegrator USP. Hasil pengujian menunjukkan bahwa semua formula patch dapat melekat pada membran mukosa gusi sapi selama lebih dari 7 jam.
Tabel 4.5. Waktu tinggal patch pada permukaan membran gusi sapi
Formula Waktu Tinggal (jam)
A1 >7
A2 >7
A3 >7
Penambahan polimer HPMC pada formula patch tidak mempengaruhi waktu pelekatan sediaan pada membran mukosa gusi. Jika dibandingkan dengan penelitian yang dilakukan oleh Doshi et al., tahun 2011, waktu tinggal patch yang dibentuk pada penelitian ini memiliki waktu tinggal yang lebih lama pada mukosa gusi. Hasil pengujian waktu tinggal yang telah dilakukan oleh` Doshi et al., tahun 2011, menunjukkan bahwa film diklofenak yang mengandung polimer HPMC sebanyak 1,5% memiliki waktu tinggal yang paling lama sekitar 74 menit dibandingkan dengan film yang mengandung polimer PVA dan kombinasi PVA - PVP. Selain itu penelitian tersebut juga menunjukkan bahwa film yang mengandung HPMC memiliki kekuatan bioadhesif yang paling tinggi. Selain itu dari penelitian yang dilakukan oleh Lalatendu tahun 2004 menunjukkan bahwa patch
UIN Syarif Hidayatullah
4.5 Derajat Pengembangan
Derajat pengembangan polimer merupakan titik kritis dalam menentukan sifat bioadhesif dari polimer tersebut. Pelekatan (adhesi) terjadi dengan cepat ketika pengembangan polimer dimulai tetapi ikatan yang dibentuk bukan ikatan yang kuat (Doshi, Koliyote & Joshi, 2011).
Tabel 4.6. Derajat pengembangan patch dalam medium buffer fosfat pH 6,8
Waktu
Derajat pengembangan dari masing-masing formula patch dapat dilihat pada tabel 4.6. Derajat pengembangan yang diamati pada menit ke-20 menunjukkan bahwa derajat pengembangan terbesar dihasilkan oleh patch
UIN Syarif Hidayatullah
kemampuannya untuk mengembang dengan derajat yang tidak terbatas ketika berkontak dengan air dan dengan cepat akan mengalami disolusi (Vimal., et al, 2010).
Gambar. 4.6. Grafik pengembangan patch dalam medium buffer fosfat pH 6,8
Karakteristik derajat pengembangan ini dapat digunakan untuk meramalkan pelepasan zat aktif dari matriks HPMC. Peningkatan jumlah polimer pada sediaan akan menyebabkan adanya peningkatan penyerapan air ke dalam matriks yang dapat menyebabkan pembentukan lapisan gel pada lapisan yang telah terhidrasi, dengan adanya peningkatan jumlah polimer dalam matriks akan menyebabkan peningkatan ketebalan dari lapisan gel tersebut. Pembentukan lapisan gel ini akan menjadi barier dan dapat menimbulkan penurunan pelepasan zat aktif melalui matriks HPMC (Chandra., et al, 2008).
4.6 Kemampuan Penetrasi Natrium Diklofenak
UIN Syarif Hidayatullah
Tabel 4.7. Persentase kumulatif difusi zat aktif melewati membran gusi sapi
Waktu (s) % Kumulatif Difusi Zat Aktif
A1 A2 A3
Tabel 4.8. Jumlah kumulatif zat aktif yang terdifusi melewati membran gusi sapi
Waktu (s) Kumulatif Difusi Zat Aktif (µg)
A1 A2 A3
UIN Syarif Hidayatullah
Gambar 4.7. Grafik persentase difusi zat aktif melalui membran gusi sapi dari masing-masing formula
Gambar 4.8. Grafik jumlah difusi zat aktif melalui membran gusi sapi dari masing-masing formula
UIN Syarif Hidayatullah
Tabel 4.9. Analisis statistik Kruskal-Wallis test dari data persentase difusi natrium diklofenak
difusi
Chi-Square 17.171
df 2
Asymp. Sig. .000
Tabel 4.10. Statistik persentase difusi natrium diklofenak
(I)
*. The mean difference is significant at the 0.05 level.
Dari hasil pengolahan data menggunakan statistik menunjukkan bahwa hasil uji difusi natrium diklofenak dari masing-masing formula menunjukkan adanya perbedaan yang signifikan yang dapat diamati dari nilai signifikansi yang dihasilkan pada pengujian. Persentase difusi natrium diklofenak dari formula A2 dan A3 menunjukkan adanya perbedaan tetapi perbedaan yang dihasilkan tidak signifikan.
UIN Syarif Hidayatullah
formula A1 yang mengandung konsentrasi larutan polimer terendah yaitu 1% diikuti oleh A3 yang mengandung konsentrasi larutan polimer 2% dan nilai fluks terkecil ditunjukkan oleh formula A2 yang mengandung konsentrasi larutan HPMC 1,5%. Tingginya nilai fluks natrium diklofenak pada formula A3 dibandingkan dengan formula A2 disebabkan adanya perbedaan ketebalan membran yang digunakan, ketebalan membran yang digunakan pada formula A2 lebih tebal dibandingkan dengan membran yang digunakan pada pengujian formula lainnya. Pengaruh perbedaan ketebalan membran gusi yang digunakan terhadap laju difusi zat aktif dari masing-masing formula dapat dilihat pada tabel 4.11.
Tabel 4.11. Fluks natrium diklofenak dari masing-masing formula
Formula Ketebalan (mm) Fluks (µgcm-2jam-1) A1 1,78 ± 0,02 28,917 ± 0,094 A2 2,16 ± 0,01 18,468 ± 0,340 A3 1,88 ± 0,00 19,746 ± 0,869
Gambar 4.9. Fluks natrium diklofenak
UIN Syarif Hidayatullah
Tabel 4.12. Pengolahan data fluks secara statistik menggunakan ANOVA
Tabel 4.13. Statistik fluks natrium diklofenak
4. 7 Kebocoran Backing Membran
Untuk meningkatkan jumlah natrium diklofenak yang difusi melalui membran gusi maka sediaan patch diberikan suatu lapisan backing. Lapisan
backing ini tidak hanya berfungsi untuk menghambat difusi natrium diklofenak ke arah rongga mulut sehingga dapat masuk ke saluran pencernaan fungsi lain dari lapisan backing ini untuk mengoptimalkan difusi natrium diklofenak dengan cara memberikan difusi yang searah (Yogananda & Rakesh, 2012).