ANALISIS KOMPONEN KIMIA FRAKSI MINYAK ATSIRI
DAUN SIRIH (Piper bettle Linn.) DAN UJI AKTIVITAS
ANTIBAKTERI TERHADAP BEBERAPA JENIS BAKTERI
GRAM POSITIF
SKRIPSI
Diajukan sebagai salah satu syarat untuk memperoleh gelar sarjana farmasi
Oleh :
FEBRIYATI
NIM : 106102003404
PROGRAM STUDY FARMASI
FAKULTAS KEDOKTERAN DAN ILMU KESEHATAN
UNIVERSITAS ISLAM NEGERI SYARIF HIDAYATULLAH
LEMBAR PERSETUJUAN SKRIPSI
NAMA : FEBRIYATI
NIM : 106102003404
JUDUL : ANALISIS KOMPONEN KIMIA FRAKSI MINYAK ATSIRI
DAUN SIRIH (Piper betle Linn.) DAN UJI AKTIVITAS
ANTIBAKTERI TERHADAP BEBERAPA JENIS BAKTERI
GRAM POSITIF
Disetujui oleh :
Pembimbing I Pembimbing II
Dr. Andria Agusta Drs. M. Yanis Musdja, M.Sc, Apt.
NIP. 196908161994031003 NIP.195601061985101001
Mengetahui,
Ketua Program Studi Farmasi
Fakultas Kedokteran dan Ilmu Kesehatan
Universitas Islam Negeri Syarif Hidayatullah Jakarta
Drs. M. Yanis Musdja, M.Sc, Apt.
LEMBAR PENGESAHAN SKRIPSI
Skripsi dengan judul
ANALISIS KOMPONEN KIMIA FRAKSI MINYAK ATSIRI DAUN SIRIH (Piper betle Linn.) DAN UJI AKTIVITAS ANTIBAKTERI TERHADAP
BEBERAPA JENIS BAKTERI GRAM POSITIF
Telah disetujui, diperiksa dan dipertahankan dihadapan tim penguji oleh :
LEMBAR PERNYATAAN
Dengan ini saya menyatakan bahwa skripsi yang berjudul :
ANALISIS KOMPONEN KIMIA FRAKSI MINYAK ATSIRI DAUN SIRIH
(Piper bettle Linn.) DAN UJI AKTIVITAS ANTIBAKTERI TERHADAP
BEBERAPA JENIS BAKTERI GRAM POSITIF
Adalah karya saya sendiri dan belum pernah diajukan dalam bentuk apapun kepada perguruan tinggi manapun. Sumber informasi yang berasal atau dikutip dari karya yang diterbitkan maupun yang tidak diterbitkan dari penulis lain telah disebutkan dalam teks dan dicantumkan dalam daftar pustaka.
Penulis,
KATA PENGANTAR
Alhamdulillah, puji dan syukur kehadirat Allah SWT yang telah melimpahkan rahmat dan karunia-Nya serta shalawat dan salam selalu tercurah kepada junjungan kita Nabi Muhammad SAW karena dengan segala rahmat dan karunia-Nya penulis dapat menyelesaikan penelitian dan penulisan skripsi dengan
judul “ANALISIS KOMPONEN KIMIA FRAKSI MINYAK ATSIRI DAUN
SIRIH (Piper bettle Linn.) DAN UJI AKTIVITAS ANTIBAKTERI
TERHADAP BEBERAPA JENIS BAKTERI GRAM POSITIF”. Skripsi ini
disusun untuk memenuhi tugas akhir sebagai salah satu syarat untuk memperoleh gelar Sarjana Farmasi pada Fakultas Kedokteran dan Ilmu Kesehatan Program Studi Farmasi Universutas Islam Negeri Syarif Hidayatullah, Jakarta.
Pada kesempatan ini perkenankanlah penulis menyampaikan ucapan terima kasih yang sebesar-besarnya serta setulus-tulusnya kepada:
1. Bapak Prof. Dr. Komarudin Hidayat, selaku Rektor Universitas Islam Negeri
Syarif Hidayatullah Jakarta.
2. Bapak Prof. Dr (hc) dr. M. K. Tadjudin Sp,And, selaku Dekan Fakultas
Kedokteran dan Ilmu Kesehatan Universitas Islam Negeri Syarif Hidayatullah Jakarta.
3. Bapak Dr. Andria Agusta dan Bapak Drs. M. Yanis Musdja, Msc., Apt,
sebagai pembimbing yang baik dan dengan sabar telah memberikan pengarahan, bimbingan, nasehat dan petunjuk selama penelitian dan penyusunan skripsi ini.
4. Bapak dan Ibu dosen yang telah memberikan ilmu dan pengetahuan hingga
penulis dapat menyelesaikan studi di jurusan Farmasi Fakultas Kedokteran dan Ilmu Kesehatan Universitas Islam Negeri Syarif Hidayatullah Jakarta.
5. Kedua orang tua tercinta, Ayahanda Munawar dan Ibunda Aripah yang selalu
6. Kepada kakanda dan adinda-adindaku tersayang terima kasih atas nasehat, dukungan, serta kasih sayang yang telah kalian berikan, hingga penulis selalu semangat menyelesaikan skripsi ini.
7. Kepada Angayi Hari Suryono, ST dan keluarga yang selalu memberikan
dukungan, motivasi dan inspirasi serta dengan segala kesabarannya tiada henti memberikan semangat dikala penulis merasa bimbang, lelah dan terjatuh dalam menyelesaikan skripsi sehingga penulis dapat bangkit kembali untuk menyelesaikan skripsi.
8. Bapak Prof. Dr. Eko Baroto Walujo, APU, sebagai kepala bidang Botani dari
Herbarium Bogoriense LIPI Cibinong yang telah memberikan kesempatan kepada penulis untuk melakukan penelitian di LIPI Cibinong.
9. Ibu Dr. Praptiwi dan Yuliasri Jamal, Msc, yang senantiasa memberikan
bimbingan dan bantuan dikala penulis mengalami kesulitan selama penelitian dan penyusunan skripsi.
10.Bapak Dedi Rosadi dan Dedi Kustiwa dari balitro yang telah menyediakan
sampel dan melakukan distilasi
11.Saudara Ahmad Futhoni dan kang Asep yang telah memberikan bantuan
selama penelitian.
12.Kepada sahabat-sahabatku tersayang, Aminah Nurhadiyah, Fiestyo Alim,
Erny Fitriana, Rahmania Hidayah dan Nida Nurnabila terima kasih atas dukungan dan doa kalian, masa-masa kuliah bersama kalian tidak akan pernah terlupakan sampai kapanpun.
13.Kepada teman-teman seperjuangan dalam penelitian yang selalu membantu
dan senantiasa menyemangati, Erny Fitriana, Nurul Gustiari, Nuryatni, Vika Fauziah, Mustikaning Ayu, Nurul Farihah, Lidya Pratiwi dan Ulfah Sadiah.
14.Kepada teman-teman Farmasi angkatan 2006, kebersamaan kita didalam suka
dan duka akan selalu terkenang di dalam hati sanubari.
15.Serta semua pihak yang tidak dapat disebutkan satu persatu yang turut
membantu menyelesaikan skripsi ini.
kerendahan hati, penulis berharap semoga hasil penelitian ini dapat bermanfaat baik bagi kalangan akademis, khususnya bagi mahasiswa farmasi, masyarakat pada umumnya dan bagi dunia ilmu pengetahuan.
Jakarta, 25 Agustus 2010
ABSTRAK
ANALISIS KOMPONEN KIMIA FRAKSI MINYAK ATSIRI DAUN SIRIH (Piper bettle Linn.) DAN UJI AKTIVITAS ANTIBAKTERI TERHADAP
BEBERAPA JENIS BAKTERI GRAM POSITIF
Sirih (Piper betle Linn.) merupakan salah satu jenis tanaman dari famili
Piperaceae yang sering digunakan untuk menyirih. Fraksi minyak atsiri daun sirih diperoleh dengan cara destilasi uap air dan difraksinasi berdasarkan perbedaan
waktu penyulingan. Kandungan relatif yang terdapat pada masing – masing fraksi
secara berurutan adalah 0,061%, 0,034%, 0,027% dan 0,015%. Analisis fraksi minyak atsiri dengan GC-MS dari fraksi jam ke 1, 2,4, dan 6 menunjukkan adanya 5 komponen kimia utama yang diduga berperan pada aktivitas antibakteri yaitu kavibetol, kariofilen, pacouli alkohol,fenol,2-metoksi-4(1-profenil)-asetat dan 4-alil-1,2-diasetoksibenzene. Fraksi minyak atsiri daun sirih telah diuji aktivitas antibakteri dan mekanisme penghambatan terhadap beberapa jenis bakteri gram positif. Aktivitas antibakteri minyak atsiri daun sirih menggunakan mikrodilusi menunjukkan bahwa ke-4 fraksi minyak atsiri daun sirih aktif terhadap Staphylococcus epidermidis dan Steptococcus mutan namun tidak menunjukkan
aktivitas terhadap Bacillus subtilis . Nilai MIC pada setiap fraksi terhadap
Staphylococcus epidermidis sebesar 0,25% sedangkan Steptococcus mutan
memilki aktivitas yang paling sensitif terhadap F4 pada nilai MIC 0,25%.
Mekanisme penghambatan pertumbuhan bakteri oleh fraksi minyak atsiri daun sirih terjadi melalui pengerusakan dinding sel mikroba uji setelah perlakuan 1 MIC dan 2 MIC.
Kata kunci : Piper betle, minyak atsiri, fraksi, aktivitas antibakteri, bakteri gram
ABSTRACT
ANALYSIS OF CHEMICAL COMPONENTS OF ESSENTIAL OIL FRACTIONS OF BETLE LEAVES (Piper betle Linn.) AND ANTI-BACTERIAL ACTIVITY TEST AGAINST SOME GRAM POSITIVE
BACTERIA. 4(1-prophenyl)-acetate and 4-allyl-1,2-diacetoxybenzene respectively. All of these main chemical constituents were propose to responsible for its antibacterial activity. The anti-bacterial activity of essential oils of beetle leaves was evaluate
with a microdilluton method. The results showed all of essential oil fractions
tested active against Staphylococcus epidermidis dan Steptococcus mutan but not
active to Bacillus subtilis. The MIC values of Staphylococcus epidermidis for all
of essential oil fractions were 0,25% While Steptococcus mutan were the most
sensitive to fourth fraction by 0.25%. Inhibition mechanism their activity was indicated through microbial cell walls vandalism test after treatment 1 MIC and 2 MIC of the oils.
Key words: Piper betle,,essential oil, fractions, antibacterial activity, gram
2.4. Aktivitas Antibakteri... 10
2.4.1. Aktivitas Antibakteri... 10
2.4.2. Mekanisme Kerja Antibakteri... 11
2.4.3. Metode Pengujian Antibakteri... 13
BAB III KERANGKA KONSEP... 14
BAB IV METODOLOGI PENELITIAN... 15
4.1. Waktu dan Tempat Penelitian... 15
4.2. Pengambilan Sampel... 15
4.3. Determinasi Tanaman... 15
4.4. Alat da Bahan... 15
4.5. Metode Penelitian... 16
4.6. Prosedur kerja 17 4.6.2. Identifikasi Komponen Kimia Fraksi Minyak Atsiri Daun Sirih... 18
4.6.3. Pengujian Aktivitas Antibakteri Fraksi Minyak Atsiri Daun Sirih... 18
4.6.4. Analisis Protein dan Asam Nukleat... 22
4.6.5. Analisis Ion Logam Ca2+ dan K+... 23
4.6.6. Analisis Perubahan Morfologi Sel dengan SEM... 23
BAB V HASIL DAN PEMBAHASAN... 25
5.1. Hasil... 25
5.1.1. Isolasi dan Penentuan Komponen Kimia Fraksi Minyak Atsiri Daun Sirih ... 25
5.1.2. Pengujian Aktivitas Antibakter i Fraksi Minyak Atsiri Daun Sirih... 29
5.1.4. Analisis Kebocoran Protein dan Asam nukleat... 31
5.1.5. Analisis Ion Logam Ca2+ dan K+... 31
5.2. Pembahasan... 33
BAB VI KESIMPULAN DAN SARAN... 43
6.1. Kesimpulan... 43
6.2. Saran... 44
DAFTAR PUSTAKA... 45
DAFTAR TABEL
Hal
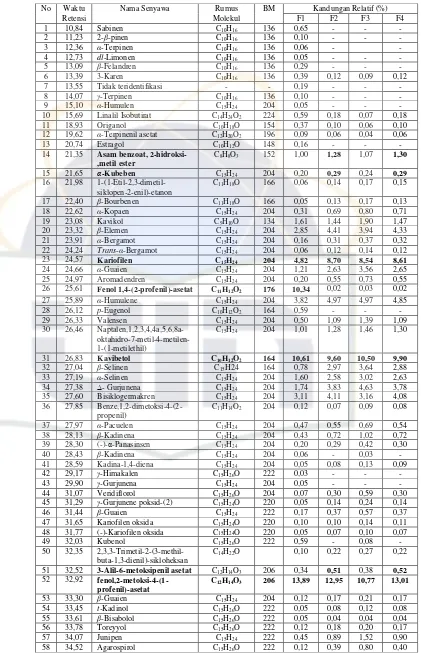
Tabel 1. Perbandingan komponen kimia antar fraksi minyak atsiri
daun Sirih ... 27 Tabel 2. Penggolongan komponen kimia antar fraksi minyak atsiri
daun Sirih ... 28 Tabel 3. Aktivitas fraksi minyak atsiri daun sirih terhadap 3 jenis bakteri
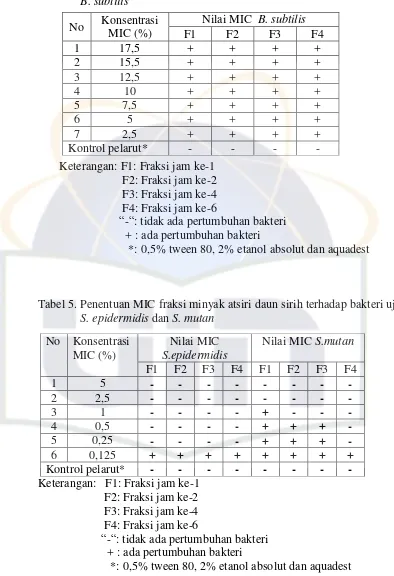
uji gram positif pada konsentrasi 50 %... 29 Tabel 4. Penentuan MIC fraksi minyak atsiri daun sirih terhadap bakteri
uji B. subtilis... 30 Tabel 5. Penentuan MIC fraksi minyak atsiri daun sirih terhadap bakteri uji
DAFTAR GAMBAR
Hal Gambar 1. Daun sirih....... 25 Gambar 2. Perbandingan komatogram antar fraksi minyak atsiri daun sirih... 30 Gambar 3. Nilai absorbansi asam nukleat dan protein fraksi jam ke-1
pada sel S. epidermidis...... 31
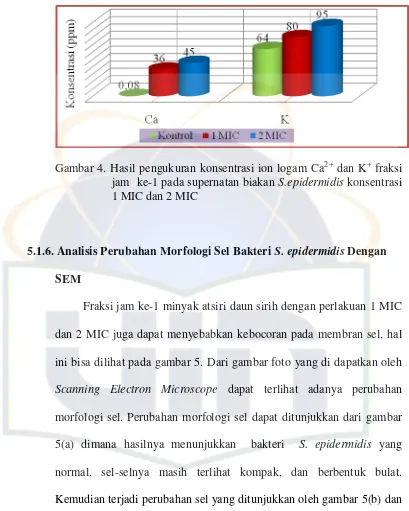
Gambar 4. Hasil pengukuran konsentrasi ion logam Ca2+ dan K+ fraksi
jam ke-1 pada supernatan biakan S.epidermidis konsentrasi
DAFTAR LAMPIRAN
Hal
Lampiran 1. Hasil determinasi daun sirih (Piper betle Linn.)... 48
Lampiran 2. Skema Kerja... 49 Lampiran 3. Hasil uji sensitivitas minyak atsiri daun sirih terhadap
ketiga jenis bakteri uji gram positif... 56
Lampiran 4. Pertumbuhan bakteri ujiterhadap fraksi minyak atsiri
daun sirih dengan metode plating... 57 Lampiran 5. Nilai absorbansi asam nukleat dan protein fraksi jam ke-1
pada sel S.epidermidis... 58
Lampiran 6. Hasil pengukuran konsentrasi ion logam Ca2+ dan K+ fraksi jam
ke-1 pada supernatan biakan bakteri S.epidermidis konsentrasi
1 MIC dan 2 MIC... 58
Lampiran 7. Perhitungan konsentrasi MIC bakteri uji B. subtilis... 62
Lampiran 8. Perhitungan konsentrasi MIC bakteri uji S. epidermidis dan
S. mutan... 63
BAB I
PENDAHULUAN
1.1. Latar Belakang
Pengetahuan tentang obat tradisional yang banyak digunakan oleh
nenek moyang pada zaman dahulu, saat ini sedang banyak digali. Hal ini
tidak terlepas dari banyaknya kendala yang ditimbulkan oleh penggunaan
obat sintetis, seperti harganya yang mahal, terjadinya resistensi bila
penggunaannya kurang tepat dan dapat menimbulkan efek samping yang
tidak dikehendaki. Masyarakat kini lebih cenderung untuk menggunakan obat
dari bahan alami dan melakukan pengobatan secara tradisional seperti yang
dilakukan pada zaman dahulu. Tumbuhan sebagai obat tradisional, biasanya
digunakan secara tunggal (satu jenis tumbuhan) atau majemuk (campuran dari
beberapa jenis tumbuhan). Bagian tumbuhan yang umum digunakan sebagai
obat tradisional adalah daun, bunga, buah, kulit batang, atau akarnya.
Penggunaannya ada yang secara langsung dalam keadaan yang masih segar,
ada pula yang diseduh ataupun direbus (Tengah, 2005).
Sirih (Piper betle) merupakan salah satu jenis tumbuhan dari famili
Piperaceae yang telah dikenal luas sehingga memiliki beberapa nama daerah,
diantaranya : sireh, suruh (Jawa). Pemanfaatan sirih yang paling umum
adalah sebagai bahan untuk sirih pinang. Bagian tumbuhan sirih untuk bahan
sirih pinang adalah daun (umumnya di Indonesia bagian barat) dan buah
(umumnya di Indonesia bagian timur). Tumbuhan dari Genus Piper, seperti
Piper nigrum, P. methysticum, P. auritum dan P. betle telah dikenal sejak
pertanian dan bahan obat - obatan dengan nilai ekonomi yang tinggi (Sumarni
et al., 2009).
Minyak atsiri merupakan minyak yang mudah menguap yang
akhir-akhir ini menarik perhatian dunia, hal ini disebabkan minyak atsiri dari
beberapa tanaman bersifat aktif biologis sebagai antibakteri dan antijamur.
Kandungan minyak atsiri daun sirih dilaporkan memiliki daya antibakteri.
Kemampuan tersebut karena adanya kandungan 4,2% minyak atsiri yang
sebagian besar terdiri dari senyawa betelphenol yang merupakan isomer
eugenol, methil eugenol, kariofilen (siskuiterpen), kavikol, kavibekol,
estragol dan terpinen (Sastroamidjojo, 1997). Analisis komponen kimia
penyusun minyak atsiri Piper betle telah dilakukan juga oleh beberapa
peneliti dan diketahui bahwa sebagai komponen utama penyusun minyak
atsirinya antara lain kariofilena (30%), Isoeugenol (22%) dan α-kubebena
(9%) (Agusta, 2000; Sulianti dan Chairul, 2002; Hertiani dan Purwantini,
2002).
Beberapa hasil penelitian tentang daun sirih telah dilaporkan, misalnya
bahwa ekstrak daun sirih pada konsentrasi 2,5%, 5% dan 10% secara invitro
dapat menghambat pertumbuhan S. aureus dan E. coli (Hermawan, 2007).
Nalina dan Rahim (2007) melaporkan bahwa ekstrak air daun sirih memiliki
aktivitas antibakteri terhadap S. mutan. Telah dilaporkan pula bahwa minyak
atsiri pada daun sirih, rimpang temu kunci, rimpang lengkuas, dan kunyit
berperan dalam aktivitas sebagai antibakteri dan anti jamur. Diduga aktivitas
tersebut disebabkan adanya kandungan senyawa fenolik bermolekul rendah
Suppakul et al., (2006) melaporkan adanya sifat antibakteri dan antioksidan
pada minyak atsiri daun sirih dan nilai MIC minyak atsiri sirih pada kisaran
12,5 - 100 µLml-1 dapat menghambat pertumbuhan semua mikroorganisme
yang diuji kecuali P. aeruginosa. Sediaan obat kumur minyak atsiri daun sirih
2,5% dapat menghambat pertumbuhan E. coli dan sediaan 10% mampu
menghambat pertumbuhan S. aureus (Rahmat et al., 2000). Minyak atsiri
daun sirih juga memiliki aktivitas dan daya hambat terhadap S. epidermidis
dengan nilai MIC 5% ( Alfarisi, 2009).
Dari penelitian sebelumnya dilaporkan bahwa minyak atsiri daun sirih
memiliki aktivitas sebagai antibakteri dengan mekanisme pengrusakan
dinding sel bakteri. Pada penelitian ini dilakukan fraksinasi komponen kimia
minyak atsiri daun sirih dan uji aktivitasnya terhadap bakteri gram positif B.
Subtilis, S. epidermidis dan S. mutan. Maka, pada penelitian ini ditujukan
pada komponen kimia fraksi minyak atsiri daun sirih yang diperoleh dari
variasi waktu pengambilan distilat terhadap aktivitas antibakteri untuk
beberapa jenis bakteri gram positif B. Subtilis, S. epidermidis dan S. mutan.
1.2. Rumusan masalah
Dalam penelitian ini yang menjadi rumusan masalah adalah sebagai berikut :
1. Apa saja komponen kimia yang terdapat dalam fraksi minyak atsiri daun
sirih yang diperoleh berdasarkan variasi waktu pengambilan fraksi?
2. Bagaimana aktivitas komponen kimia fraksi minyak atsiri daun sirih yang
diperoleh pada jam ke-1, jam ke-2, jam ke-4 dan jam ke-6 terhadap
1.3. Hipotesa
Fraksi minyak atsiri daun sirih yang diperoleh pada jam ke-1, jam ke-2,
jam ke-4 dan jam ke-6 memiliki komponen kimia yang berbeda dan aktivitas
antibakteri terhadap bakteri gram positif B. subtilis, S. epidermidis dan S.
mutan dengan merusak membran sel.
1.4. Tujuan Penelitian
1. Mengetahui komponen kimia yang terdapat dalam setiap fraksi minyak
atsiri daun sirih yang diperoleh pada jam ke-1, jam ke-2, jam ke-4 dan
jam ke-6.
2. Mengetahui aktivitas antibakteri setiap fraksi minyak atsiri daun sirih
terhadap bakteri gram positif B. subtilis, S. epidermidis dan S. mutan.
3. Mengetahui mekanisme antibakteri fraksi minyak atsiri daun sirih terhadap
bakteri uji.
1.5. Manfaat Penelitian
Memberikan landasan ilmiah dan informasi mengenai komponen kimia
fraksi minyak atsiri daun sirih dan aktivitasnya terhadap beberapa jenis
bakteri gram positif untuk menunjang penggunaan daun sirih sebagai bahan
BAB II
TINJAUAN PUSTAKA
2.1. Tanaman Daun Sirih
2.1.1. Klasifikasi
Divisi : Spermatophyta
Sub divisi : Angiospermae
Kelas : Dicotyledoneae
Ordo : Piperales
Family : Piperaceae
Genus : Piper
Spesies : Piper betle Linn
2.1.2. Nama Daerah
Burangir, napuran (Batak), siriah (Minang), buyu, ayap (Dayak),
seureuh (Sunda), sedah, suruh (Jawa), kuta kowa (Sumba), papek,
ruange (Sul.Utara), ain kamu, amu (Seram), gies, bido (Halmahera),
kenaan, bido (Irian Jaya) (Agusta, 2000).
2.1.3. Deskripsi Tanaman
Merupakan tanaman memanjat tinggi 5-15 m. Helaian daun
berbentuk bundar telur atau bundar telur lonjong, pada bagian pangkal
atau berambut pendek, tebal,berwarna putih. Panjangnya 5-18 cm dan
lebar 2,5-10,5 cm (Sudarsono et al.,1996).
2.1.3. Kandungan Kimia
Daun sirih mengandung minyak atsiri dengan kadar berkisar
antara 0,13-0,33% (v/v). Terdiri dari kavibetol, katekol, kadinen,
karvakrol, kariofilen, kavikol, 1.8 sineol, estragol, eugenol, metil
eugenol, pirokatekin, terpenil asetat, sesquiterpen, triterpen dan
terpenoid . Disamping itu juga terdapat senyawa neolignan (piperbetol,
metilpiper betol, piperol A, piperol B), krotepoksid suatu senyawa
yang mempunyai potensi sebagai sitotoksik (Sudarsono et al., 1996).
2.1.4. Khasiat
Secara empiris tanaman sirih digunakan untuk obat batuk, asma,
hidung berdarah (mimisan), mulut berbau, kepala pusing, demam nifas
(daun), gusi bengkak (getah), dan minyak atsirinya untuk radang
tenggorokan (Pudjiastuti, 1996; Sudarsono et al., 1996).
2.2. Minyak atsiri
2.2.1. Deskripsi Minyak Atsiri
Minyak atsiri adalah zat berbau yang terkandung dalam tanaman.
Minyak ini disebut juga minyak menguap karena pada suhu biasa (suhu
atsiri adalah isoprenoid, karena molekul-molekulnya tersusun dari
unit-unit isopren. Beberapa sifat umum dari minyak atsiri antara lain
tersusun oleh bermacam-macam komponen senyawa, memiliki bau
khas, mempunyai rasa getir, menggigit tergantung dari jenis komponen
penyusunnya, dalam keadaan segar dan murni minyak atsiri umumnya
tidak berwarna, tidak stabil terhadap pengaruh lingkungan baik
pengaruh udara, sinar matahari dan panas, tidak dapat bercampur
dengan air dan larut dalam pelarut organik.
Minyak atsiri dapat terbentuk secara langsung oleh protoplasma
akibat adanya peruraian lapisan resin dari dinding sel atau oleh
hidrolisis dari glikosida tertentu. Minyak atsiri sendiri bagi tanaman
berguna untuk menarik serangga yang membantu proses penyerbukan
sebagai cadangan makanan, untuk mencegah kerusakan tanaman oleh
serangga atau hewan lain dan mempengaruhi proses transpirasi (Didik
dan Mulyani, 2004).
2.3. Bakteri
2.3.1. Deskripsi Bakteri
Bakteri merupakan kelompok sel prokariotik uniseluler. Salah satu
karakteristik utama sel bakteri adalah ukuran, bentuk, struktur dan
penataan selnya yang mencakup morfologi sel. Reproduksi terutama
dengan aseksual atau pembelahan biner. Ciri umum lainnya adalah
dimana dinding sel mengandung molekul kompleks disebut
(Pelczar et al., 1998). Komponen bakteri secara umum terdiri dari
substansi membran sel, dinding sel, bahan nukleat dan ribosom
(Brooks et al., 2005; Pelczar et al., 1998).
2.3.2. Bakteri Uji
a. Bacillus subtilis
Bacillus subtilis dapat diklasifikasikan sebagai berikut :
Kingdom : Tumbuhan
bersifat aerob dan dapat membentuk spora. Bakteri ini banyak terdapat
dalam tanah, air, udara dan tumbuh-tumbuhan (Jawetz et al., 1996).
B.subtilis dapat menyebabkan beberapa jenis penyakit seperti
meningitis, endokarditis, infeksi mata dan lain-lainnya
(Syahrurachman et al., 1994).
b. Staphylococcus epidermidis
Staphylococcus epidermidis di klasifikasikan sebagai berikut :
Kingdom : Procariotae
Class : Bakteria
Ordo : Eubacterialees
Family : Micrococcaceae
Genus : Staphylococcus
Spesies : Staphylococcus epidermidis
S. epidermis merupakan bagian dari flora normal pada kulit
manusia, saluran pernafasan dan saluran pencernaan, dapat ditemukan
di udara dan lingkungan sekitar kita. Kuman ini tidak patogen, tidak
bersifat invasive, nonhemolitik, berwarna putih, tidak membentuk
koagulasi. Staphylococcus patogen sering menghemolisis darah dan
mengkoagulasi plasma (Warsa et al., 1993). S. epidermis juga dapat
menyebabkan endokarditis infektif jika sebagian besar bakteri ini
S. mutan merupakan bakteri gram positif berbentuk bulat, yang
memiliki karakteristik dapat membentuk pasangan atau rantai selama
pertumbuhannya. S. mutan dapat mensintesa berbagai macam
polisakarida seperti dextrans atau levans dari sukrosa yang memiliki
peranan penting pada proses pembentukan karies gigi (Brooks et al.,
2005).
2.4. Antibakteri
2.4.1. Aktivitas Antibakteri
Antibakteri adalah obat pembasmi bakteri khususnya bakteri
yang merugikan manusia. Berdasarkan sifat toksisitas selektif, ada
bakteri yang bersifat menghambat pertumbuhan bakteri
(bacteriostatic) dan ada yang bersifat membunuh bakteri
(bactericidal). Sulfonamid, kloramfenikol, dan tetrasikiklin
merupakan antibiotik yang bersifat bakteriostatik. Sedangkan
sefalosforin, rifampisin, aminoglikosid, isoniazid, dan kotrimoksazol
bekerja secara bakterisid (Bilbiana dan Hastowo, 1992).
Konsentrasi minimal yang diperlukan untuk menghambat atau
membunuh pertumbuhan bakteri masing-masing dikenal sebagai nilai
MIC dan MBC. Antibakteri tertentu aktivitasnya dapat meningkat
menjadi bakterisid bila kadar antibakterinya ditingkatkan melebihi
2.4.2. Mekanisme Kerja Antibakteri
a. Inhibitor Sintesis Dinding Sel
Kerusakan dinding sel atau penghambatan pada
pembentukannya dapat menyebabkan sel menjadi lisis. Dinding sel
bakteri terdiri dari polipeptidoglikan yang merupakan kompleks
mukopeptida (glikopeptida). Zat antibakteri menghambat sintesis
peptidoglikan dinding sel bakteri dengan menghambat keja enzim
traspeptidase dan enzim rasemase alanin atau dengan menghambat
sintesa asam muramat. Senyawa penisilin dan sefalosforin yang secara
struktur mirip, dan senyawa-senyawa yang tidak mirip seperti
sikloserin, vankomisin, dan basitrain merupakan zat antibakteri yang
bekerja dengan menghambat sintesis dinding sel (Setiabudy dan Gan,
1995; Chambers, 2007).
b. Inhibitor Fungsi Membran Sel
Senyawa yang bekerja langsung pada membran sel
mikroorganisme, mempengaruhi permeabilitas dan menyebabkan
kebocoran senyawa-senyawa intraselluler. Dalam hal ini termasuk
senyawa yang bersifat detergen seperti polimiksin dan amfoterisin B
yang berikatan dengan sterol-sterol dinding sel (Chambers, 2007).
Kerusakan membran sel akan mengakibatkan keluarnya berbagai
komponen penting dalam sel bakteri yaitu protein, asam nukleat dan
c. Inhibitor Sintesis Protein Sel
Bakteri memiliki ribosom dengan 70S, sedangkan manusia
memiliki 80S. Unit ribosom pada bakteri adalah 30S dan 50S.Síntesis
protein dihambat dengan memengaruhi fungsi subunit ribosom 30S
atau 50S sehingga menyebabkan penghambatan síntesis protein yang
reversibel dan mengakibatkan kematian sel. Obat bakteriostatik ini
meliputi kloramfenikol, golongan tetrasiklin, eritromisin, klindamisin,
pristinamin dan aminoglikosida (Setiabudy dan Gan, 1995; Chambers,
2007).
d. Inhibitor Sintesis Asam Nukleat
Antibakteri yang tergolong kelompok ini adalah golongan
kuinolon dan rifampin. Dalam hal ini, derivat rifampin akan berikatan
dengan enzim polimerase-RNA (pada sub unit) sehingga menghambat
sintesis RNA oleh enzim tersebut. Sementara asam nalidiksat bekerja
dengan menggaggu sintesis DNA . Sedangkan golongan kuinolon
bekerja dengan menghambat topoisomerase (Bilbiana dan Hastowo,
1992; Chambers, 2007)
e. Inhibitor Metabolisme Sel Bakteri
Dalam kelompok ini termasuk sulfonamida. Pada umumnya
bakteri memerlukan para-aminobenzoat (PABA) untuk sintesis asam
folat, yang diperlukan dalam sintesis purin. Sulfonamida memiliki
struktur seperti PABA, sehingga penggunaan sulfonamida
menghasilkan asam folat yang tidak berfungsi (Bilbiana dan Hastowo,
2.4.3. Metode Pengujian Antibakteri
a. Metode Difusi
Metode ini hanya menyajikan informasi kualitatif atau
semikuantitatif mengenai kerentanan mikroorganisme tersebut
terhadap antibiotik yang diberikan. Uji dilakukan dengan
mengaplikasikan cakram Kertas saring berisi sejumlah obat tertentu
diatas permukaan medium agar (medium padat) yang sebelumnya
telah diinokulasi bakteri uji. Setelah inkubasi 18-24 jam, dilakukan
pengukuran daerah hambatan yang jernih disekitar cakram. Diameter
daerah tersebut tergantung pada aktivitas obat terhadap mikroba yang
diuji. Nilai standar untuk ukuran daerah hambatan masing-masing
spesies bakteri dan masing-masing antibiotik memungkinkan
klasifikasi isolat secara klinis sebagai resisten, intermediet, atau rentan
(Chambers, 2007).
b. Metode Dilusi
Metode ini menggunakan antimikroba dengan kadar yang
menurun secara bertahap (seri pengenceran), baik dengan media cair
atau padat. Kemudian media diinokulasi bakteri uji dan dieramkan.
Tahap akhir dilarutkan antimikroba dengan kadar menghambat atau
BAB III
KERANGKA KONSEP
Analisis Protein & Asam Nukleat Dengan Uv-Vis
Analisis Ion-Ion Logam Dengan AAS
Analisis SEM Didistilasi uap dan air
Sampel daun sirih segar
Pengambilan fraksi
Analisa kimia dengan GCMS
Uji aktivitas antibakteri
Penentuan diameter daerah hambat
Penentuan MIC Determinasi Tanaman
BAB IV
METODOLOGI PENELITIAN
4.1. Waktu dan Tempat Penelitian
Penelitian dilaksanakan pada bulan Juni hingga Agustus 2010 dan
bertempat di Laboratorium Biosain, Puslit biologi, LIPI Cibinong, Bogor.
4.2. Pengambilan Sampel
Sampel daun sirih (Piper betle Linn.) diambil dari tanaman yang
terdapat di BALITRO (Balai Tanaman Obat dan Rempah), Cimanggu,
Bogor. Waktu pengambilan sampel dilakukan pada bulan Mei 2010.
4.3. Determinasi Tanaman
Sampel daun sirih diidentifikasi di Herbarium Bogoriense Bidang
Botani, Puslit biologi, LIPI Cibinong, Bogor.
4.4. Alat dan Bahan
1. Alat
Alat yang digunakan dalam penelitian ini antara lain perangkat
distilasi uap dan air, cawan petri, inkubator, neraca analitik, Laminar Air
Flow (LAF), autoklaf, jarum ose, mikropipet, microplate, oven, tabung
reaksi, rak tabung reaksi, spektrofotometer Uv-Vis Perkin Elmer,
Chromatography-Mass Spectrophotometer (GC-MS) Varian Saturn 2000, Scanning Eletron
Microscope (SEM) JEOL seri JSM-5310 LV, refrigerator, pipet tetes,
erlenmeyer, vial, ependrof, inkubator, inkubator shaker, vortek dan
sentrifus.
2. Bahan
Bahan yang digunakan dalam penelitian ini adalah daun sirih (Piper
bettle Linn.), aquadest, NaSO4 anhidrat, tween 80, aquadest steril, Blood
Agar Base, Nutrient Agar, Mueller Hinton Agar, Mueller Hinton Broth,
darah kambing steril, dapar fosfat pH 7,4; cacodylate buffer, glutaraldehid
2,5%, alkohol 50%, alkohol 70%, alkohol 80%, alkohol 95%, alkohol
96%, tannin acid, terbutanol dan osmium tetraoksida 1%.
3. Bakteri Uji
Bacillus subtilis, Staphylococcus epidermidis dan Steptococcus mutan.
4.5. Metode Penelitian
Kegiatan yang dilakukan untuk mencapai sasaran :
1. Isolasi fraksi minyak atsiri daun sirih
2. Identifikasi komponen kimia fraksi minyak atsiri daun sirih
3. Pengujian aktivitas antibakteri fraksi minyak atsiri daun sirih
a. Sterilisasi alat dan bahan
b. Pembuatan medium
c. Pembiakan bakteri uji
d. Pembuatan suspensi bakteri uji
f. Penentuan Minimum Inhibitor Concentration (MIC)
4. Analisis protein dan asam nukleat
5. Analisis ion logam Ca2+ dan K +
6. Analisis Perubahan Morfologi Sel dengan Scanning Electron
Microscope (SEM)
4.6. Prosedur Kerja
4.6.1. Isolasi Fraksi Minyak Atsiri Daun Sirih
Sampel daun sirih yang diperoleh dari Balai Penelitian Obat
dan Aromatik (BALITRO) dan sudah dideterminasi di Herbarium
Bogoriensis, LIPI Puslit Biologi, Cibinong, Jawa Barat. Diambil
dalam keadaan segar kemudian di sortasi dan ditimbang sebanyak ±
30 kg lalu dicuci dengan air mengalir untuk menghilangkan segala
jenis kotoran yang melekat. Setelah pencucian selesai, kemudian
dilakukan perajangan dan proses distilasi uap dan air selama 6 jam
dengan variasi waktu pengambilan distilat untuk mendapatkan fraksi
minyak atsiri dari dalam tanaman. Setiap fraksi minyak atsiri yang
telah berhasil didapatkan kemudian ditambahkan NaSO4 anhidrat
untuk menghilangkan kandungan air. Kemudian menentukan
presentase kadar setiap fraksi minyak atsri yang berhasil di dapat.
Presentase kadar fraksi minyak atsiri didapat berdasarkan berat fraksi
4.6.2. Identifikasi Komponen Kimia Fraksi Minyak Atsiri Daun Sirih
Identifikasi komponen fraksi minyak atsiri daun sirih dilakukan
selama 1 jam dengan menggunakan instrumentasi GC-MS Varian
Saturn 2000 di Laboratorium Analisis Umum, LIPI Cibinong.
Preparasi sample fraksi minyak atsiri dilakukan dengan penambahan
dietil eter. Jenis kolom yang digunakan adalah VF-17 MS panjang
30mm dan ID sebesar 0,25 mm. Gas pembawa adalah helium dengan
kecepatan aliran 1,3 ml/menit dan tekanan sebesar 10,7 Psi. Suhu
kolom diprogram dari 50 oC sampai 250 oC dengan dua tahap
kenaikan. Pada tahap awal suhu kolom dibuat konstan 50 oC selama 3
menit, lalu dinaikkan sampai 150 oC dengan temperatur 5 oC/menit
dan selanjutnya dinaikkan menjadi 250 oC dengan temperatur 3
o
C/menit. Kondisi ini dipertahankan selama 3.67 menit. Suhu injektor
selama analisis berlangsung diprogram konstan pada suhu 230 oC.
Sementara temperatur interface adalah 250 oC dan autosampling
sebanyak 2 µl. Solvent cut time selama 3 menit dan Scan MS 50-450
(M/Z).
4.6.3. Pengujian Aktivitas Antibakteri Fraksi Minyak Atsiri Daun Sirih
4.6.3.1. Sterilisasi Alat dan Bahan
a. Sterilisasi Alat
Sterilisasi dilakukan dengan cara yang sesuai terhadap
keadaan bersih dan kering. Tabung reaksi, gelas ukur, vial,
erlenmeyer ditutup mulutnya dengan alumunium voil, kemudian
semuanya disterilkan dalam autoklaf pada suhu 121 ˚C, selama
15 menit. Pinset, jarum ose, disterilkan dengan cara dipijarkan
aseptis yang sebelumnya telah dibersihkan dengan larutan
alkohol, lalu disterilkan dengan UV yang dinyalakan selama
lebih kurang 2 jam sebelum digunakan.
4.6.3.2.Pembuatan Medium
a. Blood Agar Base (BAB)
Pada pembiakan bakteri S. mutan media yang digunakan
adalah Blood Agar Base sebanyak 40 gram dilarutkan dalam 1
liter aquadest, lalu disterilkan dalam autoklaf pada suhu 121 ºC
selama 15 menit. Kemudian ditambahkan darah pada suhu 35-40 0
C sekitar 5%.
b. Nutrient Agar (NA)
Pada pembenihan bakteri B.subtilis dan S. Epidermidis
gram dilarutkan dalam 1 liter aquadest, lalu disterilkan dalam
autoklaf pada suhu 121 ºC selama 15 menit.
c. Mueller Hinton Agar
Sebanyak 38 gr serbuk Mueller Hinton Agar dilarutkan
dalam 1 liter aquadest, lalu disterilkan dengan autoklaf pada
suhu 121 ºC selama 15 menit.
d. Mueller Hinton Broth
Sebanyak 21 gr serbuk Mueller Hinton Broth dilarutkan dalam
1 liter aquadest, selanjutnya disterilkan dengan autoklaf pada
suhu 121 ºC selama 15 menit.
4.6.3.3. Pembiakan Bakteri Uji
Bakteri B. Subtilis dan S. epidermidis diinokulasikan ke
media Nutrien Agar miring sedangkan S. mutan diinokulasikan
ke media Blood Agar Base miring menggunakan ose yang telah
disterilkan dengan cara dipijarkan pada nyala api bunsen,
kemudian diinkubasi pada suhu 37 0C selama 24 jam.
4.6.3.4. Pembuatan Suspensi Bakteri Uji
Stok bakteri uji yang telah diremajakan pada agar nutrien
miring, Diambil dengan jarum ose (1 ose) dan dimasukkan
kedalam tabung yang berisi 5 ml Mueller Hinton Broth, media
Dan diinkubasi selama 18 jam. Selanjutnya dituang ke dalam
nutrien agar dan mediauntuk S. mutan ditambahkan darah steril.
Diencerkan hingga diperoleh suspensi (105) sel bakteri/ml.
Suspensi ini yang akan digunakan dalam pengujian.
4.6.3.5. Pembuatan Larutan Uji
Larutan induk dibuat emulsi dengan menggunakan cara
mencampur fraksi minyak atsiri daun sirih dengan pelarut 0.5%
tween 80, etanol absolut 2% dan aquadest. Kemudian
diencerkan hingga 17,5%; 15%; 12,5%; 10%; 7,5%; 5%; 2,5%;
1%; 0.5%; 0,25%; 0,125%.
4.6.3.6. Penentuan MIC (Rodriguez et.al., 2002)
Metode penentuan minimum inhibitor concentration adalah
adalah sebagai berikut :
Menyiapkan larutan uji yang sudah dibuat dan juga larutan
kontrol.
Menyiapkan media Mueller Hinton Broth, menyiapkan
microplate, selanjutnya tiap-tiap sumuran diisi dengan 100
µl media MHB, 100 µl suspensi bakteri 1x105 sel/ml, dan
50 µl larutan uji dengan berbagai konsentrasi, dan juga
Kemudian diinkubasikan dalam shaker 150 rpm pada suhu
37 ºC selama 24 jam.
Pembacaan hasil percobaan didasarkan pada keruh atau
tidaknya sumuran percobaan dibandingkan kontrol untuk
menentukan MIC dan juga dengan cara plating pada
media agar di cawan petri.
Percobaan dilakukan secara duplo.
4.6.4. Analisis Protein dan Asam Nukleat (Carson et al., 2002)
Suspensi bakteri uji yang telah diinkubasi selama 18 jam dalam
media Muller Hinton Broth. Sentrifus dingin, kecepatan 3500 rpm selama
15 menit. Selanjutnya filtrat dibuang dan pellet dalam tabung dicuci
dengan dapar fospat Ph 7,4 sebanyak 2 kali. Lalu suspensikan kedalam
dapar fospat Ph 7,4 hingga volume 10 ml. Ditambahkan fraksi minyak
atsiri daun sirih dengan perlakuan 1 MIC dan 2 MIC sesuai kebutuhan.
Diinkubasi kembali selama 24 jam dalam shaker 150 rpm 37 ºC.
Kemudian suspensi disentrifus selama 15 menit dengan kecepatan 3500
rpm, lalu saring dan ambil cairan supernatan. Selanjutnya ukur absobansi
dengan spektrofotometer UV-Vis pada panjang gelombang 260 nm dan
4.6.5. Analisis Ion LogamCa2+ dan K + (Cox et al., 2000)
Untuk analisis ion-ion diukur dalam bentuk ion Ca2+ dan K+ yang
keluar dari membran sel bakteri akibat perlakuan dengan minyak atsiri.
Analisis kebocoran ion dilakukan pada pelet bakteri yang dipersiapkan
seperti pada pengukuran kebocoran protein dan asam nukleat. Kebocoran
dinyatakan dengan terukurnya ion-ion logam yang terdapat pada bakteri
uji setelah dikontakkan dengan minyak atsiri pada perlakuan 1 MIC dan
2 MIC. Kebocoran ion Ca2+ dan K+ dideteksi dengan menggunkan AAS
(Atomic Absorption Spectrophotometre) Perkin Elmer a Analist 700.
Larutan sel hasil kontak dengan minyak atsiri diambil untuk diukur
mendapatkan masa sel bakteri (pelet). Kemudian pelet dicuci dengan
dapar fospat sebanyak 2 kali. Pelet difiksasi dengan glutaraldehid 2,5%
selama 4 jam, Selanjutnya disentrifus dan supernatan dibuang. Pelet
direndam kembali dengan larutan tannin acid 2% selama 18 jam
selanjutnya disentrifus. Supernatan dibuang dan pelet direndam dengan
Kemudian disentrifus kembali, dibuang supernatan dan pelet direndam
dalam osmium tetraoksida 1% dalam cacodylate buffer dibiarkan dalam
refrigerator selama 1 jam. Setelah direndam, disentrifus kembali dan
pelet dicuci dengan alkohol 50% dingin, dibiarkan 10 menit dan
disentrifus kembali selama 5 menit. Kemudian supernatan dibuang dan
pelet dikeringkan berturut-turut dengan alkohol 50%, 70%, 80% dan
alkohol 95% masing-masing selama 10 menit. Dicuci dengan alkohol
absolut dan disentrifus 5 menit sebanyak 2 kali dan dicuci kembali
dengan terbutanol 2 kali. Kemudian Oleskan apusan sel diatas potongan
bujur sangkar cover slip (slip glas) dan dikeringkan dengan terbutanol.
Slip glas yang telah diolesi dengan sel tersebut diletakkan pada stub
alumunium untuk dicoating dengan emas dalam ion coater selama 1 jam
pada kondisi vakum. Kemudian diamati dengan alat Scanning Electron
BAB V
HASIL DAN PEMBAHASAN
5.1. Hasil
5.1.1. Isolasi dan Penentuan Komponen Kimia Fraksi Minyak Atsiri
Daun Sirih
Gambar 1: Daun sirih
Metode yang digunakan untuk proses pemisahan komponen
kimia fraksi minyak atsiri daun sirih segar yang berasal dari Balitro,
Cimanggu (Bogor), adalah distilasi uap dan air (Sugiastuti, 2002;
Sulianti dan Chairul, 2002). Proses distilasi ini dilakukan dengan
menggunakan variasi waktu pengambilan minyak atsiri yaitu pada jam
ke-1, jam ke-2, jam ke-4 dan jam ke-6. Perbedaan waktu pengambilan
distilat ini memberikan hasil yang berbeda pada kandungan komponen
kimia fraksi minyak atsirinya (tabel 1). Begitu pula terhadap nilai
presentase kadar yang dihasilkan masing – masing fraksi 1,2,3 dan 4
yaitu 0.061%, 0.034%, 0.027% dan 0.015%. Namun demikian, minyak
yang diperoleh masih memiliki aroma dan warna yang sama, dengan
Dari hasil analisis GCMS diketahui bahwa keempat fraksi minyak
atsiri tersebut memiliki kromatogram yang berbeda satu sama lain
(gambar 1). Fraksi jam ke-1 memiliki 64 komponen kimia penyusun.
Sedangkan pada fraksi jam ke-2 dan jam ke-6 terdeteksi sebanyak 56
puncak dan 73 puncak untuk fraksi jam ke-4.
Identifikasi masing puncak pada kromatogram
masing-masing fraksi minyak atsiri memperlihatkan bahwa komponen
kimianya terdiri dari monoterpena, monoterpena alkohol, seksuiterpena,
seskuiterpena alkohol dan turunan fenil propanoid. Kemudian
masing-masing komponen kimia fraksi minyak atsiri daun sirih dikelompokkan
berdasarkan golongan senyawanya seperti terlihat pada (tabel 2).
Gambar 2. Perbandingan kromatogram antar fraksi minyak atsiri daun sirih
Keterangan: a: Minyak atsiri daun sirih tunggal
5.1.2. Pengujian Aktivitas Antibakteri Fraksi Minyak Atsiri Daun Sirih
Aktivitas antibakteri fraksi minyak atsiri sirih terhadap tiga
bakteri uji dapat dihitung dengan mengukur diameter daerah hambat
(DDH) pertumbuhan bakteri disekitar kertas cakram yang terlihat
jernih. Berdasarkan hasil pengujian yang disajikan dalam tabel 3 dapat
diketahui bahwa fraksi minyak atsiri sirih pada konsentrasi 50% dapat
mempengaruhi pertumbuhan ketiga bakteri dengan tingkat hambatan
yang berbeda. F2 dan F4 minyak atsiri daun sirih memiliki tingkat
sensitifitas yang paling tinggi terhadap ketiga bakteri uji dibandingkan
dengan ketiga fraksi lainnya (tabel.3).
Tabel 3. Aktivitas fraksi minyak atsiri daun sirih terhadap 3 jenis bakteri uji gram positif pada konsentrasi 50%
5.1.3. Penentuan MIC Fraksi Minyak Atsiri Daun Sirih
Penentuan nilai MIC berdasarkan atas konsentrasi minimal
fraksi minyak atsiri daun sirih yang dapat menghambat pertumbuhan
ketiga bakteri uji gram positif (tabel 4 dan tabel 5).
No Bakteri uji Diameter Daerah Hambat (mm)*
F1 F2 F3 F4
1 B. subtilis 4 8 7 7,5
2 S. epidermidis 2 4,5 2,5 5,5
3 S. mutan 5,5 13 4,5 8,5
Tabel 4. Penentuan MIC fraksi minyak atsiri daun sirih terhadap bakteri uji
5.1.4. Analisis Kebocoran Protein dan Asam Nukleat
Pemberian fraksi jam ke-1 minyak atsiri daun sirih pada beberapa
dosis MIC mengakibatkan terjadinya kerusakan sel yang diamati
dengan adanya kebocoran protein dan asam nukleat dari sel bakteri.
Fraksi jam ke-1 minyak atsiri daun sirih menyebabkan kebocoran sel
yang diamati dengan adanya peningkatan nilai absorbansi pada panjang
gelombang 260 nm dan 280 nm (gambar 3). Senyawa-senyawa yang
memberikan serapan pada panjang gelombang 260 nm adalah asam
nukleat (RNA dan DNA), sedangkan pada panjang gelombang 280 nm
diidentifikasi sebagai protein.
Gambar 3. Nilai absorbansi asam nukleat dan protein fraksi jam ke-1
pada sel S .epidermidis
5.1.5. Analisis Ion Logam Ca2+ dan K+
Fraksi jam ke-1 minyak atsiri daun sirih juga dapat menyebabkan
terlepasnya ion Ca2+ dan K+ dari sel bakteri S.epidermidis. Ion-ion yang
Gambar 4. Hasil pengukuran konsentrasi ion logam Ca2+ dan K+ fraksi
jam ke-1 pada supernatan biakan S.epidermidis konsentrasi
1 MIC dan 2 MIC
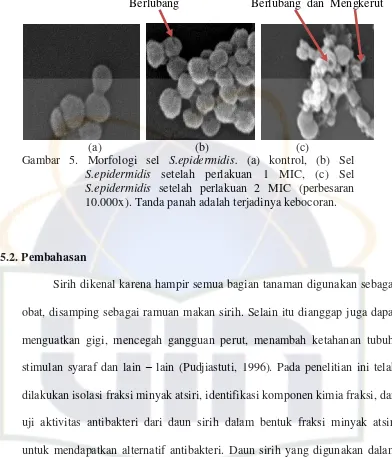
5.1.6. Analisis Perubahan Morfologi Sel Bakteri S. epidermidis Dengan
SEM
Fraksi jam ke-1 minyak atsiri daun sirih dengan perlakuan 1 MIC
dan 2 MIC juga dapat menyebabkan kebocoran pada membran sel, hal
ini bisa dilihat pada gambar 5. Dari gambar foto yang di dapatkan oleh
Scanning Electron Microscope dapat terlihat adanya perubahan
morfologi sel. Perubahan morfologi sel dapat ditunjukkan dari gambar
5(a) dimana hasilnya menunjukkan bakteri S. epidermidis yang
normal, sel-selnya masih terlihat kompak, dan berbentuk bulat.
Kemudian terjadi perubahan sel yang ditunjukkan oleh gambar 5(b) dan
gambar 5(c) dimana sel bakteri S. epidermidis yang sudah diberi
perlakuan minyak atsiri daun sirih dengan perlakuan 1 MIC dan 2 MIC
Berlubang Berlubang dan Mengkerut
(a) (b) (c)
Gambar 5. Morfologi sel S.epidermidis. (a) kontrol, (b) Sel
S.epidermidis setelah perlakuan 1 MIC, (c) Sel S.epidermidis setelah perlakuan 2 MIC (perbesaran 10.000x). Tanda panah adalah terjadinya kebocoran.
5.2. Pembahasan
Sirih dikenal karena hampir semua bagian tanaman digunakan sebagai
obat, disamping sebagai ramuan makan sirih. Selain itu dianggap juga dapat
menguatkan gigi, mencegah gangguan perut, menambah ketahanan tubuh,
stimulan syaraf dan lain – lain (Pudjiastuti, 1996). Pada penelitian ini telah
dilakukan isolasi fraksi minyak atsiri, identifikasi komponen kimia fraksi, dan
uji aktivitas antibakteri dari daun sirih dalam bentuk fraksi minyak atsiri
untuk mendapatkan alternatif antibakteri. Daun sirih yang digunakan dalam
penelitian ini merupakan daun sirih segar yang berasal dari Balitro,
Cimanggu, Bogor dan telah dideterminasi di Herbarium Bogoriense, Bidang
Botani, Puslit Biologi LIPI seperti yang tertera pada lampiran 1.
Metode yang digunakan untuk proses pemisahan komponen fraksi
minyak atsiri daun sirih adalah metode distilasi uap dan air (Sugiastuti, 2002;
Sulianti dan Chairul, 2002). Sebelum proses distilasi, daun sirih terlebih
yang melekat pada sampel.Kemudian dirajang dengan cara dipotong – potong
kecil untuk memperluas ukuran permukaan partikelnya agar mempermudah
kontak antara bahan sampel dengan uap air sehingga proses distilasi dapat
berlangsung dengan baik (Novalny, 2006).
Proses fraksinasi distilat ini dilakukan dengan menggunakan variasi
waktu pengambilan distilat yaitu pada jam ke-1 (F1), jam ke-2 (F2), jam ke-4
(F3) dan jam ke-6 (F4) untuk dapat mengamati hasil distilat yang diperoleh.
Perbedaan waktu pengambilan distilat memberikan hasil yang berbeda pada
volume distilat yang diperoleh. Hal ini berpengaruh terhadap presentase kadar
masing – masing fraksi. Hasil distilasi uap dan air secara berurutan untuk
fraksi 1,2,3, dan 4 diperoleh minyak atsiri daun sirih dengan presentase
0.061%, 0.034%, 0.027% dan 0.015%. Namun demikian, minyak yang
diperoleh masih memiliki aroma dan warna yang sama, dengan aroma daun
sirih yang khas dan berwarna kuning jernih.
Dari hasil analisa GCMS diketahui bahwa keempat fraksi tersebut
memiliki kromatogram yang berbeda satu sama lain (gambar 1). F1 memiliki
64 komponen kimia penyusun. Dengan komponen utamanya (>5%) terdiri
dari fenol 4-(2-profenil)-asetat (10,34%), kavibetol (10,61%),
fenol,2-metoksi-4(1-profenil)-asetat (13,89%) dan 4-alil-1,2-diasetoksibenzen
(27.31%). Pada F2 terdeteksi sebanyak 56 puncak dan memilki 5 komponen
utama penyusunnya, antara lain kariofilen (8.70%), kavibetol (9.60%),
fenol,2-metoksi-4(1-profenil)-asetat (12.95%), pacouli alkohol (10.23%), dan
4-alil-1,2-diasetoksibenzen (14.53%). Dari hasil tersebut dapat diketahui
dengan F2. Hasil identifikasi komponen kimia penyusun F2 menunjukkan
bahwa 48 komponen diantaranya merupakan komponen yang sama dengan
komponen penyusun F1 (Tabel 1). 16 komponen lainnya yang berbeda adalah
sabinen, -pinen, α-terpinen, dl-limonen, -felandren, -terpen, α-humulen,
estragol, himakalen, cadine, gurjunen, kubenol, longiberneol, dan
-eudesmol.
Untuk F3 terdeteksi sebanyak 73 puncak dengan komponen utamanya
adalah kariofilen (8.54%), kavibetol (10.50%), fenol,2-metoksi-4 (1-profenil)
–asetat (10.766%), pacouli alkohol (12.62%), dan 4-alil-1,2-diasetoksibenzen
(6.318%). Bila dibandingkan dengan komponen F2, sebagian komponen
penyusun F3 merupakan komponen penyusun F2 (tabel 1). 16 senyawa
lainnya sebagai penysusun komponen F3 antara lain kadinena; kubenol;
-eudesmol; safrol; (-)-α-selinene; selina-3,7(l1)diena; (-)-kariofilen-(l1);
-guaein; 2-propenol,3-(2,6,6-trimetil-1-sikloheksen-1-yl); -Selinen; Bisiklo
(3.2.0) hept-2-en-6-one,7,7-dikloro; Eudesm-7(11)-en-4-ol; sedrenol; dan
(+)-α-siperon. Jika dibandingkan dengan komponen senyawa F1, terdapat 14
komponen yang berbeda. Komponen berbeda tersebut merupakan komponen
yang sama-sama tidak terdeteksi di F2 pada F1.
Pada F4 terdapat 56 senyawa yang terdeteksi dengan kandungan
komponen utamanya antara lain kariofilen (8.61%), kavibetol (9,90%),
fenol,2-metoksi-4 (1-profenil) –asetat (13.01%), pacouli alkohol (10.08%),
dan 4-alil-1,2-diasetoksibenzen (14.64%). Jika dibandingkan dengan F3,
terdapat 19 senyawa yang tidak dimiliki oleh F4. Sebanyak 16 senyawa
merupakan komponen penyusun yang sama pada F1 dan F3 yaitu -kadinena, kubenol dan -eudesmol. Jika dibandingkan dengan F2 tidak terdapat
senyawa yang berbeda. Jika dibandingkan dengan F1 terdapat 16 senyawa
yang berbeda. Yaitu senyawa yang sama – sama tidak terdeteksi pada F2
(tabel 1) .Bila dibandingkan dengan hasil analisa minyak atsiri pada daun
sirih yang telah dilakukan para peneliti, terdapat beberapa persamaan
komponen utama penyusunnya, antara lain kariofilen, kavikol, -pinen,
kopaen, dan kamfen (Harapini et al., 1996; Rahmat et al., 2000; Jamal dan
Agusta, 2001; Parwata et al., 2009).
Identifikasi masing-masing puncak pada kromatogram masing-masing
fraksi minyak atsiri memperlihatkan bahwa komponen kimianya terdiri dari
monoterpena, monoterpena alkohol, seksuiterpena, seskuiterpena alkohol dan
turunan fenilpropanoid. Kemudian masing-masing komponen kimia fraksi
minyak atsiri daun sirih dikelompokkan berdasarkan golongan senyawanya
seperti yang tercantum pada tabel 2.
Pengujian aktivitas antibakteri fraksi minyak atsiri menggunakan
metode difusi cakram dan mikrodilusi. Metode difusi cakram merupakan
skrining awal untuk mengetahui sensivitas bakteri terhadap fraksi minyak
atsiri yang ditunjukkan dengan terbentuknya diameter daerah hambatan yang
berupa zona bening disekitar cakram kertas saring. Uji dilakukan dengan
mengaplikasikan cakram kertas saring berisi sejumlah fraksi minyak atsiri
diatas permukaan medium agar (medium padat) yang sebelumnya telah
diinokulasi bakteri uji. Setelah inkubasi 18 jam, dilakukan pengukuran daerah
pada aktivitas fraksi minyak atsiri terhadap bakteri yang diuji (Chamber,
2007). Semakin luas diameter hambatan tersebut menunjukkan semakin besar
daya antibakteri fraksi minyak atsiri daun sirih.
Dari hasil pengujian difusi cakram menunjukkan bahwa konsentrasi
50% masing –masing fraksi minyak atsiri daun sirih dapat menghambat
pertumbuhan ketiga bakteri uji. Antara lain B. subtilis, S. mutan dan S.
epidermidis. Diameter penghambatan yang terbentuk antar tiap fraksi dan
bakteri berbeda. Fraksi 2 dan Fraksi 4 merupakan fraksi yang memiliki
sensivitas tertinggi terhadap ketiga bakteri uji (tabel 3). Hal ini dapat dilihat
dari besarnya zona bening yang terbentuk disekililing cakram uji .Sedangkan
bakteri yang memiliki sensitiviyas tertinggi terhadap semua fraksi minyak
atsiri daun sirih adalah S. mutan (Tabel 3). Aktivitas penghambatan yang
tinggi dari fraksi 2 dan fraksi 4 diduga karena kedua fraksi ini memiliki
kandungan senyawa minor (<5%) asam benzoat,2-hidroksi-,metil ester; α
-kubeben; 3-alil-6-metoksifenil asetat dan 4-alil-1,2-diasetoksibenzen dengan
kandungan yang lebih tinggi daripada fraksi 1 dan 3 (tabel 1.)
Penentuan MIC menggunakan metode mikrodilusi (Maan dan
Markham, 1998; Taguri et al., 2006). Yaitu metode seri pengenceran dengan
penurunan kadar secara bertahap. Nilai MIC merupakan nilai terendah suatu
senyawa, dalam hal ini senyawa fraksi minyak atsiri yang dapat menghambat
pertumbuhan bakteri setelah inkubasi 24 jam (Chamber, 2007). Pada bakteri
B. subtilis dan S. epidermidis, hasil MIC masing – masing fraksi tidak ada
perbedaan secara bermakna. Hasil pengujian mikrodilusi didapatkan nilai
terhadap S. epidermidis adalah 0.25% (v/v), terhadap S. mutan adalah 2.5%
(F1), 1% (F2 dan F3), 0.25% (F4) beturut-turut. Walaupun S. mutan adalah
bakteri yang paling senstitif pada saat pengujian secara difusi, tetapi
aktivitasnya terhadap fraksi minyak atsiri kurang begitu peka dibandingkan
dengan S. epidermidis pada metode mikrodillusi. Dari hasil penelitian ini
menunjukkan bahwa fraksi minyak atsiri sirih tidak bersifat broad sprectrum
terhadap aktivitas ketiga bakteri uji tersebut. Bakteri S. epidermidis lebih
peka terhadap semua fraksi minyak atsiri sirih dibandingkan bakteri S. mutan
dan B. s subtilis. Sedangkan untuk fraksi minyak atsiri yang paling aktif
dalam menghambat pertumbuhan bakteri S.mutan adalah fraksi 4 (jam ke-6).
Kemungkinan ini dikarenakan adanya kontribusi komponen yang aktif pada
F4 yaitu senyawa asam benzoat,2-hidroksi-,metil ester; α-kubeben;
3-alil-6-metoksifenil asetat; dan 4-alil-1,2-diasetoksibenzen. Kemampuan suatu
antibakteri juga sangat erat kaitannya dengan perbedaan jumlah dan intensitas
komponen penyusun senyawa kimia mayor dan minor setiap fraksi minyak
atsiri sirih serta perbedaan komposisi dinding sel bakteri. Walaupun
B.Subtilis termasuk bakteri gram positif, akan tetapi bakteri ini dapat
melindungi dirinya dari molekul fraksi minyak atsiri dengan cara
pembentukan spora (Scocibusik et al., 2006, Brooks et al., 2005). Sehingga
pada saat diplating, bakteri ini kembali bergerminasi dengan kemampuan
bertahan diri membentuk spora. Jadi, untuk menembus pertahanan spora,
maka dibutuhkan lebih banyak lagi molekul fraksi minyak atsiri daun sirih.
Aktivitas antibakteri pada fraksi minyak atsiri sirih diduga disebabkan
senyawa yang mempunyai aktivitas sebagai antimikroba dalam minyak atsiri
adalah isoeugeunol dan kariofilen. Dalam daun sirih juga mengandung
hidroksikavikol, asam stearat dan palmitat yang mempunyai aktivitas sebagai
antimikroba (Nalina dan Rahim, 2006). Rahmat, et al (2000) menduga
senyawa yang berperan sebagai antibakteri dalam minyak atsiri daun sirih
adalah isoeugenol dan p-allifen . Senyawa fenolik dapat berfungsi sebagai
antimikroba karena adanya gugus OH yang bersifat racun terhadap mikroba
dan semakin banyak gugus OH yang ada pada senyawa tersebut maka
senyawa tersebut semakin beracun bagi mikroba (Cowan, 1999).
Perubahan atau kerusakan pada sel bakteri oleh senyawa bakteri
umumnya dapat di amati dalam bentuk kebocoran sel. Kerusakan sel bakteri
merupakan hasil interaksi senyawa antibakteri dengan bagian sel tertentu.
Interaksi senyawa antibakteri tersebut dapat menyebabkan sejumlah
perubahan atau kerusakan pada sel bakteri yang berpengaruh pada mekanisme
inaktivasi bakteri. Pada dosis yang tidak mematikan, bakteri mengalami luka
(injury), terjadi sejumlah perubahan dan kerusakan struktur sel bakteri yang
akhirnya dapat mempengaruhi fungsi metabolisme sel, sedangkan pada
Pemberian fraksi 1 minyak atsiri daun sirih pada sel S. epidermidis
dengan perlakuan 1 MIC dan 2 MIC dapat mengakibatkan terjadinya
kebocoran sel dan perubahan ukuran sel. Kebocoran sel dapat diamati dari
tingkat kerusakan dinding sel dan membran sel. Derajat tingkat kerusakan
dinding sel dapat diukur dari jumlah ion Ca2+ dan ion K+ yang terdapat pada
dinding sel, sedagkan tingkat kerusakan membran dapat di ukur dari bahan –
bahan yang dilepaskan oleh sel yang dapat diserap pada panjang gelombang
260 nm untuk asam nukleat dan 280 nm untuk protein dengan menggunakan
spektofotometer UV-Vis (Carson et al., 2002). Menurut Burt
(2004) yang dikutip oleh Miksusanti (2009), Asam nukleat yang terdeteksi
pada panjang gelombang 260 nm adalah RNA dan turunan RNA yaitu
nukleotida (purin, pirimidin dan ribonukleotida), sedangkan senyawa protein
yang terdeteksi adalah tirosin dan triptofan. Meningkatnya jumlah
kandungan sel yang ditemukan pada permukaan sel menandakan terjadinya
kerusakan membran sel atau perubahan permeabilitas
Dari gambar 3 dapat diketahui bahwa pemberian konsentrasi fraksi 1
minyak atsiri daun sirih terhadap sel bakteri S. epidermidis dengan
konsentrasi 1 MIC dan 2 MIC memberikan perbedaan pada peningkatan
nilai absorbansi di panjang gelombang 260 nm dan 280 nm. Nilai absorbansi
untuk sel kontrol S.epidermidis pada panjang gelombang 260 nm adalah
0.423. Pada konsentrasi 1 MIC absorbansinya mengalami peningkatan
menjadi 1.539 dan pada konsentrasi 2 MIC terjadi peningkatan absorbansi
sekitar 2 kali yaitu 2.498. Pada panjang gelombang 280 nm, absorbansi untuk
0.437 menjadi 1.680 dan 3.010 secara berurutan. Dari hasil tersebut
menunjukkan bahwa peningkatan absorbansi protein pada panjang
gelombnag 280 nm lebih tinggi daripada absorbansi untuk asam nukleat di
panjang gelombang 260 nm. Hal ini menunjukkan bahwa semakin tinggi
dosis MIC yang diberikan, maka kebocoran metabolit seluler baik protein
maupun asam nukleat semakin meningkat. Hal ini sesuai dengan penelitian
yang dilakukan oleh Suliantari (2009) bahwa semakin tinggi konsentrasi
ekstrak daun sirih yang diberikan terhadap bakteri gram positif (S. aureus, B.
cereus dan L. monocytogenes) maka kebocoran asam nukleat dan protein dari
sel bakteri yang terjadi semakin tinggi pula.
Kandungan ion-ion logam yang berada dalam sel bakteri S. epidermidis
seperti Ca2+ dan K+ akan mengalami perubahan jika diberikan senyawa
antibakteri. Pemberian 1 MIC dan 2 MIC fraksi jam ke-1 minyak atsiri daun
sirih menyebabkan perubahan kandungan ion-ion Ca2+ dan K+ pada sel
medium tumbuh. Pada gambar 3 didapatkan bahwa nilai yang didapat untuk
ion Ca2+ untuk kontrol dan pemberian fraksi jam ke-1 minyak atsiri 1 MIC,
dan 2 MIC berturut-turut adalah 0.08 ppm, 36 ppm, dan 45 ppm. Sedangkan
untuk nilai ion K+ berturut-turut adalah 64 ppm; 80 ppm; 95 ppm. Dari hasil
ini didapatkan bahwa semakin tinggi konsentrasi yang diberikan maka
semakin tinggi pula kerusakan membran sel yang terjadi. Indikasi adanya
kerusakan membran sitoplasma adalah terjadinya kebocoran kandungan
ion-ion Ca2+ dan K+ merupakan tanda kerusakan permeabilitas membran (Cox
disebabkan oleh adanya ikatan hidrogen, hidrofobik dan kation Mg2+ dan
Ca2+ bersama fosfolipida.
Seperti yang terjadi pada kebocoran sel, makin tinggi konsentrasi MIC
fraksi jam ke-1 (F1) minyak atsiri daun sirih yang digunakan, maka morfologi
sel bakteri juga semakin mengalami perubahan dibandingkan sel normal.
Kerusakan morfologi sel bakteri diamati dengan menggunakan SEM
(Fathillah et al., 2009 ). Pada S. epidermidis perbesaran 10.000 kali
menunjukkan dalam keadaan normal berbentuk bulat dengan permukaan yang
licin seperti yang terlihat pada gambar 4.a. Dengan adanya perlakuan
pemberian F1 minyak atsiri daun sirih 1 MIC, terjadi perubahan morfologi
pada membran sel nya yaitu sel menjadi berlubang dengan permukaan yang
masih rata (gambar 4.b). Sedangkan perlakuan pada konsentrasi 2 MIC, sel
berlubang dan permukaannya menjadi mengkerut dan kasar (gambar 4.c).
Dari hasil penelitian ini terlihat bahwa pada perlakuan konsentrasi 1 MIC F1
minyak atsiri daun sirih, belum menyebabkan sel bakteri rusak berat
dibandingkan dengan perlakuan 2 MIC. Walaupun terjadi kerusakan struktur
sel dan sel kehilangan isinya (ion Ca2+ dan K+), namun keseluruhan bentuk
BAB VI
KESIMPULAN DAN SARAN
6.1. Kesimpulan
1. Fraksi minyak atsiri daun sirih yang berasal dari Balitro, Cimanggu. Bogor
memiliki presentase kadar yang dihasilkan secara berurutan untuk fraksi
1,2,3 dan 4 sebesar 0,061%; 0,034%; 0,027% dan 0,015%. dan memiliki
komponen kimia sebanyak 64 senyawa (F1), 56 senyawa (F2), 73
2. Fraksi Minyak atsiri daun sirih memiliki aktivitas antibakteri terhadap
bakteri S. mutan, S. epidermidis, dan B. subtilis. Nilai MIC yang diperoleh
dari setiap fraksi minyak atsiri terhadap S. epidermidis adalah 0,25 %
(v/v). B. subtilis >17,5% (v/v)., sedangkan S. mutan F1 sebesar 2,5%
(v/v) , F2 dan F3 sebesar1% (v/v)., dan F4 sebesar 0,25% (v/v).
3. Mekanisme penghambatan antibakteri fraksi 1 minyak atsiri daun sirih
terhadap S. epidermidis adalah merusak membran sel bakteri, yang
ditandai dengan terjadinya peningkatan pelepasan senyawa metabolit
6.2. Saran
1. Perlu dilakukan penelitian lebih lanjut secara invivo untuk mengetahui
efektifitas dan toksisitasnya.
2. Perlu dilakukan penelitian lebih lanjut terhadap bakteri patogen lain untuk
DAFTAR PUSTAKA
Agusta, A. 2000. Minyak Atsiri Tumbuhan Tropika Indonesia. Penerbit ITB.
Bandung.
AlFarisi, S . 2009. Uji Mekanisme Penghambatan Antibakteri Minyak Atsiri Daun Sirih (Piper Bettle Linn; Piperaceae ) Terhadap Staphylococcus
Epidermidis. Skripsi. Fakultas Kedokteran dan Ilmu Kesehatan UIN Jakarta.
Bilbiana,L., dan Hastowo,S. 1992. Mikrobiologi. Jakarta : Rajalawi Pers.
Brooks, G.F., Butel, J.S., dan Morse, S.A., 2005. Jawetz, Melnick & Adelberg’s
Mikrobiologi Kedokteran (Medical Microbiology). diterjemahkan oleh Eddy M, Kuntaman, Eddy BW, Ni Made M, Setio H, dan Lindawati A. Edisi 1. Jilid 1. Salemba Medika. Jakarta.
Carson, C.F., Brian, J.M., Riley, T.V., 2002. Mechanism of Action of Melaleuca alternifolia (Tea Tree) Oil on Staphylococcus aureus Determined by Time Kill, Lyses, Leakage, and Salt Tolerance Assays and Electron Microscopy. Antimicrobial Agent and Chemotherapy 6 : 1914-1920.
Chambers, HF. 2007. Goodman dan Gilman Dasar Farmakologi Terapi,
diterjemahkan oleh Cucu ., Ella, E., Winny, RS., Amalia, H., July, M. Edisi 10. Jilid 2. Penerbit Buku Kedokteran EGC. Jakarta.
Cowan, M.M. 1999. Plant product asd antimicrobial agents. J. Microbiology
Reviews 612 (4) : 564 – 582.
Cox, S.D., Mann, C.M., Markham, J.L., Bell, H.C., Gustafson, J.E., Warmington,
J.R. and Wyllie, S.G.. 2000. The Mode of Antibacterial Action of The
Essential Oil of Melaleuca Alternifolia (Tea Tree Oil). J of Applied Microbiology 88 : 170-175.
Didik, G., dan Mulyani, S. 2004. Ilmu Obat Alam (Farmakognosi) Jilid I. Penebar
Swadaya. Jakarta
Fathillah, A.R., Yusoff M, Rahim ZHA. The Effect of Psidium guajava and Piper
betle extracts on the Morphology of Dental Plaque Bacteria. Pak J Med Sci 2009;25(6):928-933.
Harapani, M., Agusta, A., dan Rahayu,DC. 1996. Komponen kimia minyak atsiri
dari dua macam sirih (daun kuning dan hijau). Prosiding Symposium
Tanaman Obat Dan Aromatic. Puslitbang biologi-LIPI. Bogor. 58-63.
Hermawan, A. 2007 . Pengaruh ekstrak daun sirih (piper betle l.) terhadap pertumbuhan staphylococcus aureus dan escherichia coli Dengan metode