Lampiran 4. Foto eugenol hasil isolasi
Lampiran 5. Foto Metil Nitrat Lampiran 6. Foto Metil Eugenol
Lampiran 7. Hasil analisa eugenol dan metil eugenol melalui analisa kromatografi lapis tipis Keterangan :
E = Eugenol Me = Metil eugenol
Rf = faktor retensi (jarak yang ditempuh noda/jarak yang ditempuh pelarut)
aseton
etanol
n-heksana
kloroform Rf=0.82
Rf=0.72
Rf=0.57
Rf=0.27
aseton
Lampiran 8. Perhitungan massa teori dari metil eugenol
OK
OCH3
CH2-CH=CH2
+ CH3NO3 + KNO3
Kalium Eugenol Metil Eugenol Kalium Nitrat
OCH3
0.05 mol = gram178 gr/mol gram Metil eugenol = 8.9 gram
volume metil eugenol praktek = 6.4 ml
massa jenis=
Jadi massa metil eugenol teori = 8.9 gram
Sehingga metil eugenol yang diperoleh adalah = massa metil eugenol praktek
massa metil eugenol toeri X 100% =
6.656 gram 8.9 gram
X 100%
DAFTAR PUSTAKA
Alma,M.H., M.Ertas,S., Nitz,h., Kollmannsberger, 2007. Chemical Composition
And Content Of Essensial Oil From The Bud Of Cultivated Turkish Clove (Syzgium aromaticum L.),J.Bio Resources. Volume 2. Halaman 265
Anonim. 2006. Standar Nasional Indonesia Minyak Cengkeh SNI 06-2387-2006
Anonim. 2005. Statistik Perdagangan Luar Negeri Indonesia-Ekspor. Jakarta: Balai Pusat Statistik
Anonimous. 1976. The Merck Index. Merck and Co.Inc. New Jersey. USA
Anwar, C. 1994. The Convertion Of Eugenol Into More Valuable Substances. Doctoral dissertation. Yogyakarta: Gadjah Mada University
Bahl, A. 2004. Organic Chemistry. New Delhi: S.Chand & Company LTD
Beroza, M. 1970. Chemicals Controlling Insect Behavior. New York : Academic Press Black,A.P dan Babers, F.A. 2005. Organic Syntheses A publication of Relief Methods for
The Preparation of Organic Compounds. Washington D.C : The National Academies Press
Bresnick,S.M.D. 1996. High – Yield Organic Chemistry. USA: William & Wilkins Inc Bulan,R. 2004. Reaksi Asetilasi Dan Oksidasi Metil Isoeugenol. Program Studi Teknik
Kimia [Tesis]. FMIPA. Universitas Sumatera Utara
Council of Europe- comitte of expert on flavouring substances. 1999. Publication Datasheet on Methyl Eugenol. Document RD 4.14/2-45 submitted by the delegation of Italy for the 45th meeting in Zurich
Fessenden dan Fessenden. 1982. Kimia Organik. Edisi ketiga. Jakarta: Erlangga Guenther ,E. 1987. Minyak Atsiri jilid I. terjemahan Ketaren S. Jakarta : UI Press
Griffin Jr. R,W. 1969. Modern Organic Chemistry. Tokyo : Mc Crow Hill Book Company Hart, H. 2003. Kimia Organik . Jakarta : Erlangga
Jirovetz, L. 2010. Medical Value Of Clove. University Of Vienna. Department Pharmacy and Diagnostic. Austria
Kardinan, A. 2003. Pengendalian Hama Tanpa Pestisida. Jakarta: Agro media Pustaka
Ketaren,S. 1985. Pengantar Teknologi Minyak Atsiri. Jakarta: Penerbit Balai Pustaka
March, J. 1984. Advanced Organic Chemistry. Singapore : Mc Crow Hill International Book Co
Mulja, H. 1995. Analisis Instrumental. Surabaya : Airlangga University Press
Ngadiwiyana, I. 2004. Sintesis Metil Eugenol Dan Benzil Eugenol Dari Minyak Daun Cengkeh. Fakultas Matematika Dan Ilmu Pengetahuan Alam. Semarang : UNDIP Purba,J. 2000. Sintesis senyawa 1-(3,4 dimetoksi fenil)-2-amino-2-siano propana Turunan
Eugenol Melalui Pembentukan Senyawa Keton [Tesis]. Yogyakarta : UGM Riswiyanto, S. 2009. Kimia Organik. Jakarta : Erlangga
Ratnawati, D. 2014. Sintesis Metil Eugenol Sebagai Bahan Dasar Pembuatan Turunan Benzofenon Yang Berfungsi Sebagai Tabir Surya [Skripsi]. Fakultas MIPA. Bengkulu : UNIB
Rudyanto,M dan Hartanti, L. 2006. Konversi Satu Tahap Eugenol Menjadi Metil Isoeugenol Dengan Iradiasi Gelombang Mikro Pada Kondidi Bebas Pelarut. Surabaya: Universitas Katolik Widya Mandala
Sastrohamidjojo, H. 2004. Kimia Minyak Atsiri. Yogyakarta: UGM
Silverstein. 1986. Penyelidikan Spektroskopi Senyawa Organik. Jakarta: Erlangga
Soesanto.H. 2006. Pembuatan Isoeugenol Dari Eugenol Menggunakan Pemanasan Gelombang Mikro [Skripsi]. Departemen Teknologi Industri Pertanian. Bogor : IPB Sutthanont, Nataya, Choochote,W., Tuetun, B., Junkum, A., Jitpakdi, A., Chaithong, U.,
Riyong, D., and Pitasawat, B. 2009. Chemical Composition and Larvicidal Activity of Edible Plant Derived Essential Oils Against The Pyrethroid-Susceptible and Resistant Strains of Aedes egypti (diptera: culicidae). Department of parasitology. Faculty of medicine. Thailand : Chiang Mai University
Taufik, M., Suharjono Triatmojo, Yuni Erwanto, Umar Santoso dan Novita Kristanti .2011. Aktivitas Antibakteri Minyak Cengkeh Terhadap Bakteri Patogen. Malang
Tohawa,J.2012. Manfaat Eugenol Cengkeh Dalam Berbagai Industri di Indonesia. Balai Penelitian Tanaman Industri dan Penyegar.Jawa Barat – Indonesia
Vogel, A.I. 1985. Analisis Anorganik Kualitatif Makro Dan Semimikro. Edisi kelima. Jakarta : PT. Kalman Media Pusaka
Widayat., Cahyono, B dan Ngadiwiyono. 2012. Rancang Bangun dan Uji Alat Proses Peningkatan Cengkeh pada Klaster Minyak Atsiri Kabupaten Batang. Program Studi Ilmu Lingkungan Program Pasca Sarjana. Semarang : UNDIP
BAB 3
METODE PENELITIAN
3.1 Alat
Alat –alat yang digunakan dalam penelitian ini adalah :
Alat spektroskopi FT-IR Agilent Technologies
Alat GC-MS QP2010S Shimadzu
Alat rotarievaporasi Heidolph WB 2000
Beaker glass pyrex
Corong pisah pyrex
Corong kaca pyrex
Corong penetes quickfit
Hotplate stirrer IKA RH basic 1
Kondensor bola pyrex
Bahan- bahan yang digunakan dalam penelitian ini adalah : Minyak cengkeh
Natrium hidroksida p.a Merck
Kalium karbonat p.a Merck
n-heksana p.a Merck
Air suling -
Natrium sulfat anhidrous p.a Merck
Calsium klorida anhidrous p.a Merck
Kertas saring -
Metanol p.a Merck
Asam sulfat pekat p.a Merck
Asam nitrat pekat p.a Merck
H2SO4 25% p.a Merck
Indikator pH universal Merck
Plat aluminum GF254 Merck
3.3 Prosedur penelitian
3.3.1.Isolasi Eugenol dari Minyak Cengkeh
Sebanyak 20.8 gram NaOH pellet, dimasukkan ke dalam gelas Beaker dan dilarutkan dengan 52 ml air suling. Larutan NaOH tersebut ditambahkan kedalam 100 ml minyak cengkeh sedikit demi sedikit sambil diaduk menggunakan pengaduk magnet. Campuran tersebut dimasukkan kedalam corong pisah dan diekstraksi menggunakan pelarut n-heksana hingga terbentuk dua lapisan. Diambil lapisan bawah (fraksi polar) dan dihidrolisis dengan menambahkan H2SO4 25% sampai pH=3. Hasil hidrolisis diekstraksi dengan menggunakan
pelarut n-heksana hingga terbentuk dua lapisan dan diambil lapisan atas (fraksi n-heksan), kemudian ditambahkan dengan Na2SO4 anhidrous, didiamkan dan disaring. Fitrat hasil
penyaringan diuapkan dengan menggunakanrotarievaporator dan diperoleh eugenol sebagai residu. Eugenol tersebut dimurnikan kembali dengan destilasi vakum. Destilat yang diperoleh dianalisis melalui kromatografi lapis tipis menggunakan berbagai pelarut sebagai developer dan adsorben plat silika aluminium GF254 serta penampak noda dengan lampu UV GL-58,
diuji sifat fisiknya meliputi indeks bias, densitas, aroma dan warna, juga dilakukan analisis dengan spektroskopi FT-IR.
3.3.2. Pembuatan Metil Nitrat
Sebanyak 100 ml H2SO4(p)dimasukkan ke dalam gelas Erlenmeyer,kemudian ditambahkan
pengaduk magnet. Didinginkan hingga pada suhu 150C, lalu ditambah metanol sebanyak 25 ml setetes demi setetes sampai pada suhu 200C sambil diaduk dengan menggunakan pengaduk magnet. Setelah itu, dimasukkan campuran tersebut kedalam corong pisah dan didiamkan hingga terbentuk dua lapisan. Diambil lapisan atas, ditambahkan NaCl jenuh dan didiamkan hingga terbentuk dua lapisan. Kemudian diambil lapisan bawah dan di ukur volume metil nitrat yang diperoleh.
3.3.3 Sintesis Metil Eugenol Dengan Menggunakan Metil Nitrat
Sebanyak 6.9 gram (0.05mol) K2CO3(s) dimasukkan ke dalam gelas Beaker. Kemudian
dilarutkan dengan 50 ml aseton. Larutan kalium karbonat tersebut dimasukkan kedalam labu leher tiga. Kemudian ditambahkan sebanyak 7.7 ml (0.05 mol) eugenol hasil isolasi dari minyak cengkeh dan diaduk dengan menggunakan pengaduk magnet. Didinginkan sampai pada suhu 100C sambil diaduk. Ditambahkan 3.3 ml (0.052mol) metil nitrat setetes demi setetes melalui corong penetes selama 1 jam sambil diaduk. Direfluks selama 2 jam dan dipantau hasil reaksi dengan analisa KLT menggunakan plat silika GF254, pengembang
kloroform dan menggunakan lampu UV untuk melihat bercak noda pada plat silika. Kemudian campuran hasil refluks didinginkan dan dimasukkan kedalam corong pisah. Ditambahkan dengan aquadest hingga terbentuk dua lapisan. Lapisan atas diekstraksi menggunakan pelarut n-heksana dan diambil lapisan atas (fraksi n-heksana). Lapisan atas tersebut dicuci berturut-turut tiga kali dengan NaOH 10%, satu kali dengan air suling, satu kali dengan asam sulfat encer dan dicuci kembali dengan air suling, sehingga lapisan atas (fraksi n-heksana) bebas eugenol. Kemudian dikeringkan dengan Na2SO4(s) anhidrous,
didiamkan dan disaring. Fitrat hasil penyaringan diuapkan dengan menggunakan rotarievaporator dan diperoleh metil eugenol sebagai residu. Metil eugenol hasil pemisahan dimurnikan kembali dengan destilasi vakum yang kemudian dilanjutkan dengan analisis melalui kromatografi lapis tipis menggunakan berbagai pelarut sebagai pengembang dan adsorben plat silika aluminium GF254 serta penampak noda dengan lampu UV GL-58, juga
3.3.4. Analisis Eugenol dan Metil eugenol
a. Analisis melalui Kromatografi LapisTipis
Pemeriksaan hasil isolasi eugenol dan hasil sintesis metil eugenol dilakukan dengan menggunakan plat aluminium GF254, penampak noda lampu UV dan menggunakan pelarut
aseton, etanol, n-heksana dan kloroform sebagai pengembang.
b. Analisis Dengan spektroskopi FT-IR
Pemeriksaan hasil isolasi eugenol dan hasil sintesis metil eugenol dengan spektroskopi FT-IR dilakukan dengan mengambil sedikit cuplikan dari masing-masing eugenol dan metil eugenol dan ditempatkan di antara plat garam NaCl tanpa pengukuran jarak. Kemudian ditempatkan plat pada sel sesuai dalam ruang spektrofotometer dan diukur absorbansinya dengan alat spektrofotometer FT-IR.
c. Analisis Dengan GC-MS
3.4Bagan Penelitian
3.4.1 Isolasi Eugenol Dari Minyak Cengkeh
100 ml minyak cengkeh
dimasukkan kedalam gelas Beaker
20,8 gram NaOH(s)
dimasukkan kedalam beaker gelas Beaker
dilarutkan dengan aquadest hingga seluruh NaOH larut
ditambahkan larutan NaOH sedikit demi sedikit kedalam minyak cengkeh sambil diaduk dengan magnetik stirer
dimasukkan kedalam corong pisah
diekstraksi dengan n-heksan hingga terbentuk dua lapisan
lapisan bawah lapisan atas
dihidrolisa dengan H2SO4 25% hingga pH=3 sambil diadukdengan menggunakan magnetik stirer
dimasukkan kedalam corong pisah
diekstraksi kembali dengan n-heksan hingga membentuk dua lapisan
lapisan bawah lapisan atas
3.4.2 Pembuatan Metil Nitrat
100 ml H2SO4(p)
dimasukkan ke dalam gelas erlenmeyer
ditambahkan HNO3(p) sebanyak 50 ml
diaduk dengan menggunakan magnetik stirrer
didinginkan sampai pada suhu 150C
ditambahkan metanol setetes demi setetes sampai pada suhu 200C sambil diaduk dengan menggunakan magnetik stirrer
Campuran
dimasukkan ke dalam corong pisah
dididamkan hingga terbentuk dua lapisan
Lapisan atas Lapisan bawah
ditambahkan dengan NaCl jenuh
didiamkan hingga terbentuk dua lapisan
Lapisan atas Lapisan bawah
diukur volume metil nitrat yang diperoleh
3.4.3 Sintesis Metil Eugenol Dengan Menggunakan Metil Nitrat
6.9 gram K2CO3(s)
dimasukkan ke dalam gelas beaker dilarutkan dengan 50 ml aseton
Larutan bening
dimasukkan ke dalam labu leher tiga
ditambahkan 7.7 ml eugenol hasil isolasi
diaduk dengan menggunakan magnetik stirrer
didinginkan sampai pada suhu 100C
ditambahkan 3.2 ml metil nitrat setetes demi setetes melalui corong penetes selama 1 jam sambil diaduk dengan menggunakan magnetik stirrer
direfluks selama 2 jam pada suhu 60o-700C
didinginkan
Campuran
dimasukkan ke dalam corong pisah
ditambahkan dengan aquadest hingga terbentuk dua lapisan
Lapisan atas Lapisan bawah
diekstraksi dengan menggunakan pelarut n-heksan hingga terbentuk dua lapisan didiamkan
dicuci berturut-turut tiga kali dengan NaOH 10% ,satu kali dengan air suling, satu kali dengan asam sulfat encer dan dicuci kembali dengan air suling sehingga bebas eugenol
Lapisan bawah
Lapisan atas Lapisan atas
Lapisan bawah
ditambahkan Na2SO4 anhidrous
didiamkan
disaring
Filtrat Residu
dievaporasi filtrat sampai pelarut habis
Metil eugenol hasil pemisahan
Analisa KLT Analisa GCMS Analisa FTIR didestilasi vakum
Hasil
BAB 4
HASIL DAN PEMBAHASAN
4.1 Hasil Penelitian
4.1.1. Isolasi eugenol dari minyak cengkeh
Dari hasil penelitian yang telah dilakukan dari 100 ml minyak cengkeh yang digunakan, eugenol yang diperoleh adalah 54 ml ( rata-rata 54%). Hasil uji sifat fisik dari eugenol yang meliputi indeks bias, densitas, aroma dan warna adalah memberikan nilai berturut-turut 1.0634 g/ml (densitas), 1.5364 (indeks bias), beraroma khas cengkeh dan merupakan cairan berwarna kuning.
Analisis melalui kromatografi lapis tipis dengan menggunakan beberapa pelarut sebagai pengembang memberikan harga Rf berturut-turut yakni 0.82 (aseton), 0.72 (etanol), 0.27 (n-heksana) dan 0.57 (kloroform) dengan satu noda. Hasil analisis spektroskopi FT-IR dari eugenol hasil isolasi (Gambar 4.1) adalah sebagai berikut :
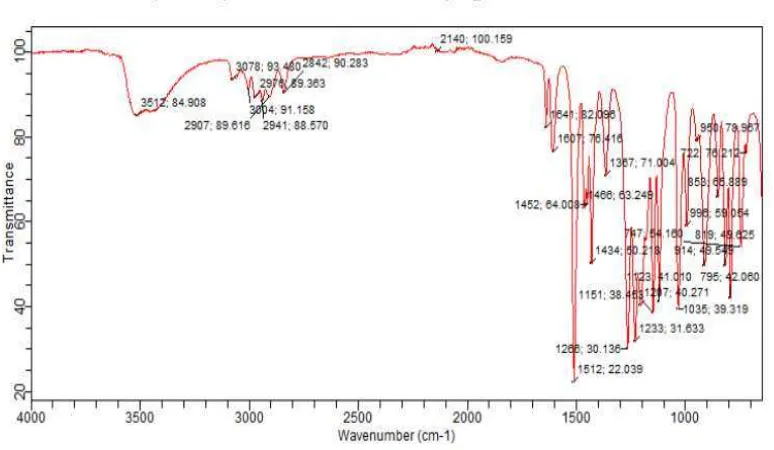
Gambar 4.1 Spektrum Eugenol
Dari data spektroskopi FT-IR, spektrum eugenol memberikan puncak-puncak serapan pada daerah bilangan gelombang 3512,84 cm-1 ; 3078,93 cm-1; 2976,89 cm-1; 1641,82 cm
-1
4.1.2 Pembuatan Metil Nitrat
Metil nitrat merupakan hasil reaksi substitusi antara metanol dengan asam nitrat dengan adanya asam sulfat. Dari 25 ml metanol yang digunakan, diperoleh metil nitrat sebanyak 20 ml yang berupa cairan bening.
4.1.3 Sintesis Metil Eugenol Dengan Menggunakan Metil Nitrat
Pada penelitian ini, metil eugenol yang didapatkan dari 7.7 ml eugenol yang digunakan adalah sebanyak 6.4 ml ( 74.78% ). Metil eugenol yang dihasilkan merupakan cairan kuning bening. Analisis melalui kromatografi lapis tipis dari berbagai pelarut sebagai pengembang memberikan harga Rf berturut-turut yakni 0.85 (aseton), 0.80 (etanol), 0.20 (n-heksana) dan 0.69 (kloroform) dengan satu noda. Hasil analisis spektroskopi FT-IR dari metil eugenol hasil sintesis (Gambar 4.2) adalah sebagai berikut :
Gambar 4.2 Spektrum Metil Eugenol
4.1.4 Analisis Metil Eugenol Hasil Sintesis Dengan GC-MS
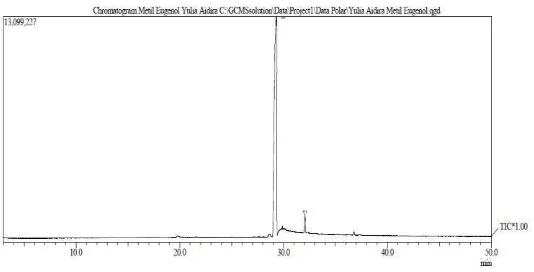
Hasil sintesis dianalisis dengan GC-MS memberikan kromatogram (Gambar 4.3) dengan kemurnian metil eugenol sebesar 97.70 %.
Gambar 4.3 Kromatogram Hasil Sintesis
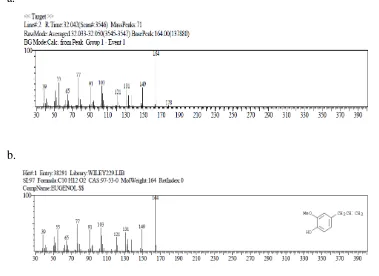
1. Puncak dengan waktu retensi (RT) 29,375 menit merupakan senyawa dengan rumus molekul C11H14O2. Data spektrum massa menunjukkan puncak ion molekul pada m/e 178
diikuti puncak fragmentasi pada m/e 163, 147, 135, 115, 103, 91, 77, 65, 51 dan 41 (Gambar 4.4). Dengan membandingkan data spektrum yang diperoleh dengan data spektrum library WILEY229 LIB, maka senyawa tersebut adalah metil eugenol.
a.
b.
Gambar 4.4 Spektrum Massa Senyawa Metil Eugenol Hasil Sintesis Keterangan :
2. Puncak dengan waktu retensi (RT) 32,044 menit merupakan senyawa eugenol yang sisa sebanyak 2.30% dengan rumus molekul C10H12O2. Data spektrum menunjukkan puncak
ion molekul pada m/e 164 diikuti puncak-puncak fragmentasi pada 149, 131, 121, 103, 91, 77, 65, 55 dan 39 (Gambar 4.5). Dengan membandingkan data spektrum yang diperoleh dengan data spektrum library WILEY229 LIB, maka senyawa tersebut adalah eugenol.
a.
b.
Gambar 4.5 Spektrum Massa Eugenol
4.2. Pembahasan
4.2.1 Isolasi Eugenol Dari Minyak Cengkeh
Eugenol diperoleh dari hasil isolasi minyak cengkeh dilakukan dengan reaksi penggaraman dan reaksi hidrolisis. Reaksi yang terjadi pada isolasi eugenol (Gambar 4.6) adalah sebagai berikut:
Gambar 4.6 Reaksi Pembentukan Eugenol Hasil Isolasi (Sastrohamidjojo, 2004)
0.82 (aseton), 0.72 (etanol), 0.27 (n-heksan) dan 0.57 (kloroform) dengan menunjukkan hanya ada satu noda.
Hasil analisis spektrofotometri inframerah (FT-IR) dari eugenol hasil isolasi memberikan puncak serapan pada daerah bilangan gelombang (ʋ) 3512,84 cm-1 yang merupakan vibrasi O-H, kemudian didukung oleh ʋ=3078,93 cm-1 yang menunjukan vibrasi stretching C-H sp2 (=CH-), ʋ= 2976,89 cm-1 menunjukkan vibrasi ulur C-H pada CH2,
ʋ=1233,31 cm-1
menunjukkan vibrasi ulur asimetrik C-O-C, ʋ=1035,39 cm-1 menunjukkan vibrasi ulur simetrik C-O-C untuk alkil eter, ʋ=1641,82 cm-1 menunjukkan gugus C=C aromatik, ʋ=1434,50 cm-1 menunjukkan gugus CH2 dan gugus vinil ditunjukkan pada
ʋ=950,79 cm-1 (Gambar 4.1).
4.2.2 Pembuatan Metil Nitrat
Metil nitrat yang dihasilkan merupakan hasil reaksi antara metanol dengan asam nitrat dengan adanya asam sulfat untuk mempercepat reaksi dan mempertahankan suasana asam dalam pembentukannya.
H2SO4(p ) + HNO3 HSO4- + NO2+ + H2O
CH3OH + NO2+ CH3ONO2
Metil Nitrat
(Fessenden, 1986).
Terbentuknya metil nitrat secara kulitatif didasarkan pada uji kelarutannya terhadap alkohol, eter dan air suling. Metil nitrat tersebut tidak larut dalam air suling tetapi larut dalam alkohol dan eter. Uji kualitatif lainnya yaitu dengan penambahan FeSO4. Metil nitrat
ditambahkan dengan asam sulfat pekat, kemudian ditambahkan FeSO4 secara perlahan-lahan
dalam suasana dingin sehingga terbentuk dua lapisan dan diamkan hingga terbentuk cincin cokelat diantara kedua lapisan yang menunjukkan adanya ion nitrat, dengan reaksi sebagai berikut :
Fe2(SO4)3.4NO Cincin Cokelat
2NO3- + 4H2SO4 + 6Fe2+ 6Fe3+ + 2NO + 4SO42- + 4H2O
4.2.3 Sintesis Metil Eugenol Menggunakan Metil Nitrat
Dari penelitian yang telah dilakukan metil eugenol diperoleh dari reaksi antara metil nitrat dengan kalium eugenolat yang dihasilkan dari reaksi antara kalium karbonat dengan eugenol hasil isolasi dari minyak cengkeh dalam pelarut aseton pada kondisi refluks.
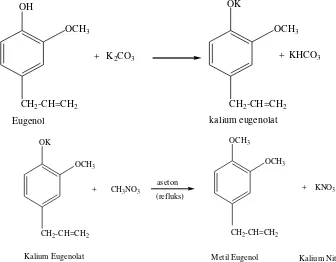
Reaksi yang terjadi pada pembuatan metil eugenol (Gambar 4.7) adalah sebagai berikut :
OH
Kalium Eugenolat Metil Eugenol Kalium Nitrat
OCH3
OCH3
CH2-CH=CH2 aseton
(refluks)
Gambar 4.7 Reaksi Pembentukan Metil Eugenol Hasil Sintesis
Eugenol mempunyai hidrogen yang terikat pada atom oksigen yang mudah diserang oleh suatu basa, dalam hal ini digunakan kalium karbonat (K2CO3) untuk membentuk ion
eugenolat, garam tersebut akan mudah larut dalam air dan mudah diserang dengan gugus pengalkilasi yaitu metil nitrat. Tahap berikutnya yaitu mereaksikan garam kalium eugenolat dengan agen pengalkilasi metil nitrat, dimana garam kalium eugenolat dapat berperan sebagai nukleofil dan metil nitrat sebagai elektrofil menghasilkan senyawa metil eugenol.
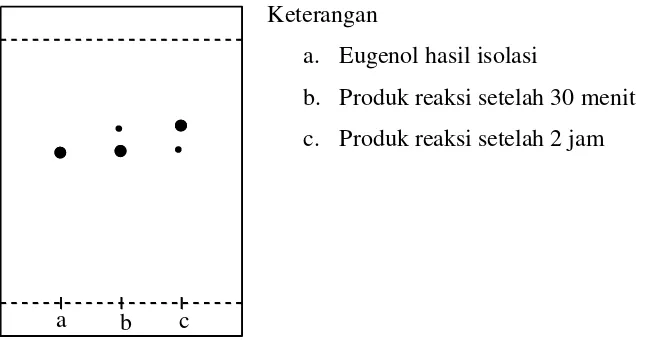
Untuk mengetahui sejauh mana berlangsungnya reaksi, dilakukan pemantauan setiap selang setengah jam melalui analisis KLT menggunakan plat aluminium dengan adsorben silika gel GF254, penampak noda lampu UV dan kloroform sebagai developer.
Keterangan
a. Eugenol hasil isolasi
b. Produk reaksi setelah 30 menit c. Produk reaksi setelah 2 jam
Gambar 4.8 Kromatogram Analisis KLT Produk Reaksi
Produk reaksi yang telah diperoleh dipisahkan dari eugenol dengan penambahan berturut-turut dengan NaOH 10%, air suling, asam sulfat encer dan air suling kembali. Produk hasil pemurnian tersebut dianalisis kembali melalui kromatografi lapis tipis dengan menggunakan berbagai pelarut sebagai pengembang yang memberikan harga Rf berturut-turut yakni 0.85 (aseton), 0.80 (etanol), 0.20 (n-heksana) dan 0.69 (kloroform) hanya menunjukkan satu noda. Dari 7.7 ml eugenol (8.2 gram) yang digunakan, menghasilkan metil eugenol sebanyak 6.4 ml (6.65 gram) atau sekitar 74.78 %.
Hasil analisis spektrofotometri inframerah (FT-IR) dari metil eugenol hasil sintesis menunjukkan hilangnya vibrasi gugus –OH pada bilangan gelombang 3512,84 cm -1 , kemudian didukung oleh puncak serapan pada daerah bilangan gelombang (ʋ) 3077,94 cm-1 yang merupakan vibrasi ulur C-H aromatik, ʋ=3000-2850 cm-1 menunjukkan vibrasi ulur C-H alkil, ʋ=1641,83 cm-1 vibrasi ulur C=C olefin, ʋ=1261,32 cm-1 merupakan vibrasi ulur asimetrik C-O-C eter, ʋ=1030,32 cm-1menunjukkan vibrasi ulur simetrik dari C-O-C untuk aril alkil eter dan ʋ=955,78 cm-1 adalah vibrasi stretching C-H dari olefin (Gambar 4.2). Indikasi keberhasilan lainnya yaitu ditandai dengan adanya lalat-lalat buah yang berdatangan di sekitar hasil reaksi karena metil eugenol memiliki aroma khas (sebagai atraktan) dalam menarik lalat buah.
4.2.4 Analisis Hasil Sintesis Dengan GC-MS
1. Berdasarkan hasil analisis GC-MS, metil eugenol yang diperoleh adalah 97.70% Spektrum massa dari metil eugenol (metil eugenil eter) memberikan puncak ion molekul M+ dengan harga m/e adalah 178 yang merupakan massa molekul metil eugenol diikuti puncak
fragmentasi pada m/e 163 (M-CH3)+, 147 (M-OCH3)+, 135 (163-CO)+, 115 (147-HOCH3)+,
103(135-HOCH3)+, 77(115-C3H2)+ atau (103-C2H2)+ dan 51( 77-C2H2)+ . Pola fragmentasi
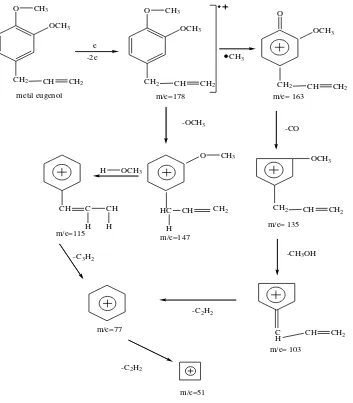
dari senyawa metil eugenol tersebut secara hipotesis (Gambar 4.9).
O
Gambar 4.9 Pola Fragmentasi Metil Eugenol
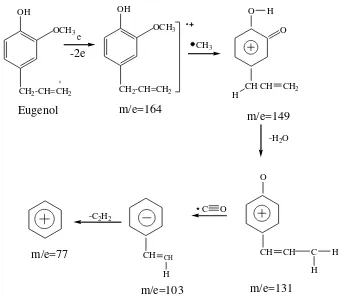
2. Berdasarkan hasil analisis GC-MS, masih terdapat senyawa eugenol sebesar 2.30%. Spektrum massa dari eugenol memberikan puncak ion molekul M+ dengan harga m/e adalah 164 yang merupakan massa molekul eugenol yang diikuti puncak fragmentasi pada m/e 149 (M-CH3)+, 131 (149-H2O)+, 103 (131-CO)+,
Pola fragmentasi dari senyawa eugenol tersebut secara hipotesis (Gambar 4.10).
BAB 5
KESIMPULAN DAN SARAN
5.1Kesimpulan
Dari penelitian yang telah dilakukan, dapat disimpulkan :
1. Eugenol dapat diisolasi dari minyak cengkeh melalui reaksi penggaraman menggunakan NaOH dilanjutkan ekstraksi dengan menggunakan n-heksana dan diikuti hidrolisis menggunakan H2SO4 25%, dimana dari sebanyak 100 ml minyak cengkeh yang
digunakan diperoleh eugenol berwarna kuning muda rata-rata 54 ml (54 % v/v).
2. Metil eugenol dapat disintesis melalui eterifikasi eugenol dengan metil nitrat dengan bantuan pereaksi K2CO3 dalam pelarut aseton pada kondisi refluks, dimana dari sebanyak
7.7 ml (8.2 gram) eugenol yang digunakan diperoleh 6.656 gram (74.78%) metil eugenol.
5.2. Saran
1. Diharapkan untuk peneliti selanjutnya dapat mengembangkan pengujian aktivitas metil eugenol selain sebagai bahan atraktan, antibakteri maupun antioksidan.
2. Diharapkan untuk peneliti selanjutnya, sebelum melakukan pembuatan metil eugenol secara industri dapat melakukan studi kelayakan untuk membandingkan pereaksi metil nitrat, metil iodida maupun dimetil sulfat untuk pembentukan metil eugenol.
BAB 2
TINJAUAN PUSTAKA
2.1Minyak Cengkeh
Minyak cengkeh merupakan minyak atsiri yang berasal dari tanaman cengkeh (Gambar 2.1). Indonesia merupakan salah satu negara penghasil minyak atsiri yang cukup penting di dunia. Diantaranya minyak atsiri yang terkenal adalah minyak cengkeh (Anonim, 2005).
Gambar 2.1 Foto Tanaman Cengkeh (Syzigium aromaticum)
Senyawa yang paling penting dalam minyak cengkeh adalah senyawa eugenol, sehingga kualitas minyak cengkeh ditentukan oleh kandungan senyawa tersebut. Dalam persyaratan mutu minyak daun cengkeh SNI 06-2387-2006 kandungan eugenol adalah 78% (Anonim, 2006). Sistematika tanaman cengkeh (Syzigium aromaticum) adalah sebagai berikut:
Divisio : Spermatophyta Sub-divisio : Angiospermae Klas : Dicotyledoneae Sub-klas : Choripetalae Ordo : Myrtales Family : Eugenia
Spesies : Eugenia Carryophyllus
5-6%. Komponen utama minyak cengkeh adalah eugenol yaitu sekitar 70-90% dan merupakan cairan tak berwarna atau kuning pucat, bila terkena cahaya matahari berubah menjadi coklat hitam yang berbau spesifik (Bulan,2004). Selain eugenol, minyak cengkeh juga mengandung senyawa lain seperti asetil eugenol ( Gambar 2.2) dan beta-caryophyllene (Gambar 2.3). Minyak cengkeh dapat diperoleh dari tanaman cengkeh bagian daun, batang/gagang dan bunga (Guenther,1987).
O
OCH3
CH2
C CH3
O
CH CH2
Gambar 2.2 Struktur asetil eugenol (Sastrohamidjojo,2004)
Gambar 2.3 Struktur beta-caryophyllene (Sastrohamidjojo, 2004)
Minyak cengkeh yang diperoleh dari bunga, batang maupun daun dari tanaman cengkeh mampu menghambat pertumbuhan organisme, termasuk diantaranya mikroba, serangga dan tanaman pengganggu ( Taufik dkk,2011).
2.2Eugenol
Gambar 2.4 Struktur Eugenol (Sastrohamidjojo,2004)
Nama : eugenol
Rumus molekul : C10H12O2
Berat molekul :164,20 g/mol
Penampilan fisik : cairan tidak berwarna hingga kekuningan Titik leleh : -9,20C
Titik didih : 2550C Indeks bias : 1.537 Densitas : 1.0663 g/ml (Anonimous,1976).
2.2.1 Reaksi-Reaksi Kimia Terhadap Eugenol
Dalam senyawa eugenol terkandung beberapa gugus fungsional, yaitu metoksi
(-OCH3), alil (-CH2-CH=CH2), fenol(-OH) dan cincin aromatik. Cincin aromatik dapat
mengalami reaksi substitusi elektrofilik pada posisi orto terhadap gugus hidroksi, pada posisi para terhadap metoksi atau posisi orto terhadap propilen, begitu juga dengan gugus olefin yang dapat ditransformasi menjadi gugus lain melalui reaksi adisi, reduksi, oksidasi dan epoksidasi. Ketiga senyawa aktif tersebut dengan menggunakan pereaksi-pereaksi tertentu dapat ditransformasi menjadi gugus-gugus lain membentuk senyawa-senyawa lain seperti isoeugenol, eugenol asetat, isoeugenol asetat, benzil alkohol, benzil isoeugenol, metil eugenol, eugenol etil eter, vanillin dan sebagainya (Sastrohamidjojo,1981 dan Tohawa, 2012). Beberapa reaksinya adalah sebagai berikut:
1. Reaksi Oksidasi Terhadap Eugenol
Vanilin dapat diperoleh melalui reaksi oksidasi terhadap eugenol (Gambar 2.6). Eugenol terlebih dahulu di isomerisasi dengan menggunakan KOH dalam glikol menghasilkan
OH
OCH3
isoeugenol (Gambar 2.5). Isoeugenol yang diperoleh dioksidasi dengan menggunakan nitribenzena dalam dimetilsulfoksida (Sastrohamidjojo, 2004).
OH
Gambar 2.5 Reaksi Pembuatan Vanilin (Sastrohamidjojo,2004) 2. Reaksi Asetilasi Terhadap Eugenol
Asetilasi eugenol (Gambar 2.6) dapat dilakukan dengan menggunakan pereaksi anhidrida asetat yang direfluks pada suhu 1300C selama 3 jam
CH3
Eugenol Anhidrida asetat asetil eugenol Asam asetat
3. Reaksi Asilasi Terhadap Eugenol Dengan Menggunakan Benzoil Klorida
Asilasi eugenol dilakukan mula-mula dengan reaksi penggaraman membentuk garam eugenolat, kemudian ditambahkan benzoil klorida dan campuran direfluks pada suhu 1200C selama 1 jam sehingga diperoleh eugenil benzoat ( Gambar 2.7).
OH
Gambar 2.7 Pembuatan Eugenil benzoat (Sastrohamidjojo,2004)
2.2.2 Metil Eugenol
Senyawa metil eugenol merupakan turunan eugenol yang dipergunakan sebagai atraktan (penarik/pemikat untuk datang) untuk menarik lalat jantan dalam pengendalian populasi lalat buah Bactrocera dorsalis (Kardinan et al., 1998).
Berikut ini struktur (Gambar 2.9), sifat fisik dan sifat kimia dari metil eugenol secara umum.
OCH
3OCH
3CH
2-CH=CH
2Nama : metil eugenol pengendalian yang ramah lingkungan dan terbukti efektif, dimana pengendalian hama lalat buah dilakukan dalam tiga cara yaitu, mendeteksi atau memonitor populasi lalat buah, menarik lalat buah kedalam perangkap kemudian disterilkan atau dimatikan dan mengacaukan lalat buah dalam perkawinan,berkumpul dan cara makan. Pada penyelidikan yang telah dilakukan di Hawai, senyawa ini mampu digunakan sebagai atraktan terhadap lalat buah oriental Dacus dorsalis Handel jantan. Pemakaian secara kombinasi antara metil eugenol dengan insektisida juga dapat membunuh lalat buah oriental dalam kurun waktu beberapa bulan. Metil eugenol dibuat dengan mereaksikan eugenol dengan dimetilsulfat (Gambar 2.9) dalam suasana basa.
OH
Gambar 2.9 Reaksi Pembuatan Metil Eugenol (Purba,2000).
2.3Metil Nitrat
Metil nitrat (Gambar 2.10) dapat dihasilkan melalui cara destilasi campuran dari asam nitrat dan metanol.
Gambar 2.10 Metil Nitrat (http://en.wikipedia.metil-nitrat.org.com)
Namun, pembuatan metil nitrat dengan cara mendestilasi campuran asam nitrat dan metanol tidak disarankan karena sekali-kali dapat menimbulkan ledakan kecil kemudian terdekomposisi memberikan warna violet.
HNO3 CH3NO3 + H2O CH3OH +
Metanol Asam nitrat Metil nitrat
Selain itu, metil nitrat juga dapat disintesis dengan reaksi substitusi asam nitrat terhadap metanol dengan menggunakan asam sulfat sebagai katalis. Reaksi yang terjadi adalah reaksi substitusi elektrofilik. Substitusi elektrofilik terjadi ketika reagen yang berperan adalah suatu elektrofil. Elektrofil adalah molekul yang dapat menerima pasangan elektron (Fessenden, 1986). Pada pembuatannya dengan menggunakan asam sulfat, mula-mula asam nitrat dan asam sulfat dicampurkan kemudian didinginkan. Setelah itu diwadah yang lain juga dicampurkan asam sulfat dan metanol dan didinginkan. Campuran asam sulfat dan metanol ditambahkan ke dalam campuran asam sulfat dan asam nitrat sedikit demi sedikit dan diaduk dengan konstan pada suhu 100C. Campuran hasil reaksi dicuci dengan air dingin dan larutan natrium klorida jenuh. Kemudian lapisan esternya ataupun lapisan atas ditambahkan dengan agen pengering. Metil nitrat yang diperoleh langsung digunakan dan tidak dapat disimpan. Reaksinya dapat digambarkan sebagai berikut:
CH3-OH HNO3
H2SO4 CH3-NO3
metanol metil nitrat
Metil nitrat sangat bersifat explosive yang biasanya digunakan sebagai bahan bakar roket. Secara umum sifat-sifat metil nitrat adalah memiliki berat molekul 77,04 g/mol, larut pada alkohol dan eter,tidak larut dengan air dan memiliki titik didih 64,60C (Anonimous,1976).
2.4Pembuatan Eter
Sintesa eter dapat dilakukan melalui beberapa metode diantaranya adalah : 1. Dehidrasi alkohol untuk membuat dialkil eter
Sintesa dengan metode ini biasanya digunakan untuk mensintesa eter simetrik seperti dietil eter, dipropil eter maupun diisopropil eter. Suatu dialkil eter yang diperoleh melalui pemanasan alkohol primer maupun alkohol sekunder dengan asam sulfat pada temperatur 1400C. Pada sintesa ini pemanasan tidak boleh dilakukan pada suhu terlalu tinggi untuk mencegah terjadinya senyawa alkena dengan reaksi seperti berikut :
2 CH3CH2OH H2SO4
1400C CH3CH2-O-CH2CH3 + H2O
CH3CH2OH H2SO4 1800C
CH2=CH2 + H2O
Dalam metode ini alkohol tersier tidak dapat digunakan sebab alkohol tersier bila dipanaskan dengan asam sulfat tidak akan menghasilkan ditersier eter melainkan memberikan suatu olefin yang dihasilkan dari dehidrasi :
(CH3)3CHOH
1400C (CH3)2C=CH2 + H2O H+
Sedangkan senyawa fenol untuk reaksi ini tidak dapat memberikan eter karena sulfonasi fenol mudah terjadi pada temperatur di bawah 1400C dan fenol mempunyai densitas elektron lebih rendah pada atom oksigennya sehingga permulaan protonasi tidak mudah terjadi.
2. Reaksi anion alkoksida atau fenoksida dengan dialkil sulfat
R-OH + Na RO- Na+ + 1/2 H2
sulfat tersebut dapat mengalami penyerangan tetapi yang kedua memerlukan kondisi yang lebih kuat berhubung karena hal tersebut menyangkut serangan muatan negatif anion fenoksida terhadap muatan negatif anion sulfat.
3. Reaksi Suatu Senyawa Alkil Halida dengan Suatu Anion Alkoksida atau Fenoksida (Sintesa Williamson)
Sintesa Williamson sangat penting karena kemudahannya untuk mensintesa eter yang tidak simetrik dan eter simetrik. Alkoksida dapat dibuat dengan mereaksikan alkohol dengan logam alkali seperti Na atau K sedangkan fenoksida dapat dibuat dari reaksi suatu fenol dengan natrium hidroksida atau dengan kalium karbonat.
CH3CH2OH + Na CH3CH2O-Na+ + 1/2 H2 yang besar ukurannya dapat menghalangi reaksi substitusi, akibatnya akan terjadi reaksi eliminasi terhadap alkil halidanya (Griffin, Jr. 1969).
4. Reaksi Alkilasi Senyawa Alkohol atau Fenol dengan Senyawa Diazo
CH2N2 + R-OH HBF4 R-O-CH3 + N2
Pembentukan metil eter melalui metoda ini memberikan hasil yang cukup kuantitatif serta dapat dilakukan dalam jumlah yang kecil (mg) dengan memberikan rendemen yang tinggi. Reaksi diazometan dengan senyawa- senyawa alkohol dapat berlangsung dengan menggunakan katalis HBF4 atau AlCl3 sedangkan untuk senyawa- senyawa fenol disebabkan
senyawa tersebut asam, reaksinya berjalan dengan baik pada temperatur kamar tanpa menggunakan suatu katalis (March,J. 1984).
5. Pemanasan Alkil Halida dengan Perak oksida kering
Metode ini hanya digunakan untuk membentuk eter simetri.
Cl
2CH3CH2 + Ag2O CH3CH2 O CH2CH3 + 2AgCl
dietil eter etil klorida
6. Alkoksimerkurasi-demerkurasi dari Alkena
Reaksi alkena dengan alkohol dengan adanya merkuri (II) trifluoroasetat dapat membentuk eter.
dapat direduksi , eliminasi maupun reaksi-reaksi dengan basa. Bila senyawa eter dipanaskan dengan asam kuat seperti HI atau HBr akan mengalami reaksi substitusi dan menghasilkan suatu alkil halida atau alkohol. Bila digunakan asam yang berlebih alkohol yang terbentuk dapat bereaksi lebih jauh menghasilkan alkil halida (Fessenden, 1983).
CH3CH2-O-CH2CH3 + HI panas CH3CH2I + HOCH2CH3
HI
CH3CH2I
Identifikasi gugus eter dalam spektrum inframerah memperlihatkan vibrasi ulur C-O-C. Di dalam spektrum serapan yang paling khas ialah sebuah pita pada daerah frekuensi 1150-1085 cm-1 untuk eter alifatik dan pada frekuensi 1270-1200 cm-1untuk senyawa eter aromatik. Pemeriksaan dengan spektroskopi massa senyawa-senyawa eter dapat mengalami fragmentasi dengan terjadinya pemutusan pada ikatan C-C yang bersebelahan dengan atom oksigen dan juga fragmentasi pada ikatan C-O posisi beta terhadap cincin serta ion yang mula-mula terbentuk selanjutnya dapat mengalami fragmentasi dan diikuti dengan puncak khas aromatik pada m/e 78 dan 77 (Silverstein, 1986).
2.5Fourier Transform Infrared Spectroscopy (FTIR)
Instrumen yang digunakan untuk mengukur resapan radiasi inframerah pada berbagai panjang gelombang disebut spektrofotometer inframerah. Penyerapan radiasi inframerah sesuai dengan perubahan energi yang memiliki orde dari 2 hingga 10 Kkal/mol (Sastrohamidjojo,1990). Spektrofotometer inframerah pada umumnya digunakan untuk menentukan gugus fungsi suatu senyawa organik dan mengetahui informasi struktur suatu senyawa organik dengan membandingkan daerah sidik jarinya. Frekuensi inframerah biasanya dinyatakan dalam satuan bilangan gelombang (wave number), yang didefenisikan sebagai banyaknya gelombang per sentimeter. Instrumen biasa memindai (scan) pada kisaran 700 sampai 5000 cm-1. Spektroskpi inframerah terutama bermanfaat untuk menetapkan jenis ikatan atom-atom yang ada dalam molekul (Hart,2003).
4000 – 200 cm -1. Metode ini sangat berguna untuk mengidentifikasi senyawa organik dan organometalik (Sagala,2013). Keadaan vibrasi dari ikatan terjadi pada keadaaan tetap , atau berkuantitas, tingkat – tingkat energi. Panjang gelombang eksak dari absorbsi oleh suatu tipe ikatan tertentu, bergantung pada macam getaran dari ikatan tersebut. Oleh karena itu, tipe ikatan yang berlainan (C-H, C-C, O-H, dan sebagainya) menyerap radiasi inframerah pada panjang gelombang dengan karakteristik yang berlainan. Banyaknya energi yang diabsorbsi oleh suatu ikatan bergantung pada perubahan dalam momen ikatan seperti vibrasi atom-atom yang saling berikatan lebih besar perubahan dalam momen ikatan mengakibatkan absorbsi sejumlah energi juga lebih besar (Fessenden,1992). Identifikasi gugus eter dalam spektrum infra merah memperlihatkan vibrasi ulur C-O-C. di dalam spektrum serapan yang paling khas adalah sebuah pita pada daerah frekuensi 1150-1085 cm-1 untuk eter alifatik dan frekuensi 1270-1200 cm-1 untuk senyawa eter aromatik (Silverstein, 1986).
2.6Kromatografi Gas/Spektrometri Massa
2.6.1 Kromatografi Gas
Kromatografi gas sebagai instrumen untuk analisis fisiko-kimia menduduki posisi yang sangat penting dan banyak dipakai, apa sebabnya:
1. Aliran fase mobil (gas)sangat terkontrol dan kecepatannya cepat
2. Sangat mudah terjadi pencampuran uap sampel ke dalam aliran fase mobil
3. Pemisahan fisik terjadi di dalam kolom yang jenisnya banyak sekali, panjang dan temperaturnya dapat diatur
4. Banyak sekali macam detektor yang dapat dipakai pada kromatografi gas
5. Kromatografi gas sangat mudah digabung dengan instrumen fisiko-kimia lainnya contohnya MS ( Mulja,1995).
2.6.2 Spektrometri Massa
Spektrometri massa adalah suatu metode analisis instrumental yang dapat dipakai untuk identifikasi dan penentuan struktur dari komponen sampel dengan cara menunjukkan masssa relatif dari molekul komponen dan massa relatif hasil pemecahannya. Pemakaian metode spektometri massa secara tersendiri antara lain ditujukan untuk :
1. Penentuan struktur molekul
2. Pembuktian isotop-isotop stabil dalam penelitian reaksi-reaksi biologi
3. Analisis kualitatif dan kuantitatif terhadap komponen yang telah diisolasi dan dimurnikan (Mulja,1995).
Oleh karena itu dari segi praktis, spektrum massa ialah suatu rekaman dari masssa partikel versus kelimpahan relatif partikel itu. Bagaimana suatu molekul atau ion pecah menjadi fragmen-fragmen bergantung pada kerangka karbon dan gugus fungsional yang ada. Oleh karena itu, struktur dan masssa fragmen memberikan petunjuk mengenai struktur molekul induknya (Fessenden,1982). Pemeriksaan dengan spektroskopi massa senyawa-senyawa eter dapat mengalami fragmentasi dengan terjadinya pemutusan pada ikatan C-C yang bersebelahan dengan atom oksigen dan juga fragmentasi pada ikatan C-O. Untuk senyawa-senyawa eter aromatik pemutusan terjadi pada ikatan C-O posisi beta terhadap cincin serta ion-ion yang mula-mula terbentuk selanjutnya dapat mengalami fragmentasi dan diikuti dengan puncak-puncak khas aromatik pada m/e 78 dan 77 (Silverstein, 1986). Contoh fragmentasi dari senyawa eter aromatik (Gambar 2.11) tersebut adalah sebagai berikut:
atau
O CH2
H
-CH2O H
H
H
H
H
H
m/e=78
H
H
H
H H
m/e=77
Gambar 2.11 Fragmentasi Anisol (Silverstein, 1986)
Anisol yang merupakan senyawa eter aromatik dengan puncak ion molekul m/e = 108 memberikan fragmentasi dengan puncak-puncak ion pada m/e =93 atau (M-CH3)+, 65 atau
(M-CH3-CO)+ dan diikuti dengan puncak-puncak khas aromatik pada m/e =78 atau
BAB 1
PENDAHULUAN
1.1 Latar Belakang
Minyak cengkeh merupakan minyak atsiri yang berasal dari tanaman cengkeh (Syzigium aromaticum), yang termasuk dalam family myrtaceae dan banyak ditanam di Indonesia, India dan Madagaskar ( Alma et al., 2007). Indonesia merupakan salah satu negara penghasil cengkeh yang besar. Eugenol (4-alil-2-metoksi-1-fenol) merupakan salah satu bahan bioaktif yang bersifat nonpolar dan dapat diisolasi melalui ekstraksi dari minyak cengkeh (Ketaren, 1985). Dalam cengkeh bagian yang terpenting adalah minyak atsiri dan dalam hal ini komponen utamanya adalah senyawa eugenol yang mempunyai aktivitas sebagai analgesik, antiseptik, antimikroba dan larvasida (Sutthanont et al., 2009). Pada eugenol terdapat beberapa gugus-gugus fungsi seperti gugus hidroksi, alil dan metoksi sehingga dapat diubah secara kimia menjadi berbagai turunannya yang memiliki aktivitas tertentu, dimana pada prinsipnya eugenol merupakan bahan awal yang sangat berguna bagi sintesis senyawa-senyawa yang lebih bermanfaat (Anwar, 1994).
Penelitian dengan material eugenol telah banyak dilakukan, khususnya untuk senyawa turunan eugenol misalnya transformasi gugus alil pada eugenol menjadi gugus aldehida pada vanilin yang digunakan sebagai bahan aditif pada makanan, demikian juga transformasi gugus hidroksil menjadi alkil, asil ataupun asetil dari turunan eugenol seperti metil eugenol, eugenil benzoat dan asetil eugenol yang dapat digunakan sebagai zat bioaditif bahan bakar solar (Sastrohamidjojo, 2004).
Pada tahun 2004, Ngadiwiyana telah melakukan sintesis metil eugenol dari minyak daun cengkeh dengan menggunakan pengalkilasi metil iodida menghasilkan rendemen metil eugenol sebesar 53%. Pada tahun 2006, Rudyanto dan Hartanti telah melakukan sintesis senyawa metil eugenol dengan mereaksikan eugenol dengan dimetil sulfat dalam media natrium karbonat dan natrium hidroksida melalui iradiasi gelombang mikro menghasilkan metil eugenol dengan rendemen sebesar 47%, begitu juga Ratnawati, 2014 yang telah melakukan sintesis metil eugenol dengan menggunakan dimetil sulfat sebagai bahan dasar pembuatan benzofenon yang berfungsi sebagai tabir surya, yang menghasilkan metil eugenol dengan kemurnian 96.98 %.
Metil nitrat merupakan bahan kimia yang dapat dihasilkan melalui reaksi substitusi terhadap metanol menggunakan asam nitrat dan asam sulfat sebagai katalis. Metil nitrat belum banyak digunakan dalam reaksi-reaksi karena sifatnya yang sangat reaktif tetapi dapat digunakan untuk sintesis senyawa organik. Dalam sintesis organik, pembuatan dari metil nitrat dapat dilakukan pada suhu rendah serta dapat digunakan langsung tanpa melalui pemurnian yang rumit.
Berdasarkan uraian yang telah dikemukakan diatas, peneliti tertarik untuk melakukan sintesis metil eugenol melalui eterifikasi gugus hidroksil dari eugenol hasil isolasi dari minyak cengkeh dengan menggunakan metil nitrat hasil reaksi dari metanol dengan asam nitrat.
1.2 Permasalahan
1. Bagaimana mengisolasi eugenol dari minyak cengkeh?
2. Bagaimana proses sintesis metil eugenol melalui eterifikasi antara metil nitrat dengan eugenol hasil isolasi dari minyak cengkeh?
1.3 Pembatasan Masalah
1. Minyak cengkeh yang diperoleh dibeli dari pasar sore Padang Bulan, Medan dalam kemasan botol kaca
2. Eugenol yang digunakan merupakan hasil isolasi dari minyak cengkeh melalui reaksi penggaraman diikuti dengan reaksi hidrolisis.
1.4 Tujuan Penelitian
1. Untuk mengisolasi eugenol dari minyak cengkeh.
2. Untuk melakukan sintesis metil eugenol melalui eterifikasi antara metil nitrat dengan eugenol hasil isolasi dari minyak cengkeh.
1.5 Manfaat Penelitian
Penelitian ini diharapkan dapat memberikan informasi di bidang kimia organik mengenai proses sintesis metil eugenol melalui eterifikasi antara metil nitrat dengan eugenol hasil isolasi dari minyak cengkeh.
1.6 Lokasi Penelitian
Penelitian ini dilakukan di Laboratorium Kimia Organik FMIPA USU Medan. Analisis spektrofotometer FT-IR eugenol dan metil eugenol yang diperoleh dilakukan di salah satu perusahaan swasta di Medan. Analisis GC-MS metil eugenol dilakukan di Laboratorium Kimia Organik FMIPA UGM Yogyakarta.
1.7 Metodologi Percobaan
Penelitian yang dilakukan bersifat eksperimen laboratorium, eugenol yang digunakan dalam penelitian ini merupakan hasil isolasi dari minyak cengkeh dan metil nitrat yang digunakan merupakan hasil reaksi metanol dengan asam nitrat. Tahap yang dilakukan adalah melalui dua proses. Proses pertama ialah reaksi penggaraman eugenol hasil isolasi dengan menggunakan K2CO3 akan menghasilkan K-eugenolat, kemudian dilanjutkan proses
eterifikasi yaitu penambahan metil nitrat dan direfluks selama 2 jam yang dipantau dengan melakukan analisis KLT menggunakan klofoform sebagai pengembang, menggunakan adsorben plat aluminium GF254 dan diperoleh metil eugenol. Eugenol hasil isolasi yang
SINTESIS METIL EUGENOL MELALUI ETERIFIKASI METIL
NITRAT DENGAN EUGENOL HASIL
ISOLASI DARI MINYAK CENGKEH
ABSTRAK
Metil eugenol telah disintesis melalui reaksi eterifikasi antara metil nitrat dengan eugenol hasil isolasi dari minyak cengkeh . Kemurnian eugenol dan metil eugenol ditunjukkan oleh data KLT dengan terbentuknya hanya satu noda pada plat silika dengan menggunakan beberapa pelarut sebagai pengembang. Terbentuknya metil eugenol didukung oleh data spektrum FTIR dengan munculnya bilangan gelombang 3077,94 cm-1; 2935,81 cm-1; 1641,84 cm-1; 1512,29 cm-1; 1261,30 cm-1; 1154,42 cm-1; 1030,29 cm-1; 955,78 cm-1; 806,50 cm -1 dan 749,56 cm-1 , dimana dengan hilangnya bilangan gelombang 3512,84 cm-1 yang terdapat pada spektrum FTIR eugenol, menunjukkan bahwa gugus hidroksil telah tersubstitusi oleh gugus metoksi . Analisa GC-MS menunjukkan kemurnian metil eugenol hasil sintesis sebesar 97.70 %.
SYNTHESIS OF METIL EUGENOL BY ETHERIFICATION WITH
METHYL NITRATE AND EUGENOL
ISOLATED FROM CLOVE OIL
ABSTRACT
Methyl eugenol had been synthesized by etherification methyl nitrate with eugenol isolated from clove oil. The purity of eugenol and metil eugenol was showed by TLC data in which one node was formed in silica plate with many of developer. The data of methyl eugenol was supported by FTIR spectrum by the forming of wave number at 3077,94 cm-1; 2935,81 cm-1; 1641,84 cm-1; 1512,29 cm-1; 1261,30 cm-1; 1154,42 cm-1; 1030,29 cm-1; 955,78 cm-1; 806,50 cm -1 and 749,56 cm-1 , the forming of methyl eugenol was provent by FTIR spectrum by the lose of wave number at 3512,84 cm -1 which showed hidroksil functional group has been changed to be methoxy functional group. GC-MS analyzer showed the pure of methyl eugenol was 97.70 %.
SINTESIS METIL EUGENOL MELALUI ETERIFIKASI METIL
NITRAT DENGAN EUGENOL HASIL ISOLASI
DARI MINYAK CENGKEH
SKRIPSI
YULIA AIDIRA A. A.
NIM : 110802031
DEPARTEMEN KIMIA
FAKULTAS MATEMATIKA DAN ILMU PENGETAHUAN ALAM
UNIVERSITAS SUMATERA UTARA
SINTESIS METIL EUGENOL MELALUI ETERIFIKASI METIL
NITRAT ENGAN EUGENOL HASIL ISOLASI
DARI MINYAK CENGKEH
SKRIPSI
Diajukan untuk melengkapi tugas dan memenuhi syarat mencapai gelar Sarjana Sains
YULIA AIDIRA A. A.
NIM : 110802031
DEPARTEMEN KIMIA
FAKULTAS MATEMATIKA DAN ILMU PENGETAHUAN ALAM
UNIVERSITAS SUMATERA UTARA
PERSETUJUAN
Judul : Sintesis Metil Eugenol Melalui Eterifikasi Metil Nitrat Dengan Eugenol Hasil Isolasi Dari Minyak Cengkeh
Kategori : Skripsi
Nama : Yulia Aidira A. A.
Nomor Induk Mahasiswa : 110802031
Program : Sarjana (S1) Kimia
Departemen : Kimia
Fakultas : Matematika dan Ilmu Pengetahuan Alam (MIPA) Universitas Sumatera Utara
Disetujui di Medan, Maret 2016
Komisi Pembimbing :
Pembimbing II Pembimbing I
Dr. Mimpin Ginting, M.S Dra. Herlince Sihotang, M.Si
NIP. 195510131986011001 NIP. 195503251986012002
Diketahui/ Disetujui oleh
Departemen Kimia FMIPA USU Ketua,
PERNYATAAN
SINTESIS METIL EUGENOL MELALUI ETERIFIKASI METIL
NITRAT DENGAN EUGENOL HASIL
ISOLASI DARI MINYAK CENGKEH
SKRIPSI
Saya mengakui bahwa skripsi ini adalah hasil karya saya sendiri, kecuali beberapa kutipan dan ringkasan yang masing-masing disebutkan sumbernya.
Medan, Maret 2016
PENGHARGAAN
Puji dan syukur penulis panjatkan kepada Tuhan Yang Maha Esa, yang telah melimpahkan kasih dan karunia-Nya sehingga penulis dapat menyelesaikan skripsi ini sebagai salah satu syarat untuk menyelesaikan pendidikan sarjana sains di FMIPA USU dengan judul “Sintesis Metil Eugenol Melalui Eterifikasi Metil Nitrat Dengan Eugenol Hasil Isolasi dari Minyak Cengkeh”.
Pada kesempatan ini penulis menyampaikan terima kasih kepada berbagai pihak yang telah membantu dalam penulisan skripsi ini kepada:
1. Bapak Dr.Sutarman M.Sc selaku Dekan FMIPA USU
2. Ibu Dra. Herlince Sihotang M.Si selaku pembimbing I dan Bapak Dr. Mimpin Ginting, M.S selaku pembimbing II yang telah banyak meluangkan waktu dan sabar membimbing penulis dalam penelitian dan menyelesaikan skripsi ini hingga selesai. 3. Ibu Dr. Rumodang Bulan MS dan Bapak Drs. Albert Pasaribu M.Sc selaku ketua dan
sekretaris departemen Kimia FMIPA USU, serta kepada Bapak Dr.Lamek Marpaung, M.Phil selaku dosen PA penulis dan kepada semua staff dosen Departemen Kimia FMIPA USU.
4. Bapak Prof. Dr. Jamaran Kaban, M.Sc selaku Ketua Bidang Kimia Organik FMIPA USU
5. Bapak Dr. Mimpin Ginting MS selaku Kepala Laboratorium Kimia Organik FMIPA USU.
6. Sahabat-sahabat penulis : Daniel T. Banjarnahor, Friska, Bernard, Hotlan, Debynati, Enabellia, Sevty, Isti, Riswandi, Renggania, Wildi, Sakinah, Firda, Bang Roympus manalu dan Bang Mars.
7. Teman-teman stambuk 2011, adik-adik stambuk 2012, 2013 dan 2014 Kimia FMIPA-USU, Asisten kimia organik FMIPA FMIPA-USU, GMNI komisariat FMIPA USU dan semua pihak yang tidak dapat disebutkan satu per satu.
Secara khusus, penulis mengucapkan terima kasih yang sebesar-besarnya kepada kedua orang tua penulis, Ayah tercinta Pardingotan Ambarita dan Ibu tercinta Mirawati Br Tarigan
yang senantiasa memberikan doa atas dukungan moril dan materil hingga akhirnya penulis menyelesaikan studi. Penulis juga ucapkan terimakasih kepada adik-adik penulis Iin, Laura dan Samuel Ambarita yang telah memberikan doa dan motivasi dalam menyelesaikan skripsi ini. Penulis menyadari bahwa skripsi ini masih jauh dari kesempurnaan karena keterbatasan penulis. Untuk itu dengan segala kerendahan hati, penulis mengharapkan saran yang bersifat membangun demi kesempurnaan skripsi ini.
Akhir kata penulis berharap semoga skripsi ini dapat bermanfaat bagi penelitian dan kemajuan ilmu pengetahuan. Tuhan memberkati kita semua.
SINTESIS METIL EUGENOL MELALUI ETERIFIKASI METIL
NITRAT DENGAN EUGENOL HASIL
ISOLASI DARI MINYAK CENGKEH
ABSTRAK
Metil eugenol telah disintesis melalui reaksi eterifikasi antara metil nitrat dengan eugenol hasil isolasi dari minyak cengkeh . Kemurnian eugenol dan metil eugenol ditunjukkan oleh data KLT dengan terbentuknya hanya satu noda pada plat silika dengan menggunakan beberapa pelarut sebagai pengembang. Terbentuknya metil eugenol didukung oleh data spektrum FTIR dengan munculnya bilangan gelombang 3077,94 cm-1; 2935,81 cm-1; 1641,84 cm-1; 1512,29 cm-1; 1261,30 cm-1; 1154,42 cm-1; 1030,29 cm-1; 955,78 cm-1; 806,50 cm -1 dan 749,56 cm-1 , dimana dengan hilangnya bilangan gelombang 3512,84 cm-1 yang terdapat pada spektrum FTIR eugenol, menunjukkan bahwa gugus hidroksil telah tersubstitusi oleh gugus metoksi . Analisa GC-MS menunjukkan kemurnian metil eugenol hasil sintesis sebesar 97.70 %.
SYNTHESIS OF METIL EUGENOL BY ETHERIFICATION WITH
METHYL NITRATE AND EUGENOL
ISOLATED FROM CLOVE OIL
ABSTRACT
Methyl eugenol had been synthesized by etherification methyl nitrate with eugenol isolated from clove oil. The purity of eugenol and metil eugenol was showed by TLC data in which one node was formed in silica plate with many of developer. The data of methyl eugenol was supported by FTIR spectrum by the forming of wave number at 3077,94 cm-1; 2935,81 cm-1; 1641,84 cm-1; 1512,29 cm-1; 1261,30 cm-1; 1154,42 cm-1; 1030,29 cm-1; 955,78 cm-1; 806,50 cm -1 and 749,56 cm-1 , the forming of methyl eugenol was provent by FTIR spectrum by the lose of wave number at 3512,84 cm -1 which showed hidroksil functional group has been changed to be methoxy functional group. GC-MS analyzer showed the pure of methyl eugenol was 97.70 %.
DAFTAR ISI
1.3 Pembatasan Masalah 3
1.4 Tujuan Penelitian 3
1.5 Manfaat Penelitian 3
1.6 Lokasi Penelitian 3
1.7 Metodologi Percobaan 3
BAB 2 TINJAUAN PUSTAKA
2.1 Minyak Cengkeh 5
2.2Eugenol 6
2.2.1 Reaksi-Reaksi Kimia Terhadap Eugenol 7
2.2.2 Metil Eugenol 10
2.3Metil Nitrat 11
2.4Pembuatan Eter 13
2.4.1 Karakteristik Senyawa Eter 16
2.5Fourier Transform Infrared Spectroscopy (FTIR) 17
2.6 Kromatografi Gas/ Spektrometri Massa 18
2.6.1 Kromatografi Gas 18
2.6.2 Spektrometri Massa 18
BAB 3 METODE PENELITIAN
3.1 Alat-alat 21
3.2 Bahan-bahan 21
3.3 Prosedur Penelitian 22
3.3.1 Isolasi Eugenol Dari Minyak Cengkeh 22
BAB 4 HASIL DAN PEMBAHASAN 4.1 Hasil Penelitian
4.1.1 Isolasi Eugenol Dari Minyak Cengkeh 28
4.1.2 Pembuatan Metil Nitrat 29
4.1.3 Sintesis Metil Eugenol Dengan Menggunakan Metil Nitrat 29
4.1.4 Analisis Hasil Sintesis Dengan GC-MS 30
4.2 Pembahasan 32
4.2.1 Isolasi Eugenol Dari Minyak Cengkeh 32
4.2.2 Pembuatan Metil Nitrat 34
4.2.3. Sintesis Metil Eugenol Menggunakan Metil Nitrat 34 4.2.4 Analisis Metil Eugenol Hasil Sintesis Dengan GC-MS 37 BAB 5 KESIMPULAN DAN SARAN
5.1 Kesimpulan 39
5.2 Saran 39
DAFTAR PUSTAKA 40
DAFTAR GAMBAR
Judul Halaman
2.1 Tanaman Cengkeh 5
2.2 Struktur Asetil Eugenol 6
2.3 Struktur beta-caryophyllene 6
2.4 Struktur Eugenol 6
2.5 Reaksi pembuatan vanilin 8
2.6 Reaksi pembuatan asetil eugenol 9
2.7 Reaksi pembuatan eugenil benzoat 9
2.8 Struktur metil eugenol 10
2.9 Reaksi pembuatan metil eugenol 11
2.10 Struktur metil nitrat 11
2.11 Fragmentasi Anisol 18
4.1 Spektrum FTIR Eugenol 27
4.2 Spektrum FTIR Metil Eugenol 28
4.3 Kromatogram Hasil Analisis Hasil sintesis 29 4.4 Spektrum Massa Metil Eugenol Hasil Sintesis 30
4.5 Spektrum Massa Eugenol Hasil Isolasi 31
4.6 Reaksi Pembentukan Eugenol 31
4.7 Reaksi Pembentukan Metil Eugenol 34
4.8 Kromatogram Analisis KLT Produk Reaksi 35
4.9 Pola Fragmentasi Metil Eugenol 36
4.10 Pola Fragmentasi Eugenol 37
DAFTAR LAMPIRAN
Judul Halaman
1. Kondisi Alat GC-MS 42
2. Spektrum Massa Dari Metil Eugenol 43
3. Spektrum Massa Dari Eugenol 44
4. Foto Eugenol Hasil Isolasi 45
5. Foto Metil Nitrat Hasil Sintesis 45
6. Foto Metil Eugenol Hasil Sintesis 45
7. Hasil Analisa Eugenol dan Metil Eugenol Melalui KLT 45
8. Perhitungan Massa Teori Metil Eugenol 46