PENGUJIAN BAKTERI Coliform PADA AIR SUMUR DI MEDAN JOHOR
TUGAS AKHIR
OLEH:
LOLA ALIA YOLANDA HARAHAP NIM 102410024
PROGRAM STUDI DIPLOMA III ANALIS FARMASI DAN MAKANAN
FAKULTAS FARMASI
UNIVERSITAS SUMATERA UTARA MEDAN
LEMBAR PENGESAHAN
PENGUJIAN BAKTERI Coliform PADA AIR SUMUR DI MEDAN JOHOR
TUGAS AKHIR
Diajukan Untuk Memenuhi Salah Satu Syarat Memperoleh Gelar Ahli Madya Pada Program Studi Diploma III Analis Farmasi dan Makanan
Fakultas Farmasi Universitas Sumatera Utara
Oleh:
LOLA ALIA YOLANDA HARAHAP NIM 102410024
Medan, April 2013 Disetujui Oleh: Dosen Pembimbing
Dra. Anayanti Arianto, M.Si., Apt. NIP 195306251986012001
Disahkan Oleh: Dekan,
KATA PENGANTAR
Puji dan syukur penulis ucapkan kepada Allah SWT yang senantiasa
melimpahkan rahmat dan karunia-Nya sehingga penulis dapat menyelesaikan
Tugas Akhir ini dengan baik.
Tugas Akhir ini berjudul “Pengujian Bakteri Coliform Pada Air Sumur Di
Medan Johor”. Pada dasarnya Tugas Akhir ini merupakan salah satu persyaratan
untuk menyelesaikan pendidikan Program Studi Diploma III Analis Farmasi dan
Makanan Fakultas Farmasi Universitas Sumatera Utara. Tugas Akhir ini disusun
berdasarkan apa yang penulis lakukan pada Praktik Kerja Lapangan (PKL) di
Balai Riset dan Standardisasi (Baristand) Industri Medan.
Dalam menyusun Tugas Akhir ini, penulis banyak mendapat bantuan dan
bimbingan dari berbagai pihak, untuk itu pada kesempatan ini penulis
mengucapkan terima kasih yang sebesar-besarnya kepada:
1. Bapak Prof. Dr. Sumadio Hadisahputra, Apt., selaku Dekan Fakultas
Farmasi Universitas Sumatera Utara.
2. Bapak Prof. Dr. Jansen Silalahi, M.App.Sc., Apt., selaku Ketua Program
Studi Diploma III Analis Farmasi dan Makanan Fakultas Farmasi
Universitas Sumatera Utara.
3. Ibu Dra. Anayanti Arianto, M.Si., Apt., selaku Dosen Pembimbing yang
telah membimbing dan memberikan nasehat serta perhatiannya kepada
4. Bapak Prof. Dr. Hakim Bangun, Apt., selaku Dosen Penasehat Akademik
penulis selama melaksanakan pendidikan pada Program Studi Diploma III
Analis Farmasi dan Makanan Fakultas Farmasi Universitas Sumatera
Utara.
5. Seluruh dosen/staf pengajar Fakultas Farmasi Universitas Sumatera Utara.
6. Ibu Nila Kesuma Sitiwati Dewi selaku koordinator Pembimbing PKL di
Balai Riset dan Standardisasi Industri Medan.
7. Seluruh staf dan karyawan Balai Riset dan Standardisasi Industri Medan
yang telah membantu selama pelaksanaan PKL.
8. Sahabatku Ilham, Nisa, Devi, Lia, Ledang, Nita, Indri, dan Femy yang
senantiasa memberi motivasi dan menghibur disaat lelah.
9. Dedek, Vitta, dan Ika teman sekelompok yang membantu penulis dalam
melaksanakan PKL di Baristand Industri Medan.
10.Teman-teman mahasiswa dan mahasiswi Program Studi Diploma III
Analis Farmasi dan Makanan angkatan 2010 yang tidak dapat penulis
sebutkan satu persatu, namun tidak mengurangi arti keberadaan mereka.
11.Terakhir dan teristimewa, penulis mengucapkan terimakasih yang
sebesar-besarnya kepada Ayahanda Mulia Soleman Harahap dan Ibunda Rosdiana
Siregar yang telah membesarkan dan mendidik penulis dengan penuh
kasih sayang dan cinta dari kecil hingga saat ini memberikan motivasi dan
restu serta materi yang tidak ternilai harganya dengan apapun. Serta
seluruh keluarga yang telah memberi dorongan baik moril maupun materil
Dalam menulis Tugas Akhir ini penulis menyadari bahwa tulisan ini tidak
luput dari kekurangan dan kelemahan. Harapan kritik dan saran yang bersifat
membangun sangat penulis harapkan demi kesempurnaan tulisan ini. Akhirnya
penulis berharap semoga Tugas Akhir ini bermanfaat bagi kita semua.
Medan, April 2013
Penulis,
Testing of Coliform Bacteria in Well Water at Medan Johor
ABSTRACT
Water is an essential material in life. Water is a major means to increase public health. The spread of water-borne desease can be. Water pollution canbe caused by the entry of human and animal feces. It can also be caused by the return of waste water in to the well directly or through leaks and openings where the soil. Coliform is a group of bacteria used as an indicator of pollution and dirt are not good conditions for water. The purpose of testing is to test Coliform bacteria on one of well water in Medan Johor.
The sampling is using well water that has been sterilized bottle. Well water sample was taken approximately 250 ml. Coliform bacteria testing is done using a method MPN (Most Probable Number) accordance with Indonesian National Standard 01-2897-1992.
The test results indicate that the well water containing Coliform bacteria examined 1600/100 ml. these results not meet the requirements of maximum level according Regulation of Health Cabinet Minister number 416/Menkes/Per/ IX/1990 namely 50/100 ml.
Pengujian Bakteri Coliform Pada Air Sumur Di Medan Johor
ABSTRAK
Air adalah materi esensial di dalam kehidupan. Air merupakan suatu sarana utama untuk meningkatkan derajat kesehatan masyarakat. Penyebaran penyakit dapat melalui air. Pencemaran air dapat disebabkan karena masuknya kotoran manusia dan binatang. Selain itu juga dapat disebabkan kembalinya air buangan ke dalam sumur secara langsung atau melalui tempat bocor dan celah-celah tanah. Coliform merupakan suatu grup bakteri yang digunakan sebagai indikator adanya polusi kotoran dan kondisi yang tidak baik terhadap air. Tujuan pengujian ini adalah untuk menguji bakteri Coliform pada salah satu air sumur yang ada di Medan Johor.
Pengambilan air sumur dilakukan menggunakan botol yang sudah disterilkan. Sampel air sumur diambil sekitar 250 ml. Pengujian bakteri Coliform ini dilakukan menggunakan metode APM (Angka Paling Mungkin) sesuai dengan Standar Nasional Indonesia 01-2897-1992.
Hasil pengujian menunjukkan bahwa air sumur yang diperiksa mengandung bakteri Coliform 1600/100 ml, hasil tersebut tidak memenuhi persyaratan kadar maksimum menurut Peraturan Menteri Kesehatan Nomor 416/Menkes/Per/IX/1990 yaitu 50/100 ml.
DAFTAR ISI
Halaman
JUDUL ... i
LEMBAR PENGESAHAN ... ii
KATA PENGANTAR ... iii
ABSTRACT ... vi
DAFTAR ISI ... vii
DAFTAR TABEL ... x
BAB I PENDAHULUAN ... 1
1.1 Latar Belakang ... 1
1.2 Tujuan ... 3
1.3 Manfaat ... 3
BAB II TINJAUAN PUSTAKA ... 4
2.1 Air ... 4
2.1.1 Sumber Air ... 4
2.1.2 Air Sumur ... 5
2.2 Bakteri Coliform ... 5
2.2.1 Definisi Coliform ... 5
2.2.2 Klasifikasi bakteri Coliform ... 6
2.3 Sterilisasi ... 7
2.3.1 Sterilisasi Uap ... 7
2.3.2 Sterilisasi Panas Kering ... 7
2.3.4 Sterilisasi dengan Radiasi Ion ... 9
2.3.5 Sterilisasi dengan Penyaringan ... 9
2.4 Media (Perbenihan) ... 10
2.5 Metode Analisis ... 11
2.6 Persyaratan Kualitas Air Bersih ... 13
BAB III METODE PENGUJIAN ... 15
3.1 Tempat Pengujian ... 15
3.2 Alat dan Bahan ... 15
3.2.1 Alat ... 15
3.2.2 Bahan ... 15
3.3 Penyiapan Sampel ... 15
3.4 Prosedur ... 16
3.4.1 Pembuatan Media ... 16
3.4.2 Pengujian Bakteri Coliform Berdasarkan SNI 01-2897-1992 ... 16
3.4.2.1 Uji Sangkaan ... 17
3.4.2.2 Uji Penegasan (Uji konfirmasi) ... 17
BAB IV HASIL DAN PEMBAHASAN ... 19
4.1 Hasil ... 19
4.2 Pembahasan ... 19
BAB V KESIMPULAN DAN SARAN ... 21
5.1 Kesimpulan ... 21
DAFTAR PUSTAKA ... 22
DAFTAR TABEL
Halaman
Tabel 1. Daftar Persyaratan Kualitas Air Bersih ... 13
Tabel 2. Daftar APM Coliform Menggunakan 5 Tabung ... 18
Testing of Coliform Bacteria in Well Water at Medan Johor
ABSTRACT
Water is an essential material in life. Water is a major means to increase public health. The spread of water-borne desease can be. Water pollution canbe caused by the entry of human and animal feces. It can also be caused by the return of waste water in to the well directly or through leaks and openings where the soil. Coliform is a group of bacteria used as an indicator of pollution and dirt are not good conditions for water. The purpose of testing is to test Coliform bacteria on one of well water in Medan Johor.
The sampling is using well water that has been sterilized bottle. Well water sample was taken approximately 250 ml. Coliform bacteria testing is done using a method MPN (Most Probable Number) accordance with Indonesian National Standard 01-2897-1992.
The test results indicate that the well water containing Coliform bacteria examined 1600/100 ml. these results not meet the requirements of maximum level according Regulation of Health Cabinet Minister number 416/Menkes/Per/ IX/1990 namely 50/100 ml.
Pengujian Bakteri Coliform Pada Air Sumur Di Medan Johor
ABSTRAK
Air adalah materi esensial di dalam kehidupan. Air merupakan suatu sarana utama untuk meningkatkan derajat kesehatan masyarakat. Penyebaran penyakit dapat melalui air. Pencemaran air dapat disebabkan karena masuknya kotoran manusia dan binatang. Selain itu juga dapat disebabkan kembalinya air buangan ke dalam sumur secara langsung atau melalui tempat bocor dan celah-celah tanah. Coliform merupakan suatu grup bakteri yang digunakan sebagai indikator adanya polusi kotoran dan kondisi yang tidak baik terhadap air. Tujuan pengujian ini adalah untuk menguji bakteri Coliform pada salah satu air sumur yang ada di Medan Johor.
Pengambilan air sumur dilakukan menggunakan botol yang sudah disterilkan. Sampel air sumur diambil sekitar 250 ml. Pengujian bakteri Coliform ini dilakukan menggunakan metode APM (Angka Paling Mungkin) sesuai dengan Standar Nasional Indonesia 01-2897-1992.
Hasil pengujian menunjukkan bahwa air sumur yang diperiksa mengandung bakteri Coliform 1600/100 ml, hasil tersebut tidak memenuhi persyaratan kadar maksimum menurut Peraturan Menteri Kesehatan Nomor 416/Menkes/Per/IX/1990 yaitu 50/100 ml.
BAB I PENDAHULUAN 1.1 Latar Belakang
Air adalah materi esensial di dalam kehidupan. Tidak ada satu pun
makhluk hidup di dunia ini yang tidak membutuhkan air. Sel hidup misalnya, baik
tumbuh-tumbuhan ataupun hewan, sebagian besar tersusun oleh air (Suriawiria,
1996).
Di Indonesia diperkiraan 100 liter/hari/kapita dengan perincian: air untuk
keperluan minum sebanyak 5 liter, memasak sebanyak 5 liter, membersihkan atau
mencuci 15 liter, mandi sebanyak 30 liter dan untuk keperluan kakus (W.C)
sebanyak 45 liter (Entjang, 2000).
Air merupakan suatu sarana utama untuk meningkatkan derajat kesehatan
masyarakat, karena air merupakan salah satu media dari berbagai macam
penularan penyakit (Kusnaedi, 2010).
Air merupakan substrat yang paling parah akibat pencemaran. Secara
langsung ataupun tidak langsung pencemar tersebut akan berpengaruh terhadap
kualitas air, baik untuk keperluan air minum, air industri ataupun keperluan
lainnya (Suriawiria, 1996).
Penyebaran penyakit dapat melalui air. Penyebarannya terjadi karena
pengotoran oleh manusia dan binatang serta penambahan vektor penyakit yang
disebabkan air (Suriawiria, 1996).
Air yang dipergunakan untuk banyak keperluan seperti untuk minum,
dari jenis virus, bakteri, jamur, protozoa dan cacing. Pencemaran biasanya
disebabkan karena masuknya kotoran manusia dan binatang ke dalamnya, misal
dalam bentuk tinja, air kencing, dan sebagainya.Pencemaran yang tidak disengaja
banyak pula terjadi, seperti kembalinya air buangan ke dalam sumur secara
langsung atau melalui tempat bocor dan celah-celah tanah, misal dari kakus ke
dalam sumur yang letaknya terlalu dekat (Suriawiria, 1996).
Menurut ketentuan WHO dan APHA, kualitas air ditentukan oleh
kehadiran dan jumlah Coli di dalamnya yaitu untuk air minum dan untuk air
lainnya. Sedang secara umum berdasarkan karakteristika kimia, fisik dan
mikrobiologik, maka kualitas air akan ditentukan berdasarkan keperluannya
(Suriawiria, 1996).
Bakteri Coliform merupakan golongan mikroorganisme yang lazim
digunakan sebagai indikator, di mana bakteri ini dapat menjadi sinyal untuk
menentukan suatu sumber air telah terkontaminasi oleh bakteri patogen atau tidak
yang berbahaya bagi kesehatan.Oleh karena itu perlu dilakukan pengujian bakteri
Coliform pada air sumur. Dalam hal ini penulis melakukan pengujian air sumur
yang ada di Medan Johor dan pengujian dilakukan di Balai Riset dan
Standardisasi Industri Medan (Baristand) dengan metode APM (Angka Paling
Mungkin) menggunakan 5 tabung berdasarkan Standar Nasional Indonesia
1.2 Tujuan
Adapun tujuan dari pengujian bakteri Coliform untuk mengetahui apakah
salah satu air sumur yang ada di Medan Johor memenuhi persyaratan kualitas air
bersih berdasarkan Peraturan Menteri Kesehatan Nomor 416/Menkes/Per/IX/1990
1.3 Manfaat
Dari hasil pengujian dapat memberikan informasi mengenai kualitas salah
satu air sumur yang ada di Medan Johor apakah memenuhi persyaratan kualitas
air bersih berdasarkan Peraturan Menteri Kesehatan Nomor 416 /Menkes/Per/IX/
BAB II
TINJAUAN PUSTAKA
2.1 Air
Air merupakan zat yang mutlak bagi setiap makhluk hidup, dan kebersihan
air adalah syarat utama bagi terjaminnya kesehatan (Dwidjoseputro, 1978).
Untuk semua ini diperlukan air yang memenuhi syarat kesehatan baik
kuantitas maupun kualitasnya (Entjang, 2000).
1. Syarat kuantitas
Jumlah air untuk keperluan rumah tangga per hari per kapita tidaklah sama
pada tiap negara (Entjang, 2000).
Kebutuhan air untuk keperluan sehari-hari, berbeda untuk tiap tempat
dantiap tingkat kehidupan. Yang jelas semakin tinggi taraf kehidupan, semakin
meningkat pula jumlah kebutuhannya (Suriawiria, 1996).
2. Syarat kualitas
Menurut Entjang (2000), air harus memenuhi syarat: fisis, khemis dan
syarat bakteriologis.
a. Syarat fisis yaitu jernih, tak berwarna, tak berasa dan tak berbau.
b. Syarat khemis yaitu tidak mengandung zat-zat yang berbahaya untuk kesehatan
seperti zat-zat racun, dan tidak mengandung mineral-mineral serta zat organik
lebih tinggi dari jumlah yang ditentukan.
c. Syarat bakteriologis yaitu tidak boleh mengandung sesuatu bibit penyakit.
2.1.1 Sumber air
1. Air dalam tanah (Ground water)
Adalah air yang diperoleh dari pengumpulan air pada lapisan tanah yang
dalam. Misalnya, air sumur, air dari mata air.
2. Air permukaan (Surface water)
Adalah air yang terdapat pada permukaan tanah.Air permukaan harus
diolah terlebih dahulu sebelum dipergunakan karena umumnya telah mengalami
pengotoran. Misalnya, air kali, rawa, danau, kolam dan air hujan.
2.1.2 Air Sumur
Air sumur merupakan sumber air yang banyak digunakan masyarakat
Indonesia. Agar air sumur memenuhi syarat kesehatan, khususnya untuk air
rumah tangga, maka air sumur harus dilindungi terhadap bahaya-bahaya
pengotoran (Entjang, 2000).
Air merupakan media yang baik untuk ditumbuhi mikroba. Dari sekian
banyak jenis mikroba yang bersifat patogen atau merugikan manusia, ada
beberapa jenis mikroba yang sangat tidak dikehendaki kehadirannya karena
mikroba tersebut berasal dari kotoran manusia dan hewan berdarah panas lainnya.
Mikroba tersebut dapat berperan sebagai bioindikator kualitas perairan (Nugroho,
2006).
2.2 Bakteri Coliform 2.2.1 Definisi Coliform
Bakteri Coliform bersifat aerob dan anaerob fakultatif, termasuk ke dalam
bakteri gram negatif, tidak membentuk spora, berbentuk batang (basil), dan dapat
Golongan bakteri Coli merupakan jasad indikator dalam air, bahan
makanan, dan sebagainya untuk kehadiran jasad berbahaya, yang mempunyai
persamaan sifat gram negatif berbentuk batang, tidak membentuk spora, dan
mampu memfermentasikan laktosa pada temperatur 37ºC dengan membentuk
asam dan gas di dalam waktu 48 jam (Suriawiria, 1996).
Coliform merupakan suatu grup bakteri yang digunakan sebagai indikator
adanya polusi kotoran dan kondisi yang tidak baik terhadap air, makanan, susu
dan produk-produk susu. Adanya bakteri koliform di dalam makanan/minuman
menunjukkan kemungkinan adanya mikroba yang bersifat enteropatogenik dan
atau toksigenik yang berbahaya bagi kesehatan (Fardiaz, 1993).
2.2.2 Klasifikasi bakteri Coliform
Bakteri koliform dapat dibedakan menjadi 2 kelompok diantaranya: 1. Koliform fekal
Kelompok bakteri koliform fekal ini diantaranya Escherichia coli.
Escherichia coli merupakan bakteri yang berasal dari kotoran hewan atau manusia
(Fardiaz, 1993). Jadi, adanya Escherichia coli pada air menunjukkan bahwa air
tersebut pernah terkontaminasi feses manusia. Pada keadaan tertentu dapat
mengalahkan mekanisme pertahanan tubuh, sehingga dapat menyebabkan diare,
peritonitis, meningitis dan infeksi-infeksi lainnya. Oleh karena itu, standar air minum
mensyaratkan bakteri Escherichia coli harus nol dalam 100 ml (Suriawiria, 1996).
2. Koliform non-fekal
Pada kelompok koliform non-fekal diantaranya, Enterobacter aerogenes
dan Klebsiela yang biasa disebut golongan perantara. Bakteri ini biasanya
Bakteri ini juga lebih banyak didapatkan di dalam habitat tanah dan air daripada
di dalam usus (Suriawiria, 1996).
2.3 Sterilisasi
Sterilisasi dalam mikrobiologi merupakan proses penghilangan semua
jenis organisme hidup, dalam hal ini adalah mikroorganisme (protozoa, fungi,
bakteri, mycoplasma, virus) yang terdapat pada suatu benda atau bahan (Pratiwi,
2008).
2.3.1 Sterilisasi Uap
Proses sterilisasi termal menggunakan uap jenuh di bawah tekanan
berlangsung di suatu bejana yang disebut autoklaf, dan mungkin merupakan
proses sterilisasi yang paling banyak digunakan (suatu siklus autoklaf yang
ditetapkan dalam farmakope untuk media atau pereaksi adalah selama 15 menit
pada suhu 121ºC kecuali dinyatakan lain). Prinsip dasar kerja alat adalah udara di
dalam bejana sterilisasi diganti dengan uap jenuh, dan hal ini dicapai dengan
menggunakan alat pembuka atau penutup khusus (Ditjen POM, 1995).
2.3.2 Sterilisasi Panas Kering
Proses sterilisasi termal untuk bahan yang tertera di Farmakope dengan
menggunakan panas kering biasanya dilakukan dengan suatu proses bets di dalam
suatu oven yang didesain khusus untuk tujuan itu. Oven modern dilengkapi
dengan udara yang dipanaskan dan disaring, didistribusikan secara merata ke
seluruh bejana dengan cara sirkulasi atau radiasi menggunakan sistem semprotan
dengan peralatan sensor, pemantau, dan pengendali parameter kritis. Validasi
sterilisasi panas uap. Unit yang digunakan untuk sterilisasi komponen seperti
wadah untuk larutan intravena, harus dijaga agar dapat dihindari akumulasi
partikel di dalam bejana sterilisasi. Rentang suhu khas yang dapat diterima di
dalam bejana sterilisasi kosong adalah lebih kurang 15 menit, jika alat sterilisasi
beroperasi pada suhu tidak kurang dari 250ºC (Ditjen POM, 1995).
2.3.3 Sterilisasi Gas
Pilihan untuk menggunakan sterilisasi gas sebagai alternatif dari sterilisasi
termal sering dilakukan jika bahan yang akan disterilkan tidak tahan terhadap
suhu tinggi pada proses sterilisasi uap atau panas kering. Bahan aktif yang
umumnya digunakan pada sterilisasi gas adalah etilen oksida dengan kualitas
mensterilkan yang dapat diterima. Keburukan dari bahan aktif ini antara lain
sifatnya yang sangat mudah terbakar, walaupun sudah dicampur dengan gas inert
yang sesuai, bersifat mutagenik, dan kemungkinan adanya residu toksik di dalam
bahan yang disterilkan, terutama yang mengandung ion klorida. Proses sterilisasi
pada umunya berlangsung di dalam bejana bertekanan yang didesain sama seperti
pada autoklaf, tetapi dengan tambahan bagian khusus yang hanya terdapat pada
alat sterilisasi yang menggunakan gas. Fasilitas yang menggunakan bahan
sterilisasi seperti ini harus didesain sedemikian rupa hingga mampu mengeluarkan
gas sesudah proses sterilisasi, mampu untuk memantau mikroba yang masih
hidup, dan mengurangi paparan gas yang sangat berbahaya terhadap petugas yang
2.3.4 Sterilisasi dengan Radiasi Ion
Perkembangan yang cepat alat kesehatan yang tidak tahan terhadap
sterilisasi panas dan kekhawatiran tentang keamanan etilen oksida mengakibatkan
peningkatan penggunaan sterilisasi radiasi. Tetapi cara ini juga dapat digunakan
pada bahan obat dan bentuk sediaan akhir. Keunggulan sterilisasi iradiasi meliputi
reaktivitas kimia rendah, residu rendah yang dapat diukur, dan kenyataan yang
membuktikan bahwa variabel yang dikendalikan lebih sedikit. Kenyataannya
sterilisasi radiasi adalah sesuatu kekhususan dalam dasar pengendalian yang
penting adalah dosis radiasi yang diserap, dan dapat diukur secara tepat. Oleh
karena sifat khas tersebut, banyak prosedur baru yang telah dikembangkan untuk
menetapkan dosis sterilisasi. Walaupun begitu, hal ini masih dalam peninjauan
dan pertimbangan, terutama mengenai kegunaannya, paling tidak, untuk
pengendalian tambahan dan tindakan keamanan. Iradiasi hanya menimbulkan
sedikit kenaikan suhu, tetapi dapat mempengaruhi kualitas dan jenis plastik atau
kaca tertentu (Ditjen POM, 1995).
2.3.5 Sterilisasi dengan Penyaringan
Sterilisasi larutan yang labil terhadap panas sering dilakukan dengan
penyaringan menggunakan bahan yang dapat menahan mikroba, hingga mikroba
yang dikandung dapat dipisahkan secara fisika. Perangkat penyaring umumnya
terdiri dari suatu matriks berpori bertutup kedap atau dirangkaikan pada wadah
yang tidak permeabel. Efektivitas suatu penyaring media atau penyaring substrat
tergantung pada ukuran pori bahan dan dapat tergantung pada daya adsorpsi
pengayakan. Ada beberapa bukti yang menyatakan bahwa pengayakan merupakan
komponen yang lebih penting dari mekanisme. Penyaring yang melepas serat,
terutama yang mengandung asbes, harus dihindarkan penggunaanya kecuali tidak
ada cara penyaringan alternatif lain yang mungkin digunakan. Jika penyaring
yang melepas serat memang diperlukan, merupakan keharusan, bahwa proses
penyaringan meliputi adanya penyaring yang tidak melepas serat diletakkan pada
arah hilir atau sesudah langkah penyaringan awal (Ditjen POM, 1995).
2.4 Media (Perbenihan)
Media merupakan bahan nutrisi yang disiapkan untuk pertumbuhan
mikroba. Media selektif dibuat untuk menekan pertumbuhan bakteri yang tidak
diinginkan dan meningkatkan pertumbuhan bakteri yang diinginkan (Suryanto dan
Munir, 2006).
Dalam pengujian bakteri Coliform, media (perbenihan) yang digunakan
adalah sebagai berikut:
a. Lactose Broth (Single Strength)
Beef extract 3 gram
Peptone 5 gram
Lactose 5 gram
Air suling 1 liter
Larutkan bahan-bahan, atur pH 6,8. Masukkan sebanyak 10 ml ke dalam
tabung kimia yang berisi tabung Durham terbalik. Sterilkan selama 15 menit pada
b. Lactose Broth (Double Strength)
Beef extract 6 gram
Peptone 10 gram
Lactose 10 gram
Air suling 1 liter
Larutkan bahan-bahan, atur pH 6,8. Masukkan ke dalam tabung sebanyak
10 ml. Sterilkan selama 15 menit pada suhu 121°C (SNI, 1992).
c. Brilliant Green Lactose Bile Broth 2% (BGLB 2%)
Peptone 10 gram
Lactose 10 gram
Oxgall bile 20 gram
Brilliant green 0,0125 gram
Air suling 1 liter
Larutkan peptone dan lactose dalm 500 ml air suling.Tambahkan 20 g
oxgall yang dilarutkan dalam 200 ml air suling. Campurkan kedua larutan
tersebut, lalu jadikan 950 ml, atur pH 7,4 (SNI, 1992).
Tambahkan air suling hingga 1 liter, kemudian masukkan 10 ml ke dalam
tabung kimia yang mengandung tabung Durham terbalik. Sterilkan dalam autoklaf
pada 121°C selama 15 menit. Sesudah sterilisasi pH 7,2 (SNI, 1992).
2.3 Metode Analisis
Prinsip penentuan angka bakteri Coliform adalah ditandai dengan
terbentuknya gas dalam tabung Durham, setelah sampel diinkubasikan dalam
dirujuk kepada tabel MPN (Most Probable Number)/APM (Angka Paling
Mungkin) (SNI, 1992).
Dalam metode MPN digunakan medium cair di dalam tabung reaksi, di
mana perhitungan dilakukan berdasarkan jumlah tabung yang positif, yaitu yang
ditumbuhi oleh mikroba setelah inkubasi pada suhu dan waktu tertentu.
Pengamatan tabung yang positif dapat dilihat dengan mengamati timbulnya
kekeruhan, atau terbentuknya gas di dalam tabung Durham terbalik (Waluyo,
2010).
Perhitungan kelompok bakteri Coli menggunakan metode MPN (Most
Probable Number), dengan jumlah 3-3-3 atau 5-5-5 tanpa memperhatikan apakah
jenis-jenis di dalam kelompok tersebut termasuk Coli-fekal/FCB (Fecal Coli
Bacterial) ataupun non-FCB (Suriawiria, 1996). Lebih banyak tabung yang
digunakan menunjukkan ketelitian yang lebih tinggi (Waluyo, 2010).
Adapun analisis kehadiran golongan bakteri Coli dilakukan dengan
tahapan-tahapan sebagai berikut:
a. Tes Pendugaan (Presumptive Test)
Medium yang digunakan adalah kaldu laktosa. Tes ini dikatakan positif
jika setelah inkubasi 37°C selama 48 jam laktosa yang telah difermentasi akan
berubah warna dan terbentuk gas yang ditampung oleh tabung Durham yang
diletakkan terbalik (Nugroho, 2006).
Mungkin sekali gas yang tertampung dalam tabung Durham itu berasal dari
Untuk menghilangkan keragu-raguan ini perlulah diadakan test berikutnya, yaitu
“uji kepastian” (Dwidjoseputro, 1978).
b. Tes Konfirmasi/Uji kepastian (Confirmed Test)
Merupakan tes lanjutan dari tes pendugaan. Dari tabung yang positif pada
tes pendugaan, dilakukan tes menggunakan medium BGLB (Brilliant Green
Lactose Broth) yang dapat menghambat pertumbuhan bakteri gram positif dan
sebaliknya, yaitu menstimulasi pertumbuhan bakteri gram negatif seperti Coliform
(Nugroho, 2006).
2.6 Persyaratan Kualitas Air Bersih
Persyaratan kualitas air bersih yang ditetapkan oleh Peraturan Menteri
Kesehatan Republik Indonesia Nomor 416/Menkes/Per/IX/1990 dapat dilihat
[image:26.595.114.510.473.692.2]pada Tabel 1.
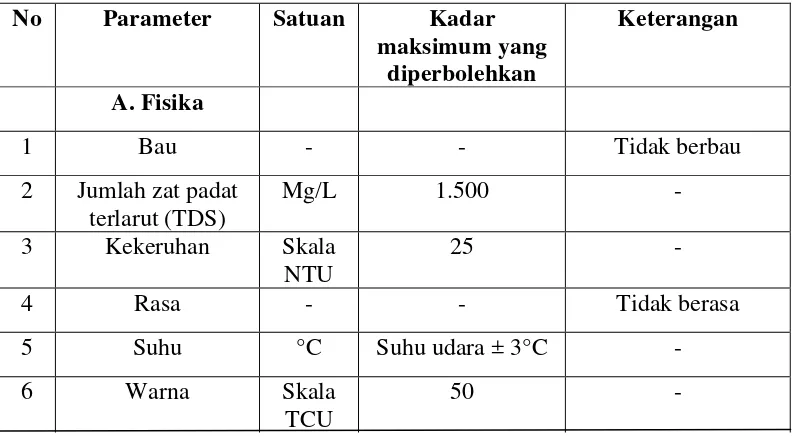
Tabel 1. Daftar Persyaratan Kualitas Air Bersih No Parameter Satuan Kadar
maksimum yang diperbolehkan
Keterangan
A. Fisika
1 Bau - - Tidak berbau
2 Jumlah zat padat terlarut (TDS)
Mg/L 1.500 -
3 Kekeruhan Skala
NTU
25 -
4 Rasa - - Tidak berasa
5 Suhu °C Suhu udara ± 3°C -
6 Warna Skala
TCU
B. Kimia a. Kimia Anorganik
1 pH - 6,5 – 9,0 Merupakan batas
minimum dan maksimum. Khusus air hujan pH minimum 5,5
2 Arsen Mg/L 0,05 -
3 Besi Mg/L 1,0 -
4 Nitrat Mg/L 10 -
5 Nitrit Mg/L 1,0 -
b. Kimia Organik
1 Chloroform Mg/L 0,03 -
2 Detergen Mg/L 0,5 -
3 Methoxychlor Mg/L 0,10 -
4 Pentachlorophenol Mg/L 0,01 -
5 Zat Organik (KMnO4)
Mg/L 10 -
C. Mikrobiologik
1 Total Koliform
(MPN)
Jumla h per 100 ml
50 Bukan air
perpipaan
Jumla h per 100 ml
10 Air perpipaan
D. Radioaktivitas 1 Aktivitas Alpha
(Gross Alpha Activity)
Bg/L 0,1 -
2 Aktivitas Beta
(Gross Beta Activity)
BAB III
METODE PENGUJIAN
3.1 Tempat Pengujian
Pengujian bakteri Coliform pada air sumur di Medan Johor dilakukan di
Balai Riset dan Standardisasi (Baristand) Industri Medan yang berada di jalan
Sisingamangaraja No. 24 Medan. Dilakukan sesuai dengan Standar Nasional
Indonesia 01-2897-1992.
3.2 Alat dan Bahan 3.2.1 Alat
Alat-alat yang digunakan dalam percobaan ini adalah autoklaf 121°C,
batang pengaduk, beaker glass, botol bertutup, gelas ukur, inkubator 36±1°C,
kompor gas, oven, pipet ukur 1 ml, pipet ukur 10 ml, timbangan analitik, rak
tabung, sengkelit (ose), spatula, tabung reaksi (15 x 150 mm), tabung reaksi (18 x
180 mm), tabung Durham (75 x 10 mm).
3.2.2 Bahan
Bahan-bahan yang digunakan dalam percobaan ini adalah air sumur,
akuades, alkohol 70%, Lactose Broth(LB), Brilliant Green Lactose Bile Broth 2%
(BGLB 2%).
3.3 Penyiapan Sampel
Air sumur yang diambil ditarik menggunakan pompa air yang dialirkan
melalui kran. Sebelum air ditampung, kran terlebih dahulu disterilkan dengan
alkohol 70% kemudian air dialirkan selama 15 menit. Setelah itu, tampung air
dengan alkohol 70%. Botol sampel terbuat dari gelas, mempunyai penutup yang
pas dan kuat, harus steril, dapat menampung ± 250 ml sampel.
3.4 Prosedur
3.4.1 Pembuatan Media (Perbenihan) a. Lactose Broth (Single Strength)
Media ditimbang sebanyak 1,3 gram, dilarutkan dengan 100 ml akuades,
pindahkan masing-masing 10 ml ke dalam sepuluh tabung reaksi yang berisi
tabung Durham terbalik. Kemudian sterilkan dengan autoklaf pada suhu 121°C
selama 15 menit.
b. Lactose Broth (Double Strength)
Media ditimbang sebanyak 1,3 gram, dilarutkan dengan 50 ml akuades,
pindahkan masing-masing 10 ml ke dalam lima tabung reaksi yang berisi tabung
Durham terbalik. Kemudian sterilkan dengan autoklaf pada suhu 121°C selama 15
menit.
c. Brilliant Green Lactose Bile Broth 2% (BGLB 2%)
Media ditimbang sebanyak 5,6 gram, dilarutkan dengan 140 ml akuades,
pindahkan masing-masing 10 ml ke dalam 14 tabung reaksi yang berisi tabung
Durham terbalik. Kemudian sterilkan dengan autoklaf pada suhu 121°C selama 15
menit.
3.4.2.1 Uji Sangkaan
1. Pipet masing-masing 10 ml sampel ke dalam 5 tabung yang pertama berisi 10
ml Lactose Broth double strength yang di dalamnya terdapat tabung Durham
terbalik.
2. Pipet masing-masing 1 ml dan 0,1 ml sampel ke dalam 5 tabung yang kedua
dan ketiga yang berisi 10 ml perbenihan yang sama tetapi yang single strength.
3. Simpan semua tabung dalam lemari pengeram (inkubator) pada suhu 36 ± 1°C
selama 24 dan 48 jam.
4. Setelah 24 jam kemudian catat jumlah tabung yang membentuk gas pada
masing-masing tabung dan simpan lagi tabung yang tidak membentuk gas
dalam inkubator pada suhu 36 ± 1°C selama 24 jam, kemudian catat jumlah
tabung yang membentuk gas.
3.4.2.2 Uji Penegasan (Uji konfirmasi)
1. Pindahkan sebanyak 1 sengkelit dari tiap tabung yang membentuk gas pada
media LB ke dalam tabung yang berisi 10 ml Brilliant Green Lactose Bile
broth 2% (BGLB 2%).
2. Masukkan semua tabung ke dalam lemari pengeram (inkubator) pada suhu 36
± 1°C selama 24-48 jam. Adanya gas pada tabung BGLB memperkuat adanya
bakteri Coliform pada sampel.
3. Catat jumlah tabung yang positif gas pada uji penegasan.
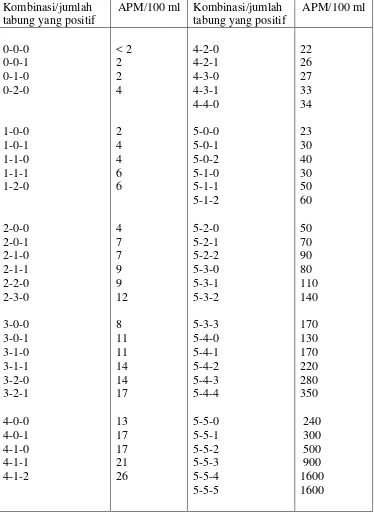
Tabel 2. Daftar APM Coliform Menggunakan 5 Tabung Kombinasi/jumlah
tabung yang positif
APM/100 ml Kombinasi/jumlah tabung yang positif
BAB IV
HASIL DAN PEMBAHASAN
4.1 Hasil
Hasil pengujian bakteri Coliform pada air sumur yang dilaksanakan di
Laboratorium Mikrobiologi Balai Riset dan Standardisasi (Baristand) Industri
[image:32.595.112.514.304.418.2]Medan dapat dilihat pada Tabel 3.
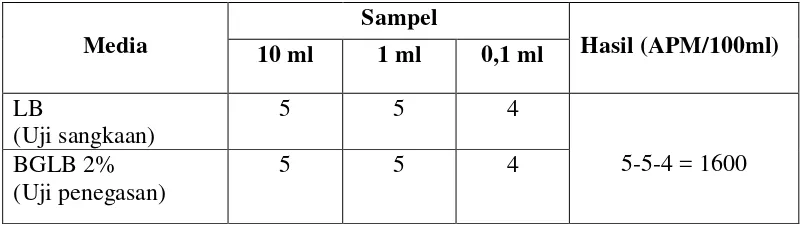
Tabel 3. Hasil pengujian bakteri Coliform pada air sumur
Media
Sampel
Hasil (APM/100ml) 10 ml 1 ml 0,1 ml
LB
(Uji sangkaan)
5 5 4
5-5-4 = 1600 BGLB 2%
(Uji penegasan)
5 5 4
4.2 Pembahasan
Dari tabel di atas dapat dilihat bahwa kombinasi/jumlah tabung yang
positif yang terjadi pada media BGLB 2% (uji penegasan/uji konfirmasi) yaitu
5-5-4, hal ini ditandai dengan adanya kekeruhan dan gelembung gas, maka Angka
Paling Mungkin pengujian bakteri Coliform pada air sumur sesuai dengan daftar
APM Coliform menggunakan 5 tabung adalah 1600/100 ml, hasil tersebut tidak
memenuhi persyaratan kadar maksimum menurut Peraturan Menteri Kesehatan
Nomor 416/Menkes/Per/IX/1990 yaitu 50/100 ml.
Menurut Nugroho (2006), golongan bakteri Coli merupakan indikator
alami baik di dalam air tampak jernih maupun air kotor, yang dapat
temperatur 37°C. Bakteri koliform dapat digunakan sebagai indikator karena
densitasnya berbanding lurus dengan tingkat pencemaran air.
Pencemaran ini dapat disebabkan karena masuknya kotoran manusia dan
binatang. Selain itu juga dapat disebabkan kembalinya air buangan ke dalam
sumur secara langsung atau melalui tempat bocor atau celah-celah tanah
BAB V
KESIMPULAN DAN SARAN
5.1 Kesimpulan
Bakteri Coliform yang terdapat pada salah satu air sumur di Medan Johor
adalah 1600/100 ml dan air sumur tersebut tidak memenuhi persyaratan kualitas
air bersih Peraturan Menteri Kesehatan Nomor 416/Menkes/Per/IX/1990.
5.2. Saran
Disarankan kepada peneliti selanjutnya untuk melakukan pengujian air
sumur yang diuji dengan menggunakan parameter lain, seperti parameter fisika,
kimia, dan radioaktivitas. Hal tersebut sangat dibutuhkan untuk mengetahui
kualitas air bersih apakah layak atau tidak untuk digunakan dalam keperluan
DAFTAR PUSTAKA
Ditjen POM. (1995). Farmakope Indonesia Edisi IV. Jakarta: Departemen Kesehatan RI. Hal. 1112-1116.
Dwidjoseputro, D. (1978). Dasar-Dasar Mikrobiologi. Jakarta: Djambatan. Hal. 159, 162.
Entjang, I. (2000). Ilmu Kesehatan Masyarakat. Bandung: PT. Citra Aditya Bakti. Hal. 75-77.
Fardiaz, S. (1993). Analisis Mikrobiologi Pangan. Jakarta: Raja Grafindo Persada. Hal. 68, 70.
Kusnaedi. (2010). Mengolah Air Kotor untuk Air Minum. Jakarta: Penebar Swadaya. Hal. 3-7.
Menkes RI. (1990). Daftar Persyaratan Kualitas Air Bersih. Jakarta: Peraturan Menteri Kesehata RI. Hal. 12-13.
Nugroho, A. (2006). Bioindikator Kualitas Air. Jakarta: Universitas Trisakti. Hal. 19-22.
Pelczar, J.R. (1958). Microbiology. New York London: University of Maryland. Hal. 406.
Pratiwi, S.T. (2008). Mikrobiologi Farmasi. Yogyakarta: Erlangga. Hal. 136. SNI. (1992). Cara Uji Cemaran Mikroba. Jakarta: Badan Standardisasi Nasional.
Hal. 9, 11-12, 36, 40-41.
Suriawiria, U. (1996). Mikrobiologi Air dan Dasar-Dasar Pengolahan Buangan Secara Biologis. Bandung: Alumni. Hal. 5, 68-69, 74, 79, 86-87.
Suryanto, D., dan Munir, E. (2006). Bahan Ajar Mikrobiologi. Medan: Sumatera Utara. Hal. 37, 39, 51.
LAMPIRAN
Sampel Air Sumur
Timbangan Analitik
Oven
Autoklaf
Pada media Lactose Broth (double strength) dan Lactose Broth (single strength)
Pada media Lactose Broth (single strength)