PENGARUH KONSENTRASI EMULSI LILIN DAN LAMA PENYIMPANAN TERHADAP MUTU BUAH JERUK MANIS (Citrus sinensis, Linn.)
SKRIPSI
DIAJUKAN OLEH:
FERONICA PAULINA M. SIMBOLON NIM 040804010
FAKULTAS FARMASI
UNIVERSITAS SUMATERA UTARA MEDAN
PENGARUH KONSENTRASI EMULSI LILIN DAN LAMA PENYIMPANAN TERHADAP MUTU BUAH JERUK MANIS (Citrus sinensis, Linn.)
SKRIPSI
Diajukan untuk melengkapi salah satu syarat untuk mencapai gelar Sarjana Farmasi pada Fakultas Farmasi
Universitas Sumatera Utara
FERONICA PAULINA M. SIMBOLON NIM 040804010
FAKULTAS FARMASI
UNIVERSITAS SUMATERA UTARA MEDAN
Pengesahan Skripsi
PENGARUH KONSENTRASI EMULSI LILIN DAN LAMA PENYIMPANAN TERHADAP MUTU BUAH JERUK MANIS (Citrus sinensis, Linn.)
DIAJUKAN OLEH:
FERONICA PAULINA M. SIMBOLON NIM 040804010
Dipertahankan di hadapan Panitia Penguji Skripsi Fakultas Farmasi
Universitas Sumatera Utara Pada Tanggal : Desember 2008 Pembimbing I, Panitia Penguji,
(Dra. Masria L. Tambunan, M.Si., Apt.) (Prof. Dr. Jansen Silalahi, M.App.Sc,Apt.) NIP 130 604 974 NIP 130 804 138
Pembimbing II, (Dra. Masria L. Tambunan, M.Si., Apt.) NIP 130 604 974
(Drs. Imannuel S. Meliala, M.Si., Apt.) (Dra. Saleha Salbi, M.Si., Apt.) NIP 131 283 718 NIP 130 817 963
(Drs. Syahrial Yoenoes, SU., Apt.) NIP 131 286 001
Dekan,
(Prof. Dr. Sumadio Hadisahputra, Apt.) NIP 131 283 716
KATA PENGANTAR
Puji dan syukur kepada Tuhan Yang Maha kuasa atas anugerah dan kasih
setia-Nya, sehingga penulis dapat menjalani masa perkuliahan dan penelitian hingga
akhirnya menyelesaikan penyusunan skripsi ini.
Ucapan terima kasih yang tulus tiada terhingga kepada Ayahanda Tombang
Simbolon dan ibunda Netty Silaban yang tercinta, serta kepada kakakku Shinta,
adikku Samuel dan Rouli yang telah sabar dan setia memberikan perhatian,
dorongan semangat dan doa kepada penulis selama perkuliahan hingga
penyelesaian skripsi ini.
Penulis juga mengucapkan terima kasih yang sebesar-besarnya kepada:
1. Ibu Dra. Masria L. Tambunan, M.Si., Apt. dan Bapak Drs. Imannuel S.
Meliala, M.Si., Apt., selaku dosen pembimbing yang telah membimbing penulis
dengan kesabaran selama melakukan penelitian hingga selesainya penulisan
skripsi ini, juga kepada Bapak Drs. Nahitma Ginting, M.Si., Apt. yang telah
banyak memberikan masukan untuk penelitian ini.
2. Bapak Prof. Dr. Jansen Silalahi, M.App.Sc,Apt., Ibu Dra. Saleha Salbi, M.Si.,
Apt., dan Bapak Drs. Syahrial Yoenoes, SU., Apt., selaku dosen penguji yang
telah memberikan petunjuk dan bimbingan untuk penyelesaian skripsi ini.
3. Bapak Prof. Dr. rer nat Effendy De Lux Putra, SU., Apt., selaku penasehat
akademik dan seluruh dosen staf pengajar Fakultas Farmasi yang telah
memberikan motivasi dan bimbingan selama masa pendidikan.
4. Bapak Prof. Dr. Sumadio Hadisahputra, Apt, selaku dekan Fakultas Farmasi
5. Kepada teman-temanku stambuk 2004 khususnya “KANTIN” dan “KAPAS”
atas dukungan semangat dan kebersamaan selama masa pendidikan, “SOLA
GRATIA” yang selalu menjadi tempatku berbagi, Bona R3, Qenten Angels dan
Blue Mio yang selalu setia menemaniku.
6. Abang, kakak, dan adik-adik Fakultas Farmasi atas dukungan dan semangat
kepada penulis.
Akhirnya penulis berharap semoga skripsi ini dapat menjadi sumbangan
yang bermanfaat bagi ilmu pengetahuan pada umumnya dan ilmu farmasi pada
khususnya.
Medan, Desember 2008
Penulis,
ABSTRAK
Telah dilakukan penelitian untuk mengetahui pengaruh konsentrasi emulsi
lilin dan lama penyimpanan terhadap kadar vitamin C dan nilai organoleptik
(warna, aroma dan rasa) dari buah jeruk manis (Citrus sinensis, Linn.). Penelitian
ini menggunakan metode rancangan acak lengkap (RAL) dengan dua faktor yaitu:
konsentrasi emulsi lilin (K1=0%, K2=3%, K3= 6%, K4=9%) dan lama penyimpanan
(L1=0 hari, L2=5 hari, L3=10 hari, L4=15 hari, L5=20 hari).
Penetapan kadar vitamin C dilakukan dengan titrasi menggunakan
2,6-diklorofenol indofenol dan nilai organoleptik (warna, aroma dan rasa) ditentukan
dengan uji hedonik menggunakan panelis tak terlatih.
Hasil penelitian menunjukkan bahwa konsentrasi emulsi lilin memberikan
pengaruh yang berbeda sangat nyata terhadap kadar vitamin C dan nilai
organoleptik (warna, aroma dan rasa). Dimana kadar vitamin C, nilai organoleptik
warna dan aroma meningkat dengan meningkatnya konsentrasi emulsi lilin
sedangkan nilai organoleptik rasa meningkat sampai dengan K3 dan menurun pada
K4. Lama penyimpanan memberikan pengaruh yang berbeda sangat nyata terhadap
kadar vitamin C dan nilai organoleptik rasa. Dimana kadar vitamin C dan nilai
ABSTRACT
The researches to know effects of the concentration of waxy emulsion and
the storage time to concentration of vitamin C and organoleptic value (color, odor
and flavor) of sweet orange (Citrus sinensis, Linn.) have been conducted. This
research applied completely randomized design method with two factors. The first
factor was the concentration of waxy emulsion (K1=0%, K2=3%, K3= 6%, K4=9%)
and the second factor was the storage time (L1=0 day, L2=5 days, L3=10 days,
L4=15 days, L5=20 days).
The concentration of vitamin C was measured by titration using
2,6-dichlorofenol indophenols. The organoleptic value (color, odor and flavor) was
done by hedonic test used untrained panelist.
The result of the research showed that the concentration of waxy emulsion
gave the significant effect to the concentration of vitamin C and organoleptic value
(color, odor and flavor). The concentration of vitamin C and organoleptic value
(color and odor) were increased with the increasing of the concentration of waxy
emulsion and organoleptic value of flavor were increased till K3 and decreased at
K4. The storage time gave the significant effect to the concentration vitamin C and
organoleptic value of flavor. The concentration of vitamin C and organoleptic value
DAFTAR ISI
Halaman
JUDUL ... i
HALAMAN PENGESAHAN ... ii
ABSTRAK ... iii
ABSTRACT ... iv
DAFTAR ISI ... v
DAFTAR TABEL ... viii
DAFTAR GAMBAR ... ix
BAB I. PENDAHULUAN ... 1
1.1 Latar Belakang ... 1
1.2 Perumusan Masalah ... 3
1.3 Hipotesis ... 4
1.4 Tujuan Penelitian ... 4
1.5 Manfaat Penelitian... 5
BAB II. TINJAUAN PUSTAKA... 6
2.1 Jeruk Manis... 7
2.1.1 Sistematika Tumbuhan……….. 7
2.1.2 Komposisi Kimia dan Nilai Gizi Buah Jeruk Manis……. 8
2.2 Vitamin C……… 9
2.2.1 Uraian Bahan………. 9
2.2.2 Stabilitas………... 10
2.2.3 Fungsi Fisiologis Dalam Tubuh……… 11
2.3 Penetapan Kadar Vitamin C……….. 13
2.4 Pelilinan……….14
2.5 Emulsi Lilin………15
2.6 Penyimpanan………. 16
BAB III. METODOLOGI PENELITIAN... 17
2.1 Alat-alat ... 17
2.2 Bahan-bahan ...17
2.3 Prosedur Penelitian ... 17
2.3.1 Pengambilan Sampel ... 17
2.3.2 Pembuatan dan Pembakuan Larutan Pereaksi ... 18
2.3.2.1 Pembuatan Larutan 2,6-Diklorofenol indofenol... 18
2.3.2.2 Pembuatan Larutan Asam Metafosfat Asetat...18
2.3.2.2 Pembuatan Emulsi Lilin……….18
2.3.2.4 Pembakuan 2,6-Diklorofenol indofenol…………. 19
2.3.3 Pengolahan Sampel ... 20
2.3.3.1 Penyiapan Sampel... 20
2.3.3.2 Pelapisan Emulsi Lilin...20
2.3.4 Pengumpulan Data... 21
2.3.4.1 Penetapan Kadar Vitamin C... 21
2.3.4.2 Uji Organoleptik... 22
2.4 Analisis Data... 22
BAB III. HASIL DAN PEMBAHASAN ...25
3.1Kadar Vitamin C ……... 26
3.1.2 Pengaruh Lama Penyimpanan Terhadap Kadar
Vitamin C………..……….28
3.1.3 Pengaruh Interaksi Konsentrasi Emulsi Lilin dan Lama Penyimpanan Terhadap Kadar Vitamin C...30
3.2Nilai Organoleptik Warna... 32
3.2.1 Pengaruh Konsentrasi Emulsi Lilin Terhadap Nilai Organoleptik Warna... 32
3.2.2Pengaruh Lama Penyimpanan Terhadap Nilai Organoleptik Warna………..…..34
3.2.3 Pengaruh Interaksi Konsentrasi Emulsi Lilin dan Lama Penyimpanan Terhadap Nilai Organoleptik Warna……....34
3.3 Nilai Organoleptik Aroma………...36
3.3.1 Pengaruh Konsentrasi Emulsi Lilin Terhadap Nilai Organoleptik Aroma……….….36
3.3.2 Pengaruh Lama Penyimpanan Terhadap Nilai Organoleptik Aroma……….…….37
3.3.3 Pengaruh Interaksi Konsentrasi Emulsi Lilin dan Lama Penyimpanan Terhadap Nilai Organoleptik Aroma……...38
3.4 Nilai Organoleptik Rasa………..39
3.4.1 Pengaruh Konsentrasi Emulsi Lilin Terhadap Nilai Organoleptik Rasa……….40
3.4.2 Pengaruh Lama Penyimpanan Terhadap Nilai Organoleptik Rasa……….41
3.4.3 Pengaruh Interaksi Konsentrasi Emulsi Lilin dan Lama Penyimpanan Terhadap Nilai Organoleptik Aroma…...43
BAB IV. KESIMPULAN DAN SARAN ... 46
4.1 Kesimpulan ... 46
4.2 Saran ... 46
DAFTAR PUSTAKA ... 47
ABSTRAK
Telah dilakukan penelitian untuk mengetahui pengaruh konsentrasi emulsi
lilin dan lama penyimpanan terhadap kadar vitamin C dan nilai organoleptik
(warna, aroma dan rasa) dari buah jeruk manis (Citrus sinensis, Linn.). Penelitian
ini menggunakan metode rancangan acak lengkap (RAL) dengan dua faktor yaitu:
konsentrasi emulsi lilin (K1=0%, K2=3%, K3= 6%, K4=9%) dan lama penyimpanan
(L1=0 hari, L2=5 hari, L3=10 hari, L4=15 hari, L5=20 hari).
Penetapan kadar vitamin C dilakukan dengan titrasi menggunakan
2,6-diklorofenol indofenol dan nilai organoleptik (warna, aroma dan rasa) ditentukan
dengan uji hedonik menggunakan panelis tak terlatih.
Hasil penelitian menunjukkan bahwa konsentrasi emulsi lilin memberikan
pengaruh yang berbeda sangat nyata terhadap kadar vitamin C dan nilai
organoleptik (warna, aroma dan rasa). Dimana kadar vitamin C, nilai organoleptik
warna dan aroma meningkat dengan meningkatnya konsentrasi emulsi lilin
sedangkan nilai organoleptik rasa meningkat sampai dengan K3 dan menurun pada
K4. Lama penyimpanan memberikan pengaruh yang berbeda sangat nyata terhadap
kadar vitamin C dan nilai organoleptik rasa. Dimana kadar vitamin C dan nilai
ABSTRACT
The researches to know effects of the concentration of waxy emulsion and
the storage time to concentration of vitamin C and organoleptic value (color, odor
and flavor) of sweet orange (Citrus sinensis, Linn.) have been conducted. This
research applied completely randomized design method with two factors. The first
factor was the concentration of waxy emulsion (K1=0%, K2=3%, K3= 6%, K4=9%)
and the second factor was the storage time (L1=0 day, L2=5 days, L3=10 days,
L4=15 days, L5=20 days).
The concentration of vitamin C was measured by titration using
2,6-dichlorofenol indophenols. The organoleptic value (color, odor and flavor) was
done by hedonic test used untrained panelist.
The result of the research showed that the concentration of waxy emulsion
gave the significant effect to the concentration of vitamin C and organoleptic value
(color, odor and flavor). The concentration of vitamin C and organoleptic value
(color and odor) were increased with the increasing of the concentration of waxy
emulsion and organoleptic value of flavor were increased till K3 and decreased at
K4. The storage time gave the significant effect to the concentration vitamin C and
organoleptic value of flavor. The concentration of vitamin C and organoleptic value
BAB I PENDAHULUAN 1.1 Latar Belakang
Jeruk manis (Citrus sinensis, Linn.) merupakan komoditi hasil pertanian
Indonesia yang sangat diminati konsumen dari dalam dan luar negeri. Jeruk
mengandung beragam zat gizi dan non gizi yang bermanfaat dalam mencegah
kanker dan meningkatkan kesehatan. Masyarakat yang mengkonsumsi buah jeruk
dalam jumlah relatif banyak dalam makanan sehari-hari memiliki risiko penyakit
degeneratif yang rendah. Salah satu komponen bioaktif yang berkhasiat dalam buah
jeruk adalah vitamin C ( Silalahi, 2006).
Vitamin C memiliki fungsi fisiologis yang penting bagi tubuh. Vitamin ini
berperan sebagai antioksidan dalam makanan maupun dalam berbagai proses tubuh.
Sebagai contoh, di dalam tubuh, vitamin C dapat melindungi asam lemak tak jenuh
rantai panjang, vitamin E dan vitamin A dari oksidasi. Ini adalah fungsi yang
penting karena asam lemak tak jenuh rantai panjang dan vitamin E adalah
komponen esensial untuk mempertahankan keutuhan membran sel (William and
Caliendo, 1984). Vitamin C juga dapat mencegah munculnya penyakit skorbut
dengan dosis yang tepat dan defisiensi vitamin C dapat menyebabkan melemahnya
struktur kolagen sehingga terjadi gusi berdarah serta rasa sakit pada persendian,
kerusakan jaringan penyakit, dan lamanya proses penyembuhan luka, yang
semuanya itu adalah gejala skorbut (Silalahi, 2006).
Buah jeruk manis dihasilkan di berbagai daerah di tanah air sesuai dengan
musimnya, di mana pada waktu panen besar produksi berlebihan sehingga harga di
termasuk komoditas hortikultura yang mempunyai sifat bawaan mudah rusak dan
tidak tahan lama disimpan. Salah satu penyebab kerusakan adalah masih
berlangsungnya aktivitas fisiologi sehingga terjadi perubahan fisik, perubahan
warna, kehilangan berat dan penurunan nilai nutrisinya. Akibat perubahan warna,
tekstur, bau dan rasa yang terjadi, mutu jeruk menjadi rendah (Aak, 1994). Selain
itu dalam penyimpanan terjadi perubahan komposisi kimia khususnya
senyawa-senyawa yang labil seperti vitamin C (asam askorbat) akibat proses oksidasi
(Pracaya, 2003).
Proses oksidasi dapat menyebabkan berkurangnya asam askorbat, karena
asam askorbat sangat peka terhadap oksidasi terutama oleh karena adanya enzim
asam askorbat oksidase yang terdapat dalam jaringan tanaman (Apandi, 1984).
Asam askorbat sangat mudah teroksidasi menjadi L-dehidroaskorbat yang masih
mempunyai keaktifan sebagai vitamin C. Asam L-dehidroaskorbat secara kimia
sangat labil dan dapat mengalami perubahan lebih lanjut menjadi asam
L-diketogulat yang tidak memiliki keaktifan vitamin C lagi (Winarno dan Aman,
1981).
Salah satu cara yang dapat dilakukan untuk memperpanjang daya simpan
buah adalah teknologi pelapisan lilin. Teknik ini mampu memperpanjang umur
simpan beberapa produk hortikultura pada suhu ruang, selain itu mampu
mempertahankan mutu produk selama penyimpanan. Keunggulan teknik ini adalah
biaya investasinya relatif kecil di mana prosedur pelaksanaannya mudah dan
sederhana. Teknik ini merupakan pertimbangan utama dalam penanganan pasca
minim akan fasilitas pasca panen dan terutama di daerah tropis, dimana tingkat
kerusakan pasca panennya cukup tinggi (Hadiwiyoto dan Soehardi, 1981).
Lilin yang biasa digunakan adalah lilin parafin, lilin karnauba dan lilin tebu.
Cara pemberian lapisan lilin yang paling praktis adalah dengan menggunakan
emulsi lilin dalam air. Emulsi lilin dalam air dapat digunakan tanpa harus
mengeringkan buah terlebih dahulu (Pantastico, 1986).
Lapisan lilin dengan kepekatan yang cukup dapat diberikan untuk
menghindarkan oksidasi pada buah dan dapat memberikan perlindungan yang
diperlukan terhadap luka dan goresan kecil pada permukaan buah. Lilin sering
dikombinasikan dengan fungisida dan bakterisida untuk mengendalikan
pembusukan (Hadiwiyoto dan Soehardi, 1981).
Berdasarkan uraian di atas maka penulis tertarik untuk meneliti sejauh
mana pengaruh konsentrasi emulsi lilin dan lama penyimpanan terhadap mutu buah
jeruk manis (Citrus sinensis Linn) serta untuk mendapatkan konsentrasi emulsi lilin
dan lama penyimpanan yang optimum. Adapun parameter yang diukur adalah
vitamin C dan organoleptik (warna, aroma dan rasa).
1.2 Perumusan Masalah
a. Apakah ada pengaruh konsentrasi emulsi lilin terhadap kadar vitamin C dan
nilai organoleptik (warna,aroma dan rasa) buah jeruk manis (Citrus sinensis,
Linn.)?
b. Apakah ada pengaruh lama penyimpanan terhadap kadar vitamin C dan nilai
c. Apakah ada pengaruh kombinasi perlakuan konsentrasi emulsi lilin dan lama
penyimpanan terhadap kadar vitamin C dan nilai organoleptik (warna,aroma dan
rasa) buah jeruk manis (Citrus sinensis, Linn.)?
1.3 Hipotesis
a. Konsentrasi emulsi lilin dapat mempengaruhi kadar vitamin C dan nilai
organoleptik (warna,aroma dan rasa) buah jeruk manis (Citrus sinensis, Linn.).
b. Lama penyimpanan dapat mempengaruhi kadar vitamin C dan nilai
organoleptik (warna,aroma dan rasa) buah jeruk manis (Citrus sinensis, Linn.).
c. Kombinasi perlakuan konsentrasi emulsi lilin dan lama penyimpanan
mempengaruhi kadar vitamin C dan nilai organoleptik (warna,aroma dan rasa)
buah jeruk manis (Citrus sinensis, Linn.).
1.4 Tujuan Penelitian
a. Untuk mengetahui pengaruh konsentrasi emulsi lilin terhadap kadar vitamin C
dan nilai organoleptik (warna,aroma dan rasa) buah jeruk manis (Citrus
sinensis, Linn.).
b. Untuk mengetahui pengaruh lama penyimpanan terhadap kadar vitamin C dan
nilai organoleptik (warna,aroma dan rasa) buah jeruk manis (Citrus sinensis,
Linn.).
c. Untuk mengetahui pengaruh kombinasi perlakuan konsentrasi emulsi lilin dan
lama penyimpanan terhadap kadar vitamin C dan nilai organoleptik
(warna,aroma dan rasa) buah jeruk manis (Citrus sinensis, Linn.).
1.5 Manfaat Penelitian
Dari hasil penelitian ini diharapkan dapat dijadikan sumber informasi
ditinjau dari kadar vitamin C dan nilai organoleptik (warna,aroma dan rasa) selama
BAB II
TINJAUAN PUSTAKA 2.1 Jeruk Manis
Tanaman jeruk dikenal dengan nama latin Citrus sinensis Linn. Tumbuhan
ini merupakan tanaman yang dapat tumbuh baik di daerah tropis dan subtropis.
Jeruk manis dapat beradaptasi dengan baik didaerah tropis pada ketinggian
900-1200 meter di atas permukaan laut dan udara senantiasa lembab, serta mempunyai
persyaratan air tertentu (Rismunandar, 1986). Tanaman jeruk manis dapat mencapai
ketinggian 3-10 m. Tangkai daun 0,5-3,5 cm. Daun berbentuk elips atau bulat telur
memanjang. Buah jeruk berbentuk bulat atau bulat rata dan memiliki kulit buah
yang tebal (sekitar 0,3 – 0,5 cm), daging buah kuning, jingga atau
kemerah-merahan. Daging buah terbagi-bagi atas 8-13 segmen yang mengelilingi sumbu
buah. Biji jeruk berbentuk bulat telur dan berwarna putih atau putih keabuan
(Steenis, 1987).
2.1.1 Sistematika Tumbuhan
Divisi : Spermatophyta
Kelas : Angiospermae
Sub Kelas : Monocotyledoneae
Bangsa : Rutales
Suku : Rutaceae
Marga : Citrus
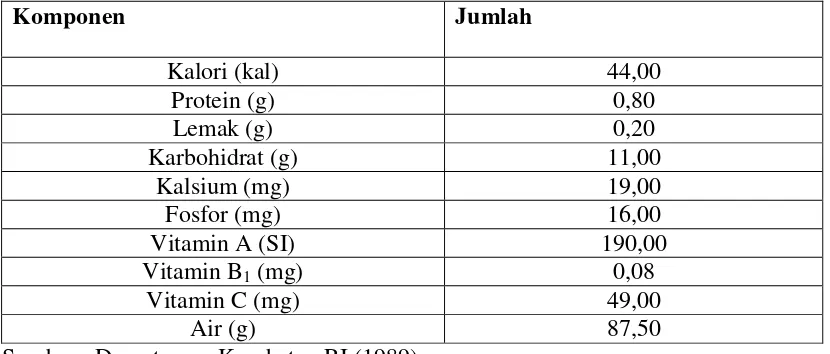
2.1.2 Komposisi Kimia dan Nilai Gizi Buah Jeruk Manis
Komposisi kimia dan nilai gizi pada sari buah jeruk manis dapat dilihat pada
tabel 1.
Tabel 1. Komposisi Kimia dan Nilai Gizi per 100 gram Sari Buah Jeruk Manis
Komponen Jumlah
Kalori (kal) 44,00
Protein (g) 0,80
Lemak (g) 0,20
Karbohidrat (g) 11,00
Kalsium (mg) 19,00
Fosfor (mg) 16,00
Vitamin A (SI) 190,00
Vitamin B1 (mg) 0,08
Vitamin C (mg) 49,00
Air (g) 87,50
Sumber : Departemen Kesehatan RI (1989)
2.2 Vitamin C
Vitamin C adalah vitamin yang tergolong vitamin yang larut dalam air.
Sumber Vitamin C sebagian besar tergolong dari sayur-sayuran dan buah-buahan
terutama buah-buahan segar. Asupan gizi rata-rata sehari sekitar 30 sampai 100 mg
vitamin C yang dianjurkan untuk orang dewasa. Namun, terdapat variasi kebutuhan
dalam individu yang berbeda (Sweetman, 2005).
Gambar 1. Rumus bangun vitamin C
b. Rumus molekul : C6H8O6
c. Berat molekul : 176,13
d. Nama kimia : L-Asam askorbat
e. Pemerian : Hablur atau serbuk putih atau agak kuning. Oleh pengaruh cahaya lambat laun menjadi berwarna gelap. Dalam
keadaan kering stabil diudara, dalam larutan cepat teroksidasi.
f. Kelarutan : Mudah larut dalam air; agak sukar larut dalam etanol; tidak
larut dalam kloroform, dalam eter dan dalam benzena.
2.2.2 Stabilitas
Asam askorbat merupakan ester siklik. Dalam larutan air mudah teroksidasi
(reaksinya bolak-balik) membentuk asam dehidro-askorbat (Connors, dkk., 1986).
Asam askorbat bersifat sangat sensitif terhadap pengaruh-pengaruh luar
yang menyebabkan kerusakan seperti suhu, konsentrasi gula dan garam, pH,
oksigen, enzim, dan katalisator logam (Andarwulan dan Koswara, 1989).
Asam dehidro-askorbat dapat mengalami hidrolisis lebih lanjut membentuk
produk degradasi yang bereaksi tidak bolak-balik asam diketoglukonat dan asam
oksalat. Asam askorbat juga gampang mengalami degradasi di bawah kondisi
anaerob, membentuk furfural dan karbon dioksida. Profil laju-pH bagi keduanya
baik degradasi aerob maupun anaerob akan mencapai maksimal pada sekitar pH 4
(Connors, dkk., 1986).
Suatu larutan asam askorbat 5% dalam air memiliki pH 2.1-2.6, pH dari
10% larutan kalsium askorbat dalam air adalah antara 6.8 dan 7.4, dan pH dari
maksimum terjadi dekat pH 3 dan pH 6. Stabilitas asam askorbat dalam bentuk
sediaan padat cukup baik, asal kelembabannya dikendalikan (Connors, dkk., 1986).
2.2.3 Fungsi Fisiologis Dalam Tubuh
Beberapa fungsi asam askorbat dipercaya berhubungan dengan konversi reaksi reduksi-oksidasinya di dalam jaringan tubuh. Salah satu fungsi vitamin C
adalah sebagai antioksidan. Beberapa zat dalam makanan, didalam tubuh
dihancurkan atau dirusak jika mengalami oksidasi. Sering kali, zat tersebut
dihindari dari oksidasi dengan menambahkan antioksidan. Suatu antioksidan adalah
zat yang dapat melindungi zat lain dari oksidasi dimana dirinya sendiri yang
teroksidasi. Vitamin C, karena memiliki daya antioksidan, sering ditambahkan pada
makanan untuk mencegah perubahan oksidatif (William and Caliendo, 1984).
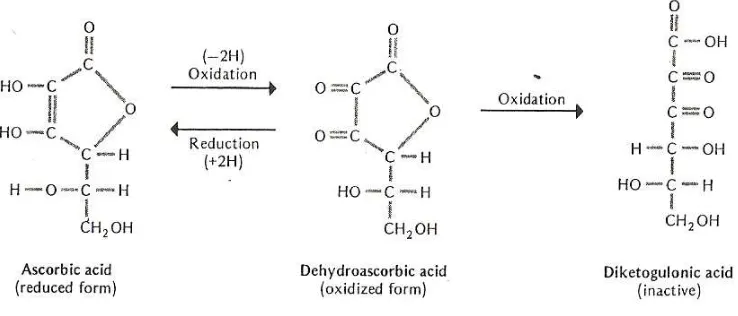
Gambar 2. Reduksi-Oksidasi dari Vitamin C
Salah satu fungsi utama vitamin C berkaitan dengan sintesis kolagen.
Kolagen adalah sejenis protein yang merupakan salah satu komponen utama dari
jaringan ikat, tulang-tulang rawan, matriks tulang, dentin, lapisan endotelium
pembuluh darah dan lain-lain. Vitamin C ini bertindak sebagai enzim atau
ko-faktor pada proses hidroksilasi, baik secara aktif maupun sebagai zat reduktor.
jenis asam amino yang merupakan komponen utama dari kolagen. Vitamin C juga
berperan dalam proses penyembuhan luka (Tjokronegoro, 1985).
Kekurangan asupan vitamin C dapat menyebabkan skorbut. Dalam
kasus-kasus skorbut spontan, biasanya terjadi gigi mudah tanggal, gingivitis, dan anemia,
yang mungkin disebabkan oleh adanya fungsi spesifik asam askorbat dalam sintesis
hemoglobin. Skorbut dikaitkan dengan gangguan sintesis kolagen yang
manifestasinya berupa luka yang sulit sembuh, gangguan pembentukan gigi, dan
robeknya kapiler, yang banyak menyebabkan petechiae dan gabungannya yang
membentuk ecchymoses. Sementara ecchymoses dianggap berhubungan dengan
kebocoran pembuluh darah kapiler akibat adhesi sel-sel andotel yang kurang
memadai, diduga pula bahwa jaringan berserabut perkapiler mengalami kerusakan
pada kondisi skorbut sehingga pembuluh darah kapiler menjadi lemah dan robek
jika mendapat tekanan (Gilman, et al, 1996).
2.2.4 Perubahan Vitamin C Dalam Buah
Buah yang masih mentah mengandung vitamin C yang cukup banyak dan
semakin tua buah semakin berkurang kandungan vitamin C – nya. Vitamin C juga
disebut asam askorbat dapat disintesis dari D-glukosa atau D-galaktosa merupakan
gula heksosa (Winarno dan Aman, 1981).
Pada umumnya semakin banyak mendapat sinar matahari pada waktu
tanaman tumbuh, semakin banyak pula kandungan asam askorbat (Apandi, 1984).
Hal ini disebabkan semakin banyak mendapat cahaya, setiap proses fotosintesis
akan semakin giat dan gula heksosa akan semakin banyak terbentuk. Kandungan
penyimpanan yang tinggi. Kandungan asam askorbat setelah penyimpanan kira-kira
1/2 sampai 2/3 pada waktu panen (Pantastico, 1986).
Kerusakan mekanis juga dapat menyebabkan berkurangnya asam askorbat,
karena asam askorbat sangat peka terhadap adanya oksidasi terutama oleh karena
adanya enzim asam askorbat oksidase yang terdapat dalam jaringan tanaman
(Apandi, 1984). Enzim lain yang dapat merusak asam askorbat secara tidak
langsung adalah fenolase, sitokhrom oksidase dan peroksidase. Asam askorbat
sangat mudah teroksidasi menjadi L-dehidroaskorbat yang masih mempunyai
keaktifan sebagai vitamin C. Asam L-dehidroaskorbat secara kimia sangat labil dan
dapat mengalami perubahan lebih lanjut menjadi asam L-diketogulat yang tidak
memiliki keaktifan vitamin C lagi (Winarno dan Aman, 1981).
2.3 Penetapan Kadar Vitamin C
Berdasarkan titrasi dengan 2,6-diklorofenol indofenol, dimana terjadi reaksi
reduksi 2,6- diklorofenol indofenol dengan adanya vitamin C dalam larutan asam.
(Hashmi, 1986).
Larutan 2,6-diklorofenol indofenol dalam suasana netral atau basis akan
berwarna biru sedang dalam suasana asam akan berwarna merah muda. Apabila
2,6-diklorofenol indofenol direduksi oleh asam askorbat maka akan menjadi tidak
berwarna, dan bila semua asam askorbat sudah mereduksi 2,6-diklorofenol
indofenol maka kelebihan larutan 2,6-diklorofenol indofenol sedikit saja sudah akan
terlihat dengan terjadinya pewarnaan. Untuk perhitungan maka perlu dilakukan
standarisasi larutan dengan vitamin C standar (Sudarmadji, 1989).
Reaksi yang terjadi antara 2,6-diklorofenolindofenol dan vitamin C dapat
2.4 Pelilinan
Pada seluruh permukaan luar kulit buah-buahan memiliki lapisan lilin yang
alami. Tiap buah memiliki ketebalan lapisan yang berbeda-beda. Lapisan lilin alami
tersebut sebagian hilang akibat pencucian. Oleh karena itu, pemberian lilin terhadap
buah-buahan pascapanen amat diperlukan. Pelapisan lilin dapat mencegah serangan
patogen-patogen pembusuk terutama pada buah-buahan yang memiliki luka atau
goresan-goresan kecil pada permukaan kulit buah. Artinya, kerusakan atau
pembusukan pada saat buah dalam penyimpanan dapat dicegah (Zuhairini, 1996).
Pemberian lilin dapat juga dipergunakan untuk menjaga kesegaran dan
memperpanjang daya simpan buah. Lapisan lilin pada permukaan kulit buah dapat
menekan laju respirasi dan transpirasi buah. Sehingga, kehilangan berat dan
pengerutan buah selama penyimpanan dapat dicegah. Selain itu pelapisan lilin juga
membuat penampakan buah menjadi mengkilat dan lebih menarik. Di
tempat-tempat yang tidak memiliki fasilitas penyimpanan dengan suhu dingin, pelapisan
lilin merupakan cara yang terbaik untuk memperpanjang kesegaran buah bila
Beberapa syarat yang diperlukan untuk lilin sebagai bahan pelapis antara
lain tidak mempengaruhi bau dan rasa komoditi yang akan dilapisi, mudah kering,
tidak mudah pecah, mengkilap dan licin, tidak menghasilkan permukaan yang tebal,
murah harganya dan tidak bersifat racun (Wills et al., 1981).
Pemberian lapisan lilin dapat dilakukan dengan berbagai cara antara lain
dengan pembusaan, penyemprotan, pencelupan, atau dengan pengolesan. Pada
tempat-tempat yang tidak memiliki alat untuk melapisi lilin (seperti alat pembusa,
alat penyemprot, atau alat pengoles berupa kuas yang dipasang pada konveyor),
pelapisan lilin dengan cara pencelupan adalah yang paling efektif. Buah-buahan
yang telah dibersihkan dan diberi fungisida langsung dibenamkan pada tangki
pencelupan yang berisi lilin cair selama 30 detik. Cara ini memang sederhana, tetapi
bila tidak dilakukan secara professional dapat diperoleh endapan lilin yang tebal
menempel pada kulit buah. Pelapisan lilin dengan cara pembusaan adalah cara yang
paling baik. Pelapisan lilin dengan cara pembusaan akan diperoleh lapisan lilin yang
tipis (setelah airnya menguap). Pelapisan lilin ini selain dapat dikombinasi dengan
fungisida, juga dapat dikombinasi dengan zat pengatur tumbuh atau dengan
penurunan suhu (Zuhairini, 1996).
2.5 Emulsi Lilin
Lilin yang biasa digunakan adalah lilin parafin, lilin karnauba dan lilin tebu.
Cara pemberian lapisan lilin yang paling praktis adalah dengan menggunakan
emulsi lilin alam atau resin buatan dalam air. Emulsi lilin dalam air dapat digunakan
tanpa harus mengeringkan buah lebih dahulu. Zat-zat pengemulsi yang cocok
dicampurkan untuk mendapat emulsi yang baik adalah trietanolamin dan asam oleat
Emulsi adalah suatu dispersi dimana fase terdispersi terdiri dari
bulatan-bulatan kecil zat cair yang terdistribusi ke seluruh pembawa yang tidak bercampur.
Dalam batasan emulsi, fase terdispersi dianggap sebagai fase dalam dan medium
pendispersi sebagai fase luar atau fase kontinu. Emulsi yang mempunyai fase dalam
minyak dan fase luar air disebut emulsi minyak dalam air dan biasanya diberi tanda
sebagai emulsi m/a. Sebaliknya emulsi yang mempunyai fase dalam air dan fase
luar minyak disebut emulsi air dalam minyak dan dikenal sebagai emulsi a/m.
Karena fase luar dari suatu emulsi bersifat kontinu, suatu emulsi minyak dalam air
bisa diencerkan atau ditambah dengan air atau suatu preparat dalam air. Umumnya
untuk membuat suatu emulsi yang stabil, perlu fase ketiga atau bagian ketiga dari
emulsi, yakni zat pengemulsi/emulsifying agent (Ansel, 1989).
Emulsi menggunakan zat pengemulsi sintetik, umumnya dibuat sebagai
berikut : zat pengemulsi yang mudah larut dalam air, telebih dahulu dilarutkan
dalam air atau fase air sedangkan zat pengemulsi yang mudah larut dalam minyak,
terlebih dahulu dilarutkan dalam minyak atau fase minyak; lemak atau malam
dipanaskan 100 di atas suhu leburnya. Fase air terlebih dahulu dipanaskan 20 di atas
suhu fase minyaknya dan tambahkan sedikit demi sedikit ke dalam fase minyak
sambil dikocok kuat-kuat, kocok terus hingga dingin. Pemanasan selama pembuatan
emulsi harus dilakukan sedemikian rupa sehingga tidak terjadi lewat panas. Semua
alat perlengkapan yang digunakan untuk pembuatan emulsi harus bersih dan kering
(Ditjen POM, 1978).
Cara pembuatan emulsi lilin standar (12%) adalah dengan memanaskan 120
g lilin pada suhu 900C sampai mencair. Lalu ke dalam lilin yang mencair tersebut
ditambahkan 40 g trietanolamin, sambil terus diaduk suhu dipertahankan pada 900C.
Tahap terakhir, tambahkan ke dalam emulsi lilin tersebut air mendidih sebanyak
850 ml. Bila semuanya telah bercampur, segera angkat dari tempat pemanasan dan
segera didinginkan dengan air mengalir sambil diaduk (Zuhairini, 1996).
2.6 Penyimpanan
Penyimpanan buah-buahan segar dimaksudkan untuk memperpanjang daya
gunanya dan dalam keadaan tertentu memperbaiki mutunya, selain dari itu juga
menghindarkan banjirnya produk di pasar, membantu pemasaran yang teratur dan
mempertahankan mutu produk yang masih hidup. Tujuan utama penyimpanan
adalah pengendalian laju respirasi, trasnpirasi, infeksi penyakit dan
mempertahankan produk dalam bentuk yang paling berguna bagi konsumen. Umur
simpan dapat diperpanjang dengan pengendalian penyakit-penyakit pasca panen,
pengaturan atmosfir, perlakuan kimiawi, penyinaran dan pendinginan (Pantastico,
1986).
Untuk mendapatkan buah senantiasa dalam keadaan segar dibutuhkan
keadaan yang optimal dalam penyimpanannya. Hal ini penting untuk menjamin
daya simpan buah semaksimal mungkin. Suhu penyimpanan untuk setiap jenis
buah-buahan tidak sama. Suhu harus dapat dijaga agar tetap konstan, demikian pula
kelembabannya. Kelembaban udara yang rendah dapat mempercepat terjadinya
transpirasi atau penguapan sehingga dapat menyebabkan kehilangan bobot yang
cukup besar selama penyimpanan. Penyusutan bobot menyebabkan buah mengerut
dan layu serta dapat mempercepat pertumbuhan jasad renik pembusuk sehingga
Pada penyimpanan buah-buahan, sirkulasi udara harus tetap dijaga.
Pemerataan sirkulasi udara dapat dibantu dengan bantuan kipas angin. Penyusunan
buah-buahan yang telah dikemas dalam gudang penyimpanan diatur sedemikian
rupa sehingga tidak mengganggu sirkulasi udara di antara peti-peti kemasan. Peti
tidak boleh berhimpit dengan dinding atau lantai agar respirasi yang berlangsung
pada buah tidak menyebabkan pengab atau panas. Kelembapan sangat berpengaruh
terhadap perkembangan buah, terutama buah yang disimpan. Kelembapan yang
tidak sesuai dapat menimbulkan kerusakan baik secara langsung maupun tidak
langsung. Kelembapan yang rendah dan diimbangi dengan suhu yang tinggi akan
mempercepat terjadinya transpirasi. Bila transpirasi berlangsung dalam waktu yang
cukup lama maka buah akan mengerut terutama bila buah yang dipetik belum
mencapai usia maksimal (belum matang benar). Kelembapan yang tinggi tidak
begitu berpengaruh buruk terhadap perkembangan buah dalam penyimpanan. Tetapi
dapat menimbulkan kerugian secara tidak langsung. Kelembapan yang tinggi
memacu pertumbuhan mikroba pembusuk terlebih bila buah disimpan pada suhu
kamar (Zuhairini, 1996).
BAB III
METODOLOGI PENELITIAN
Penelitian ini bersifat eksperimental yaitu dengan membandingkan variasi
konsentrasi emulsi dan variasi lama penyimpanan terhadap kadar vitamin C dan
nilai organoleptik (warna,rasa dan aroma) sebagai parameter. Penelitian dilakukan
di Laboratorium Sintesis Bahan Obat, Fakultas Farmasi, Universitas Sumatera
Utara.
2.1 Alat-alat
Alat-alat yang digunakan dalam penelitian ini adalah alat-alat gelas, batang
pengaduk, cawan penguap, statif dan klem, buret, mikroburet, eksikator, magnetic
bar , blender (Philips), hotplate magnetic stirrer (Cimarec 2), neraca analitik
(Mettler Toledo), termometer (fischer).
2.2 Bahan-bahan
Bahan- bahan yang digunakan dalam penelitian ini adalah air suling, parafin
padat, benomyl 50 WP, asam askorbat BPFI , trietanolamin (TEA), asam oleat dan
bahan-bahan kimia yang berkualitas proanalisa (E. Merck) : asam metafosfat,
2,6-diklorofenol indofenol, natrium bikarbonat, asam asetat glasial.
2.3 Prosedur Penelitian 2.3.1 Pengambilan Sampel
Pengambilan sampel dilakukan secara purposif tanpa membandingkannya
dengan tumbuhan yang sama pada daerah lain. Buah jeruk manis diambil dari
daerah Kinepen, Kec. Munthe, Kab. Karo, Sumatera Utara. Buah jeruk manis yang
diambil adalah buah yang siap panen yaitu berwarna kuning kehijauan dan diambil
2.3.2 Pembuatan Dan Pembakuan Larutan Pereaksi 2.3.2.1 Pembuatan Larutan 2,6-Diklorofenol indofenol
Timbang seksama 50 mg 2,6-diklorofenol indofenol natrium P yang
sebelumnya telah dikeringkan di atas silika gel P dalam eksikator selama 24 jam,
tambahkan 50 air yang mengandung 42 mg natrium bikarbonat P, kocok kuat dan
jika sudah terlarut tambahkan air hingga 200,0 ml. Saring ke dalam botol bersumbat
kaca berwarna coklat (Ditjen POM, 1995).
2.3.2.2 Pembuatan Larutan Asam Metafosfat Asetat
Asam metafosfat P 30 g dilarutkan dalam 80 ml asam asetat glasial P,
tambahkan air suling secukupnya hingga 1 liter. Simpan ditempat sejuk dan
digunakan dalam waktu dua hari (Ditjen POM, 1979).
2.3.2.3 Pembuatan Emulsi lilin
a. Formula Emulsi lilin 9% :
Parafin padat : 90 gram
Asam oleat : 15 gram
Trietanolamin : 30 gram
Air ad 1000 ml
b. Formula Emulsi lilin 6% :
Parafin padat : 60 gram
Asam oleat : 10 gram
Trietanolamin : 20 gram
Air ad 1000 ml
c. Formula Emulsi lilin 3% :
Asam oleat : 5 gram
Trietanolamin : 10 gram
Air ad 1000 ml
(Zuhairini, 1996)
Cara Pembuatan :
Fase lilin dibuat dengan melebur parafin padat dalam beaker glass (sampai
suhu 60-670C) lalu ditambahkan asam oleat sedikit demi sedikit sambil diaduk. Fase
air dibuat dengan mencampurkan trietanolamin ke dalam 800 ml air lalu
dipanaskan sampai suhu 700C sambil diaduk. Lalu fase air ditambahkan secara
perlahan-lahan ke dalam fase lilin sambil diaduk kuat-kuat, dicukupkan volumenya
dengan air (suhu 700C) hingga 1000 ml. Dilanjutkan pengadukan hingga dingin
(Ditjen POM, 1978).
2.3.2.4 Pembakuan 2,6-diklorofenol indofenol
Ditimbang seksama 50 mg asam askorbat BPFI, pindahkan ke dalam labu
tentukur 50 ml bersumbat kaca dengan bantuan volume secukupnya asam
metafosfat asetat LP sampai tanda. Segera pipet 2 ml ke dalam labu erlenmeyer 50
ml berisi 5 ml larutan asam metafosfat asetat LP dan secara cepat titrasi dengan
larutan 2,6-diklorofenol indofenol hingga warna merah muda mantap tidak kurang
dari 5 detik. Lakukan titrasi blanko menggunakan 7 ml larutan asam metafosfat
asetat P ditambah dengan sejumlah volume air setara dengan volume larutan
2,6-diklorofenol indofenol yang digunakan dalam titrasi larutan asam askorbat. Kadar
larutan baku dinyatakan dalam kesetaraan, dalam mg asam askorbat (Ditjen POM,
1995).
Kesetaraan vitamin C dihitung dengan rumus :
Kesetaraan = Vpemipetan x Berat Vitamin C x % Kadar Vlabu x Fp x (Vtitrasi – Vblanko)
Keterangan :
Vpemipetan : Volume pemipetan (ml)
Fp : Faktor Pengenceran
Vlabu : Volume labu takar (ml)
%Kadar : kemurnian vitamin C
(Perhitungan dapat dilihat pada lampiran 11)
2.3.3 Pengolahan Sampel 2.3.3.1 Penyiapan Sampel
a. Untuk pelapisan emulsi lilin :
Buah yang baru dipanen disortir dengan baik. Dipilih buah yang bentuk,ukuran
dan warna homogen. Selanjutnya dicuci dengan air bersih kemudian dilap
dengan kain bersih.
b. Untuk penetapan kadar vitamin C :
Buah jeruk yang telah dilapisi lilin dibelah menjadi dua bagian, dibuang biji dan
kulitnya kemudian diblender.
c. Untuk penetapan nilai organoleptik :
Buah jeruk yang telah dilapisi lilin dicuci dengan air bersih kemudian dilap
2.3.3.2 Pelapisan Emulsi lilin
Buah jeruk dicelupkan ke dalam Benomyl 50 WP 0,4% selama 30 detik lalu
ditiriskan dan dikering anginkan. Lalu buah yang telah kering dicelupkan ke dalam
emulsi lilin sesuai dengan perlakuan yaitu : 0%, 3%, 6% dan 9%. Pencelupan
dilakukan secara merata keseluruh permukaan buah selama 1 menit. Selanjutnya
buah dikering anginkan sehingga emulsi mengering menutupi permukaan kulit
buah. Kemudian dikemas dengan menggunakan kardus dalam keadaan tidak
bertindihan, dan disimpan pada suhu kamar sesuai dengan perlakuan yaitu : 0 hari,
5 hari, 10 hari, 15 hari dan 20 hari.
2.3.4 Pengumpulan Data
2.3.4.1 Penetapan Kadar Vitamin C
Sampel ditimbang sejumlah 10 g, dimasukkan kedalam labu ukur 100 ml
dan ditambahkan asam metafosfat asetat sampai volume 100 ml, dikocok kemudian
disaring, ± 3 ml filtrat pertama dibuang. Filtrat yang diperoleh dipipet 10 ml
dimasukkan kedalam labu ukur 50 ml dan ditambahkan asam metafosfat asetat
sampai volume 50 ml, dikocok kemudian disaring. Filtrat yang diperoleh dipipet 15
ml ke dalam Erlenmeyer. Kemudian dititrasi dengan larutan 2,6-diklorofenol
indofenol sampai warna merah jambu sebagai titik akhir titrasi yang stabil selama
15 detik, dilakukan titrasi blanko (AOAC, 1990).
Kadar Vitamin C dihitung dengan rumus :
Kadar Vitamin C ( mg/g) = (Vt – Vb) x K x VL x FP Vp x W
Keterangan :
Vt : volume titrasi (ml)
K : kesetaraan
VL : volume larutan (ml)
FP : faktor pengenceran
Vp : volume pemipetan
W : berat sampel (g)
(Perhitungan dapat dilihat pada lampiran 12)
2.3.4.2 Uji Organoleptik
Uji organoleptik yang digunakan adalah uji kesukaan. Prinsipnya adalah
untuk melihat derajat penerimaan konsumen/panelis terhadap atribut warna, aroma
dan rasa dengan merujuk pada tingkat kesukaan. Tingkat penerimaan ini dinyatakan
dalam uji hedonik dan numerik (Soekarto, 1981).
SKALA HEDONIK SKALA NUMERIK
tidak suka 1
agak suka 2
suka 3
sangat suka 4
amat sangat suka 5
Prosedur uji organoleptik :
Panelis diberikan penjelasan singkat mengenai bahan yang diperiksa dan
cara penilaian. Kemudian buah jeruk manis yang telah mengalami perlakuan
pelapisan emulsi lilin disuguhi kepada panelis untuk dilihat, dicium dan dirasai.
Setelah panelis melakukan pengamatan, panelis diminta untuk memberi tanggapan
berdasarkan tingkat kesukaan dengan penilaian mereka masing-masing. Dilakukan
dengan interval waktu 5 hari, dimulai dari hari 0 sampai hari ke 20 dan dilakukan
Untuk penganalisaan, skala hedonik ditransformasi menjadi skala numerik.
Dengan data numerik dapat dilakukan analisa statistik.
2.4 Analisis Data
Pada penelitian dilakukan analisa data statistik dengan menggunakan
analisis sidik ragam yang bertujuan untuk menguji hipotesis sehingga dapat
diketahui apakah ada perbedaan pengaruh tunggal dan interaksi dari perlakuan yang
dicobakan (perhitungan analisis sidik ragam dapat dilihat pada lampiran 13,hal.51).
Pelaksanaan penelitian ini menggunakan model Rancangan Acak Lengkap (RAL)
dalam bentuk faktorial dengan 2 perlakuan, yaitu sebagai berikut:
Faktorial A : Perlakuan konsentrasi emulsi lilin yang terdiri dari 4 taraf, yaitu :
K0 = konsentrasi 0%
K1 = konsentrasi 3%
K2 = konsentrasi 6%
K3 = konsentrasi 9%
Faktorial B : Perlakuan lama penyimpanan yang terdiri dari 4 taraf, yaitu :
L0 = lama penyimpanan 0 hari
L1 = lama penyimpanan 5 hari
L2 = lama penyimpanan 10 hari
L3 = lama penyimpanan 15 hari
L4 = lama penyimpanan 20 hari
Kombinasi perlakuan t: 5 x 4 = 20, maka jumlah ulangan (n) adalah :
(t-1) (n-1) ≥ 15
(20-1) (n-1) ≥ 15
(n-1) ≥ 0,79
n ≥ 1,79
Maka, replikasi setiap unit perlakuan harus lebih besar dari 1,79.
Metode pengolahan data adalah sebagai berikut :
Yijk = μ + αi + βj +(αβ)ij + εijk
dimana :
Yijk = hasil pengamatan dari faktor K pada taraf ke-i dan faktor L dari taraf
ke-j dan ulangan ke-k
μ = efek nilai tengah
αi = efek dari faktor K pada taraf ke-i
βj = efek dari faktor L pada taraf ke-j
(αβ)ij = efek interaksi dari faktor K pada taraf ke-i dengan faktor L pada taraf
ke-j
εijk = efek galat dari faktor K pada taraf ke-i dengan faktor L pada taraf ke-j
BAB IV
HASIL DAN PEMBAHASAN
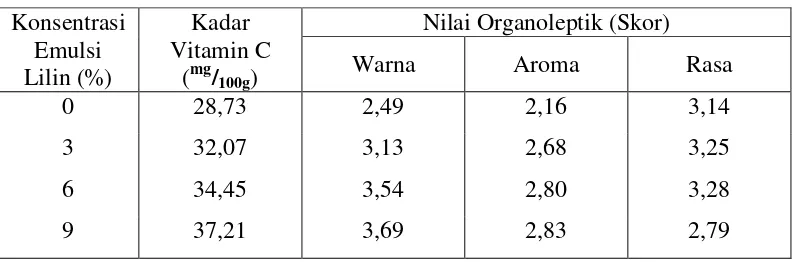
Hasil penelitian secara umum pengaruh konsentrasi emulsi lilin terhadap
parameter yang diamati, yaitu kadar vitamin C, nilai organoleptik warna, aroma dan
[image:38.595.106.504.251.382.2]rasa yang dihasilkan dapat dilihat pada tabel 1.
Tabel 1. Pengaruh Konsentrasi Emulsi Lilin Terhadap Mutu Buah Jeruk Manis
Dari tabel 1 dapat dilihat bahwa kadar vitamin C, nilai organoleptik warna
dan aroma meningkat seiring dengan peningkatan konsentrasi emulsi lilin hingga
9%, sedangkan nilai organoleptik rasa meningkat sampai dengan konsentrasi emulsi
hingga 6% dan mengalami penurunan kembali pada konsentrasi emulsi 9%.
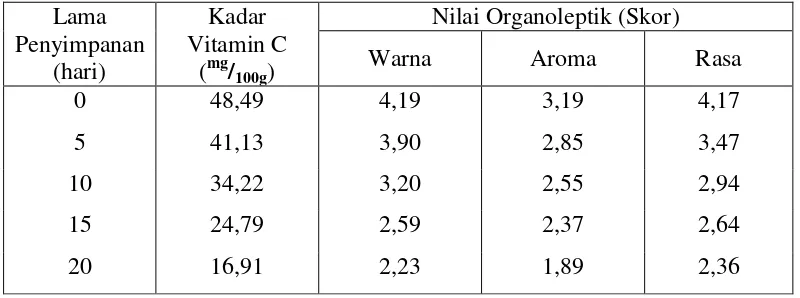
Hasil penelitian secara umum pengaruh lama penyimpanan terhadap
parameter yang diamati, yaitu kadar vitamin C, nilai organoleptik warna, aroma dan
rasa yang dihasilkan dapat dilihat pada tabel 2. Konsentrasi
Emulsi Lilin (%)
Kadar Vitamin C
(mg/100g)
Nilai Organoleptik (Skor)
Warna Aroma Rasa
0 28,73 2,49 2,16 3,14
3 32,07 3,13 2,68 3,25
6 34,45 3,54 2,80 3,28
Tabel 2. Pengaruh Lama Penyimpanan Terhadap Mutu Buah Jeruk Manis
Dari tabel 2 dapat dilihat bahwa kadar vitamin C, nilai organoleptik warna,
aroma dan rasa menurun seiring dengan lama penyimpanan hingga 20 hari
Hasil analisa data secara statistik dari setiap parameter yang diamati dapat
dilihat pada uraian berikut :
3.1 Kadar Vitamin C
Data hasil pengamatan kadar vitamin C dapat dilihat pada lampiran 2.
Pengaruh masing-masing perlakuan terhadap kadar vitamin C yang dihasilkan
adalah sebagai berikut :
3.1.1 Pengaruh Konsentrasi Emulsi Lilin Terhadap Kadar Vitamin C
Hasil analisis pengaruh konsentrasi emulsi lilin terhadap kadar vitamin C
dapat dilihat dari analisa sidik ragam pada lampiran 3, bahwa konsentrasi emulsi
lilin memberikan pengaruh yang berbeda sangat nyata pada taraf 1% terhadap kadar
vitamin C yang dihasilkan. Pengujian lebih lanjut dengan Least Significant Ranges
(LSR) menunjukkan tingkat perbedaan pengaruh konsentrasi emulsi lilin pada
setiap taraf yang diberi tanda notasi huruf terhadap kadar vitamin C seperti yang
tertera pada tabel 3. Lama
Penyimpanan (hari)
Kadar Vitamin C
(mg/100g)
Nilai Organoleptik (Skor)
Warna Aroma Rasa
0 48,49 4,19 3,19 4,17
5 41,13 3,90 2,85 3,47
10 34,22 3,20 2,55 2,94
15 24,79 2,59 2,37 2,64
Tabel 3. Pengujian Least Significant Ranges (LSR) Pengaruh Konsentrasi Emulsi Lilin Terhadap Kadar Vitamin C
Keterangan : - Notasi huruf yang berbeda menunjukkan beda nyata pada taraf 5% dan beda sangat nyata pada taraf 1%
- Konsentrasi emulsi, K1 = 0 %; K2 = 3%; K3 = 6%; K4 = 9 %
Dari tabel 3 dapat dilihat bahwa pada taraf 1% perlakuan konsentrasi emulsi
lilin memberikan pengaruh berbeda sangat nyata antara K1 dengan K2, K3, K4; K2
dengan K3, K4; dan K3 dengan K4.
Pengaruh konsentrasi emulsi lilin terhadap kadar vitamin C secara jelas
dapat dilihat pada gambar 1. Dimana kadar vitamin C tertinggi diperoleh pada
perlakuan K4 (37,21 mg/100g) dan kadar vitamin C terendah diperoleh pada perlakuan
K1 (28,73 mg/100g).
Gambar 1. Pengaruh Konsentrasi Emulsi Lilin Terhadap Kadar Vitamin C
Semakin tinggi konsentrasi emulsi lilin pada permukaan buah maka semakin
besar kemampuan emulsi lilin untuk mencegah masuknya oksigen ke dalam buah,
Jarak LSR Perlakuan Rataan Notasi Huruf
0,05 0,01 0,05 0,01
- - - K1 28,73 a A
2 0,1536 0,2549 K2 32,07 b B
3 0,1590 0,2446 K3 34,45 c C
4 0,1616 0,2509 K4 37,21 d D
0 10 20 30 40
0 3 6 9
Konsentrasi Emulsi Lilin (%)
[image:40.595.111.471.489.649.2]akibatnya oksigen dalam buah akan berkurang sehingga vitamin C yang teroksidasi
pun sedikit.
Proses oksidasi dapat menyebabkan berkurangnya asam askorbat, karena
asam askorbat sangat peka terhadap oksidasi terutama oleh karena adanya enzim
asam askorbat oksidase yang terdapat dalam jaringan tanaman (Apandi, 1984).
Asam askorbat sangat mudah teroksidasi menjadi L-dehidroaskorbat yang masih
mempunyai keaktifan sebagai vitamin C. Asam L-dehidroaskorbat secara kimia
sangat labil dan dapat mengalami perubahan lebih lanjut menjadi asam
L-diketogulat yang tidak memiliki keaktifan vitamin C lagi (Winarno dan Aman,
1981).
Lapisan lilin dengan kepekatan yang cukup dapat diberikan untuk
menghindarkan oksidasi pada buah (Hadiwiyoto dan Soehardi, 1981).
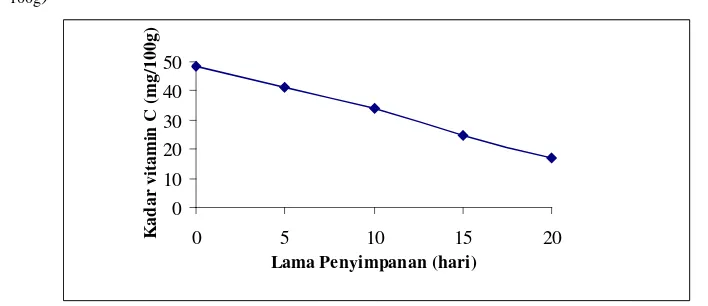
3.1.2 Pengaruh Lama Penyimpanan Terhadap Kadar Vitamin C
Hasil analisis pengaruh lama penyimpanan terhadap kadar vitamin C dapat
dilihat dari analisa sidik ragam pada lampiran 3, bahwa lama penyimpanan
memberikan pengaruh yang berbeda sangat nyata pada taraf 1% terhadap kadar
vitamin C yang dihasilkan. Pengujian lebih lanjut dengan Least Significant Ranges
(LSR) menunjukkan tingkat perbedaan pengaruh lama penyimpanan pada setiap
taraf yang diberi tanda notasi huruf terhadap kadar vitamin C seperti yang tertera
Tabel 4. Pengujian Least Significant Ranges (LSR) Pengaruh Lama Penyimpanan Terhadap Kadar Vitamin C
Keterangan tabel 4: - Notasi huruf yang berbeda menunjukkan beda nyata pada
taraf 5% dan beda sangat nyata pada taraf 1%
- Lama Penyimpanan, L1 = 0 hari; L2 = 5 hari; L3 = 10 hari; L4 = 15 hari; L5 = 20 hari
Dari tabel 4 dapat dilihat bahwa pada taraf 1% perlakuan lama penyimpanan
memberikan pengaruh berbeda sangat nyata antara L1 dengan L2, L3, L4; L2 dengan
L3, L4; dan L3 dengan L4.
Pengaruh lama penyimpanan terhadap kadar vitamin C secara jelas dapat
dilihat pada gambar 2. Dimana kadar vitamin C tertinggi diperoleh pada perlakuan
L1 (48,49 mg/100g) dan kadar vitamin C terendah diperoleh pada perlakuan L5 (16,91
mg /100g).
Gambar 2. Pengaruh Lama Penyimpanan Terhadap Kadar Vitamin C
Semakin lama waktu penyimpanan maka proses oksidasi yang terjadi pada
buah semakin meningkat. Asam askorbat sangat mudah teroksidasi menjadi
L-Jarak LSR Perlakuan Rataan Notasi Huruf
0,05 0,01 0,05 0,01
- - - L1 48,49 a A
2 0,8228 1,1009 L2 41,13 b B
3 0,8658 1,1497 L3 34,22 c C
4 0,8916 1,1812 L4 24,79 d D
5 0,9117 1,2013 L5 16,91 e E
0 10 20 30 40 50
0 5 10 15 20
Lama Penyimpanan (hari)
[image:42.595.114.468.512.665.2]dehidroaskorbat yang masih mempunyai keaktifan sebagai vitamin C. Asam
L-dehidroaskorbat secara kimia sangat labil dan dapat mengalami perubahan lebih
lanjut menjadi asam L-diketogulat yang tidak memiliki keaktifan vitamin C lagi
(Winarno dan Aman, 1981). Reaksi kerusakan vitamin C selama penyimpanan
umumnya mengikuti reaksi orde I yaitu semakin lama waktu penyimpanan maka
semakin banyak jumlah vitamin C yang rusak (Andarwulan dan Koswara, 1992),
akibatnya kadar vitamin C dalam buah menjadi semakin kecil.
3.1.3 Pengaruh Kombinasi Konsentrasi Emulsi Lilin dan Lama Penyimpanan Terhadap Kadar Vitamin C
Hasil analisis Pengaruh kombinasi konsentrasi emulsi lilin dan lama
penyimpanan terhadap kadar vitamin C dapat dilihat dari analisa sidik ragam pada
lampiran 3, bahwa kombinasi emulsi lilin dan lama penyimpanan memberikan
pengaruh yang berbeda sangat nyata pada taraf 1% terhadap kadar vitamin C yang
dihasilkan. Pengujian lebih lanjut dengan Least Significant Ranges (LSR)
menunjukkan tingkat perbedaan pengaruh kombinasi emulsi lilin dan lama
penyimpanan pada setiap taraf yang diberi tanda notasi huruf terhadap kadar
vitamin C seperti yang tertera pada tabel 5.
Jarak LSR Perlakuan Rataan Notasi Huruf
0,05 0,01 0,05 0,01
- - - K1L1 48,52 a A
2 1,8402 2,4622 K1L2 38,27 bk B
3 1,9364 2,5712 K1L3 27,76 c C
4 1,9941 2,6417 K1L4 19,00 d D
5 2,0390 2,6866 K1L5 10,62 e E
6 2,0710 2,7187 K2L1 48,52 a A
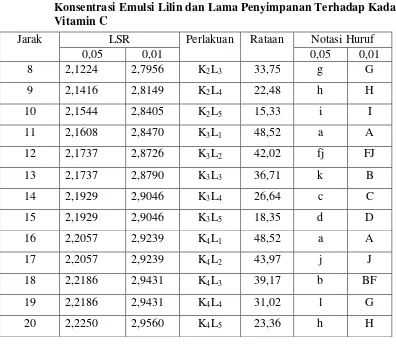
Tabel 5. Pengujian Least Significant Ranges (LSR) Pengaruh Kombinasi Konsentrasi Emulsi Lilin dan Lama Penyimpanan Terhadap Kadar Vitamin C
Keterangan : - Notasi huruf yang berbeda menunjukkan beda nyata pada taraf 5% dan beda sangat nyata pada taraf 1%
- Konsentrasi emulsi, K1 = 0 %; K2 = 3 %; K3 = 6%; K4 = 9 %
- Lama Penyimpanan, L1 = 0 hari; L2 = 5 hari; L3 = 10 hari;
L4 = 15 hari; L5 = 20 hari
Dari tabel 5 dapat dilihat perlakuan yang memberikan pengaruh berbeda
sangat nyata pada taraf 1% dan perlakuan yang memberikan pengaruh berbeda
nyata pada taraf 5%.
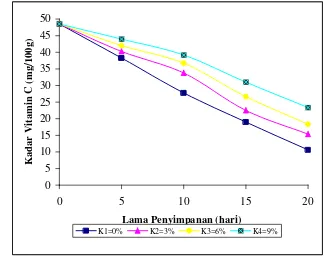
Pengaruh kombinasi konsentrasi emulsi lilin dan lama penyimpanan
terhadap kadar vitamin C secara jelas dapat dilihat pada gambar 3. Dimana kadar
vitamin C tertinggi diperoleh pada perlakuan dengan lama penyimpanan 0 hari (L1)
untuk semua variasi konsentrasi emulsi lilin yaitu sebesar 48,52 mg/100g dan kadar
Jarak LSR Perlakuan Rataan Notasi Huruf
0,05 0,01 0,05 0,01
8 2,1224 2,7956 K2L3 33,75 g G
9 2,1416 2,8149 K2L4 22,48 h H
10 2,1544 2,8405 K2L5 15,33 i I
11 2,1608 2,8470 K3L1 48,52 a A
12 2,1737 2,8726 K3L2 42,02 fj FJ
13 2,1737 2,8790 K3L3 36,71 k B
14 2,1929 2,9046 K3L4 26,64 c C
15 2,1929 2,9046 K3L5 18,35 d D
16 2,2057 2,9239 K4L1 48,52 a A
17 2,2057 2,9239 K4L2 43,97 j J
18 2,2186 2,9431 K4L3 39,17 b BF
19 2,2186 2,9431 K4L4 31,02 l G
0 5 10 15 20 25 30 35 40 45 50
0 5 10 15 20
Lama Penyimpanan (hari)
K ad ar V it am in C ( m g/ 100g)
K1=0% K2=3% K3=6% K4=9%
vitamin C terendah diperoleh pada perlakuan kombinasi K1L5 yaitu sebesar 10,62
[image:45.595.138.465.141.400.2]mg /100g.
Gambar 3. Pengaruh Kombinasi Konsentrasi Emulsi Lilin Dan Lama Penyimpanan Terhadap Kadar Vitamin C
Kadar vitamin C yang tinggi pada hari 0 tidak dapat memberikan gambaran
yang signifikan mengenai pengaruh kombinasi karena buah jeruk masih terdapat
dalam keadaan segar dan belum banyak mengalami proses oksidasi. Dengan
bertambahnya waktu penyimpanan dan menurunnya konsentrasi emulsi maka
vitamin C akan semakin menurun seperti yang dapat dilihat pada gambar 3 dimana
kadar vitamin C terendah terdapat pada perlakuan kombinasi K1L5.
3.2 Nilai Organoleptik Warna
Data hasil pengamatan nilai organoleptik warna dapat dilihat pada lampiran
4. Pengaruh masing-masing perlakuan terhadap nilai organoleptik warna yang
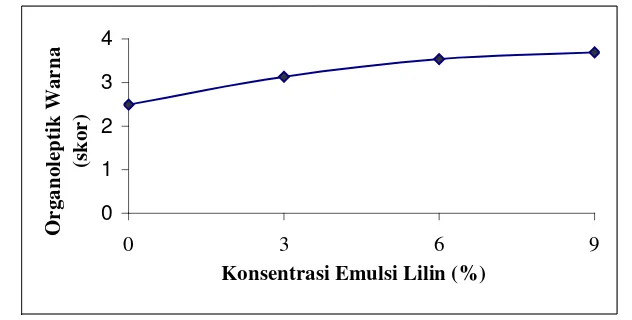
3.2.1 Pengaruh Konsentrasi Emulsi Lilin Terhadap Nilai Organoleptik Warna
Hasil analisis pengaruh konsentrasi emulsi lilin terhadap nilai organoleptik
warna dapat dilihat dari analisa sidik ragam pada lampiran 5, bahwa konsentrasi
emulsi lilin memberikan pengaruh yang berbeda sangat nyata pada taraf 1%
terhadap nilai organoleptik warna yang dihasilkan. Pengujian lebih lanjut dengan
Least Significant Ranges (LSR) menunjukkan tingkat perbedaan pengaruh
konsentrasi emulsi lilin pada setiap taraf yang diberi tanda notasi huruf terhadap
[image:46.595.104.501.384.515.2]nilai organoleptik warna seperti yang tertera pada tabel 6.
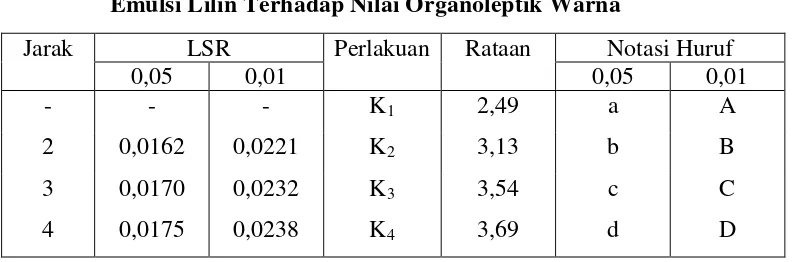
Tabel 6. Pengujian Least Significant Ranges (LSR) Pengaruh Konsentrasi Emulsi Lilin Terhadap Nilai Organoleptik Warna
Keterangan : - Notasi huruf yang berbeda menunjukkan beda nyata pada taraf 5% dan beda sangat nyata pada taraf 1%
- Konsentrasi emulsi, K1 = 0 %; K2 = 3 %; K3 = 6%; K4 = 9 %
Dari tabel 6 dapat dilihat bahwa pada taraf 1% perlakuan konsentrasi emulsi
lilin memberikan pengaruh berbeda sangat nyata antara K1 dengan K2, K3, K4; K2
dengan K3, K4; dan K3 dengan K4.
Pengaruh konsentrasi emulsi lilin terhadap nilai organoleptik warna secara
jelas dapat dilihat pada gambar 4. Dimana warna yang paling disukai diperoleh
Jarak LSR Perlakuan Rataan Notasi Huruf
0,05 0,01 0,05 0,01
- - - K1 2,49 a A
2 0,0162 0,0221 K2 3,13 b B
3 0,0170 0,0232 K3 3,54 c C
0 1 2 3 4
0 3 6 9
Konsentrasi Emulsi Lilin (%)
O r gan ol e p ti k War n a (sk or )
pada perlakuan K4 (skor 3,69) dan warna yang agak disukai diperoleh pada
[image:47.595.143.459.168.328.2]perlakuan K1 (skor 2,49).
Gambar 4. Pengaruh Konsentrasi Emulsi Lilin Terhadap Nilai Organoleptik Warna
Dengan semakin bertambahnya konsentrasi emulsi lilin maka proses
respirasi akan semakin lambat. Sehingga aktivitas metabolisme menurun, akibatnya
perombakan molekul klorofil terhambat. Seperti terdapat pada kebanyakan buah,
perubahan warna hijau ke kuning dalam buah jeruk ditandai dengan hilangnya
klorofil dan munculnya zat warna karotenoid (Pantastico, 1993).
Penampakan buah jeruk yang tidak baik seperti bercak-bercak coklat juga
diakibatkan tidak adanya perlindungan dari pelapisan lilin sehingga buah mudah
mengalami kerusakan terutama pada sel-sel minyak epidermal pada kulit jeruk.
Lapisan lilin dengan kepekatan yang cukup dapat diberikan untuk
menghindarkan oksidasi pada buah dan dapat memberikan perlindungan yang
diperlukan terhadap luka dan goresan kecil pada permukaan buah (Hadiwiyoto dan
3.2.2 Pengaruh Lama Penyimpanan Terhadap Nilai Organoleptik Warna
Dari hasil analisa sidik ragam pada lampiran 5, dapat dilihat bahwa lama
penyimpanan memberikan pengaruh tidak nyata terhadap nilai organoleptik warna
sehingga pengujian dengan Least Significant Ranges (LSR) tidak dilanjutkan.
Pengaruh lama penyimpanan terhadap nilai organoleptik warna secara jelas
dapat dilihat pada gambar 5. Dimana warna yang paling disukai diperoleh pada
perlakuan L1 (0 hari) dengan skor 4,19 dan warna yang agak disukai diperoleh pada
[image:48.595.141.445.307.458.2]perlakuan L4 dengan skor 2,23.
Gambar 5. Pengaruh Lama Penyimpanan Terhadap Nilai Organoleptik Warna
Semakin lama waktu penyimpanan maka semakin menurun nilai
organoleptik warna. Hal ini disebabkan karena semakin banyak klorofil yang terurai
dan sel-sel minyak epidermal pada kulit jeruk semakin banyak mengalami
kerusakan sehingga penampakan menjadi semakin tidak baik.
3.2.3 Pengaruh Kombinasi Konsentrasi Emulsi Lilin dan Lama Penyimpanan Terhadap Nilai Organoleptik Warna
Dari hasil analisa sidik ragam pada lampiran 5, dapat dilihat pengaruh
kombinasi konsentrasi emulsi lilin dan lama penyimpanan memberikan pengaruh
tidak nyata terhadap nilai organoleptik warna sehingga pengujian dengan Least
Significant Ranges (LSR) tidak dilanjutkan. 0 1 2 3 4 5
0 5 10 15 20
Lama Penyimpanan (hari)
0 1 2 3 4 5
0 5 10 15 20
Lama Penyimpanan (hari)
O
r
gan
ol
e
p
ti
k
War
n
a (
sk
or
)
K1 K2 K3 K4
Pengaruh kombinasi konsentrasi emulsi lilin dan lama penyimpanan
terhadap nilai organoleptik warna secara jelas dapat dilihat pada gambar 6. Dimana
warna yang paling disukai diperoleh pada perlakuan L1 (0 hari) untuk berbagai
variasi konsentrasi emulsi dengan skor 4,19 dan warna yang tidak disukai diperoleh
[image:49.595.146.454.223.497.2]pada perlakuan K1L5 dengan skor 1,00.
Gambar 6. Pengaruh Kombinasi Konsentrasi Emulsi Lilin Dan Lama Penyimpanan Terhadap Nilai Organoleptik Warna
Dari gambar 6 dapat dilihat dengan bertambahnya waktu penyimpanan dan
menurunnya konsentrasi emulsi maka nilai organoleptik warna akan semakin
menurun dimana nilai terendah terdapat pada perlakuan kombinasi K1L5. Hal ini
diakibatkan perombakan klorofil dan kerusakan sel-sel minyak epidermal
3.3 Nilai Organoleptik Aroma
Data hasil pengamatan nilai organoleptik aroma dapat dilihat pada lampiran
6. Pengaruh masing-masing perlakuan terhadap nilai organoleptik aroma yang
dihasilkan adalah sebagai berikut :
3.3.1 Pengaruh Konsentrasi Emulsi Lilin Terhadap Nilai Organoleptik Aroma
Hasil analisis pengaruh konsentrasi emulsi lilin terhadap nilai organoleptik
aroma dapat dilihat dari analisa sidik ragam pada lampiran 7, bahwa konsentrasi
emulsi lilin memberikan pengaruh yang berbeda sangat nyata pada taraf 1%
terhadap nilai organoleptik aroma yang dihasilkan. Pengujian lebih lanjut dengan
Least Significant Ranges (LSR) menunjukkan tingkat perbedaan pengaruh
konsentrasi emulsi lilin pada setiap taraf yang diberi tanda notasi huruf terhadap
[image:50.595.103.500.437.574.2]nilai organoleptik aroma seperti yang tertera pada tabel 7.
Tabel 7. Pengujian Least Significant Ranges (LSR) Pengaruh Konsentrasi Emulsi Lilin Terhadap Nilai Organoleptik Aroma
Keterangan : - Notasi huruf yang berbeda menunjukkan beda nyata pada taraf 5% dan beda sangat nyata pada taraf 1%
- Konsentrasi emulsi, K1 = 0 %; K2 = 3 %; K3 = 6%; K4 = 9 %
Dari tabel 7 dapat dilihat bahwa pada taraf 1% perlakuan konsentrasi emulsi
lilin memberikan pengaruh berbeda sangat nyata antara K1 dengan K2, K3, K4; K2
dengan K3, K4.
Jarak LSR Perlakuan Rataan Notasi Huruf
0,05 0,01 0,05 0,01
- - - K1 2,157 a A
2 0,0581 0,0792 K2 2,677 b B
3 0,0611 0,0831 K3 2,798 c C
Pengaruh konsentrasi emulsi lilin terhadap nilai organoleptik aroma secara
jelas dapat dilihat pada gambar 7. Dimana aroma yang paling disukai diperoleh
pada perlakuan K4 (skor 2,83) dan aroma yang agak disukai diperoleh pada
[image:51.595.169.451.232.378.2]perlakuan K1 (skor 2,16).
Gambar 7. Pengaruh Konsentrasi Emulsi Lilin Terhadap Nilai Organoleptik Aroma
Semakin tinggi konsentrasi emulsi lilin pada permukaan buah maka
penguapan minyak atsiri pada kulit jeruk manis dapat dihambat. Aroma yang khas
pada jeruk dihasilkan oleh produk atsiri berupa senyawa-senyawa terpenoid
(Pantastico, 1993).
3.3.2 Pengaruh Lama Penyimpanan Terhadap Nilai Organoleptik Aroma
Dari hasil analisa sidik ragam pada lampiran 7, dapat dilihat bahwa lama
penyimpanan memberikan pengaruh tidak nyata terhadap nilai organoleptik Aroma
sehingga pengujian dengan Least Significant Ranges (LSR) tidak dilanjutkan.
Pengaruh lama penyimpanan terhadap nilai organoleptik aroma secara jelas
dapat dilihat pada gambar 8. Dimana aroma yang paling disukai diperoleh pada
perlakuan L0 (skor 3,19) dan aroma yang agak disukai diperoleh pada perlakuan L5
(skor 1,89).
0 1 2 3
0 3 6 9
Konsentrasi Emulsi Lilin (%)
Gambar 8. Pengaruh Lama Penyimpanan Terhadap Nilai Organoleptik Aroma
Semakin lama waktu penyimpanan maka penguapan minyak atsiri pada kulit
jeruk manis semakin meningkat yang mengakibatkan aroma dari buah jeruk manis
semakin berkurang.
3.3.3 Pengaruh Kombinasi Konsentrasi Emulsi Lilin dan Lama Penyimpanan Terhadap Nilai Organoleptik Aroma
Dari hasil analisa sidik ragam pada lampiran 7, dapat dilihat pengaruh
kombinasi konsentrasi emulsi lilin dan lama penyimpanan memberikan pengaruh
tidak nyata terhadap nilai organoleptik aroma sehingga pengujian dengan Least
Significant Ranges (LSR) tidak dilanjutkan.
Pengaruh kombinasi konsentrasi emulsi lilin dan lama penyimpanan
terhadap nilai organoleptik aroma secara jelas dapat dilihat pada gambar 9. Dimana
aroma yang paling disukai diperoleh pada perlakuan L0 (skor 3,19) dan aroma yang
agak disukai diperoleh pada perlakuan L5 (skor 1,89). 0
1 2 3 4
0 5 10 15 20
Lama Penyimpanan (hari)
0 1 2 3 4
0 5 10 15 20
Lama Penyimpanan (hari)
O
rgn
ol
ept
ik A
rom
a
(s
kor
)
[image:53.595.158.459.169.433.2]K1 K2 K3 K4
Gambar 9. Pengaruh Kombinasi Konsentrasi Emulsi Lilin dan Lama Penyimpanan Terhadap Nilai Organoleptik Aroma
Dari gambar 9 dapat dilihat dengan bertambahnya waktu penyimpanan dan
menurunnya konsentrasi emulsi maka nilai organoleptik aroma akan semakin
menurun dimana nilai terendah terdapat pada perlakuan kombinasi K1L5. Hal ini
diakibatkan penguapan minyak atsiri pada kulit jeruk manis yang semakin
meningkat dan mengakibatkan aroma dari buah jeruk manis semakin berkurang
Aroma yang khas pada jeruk dihasilkan oleh produk atsiri berupa senyawa-senyawa
3.4 Nilai Organoleptik Rasa
Data hasil pengamatan nilai organoleptik rasa dapat dilihat pada lampiran 8.
Pengaruh masing-masing perlakuan terhadap nilai organoleptik rasa yang dihasilkan
adalah sebagai berikut :
3.4.1 Pengaruh Konsentrasi Emulsi Lilin Terhadap Nilai Organoleptik Rasa
Hasil analisis pengaruh konsentrasi emulsi lilin terhadap nilai organoleptik
rasa dapat dilihat dari analisa sidik ragam pada lampiran 9, bahwa konsentrasi
emulsi lilin memberikan pengaruh yang berbeda sangat nyata pada taraf 1%
terhadap nilai organoleptik rasa yang dihasilkan. Pengujian lebih lanjut dengan
Least Significant Ranges (LSR) menunjukkan tingkat perbedaan pengaruh
konsentrasi emulsi lilin pada setiap taraf yang diberi tanda notasi huruf terhadap
[image:54.595.105.504.451.585.2]nilai organoleptik rasa seperti yang tertera pada tabel 9.
Tabel 8. Pengujian Least Significant Ranges (LSR) Pengaruh Konsentrasi Emulsi Lilin Terhadap Nilai Organoleptik Rasa
Keterangan : - Notasi huruf yang berbeda menunjukkan beda nyata pada taraf 5% dan beda sangat nyata pada taraf 1%
- Konsentrasi emulsi, K1 = 0 %; K2 = 3 %; K3 = 6%; K4 = 9 %
Dari tabel 8 dapat dilihat bahwa pada taraf 1% perlakuan konsentrasi emulsi
lilin memberikan pengaruh berbeda sangat nyata antara K1 dengan K2, K3, K4; K2
dengan K4; dan K3 dengan K4.
Jarak LSR Perlakuan Rataan Notasi Huruf
0,05 0,01 0,05 0,01
- - - K1 3,14 a A
2 0,0158 0,0289 K2 3,25 b B
3 0,0158 0,0298 K3 3,28 c B
0 1 2 3 4
0 3 6 9
Konsentrasi Emulsi lilin (%)
O
rg
an
o
lep
ti
k
R
asa
(sko
r)
Pengaruh konsentrasi emulsi lilin terhadap nilai organoleptik rasa secara
jelas dapat dilihat pada gambar 10. Dimana rasa yang paling disukai diperoleh pada
perlakuan K3 (skor 3,28) dan rasa yang agak disukai diperoleh pada perlakuan K4
[image:55.595.108.455.217.400.2](skor 2,79).
Gambar 10. Pengaruh Konsentrasi Emulsi Lilin Terhadap Nilai Organoleptik Rasa
Semakin tinggi konsentrasi emulsi lilin pada permukaan buah maka semakin
besar kemampuan emulsi lilin untuk mencegah serangan patogen-patogen
pembusuk (Zuhairini, 1996). Namun konsentrasi emulsi lilin yang terlalu besar
dapat menimbulkan rasa buah yang tidak normal. Hal ini disebabkan karena adanya
penyerapan material lilin pada kulit jeruk sehingga menganggu rasa buah jeruk.
3.4.1 Pengaruh Lama Penyimpanan Terhadap Nilai Organoleptik Rasa
Hasil analisis pengaruh lama penyimpanan terhadap nilai organoleptik rasa
dapat dilihat dari analisa sidik ragam pada lampiran 9, bahwa lama penyimpanan
memberikan pengaruh yang berbeda sangat nyata pada taraf 1% terhadap nilai
organoleptik rasa yang dihasilkan. Pengujian lebih lanjut dengan Least Significant
0 1 2 3 4 5
0 5 10 15 20
Lama Penyimpanan (hari)
O r gan ol e p ti k R as a (s k o r )
yang diberi tanda notasi huruf terhadap nilai organoleptik rasa seperti yang tertera
[image:56.595.103.507.175.314.2]pada tabel 9.
Tabel 9. Pengujian Least Significant Ranges (LSR) Pengaruh Lama Penyimpanan Terhadap Nilai Organoleptik Rasa
Keterangan tabel 4: - Notasi huruf yang berbeda menunjukkan beda nyata pada
taraf 5% dan beda sangat nyata pada taraf 1%
- Lama Penyimpanan, L1 = 0 hari; L2 = 5 hari; L3 = 10 hari; L4 = 15 hari; L5 = 20 hari
Dari tabel 9 dapat dilihat bahwa pada taraf 1% perlakuan konsentrasi emulsi
lilin memberikan pengaruh berbeda sangat nyata antara K1 dengan K2, K3, K4; K2
dengan K3, K4; dan K3 dengan K4.
Pengaruh lama penyimpanan terhadap nilai organoleptik rasa secara jelas
dapat dilihat pada gambar 11. Dimana rasa yang paling disukai diperoleh