BAB I PENDAHULUAN A. Latar Belakang
Asam asetilsalisilat (asetosal) adalah obat yang mempunyai aktivitas farmakologik sebagai anti-inflamasi, analgesik dan anti-piretik. Asetosal disintesis pertama kali oleh Dr Felix Hoffmann tahun 1897 sudah dalam bentuk stabil dan murni di laboratorium Farbentabrik Freidrich Bayer di kota Elberfeld, Jerman. Dan akhirnya asetosal diproduksi secara massal oleh Bayer yang terkenal dengan brandname-nya adalah aspirin hingga hari ini. Nama tersebut diperoleh dari singkatan “a” untuk asetil dan “spir”untuk nama famili tanamanSpireayang mengandung senyawa turunan asam salisilat (Anonim, 2008; Clarke, 2005; Matiaset al., 2004).
Dewasa ini, selain pada awalnya asetosal berkhasiat sebagai anti-piretik dan analgesik yang tidak perlu diragukan lagi, ternyata juga berkhasiat anti-inflamasi pada dosis yang dinaikkan. Bukti terakhir menyatakan bahwa asetosal juga dapat digunakan sebagai anti-platelet untuk mengobati penyakit jantung dan gangguan sistem pembuluh darah (Anonim 2007; Matiaset al., 2004; Mousa, 2004; Rainsford, 2004)
Konsumsi asetosal selalu meningkat bahkan tahun 1997 di Amerika diperkirakan mencapai 20 ribu ton setahun. Di Indonesia obat bermerek yang mengandung asam asetilsalisilat dalam bentuk sediaan tablet saja telah mencapai lebih dari 30 nama, belum lagi bentuk sediaan lainnya, dan ditambah lagi sediaan generik yang banyak beredar di pasaran. Jika dihitung, jumlah obat yang mengandung asetosal yang beredar di masyarakat sudah demikian banyaknya (hingga saat ini penulis belum menemukan data yang valid) dan hal ini memerlukan pengawasan mutu yang tidak mudah untuk dilakukan (Anonim, 2007; Matiaset al., 2004).
metabolit asetosal dalam serum darah untuk mengatur dosis terapi (Matias et al., 2004, Rainsford, 2004).
Metode penetapan kadar asetosal telah banyak dikembangkan, diantaranya titrasi asam basa, spektrofotometri sinar ultraviolet dan tampak yang memanfaatkan reaksi Trinder yang didasari atas reaksi hidrolisis asetosal yang tahap berikutnya dalam prosedurnya tersebut akan menghasilkan senyawa yang berwarna ungu-biru kuat yang terbentuk antara asam salisilat dan besi(III). Beberapa penelitian juga telah mengembangkan metode otomatisasi metode spektrofotometri sinar tampak dengan menggunakan metode flow injection analysis pada tahap hidrolisisnya (Matias et al., 2004; Rainsford, 2004).
Metode spektrofluorometri, inframerah, kromatografi utamanya HPLC dan GC, dan Spektrofotometri Serapan Atom pun juga telah dikembangkan dan dideskripsikan secara detail untuk menetapkan kadar asetosal dan metabolitnya, asam salisilat. Yang mungkin terbaru adalah metode immunoassay dan spektrofotometri NMR. Beberapa metode tersebut telah jarang digunakan, hal ini dimungkinkan karena tingkat kesulitan dalam pengerjaannya dan prosedur preparasi sampel yang terlalu melelahkan, beberapa metode diantaranya membutuhkan peralatan yang mahal dan tak jarang memerlukan prosedur ekstraksi (Matiaset al., 2004; Rainsford, 2004).
Produk sediaan obat yang mengandung asetosal tidak terbilang lagi banyaknya yang beredar di pasaran Indonesia, yang seharusnya dalam kualitas prima hingga sampai di tangan konsumen dan siap dikonsumsi. Untuk menjaga kualitas tersebut dengan melihat jumlah sampel yang sangat besar, diperlukan pengembangan suatu metode penetapan kadar yang cepat, murah dan sederhana tanpa menggunakan alat yang rumit dan dapat memberikan hasil yang diinginkan. Namun sebagai langkah pendahuluan penulis menggunakan bantuan TLC Scanner dalam menganalisis bercak yang dihasilkan, Dalam hal ini, prosedur uji bercak dapat menjadi alternatif yang menjanjikan (Matiaset al., 2004).
ditetapkan kadarnya menggunakan metode refleksi sinar kembali berdasar pada reaksi pembentukan warna ungu-biru mantap antara asam salisilat dan besi(III) (Matiaset al., 2004).
B. Perumusan Masalah
Berdasarkan latar belakang yang telah diuraikan maka dapat dirumuskan permasalahan yaitu: apakah metode penetapan kadar asam asetilsalisilat dalam sediaan obat memanfaatkan sinar reflektan terukur dari bercak yang dihasilkan dapat memenuhi validitas suatu metode analisis?
C. Tujuan Penelitian
Penelitian ini bertujuan untuk mengetahui validitas metode penetapan kadar asam asetilsalisilat dalam sediaan obat memanfaatkan sinar reflektan terukur dari bercak yang dihasilkan.
D. Tinjauan Pustaka
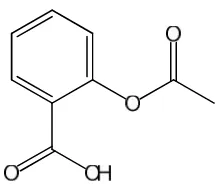
a. Asam Asetilsalisilat
Gambar 1. Struktur Kimia dari Asam Asetilsalisilat (Clarke, 2005)
Keberadaan asam asetilsalisilat dapat dideteksi secara kualitatif melalui tes warna setelah mengalami reaksi hidrolisis terlebih dahulu, antara lain dengan menggunakan pereaksi McNally akan memberikan warna merah (Clarke, 2005), dan dengan besi(III) akan memberikan warna ungu-biru mantap (Anonim, 1991; Matias et al., 2004). Asam asetilsalisilat mempunyai nilai pKa 3,5 (25oC) dan nilai logP (oktanol/dapar pH 7,4) sebesar -1,1, dengan nilai E1%1cmdalam larutan asam adalah 466 (230 nm), 68 (278 nm), sedangkan dalam larutan basa adalah 409 (231 nm), dan 190 (298 nm) (Clarke, 2005).
Kilas balik sejarah dari asam asetilsalisilat dapat ditelusuri dari berbagai pustaka baik dalam bentuk buku, jurnal atau pun artikelonline. Dimulai dari seorang ahli kimia Perancis, Charles Frederich von Gerhardt telah menggunakan reaksi asetilasi dan menghasilkan asam asetilsalisilat tahun 1853 dari reaksi antara natrium salisilat dengan asetil klorida, tetapi ditemukan oleh Kraut bahwa produk hasil tidak murni dan ditemukan pula reaksi hidrolisis alkalin dari asam asetilsalisilat menjadi asam asetat dan asam salisilat (Rainsford, 2004)
Akhirnya dalam pencariannya untuk anti-rematik yang efektif dan lebih baik tingkat toleransinya untuk ayahnya, Dr. Felix Hoffmann berhasil mensintesis asam asetilsalisilat, kandungan aktif dari Aspirin, yang murni dan stabil untuk pertama kalinya melalui reaksi asetilasi fenol (Anonim, 2008; Rainsford, 2004).
Asam asetilsalisilat dalam bentuk tak terionnya cukup dapat larut dalam lemak dengan nilai LogP antara oktanol dan air adalah 1,19, dimana asam salisilat lebih larut dalam lemak dengan nilai LogP sebesar 2,26 sehingga keduanya mudah terabsorpsi dalam lambung jika dalam bentuk terionnya. Hal ini dikarenakan adanya peningkatan nilai pH lambung yang memberikan kesempatan mukosa lambung menyerap bentuk tak terionnya asam asetilsalisilat. Kesulitan absorpsi dalam lambung menyebabkan segera seluruh asam asetilsalisilat ditransfer ke dalam usus halus dan dengan cepatnya asam asetilsalisilat akan terabsorpsi (Rainsford, 2004).
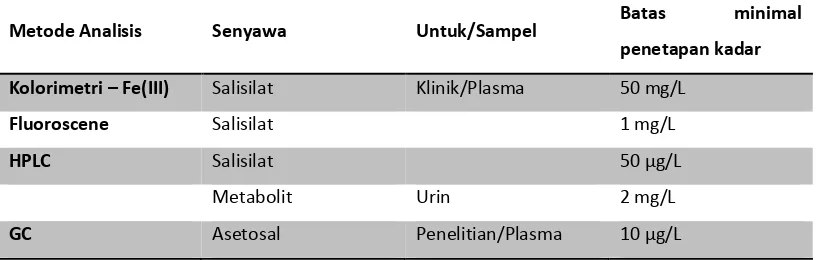
Beberapa metode penetapan kadar dari asam asetilsalisilat dan metabolitnya asam salisilat dapat dilihat padaTabel 1.
Tabel 1. Penetapan kadar asetosal dan asam salisilat untuk penelitian dan klinik (Rainsford, 2004)
Metode Analisis Senyawa Untuk/Sampel Batas minimal
penetapan kadar Kolorimetri – Fe(III) Salisilat Klinik/Plasma 50 mg/L
Fluoroscene Salisilat 1 mg/L
HPLC Salisilat 50 µg/L
Metabolit Urin 2 mg/L
GC Asetosal Penelitian/Plasma 10 µg/L
Asam asetilsalisilat menurut Farmakope Indonesia edisi IV (1995) ditetapkan kadarnya menggunakan metode HPLC dengan ketentuan: fase gerak yang digunakan adalah larutan 2 gram natrium 1-heptanasulfonat P dalam campuran 850 mL air dan 150 mL asetonitril P yang ditambahkan asam asetat glacial P hingga pH 3,4; dan fase diam adalah kolom dengan bahan pengisi L1 yang berukuran 4,0 mm x 30 cm dengan laju alir 2 mL per menit dan panjang gelombang detector UV pada 280 nm. Larutan baku disiapkan dengan cara timbang seksama sejumlah asam asetilsalisilat BPFI dan larutkan dalam larutan pengencer (asetonitril P : asam format P dengan perbandingan 99 : 1) hingga kadar lebih kurang 0,5 mg/mL. Larutan uji disiapkan dengan cara timbang dan serbukkan tidak kurang dari 20 tablet. Timbang seksama sejumlah serbuk setara dengan lebih kurang 100 mg asam asetilsalisilat, masukkan ke dalam wadah yang sesuai. Tambahkan 20,0 mL larutan pengencer dan lebih kurang 10 manik kaca, kocok kuat-kuat selama lebih kurang 10 menit dan sentrifuse (larutan persediaan). Ukur seksama sejumlah volume larutan persediaan, encerkan secara kuantitatif dalam 9 volume larutan pengencer. Prosedur pengerjaannya adalah suntikkan secara terpisah masing-masing lebih kurang 1,0 µL larutan baku dan larutan uji ke dalam alat dan ukur respon puncak utama. Hitung jumlah dalam mg, asam asetilsalisilat, C9H8O4, dalam bagian tablet yang digunakan dengan rumus:
200 C x (ru/rs)
Penetapan kadar asam asetilsalisilat menggunakan metode kolorimetri dengan asumsi semua asam asetilsalisilat telah terhidrolisis sempurna sehingga prosedur yang digunakan sama dengan prosedur untuk penetapan kadar asam salisilat secara kolorimetri mengikuti langkah berikut:
Pembuatan kurva baku, sejumlah 200 mg asam salisilat baku dipanaskan selama 1 jam pada suhu 100oC, kemudian ditimbang dan dilarutkan dalam 15 mL etanol dan diencerkan dengan air hingga 1 L. Secara kuantitatif diambil sejumlah 5, 10, 15, 20, dan 25 mL masing-masing dimasukkan dalam labu takar 100 mL, kemudian ditambahkan besi(III) nitrat 1% dalam larutan asam nitrat 1%. Larutan kemudian diencerkan hingga tanda dengan air dan pH larutan dijaga antara 5-6. Larutan ini masing-masing diukur dengan spektrometri pada 525 nm. Hasil yang diperoleh dibuat dalam grafik kurva baku antara konsentrasi larutan baku dan absorbansi yang diperoleh (Higuchi dan Hanssen, 1961).
Prosedur penetapan kadar, sampel yang telah diserbukkan pada metode HPLC sebelumnya ditimbang sejumlah tertentu setara dengan 200 mg asam salisilat kemudian dihidrolisis dengan 15 mL NaOH 0,5M menggunakan pemanasan perlahan sehingga reaksi sempurna dan pH larutan dibuat hingga 5 – 6 dengan asam nitrat 0,1M. Larutan ini diencerkan dengan air hingga 1 L dan jika perlu dilakukan penyaringan dimana 50 mL filtrat yang pertama dibuang. Secara kuantitatif ambil sejumlah 25 mL dan dimasukkan dalam labu takar 100 mL, tambahkan 5 mL besi(III) nitrat 1%. Larutan kemudian diencerkan dengan air hingga tanda dan diukur dengan spectrometer pada 525 nm, kemudian hasil yang diperoleh diplotkan pada kurva baku sehingga diperoleh kadar yang sebenarnya dari sampel (modifikasi dari Higuchi dan Hanssen, 1961).
b. Analisis Uji Bercak
dapat digunakan untuk penetapan kadar secara kuantitatif memanfaatkan sinar reflektan dan sinar transmisi terhadap bercak yang dihasilkan pada uji bercak (Winslow dan Liebhafsky, 1949).
Kemudian pengembangan metode analisis kuantitatif menggunakan uji bercak terus dilakukan, tahun 1954, McCready dan McComb melakukan uji kuantitatif gula pada kertas kromatogram memanfaatkan bercak yang dihasilkan yang kemudian diukur sinar yang terrefleksikan kembali sehingga dikenal sebagai metode sinar reflektan pada bercak (McCready dan McComb, 1954). Disusul oleh Feigl (1955) yang melakukan uji bercak secara kuantitatif terhadap beberapa senyawa organik diantaranya adalah fenol, turunan asil-amina aromatic, ariluretane, monoarilurea, dan penggunaan asam sulfonat dan iodine sebagai pereaksi uji bercak (Feigl, 1955).
DAFTAR PUSTAKA
Anonim, 1991,Basic Tests for Pharmaceutical Dosage Forms, WHO, Geneva.
Anonim, 1995,Farmakope Indonesia, Edisi IV, Depkes RI, Jakarta.
Anonim, 2007,Informasi Spesialite Obat Indonesia, Volume 42, Penerbit ISFI, Jakarta.
Anonim, 2008, World of Aspirin, http://www.aspirin.com/, diakses tanggal 09 Maret 2008
Clarke, 2005,Clarke’s Analysis of Drugs and Poisons, Pharmaceutical Press.
Edberg, S.C., Gam, K., Bottenbley, C.J., dan Singer, J.M., 1976, Rapid Spot Test for Determinations of Esculin Hydrolysis, J. Clin. Microbiol., 4: 180-184.
Ermer, J. and Miller, J.H.M, 2005, Method Validation in Pharmaceutical Analysis, Wiley-Interscience
Favero, J.A., dan Tubino, M., 2003, Semi-Quantitative “Spot-test” of Cyanide,Analytical Science,19: 1139-1143.
Feigl, F, 1955, Organic Spot Test Analysis, Analytical Chem., 27 (8): 1315-1318.
Ferreira, L.F.V., Machado, I.F., Oliveira, A.S., Da Silva, J.P., Krawczyk, A., dan Sikorski, M., 2007, Surface Photochemistry: Diffuse Reflectance studies of Thioketones included intop-tert-butylcalix[6 and 8]arenes,J. Molecular Structure,827: 11-19.
Ghauch, A., Turnar, C., Fachinger, C., Rima, J., Charef, A., Suptil, J., dan Bouyer, M.M., 2000, Use of Diffuse Reflectance Spectrometry in Spot Test Reactions for Quantitative Determinations of Cations in Water, Chemosphere, 40: 1327-1333.
Gotardo, M.A., Gigante, A.C., dan Pezza, H.R., 2004, Determination of Furesemide in Pharmaceutical Formulations by Diffuse Reflectance Spectroscopy, Talanta, 64: 361-365.
Götzl, A., dan Riepe, W., 2001, Mercury Determination – SPME and Colorimetric Spot Test, Talanta, 54: 821-827.
Higuchi, T. dan Hanssen, E.B., 1961,Pharmaceutical Analysis, Interscience Publishers.
Kemper, T., dan Sommer, S., 2002, Estimate of Heavy Metal Contamination in Soils after a mining Accident using Reflectance Spectrsocopy, Environ. Sci. Technol., 36: 2742-2747.
Matias, F.A.A., Vila, M.M.D.C., dan Tubino, M., 2004, Quantitative Reflectance Spot Test for the Determination of Acetylsalicylic Acid in Pharmaceutical Preparations, J. Braz. Chem. Soc.,15(2): 327-330.
McCready, R.M., dan McComb, E.A., 1954, Quantitative Determination of Sugar on Paper Chromatograms by a Reflectance Method, Analytical Chem., 26 (1): 1645-1647.
Mousa, S.A., 2004, Anticoagulants, Antiplatelets, and Thrombolytics, Methods in Moleculer Medicine, Humana Press.
Pezza, L., Tubino, M., Melios, C.B., dan Pezza, H.R., 2000, Rapid Spot Test Analysis for Detection of Dipyrone in Pharmaceutical Preparations, Analytical Sciences, 16: 313-315.
Rainsford, K.D., 2004,Aspirin and Related Drugs, CRC Press.
Ribeiro, P.R.S., Pezza, L., dan Pezza, H.R., 2006, determination of Methyldopa in Pharmaceutical Formulations by Combined Spot Test-Diffuse Reflectance Spectroscopy,J. Braz. Chem. Soc.,17(4).
Tubino, M., dan de Souza, R.L., 2006, Determination of Diclofenac in Pharmaceutical Ppreparations by Diffuse Reflectance Photometry,Talanta,68: 776-780.
Tubino, M., de Souza, R.L., dan Hoehr, N.F., 2004, Rapid Quantitative Turbidimetric Spot Test Analysis of Potassium in Blood Serum,J. Braz. Chem. Soc.,15(5): 635-639.
Umberger, C.J., dan Fiorese, F.F., 1963, Detection and Quantitative Determination of Glycine with Pyridine and p-Nitrobenzoyl Chloride, Clin. Chem, 9 (1): 79-90.
Winslow, E.H. dan Liebhafsky, H.A., 1949, Spectrometric Study of Spot Tests, Analytical Chem., 21 (11): 1338-1342.
Xie, L. dan Lu, J., 2001, In Situ UV-Vis Diffuse Reflectance Studies on Lithium-intercalated Carbons,J. Electroanalytical Chem.,497: 159-162.
Zaporozhets, O.A., dan Tsyukalo, L.Y., 2002, Xylenol Orange Adsorbed on Silica Surface as a Solid Phase Reagent for Lead Determination using Diffuse Reflectance Spectroscopy,Talanta,58: 861-868.
LAPORAN HASIL
PENELITIAN DOSEN MUDA
PENETAPAN KADAR ASAM ASETILSALISILAT DALAM SEDIAAN OBAT
MEMANFAATKAN SINAR REFLEKTAN TERUKUR
DARI BERCAK YANG DIHASILKAN DENGAN TLC
SCANNER
Oleh
Andi Suhendi, S.Farm., Apt. Broto Santoso, S.F., Apt.
FAKULTAS FARMASI
RINGKASAN
PENELITIAN DOSEN MUDA
PENETAPAN KADAR ASAM ASETILSALISILAT DALAM SEDIAAN OBAT
MEMANFAATKAN SINAR REFLEKTAN TERUKUR
DARI BERCAK YANG DIHASILKAN DENGAN TLC
SCANNER
Oleh
Andi Suhendi, S.Farm., Apt.
Broto Santoso, S.F., Apt.
FAKULTAS FARMASI
PENETAPAN KADAR ASAM ASETILSALISILAT DALAM SEDIAAN OBAT
MEMANFAATKAN SINAR REFLEKTAN TERUKUR DARI BERCAK YANG
DIHASILKAN DENGAN TLC
SCANNER
Andi Suhendi dan Broto Santoso
Asam asetilsalisilat (asetosal) adalah obat yang mempunyai aktivitas
farmakologik sebagai anti-inflamasi, analgesik dan anti-piretik. Asetosal juga dapat
digunakan sebagai anti-platelet untuk mengobati penyakit jantung dan gangguan sistem
pembuluh darah (Anonim, 2008; Anonim 2007; Clarke, 2005; Matiaset al., 2004; Mousa,
2004; Rainsford, 2004).
Konsumsi asetosal selalu meningkat bahkan tahun 1997 di Amerika diperkirakan
mencapai 20 ribu ton setahun. Di Indonesia obat bermerek yang mengandung asam
asetilsalisilat dalam bentuk sediaan tablet saja telah mencapai lebih dari 30 nama,
belum lagi bentuk sediaan lainnya, dan ditambah lagi sediaan generik yang banyak
beredar di pasaran. Jika dihitung, jumlah obat yang mengandung asetosal yang beredar
di masyarakat sudah demikian banyaknya. Hal ini memerlukan pengawasan mutu yang
tidak mudah untuk dilakukan (Anonim, 2007; Matiaset al., 2004).
Penetapan kadar asetosal dalam sediaan obat sangatlah penting untuk uji
kualitas produk sebelum, selama proses produksi dan/atau setelah menjadi produk
akhir, serta selama produk tersebut berada di pasaran sebelum digunakan oleh
konsumen (Matiaset al., 2004, Rainsford, 2004).
Metode penetapan kadar asetosal telah banyak dikembangkan, diantaranya
titrasi asam basa, spektrofotometri sinar ultraviolet dan tampak, otomatisasi metode
spektrofotometri sinar tampak dengan menggunakan metode flow injection analysis
pada tahap hidrolisisnya, metode spektrofluorometri, inframerah, kromatografi
utamanya HPLC dan GC, dan Spektrofotometri Serapan Atom pun juga telah
dikembangkan dan dideskripsikan secara detail untuk menetapkan kadar asetosal dan
metabolitnya, asam salisilat; dan yang terbaru metode immunoassay dan
spektrofotometri NMR (Matiaset al., 2004; Rainsford, 2004).
Produk sediaan obat yang mengandung asetosal tidak terbilang lagi banyaknya
yang beredar di pasaran Indonesia, yang diharuskan dalam kualitas prima hingga sampai
di tangan konsumen dan siap dikonsumsi. Untuk menjaga kualitas tersebut dengan
penetapan kadar yang cepat, murah, portabel, dan sederhana tanpa menggunakan alat
yang rumit dan dapat memberikan hasil yang diinginkan. Langkah pendahuluan dalam
pencarian metode alternatif dengan menggunakan bantuan TLC Scanner dalam
menganalisis bercak yang dihasilkan sehingga prosedur uji bercak dapat menjadi
alternatif yang menjanjikan (Matiaset al., 2004).
Uji kualitatif penampakan bercak didasarkan atas reaksi perubahan warna
melalui reaksi kimia antara analit dan pereaksi. Perubahan warna ini terjadi secara
proporsional terhadap konsentrasi dari analit sehingga metode penetapan kadar
berdasar reaksi bercak dapat diajukan untuk dikembangkan. Dalam penelitian ini
nantinya, beberapa konsentrasi asetosal dari beberapa sediaan obat bermerek
ditetapkan kadarnya menggunakan metode refleksi sinar kembali berdasar pada reaksi
pembentukan warna ungu-biru mantap antara asam salisilat dan besi(III) (Matiaset al.,
2004).
Penelitian ini bertujuan untuk mengetahui validitas metode penetapan kadar
asam asetilsalisilat dalam sediaan obat memanfaatkan sinar reflektan terukur dari
bercak yang dihasilkan. Metode yang digunakan adalah validasi beberapa parameter
yang dipersyaratkan terhadap metode pengukuran konsentrasi yang diperoleh dari hasil
konversi jumlah sinar reflektan yang didapat dengan kurva baku eksternal asam salisilat.
Asetosal tidak dapat ditetapkan kadarnya dengan mengukur bercak yang
dihasilkan sebelum dilakukan hidrolisis terlebih dahulu karena asetosal tidak dapat
membentuk kompleks dengan Fe(NO3)3. Beberapa buku seperti farmakope Indonesia
dan Higuchi (1976) menyebutkan bahwa hidrolisis dilakukan dalam suasana basa
(NaOH), namun setelah dilakukan optimasi hasil optimum diperoleh dengan basa yang
digunakan KOH. Kondisi optimum ini kemudian dipakai untuk membuat kurva standar
dan dari dihasilkan persamaan regresi liniernya
y=7495x + 830 (r=0,996). Parameter-parameter
validasi metode analisis: 1) akurasi; parameter
akurasi membuktikan kedekatan hasil
pemeriksaan dengan nilai yang sebenarnya. Ada
dua cara untuk menetapkan parameter akurasi,
yaitu metode simulasi dan penambahan baku.Tabel 1 menyajikan hasil dari penetapan
memanfaatkan sinar reflektan dari TLC Scanner pada spot yang dibuat dari larutan
sampel.
DariTabel 1dapat ditarik kesimpulan bahwa kesemua hasil perolehan kembali
belum memenuhi syarat (98-102% dengan relative standard deviation (RSD) <1%)
namun untuk reference source yang kurang strict (AOAC, 1993), dinyatakan bahwa
berdasarkan kadar yang semakin kecil maka nilai deviasi diperoleh akan semakin besar
dan dalam hal ini batasan keterimaannya juga semakin besar, 2) Presisi antara; hasil
perhitungan presisi berdasarkan perbedaan hari penentuan kadar diperoleh nilai RSD
adalah 0,270% berarti dapat dinyatakan bahwa adanya perbedaan hari pelaksanaan
metode penetapan kadar asam asetil salisilat tidak mempengaruhi hasil kadar yang
diperoleh. Konsentrasi analit asam asetil salisilat menggunakan model sinar reflektan
yang ditemukan dengan beda hari pelaksanaan (presisi antara satu parameter, yaitu
hari) tidak berbeda atau bisa dikatakan masih memenuhi reproducible factor, 3)
Ripitabilitas; nilai RSD (standar deviasi relatif) yang diperoleh dalam penelitian ini adalah
2,079%; sehingga dalam hal ini masih memenuhi syarat keberterimaan yang
diperbolehkan yaitu dalam batas antara 2,10% - 2,90% (Ermer dan Miller, 2005). Metode
ini berarti masih memenuhi syarat dan dapat menjadi acuan untuk model penetapan
kadar obat yang mengandung asam asetil salisilat, 4) Linieritas; nilai regresi linear yang
diperoleh adalah 0,938 dan ini belum memenuhi syarat keberterimaan yang
diperbolehkan (nilai r harus > 0,98). Walaupun nilai r tidak memenuhi persyaratan,trend
data yang diperoleh menunjukan sifat linearitas yaitu konsentrasi semakin besar respon
(luas area) yang diperoleh juga meningkat. Hal ini dapat disebabkan karena waktu
pemipetan, posisi mikropipet tidak selalu mendekati tegak lurus sehingga hasil spot yang
diperoleh kurang lebih tidak sama satu dengan lainnya, dan 5) LOQ; Limit of
Quantification (LOQ) perlu dilakukan dan dihitung dengan cara signal to noise atau
dengan kurva standar eksternal atau internal untuk metode penetapan kadar yang baru.
Nilai LOQ yang didapatkan adalah 0,647%; berarti kadar minimum yang bisa ditetapkan