UIN SYARIF HIDAYATULLAH JAKARTA
EFEK IRADIASI GAMMA TERHADAP
KEMAMPUAN KITOSAN DALAM MENURUNKAN
KADAR KOLESTEROL SECARA
IN VITRO
SKRIPSI
MELIA PUSPITASARI
1110102000065
FAKULTAS KEDOKTERAN DAN ILMU KESEHATAN
PROGRAM STUDI FARMASI
JAKARTA
ii
UIN SYARIF HIDAYATULLAH JAKARTA
EFEK IRADIASI GAMMA TERHADAP
KEMAMPUAN KITOSAN DALAM MENURUNKAN
KADAR KOLESTEROL SECARA
IN VITRO
SKRIPSI
Diajukan sebagai salah satu syarat memperoleh gelar sarjana Farmasi
MELIA PUSPITASARI
1110102000065
FAKULTAS KEDOKTERAN DAN ILMU KESEHATAN
PROGRAM STUDI FARMASI
JAKARTA
HALAMAN PERNYATAAN ORISINALITAS
Skripsi ini adalah hasil karya saya sendiri, dan semua sumber baik yang dikutip maupun dirujuk
telah saya nyatakan dengan benar.
Nama : Melia Puspitasari
NIM : 1110102000065
Tanda Tangan :
iv HALAMAN PERSETUJUAN PEMBIMBING
Nama : Melia Puspitasari
NIM : 1110102000065
Program Studi : Farmasi
Judul : Efek Iradiasi Gamma Terhadap Kemampuan Kitosan
Dalam Menurunkan Kadar Kolesterol Secara In Vitro
HALAMAN PENGESAHAN
Skripsi ini diajukan oleh :
Nama : Melia Puspitasari
NIM : 1110102000065
Program Studi : Farmasi
Judul Skripsi : Efek Iradiasi Gamma Terhadap Kemampuan Kitosan Dalam
Menurunkan Kadar Kolesterol Secara In Vitro
Telah berhasil dipertahankan di hadapan Dewan Penguji dan diterima sebagai bagian persyaratan yang diperlukan untuk memperoleh gelar Sarjana Farmasi pada Program Studi Farmasi Fakultas Kedokteran dan Ilmu Kesehatan Universitas Islam Negeri (UIN) Syarif Hidayatullah Jakarta
DEWAN PENGUJI
Ditetapkan di : Ciputat
vi UIN Syarif Hidayatullah Jakarta ABSTRAK
Nama : Melia Puspitasari
Program Studi : Farmasi
Judul : Efek Iradiasi Gamma Terhadap Kemampuan Kitosan Dalam Menurunkan Kadar Kolesterol Secara In Vitro
Kitosan merupakan biopolimer alami kedua terbanyak di alam setelah selulosa, salah satunya dihasilkan dari limbah kulit udang. Derajat deasetilasi dan berat molekul merupakan parameter utama yang mempengaruhi karakteristik kitosan. Penelitian sebelumnya menyebutkan bahwa kitosan memiliki aktivitas hipokolesterolemia secara in vitro. Mengacu pada penelitian tersebut, dilakukan uji skrining awal efek iradiasi gamma terhadap kemampuan kitosan dalam menurunkan kadar kolesterol secara in vitro. Tujuan dari penelitian ini adalah untuk mengetahui pengaruh iradiasi gamma terhadap derajat deasetilasi kitosan, berat molekul viskositas rata-rata (Mv) kitosan, serta aktivitas penurunan kadar kolesterol. Hasil penelitian menunjukkan bahwa derajat deasetilasi kitosan non iradiasi adalah 96,658% dan kitosan iradiasi adalah 94,073%. Radiasi juga menyebabkan penurunan berat molekul viskositas (Mv) kitosan yaitu semakin besar dosis radiasi menghasilkan kitosan dengan berat molekul viskositas yang semakin rendah. Pada penelitian ini dilakukan uji aktivitas penurunan kadar kolesterol kitosan non iradiasi dan kitosan iradiasi dengan 3 dosis radiasi yang berbeda yaitu 50, 100, dan 150 kGy. Uji penurunan kadar kolesterol pada penelitian ini menggunakan metode Rudel-Morris dan Zak (FeCl3-H2SO4) secara in vitro. Serapan dari kolesterol yang tidak diikat dengan kitosan diukur dengan menggunakan spektrofotometer Uv-Vis. Hasil dari penelitian ini menunjukkan rata-rata persentase penurunan kadar kolesterol dari kitosan 0 kGy, 50 kGy, 100 kGy dan 150 kGy berturut-turut adalah 5,10%; 15,14%; 31,02%; and 42,62%. Berdasarkan kemampuan pengikatan kolesterol oleh kitosan, kitosan 150 kGy mempunyai aktivitas penurunan kadar kolesterol yang tertinggi. Selain itu, hasil uji ANOVA menunjukkan bahwa persentase penurunan kadar kolesterol dari kitosan 150 kGy berbeda secara bermakna dengan kitosan 0, 50, dan 100 kGy.
ABSTRACT
Name : Melia Puspitasari Program Study : Pharmacy
Tittle : The Effect of Gamma Irradiation on the Ability of Chitosan to Reduce Cholesterol Level In Vitro
Chitosan is the second largest natural biopolymer in nature after cellulose which is produced from shrimp shell waste. The degree of deacetylation and molecular weight of chitosan is the main parameters that affect the characteristics of chitosan. The previous study reported that the chitosan had in vitro hipokolesterolemia activity. The initial screening test of the effect of gamma irradiation on the activity of chitosan in lowering cholesterol levels in vitro has been conducted. The purpose of this research is to determine the effect of gamma irradiation on the degree of deacetylation of chitosan, viscosity average molecular weight (Mv) of chitosan, and cholesterol lowering activity. The results showed that the degree of deacetylation of non-irradiated chitosan is 96.658% and irradiated chitosan is 94.073%. Radiation also caused a decrease in the viscosity molecular weight (Mv) of chitosan which the greater doses of radiation produce the lower viscosity molecular weight chitosan. In this experiment the cholesterol lowering activity of unirradiated and irradiated chitosan in three irradiation doses 50, 100, and 150 kGy. Cholesterol lowering activity was tested in vitro using Rudel-Morris and Zak (FeCl3-H2SO4) method. Absorbance of cholesterol which is not bound to chitosan was measured using Uv-Vis spectrophotometer. The results of this study showed that the reduction average percentage in cholesterol levels of chitosan 0 kGy, 50 kGy, 100 kGy and 150 kGy respectively is 5,10%; 15,14%; 31,02%; and 42,62%. Based on the binding ability of cholesterol by chitosan, chitosan 150 kGy had the highest cholesterol-lowering activity. Moreover, the statistical analysis ANOVA showed that the percentage in cholesterol level of chitosan irradiated with 150 kGy has the significant differences with chitosan 0, 50, and 100 kGy.
viii UIN Syarif Hidayatullah Jakarta
KATA PENGANTAR
Alhamdulillahirabbil`alamiin, segala puji dan syukur penulis ucapkan
kehadirat Allah SWT yang telah melimpahkan rahmat, taufik dan hidayah-Nya
sehingga penulis dapat menyelesaikan penyusunan skripsi ini hingga selesai.
Shalawat serta salam penulis curahkan kepada junjungan kita Nabi Muhammad
SAW beserta keluarga, para sahabat serta kita sebagai umatnya. Penulisan skripsi
yang berjudul “Efek Iradiasi Gamma Terhadap Kemampuan Kitosan Dalam
Menurunkan Kadar Kolesterol Secara In Vitro” bertujuan untuk memenuhi
persyaratan guna memperoleh gelar Sarjana Farmasi pada Fakultas Kedokteran dan
Ilmu Kesehatan Universitas Islam Negeri Syarif Hidayatullah Jakarta.
Pada kesempatan ini penulis menyadari bahwa dalam penelitian dan
penyusunan skripsi ini tidak akan terwujud tanpa adanya bantuan, bimbingan, dan
dukungan dari berbagai pihak. Oleh karena itu penulis mengucapkan terimakasih
kepada:
1. Dr. Darmawan Darwis., Apt dan Yardi Ph.D, Apt sebagai dosen
pembimbing yang dengan sabar telah memberikan banyak masukan, ilmu,
bimbingan, waktu, tenaga, dan dukungan kepada penulis.
2. Prof. Dr. (hc). Dr. M.K. Tadjudin, Sp.And selaku Dekan Fakultas Kedokteran
dan Ilmu Kesehatan UIN Syarif Hidayatullah Jakarta.
3. Drs. Umar Mansur, M.Sc selaku Ketua Program Studi Farmasi Fakultas
Kedokteran dan Ilmu Kesehatan UIN Syarif Hidayatullah Jakarta.
4. Seluruh dosen di Program Studi Farmasi Fakultas Kedokteran dan Ilmu
Kesehatan Universitas Islam Negeri Syarif Hidayatullah Jakarta atas ilmu
pengetahuan yang telah diberikan kepada saya.
5. Kedua orang tua, ayahanda M. Soleh dan ibunda tercinta Ayati yang selalu
memberikan kasih sayang, semangat, dan doa yang tidak pernah putus dan
dukungan baik moril maupun materil.
6. Kakak-kakak dan keponakan tersayang Maryati, Ayanih, Hasanudin, Arif,
Haerudin Hidayat, Asep Syaiful, Lina, Ike, dan Silvi yang telah memberikan
kasih sayang, doa, semangat, dan dukungan baik moril maupun materi
sehingga penelitian ini dapat berjalan dengan lancar.
7. Seluruh keluarga besar Prodi Farmasi FKIK yang telah memberikan
amat besar.
8. Ibu Dewi, Ibu Susi, Ibu Ayu, Ibu Ilin, dan Ibu Yoyoh yang telah membantu
dan memberikan masukan kepada penulis selama penelitian di BATAN.
Serta seluruh keluarga besar Staf BATAN yang telah memberikan
kesempatan dan kemudahan untuk melakukan penelitian serta bantuan dan
dukungan yang amat besar.
9. Sahabat-sahabatku tercinta “Ngocol” Zakiya Kamila. M, Fathmah Syafiqoh,
Jaga Paramudita, Diah Azizah, Dias Prakatindih, Syarifatul Mufidah, Desi
Syifa, dan Afifah Nurul Izzah atas kebersaaman, persaudaraan, bantuan,
semangat, motivasi dan dukungan sejak awal perkuliahan sampai saat ini.
10.Teman – teman Farmasi 2010 Andalusia atas persaudaraan dan kebersamaan kita selama di bangku perkuliahan.
11.Seluruh laboran Farmasi UIN Syarif Hidayatullah Jakarta yang telah
membantu mempersiapkan alat dan bahan selama penelitian.
12.Semua pihak yang telah membantu selama penelitian dan penyelesaian
skripsi baik secara langsung maupun tidak langsung yang namanya tidak
dapat penulis sebutkan satu persatu.
Penulis menyadari bahwa penyusunan skripsi ini masih belum sempurna dan
banyak kekurangan. Oleh karena itu saran serta kritik yang membangun sangat
diharapkan. Semoga skripsi ini dapat bermanfaat bagi penulis dan pembaca. Akhir
kata, penulis berharap Allah SWT berkenan membalas segala kebaikan semua pihak
yang telah membantu saya dalam penelitian ini. Amiin Ya Rabbal’alamiin.
Ciputat, 23 September 2014
x UIN Syarif Hidayatullah Jakarta
HALAMAN PERNYATAAN PERSETUJUAN PUBLIKASI TUGAS AKHIR UNTUK KEPENTINGAN AKADEMIK
Sebagai civitas akademik Universitas Islam Negeri (UIN) Syarif Hidayatullah Jakarta, saya yang bertanda tangan di bawah ini:
Nama : Melia Puspitasari
NIM : 1110102000065
Program Studi : Farmasi
Fakultas : Kedokteran dan Ilmu Kesehatan
Jenis Karya : Skripsi
Demi pengembangan ilmu pengetahuan, saya menyetujui skripsi/karya ilmiah saya, dengan judul :
EFEK IRADIASI GAMMA TERHADAP KEMAMPUAN KITOSAN DALAM MENURUNKAN KADAR KOLESTEROL SECARA IN VITRO
untuk dipublikasikan atau ditampilkan di internet atau media lain yaitu Digital
Library Perpustakaan Universitas Islam Negeri (UIN) Syarif Hidayatullah Jakarta
untuk kepentingan akademik sebatas sesuai dengan Undang-Undang Hak Cipta.
Demikian pernyataan persetujuan publikasi karya ilmiah ini saya buat dengan sebenarnya.
Dibuat di : Ciputat
Pada Tanggal : 23 September 2014
DAFTAR ISI HALAMAN PERSETUJUAN PUBLIKASI KARYA ILMIAH... DAFTAR ISI ...
2.1.1 Definisi Kitosan dan Proses Pembuatan Kitosan...
xii UIN Syarif Hidayatullah Jakarta 2.5. Metode Perhitungan Berat Molekul Viskositas Kitosan...
2.6. Uji In Vitro Penurunan Kadar Kolesterol... BAB 3 METODOLOGI PENELITIAN ... 3.1. Waktu dan Lokasi Penelitian...
3.2. Alat dan Bahan...
3.2.1 Alat ...
3.2.2 Bahan ...
3.2.2.1 Bahan Uji...
3.2.2.2 Bahan Kimia...
3.3. Prosedur Penelitian ...
3.3.1 Sampel Kitosan...
3.3.2 Iradiasi Kitosan...
3.3.3 Perhitungan Derajat Deasetilasi...
3.3.4 Pengukuran Berat Molekul Viskositas Kitosan...
3.3.5 Pengujian Penurunan Kadar Kolesterol In Vitro... 3.3.5.1 Pembuatan Reagen FeCl3...
3.3.5.2 Pembuatan Asam Asetat 1%...
3.3.5.3 Pembuatan Larutan Baku Kolesterol Etanol.
3.3.5.4 Pembuatan Kurva Standar...
3.3.5.5 Pengukuran Kadar Kolesterol...
3.3.5.6 Analisa Data...
BAB 4 HASIL DAN PEMBAHASAN... 4.1 Sampel Kitosan dan Iradiasi Kitosan...
4.2 Penetapan Derajat Deasetilasi Kitosan ...
4.3 Berat Molekul Viskositas (Mv) Kitosan...
4.5 Analisa Stratistik...
BAB 5 KESIMPULAN DAN SARAN... 5.1 Kesimpulan...
5.2 Saran...
DAFTAR PUSTAKA ... LAMPIRAN ...
38
40 40
40
xiv UIN Syarif Hidayatullah Jakarta
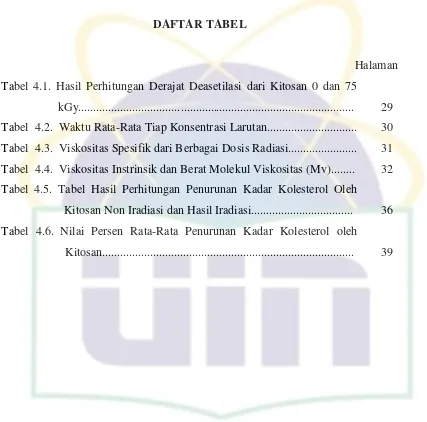
DAFTAR TABEL
Halaman
Tabel 4.1. Hasil Perhitungan Derajat Deasetilasi dari Kitosan 0 dan 75
kGy...
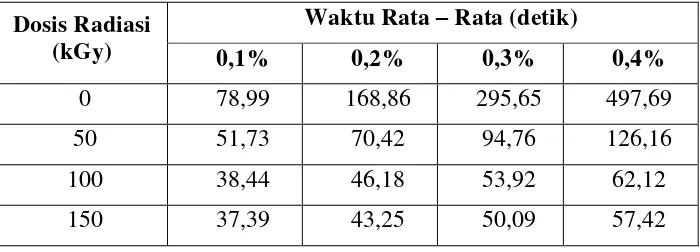
Tabel 4.2. Waktu Rata-Rata Tiap Konsentrasi Larutan...
Tabel 4.3. Viskositas Spesifik dari Berbagai Dosis Radiasi...
Tabel 4.4. Viskositas Instrinsik dan Berat Molekul Viskositas (Mv)...
Tabel 4.5. Tabel Hasil Perhitungan Penurunan Kadar Kolesterol Oleh
Kitosan Non Iradiasi dan Hasil Iradiasi...
Tabel 4.6. Nilai Persen Rata-Rata Penurunan Kadar Kolesterol oleh
Kitosan...
29
30
31
32
36
DAFTAR GAMBAR
Halaman
Gambar 2.1. Perbedaan Struktur Kimia Kitin dan Kitosan...
Gambar 2.2. Deasetilasi Kitin Menjadi Kitosan...
Gambar 2.3. Struktur Kimia Kolesterol...
Gambar 4.1. Pemutusan Rantai Kitosan Pada Ikatan 1,4-β-glikosida... Gambar 4.2. Grafik Hubungan Dosis Radiasi dengan Berat Molekul
Viskositas (Mv) Rata-Rata Kitosan...
Gambar 4.3. Struktur Kimia Kolesterol...
Gambar 4.4. Kurva Standar Larutan Kolesterol...
Gambar 4.5. Persentase Penurunan Kadar Kolesterol oleh Kitosan Non
Iradiasi dan Hasil Iradiasi...
Gambar 4.6. Simulasi Pengikatan Molekul Kolesterol-Kitosan...
6
7
11
28
32
33
35
36
xvi UIN Syarif Hidayatullah Jakarta
DAFTAR LAMPIRAN
Halaman
Lampiran 1. Kerangka Penelitian ...
Lampiran 2. Skema Pengukuran Berat Molekul Viskositas (Mv) Kitosan..
Lampiran 3. Skema Uji In Vitro Aktivitas Penurunan Kadar
Kolesterol...
Lampiran 4. Perhitungan Pembuatan Buffer Asetat...
Lampiran 5. Perhitungan Derajat Deasetilasi (DD) Kitosan...
Lampiran 6. Spektrum 1H NMR Kitosan 0 kGy dan 75 kGy...
Lampiran 7. Hasil Pengukuran Waktu Rata-Rata Larutan Kitosan 0, 50,
100, dan 150 kGy pada Tiap Konsentrasi 0,1%, 0,2%, 0,3
%, dan 0,4%...
Lampiran 8. Hasil Perhitungan Viskositas Spesifik (ƞsp) Kitosan 0, 50, 100, dan 150 kGy pada Tiap Konsentrasi 0,1%, 0,2%, 0,3
%, dan 0,4%...
Lampiran 9. Nilai Viskositas Intrinsik [ƞ] Kitosan 0, 50, 100, dan 150 kGy pada Masing-masing Konsentrasi 0,1%, 0,2%, 0,3 %,
dan 0,4%...
Lampiran 10. Grafik Penentuan Nilai Viskositas Instrinsik [η]...
Lampiran 11. Penentuan Berat Molekul Viskositas Rata-Rata (Mv)
Kitosan...
Lampiran 12. Kurva Standar...
Lampiran 13. Nilai Absorbansi Larutan Uji Kitosan...
Lampiran 14. Contoh Perhitungan Kadar Kolesterol Akhir (ppm) (B)...
Lampiran 15. Penentuan Persentase Penurunan Kadar Kolesterol Oleh
Kitosan 0, 50, 100, dan 150 kGy...
Lampiran 16. Contoh Perhitungan Analisis Persentase Penurunan Kadar
Kolesterol Terhadap Kitosan 0 kGy...
Lampiran 17. Hasil Uji Statistik Persen Penurunan Kolesterol Kitosan 0,
50, 100, dan 150 kGy...
Lampiran 19. Gambar Kitosan Sebelum dan Sesudah Radiasi...
Lampiran 20. Gambar Penentuan Waktu Alir Larutan dengan Viskometer
Ostwald... Lampiran 21. Gambar Pengujian Penurunan Kadar Kolesterol secara In
Vitro... 70
71
xviii UIN Syarif Hidayatullah Jakarta
DAFTAR ISTILAH
ANOVA : Analysis of Variance BM : Berat Molekul
BNT : Beda Nyata Terkecil
DD : Degree of Deacetylation (Derajat Deasetilasi)
HDL : High-density lipoprotein
kGy : kiloGray
LDL : Low-density lipoprotein
LSD : Least Significant Difference
Mv : Viscosity Average Molecular Weight
NMR : Nuclear Magnetic Resonance TG : Trigliserida
1.1 Latar Belakang
Seiring dengan semakin modernnya kehidupan, manusia dituntut
untuk serba cepat dalam aktivitasnya. Hal ini menyebabkan sebagian
masyarakat cenderung mengonsumsi makanan cepat saji (fast food) yang banyak mengandung lemak. Jika tidak diiringi dengan olahraga yang cukup,
hal ini dapat mengakibatkan munculnya timbunan lemak dalam tubuh,
terutama kolesterol. Salah satu penyakit akibat perubahan gaya hidup tersebut
adalah hiperkolesterolemia. Tingginya kadar kolesterol dalam darah juga
menyebabkan resiko terjadinya aterosklerosis yang merupakan faktor utama
penyebab penyakit jantung koroner yang merupakan penyebab kematian
tertinggi di dunia. Menurut WHO, pada tahun 2005 sekitar 7,6 juta jiwa
meninggal dunia akibat penyakit jantung koroner (Ridwan, 2002). Karena itu,
perlu dicarikan pemecahan dengan pendekatan ke arah pencegahan dan
peningkatan kualitas hidup.
Beberapa obat sintesis yang dapat digunakan untuk menurunkan kadar
kolesterol antara lain derivat asam fibrat, pengikat asam empedu, penghambat
HMG-CoA reduktase, dan asam nikotinat (Tjay, 2007). Pada umumnya, obat
sintesis lebih efektif dalam menurunkan kadar lipid plasma darah, namun
memiliki kekurangan. Kekurangan tersebut antara lain harganya mahal dan
efek samping yang ditimbulkan oleh senyawa tersebut menimbulkan
kecemasan dan ketidaknyamanan dalam pengobatan. Kondisi ini
menyebabkan sebagian masyarakat memilih bahan yang berasal dari alam
sebagai cara pengobatan dengan harga yang terjangkau, mudah dan resiko
efek samping yang lebih ringan (Aji etal., 2009).
Salah satu bahan alam yang belum banyak dieksplorasi di Indonesia
adalah kekayaan alam yang berasal dari perairan, padahal Indonesia dikenal
sebagai negara maritim. Wilayah perairan Indonesia juga merupakan sumber
2
UIN Syarif Hidayatullah Jakarta
merupakan komoditas ekspor yang dapat diandalkan sebagai sektor perikanan
di Indonesia yang saat ini mengalami peningkatan produksi, baik usaha
penangkapan di alam maupun hasil budidaya dengan tambak udang. Selama
tahun 2010-2011 potensi budidaya udang rata-rata meningkat sebesar 6,10 %.
Statistik Kelautan & Perikanan melaporkan pada tahun 2011, Indonesia
memproduksi udang dengan total 400.388 ton. Dari total produksi tersebut,
75% nya digunakan untuk memenuhi kebutuhan ekspor. Udang umumnya
diekspor hanya bagian daging dalam bentuk beku tanpa kepala dan kulit. Dari
proses pengupasan udang menyisakan kulit udang yang bisa mencapai
60-70% dari berat total udang (Darmawan et al., 2007).
Hasil pengupasan udang tersebut dianggap sebagai limbah yang belum
termanfaatkan secara baik dan berdaya guna. Salah satu alternatif upaya
pemanfaatan limbah cangkang udang menjadi produk yang bernilai ekonomis
tinggi adalah dengan mengekstraksi senyawa kitin yang terdapat di dalamnya,
lalu dengan proses deasetilasi kitin diolah menjadi kitosan, karena kitosan
mempunyai karakteristik fisika kimia yang lebih baik dibandingkan dengan
kitin (Rinaudo, 2006).
Kitosan memiliki gugus amina bebas yang membuat polimer ini
bersifat polikationik, sehingga polimer ini potensial untuk diaplikasikan
dalam pengolahan limbah, obat-obatan, dll (Shahidi et al., 1999). Kitosan mempunyai karakteristik fisik, biologi dan kimiawi yang baik sehingga telah
diizinkan sebagai bahan tambahan pangan di Jepang sejak 1983 dan Korea
sejak 1995 (Yogeshkumar N et al., 2013). Berdasarkan SK Badan POM RI No. HK. 00.05.52.6581 tahun 2007, kitosan diperbolehkan untuk digunakan
pada produk pangan di Indonesia. Mengingat sifat-sifatnya yang baik itulah,
maka dalam 20 tahun terakhir kitosan menjadi perhatian yang besar dari para
peneliti.
Sejak dua dekade yang lalu, PAIR BATAN telah berhasil mengisolasi
kitin dari limbah kulit udang dan mendeasetilasi kitin menjadi kitosan. Bahan
kitosan ini telah digunakan di bidang pertanian, selain itu kitosan juga dapat
digunakan di bidang farmasi dan kesehatan, antara lain sebagai antidiabetes
farmasi (Liu et al., 2008). Salah satu studi mengenai efek hipokolesterolemia oleh kitosan dikemukakan oleh Liu et al., (2008). Penelitiannya menunjukkan bahwa pemberian kitosan dengan derajat deasetilasi yang sama menghasilkan
kapasitas pengikatan kolesterol yang meningkat secara in vitro seiring penurunan berat molekul. Hal ini diperkirakan bahwa berat molekul dari
kitosan berpengaruh terhadap efek hipokolesterolemia. Penelitian secara in
vitro telah menunjukkan bahwa bila kitosan dicampur dengan kolesterol akan
terjadi reaksi pengikatan antara kitosan dengan kolesterol (Hawab, 2002).
Terikatnya molekul kolesterol oleh kitosan diharapkan dapat mengurangi
masuknya kolesterol berlebih ke dalam peredaran darah.
Berat molekul dan derajat deasetilasi sangat berpengaruh terhadap
kemampuan kitosan dalam aplikasinya. Salah satu metode untuk mengurangi
berat molekul kitosan dapat dilakukan dengan cara iradiasi gamma pada
kitosan yang dapat menyebabkan terjadinya pemutusan rantai molekul
kitosan sehingga menghasilkan kitosan dengan rantai molekul yang lebih
pendek dan iradiasi juga dapat berguna sebagai proses sterilisasi kitosan
tersebut. Teknologi radiasi memiliki beberapa keunggulan yaitu iradiasi dapat
dilakukan pada suhu kamar, tidak meninggalkan residu kimia seperti pada
proses kimia dan enzimatik, dan ramah lingkungan. Iradiasi juga tidak
menyebabkan bahan yang diiradiasi tersebut menjadi radioaktif dan juga tidak
menyebabkan toksik, sehingga obat yang dihasilkan dapat dikonsumsi dengan
aman (Pusat Diseminasi Iptek Nuklir).
Dari uraian diatas perlu adanya penelitian untuk meneliti efek kitosan
(produk BATAN) non iradiasi dan hasil iradiasi terhadap pengaruh
penurunan kadar kolesterol secara in vitro dengan menggunakan metode kolorimetri dari Rudel-Morris dan Zak yang merupakan skrining awal untuk
4
UIN Syarif Hidayatullah Jakarta
1.2 Rumusan Masalah
Berdasarkan latar belakang di atas, maka dirumuskan masalah penelitian
sebagai berikut :
1. Bagaimanakah pengaruh iradiasi gamma terhadap derajat
deasetilasi dan berat molekul kitosan?
2. Apakah kitosan yang telah diiradiasi memiliki kemampuan dalam
menurunkan kadar kolesterol secara in vitro?
3. Apakah ada perbedaan kemampuan penurunan kadar kolesterol
dari kitosan hasil iradiasi dengan kitosan tanpa iradiasi?
1.3 Tujuan Penelitian
Penelitian ini bertujuan untuk :
1. Mengetahui pengaruh iradiasi gamma terhadap derajat deasetilasi
dan berat molekul kitosan.
2. Mengetahui apakah kitosan yang telah diiradiasi memiliki
kemampuan dalam menurunkan kadar kolesterol secara in vitro. 3. Mengetahui perbedaan kemampuan kitosan iradiasi dengan kitosan
tanpa iradiasi dalam menurunkan kadar kolesterol.
1.4 Manfaat Penelitian
Manfaat yang diharapkan dari penelitian ini adalah:
1. Memberikan informasi ilmiah bagi peneliti tentang aktivitas
kitosan iradiasi dan kitosan tanpa iradiasi dalam menurunkan kadar
kolesterol.
2. Memanfaatkan sumber daya alam yang belum terolah.
3. Sebagai pengetahuan dalam bidang ilmu kimia bahan alam dan
bidang industri farmasi dalam upaya pengembangan obat
antikolesterol yang dihasilkan dari kitosan non iradiasi atau hasil
1.5 Hipotesis
Kitosan hasil iradiasi yang diproduksi oleh BATAN mempunyai
aktivitas penurunan kadar kolesterol dilihat dari kemampuannya dalam
6 UIN Syarif Hidayatullah Jakarta
BAB 2
TINJAUAN PUSTAKA
2.1 Kitosan
2.1.1 Definisi Kitosan dan Proses Pembentukan Kitosan
Kitosan (poli-β-(1,4)-D-glukosamin) merupakan polimer karbohidrat yang diturunkan dari deasetilasi kitin yang merupakan
biopolimer alami yang berlimpah setelah selulosa (No H.K, 2007). Kitin
(poli-β-(1,4)-N-asetil-D-glukosamin) merupakan penyusun utama eksoskeleton dari hewan air golongan crustacea seperti kepiting dan udang. Kulit udang mengandung protein (25%-40%), kalsium karbonat
(45%-50%), dan kitin (15%-20%), tetapi besarnya kandungan komponen
tersebut tergantung pada jenis udangnya. Kitosan tersusun oleh monomer
2-amino-2-deoksi-D-glukosa dengan ikatan glikosida pada posisi β(1,4) sehingga kitosan merupakan polimer rantai panjang glukosamin dengan
rumus molekul (C6H11NO4)n. Kitin dan kitosan memiliki struktur yang
mirip dengan selulosa. Perbedaannya terletak pada posisi C2 dimana pada
kitin posisi C2 adalah gugus asetamida, sedangkan pada kitosan posisi C2
adalah gugus amina (Kim, 2011).
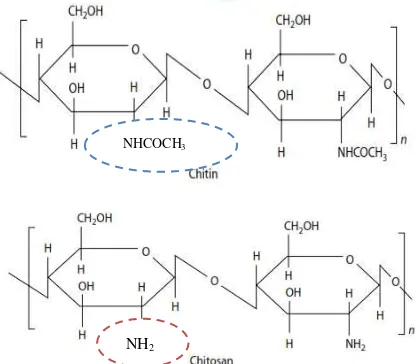
Gambar 2.1 Perbedaan Struktur Kimia Kitin dan Kitosan
[Sumber : Kim, 2011] NHCOCH3
Kitosan dibentuk melalui proses demineralisasi, deproteinasi, dan
deasetilasi. Demineralisasi dilakukan dengan menggunakan larutan asam
encer yang bertujuan untuk menghilangkan mineral yang terkandung
dalam bahan baku. Deproteinasi dilakukan dengan menggunakan larutan
basa encer untuk menghilangkan sisa-sisa protein yang masih terdapat
dalam bahan baku. Dan deasetilasi untuk menghilangkan gugus asetil
(Kim, 2011).
Proses deasetilasi (penghilangan gugus asetil) kitin menjadi kitosan
dapat dilakukan secara kimiawi maupun enzimatis. Secara kimiawi,
deasetilasi kitin dilakukan dengan penambahan NaOH, sedangkan secara
enzimatis digunakan enzim kitin deasetilase (Kim, 2011). Deasetilasi
adalah proses pemutusan gugus asetil dari glukosamin, derajat deasetilasi
menunjukkan banyaknya gugus asetil yang putus dari gugus glukosamin
dan jumlah presentase dari gugus amino pada struktur polimer. Semakin
besar derajat deasetilasi maka semakin banyak pula kitosan yang terbentuk
dari kitin, sehingga lebih mudah larut dalam asam encer. Deasetilasi kitin
akan menghilangkan gugus asetil dan menyisakan gugus amino yang
bermuatan positif, sehingga kitosan bersifat polikationik (Shahidi et al., 1999). Proses lepasnya gugus asetil (deasetilasi) dari bentuk kitin menjadi
kitosan dapat diamati dalam Gambar 2.2.
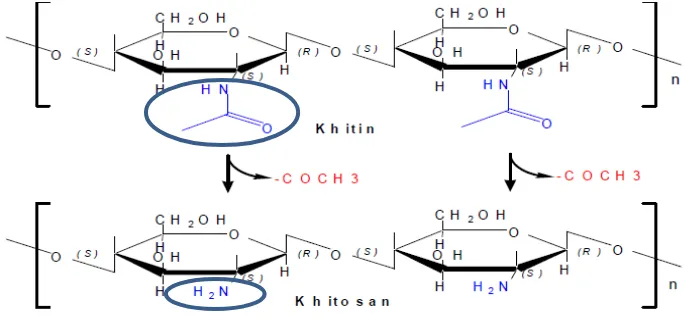
Gambar 2.2 Deasetilasi Kitin Menjadi Kitosan
8
UIN Syarif Hidayatullah Jakarta
2.1.2 Karakteristik Kitosan
Secara umum kitosan mempunyai bentuk fisik berupa padatan
amorf berwarna putih dengan struktur kristal yang tidak berubah dari
bentuk kitin. Kitosan mempunyai karakteristik kimia dan biologi sebagai
berikut (Dutta, 2004):
Karakteristik Kimia :
Memiliki gugus amino reaktif
Memiliki gugus hidroksil reaktif
Mampu mengkelat logam-logam transisi
Karakteristik Biologi :
Biokompatibel (polimer alami, biodegradabel didalam tubuh manusia, aman, dan tidak toksik)
Mampu berikatan dengan sel mamalia dan mikroba dengan kuat
Mempercepat pembentukan osteoblas yang bertanggung jawab untuk
pembentukan tulang
Hemostatik
Fungistatik dan spermisid
Antitumor dan antikolesterol
Dua faktor utama yang menjadi ciri dari kitosan adalah viskositas
atau berat molekul dan derajat deasetilasi. Oleh sebab itu, pengendalian
kedua parameter tersebut dalam proses pengolahannya akan menghasilkan
kitosan dengan berbagai karakteristik yang dapat diaplikasikan di berbagai
bidang. Derajat deasetilasi dapat didefinisikan sebagai rasio gugus
asetamida dan gugus amino, dan menunjukkan sejauh mana proses
deasetilasi berjalan. Derajat deasetilasi dan berat molekul berperan penting
dalam kelarutan kitosan (Shahidi et al., 1999). Metode untuk menganalisis DD antara lain dengan cara titrasi, HPLC, IR, 1H NMR, dan 13C NMR.
Kitosan berbentuk spesifik dan mengandung gugus amino dalam rantai
utamanya. Kitosan adalah gula yang unik, karena polimer ini mempunyai
gugus amin bermuatan positif, sedangkan polisakarida lain umumnya
bersifat netral atau bermuatan negatif (Czechowska-Biskup, 2012). Gugus
seperti asam lemak dan asam empedu (Aranaz et al., 2009). Nitrogen pada gugus amin kitosan berfungsi sebagai donor elektron dalam pengikatan
selektif logam tertentu. Kitosan larut dalam asam asetat, asam laktat, asam
malat, asam format dan suksinat. Kitosan mempunyai kelarutan yang lebih
baik daripada kitin. Suatu molekul dikatakan kitosan bila menghasilkan
derajat deasetilasi (DD) dengan kisaran DD mencapai 60-100%
(Yogeshkumar N, 2013).
Kitosan menunjukkan sifat-sifat polimer biomedis misalnya
non-toksik, biokompatibel, dan biodegradabel. Kitosan memiliki tiga tipe
gugus fungsional reaktif, yaitu sebuah gugus amino serta dua gugus
hidroksil yang masing-masing berada pada posisi C-2, C-3 dan C-6.
Modifikasi kimiawi dari ketiga gugus ini menyebabkan kitosan memiliki
banyak kegunaan untuk diaplikasikan pada berbagai bidang baik pertanian,
kesehatan, dan lain-lain (Shahidi et al., 1999).
Sifat-sifat kitosan seperti kelarutan, bobot molekul yang relatif
besar, dan juga viskositas yang tinggi menyebabkan kendala dalam
aplikasinya. Oleh karena itu dibutuhkan turunan kitosan yang lebih mudah
larut air dan viskositas yang rendah. Sifat-sifat tersebut dimiliki oleh
oligomer dari kitosan (oligokitosan). Oligokitosan merupakan senyawa
hasil hidrolisis kitosan, baik secara kimiawi (dengan asam kuat), secara
enzimatis (dengan enzim kitosanase), dan menggunakan iradiasi.
2.1.3 Manfaat Kitosan
Banyak sekali potensi kitosan yang sudah banyak diteliti, mulai
dari pangan, mikrobiologi, kesehatan, pertanian, dan sebagainya.
Mengingat kitosan mempunyai gugus amin yang reaktif dan gugus
hidroksil yang banyak serta kemampuannya membentuk gel maka kitosan
dapat berperan sebagai komponen reaktif, pengkelat, pengikat,
pengabsorbsi, penstabil, pembentuk film, penjernih, plokulan, koagulan
(Shahidi et al., 1999). Aplikasi kitosan dalam bidang pangan salah satunya yaitu sebagai makanan berserat sehingga dapat meningkatkan massa feses,
10
UIN Syarif Hidayatullah Jakarta
kolesterol. Dalam bidang kesehatan dapat berperan sebagai antibakteri,
antihiperkolesterolemia, antikoagulan dalam darah, pengganti saluran
darah, anti tumor (penggumpal) sel-sel leukimia (Aranaz et al., 2009). Kitosan telah digunakan secara luas di industri makanan, kosmetik,
kesehatan, farmasi dan pertanian serta pada pengolahan air limbah. Di
industri makanan, kitosan dapat digunakan sebagai suspensi padat,
pengawet, penstabil warna, penstabil makanan, bahan pengisi, pembentuk
gel, tambahan makanan hewan dan sebagainya (Aranaz et al., 2009). 2.1.4 Kitosan sebagai Antikolesterol
Kitosan dapat digunakan sebagai obat antikolesterol. Kitosan
mampu menurunkan kolesterol LDL (kolesterol jahat) sekaligus
meningkatkan komposisi perbandingan kolesterol HDL (kolesterol baik)
terhadap LDL, sehingga peneliti Jepang menyebutnya hypocholesteromic agent yang efektif, karena mampu menurunkan kadar kolesterol darah tanpa efek samping. Kitosan mempunyai potensi sebagai
hipokolesterolemik yang tinggi, dalam saluran pencernaan, senyawa ini
berinteraksi dengan lemak membentuk misela atau emulsifikasi lipid pada
fase absorbsi (Deuchi et al., 1994). Kitosan dapat menyerap 97% lemak tubuh yang dianggap lebih unggul dibandingkan jenis polimer lain seperti
selulosa, karagenan, agar-agar, dan lain–lain. Knorr (1984) menyatakan bahwa kitosan merupakan senyawa yang tidak beracun sebagai unsur serat
makanan dan dapat menurunkan kadar kolesterol. Aktivitas
hipokolesterolemia dari kitosan menghasilkan efek yang lebih baik ketika
derajat deasetilasinya tinggi (90%), sehingga menghasilkan ikatan
elektrostatik yang lebih kuat antara kitosan dan substansi anion seperti
asam lemak dan asam empedu (Liu et al.,2008)
2.2 Kolesterol
2.2.1 Definisi Kolesterol
Kolesterol (C27H45OH) (Yun.: chole = empedu, stereos = padat) adalah zat alamiah dengan sifat fisik serupa lemak tetapi berumus steroida,
bangun esensial bagi tubuh untuk sintesa zat-zat penting, seperti membran
sel dan bahan isolasi sekitar serat saraf, begitu pula hormon kelamin dan
anak-ginjal, vitamin D serta asam empedu (Tjay, 2007). Kolesterol
sebagian besar disintesiskan oleh hati dan sebagian kecil diserap dari diet.
Kolesterol merupakan produk khas dari metabolisme hewan dan oleh
karenanya terdapat dalam makanan yang berasal dari hewan seperti
daging, hati, otak dan kuning telur. Keberadaan kolesterol dalam
pembuluh darah yang kadarnya tinggi akan membuat endapan/kristal
lempengan yang akan mempersempit/menyumbat pembuluh darah. Kadar
kolesterol didalam darah adalah dibawah 200 mg/dl. Apabila melampaui
batas normal maka disebut sebagai hiperkolesterolemia (Tjay,2007).
Sintesa. Dalam keadaan normal hati melepaskan kolesterol ke darah sesuai kebutuhan. Tetapi bila diet mengandung terlampau banyak
kolesterol atau lemak hewani jenuh maka kadar kolesterol darah akan
meningkat (Tjay, 2007).
Gambar 2.3 Struktur Kimia Kolesterol
[Sumber: www.chemicalbook.com]
2.2.2 Fungsi Kolesterol
Fungsi kolesterol dalam tubuh antara lain merupakan zat essensial
untuk membran sel tubuh, merupakan bahan pokok untuk pembentukan
garam empedu yang diperlukan untuk proses pencernaan lemak atau
minyak, dan merupakan bahan baku untuk membentuk hormon steroid,
misalnya: progesteron dan estrogen pada wanita, testosteron pada pria,
12
UIN Syarif Hidayatullah Jakarta
untuk pembentukan membran sel dan disintesis di seluruh jaringan, tetapi
90% disintesis dalam sel mukosa usus dan hepatosit (Tjay, 2007).
Kolesterol yang disintesa diubah menjadi jaringan, hormon dan
vitamin yang kemudian beredar ke dalam tubuh melalui darah. Namun
demikian, kolesterol ada yang kembali ke hati untuk diubah menjadi asam
empedu dan garam. Linder (1992) menyatakan bahwa orang dewasa
rata-rata membutuhkan 1.1 gram kolesterol untuk kebutuhan tubuhnya. Dari
jumlah itu, 25-40% atau 200-300 mg secara normal berasal dari makanan
dan selebihnya dari endogen (biosintesis) terutama oleh hati kemudian
oleh usus kecil. Kadar kolesterol normal dalam plasma pada orang dewasa
normal sebesar 120-220 mg/dl. Biasanya kadar kolesterol yang melebihi
batas ini dianggap sebagai hiperkolesterolemia.
2.2.3 Lipoprotein
Kolesterol bersifat tidak larut dalam air sehingga diperlukan suatu
alat transportasi untuk beredar dalam darah yaitu apoprotein yang
merupakan salah satu jenis protein. Kolesterol akan membentuk kompleks
dengan apoprotein sehingga membentuk suatu ikatan yang disebut
lipoprotein. Lipoprotein adalah jenis lipid plasma yang bersifat hidrofobik.
Secara umum lipoprotein yang dikenal yaitu HDL, LDL, chyclomicron, VLDL, tetapi dua jenis liporpotein utama yaitu HDL dan LDL (Tjay,
2007).
Lipoprotein jenis pertama adalah lipoprotein dengan densitas tinggi
atau High-density lipoprotein (HDL) dikenal sebagai kolesterol baik, berperan dalam membawa kolesterol dalam darah dari jaringan tubuh
kembali ke hati untuk dieliminasi. Kadar HDL yang tinggi dalam darah
adalah kondisi yang baik bagi tubuh. Apabila kadar HDL rendah (< 40)
dalam darah, maka hal ini dapat memicu terjadinya pembentukan plak
pada arteri jantung, serangan jantung dan kematian kardiovaskular.
Lipoprotein jenis kedua adalah lipoprotein dengan densitas rendah atau
jantung dan kematian kardiak. LDL berfungsi mengangkut kolesterol dari
hati ke jaringan tubuh yang membutuhkan (Tjay, 2007).
2.2.4 Hiperkolesterolemia
Hiperkolesterolemia adalah suatu keadaan tingginya kadar
kolesterol dalam darah. Ada tiga tingkatan kolesterol dalam serum, yaitu
kolesterol serum normal dengan kolesterol total < 200 mg/dl, kolesterol
serum tinggi yang dapat menyebabkan kondisi hiperkolesterolemia sedang
(240-289 mg/dl) dan kolesterol serum sangat tinggi yang dapat
menyebabkan hiperkolesterolemia berat (>290 mg/dl) (Tjay, 2007)
Beberapa bahan kimia yang diindikasikan memiliki potensi
hipokolesterolemik adalah sitosterol, niasin, vitamin C, vitamin E dan
karoten. Adapun mekanisme penurunan kolesterol oleh serat pangan
adalah: kolesterol yang disintesa maupun yang berasal dari makanan
beredar dalam darah. Sebagian kolesterol akan diubah menjadi asam
empedu, masuk ke dalam usus dan berubah menjadi feses, kemudian
diekskresikan ke luar. Semakin banyak kolesterol tubuh yang
diekskresikan melalui empedu, semakin banyak pula kolesterol dikurangi
dari darah. Hal inilah yang menyebabkan penurunan kadar kolesterol di
dalam darah. Peranan serat pangan adalah meningkatkan produksi asam
empedu dan mengeliminasi ke dalam usus untuk diekskresikan sebagai
feses. Pengaruh serat pangan terhadap penurunan kadar kolesterol apabila
telah terjadi peningkatan kolesterol di dalam darah.
2.2.5 Antilipemika
Antilipemika adalah obat yang dapat menurunkan kadar kolesterol
dan/atau TG darah yang tinggi. Menurut Tjay (2007) obat-obat tersebut
sekarang ini tersedia dalam 4 kelompok utama:
a. Damar penukar anion/pengikat asam empedu: kolestiramin dan
kolestipol.
Berdaya mengikat asam empedu sehingga sekresi kolesterol
14
UIN Syarif Hidayatullah Jakarta
kolesterol total dengan 8-15%, bersama nikotinat sampai 40% dan
bekerja sinergistis dengan penghambat-HMG-CoA reduktase.
Kombinasi terakhir mampu menurunkan kadar LDL-kolesterol dengan
50-60%.
Efek samping dari kolestiramin berupa gangguan lambung-usus,
terutama obstipasi. Rasanya tidak enak. Resorpsi dari vit A, D, E, K
dapat berkurang.
b. Asam nikotinat dan acipimox terutama menurunkan TG dan VLDL,
efeknya terhadap kolesterol total dan LDL lebih ringan. Berhubung
efek sampingnya yang tidak nyaman (vasodilatasi pembuluh muka,
flushing) dan rasa panas, nyeri kepala, gatal-gatal dan iritasi kulit,
juga penglihatan berkurang, khususnya digunakan sebagai obat
tambahan pada damar dari fibrat.
c. Fibrat: klofibrat, simfibrat dan fenofibrat. Berkhasiat menurunkan TG dan VLDL dengan kuat, kolesterol total hanya sedikit. LDL dapat
diturunkan pula, sedangkan HDL dinaikkan sedikit, kecuali
gemfibrozil yang menaikkan HDL dengan kuat. Singkatnya fibrat
meningkatkan kadar HDL (10 %) dan menurunkan kadar LDL dengan
10-15%.
Efek samping dari klofibratyang paling sering berupa gangguan
(sementara) saluran cerna, kadang kala nyeri kepala, kantuk,
eksanterna, stimulasi nafsu makan, rambut rontok dan impotensi.
Semua senyawa fibrat dapat menyebabkan suatu sindroma myositis (radang otot) yang insidensinya lebih meningkat bila pada saat
bersamaan menggunakan zat penghambat reduktase.
d. Statin: lovastatin, simvastatin, pravastatin, atorvastatin, dan
rosuvastatin.
Senyawa penghambat-reduktase (HMG-CoA-reductase-inhibitors) ini berdaya menurunkan sintesa kolesterol endogen dalam hati dan dengan demikian terjadi penurunan kolesterol total dengan
HDL dinaikkan. Dapat dikombinasi dengan damar untuk pengobatan
hiperlipidemia yang parah.
Efek sampingnya pada umumnya ringan, antara lain nyeri otot
(2-11% myopathie) reversibel, yang adakalanya menjadi gangguan otot parah yang disebut rhabdomyolysis. Juga terapi kombinasi senyawa statin lain dan fibrat (mis. fenofibrat - pravastatin) dapat
menimbulkan gangguan yang ditandai nyeri dan lemah otot
mendadak, gejala-gejala flu dan urin berwarna gelap. Efek samping
yang paling sering terjadi dan berupa rasa letih dan nyeri otot,
terutama dari bokong dan tungkai atas.
2.3 Radiasi
2.3.1 Definisi Radiasi
Proses yang kejadiannya berlangsung tanpa unsur kesengajaan atau
tanpa adanya perlakuan khusus disebut radiasi yaitu pancaran energi atau
partikel berenergi oleh suatu sumber, misalnya: bentuk mutasi pada
tanaman dapat terjadi secara alamiah (spontan) akibat radiasi sinar kosmik
di alam. Sedangkan iradiasi adalah suatu teknik yang digunakan untuk
pemakaian radiasi secara sengaja dan terarah atau proses yang kejadiannya
berlangsung karena adanya perlakuan khusus terhadap sesuatu obyek yang
dilakukan secara disengaja (misalnya untuk tujuan melakukan suatu
pengamatan atau penelitian), contoh: bahan makanan yang telah diiradiasi
(the irradiated food) dengan sinar gamma dapat menjadi awet dan tidak cepat membusuk ataupun rusak (Leswara, 2005). Proses radiasi saat ini
banyak digunakan dalam berbagai bidang seperti sterilisasi alat-alat
kedokteran, pengawetan bahan makanan, serta digunakan juga untuk
diagnosa maupun terapi suatu penyakit yang dalam hal ini digunakan suatu
radionuklida. Selain itu radiasi juga dapat berfungsi sebagai salah satu
metode untuk memutus bobot molekul suatu senyawa. Proses radiasi
adalah metode yang paling menjanjikan, karena prosesnya yang sederhana,
dapat dilakukan pada suhu kamar dan tidak ada pemurnian produk yang
16
UIN Syarif Hidayatullah Jakarta
perubahan struktur utama dari suatu senyawa yang diputus berat
molekulnya (Chmielewski, 2005).
2.3.2 Macam-macam Radiasi
Menurut Leswara (2005) ada tiga jenis radiasi yang sering kali
dipancarkan dari inti radioaktif yaitu radiasi alfa, beta, dan gamma.
1. Partikel Alfa
Radiasi alfa terbentuk oleh partikel – partikel zat yang terdiri dari dua proton dan dua neutron. Jadi, partikel alfa sama dengan inti Helium
yang kehilangan dua buah elektron. Di dalam udara partikel alfa
terdapat dalam rentang kira-kira 5 cm, tetapi di dalam jaringan kurang
dari 100µ.
2. Partikel Beta
Radiasi beta ada dua jenis, oleh karena itu kita mengenal dua jenis
elektron yaitu negatron (elektron bermuatan negatif) dan positron
(elektron bermuatan positif). Positron dan negatron adalah sama,
kecuali dalam hal muatannya yaitu +1 dan -1. Elektron – elektron ini dipancarkan dari inti radioaktif yang disebut partikel beta. Partikel
beta mempunyai rentang lebih dari 3 meter di dalam udara dan
kira-kira 1 mm di dalam jaringan.
3. Radiasi Gamma
Radiasi gamma adalah gelombang elektromagnetik sedangkan
radiasi alfa dan beta adalah partikel-partikel. Sinar gamma
diradiasikan sebagai foton atau kuantum energi dengan kecepatan c =
3,0 x 1010 cm/det. Perbedaan radiasi gamma dengan sinar X dan sinar
UV, sinar tampak dan sinar lainnya hanya dalam panjang gelombang
atau frekuensinya saja. Sinar gamma bersifat penetrasi yang paling
besar diantara radiasi – radiasi yang dipancarkan oleh radioisotop (kecuali netrino) dan dapat dengan mudah menembus jaringan lebih
dari 30 cm dan timbal (Pb) dengan ketebalan beberapa inci.
Sinar radiasi yang umumnya digunakan saat ini adalah radiasi
aplikasi dalam kehidupan manusia, dikarenakan sinar gamma dapat
menembus beberapa bahan, dan sinar gamma tidak akan membuatnya
menjadi radioaktif. Sejauh ini ada tiga radionuklida pemancar gamma
yang paling sering digunakan yakni cobalt-60, cesium-137 dan
technetium-99m.
1. Cesium -137 digunakan dalam perawatan kanker, mengukur dan
mengontrol aliran fluida pada beberapa proses industri, menyelidiki
subterranean strata pada oil wells, dan memastikan level pengisian yang tepat untuk paket makanan, obat – obatan dan produk yang lain.
2. Cobalt-60 bermanfaat untuk: sterilisasi peralatan medis di rumah
sakit, pasteurize beberapa makanan dan rempah, sebagai terapi kanker, dan mengukur ketebalan logam dalam stell mills.
3. Tc-99m adalah isotop radioaktif yang paling banyak digunakan secara luas untuk studi diagnosa sebagai radiofarmaka.
(Technetium-99m memiliki waktu paruh yang lebih singkat).
Radiofarmaka ini digunakan untuk mendiagnosa otak, tulang, hati
dan juga mampu menghasilkan pencitraan yang dapat digunakan
untuk mendiagnosa aliran darah pasien.
2.4 Spektrofotometer UV-Vis
Spektrofotometer yang sesuai untuk pengukuran di daerah
spektrum ultraviolet dan sinar tampak terdiri atas suatu sistem optik
dengan kemampuan menghasilkan sinar monokromatis dalam jangkauan
panjang gelombang 200-800 nm. Suatu spektrum ultraviolet meliputi
daerah bagian ultraviolet (190-380 nm), spektrum Vis (Visible) bagian sinar tampak (380-780 nm) (Gandjar, 2007).
Pengukuran dengan alat spektrofotometer UV-Vis didasarkan pada hubungan antara berkas radiasi elektromagnetik yang ditransmisikan
(diteruskan) atau yang diabsorbsi dengan tebalnya cuplikan dengan
18
UIN Syarif Hidayatullah Jakarta
Hubungan tersebut dinyatakan dalam Hukum Lambert-Beer
(Gandjar, 2007) :
Instrumentasi dari spektrofotometer UV-Vis ini dapat diuraikan sebagai berikut (Gandjar, 2007):
1. Suatu sumber energi cahaya yang berkesinambungan yang meliputi
daerah spektrum yang mana alat tersebut dirancang untuk
beroperasi.
2. Suatu monokromator, yakni sebuah piranti untuk memencilkan pita
sempit panjang gelombang dari spektrum lebar yang dipancarkan
oleh sumber cahaya.
3. Suatu wadah untuk sampel (dalam hal ini digunakan kuvet).
4. Suatu detektor, yang berupa transduser yang merubah energi cahaya menjadi suatu isyarat listrik.
5. Suatu amplifier (pengganda) dan rangkaian yang merubah energi cahaya menjadi suatu isyarat listrik.
Syarat-syarat senyawa yang dapat dianalisis menggunakan UV-Vis yaitu : 1) Bahan mempunyai gugus kromofor (UV)
2) Bahan tidak mempunyai gugus kromofor tapi berwarna (Visible) 3) Bahan tidak mempunyai gugus kromofor tidak berwarna, ditambahkan
pereaksi warna (Visible)
4) Bahan tidak mempunyai gugus kromofor dibuat turunannya yang
mempunyai gugus kromofor (UV).
Menurut Gandjar (2007) ada beberapa hal yang harus diperhatikan
yang semula tidak berwarna yang akan dianalisis dengan spektrofotometri
visibel karena senyawa tersebut harus diubah terlebih dahulu menjadi
senyawa yang berwarna. Berikut adalah tahapan-tahapan yang harus
diperhatikan:
a. Pembentukan molekul yang dapat menyerap sinar UV-Vis
Hal ini perlu dilakukan jika senyawa yang dianalisis tidak
menyerap pada daerah tersebut. Cara yang digunakan adalah dengan
merubah menjadi senyawa lain atau direaksikan dengan pereaksi
tertentu. Pereaksi yang digunakan harus memenuhi beberapa
persyaratan yaitu:
Reaksinya selektif dan sensitif
Reaksinya cepat, kuantitatif, dan reprodusibel
Hasil reaksi stabil dalam jangka waktu yang lama
b. Pembuatan kurva baku
Dibuat seri larutan baku dari zat yang akan dianalisis dengan
berbagai konsentrasi. Masing-masing absorbansi larutan dengan
berbagai konsentrasi diukur, kemudian dibuat kurva yang merupakan
hubungan antara absorbansi dengan konsentrasi. Bila hukum
Lambert-Beer terpenuhi maka kurva baku berupa garis lurus.
c. Pembacaan absorbansi sampel atau cuplikan
2.5 Metode Perhitungan Berat Molekul Viskositas (Mv) Kitosan (Hwang, et al., 1997)
Berat molekul merupakan variabel yang penting, sebab
berhubungan langsung dengan sifat-sifat fisika polimer. Pada umumnya
polimer dengan berat molekul yang lebih tinggi bersifat lebih kuat. Namun
berat molekul yang terlalu tinggi menyebabkan kesukaran dalam
memproses polimer tersebut. Metode yang mudah untuk penetapan berat
molekul adalah metode viskositas larutan menggunakan alat viskometer
dengan cara menghitung perbandingan antara waktu alir larutan polimer
terhadap waktu alir pelarut murni. Viskositas merupakan ukuran yang
20
UIN Syarif Hidayatullah Jakarta
viskositas larutan polimer terhadap viskositas pelarut murni dapat dipakai
untuk menentukan massa molekul nisbi polimer. Keunggulan dari metode
ini adalah lebih cepat, lebih mudah, alatnya murah serta perhitungannya
lebih sederhana. Alat yang digunakan adalah Viskometer Ostwald.
Berat molekul kitin dan kitosan diukur berdasarkan viskositas
instrinsik (ƞ). Sejumlah kitosan dilarutkan dalam 0,05, 0,1, 0,2, dan 0,3 M NaCl/ 0,1 M CH3COOH lalu dimasukkan ke dalam viskometer. Kemudian
10 mL pelarut dimasukkan ke dalam tabung viskometer ostwald dalam
media air pada suhu 25°C. Data yang diperoleh dipetakan pada grafik
ƞsp/C terhadap C. Viskositas intrinsik adalah titik pada grafik yang menunjukkan nilai C=0. Berat molekul viskositas (Mv) ditentukan
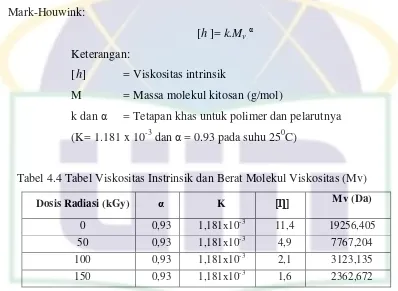
berdasarkan persamaan Mark-Houwink yaitu:
[ƞ] = kMα
Keterangan:
[ƞ] = Viskositas intrinsik M = Massa molekul (g/mol)
K dan a = Tetapan khas untuk polimer dan pelarutnya
2.6 Uji In Vitro Penurunan Kadar Kolesterol [Rudel-Morris, (1973), Sutioso, (2012), Rao, (1992)]
Kemampuan pengikatan kolesterol didasarkan pada pengukuran
kolesterol dalam larutan kolesterol-etanol setelah penambahan sediaan uji
atau sampel dengan masa inkubasi 60 menit pada suhu 37oC menggunakan
metode dari Rudel-Morris dan metode Zak, yaitu penambahan reaksi
pewarnaan antara FeCl3 dalam asam asetat glasial dan H2SO4(p) sebagai
katalisator. Jumlah kolesterol bebas ditentukan dengan mengukur serapan.
Serapan diukur menggunakan spektrofotometer UV-Visibel pada panjang
BAB 3
METODOLOGI PENELITIAN
3.1 Waktu dan Lokasi Penelitian
Penelitian ini dilaksanakan pada bulan Maret 2014 hingga Agustus
2014 di Laboratorium Bahan Kesehatan, Bidang Proses Radiasi, Pusat
Aplikasi Isotop dan Radiasi (PAIR), BATAN Pasar Jumat, Jakarta Selatan.
Serta di Laboratorium penelitian 2 (PDR), Fakultas Kedokteran dan Ilmu
Kesehatan, UIN Syarif Hidayatullah Jakarta.
3.2 Alat dan Bahan 3.2.1 Alat
Alat yang digunakan dalam penelitian ini terdiri dari Iradiator
gamma IRKA, penangas air (Eyela), inkubator (France Etuves), timbangan
analitik (Acculab Bl-210S), spektrofotometer UV-Vis (Hitachi U-2910), viskometer ostwald (Cannon 150 P863), H1 NMR (Jeol JNM ECA-500
MHz), vorteks (Wiggen Hauser), lemari asam, sentrifugator, tabung
sentrifus, labu ukur, gelas kimia, batang pengaduk, pipet tetes, spatula,
tabung reaksi bertutup, kaca arloji, blender, gelas ukur, mikropipet, pipet
gondok dan bulp, alumunium foil, kuvet, stopwatch.
3.2.2 Bahan 3.2.2.1 Bahan Uji
Bahan uji yang digunakan adalah kitosan yang diproduksi oleh
Badan Tenaga Nuklir Nasional (BATAN), Pusat Aplikasi Isotop dan
Radiasi (PAIR) dan Kolesterol (Sigma).
3.2.2.2 Bahan Kimia
Bahan-bahan kimia yang dibutuhkan dalam penelitian ini meliputi
FeCl3.6H2O (Merck), aquadest, H2SO4(p) (Merck), etanol 95% (pa)
22
UIN Syarif Hidayatullah Jakarta
3.3 Prosedur Penelitian 3.3.1 Sampel Kitosan
Kitosan yang akan digunakan yaitu hasil produksi dari BATAN
yang sudah tersedia dan telah melalui proses demineralisasi, deproteinasi,
dan deasetilasi.
3.3.2 Iradiasi Kitosan
Pada proses iradiasi terhadap kitosan, sumber radiasi yang
digunakan yaitu menggunakan radiasi gamma 60Co dengan berbagai dosis
iradiasi. Kitosan dikemas ke dalam tiga plastik klip untuk tiga dosis dan
masing-masing diberi label dosis energi radiasi yaitu 50, 100, dan 150
kGy. Kemudian kitosan yang telah dikemas tersebut dimasukkan ke dalam
alat iradiator. Iradiasi tersebut dilakukan dengan kecepatan dosis 10
kGy/jam.
3.3.3 Perhitungan Derajat Deasetilasi (Czechowska-Biskup, 2012)
Perhitungan derajat deasetilasi (DD) kitosan dengan menggunakan
instrument 1H-NMR. Serbuk Kitosan dilarutkan dalam larutan D2O dan
asam asetat D2O sampai kitosan larut sempurna, kemudian diinjekkan ke
dalam instrument 1H-NMR, lalu dibaca hasilnya.
3.3.4 Pengukuran Berat Molekul Viskositas (Mv) Kitosan (Hwang, et al, 1997)
a. Pembuatan 0,2 M Asam asetat
Sebanyak 12 g asam asetat dilarutkan dalam 1000 mL aquades.
b. Pembuatan 0,1 M Natrium asetat
Sebanyak 8,2 g Natrium asetat dilarutkan dalam 1000 mL aquades.
c. Pembuatan Buffer asetat pH 4,3 250 mL
Menghitung pH 4,3 untuk mendapatkan volume (mL) asam asetat 0,2
M yang diperlukan yaitu sebanyak 147,2 mL, kemudian hitung
volume (mL) natrium asetat yang diperlukan untuk ditambahkan ke
d. Pembuatan larutan kitosan 0,1 % dalam larutan Buffer pH 4,3
Sebanyak 0,05 g kitosan dilarutkan dalam 50 mL Buffer pH 4,3.
e. Pembuatan larutan kitosan 0,2% dalam larutan Buffer pH 4,3
Sebanyak 0,1 g kitosan dilarutkan dalam 50 mL Buffer pH 4,3.
f. Pembuatan larutan kitosan 0,3% dalam larutan Buffer pH 4,3
Sebanyak 0,15 g kitosan dilarutkan dalam 50 mL Buffer pH 4,3.
g. Pembuatan larutan kitosan 0,4% dalam larutan Buffer pH 4,3
Sebanyak 0,2 g kitosan dilarutkan dalam 50 mL Buffer pH 4,3.
Semua konsentrasi larutan kitosan dibuat triplo untuk
masing-masing kitosan hasil iradiasi (50 kGy, 100 kGy, 150 kGy) dan kitosan non
iradiasi, kemudian setelah larutan kitosan dibuat didiamkan terlebih dahulu
minimal selama 24 jam dan maksimal 3 hari sebelum digunakan. Setelah
itu sebanyak 10 mL pelarut dimasukkan ke dalam tabung ostwald, kemudian tabungnya dimasukkan ke dalam media air (25oC), kemudian
larutan dihisap dengan pushball hingga melewati 2 batas dibagian atas viskometer, lalu kendurkan cairan sampai batas pertama lalu mulai
perhitungan menggunakan stopwatch (dalam detik) hingga batas kedua. Hasil yang diperoleh dicatat. Pengukuran dilakukan sebanyak tiga kali.
Langkah yang sama dilakukan untuk larutan kitosan 0,1 %; 0,2%; 0,3%;
dan 0,4% dari kitosan hasil iradiasi dan non iradiasi. Viskositas spesifik
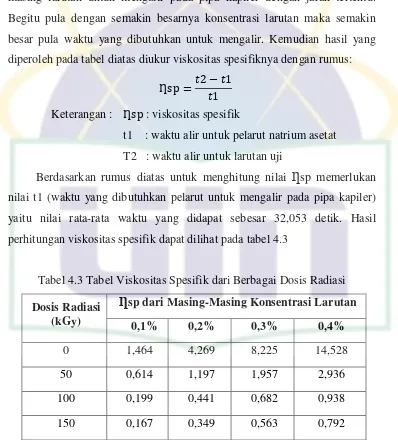
dihitung dengan persamaan di bawah ini:
ƞsp
Dimana ƞsp adalah viskositas spesifik, t2 adalah waktu alir untuk larutan dan t1 adalah waktu alir untuk pelarut. Viskositas intrinsik diperoleh
dengan memplotkan hasil ƞsp/C terhadap C. Kemudian berat molekul viskositas kitosan dihitung dengan menggunakan persamaan
Mark-Houwink:
[h ]= k.M α Keterangan:
[h] = Viskositas intrinsik
24
UIN Syarif Hidayatullah Jakarta
k dan α = Tetapan khas untuk polimer dan pelarutnya (K= 1.181 x 10-3 dan α = 0.93 pada suhu 250C)
3.3.5 Pengujian Penurunan Kadar Kolesterol secara In Vitro (Rudel and
Morris, 1973; Sutioso, 2012; Rao, 1992; Nalole, 2009)
3.3.5.1 Pembuatan Reagen FeCl3
Sebanyak 8,402 gram FeCl3.6H2O dilarutkan dalam 100 mL asam
asetat glasial, larutan ini akan tetap stabil hingga beberapa bulan
kedepan.
3.3.5.2 Pembuatan Asam Asetat 1%
Sebanyak 1 mL Asam Asetat glasial dan ad 100 mL dengan
aquades.
3.3.5.3 Pembuatan Larutan Baku Kolesterol Etanol
Dibuat larutan induk kolesterol dengan konsentrasi 1000 ppm
yaitu dengan cara melarutkan 100,0 mg serbuk kolesterol dalam 100
mL etanol absolut (95%) pada suhu ± 45oC diatas waterbath. 3.3.5.4 Pembuatan Kurva Standar
a. Penentuan Panjang Gelombang Maksimum (λmaks)
Dilakukan scanning panjang gelombang dari larutan standar kolesterol dengan konsentrasi 100 ppm dalam labu 5 mL yang diambil
dari larutan induk 1000 ppm sebanyak 0,5 mL lalu di ad dengan etanol
95% sampai volum 5 mL, kemudian ditambahkan 2,0 mL reagen FeCl3
kemudian divorteks dan didiamkan selama 10 menit, dan menutup
lapisan luar tabungnya dengan alumunium voil untuk melindungi dari
cahaya. Lalu masing-masing larutan ditambahkan 1,0 mL H2SO4(p) dan
campuran larutan dihomogenkan dengan menggunakan vorteks,
kemudian didiamkan selama 30 menit. Dilakukan pengukuran
b. Pembuatan Seri Konsentrasi Larutan Baku Kolesterol dan Pengukuran
Kurva standar
Dari larutan induk kolesterol konsentrasi 1000 ppm dibuat 5 seri
konsentrasi yaitu diambil dari larutan induk tersebut sebanyak 0,5; 0,75;
1; 1,25; dan 1,5 mL kemudian dicukupkan volumenya masing-masing
hingga 5 mL dengan etanol 95%, sehingga dihasilkan masing-masing
larutan dengan konsentrasi 100, 150, 200, 250, dan 300 ppm.
Masing-masing larutan tersebut ditambahkan 2,0 mL reagen FeCl3 kemudian
divorteks dan didiamkan selama 10 menit, dan menutup lapisan luar
tabungnya dengan alumunium voil untuk melindungi dari cahaya. Lalu
masing-masing larutan ditambahkan 1,0 mL H2SO4(p) dan campuran
larutan dihomogenkan dengan menggunakan vorteks, kemudian
didiamkan selama 30 menit dan diukur absorbansinya pada panjang
gelombang maksimum 526 nm sesuai hasil scanning sebelumnya. 3.3.5.5 Pengukuran Kadar Kolesterol
Sampel kitosan hasil iradiasi (50 kGy, 100 kGy, 150 kGy) dan
non iradiasi masing-masing ditimbang sebanyak 30,0 mg (triplo) lalu
masing-masing dilarutkan dengan asam asetat 1% sebanyak 20 tetes,
kemudian masing-masing ditambahkan 5 mL larutan kolesterol dengan
konsentrasi 300 ppm. Campuran masing-masing larutan dihomogenkan
dengan menggunakan vorteks dan diinkubasi pada suhu 37oC selama 60
menit, kemudian disentrifus pada 4000 rpm selama 5 menit.
Masing-masing kolesterol yang tersisa dalam supernatan diambil (5 mL) dan
dipindahkan ke dalam tabung reaksi bertutup. Masing-masing
supernatan tersebut ditambahkan 2,0 mL reagen FeCl3 kemudian
divorteks dan didiamkan selama 10 menit, dan menutup lapisan luar
tabungnya dengan alumunium voil untuk melindungi dari cahaya. Lalu
masing-masing larutan ditambahkan 1,0 mL H2SO4(p) dan campuran
larutan dihomogenkan dengan menggunakan vorteks, dengan demikian
jumlah pengenceran terhadap awal sebanyak 5/6 dan dilanjutkan
dengan 5/8, sehingga total pengenceran 5/6 x 5/8 = 25/48. Kemudian
26
UIN Syarif Hidayatullah Jakarta
gelombang maksimum 526 nm sesuai hasil scanning sebelumnya. Kurva standar digunakan untuk menentukan konsentrasi kolesterol yang
tersisa.
Persentase penurunan kadar kolesterol ditentukan dengan rumus :
A = X100%
C B C
Keterangan :
A = % penurunan kadar kolesterol
B = kadar kolesterol akhir dikali pengenceran 48/25
C = kadar kolesterol awal
3.3.5.6 Analisa Data
Data yang diperoleh dianalisis dengan uji Saphiro Wilk untuk melihat distribusi data dan dianalisis dengan uji Levene untuk melihat homogenitas data. Jika data terdistribusi normal dan homogenitas maka
dilanjutkan dengan uji Analysis of Variance (ANOVA) satu arah dengan taraf kepercayaaan 95% sehingga dapat diketahui apakah
perbedaan yang diperoleh bermakna atau tidak dengan nilai signifikansi
BAB 4
HASIL DAN PEMBAHASAN
4.1 Sampel Kitosan dan Iradiasi Kitosan
Kitosan yang digunakan pada penelitian ini adalah produk yang
dihasilkan oleh Pusat Aplikasi Isotop dan Radiasi (PAIR), BATAN. Bahan
baku kitosan tersebut berasal dari limbah kulit udang yang telah disortir dan
hanya diambil bagian punggungnya saja, karena bagian terbaik dari kulit
udang adalah bagian punggung yang lebih mudah diproses. Sedangkan kulit
bagian kepala ataupun kaki strukturnya lebih keras sehingga lebih susah
diproses, hal tersebut telah dibuktikan oleh pihak BATAN.
Kitin dalam cangkang udang terdapat sebagai mukopolisakarida yang
berikatan dengan garam-garam anorganik, terutama kalsium karbonat
(CaCO3), protein dan lipida termasuk pigmen-pigmen. Oleh karena itu
untuk memperoleh kitin dari cangkang udang melibatkan proses-proses
seperti pemisahan protein (deproteinasi) dengan menggunakan NaOH 1 N
dan pemisahan mineral (demineralisasi) dengan menggunakan HCl 1 N.
Sedangkan untuk mendapatkan kitosan dilanjutkan dengan proses
deasetilasi (penghilangan gugus asetil) yang dilakukan menggunakan NaOH
dengan konsentrasi 50% (b/v) selama 8 jam sambil dipanaskan pada suhu
90oC. Kitosan tersusun oleh monomer 2-amino-2-deoksi-D-glukosa dengan
ikatan glikosida pada posisi β(1,4) sehingga kitosan merupakan polimer
rantai panjang glukosamin dengan rumus molekul (C6H11NO4)n. Kitin dan
kitosan memiliki struktur yang mirip dengan selulosa, sehingga akan
menegalami degradasi bila diiradiasi (Kim, 2011).
Kitosan yang sudah diproduksi oleh BATAN tersebut kemudian
diiradiasi dengan memasukkan kitosan ke dalam alat iradiator gamma IRKA
dimana sebelumnya masing-masing kitosan sesuai dosis radiasi dikemas ke
dalam plastik klip. Iradiasi dilakukan menggunakan sumber radiasi sinar
gamma yang berasal dari sumber radiasi isotop 60Co pada dosis 50, 100, dan
150 kGy dengan kecepatan dosis 10 kGy/jam. Pemilihan dosis tersebut
28
UIN Syarif Hidayatullah Jakarta
untuk mendapatkan oligokitosan yaitu 75-100 kGy, begitu juga berdasarkan jurnal
Choi (2002) yang mengatakan bahwa dosis radiasi 100 kGy menggunakan iradiasi
gamma cukup untuk degradasi kitosan, sehingga dipilih dosis 50, 100, dan 150
kGy. Kitosan yang sudah diiradiasi mengalami pemutusan rantai pada ikatan
1,4-β-glikosida, sehingga menghasilkan kitosan iradiasi (oligokitosan) yang mempunyai BM yang lebih rendah dari kitosan tanpa iradiasi. Pemutusan rantai
kitosan pada ikatan 1,4-β-glikosida dapat dilihat pada gambar 4.1 di bawah ini.
Gambar 4.1 Pemutusan Rantai Kitosan pada Ikatan 1,4-β-glikosida
[Sumber : Kim, 2011]
4.2 Penetapan Derajat Deasetilasi Kitosan
Parameter utama yang mempengaruhi karakteristik kitosan adalah
derajat deasetilasi dan berat molekul. Derajat deasetilasi adalah persentase
banyaknya gugus asetil yang hilang dan berubah menjadi gugus amina.
Semakin besar derajat deasetilasi maka semakin banyak pula kitosan yang
terbentuk dari kitin, sehingga lebih mudah larut dalam asam encer.
Kelarutan ini disebabkan oleh adanya gugus NH2 pada posisi C-2 pada
gugus D-Glukosamin. Dengan adanya gugus NH2 tersebut membuat kitosan
bersifat polikationik sehingga dapat lebih larut dalam asam serta membuat
aplikasi penggunaan kitosan semakin luas. Metode untuk menganalisis DD
antara lain dengan cara titrasi, HPLC, IR, 1H NMR, dan 13C NMR
(Czechowska-Biskup, 2012). Spektroskopi 1H NMR merupakan salah satu
metode yang paling akurat untuk mengukur derajat deasetilasi. Derajat
deasetilasi dapat dihitung dengan menggunakan integral dari peak proton
H1 N-glukosamin, peak proton H1 N-Asetilglukosamin, dan peak dari tiga
proton pada gugus asetil (H-Ac). Berikut ini adalah beberapa formula yang
Keterangan : IH1-GlcN : integral H dari N-Glukosamin
I
H1-GlcNAc : integral H dari N-Asetilglukosamin
1
H-Ac : integral H dari Asetil
Dapat dilihat pada lampiran 6 menunjukkan bahwa hasil spektrum 1H
NMR dari kitosan hasil iradiasi dan non iradiasi. Berdasarkan dengan
melihat hasil spektrum tersebut, formula (1) dan (2) tidak dapat digunakan
karena peak pada H-Ac mengalami overlapping dengan asam asetat yang digunakan (Lavertu, 2003). Sehingga untuk perhitungan derajat deasetilasi
tersebut hanya dapat dihitung dengan menggunakan formula (3). Interpretasi
spektrum 1H NMR yang dihasilkan terhadap integral dari peak proton H1
N-glukosamin dan peak proton H1 N-AsetilN-glukosamin berdasarkan dengan
melihat gambar spektrum pada jurnal dari Czechowska-Biskup (2012) yang
memperlihatkan bahwa pada daerah sekitar 4-5 ppm terdapat integral
spesifik dari peak IH1-GlcN dan IH1-GlcNAc, yaitu daerah sekitar 4,3-4,4 ppm
merupakan peak integral dari IH1-GlcNAc dan pada daerah 4,7-4,8 ppm
merupakan peak integral dari IH1-GlcN.
Tabel 4.1 Hasil Perhitungan Derajat Deasetilasi dari Kitosan 0 dan 75 kGy
Dosis
Pada tabel 4.1 di atas menunujukkan bahwa tidak ada perbedaan yang