ANALISIS CEMARAN DAGING BABI PADA KORNET SAPI DI WILAYAH CIPUTAT DENGAN MENGGUNAKAN METODE
POLYMERASE CHAIN REACTION (PCR)
SKRIPSI
Diajukan sebagai salah satu syarat untuk memperoleh gelar Sarjana Farmasi (S.Far)
Oleh :
YOPI MULYANA 106102003439
PROGRAM STUDI FARMASI
FAKULTAS KEDOKTERAN & ILMU KESEHATAN UNIVERSITAS ISLAM NEGERI SYARIF HIDAYATULLAH
ii NAMA : YOPI MULYANA
NIM : 106102003439
JUDUL SKRIPSI : ANALISIS CEMARAN DAGING BABI PADA KORNET SAPI DI WILAYAH CIPUTAT DENGAN MENGGUNAKAN METODE POLYMERASE
CHAIN REACTION (PCR)
Disetujui oleh,
Pembimbing I Pembimbing II
Zilhadia, M.Si.,Apt. NIP: 197308222008012007
Dr. Wahyu Purbowasito NIP: 196612141986081001
Mengetahui,
Ketua Program Studi Farmasi UIN Syarif Hidayatullah Jakarta
iii
Skripsi dengan judul:
ANALISIS CEMARAN DAGING BABI PADA KORNET SAPI DI WILAYAH CIPUTAT DENGAN MENGGUNAKAN METODE
POLYMERASE CHAIN REACTION (PCR)
Telah disetujui, diperiksa dan dipertahankan di hadapan tim penguji oleh:
YOPI MULYANA NIM: 106102003439
Menyetujui,
Pembimbing
1. Pembimbing I Zilhadia, M.Si.,Apt. ...
2. Pembimbing II Dr. Wahyu Purbowasito ...
Penguji ...
1. Ketua Penguji Drs. M. Yanis Musdja, M.Sc., Apt. ...
2. Anggota Penguji I Drs. M. Yanis Musdja, M.Sc., Apt. ...
3. Anggota Penguji II Farida Sulistiawati, M.Si., APt. ...
4. Anggota Penguji III Supandi, M.Si., Apt. ...
Mengetahui,
Dekan Fakultas Kedokteran dan Ilmu Kesehatan UIN Syarif Hidayatullah Jakarta
Tanggal lulus: 14 Desember 2010
iv
Dengan ini saya menyatakan bahwa skripsi yang berjudul:
ANALISIS CEMARAN DAGING BABI PADA KORNET SAPI DI WILAYAH CIPUTAT DENGAN MENGGUNAKAN METODE
POLYMERASE CHAIN REACTION (PCR)
ADALAH KARYA SAYA SENDIRI DAN BELUM PERNAH DIAJUKAN
DALAM BENTUK APAPUN KEPADA PERGURUAN TINGGI MANAPUN.
SUMBER INFORMASI YANG BERASAL ATAU DIKUTIP DARI KARYA
YANG DITERBITKAN MAUPUN YANG TIDAK DITERBITKAN DARI
PENULIS LAIN TELAH DISEBUTKAN DALAM TEKS DAN
DICANTUMKAN DALAM DAFTAR PUSTAKA.
Jakarta, Desember 2010
v
Judul: Analisis Cemaran Daging Babi Pada Kornet Sapi di Wilayah Ciputat dengan Menggunakan Metode Polymerase Chain Reaction (PCR)
Telah dilakukan penelitian yang bertujuan untuk mengidentifikasi kandungan daging babi pada kornet sapi berdasarkan pada fragmen DNA spesifik babi. Penelitian ini menggunakan metode PCR yang sensitif untuk mengidentifikasi perbedaan suatu spesies berdasarkan keragaman DNA. Total DNA dari enam merek kornet diisolasi dengan menggunakan cell lysis buffer (Tris-EDTA pH 8 dan SDS 1% w/v). Daging babi dan daging sapi digunakan sebagai kontrol. Genom yang dihasilkan diamplifikasi dengan menggunakan masing-masing satu pasang primer yang spesifik untuk babi dan spesifik untuk sapi pada DNA mitokondria. PCR dengan menggunakan primer spesifik DNA sapi menghasilkan amplikon dengan ukuran 271 bp dan dengan menggunakan primer spesifik DNA babi menghasilkan amplikon dengan ukuran 227 bp. Metode PCR dengan menggunakan primer spesifik DNA babi dapat mengamplifikasi DNA babi hingga 0,1% daging babi dalam campuran daging babi dan daging sapi. Semua sampel kornet sapi yang diuji dengan metode PCR dapat teramplifikasi dengan menggunakan primer spesifik DNA sapi, sedangkan dengan menggunakan primer spesifik DNA babi dapat teramplifikasi satu sampel kornet.
vi
Title: Analysis of Porcine Contamination on Beef Corned in Ciputat Area by Using Method of Polymerase Chain Reaction (PCR)
Analysis of porcine on beef corned in Ciputat area by using polymerase chain reaction method has been done to identify porcine contamination in beef corned based on fragments of pig specific DNA. This research used PCR method which is sensitive in identifying different species from DNA diversity. The DNAs obtained from six corned brands were isolated by using cell lysis buffer (Tris-EDTA pH 8 dan SDS 1% w/v). In order to ensure the validity in differentiating the DNAs of pig and cow, the researcher used porcine and beef as controls. The obtained genoms were amplified by using one pair of primer which was both specific for porcine and beef in mitochondrial DNA. PCR method using specific primer of cow’s DNA resulted an amplikon at 271 bp and PCR method using specific primer of pig’s DNA resulted an amplikon at 227 bp. PCR method by using specific primer of pig’s DNA could only amplify up to 0,1% of porcine in the mixture of porcine and beef. All the sample of beef corneds tested with PCR method using specific primer of cow’s DNA could be amplified, whereas only one of the provided beef corned samples could be amplified by PCR method using specific primer of pig’s DNA.
vii
Puji dan sanjungku untuk Allah Tuhanku, yang menunjukan arah yang
benar, yang memberi petunjuk ke arah kebaikan dan hanya dari-Nya lah segala
kekuatan sehingga penulis dapat menyelesaikan skripsi ini. Shalawat serta salam
semoga tersampaikan kepada junjungan alam, nabi Muhammad SAW, seorang
rosul terpercaya, kepada keluarganya, sahabatnya, dan para pengikutnya hingga
tiba hari pembalasan.
Tulisan ini tidak akan bernilai seutuhnya, hingga orang-orang baik
membantu dan mendukung penulis dalam menyelesaikannya. Ketulusan hati
penulis untuk menuturkan terima kasih kepada orang-orang dermawan atas
bantuannya; materi, teori, ilmu, waktu dan semuanya yang begitu berharga.
Terima kasih kepada Ibu Zilhadia M.Si., Apt. selaku pembimbing I, atas
bantuan, bimbingan serta motivasinya, dan Bapak Dr. Wahyu Purbowasito, selaku
pembimbing II, atas bimbingan dan arahannya kepada penulis.
Orang baik hati yang memberikan kesempatan kepada penulis dalam
berkarya Bapak M. Yanis Musdja M.Sc., Apt. Ketua Program Studi Farmasi,
Bapak Prof. Dr. (hc) dr. M.K. Tadjudin, Sp.And. selaku Dekan Fakultas
Kedokteran dan Ilmu Kesehatan, dan Bapak Dr. Bambang Marwoto Apt., M.Eng.,
selaku kepala Balai Pengkajian Bioteknologi-BPPT yang telah mengijinkan
penulis untuk melakukan studi di Balai Pengkajian Bioteknologi-BPPT, serta
tidak lupa kepada dosen-dosen farmasi, atas ilmu dan ”sharing”nya, penulis ucapkan terima kasih.
Orang tua penulis, Bapak Mamal Kamaludin dan Ma Teti Sumaeti,
motivator terbaik di dunia ini, Kakak (A’ Aris & A’ Eko) dan Adik tercinta, Putri. Bapak Ir. H. Jonih Rahmat S.H.I., dan Ibu Hj. Sri Wardani, ’malaikat cinta’ kami di yayasan Ar-Rahmah, yang dari merekalah penulis belajar makna cinta, makna kehidupan dalam sekolah alam ini.
Istri penulis yang begitu sabar menemani perjalanan penulis menapaki
viii
Pa Imam, Pa Dudi, Bu Uli & Pa Aa), terima kasih atas bimbingannya, dan staf
Mercian, Jepang. Terima kasih atas kebaikannya selama ini.
Kakak-kakak dari biologi UI (ba’ Rerin, ba’ Ulima & ba’ Rara) dan
kakak-kakak dari Bioteknologi Al-Azhar (ba’ Driya & ba’ Wika), adik-adik
Biokimia IPB (Syifa, Ganep, Ayu, Fitri, Bowo & Helmi), juga tak lupa Keysuke, terima kasih telah mengisi hari-hari penulis selama di Biotek-Serpong.
Teman-teman yayasan Ar-Rahmah, yang centil dan menggemaskan,
meskipun sering mengesalkan, kalian adalah kebanggaan, terima kasih atas
dukungan, canda, dan pijitan-pijitannya kala lelah.
Teman yang selalu siap membantu kala sulit menghadang, lelah menerpa,
orang baik dan bijak, Syaikhul Azis dan Laukha Mahfudzoh, terima kasih atas
bantuannya selama ini. Rico, teman yang rela berkorban, Wa Mamet (Rahmat)
dan Ust. Oim (Muhammad Wali Abdurrahim), terima kasih banyak atas
bantuannya. Serta tidak lupa Alim terima kasih telah menjadi teman akhir-akhir
masa perjuangan, dan Ajeng Ayu terima kasih banyak atas bantuan dan
dukungannya.
Teman-teman Farmasi 2006, kakak kelas, adik kelas penulis, dan semua
pihak yang membantu penulis dalam menyelesaikan skripsi ini, yang tidak dapat
disebutkan satu-persatu.
Akhir kata penulis berharap semoga karya yang sederhana ini, turut
memperkaya hasanah ilmu dan juga dapat bermanfaat bagi masyarakat.
Jakarta, Desember 2010
ix
Halaman
ABSTRAK ... v
ABSTRACK ... vi
KATA PENGANTAR ... vii
DAFTAR ISI ... ix
DAFTAR TABEL ... xi
DAFTAR GAMBAR ... xii
DAFTAR LAMPIRAN ... xiii
BAB I PENDAHULUAN 1.1 Latar belakang ... 1
1.2 Perumusan Masalah ... 4
1.3 Tujuan Penelitian ... 4
1.4 Manfaat Penelitian ... 4
BAB II TINJAUAN PUSTAKA 2.1. Sel ... 6
2.2 DNA ... 7
2.2.1. Pengertian DNA ... 7
2.2.2. Ekstraksi dan purifiksi DNA ... 8
2.3 Metode PCR ... 10
2.4 Primer spesifik DNA ... 15
2.5 Desain primer DNA ... 17
2.6 DNA Mitokondria ... 18
2.7 Elektroforesis gel ... 20
BAB III KERANGKA KONSEP ... 23
BAB IV METODOLOGI PENELITIAN 4.1 Waktu dan Tempat ... 24
4.2 Alat dan Bahan ... 24
4.2.1 Alat ... 24
4.2.2 Bahan ... 25
x
4.4.1 Pengumpulan sampel ... 25
4.4.2 Isolasi DNA ... 25
4.4.2.1. Isolasi DNA dari daging segar ... 26
4.4.2.2. Isolasi DNA dari daging kornet ... 27
4.4.3 Pembuatan gel agarosa dan elektroforesis ... 30
4.4.4 Gel documentation ... 31
4.4.5 Amplifikasi PCR ... 31
4.4.6 Uji spesifikasi primer ... 32
4.4.7 Uji sensitifitas primer spesifik DNA babi ... 32
BAB V HASIL DAN PEMBAHASAN 5.1 Hasil ... 34
5.2 Pembahasan ... 39
BAB VI KESIMPULAN DAN SARAN 6.1 Kesimpulan ... 48
6.2 Saran ... 49
DAFTAR PUSTAKA ... 50
xi
Tabel 1 Efek inhibitor terhadap aktivitas taq polymerase ... 13
Tabel 2 Ukuran pemisahan molekul DNA linear pada standar gel agarosa ... 21
Tabel 3 Gradien konsentrasi campuran daging babi dan daging sapi ... 33
Tabel 4 Konsentrasi dan kemurnian hasil isolasi genom ... 55
Tabel 5 Komposisi campuran reaksi PCR ... 56
xii
Gambar 1. Sel eukariotik dan sel prokaryotik ... 6
Gambar 2. Struktur DNA ... 7
Gambar 3. Diagram skematik aplikasi isolasi DNA dengan menggunakan
metode fenol-kloroform ... 10
Gambar 4. Skematik PCR secara teoritik ... 11
Gambar 5. Tampilan skematik dari DNA mitokondria vertebrata ... 19
Gambar 6. Hasil elektroforesis isolasi genom daging babi, daging sapi, dan
campuran daging babi dan daging sapi ... 34
Gambar 7. Hasil elektroforesis produk PCR menggunakan primer spesifik
DNA sapi dan primer spesifik DNA babi pada daging segar ... 34
Gambar 8. Hasil elektroforesis isolasi genom dari daging sapi segar dan
kornet dengan berbagai perlakuan ... 35
Gambar 9. Hasil elektroforesis produk PCR daging kornet dengan berbagai
perlakuan menggunakan primer spesifik DNA sapi ... 35
Gambar 10. Hasil elektroforesis produk PCR dengan menggunakan primer
spesifik DNA sapi pada campuran daging babi dan daging sapi ... 36
Gambar 11. Hasil elektroforesisproduk PCR dengan menggunakan primer
spesifik DNA babi pada campuran daging babi dan daging sapi... 36
Gambar 12. Hasil elektroforesis isolasi genom sampel kornet ... 37
Gambar 13. Hasil elektroforesis produk PCR dengan menggunakan primer
spesifik DNA sapi pada sampel kornet ... 37
Gambar 14. Hasil elektroforesis produk PCR dengan menggunakan primer
spesifik DNA babi sampel kornet ... 38
xiii
Lampiran 1. Konsentrasi dan kemurnian hasil isolasi genom ... 55
Lampiran 2. Kondisi PCR ... 56
Lampiran 3. Komposisi campuran reaksi PCR ... 56
1 BAB I
PENDAHULUAN
1.1 Latar belakang
Indonesia dengan penduduk yang mayoritas muslim membutuhkan
jaminan kehalalan produk pangan untuk dikonsumsi. MUI dengan LP-POM
MUI berusaha memberikan ketenangan kepada masyarakat muslim
Indonesia dalam hal konsumsi pangan dengan menerapkan adanya
sertifikasi halal MUI.
Pada dasarnya, Islam mengajarkan bahwa asal sesuatu yang
diciptakan Allah adalah halal dan mubah. Tidak ada satupun yang haram,
kecuali ada nas yang sah dan tegas dari syar’i untuk mengharamkannya. Jika
tidak ada nas yang sah (misalnya karena ada sebagian hadits lemah) atau
tidak ada nas yang tegas yang menunjukkan haram, maka hal tersebut tetap
sebagaimana asalnya, yaitu mubah (Qordowi, 1993).
Sejumlah produk telah disertifikasi halal oleh MUI, termasuk produk
pangan daging. Akan tetapi, masyarakat muslim masih merasakan
ketidaktenangan dalam hal kehalalan produk daging yang biasa dikonsumsi,
karena beberapa produsen berusaha meraih keuntungan yang lebih besar
dengan menggunakan daging babi dalam produk yang tercantum
dikemasannya sebagai daging sapi.
Beberapa kasus adanya pencampuran daging babi terhadap daging
sapi baik dalam daging mentah maupun dalam produk olahan terjadi di
Indonesia. Pada tahun 2009, adanya pencampuran daging babi dalam daging
(Sholeh, 2009), di Semarang dan Jawa Tengah. Kandungan daging babi
juga ditemukan dalam dendeng sapi di kota Malang, Jawa Timur (Irawati,
2009).
Beberapa metode analisis telah dikembangkan untuk mengidentifikasi
perbedaan kandungan daging dalam suatu produk. Teknik analisis kimia
instrumen dengan menggunakan FTIR telah digunakan dalam analisis
kandungan asam lemak (Harahap, 2008). Saeed et al. (1989) telah
melakukan analisis trigliserida jenuh babi menggunakan kromatografi cair
dengan sistem reverse phase column dan deteksi Ultra Violet (UV).
Disamping itu, analisis perbedaan kandungan daging juga dilakukan dengan
menggunakan imunoelektroforesis (Necidova et al., 2002) dan imunoassay
(ELISA).
Teknik lainnya untuk mengidentifikasi kandungan daging yang
berbeda dalam suatu produk adalah dengan menggunakan metode
identifikasi molekular yang berdasarkan pada analisis DNA. Sejumlah
teknik analisis DNA telah dilakukan untuk mengidentifikasi perbedaan
komposisi DNA pada makanan daging olahan. Random Amplified
Polymorphic DNA-Polymerase Chain Reaction (RAPD-PCR) merupakan
salah satu teknik yang digunakan dalam membedakan spesies yang
dikandung dalam produk daging olahan (Calvo et al., 2001). Teknik tersebut
merupakan teknik analisis yang digunakan untuk mendeteksi DNA pada satu
jenis makhluk hidup dan kurang tepat jika digunakan untuk mendeteksi
produk makanan komersial yang terdiri dari campuran beberapa jenis daging
Metode lainnya adalah dengan menggunakan teknik Polymerase
Chain Reaction-Restriction Fragment Length Polymorphism (PCR-RFLP)
(Ong et al., 2007; Novianingsih, 2008; Lenstra et al., 2001) dan dengan
menggunakan primer spesifik DNA terhadap informasi genetik dari suatu
spesies tertentu (Ilhak et al., 2006; Abdullah, 2008; Kesmen et al., 2009;
Calvo et al., 2001; Walker et al., 2002). Metode analisis dengan
menggunakan DNA memiliki beberapa keuntungan, yaitu pertama, DNA
dapat ditemukan di semua tipe sel pada suatu individu dengan informasi
genetik yang identik. Kedua, DNA merupakan molekul yang stabil dalam
proses ekstraksi dan analisis DNA sangat mungkin dikerjakan dari beberapa
tipe sampel yang berbeda (Jain, 2004).
Analisis PCR menggunakan primer spesifik DNA dengan
memanfaatkan urutan DNA mitokondria merupakan metode yang umum
digunakan saat ini untuk mengidentifikasi spesies tertentu (Abdullah et al.,
2008; Kesmen et al., 2009; Calvo et al., 2001; Ilhak et al., 2001).
Penggunaan DNA mitokondria dalam analisis PCR dapat meningkatkan
sensitifitas, karena setiap sel memiliki sekitar seribu mitokondria dan setiap
mitokondria memiliki sepuluh salinan DNA. Sehingga, terdapat sekitar
sepuluh ribu salinan DNA mitokondria dalam sel (Jain, 2004).
Penelitian ini bertujuan untuk mengidentifikasi terdapat tidaknya
kandungan daging babi dalam produk kornet yang dijual di wilayah Ciputat
menggunakan teknik PCR dengan primer spesifik DNA yang didasarkan
pada informasi DNA mitokondria. Dengan menggunakan primer spesifik
vitro dengan menggunakan mesin PCR, hasil amplifikasi diidentifikasi
dengan menggunakan elektroforesis gel, sehingga akan terlihat pita DNA
sesuai dengan ukuran panjang DNA yang diamplifikasi. Pita ini
dibandingkan dengan pita DNA dari daging babi dan daging sapi sebagai
pembanding.
1.2 Rumusan masalah
1. Bagaimanakah kondisi optimal isolasi DNA pada kornet sapi?
2. Bagaimanakah kondisi optimal untuk amplifikasi primer spesifik DNA
babi sehingga menghasilkan produk PCR?
3. Apakah reaksi PCR dengan menggunakan primer spesifik DNA babi
dapat mengamplifikasi DNA pada kornet sapi?
1.3 Tujuan penelitian
1. Menentukan kondisi optimal dalam proses isolasi DNA pada kornet
sapi.
2. Menentukan kondisi optimal dalam proses PCR untuk menghasilkan
produk PCR yang dapat digunakan sebagai dasar analisis cemaran
kandungan daging babi pada produk pangan kornet.
3. Mendeteksi adanya kandungan daging babi dalam kornet yang dijual di
wilayah Ciputat dengan menggunakan teknik PCR.
1.4 Manfaat Penelitian
Manfaat dari penelitian ini adalah untuk memberikan informasi
kepada masyarakat tentang keamanan dan kehalalan produk makanan yang
kornet, sehingga masyarakat lebih berhati-hati dan bijaksana dalam
6 BAB II
TINJAUAN PUSTAKA
2.1. Sel
Sel merupakan unit terkecil dari makhluk hidup, dalam arti bahwa sel
dapat hidup tanpa kehadiran sel yang lain. Di alam, sel dapat dibagi ke dalam
dua kelompok, yaitu prokariotik (sel bakteri) dan eukariotik. Sel prokariotik
pada umumnya memiliki ukuran yang lebih kecil dengan struktur sederhana,
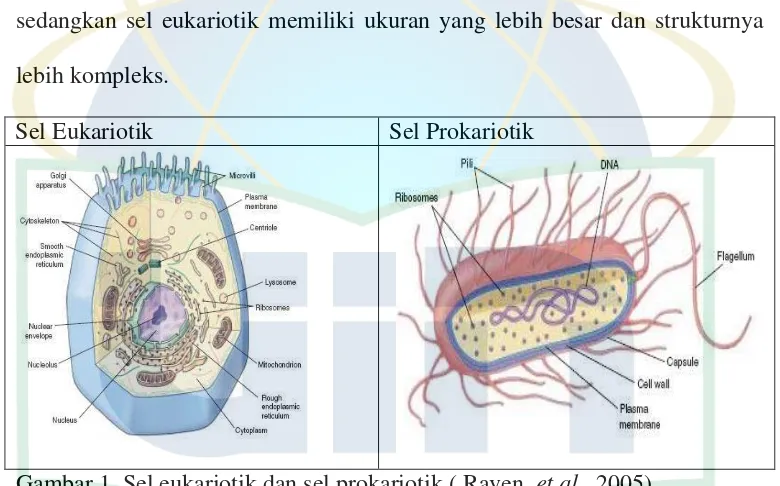
sedangkan sel eukariotik memiliki ukuran yang lebih besar dan strukturnya
lebih kompleks.
[image:20.595.128.518.275.518.2]Sel Eukariotik Sel Prokariotik
Gambar 1. Sel eukariotik dan sel prokariotik ( Raven, et al., 2005)
Perbedaan utama antara sel prokariotik dan sel eukariotik adalah
terletak pada lokasi materi genetiknya (DNA). DNA prokariotik tidak
dibatasi oleh membran inti, sedangkan pada sel eukariotik dibatasi oleh
2.2. DNA
2.2.1. Pengertian DNA
DNA merupakan polimer linear rantai panjang yang terdiri atas
nukleotida. Nukleotida yaitu unsur pembangun asam nukleat yang
mengandung satu gugus fosfat, gula, dan sebuah basa purin atau
pirimidin (molekul-molekul berbentuk cincin pipih mengandung
nitrogen dan karbon). Jika nukleotida-nukleotida itu tersambung dalam
jumlah besar disebut polinukleotida (Watson et al.,1988).
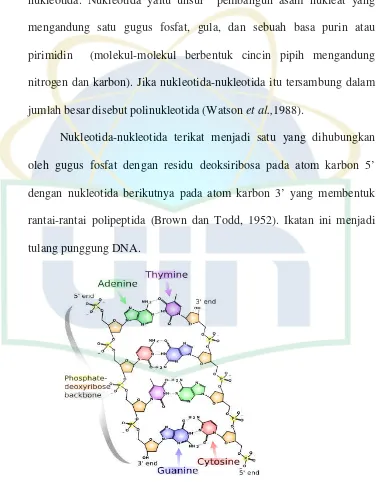
Nukleotida-nukleotida terikat menjadi satu yang dihubungkan
oleh gugus fosfat dengan residu deoksiribosa pada atom karbon 5’
dengan nukleotida berikutnya pada atom karbon 3’ yang membentuk
rantai-rantai polipeptida (Brown dan Todd, 1952). Ikatan ini menjadi
[image:21.595.135.511.175.657.2]tulang punggung DNA.
Gambar 2. Struktur DNA (http://www.websters-online-dictionary.org)
DNA terdiri dari basa purin (adenosin dan guanin) dan pirimidin
sedangkan jumlah guanin sama dengan jumlah sitosin (Chargaff, 1951).
Masing-masing basa purin dan pirimidin dihubungkan oleh ikatan
hidrogen. Meskipun ikatan-ikatan hidrogen ini sangat lemah, namun
setiap nukleotida mengandung begitu banyak basa sehingga
rantai-rantai komplementernya tidak pernah terpisah secara spontan pada
kondisi fisiologis. Akan tetapi, jika DNA terkena pengaruh suhu yang
mendekati titik didih, maka banyak pasangan DNA yang putus sehingga
heliks gandanya terbelah menjadi rantai-rantai komplementernya
(denaturasi) (Watson dan Crick, 1953).
Proses denaturasipun dapat dipengaruhi oleh pH yang ekstrim
(pH<3 atau pH>10). Namun proses denaturasi ini dapat kembali lagi
pada posisi normal (renaturasi) membentuk heliks-heliks ganda asal jika
kondisi dikembalikan kepada suhu subdenaturasi (mendekati 600
2.2.2. Ekstraksi dan Purifikasi DNA
C)
(Marmur dan Lane, 1958). Akan tetapi proses renaturasi dapat menjadi
tidak sempurna jika suhu tidak begitu mengikat atau suhu lebih rendah
(Marmur et al., 1958).
DNA (Deoxyribonucleic Acid) pada organisme tingkat tinggi
seperti manusia, hewan dan tumbuhan terdapat di dalam inti sel, dan
beberapa organel lain di dalam sel, seperti mitokondria (DNA
mitokondria) dan kloroplas. Ekstraksi DNA dari organisme eukariot
dilakukan dengan melalui proses penghancuran dinding sel (lysis of cell
DNA (precipitation of DNA) dan pemanenan. (Sulandari, S., dan Arifin,
M.S.Z., 2003).
Secara umum, kualitas DNA dapat ditentukan oleh keberadaan
kontaminasi RNA, protein, lipid, dan konstituen sel lainnya yang
berhubungan dengan enzim restriksi, ligase, dan DNA polimerase
termostabil. Yang lebih penting adalah preparasi harus terbebas dari
DNA nuklease yang dapat merusak DNA (Merante et al., 1998).
Metode yang biasa digunakan untuk melisiskan sel adalah dengan
menggunakan buffer yang mengandung satu atau lebih deterjen,
contohnya SDS (B), NP-40, atau Triton X-100. Setelah hancur, residu
dari protein dan lipid dapat dihilangkan dengan menggunakan fenol dan
kloroform. Isoamil alkohol dapat digunakan untuk membantu
pemisahan fase air dan fase organik. Dengan perbandingan
masing-masing fenol, kloroform, dan isoamil alkohol sebesar 25:24:1 (Burden
dan Whitney, 1995; Mülhardt, 2007). Secara skematik, aplikasi isolasi
DNA dengan menggunakan metode fenol-kloroform dapat dilihat pada
gambar 3.
Berbagai teknik ekstraksi telah dikembangkan dari prinsip dasar
tersebut, sehingga saat ini muncul teknik ekstraksi dan purifikasi DNA
dalam bentuk kit. Prinsip dasar ekstraksi DNA adalah serangkaian
proses untuk memisahkan DNA dari komponen sel lainnya. Hasil
Gambar 3: Diagram skematik aplikasi isolasi DNA dengan menggunakan metode fenol-kloroform (Marante et al., 1998)
2.3. Metode PCR
Polymerase Chain Reaction (PCR) merupakan metode untuk
mengamplifikasi primer dari urutan DNA secara spesifik dengan
menggunakan media enzimatik (Kolmodin dan Birch, 2002) dan sangat
mudah terkontaminasi baik dari luar mesin PCR ataupun dari bahan
amplifikasi sebelumnya (McDonagh, 2003). Kualitas dan spesifitas
amplifikasi dengan menggunakan PCR bergantung pada kondisi
amplifikasinya yaitu (1) program siklus amplifikasi (suhu, primer,
nukleotida, polymerase, konsentrasi magnesium, waktu dan jumlah siklus),
[image:24.595.125.509.96.544.2]alamiah target DNA sampel (untai tunggal/single stranded atau untai
ganda/double stranded) (Committee on DNA Technology in Forensic
Science, 2002).
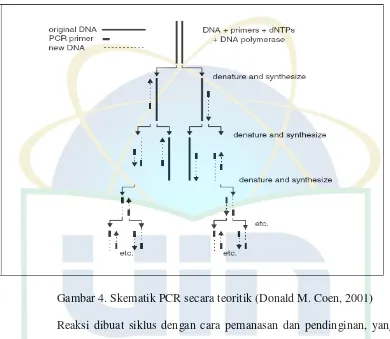
[image:25.595.115.505.166.505.2]
Gambar 4. Skematik PCR secara teoritik (Donald M. Coen, 2001)
Reaksi dibuat siklus dengan cara pemanasan dan pendinginan, yang
mencakup terjadinya denaturasi template, penempelan primer (annealing)
dan elongasi fragmen DNA spesifik. Tahap denaturasi berlangsung dengan
cepat pada suhu 94-950 C, sedangkan penempelan primer bergantung pada
Tm (melting temperature) dari primer template hybrid. Dalam
Masing-masing siklus, fragmen target akan meningkat secara eksponensial. Setelah
35 siklus ribuan fragmen yang dikopi akan didapatkan. Untuk menganalisis
DNA spesifik hasil dari PCR, dapat menggunakan elektroforesis yang
untuk mendeteksi struktur primer DNA. Selain itu, sequensing juga dapat
digunakan untuk mengetahui terjadinya mutasi (Crocker, 2003).
Untuk memprediksi Tm dari primer, pengaturan konsentrasi primer
dan konsentrasi keseluruhan garam biasanya dengan menggunakan software,
sedangkan untuk mendapatkan suhu terbaik dalam proses annealing adalah
dengan cara optimasi. Kebanyakan template mengalami proses elongasi
pada suhu 720
Berikut adalah komponen penting dalam PCR (Sambrook dan
Russel, 2001).
C (Kolmodin, 2002).
1. DNA polymerase termostabil yang mengkatalisis sintesis DNA
Terdapat banyak enzim yang dapat digunakan untuk mengkatalisis
sintesis DNA. Yang paling banyak digunakan adalah taq polymerase
(0,5-2,5 unit per standar reaksi 2,5-50 µl). Standar PCR mengandung
2x1012 sampai 10x1012 molekul enzim. Enzim menjadi berkurang
ketika produk yang diamplifikasi mencapai nilai akumulasi 1,4x1012
hingga 7x1012
Taq polymerase merupakan DNA polymerase yang diisolasi dari
bakteri Thermus aquaticus. Beberapa enzim yang serupa dapat diisolasi
dari organisme thermophilic lain. termasuk Thermus thermophilus, Th.
flaws, Th. litoralis, Pyrococcus furiosus, dan Bacillus
stearothermophilus. .
Taq polymerase telah diisolasi dari Th. aquaticus dengan
beberapa strain yang berbeda, dan masing-masing memiliki
adalah strain YT-1 yang pada saat ini dapat dihasilkan dari klon
rekombinan (Weir, 1993).
Aktifitas enzim bergantung pada kation ion bivalen. Konsentrasi
optimum MgCl2 adalah 2 mM. laju polimerisasi maksimum dihasilkan
dengan 0,7-0,8 mM dNTPs. Inhibisi substrat diamati pada konsentrasi
dNTPs 4-6 mM. Kation monovalen juga memiliki efek terhadap
aktifitas enzim. Kondisi optimum adalah 50 m/V KCl, dimana inhibisi
[image:27.595.137.509.247.681.2]terjadi pada konsentrasi >75 n%V KC1. NaCl, NH4Cl, dan NH4
Tabel 1. Efek inhibitor terhadap aktifitas taq polymerase I
asetat
tidak dapat menggantikan KCl tanpa penurunan aktifitas yang spesifik.
Bahan pendenaturasi seperti deterjen dan pelarut dalam konsentrasi
yang rendah dapat ditoleransi oleh taq polymerase (Landgraf dan
Wolfes, 1993).
Sumber: Landgraf , A., Wolfes, H., (1993) dalam Enzymes of Molecular biology
Inhibitor Konsentrasi Aktivitas
UREA <0.5 M 100
1 O M 118
1.5 M 107
2.O M 82
SDS 0.001 % 105
0.01 % 10
0.1 % <01
Etanol <3 % 100
10 % 110
DMSO <l % 100
10 % 53
20 % 110
DMF <5 % 100
10 % 82
2. Sepasang Oligonukleotida Primer
Kehati-hatian dalam desain primer dibutuhkan untuk menghasilkan
produk yang diinginkan. Primer memberikan pengaruh yang besar pada
kesuksesan pengerjaan PCR. Reaksi standar mengandung jumlah primer
yang terbatas, khususnya 0,1-0,5 µM pada masing-masing primer
(6x1012 sampai 3x1013
3. Deoksinukleosida Trifosfat (dNTPs)
molekul). Jumlah ini cukup untuk 30 siklus
amplifikasi untuk 1 kb segmen DNA. Dalam jumlah yang lebih besar
akan mengakibatkan mispriming, yang membuat amplifikasi yang tidak
spesifik.
PCR standar mengandung jumlah dATP, dTTP, dCTP dan dGTP
yang equimolar. Konsentrasi 200-250 µM dari masing-masing dNTP,
direkomendasikan untuk taq polymerase dalam reaksi yang mengandung
1,5 mM MgCl2
4. Kation Divalen
. Jumlah tersebut harus menghasilkan ∼6-6,5 µg DNA dalam 50 µl, yang cukup sama untuk reaksi multipleks delapan pasang
primer atau lebih yang digunakan pada waktu yang sama.
Semua taq polymerase membutuhkan kation divalen bebas
(biasanya Mg2+ ) untuk aktifitasnya. Ion kalsium cukup menginaktifkan
polymerase, karena dNTPs dan oligonukleotida berikatan dengan Mg2+.
Konsentrasi molar kation harus melebihi konsentrasi molar gugus fosfat
yang disumbangkan oleh dNTPs dan primer. Untuk itu, tidak mungkin
direkomendasikan konsentrasi optimal dari Mg2+ dalam semua kondisi,
kasus, peningkatan konsentrasi mg2+
5. Buffer
hingga 4,5 atau 6 mM dapat
menurunkan nonspesifik priming.
Tris-Cl disesuaikan pada pH antara 8,3 hingga 8,8 pada suhu
ruang, yang dimasukan ke dalam standar PCR pada konsentrasi 10 mM.
ketika diinkubasi pada suhu 720
6. Kation Monovalen
C (suhu yang biasa digunakan untuk fase
ekstensi PCR), pH campuran turun menghasilkan buffer dengan pH ∼7,2.
Buffer PCR standar mengandung 50 mM KCl yang bekerja baik
untuk mengamplifikasi segmen DNA yang panjangnya >500 bp. Dengan
menaikan konsentrasi KCl hingga ∼70-100 mM seringkali dapat
meningkatkan hasil dari segmen DNA yang pendek.
7. Template DNA
Template DNA mengandung urutan target yang akan ditambahkan
pada PCR dalam bentuk single strand atau double strand. Amplifikasi
Template DNA sirkular sangat tidak efisien dibandingkan dengan DNA
linear.
2.4. Primer spesifik DNA
Dengan menggunakan teknik DNA rekombinan telah dihasilkan klon
DNA “spesies spesifik” dan dapat digunakan sebagai DNA probe untuk
mendeteksi spesies tertentu dalam suatu produk daging olahan. Ada
beberapa pendekatan yang dapat digunakan untuk mengembangkan pelacak
teknik PCR, saat ini merupakan salah satu cara yang relatif dapat dilakukan.
Pengembangan penanda spesifik gen dengan memanfaatkan informasi dari
database yang diakses dari internet.
Dua dari tiga puluh tiga produk makanan yang berlabel halal di Saudi
Arabia dideteksi oleh Abdullah (2008) dengan menggunakan primer spesifik
DNA babi dan terbukti mengandung cemaran daging babi. Calvo et al.
(2001) telah mengembangkan metode PCR dalam mendeteksi kandungan
babi dalam produk daging yang telah dipanaskan dan daging yang belum
dipanaskan. Isolasi DNA spesifik babi dilakukan secara berulang, setelah
dianalisis hasil urutan secara berulang, sepasang primer disintesis. Untuk
memastikan efektifitas dan spesifisitas, pengujian dilakukan terhadap 55
sampel DNA dari darah babi yang berasal dari peternakan yang berbeda dan
menunjukan hasil yang positif. Sedangkan sebanyak 200 sampel dengan
spesies yang berbeda, menunjukan hasil yang negatif.
Urutan primer dapat dibuat dengan menggunakan software komputer.
Urutan nukleotida dianalisis BLAST untuk menentukan daerah-daerah
terkonservasi, dan urutan nukleotidanya dikonfirmasi. Dua diantara daerah
tersebut dipilih untuk dasar merancang sepasang primer. Perancangan ini
dapat dilakukan dengan program primer3 secara online ataupun secara
semimanual dengan memperhatikan parameter-parameter yang umum,
antara lain jumlah nukleotida, kandungan GC 50% atau lebih (Santoso,
2.5. Desain primer DNA
Pemilihan primer dalam PCR menentukan efisiensi dan spesifisitas
PCR. Tujuan dari desain primer adalah spesifitas yang dihasilkan hanya
ketika masing-masing bagian pasang menempel dengan stabil pada target
urutan dalam template DNA (Sambrook dan Russel, 2001). Primer akan
menempel pada daerah spesifik dan menjadi inisiasi perpanjangan dan
penanda akhir dari daerah yang dipilih. Pemilihan primer berhubungan
dengan Tm (melting temperature) yaitu suhu pada saat untai DNA terpecah
menjadi setengah untai tunggal dan setengahnya lagi untai ganda. Tm
mencirikan stabilitas bentuk DNA hybrid, karenanya Tm menjadi pusat
parameter dalam desain primer. Tm dipengaruhi oleh panjang primer, urutan
primer, konsentrasi garam, konsentrasi primer, dan ada tidaknya agen
denaturasi (denaturan) (Chen, 2002).
Mulhardt (2007) dalam bukunya Molecular Biology and Genomics,
The Experimenter Series menyatakan bahwa ada beberapa persamaan yang
dapat digunakan untuk memperkirakan Tm, dengan menggunakan varian
yang sederhana, Tm dari komponen GC primer dapat diperkirakan dengan
menggunakan persamaan berikut:
Tm = 4×(nomor G atau C)+2×(nomor A atau T)
persamaan ini hanya dapat digunakan untuk primer yang pendek dengan
panjang sekitar 20 basa.
Primer dengan komposisi G+C yang tinggi (GC %) memiliki Tm
memiliki dua ikatan hidrogen. Tm primer biasanya meningkat sesuai
dengan panjangnya.
Berikut adalah langkah-langkah pemilihan primer (Sambrook dan Russel,
2001).
a. Analisis gen target untuk priming site yang potensial
b. Membuat daftar yang memungkinkan untuk forward dan reverse
c. Memilih pasangan yang terbaik dari forward dan reverse primer
yang sama komposisi G+C nya
2.6. DNA Mitokondria
Mitokondria memiliki diameter 1–2 μm dan mengandung berm
acam-macam salinan DNA yang berbentuk sirkular. Jumlah dan bentuk
mitokondria berbeda-beda untuk setiap sel dengan tipe yang berbeda dan
dapat berubah. Rata-rata sel eukariotik mengandung 103-104 salinan
mitokondria (Passarge, 2007), karena DNA mitokondria diekspresikan
dalam spesies atau gen yang berbeda setelah mengalami evolusi (Kumari,
2007).
Ukuran genom mitokondria hewan berkisar 14000-39000 pasang
basa. Ukuran genom mitokondria minimum untuk berfungsinya mitokondria
hewan multiseluler adalah 14000 pasang basa. DNA mitokondria merupakan
DNA rantai ganda yang berbentuk sirkular. Ukuran DNA mitokondria relatif
sangat kecil dibandingkan dengan ukuran genom intinya. Karena ukuran
genomnya yang relatif kecil ini, maka genom ini dapat dipelajari secara
mitokondria secara luas telah digunakan untuk mempelajari evolusi genetik,
karena mudah didapatkan, memiliki laju evolusi yang cepat, dan secara
umum mengikuti pola keturunan (Kumari, 2007).
Lockley dan Bardsley (2000) dalam Kumari (2007) menyatakan
bahwa hewan memiliki DNA mitokondria berbentuk sirkular dengan ukuran
kecil (15-20 kb), terdiri dari 37 gen yang menyandi tRNAs, 2 rRNAs, dan
13 mRNAs. mRNAs merupakan gen penyandi protein, terutama
menyangkut transpor elektron dan fosforilasi oksidatif mitokondria.
DNA mitokondria hewan secara umum memiliki jumlah dan jenis gen
yang sama, yaitu 13 daerah yang mengkode protein (URF1, URF2, URF3,
URF4, URF5, URF6, URFA6L, URF4L, Cytochrome Oxidase unit I,
Cytochrome Oxidase unit II, Cytochrome Oxidase unit III, Cytochrome b
danATPase 6); 2 gen pengkode rRNA yaitu 12S rRNA dan 16S rRNA; 22
[image:33.595.133.513.182.667.2]gen pengkode tRNA (Solihin, 1994).
Genom mitokondria disusun dengan efisien, tidak memiliki intron,
memiliki wilayah intergenik yang kecil yang membuat pembacaan frame
seringkali mengalami tumpang tindih (overlap) (Lockley and Bardsley,
2000).
2.7. Elektroforesis gel
Elektroforesis merupakan teknik yang sederhana, cepat dan dapat
dilakukan untuk memisahkan fragmen DNA yang tidak dapat dipisahkan
dengan menggunakan prosedur lain. Selain itu, lokasi DNA di dalam gel
dapat ditentukan secara langsung melalui bercak warna fluoresens yang
berinterkalasi dengan konsentrasi yang rendah (Sambrook dan Russel,
2001).
Gel agarosa merupakan metode yang sederhana dan efektif untuk
memisahkan dan mengidentifikasi fragmen DNA dengan panjang 0,5-25 kb.
Agarosa dilarutkan dalam buffer dengan pemanasan hingga terlarut,
kemudian dimasukan ke dalam wadah cetakan gel yang telah tersedia sisir
untuk meletakan sampel, dalam waktu yang tidak lama, agarosa akan
mengeras, dan gel yang terbentuk ditempatkan dalam wadah laju migrasi
(flow-migration chamber), buffer elektroforesis ditambahkan hingga gel
terendam oleh larutan buffer. DNA dimasukan ke dalam sumur, dan arus
dialirkan (biasanya 50 dan 150 volt). Setelah DNA bergerak dengan jarak
yang cukup, gel ditandai dengan pewarnaan dan diamati dengan
Agarosa merupakan polimer linear yang mengandung residu D- dan L-
galaktosa yang digabung oleh α-(13) dan β-(1-4) glycoside, yang berasal
dari rumput laut. Rantai agarosa berbentuk serat helik yang berkumpul
menjadi struktur yang melingkar (supercoil) dengan jari-jari 20-30 nm.
Elatin dari agarosa dihasilkan dalam mesh tiga dimensi yang diameternya 50
nm hingga >200 nm (Sambrook dan Russel, 2001).
Faktor-faktor yang menentukan jarak migrasi DNA melalui gel
agarosa (Sambrook dan Russel, 2001).
1. Ukuran molekul DNA
Molekul besar berpindah lebih lambat karena membutuhkan usaha
yang besar dan kurang efisien melewati pori-pori gel dibandingkan
dengan molekul yang kecil.
2. Konsentrasi agarosa
Fragmen DNA linear memberikan jarak perpindahan yang berbeda
melalui gel yang mengandung konsentrasi yang berbeda.
Tabel 2. Ukuran pemisahan molekul DNA linear pada standar gel agarosa
Konsetrasi agarosa (% [w/v])
Jarak pemisahan DNA linear (kb)
0,3 5-60
0,6 1-20
0,7 0,8-10
0,9 0,5-7
1,2 0,4-6
1,5 0,2-3
2,0 0,1-2
[image:35.595.137.517.184.691.2]3. Konformasi DNA
DNA bentuk I (superhelical circular), bentuk II (nicked circular)
dan bentuk III (linear) berpindah melalui gel agarosa pada jarak yang
berbeda. Pergerakan relatif dari ketiga bentuk utamanya bergantung pada
konsentrasi dan tipe agarosa yang digunakan, selain itu dipengaruhi juga
oleh kekuatan arus listrik yang digunakan, kekuatan buffer ionik dan
bentuk superhelical dari DNA bentuk I. Pada beberapa kondisi, DNA
bentuk I lebih cepat daripada DNA bentuk III, tetapi pada kondisi yang
lain DNA bentuk III lebih cepat daripada DNA bentuk I.
4. Voltase yang digunakan
Perpindahan molekul DNA di dalam gel dirangsang oleh arus
listrik yang mengalir dari kutub negatif menuju kutub positif. Pada
voltase rendah, DNA linear mengalami perpindahan secara proporsional.
Semakin besar tegangan arus listrik, maka perpindahan molekul DNA
semakin cepat, demikian pula sebaliknya. Untuk mencapai resolusi
maksimum dari fragmen DNA dengan ukuran >2 kb, gel agarosa harus
dijalankan tidak boleh lebih dari 5-8 V/cm.
5. Tipe agarosa
Terdapat dua tipe utama dari agarosa yaitu agarosa standar dan
agarosa pada suhu rendah (low-melting temperature).
6. Buffer elektroforesis
Mobilitas elektroforesis DNA dipengaruhi oleh komposisi dan
23
KERANGKA KONSEP
Daging kornet sapi
Cek dengan PCR
+ mengandung DNA babi
- tidak mengandung DNA babi • Isolasi DNA
Cek hasil isolasi DNA dan identifikasi produk
PCR dengan menggunakan elektroforesis
Set primer spesifik
Gel Documentation
Apakah mengandung DNA babi??
• Optimasi Isolasi DNA
pada daging segar
• PCR
• Optimasi kondisi PCR
pada daging segar
24 BAB IV
METODOLOGI PENELITIAN
4.1. Waktu dan Tempat
Penelitian ini dilaksanakan di Laboratorium Teknologi Gen, Balai
Pengkajian Bioteknologi-BPPT Serpong, Tangerang. Waktu pelaksanaan
dari bulan Juni 2010 hingga Oktober 2010.
4.2. Alat dan Bahan
4.2.1. Alat
Alat yang digunakan adalah mortar, pestle, pipet mikro
0,1--2 μl, 2-20 μl, 20-200 μl, 100-1000 μl [Finnpipette, BIO-RAD,
Nichiryo, BenchMate], tip 10 μl, 100 μl dan 1000 μl [Sorenson],
freezer -20° C [Angelantoni Scientifica], lemari pendingin 4° C
[Glacio-TOSHIBA], mesin PCR [TaKaRa & BIO-RAD],
thermostat & shaking bath [Heto], tabung sentrifugasi 15 ml
[Iwaki, Corning, FALCON, BIOLOGIX], tabung mikrosentrifugasi
1,5 ml [Sorenson], tabung mikrosentrifugasi 200 μl [Axygen], rak
tabung, mesin sentrifugasi [Beckman J2-HS & Tomy], timbangan
[Mettler], ice maker [HOSHIZAKI], vorteks [Heidolph], magnetic
stirrer [Heidolph MR3001], inkubator [memmert], microwave
[National], heat block [Thermolyne], spatula, gunting,
elektroforesis tray [Bio-rad], chamber elektroforesis [Mupid2],
comb, gel documentation, dan spektrofotometer Nano Drop
ND-1000. Alat gelas yang digunakan adalah gelas ukur, labu
dan tabung penyimpanan bahan (50 ml, 100 ml, 250 ml & 500 ml)
[Schott-DURAN].
4.2.2. Bahan
Bahan yang digunakan dalam penelitian ini adalah daging
babi, daging sapi dan produk kornet sapi yang dijual di wilayah
Ciputat. Bahan lain yang digunakan yaitu TE (Tris-Cl & EDTA)
pH 8,0, etanol 70%, isopropanol, NaCl 5 M, DNase-free RNase,
Proteinase K, buffer PCR Fast Star Taq DNA Polymerase (Roche),
agarosa, buffer 1xTAE, sybr safe 1x, loading dye dan ddH2
4.3. Tahapan Penelitian
O.
1. Pengumpulan sampel
2. Isolasi DNA sampel dan pembanding
3. Amplifikasi DNA
4. Pembuatan gel agarosa dan elektroforesis
5. Identifikasi hasil PCR dengan menggunakan elektroforesis
6. Dokumentasi gel
4.4. Prosedur Kerja
4.4.1. Pengumpulan sampel
Sampel kornet sapi dikumpulkan dari semua merek yang beredar
di wilayah Ciputat dengan jumlah sampel sebanyak 6 merek produk
kornet sapi dengan produsen yang berbeda.
4.4.2. Isolasi DNA
Proses isolasi DNA pada daging berbeda antara isolasi DNA pada
disebabkan adanya senyawa tambahan pada daging kornet sehingga
memerlukan proses optimasi.
4.4.2.1. Isolasi DNA pada daging segar
DNA pada daging segar diisolasi dari daging sapi, daging
babi dan campuran daging babi dan daging sapi. Campuran
daging sapi dan daging babi ini digunakan untuk menguji
sensitifitas primer spesifik babi.
Proses isolasi DNA pada daging segar adalah sebagai berikut:
Sebanyak 500 mg daging dihaluskan, kemudian dimasukkan ke
dalam tabung sentrifugasi 15 ml, ditambahkan 8 ml cell lysis
buffer (Tris-EDTA pH 8 dan SDS 1% w/v), ditambahkan 5 µl
proteinase K dan diinkubasi pada suhu 550 C selama 16-18 jam.
Selanjutnya, campuran ditambahkan 5 µl RNAse, kemudian
diinkubasi selama 1 jam pada suhu 370 C. Sebanyak 750 µl dari
campuran tersebut dipindahkan ke dalam tabung sentrifugasi 1,5
ml dan kemudian disentrifugasi pada kecepatan 12000 rpm selama
10 menit. Supernatan yang terbentuk ditambahkan 300 µl natrium
klorida 5 M yang kemudian dihomogenkan dan disentrifugasi
pada kecepatan 12000 rpm selama 10 menit. Supernatan yang
terbentuk dipisahkan kemudian ditambah dengan 750 µl
kloroform-isoamilalkohol (24:1), kemudian dihomogenkan dan
disentrifugasi pada kecepatan 12000 rpm selama 5 menit. Setelah
itu supernatan dipisahkan dan ditambahkan isopropanol (equal
disentrifugasi pada kecepatan 12000 rpm, supernatan yang
terbentuk dibuang, pelet ditambahkan dengan 600 µl etanol 70%,
dihomogenkan dan disentrifugasi pada kecepatan 12000 rpm
selama 10 menit. Supernatan yang terbentuk dibuang, DNA
dikeringkan dalam desikator selama 10 menit kemudian
ditambahkan buffer TE 30 µl. Keberadaan DNA dicek dengan
menggunakan elektroforesis dan konsentrasinya dicek dengan
menggunakan spektrofotometri nanodrop 1000. DNA yang telah
dilarutkan buffer TE disimpan pada suhu -200
4.4.2.2. Isolasi DNA pada kornet
C untuk PCR.
• Preparasi sampel
Untuk mendapatkan DNA dari daging kornet,
diperlukan preparasi pada sampel, sehingga senyawa
tambahan yang terdapat di dalam produk kornet tidak
mengganggu proses isolasi DNA. Proses preparasi yang
dilakukan adalah dengan menggunakan pencucian dan
pemanasan. Proses ini merupakan serangkaian cara untuk
memisahkan senyawa tambahan, yang nantinya hanya akan
digunakan satu proses preparasi terbaik sebagai metode
terpilih dan digunakan dalam proses isolasi DNA pada
sampel.
- Pencucian
Masing-masing sebanyak 1 gr daging kornet
berbeda, kemudian ditambahkan dengan pelarut yang
berbeda kepolarannya untuk setiap tabung. Pelarut
yang digunakan yaitu pelarut polar (air) pada tabung
pertama dan pelarut non polar (n-heksan) pada tabung
kedua. Daging ditiriskan, kemudian masing-masing
dihaluskan. Daging yang sudah halus hasil pencucian
kemudian ditambahkan cell lysis buffer untuk isolasi
DNA.
- Pemanasan
Sebanyak 1 gr daging kornet dihaluskan, kemudian
diletakan di atas kertas saring dengan diameter 10 cm.
Daging tersebut dipanaskan pada suhu ± 700
• Isolasi DNA
C selama
15 menit. Dengan pemanasan ini diharapkan lemak
akan mencair dan terserap oleh kertas saring. Hasil
pemanasan ini kemudian ditambahkan cell lysis buffer
untuk isolasi DNA.
Masing-masing sebanyak 1 gr daging kornet dari hasil
perlakuan (pencucian dan pemanasan) dimasukan ke dalam
tabung sentrifugasi 15 ml dan ditambahkan 8 ml cell lysis
buffer (Tris-EDTA pH 8 dan SDS 1% w/v), kemudian
ditambahkan 5 µl proteinase K dan diinkubasi pada suhu 550
C selama 16-18 jam. Selanjutnya ditambahkan 5 µl RNAse,
pada kecepatan 8000 rpm selama 10 menit, supernatan yang
terbentuk ditambahkan 4 ml natrium klorida 5 M,
dihomogenkan kemudian disentrifugasi pada kecepatan 8000
rpm selama 10 menit. Supernatan yang didapat dipisahkan
dan ditambahkan dengan 4 ml kloroform-isoamilalkohol
(24:1), dihomogenkan kemudian disentrifugasi pada
kecepatan 8000 rpm selama 5 menit. Selanjutnya supernatan
dipisahkan dan ditambahkan dengan isopropanol (equal
volume), dihomogenkan dan diinkubasi selama semalam
pada suhu -200 C. Campuran disentrifugasi pada kecepatan
8000 rpm, kemudian supernatan dibuang, pelet ditambahkan
dengan 500 µl buffer TE. Larutan DNA yang didapatkan
dipindahkan ke dalam tube 1,5 ml, kemudian ditambahkan
dengan 400 µl kloroform-isoamilalkohol (24:1) dan
disentrifugasi pada kecepatan 12000 rpm selama 5 menit.
Penambahan kloroform-isoamilalkohol ini diulangi sebanyak
2 kali, setelah itu supernatan yang dihasilkan ditambahkan
dengan isopropanol (equal volume), diinkubasi selama 30
menit dan disentrifugasi pada kecepatan 12000 rpm, pelet
yang dihasilkan ditambah dengan 200 µl etanol 70%,
dihomogenkan dan disentrifugasi pada 12000 rpm selama 10
menit. Supernatan dibuang, DNA dikeringkan dalam
desikator selama 10 menit dan ditambahkan dengan buffer TE
menggunakan elektroforesis dan konsentrasinya dicek dengan
menggunakan spektrofotometri nanodrop 1000. DNA yang
telah dilarutkan TE disimpan pada suhu -200
• Pemilihan metode terbaik
C untuk PCR.
Dari hasil isolasi dengan menggunakan berbagai
perlakuan tersebut, kemudian dipilih hasil yang terbaik
berdasarkan konsentrasi, kemurnian, pita genom dan hasil
amplifikasi dengan menggunakan PCR.
4.4.3. Pembuatan Gel Agarosa dan Elektroforesis
4.4.3.1. Pembuatan gel agarosa
Gel agarosa 1,2% dibuat dengan menambahkan 0,36 gr
agarosa dalam 30 ml buffer TAE 1x, dipanaskan hingga larut
(1 menit 20 detik) dalam microwave, Larutan agarosa
didinginkan hingga suhu 400
4.4.3.2. Elektroforesis
C dan ditambah dengan sybr safe
0,3 μl, dituang ke dalam tray, Agarosa didinginkan hingga
membeku selama 30-45 menit.
Gel diangkat dari cetakan dan dimasukan ke dalam
chamber elektroforesis kemudian ditambahkan buffer TAE 1x
sehingga gel terendam kira-kira 1 mm. Sebanyak 10 µl sampel
DNA dicampur dengan 2 µl loading dye kemudian
dimasukkan ke dalam sumur gel. Alat elektroforesis
bergerak menuju muatan positif. Hasil elektroforesis dilihat
dengan menggunakan dokumentasi gel (gel documentation).
4.4.4. Gel documentation
Komputer dan kamera digital dinyalakan. Gel agarosa hasil dari
elektroforesis dimasukan ke dalam UV transiluminator. UV
transiluminator dinyalakan dan pita DNA akan berpendar saat
terkena sinar UV. Hasil gel agarosa saat disinari UV
didokumentasikan dalam komputer.
4.4.5.Amplifikasi PCR
Campuran reaksi total PCR dibuat dalam volume 50 µl pada
tabung 0,2 ml. Amplifikasi menggunakan dua jenis primer yaitu primer
spesifik untuk babi; forward: 5’- CAT TCG CCT CAC TCA CAT
TAA CC -3’, reverse: 5’- AAG AGA GAG TTC TAC GGT CTG
TAG- 3’ (Kesmen et al., 2009) dan primer spesifik untuk sapi;
forward: 5’- GCC ATA TAC TCT CCT TGG TGA CA - 3’, dan
reverse: 5’- GTA GGC TTG GGA ATA GTA CGA - 3’ (Ilhak, 2006).
Campuran reaksi dibuat dengan menggunakan Fast star Taq DNA
Polymerase dan kemudian larutan dihomogenkan (lampiran 4). Mesin
thermal cycler dice diprogram dengan kondisi denaturasi awal pada
suhu 940 C selama 5 menit, denaturasi pada suhu 940 C selama 45 detik,
annealing pada suhu 610 C selama 45 detik, elongasi 720 C selama 90
detik, elongasi akhir pada suhu 720 C selama 5 menit dan suhu
Amplifikasi DNA pada daging segar dan daging kornet
menggunakan program PCR yang sama, yang membedakan adalah
jumlah siklus yang digunakan. Pada proses amplifikasi daging segar,
untuk menghasilkan amplikon yang jelas terbaca pada saat
elektroforeis cukup dengan menggunakan 30 siklus, sedangkan pada
daging kornet membutuhkan 35 siklus.
4.4.6. Uji spesifikasi primer
Masing-masing primer yang digunakan diuji spesifikasinya
dengan menggunakan PCR. Primer spesifik DNA babi digunakan
untuk mengamplifiksi DNA dari daging babi dan DNA dari daging
sapi. Begitu juga primer spesifik DNA sapi digunakan untuk
mengamplifikasi DNA dari daging sapi dan DNA dari daging babi.
Hasil PCR kemudian dielektroforesis dan dibandingkan. Primer
spesifik DNA sapi dikatakan spesifik jika hanya mengamplifikasi
DNA dari daging sapi, tetapi tidak dapat mengampifikasi DNA
dari daging babi. Begitu juga primer spesifik DNA babi dikatakan
spesifik jika hanya mengamplifikasi DNA dari daging babi dan
tidak dapat mengamplifikasi DNA dari daging sapi.
4.4.7. Uji sensitifitas primer spesifik DNA babi
Primer spesifik DNA babi diuji sensitifitasnya dengan
menggunakan PCR. Template DNA diambil dari hasil isolasi
pencampuran daging antara daging babi dan daging sapi. Gradien
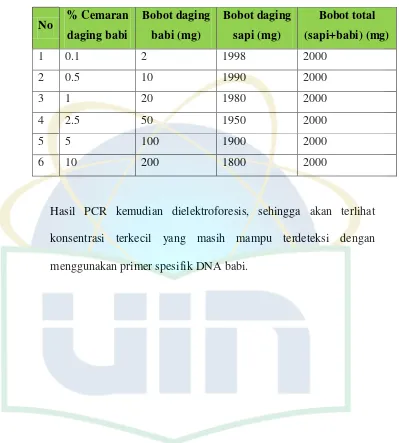
Tabel 3. Gradien konsentrasi campuran daging babi dan daging sapi
No % Cemaran daging babi
Bobot daging babi (mg)
Bobot daging sapi (mg)
Bobot total (sapi+babi) (mg)
1 0.1 2 1998 2000
2 0.5 10 1990 2000
3 1 20 1980 2000
4 2.5 50 1950 2000
5 5 100 1900 2000
6 10 200 1800 2000
Hasil PCR kemudian dielektroforesis, sehingga akan terlihat
konsentrasi terkecil yang masih mampu terdeteksi dengan
34
HASIL DAN PEMBAHASAN
[image:48.595.89.504.175.709.2]5.1Hasil
Gambar 6. Hasil elektroforesis isolasi genom daging babi, daging sapi dan
campuran daging babi dan daging sapi
Gambar 7. Hasil elektroforesis produk PCR menggunakan primer spesifik
DNA sapi dan primer spesifik DNA babi pada daging segar Keterangan:
1. 0,1% daging babi; 99,9% daging sapi 2. 0,5% daging babi; 99,5% daging sapi 3. 1% daging babi; 99% daging sapi 4. 2,5% daging babi; 97,5% daging sapi 5. 5% daging babi; 95% daging sapi 6. 10% daging babi; 90% daging sapi 7. Daging sapi 8. Daging babi 1000 bp
500 bp 300 bp 200 bp
M 1 2 3 4 M
1000 bp
500 bp 300 bp 200 bp
Gambar 8. Hasil elektroforesis isolasi genom dari daging sapi segar dan
kornet dengan berbagai perlakuan
Gambar 9. Hasil elektroforesis produk PCR daging kornet dengan
berbagai perlakuan menggunakan primer spesifik DNA
sapi
Keterangan :
1. Daging sapi segar tanpa perlakuan 2. Daging sapi segar dengan pemanasan 3. Daging sapi segar dicuci dengan
n-heksan
4. Daging sapi segar dicuci dengan air 5. Kornet tanpa perlakuan
6. Kornet dengan pemanasan 7. Kornet dicuci dengan n-heksan 8. Kornet dicuci dengan air M. Ladder 100 bp
Keterangan : 1.Tanpa perlakuan
2.Perlakuan dengan pemanasan 3. Dicuci dengan n-heksan 4. Dicuci dengan air M. Ladder 100 bp
1000 bp
500 bp 300 bp
200 bp
271 bp
M 1 2 3 4
1000 bp
Gambar 10. Hasil elektroforesis produk PCR dengan menggunakan primer
spesifik DNA sapi pada campuran daging babi dan daging sapi
Gambar 11. Hasil elektroforesis produk PCR dengan menggunakan
primer spesifik DNA babi pada campuran daging babi dan
daging sapi 1000 bp 500 bp 300 bp 200 bp Keterangan:
1. 0,1% daging babi; 99,9% daging sapi 2. 0,5% daging babi; 99,5% daging sapi 3. 1% daging babi; 99% daging sapi 4. 2,5% daging babi; 97,5% daging sapi 5. 5% daging babi; 95% daging sapi 6. 10% daging babi; 90% daging sapi 7. Daging sapi 8. Daging babi
Keterangan:
1. 0,1% daging babi; 99,9% daging sapi 2. 0,5% daging babi; 99,5% daging sapi 3. 1% daging babi; 99% daging sapi 4. 2,5% daging babi; 97,5% daging sapi 5. 5% daging babi; 95% daging sapi 6. 10% daging babi; 90% daging sapi 7. Daging sapi 8. Daging babi
Gambar 12. Hasil elektroforesis isolasi genom sampel kornet
Gambar 13. Hasil elektroforesis produk PCR dengan menggunakan primer
spesifik DNA sapi pada sampel kornet Keterangan:
1. Sampel kornet no. 1 2. Sampel kornet no. 2 3. Sampel kornet no. 3 4. Sampel kornet no. 4 5. Sampel kornet no. 5 6. Sampel kornet no. 6 M. Ladder 100 bp
Keterangan:
1. Sampel kornet no. 1 2. Sampel kornet no. 2 3. Sampel kornet no. 3 4. Sampel kornet no. 4 5. Sampel kornet no. 5 6. Sampel kornet no. 6 7. Daging sapi dengan primer spesifik DNA sapi
8. Daging babi dengan primer spesifik DNA babi
Gambar 14. Hasil elektroforesis produk PCR dengan menggunakan primer spesifik DNA babi sampel kornet
Keterangan:
1. Sampel kornet no. 1 2. Sampel kornet no. 2 3. Sampel kornet no. 3 4. Sampel kornet no. 4 5. Sampel kornet no. 5 6. Sampel kornet no. 6 7. Daging babi dengan primer spesifik DNA babi
8. Daging sapi dengan primer spesifik DNA sapi
M. Ladder 100bp 1000 bp
500 bp 300 bp 200 bp
5.2. Pembahasan
5.2.1 Isolasi Genom
Genom diisolasi dari sampel kornet yang berasal dari toko, pasar
dan swalayan yang terdapat di wilayah Ciputat dengan jumlah 6 merek
kornet, sedangkan daging babi dan daging sapi didapatkan dari pasar
Bogor. Metode isolasi yang digunakan adalah dengan menggunakan
cell lysis buffer (Tris-EDTA pH 8 dan SDS 1% w/v) seperti yang
dilakukan oleh Kesmen et al. (2009) dengan melakukan beberapa
modifikasi. Modifikasi yang dilakukan adalah pada volume sampel,
kecepatan sentrifugasi, dan pengendapan protein.
Sampel yang diisolasi sebanyak satu gram dan diinkubasi
dengan menggunakan cell lysis buffer pada suhu 550
Metode ini menggunakan SDS (Sodium Dodesil Sulfat/Natrium
Lauryl Sulfat) sebagai deterjen kationik untuk melisiskan dinding sel
dengan cara melarutkan membran lipid, sehingga dinding sel menjadi
rusak dan mengeluarkan komponen-komponennya yaitu protein, lipid,
karbohidrat, DNA dan RNA (Dale & Malcom, 2002). SDS yang
digunakan sebanyak 1% (w/v) (Malisa, 2006; Kesmen et al., 2009) C selama 16-18
jam yang kemudian disentrifugasi pada kecepatan 8000 rpm.
Sedangkan Kesmen et al. (2009) menggunakan supernatan hasil
inkubasi hanya 750 µl. Volume ini tidak bermasalah jika digunakan
pada sampel daging segar, akan tetapi daging pada sampel kornet telah
mengalami pengolahan, sehingga DNA yang terdapat di dalam sel
dari total volume cell lysis buffer yang terdiri 10 mM Tris-Cl pH 80,1
mM EDTA pH 8,0. Tris merupakan dapar yang berfungsi untuk
menjaga pH, sangat larut dalam air dan inert untuk berbagai jenis
reaksi enzimatik (Sambrook & Russel, 2001). Menurut Ageno (1969),
kondisi basa dapat memecah DNA, begitu juga dengan kondisi asam
menyebabkan DNA terdenaturasi (Marmur & Lane, 1958), sehingga
pH ekstrim dapat mengganggu proses isolasi DNA, sedangkan EDTA
(Ethylene Diamine Tetra Acetic acid) berfungsi sebagai bahan
pengkhelat yang mengikat kation divalen, sehingga menjadikan
ketidakstabilan membran (Dale & Malcom 2002; Raven, 2002;
Harisha, S., 2007), disamping itu kehadiran kation divalen menjadi
kofaktor bagi DNAse, sehingga dengan pengikatan kation divalen,
aktifitas DNAse dapat dihambat (Weir, 1993).
Kontaminan protein dihilangkan dengan menggunakan
proteinase K (Fermentas), salah satu dari enzim golongan serin
protease (Ebeling, W., et al., 1974; Sweeney & Walker, 1993) yang
merupakan protease endolitik, memecah ikatan peptida sisi karboksilat
pada gugus alipatik dan aromatik, khususnya alanin (Sweeney &
Walker, 1993). Protein yang telah rusak dipisahkan dari larutan
bersamaan dengan karbohidrat dan komponen lainnya yang telah lisis
dengan menggunakan sentrifugasi.
Pada proses pengendapan protein, natrium klorida 5 M
digunakan sebagai pengendap protein. Konsentrasi garam yang tinggi
dimana keberadaan ion dari garam menghasilkan penurunan muatan
suspensi. Dalam suspensi koloid, pada kondisi pH isoionik, muatan
protein kurang berpengaruh dibandingkan dengan gaya dari suspensi,
protein memiliki kelarutan yang minimal dan dapat mengendap.
Pengendapan protein secara umum bergantung pada derajat hidrasi,
yaitu pengikatan molekul air oleh sisi luar protein dan bertindak
sebagai faktor penstabil dalam suspensi. Beberapa titik konsentrasi
garam dapat menurunkan zeta potensial menjadi nol dan protein akan
mengendap. Efek ini ditingkatkan dengan kompetisi molekul air
dengan konsentrasi garam yang tinggi. (Holme, David. J & Hazel
Peck, 1998). Selain itu, protein mempunyai perbedaan kelarutan dalam
larutan garam, nilai kelarutanya relatif, dan dengan meningkatkan
konsentrasi garam, kebanyakan protein akan mengendap (Harisha, S.,
2007).
Residu dari protein dan lipid dihilangkan dengan menggunakan
kloroform dan isoamilalkohol. Kloroform merupakan pelarut organik
yang dapat mendenaturasi dan memisahkan kontaminasi protein.
Pelarut ini mempunyai massa jenis yang lebih besar daripada air,
sehingga pada saat ekstraksi dalam campuran, kedua pelarut berada
pada fase bawah (Burden dan Whitney, 1995). Isoamil alkohol dapat
digunakan untuk membantu pemisahan fase air dan fase organik
dengan perbandingan masing-masing kloroform dan isoamil alkohol
2009). Presipitasi protein ini dilakukan sebanyak dua kali pengendapan
untuk membuang residu protein yang tertinggal.
DNA total dipisahkan dari larutan dengan cara pengendapan
dengan menggunakan isopropanol (Sambrook & Russel, 2001).
Dengan adanya NaCl di dalam larutan akan menyebabkan DNA
kurang hidrofil, sehingga kelarutannya di dalam air menjadi berkurang.
Hal ini terjadi karena NaCl akan terionisasi menjadi Na+ dan Cl-, ion
positif Na+ akan menetralisir muatan negatif gugus fosfat pada DNA,
yang menyebabkan DNA menjadi kurang hidrofil. Dengan
penambahan isopropanol, yang mempunyai konstanta dielektrik yang
lebih rendah daripada air, membuat interaksi Na+ dengan PO3
-Genom divisualisasikan dengan menggunakan elektroforesis gel
agarosa 1,2% dengan tegangan 100 volt. Loading dye yang terdiri dari
glycerol dan bromphenol blue dicampurkan ke dalam genom, Glycerol
berfungsi sebagai pemberat, sehingga DNA berada di bawah sumur
gel, sedangkan bromphenol blue berfungsi sebagai visualisasi pada gel
(Carson, 2006), sehingga jarak yang diharapkan dapat ditentukan, dan
proses running tidak melebihi batas gel.
lebih
mudah, sehingga membuat DNA kurang hidrofil dan DNA dapat
mengendap.
Gambar 6 menunjukan hasil isolasi genom dari daging sapi,
babi, dan dari campuran daging babi dan daging sapi. Gambar ini
menunjukan pita yang smear. Genom yang smear pada hasil
[image:56.595.135.516.157.514.2]Genom mengalami fragmentasi menjadi banyak fragmen yang berbeda
ukuran dan tertahan pada gel sesuai dengan ukurannya yang
menghasilkan gambar yang smear. Genom yang mengalami
fragmentasi dipengaruhi oleh banyak faktor, diantaranya adalah
lamanya waktu homogenasi dengan menggunakan lysis buffer
(Aljanabi et al., 1999) penggerusan dengan menggunakan mortar yang
cukup kuat (Santiana, 2010), dan aktifitas DNAse yang dapat
memotong ikatan pospodiester DNA (Weir, 1993).
Konsentrasi genom hasil isolasi diukur dengan menggunakan
spektrofotometer Nano Drop ND-1000 pada panjang gelombang 260
nm. Konsentrasi yang dihasilkan dari masing-masing sampel bervariasi
antara 1000 ng/ μl – 2800 ng/ μl dengan jumlah sampel sebanyak satu
gram (lampiran 1). Dengan menggunakan jumlah yang sama, nilai
konsentrasi yang didapatkan daging segar ±3 kali lebih besar
dibandingkan konsentrasi yang didapatkan dari daging kornet. Ini
menunjukan adanya pengaruh pengolahan pada daging kornet terhadap
stabilitas DNA.
Perbandingan antara panjang gelombang 260 nm dan 280 nm
(260/280) merupakan nilai kemurnian DNA (Harisha, S., 2007). Nilai
kemurnian yang dihasilkan dari genom yang diperoleh memiliki nilai
antara 1,6-1,9 (lampiran 1). Menurut Stephenson (2003) nilai
kemurnian kurang dari 1,8 menunjukan adanya kontaminasi protein.
Nilai ini dipengaruhi oleh kandungan protein yang sangat tinggi dalam
menggunakan kloroform-isoamil alkohol dapat meningkatkan
kemurnian DNA dari sampel daging. Masih menurut Stephenson
(2003) dalam bukunya Calculations in molecular biology and
biotechnology, a guide to mathematics in the laboratory DNA yang
bebas dari protein mempunyai nilai mendekati 1,8, sedangkan nilai
yang lebih dari 2,0 menunjukan adanya kandungan RNA (Stephenson,
2003).
Gambar 8 merupakan hasil elektroforesis genom dengan
berbagai perlakuan. Genom yang dihasilkan dari daging segar cukup
jelas, sedangkan genom yang dihasilkan dari daging kornet tidak
begitu jelas terlihat, yang menunjukan pecahnya genom. Jika dilihat
dari konsentrasi dan kemurniannya (lampiran 1), rata-rata konsentrasi
yang didapatkan cukup besar untuk mendapatkan pita genom, akan
tetapi hal ini tidak terjadi, karena pembacaan yang dilakukan alat
spektrofotometer pada panjang gelombang 260 nm adalah gugus
kromofor dari basa purin dan pirimidin (Weaver, F. Robert, 2004)
yang merupakan basa dari DNA, sehingga, meskipun urutan DNAnya
terputus, akan tetapi, konsentrasi yang terbaca akan tetap besar.
Sampel nomor 8 (gambar 8) yang merupakan hasil isolasi yang
sampelnya dicuci dengan menggunakan air, menampilkan pita DNA
yang tebal dibandingkan dengan perlakuan yang lain. Metode ini yang
menjadi acuan dalam proses isolasi daging kornet berikutnya. Dari
hasil elektroforesis dengan menggunakan berbagai perlakuan ini,
[image:58.595.138.515.187.519.2]kornet, yaitu dengan pencucian menggunakan air (gambar 8). Dari
gambar 12 terlihat pada sampel nomor 4 pita genom sangat tebal
dibandingkan pita genom yang lainnya. Jumlah sampel sebanyak 2
gram (2 kali dari jumlah sampel yang lain) dan perendaman dengan
menggunakan air selama lebih dari 2 hari menjadikan
senyawa-senyawa additive yang bersifat polar yang terdapat di dalam sampel
dapat ditarik oleh air, sehingga tidak mengganggu proses isolasi.
5.2.2 Polymerase Chain Reaction (PCR)
DNA mitokondria diamplifikasi dengan menggunakan primer
spesifik untuk spesies sapi (Ilhak, 2006) dan primer spesifik untuk
spesies babi (Kesmen et al., 2009). Primer diuji spesifikasinya yaitu
dengan cara kedua primer digunakan untuk mengamplifikasi daging
sapi segar dan daging babi segar. Gambar 7 menunjukan hasil uji
spesifik primer yang digunakan. Dari gambar 7 dapat terlihat bahwa
primer spesifik untuk sapi hanya dapat mengamplifikasi sekuen DNA
pada spesies sapi, sedangkan tidak dapat mengamplifikasi sekuen
DNA pada spesies babi, begitu juga sebaliknya, primer yang spesifik
untuk babi hanya dapat mengamplifikasi sekuen DNA pada spesies
babi dan tidak dapat mengamplifikasi sekuen DNA spesies sapi.
Reaksi PCR yang dilakukan menggunakan genom dengan
konsentrasi 100 ng/µl. Konsentrasi ini optimal untuk mendapatkan
amplikon yang tebal pada 30 siklus untuk daging segar, akan tetapi
untuk sampel daging kornet dibutuhkan 35 siklus. Amplifikasi
[image:59.595.138.518.180.535.2]C untuk kedua primer. Komponen yang penting dalam proses
amplifikasi PCR adalah Mg2+ yang berfungsi sebagai penstabil enzim,
disamping itu, konsentrasi Mg2+ mempengaruhi penempelan primer
(Khosravinia & Ramesha, 2007). Konsentrasi MgCl2
Gambar 11 menunjukan sensitifitas primer yang digunakan
terhadap campuran daging babi terhadap daging sapi pada 30 siklus.
Seperti yang dilakukan Kesmen et al. (2009), primer ini dapat
mengamplifikasi sekuen DNA hingga 0,1%, meskipun pada
konsentrasi 0,1% daging babi terhadap campuran daging babi dan
daging sapi menghasilkan pita yang sangat tipis.
yang digunakan
dalam campuran reaksi adalah 5 mM (Ilhak, 2006) dan campuran
lainnya mengikuti standar yang direkomendasikan (lampiran 4).
Gambar 9 merupakan hasil elektroforesis produk PCR dari
genom yang mengalami perlakuan yang berbeda-beda. Primer yang
digunakan adalah primer yang spesifik untuk spesies sapi. Terlihat
bahwa dengan dilakukan pencucian menggunakan air pada sampel
daging kornet, menunjukan adanya bagian dari genom yang
teramplifikasi (nomor 4 gambar 9).
Proses amplifikasi untuk spesies sapi terletak pada daerah lokus
tRNA lysine pada sekuen DNA mitokondria dengan panjang produk
271 pasang basa, sedangkan untuk spesies babi pada lokus ND5 CDS
pada sekuen DNA mitokondria dengan panjang produk 227 pasang
basa. Amplifikasi sekuen DNA mitokondria pada sampel