PENETAPAN KADAR ALKALI BEBAS
PADA SABUN MANDI SEDIAAN PADAT
SECARA TITRIMETRI
TUGAS AKHIR
OLEH:
NADYA DWI RIZKY
NIM 102410036
PROGRAM STUDI DIPLOMA III
ANALIS FARMASI DAN MAKANAN
FAKULTAS FARMASI
UNIVERSITAS SUMATERA UTARA
MEDAN
KATA PENGANTAR
Segala puji dan syukur penulis panjatkan atas kehadirat Allah SWT yang
telah melimpahkan rahmat dan karunia-Nya, sehingga penulis dapat menyusun
dan menyelesaikan Tugas Akhir berjudul “Penetapan Kadar Alkali Bebas Pada
Sabun Mandi Sediaan Padat Secara Titrimetri”. Tugas Akhir ini disusun sebagai
salah satu syarat untuk dapat menyelesaikan pendidikan Program Studi Diploma
III Analis Farmasi dan Makanan di Fakultas Farmasi Universitas Sumatera Utara,
Medan.
Penulis menyadari sepenuhnya bahwa tanpa bantuan, bimbingan, dan
dukungan dari berbagai pihak, penulis tidak akan dapat menyelesaikan Tugas
Akhir ini sebagaimana mestinya. Penulis mengucapkan terima kasih yang
sebesar-besarnya kepada berbagai pihak antara lain:
1. Bapak Prof. Dr. Sumadio Hadisahputra, Apt., selaku Dekan Fakultas Farmasi
Universitas Sumatera Utara Medan.
2. Ibu Prof. Dr. Julia Reveny, M.Si., Apt., selaku Dosen Pembimbing Tugas
Akhir yang telah banyak memberikan bimbingan dan pengarahan dengan
penuh perhatian hingga Tugas Akhir ini selesai.
3. Bapak Prof. Dr. Jansen Silalahi, M.App.Sc., Apt., selaku Ketua Program
Studi Diploma III Analis Farmasi dan Makanan Fakultas Farmasi Universitas
Sumatera Utara.
4. Ibu Dra. Juanita Tanuwijaya, M.Si., Apt., sebagai Dosen Pembimbing
Akademik yang telah memberikan nasehat dan pengarahan kepada penulis
5. Bapak Drs. I Gde Nyoman Suandi, M.M., Apt., selaku Kepala Balai Besar
Pengawas Obat dan Makanan di Medan yang telah memberi izin pelaksanaan
praktik kerja lapangan.
6. Ibu Lambok Oktavia SR, M.Kes, Apt., selaku koordinator pembimbing
praktik kerja lapangan di Balai Besar Pengawas Obat dan Makanan di Medan.
7. Bapak dan Ibu staff Pegawai di Balai Besar Pengawas Obat dan Makanan di
Medan yang telah memberikan kesempatan kepada penulis untuk melakukan
praktik kerja lapangan.
8. Bapak dan Ibu dosen beserta seluruh staff Pegawai Fakultas Farmasi
Program Studi Diploma III Analis Farmasi dan Makanan Fakultas Farmasi
Universitas Sumatera Utara.
Secara khusus, penulis mengucapkan terima kasih yang tiada terhingga
kepada Ayahanda Misno dan Ibunda Sri Wardhana Ritonga, kakak penulis Henny
Debby Utari, S.Pd., adik penulis Tissa Pratiwi Putri dan teman dekat penulis Lutfi
Arifin yang telah memberikan perhatian, doa, semangat, motivasi dan
pengorbanan baik moril maupun materil dalam penyelesaian Tugas Akhir ini.
Terima kasih kepada teman sekelompok Praktik Kerja Lapangan Tika,
Hijjatul, Ely yang saling mendukung dan bahu membahu selama Praktik Kerja
Lapangan hingga Tugas Akhir ini selesai dan seluruh teman-teman mahasiswa
Analis Farmasi dan Makanan angkatan 2010 yang tidak dapat penulis sebutkan
satu persatu, namun tidak mengurangi arti keberadaan mereka.
Dalam menulis Tugas Akhir ini, Penulis menyadari bahwa sepenuhnya isi
masih jauh dari kesempurnaan, untuk itu dengan segala kerendahan hati, penulis
mengharapkan kritik dan saran yang bersifat membangun demi kesempurnaan
Tugas Akhir ini dan demi peningkatan mutu penulisan Tugas Akhir di masa yang
akan datang.
Akhir kata, penulis sangat berharap semoga Tugas Akhir ini dapat
memberikan manfaat kepada semua pihak yang memerlukan.
Medan, April 2013
Penulis,
PENETAPAN KADAR ALKALI BEBAS
PADA SABUN MANDI SEDIAAN PADAT SECARA TITRIMETRI
ABSTRAK
Sabun mandi sediaan padat merupakan senyawa natrium atau kalium dengan asam lemak dari minyak nabati atau lemak hewani berbentuk padat, lunak, dan berbusa yang digunakan sebagai pembersih, dengan menambahkan zat wangi dan bahan lainnya yang tidak membahayakan kesehatan.
Alkali bebas merupakan alkali dalam sabun yang tidak diikat sebagai senyawa. Kelebihan alkali bebas pada sabun dapat disebabkan karena konsentrasi alkali yang pekat atau berlebih pada proses penyabunan. Sabun yang mengandung alkali tinggi biasanya digunakan untuk sabun cuci.
Penetapan kadar alkali bebas dalam sabun mandi sediaan padat bertujuan untuk mengetahui apakah kadar alkali bebas yang terdapat dalam sabun mandi sediaan padat memenuhi persyaratan yang ditetapkan dalam Standar Nasional Indonesia (SNI). Penetapan kadar alkali bebas dilakukan menurut metode titrimetri sesuai dengan prosedur dan alat yang digunakan di laboratorium Kosmetika dan Alat Kesehatan di Balai Besar Pengawas Obat dan Makanan Medan. Sabun mandi sediaan padat yang diuji mengandung alkali bebas dengan kadar 0,0536 %. Dari hasil yang diperoleh, sabun mandi sediaan padat yang diuji memenuhi persyaratan kadar alkali bebas, sesuai dengan SNI 06-3532-1994, dimana kadar alkali bebas yang diperbolehkan untuk sabun mandi sediaan padat tidak lebih dari 0,14 %.
DETERMINATION OF FREE ALKALI CONTENT THE SOAP BATH PREPARATIONS IN SOLID TITRIMETRI
ABSTRACT
SOAP bath preparations of solid compounds of sodium or potassium with fatty acids from vegetable oils or animal fats are dense, soft, and used as a foaming cleanser, by adding fragrant substance and other materials that are not harmful to health.
Of Alkali lye in the SOAP is free not bound as a compound. The excess lye free SOAP can be caused due to the concentration of alkali concentrations or excess in the process of penyabunan. Soaps containing high alkaline is commonly used for SOAP.
Determination of free alkali content in SOAP bath solid preparations aimed to find out whether the levels of alkalis contained in SOAP-free wash of solid preparations meet the requirements set out in the National standard of Indonesia (SNI). Determination of free alkali content made according to the method of titrimetri in accordance with the procedures and tools used in the laboratory of Cosmetic and Wellness Tools on the porch of the Watchdog food and drug Field. SOAP bath preparations tested contain solid alkali-free with 0,0536%. From the results obtained, the solid material of bath soaps tested compliant non alkaline levels, according to SNI 06-3552-1994, where levels of alkali-free SOAP is allowed for a solid dosage not more than 0.05%.
DAFTAR ISI
Halaman
Lembar Judul ... i
Lembar Pengesahan ... ii
Kata Pengantar ... iii
Abstrak ... vi
Daftar Isi ... vii
Daftar Tabel ... x
Daftar Lampiran ... xi
BAB I PENDAHULUAN ... 1
1.1 Latar Belakang ... 1
1.2 Tujuan ... 3
1.3 Manfaat ... 3
BAB II TINJAUAN PUSTAKA ... 4
2.1 Sabun ... 4
2.1.1 Pengertian Sabun ... 4
2.1.2 Komposisi Sabun ... 5
2.1.3 Fungsi Sabun ... 8
2.1.4 Efek Samping Sabun pada Kulit ... 8
2.1.5 Proses Pembuatan Sabun ... 12
2.2 Sabun Mandi Padat ... 13
2.2.1 Pengertian Sabun Mandi Padat ... 13
2.3 Alkali Bebas ... 16
2.3.1 Pengertian Alkali Bebas ... 16
2.3.2 Efek Samping Alkali pada Kulit ... 17
2.3.3 Kandungan Alkali pada Sabun ... 18
2.4 Metode Titrimetri ... 18
2.4.1 Penggolongan Titrimetri ... 18
2.4.2 Asidimetri – Alkalimetri ... 20
BAB III METODE PERCOBAAN ... 23
3.1 Tempat Pengujian ... 23
3.2 Alat ... 23
3.3 Bahan ... 23
3.4 Sampel ... 23
3.5 Prosedur ... 24
3.5.1 Pembuatan Pereaksi ... 24
3.5.2 Persiapan Contoh Uji ... 25
3.5.3 Cara Uji Sampel ... 25
3.6 Interpretasi Hasil ... 26
BAB IV HASIL DAN PEMBAHASAN ... 27
4.1 Hasil ... 27
4.2 Pembahasan ... 27
BAB V KESIMPULAN DAN SARAN ... 28
5.1 Kesimpulan ... 28
DAFTAR PUSTAKA ... 29
DAFTAR TABEL
Halaman
DAFTAR LAMPIRAN
Halaman
Lampiran 1 Data Penimbangan dan Perhitungan Pembakuan HCl
dan KOH ... 31
Lampiran 2 Data Penetapan Kadar Alkali Bebas pada Sabun Mandi
PENETAPAN KADAR ALKALI BEBAS
PADA SABUN MANDI SEDIAAN PADAT SECARA TITRIMETRI
ABSTRAK
Sabun mandi sediaan padat merupakan senyawa natrium atau kalium dengan asam lemak dari minyak nabati atau lemak hewani berbentuk padat, lunak, dan berbusa yang digunakan sebagai pembersih, dengan menambahkan zat wangi dan bahan lainnya yang tidak membahayakan kesehatan.
Alkali bebas merupakan alkali dalam sabun yang tidak diikat sebagai senyawa. Kelebihan alkali bebas pada sabun dapat disebabkan karena konsentrasi alkali yang pekat atau berlebih pada proses penyabunan. Sabun yang mengandung alkali tinggi biasanya digunakan untuk sabun cuci.
Penetapan kadar alkali bebas dalam sabun mandi sediaan padat bertujuan untuk mengetahui apakah kadar alkali bebas yang terdapat dalam sabun mandi sediaan padat memenuhi persyaratan yang ditetapkan dalam Standar Nasional Indonesia (SNI). Penetapan kadar alkali bebas dilakukan menurut metode titrimetri sesuai dengan prosedur dan alat yang digunakan di laboratorium Kosmetika dan Alat Kesehatan di Balai Besar Pengawas Obat dan Makanan Medan. Sabun mandi sediaan padat yang diuji mengandung alkali bebas dengan kadar 0,0536 %. Dari hasil yang diperoleh, sabun mandi sediaan padat yang diuji memenuhi persyaratan kadar alkali bebas, sesuai dengan SNI 06-3532-1994, dimana kadar alkali bebas yang diperbolehkan untuk sabun mandi sediaan padat tidak lebih dari 0,14 %.
DETERMINATION OF FREE ALKALI CONTENT THE SOAP BATH PREPARATIONS IN SOLID TITRIMETRI
ABSTRACT
SOAP bath preparations of solid compounds of sodium or potassium with fatty acids from vegetable oils or animal fats are dense, soft, and used as a foaming cleanser, by adding fragrant substance and other materials that are not harmful to health.
Of Alkali lye in the SOAP is free not bound as a compound. The excess lye free SOAP can be caused due to the concentration of alkali concentrations or excess in the process of penyabunan. Soaps containing high alkaline is commonly used for SOAP.
Determination of free alkali content in SOAP bath solid preparations aimed to find out whether the levels of alkalis contained in SOAP-free wash of solid preparations meet the requirements set out in the National standard of Indonesia (SNI). Determination of free alkali content made according to the method of titrimetri in accordance with the procedures and tools used in the laboratory of Cosmetic and Wellness Tools on the porch of the Watchdog food and drug Field. SOAP bath preparations tested contain solid alkali-free with 0,0536%. From the results obtained, the solid material of bath soaps tested compliant non alkaline levels, according to SNI 06-3552-1994, where levels of alkali-free SOAP is allowed for a solid dosage not more than 0.05%.
BAB I PENDAHULUAN
1.1Latar Belakang
Sebagai insan sosial, manusia memerlukan hubungan harmonis satu
dengan lainnya dan salah satunya adalah penampilan yang rapi dan bersih. Untuk
itu kita memerlukan bahan yang kita kenal sekarang sebagai kosmetika.
Kosmetika yang paling tua yang dikenal manusia adalah sabun, bahan pembersih
kulit yang dipakai selain untuk membersihkan juga untuk pengharum kulit. Tanpa
sabun, mandi terasa tidak bersih karena sabun berfungsi untuk mengangkat
kotoran yang menempel di tubuh kita. Kebersihan tubuh memang penting bagi
manusia dan itu diinformasikan melalui petunjuk baik di dalam keluarga maupun
di dalam lingkungan masyarakat yang lebih luas (Wasitaatmadja, 1997).
Sabun adalah garam logam alkali (Li, Na, atau K) dari asam lemak
berantai panjang. Sabun tidak berguna dalam air asam. Dalam air asam, ion
karboksilat dari molekul sabun mengambil proton dan membentuk asam yang tak
mengion. Asam lemak mengendap sebagai kerak buih karena tak dapat
membentuk misel. Sabun juga tidak berguna dalam air sadah, yakni air yang
mengandung ion kalsium, magnesium, atau besi. Ion karboksilat membentuk
garam yang tak larut dengan ion di dalam air (Wilbraham, 1992).
Misel adalah struktur bulat yang terdiri dari ratusan molekul garam asam
lemak. Misel tersusun dengan gugus polar dari garam asam lemak disebelah luar
dan rantai hidrofobik yang tertanam disebelah dalam, jauh dari air (Stephen,
Alkali bebas merupakan alkali dalam sabun yang tidak diikat sebagai
senyawa. Kelebihan alkali bebas dalam sabun tidak boleh lebih dari 0,1% untuk
sabun Na dan 0,14% untuk sabun KOH karena alkali mempunyai sifat yang keras
dan menyebabkan iritasi pada kulit (Qisti, 2009).
Sabun mandi yang baik harus memenuhi syarat mutu sabun mandi yaitu
kadar air, jumlah asam lemak, alkali bebas, asam lemak bebas dan atau lemak
netral, dan minyak mineral. Sabun mandi padat adalah senyawa natrium atau
kalium dengan asam lemak dari minyak nabati atau lemak hewani berbentuk
padat, lunak, dan berbusa yang digunakan sebagai pembersih, dengan
menambahkan zat wangi dan bahan lainnya yang tidak membahayakan kesehatan.
Salah satu syarat yang harus dipenuhi pada sabun mandi sediaan padat
adalah kadar alkali bebas. Berdasarkan SNI 06–3532–1994 telah ditetapkan
bahwa kadar alkali bebas pada sabun mandi sediaan padat adalah tidak lebih dari
0,14%. Jika lebih dari 0,14% maka dinyatakan tidak memenuhi syarat. Tugas
akhir ini berjudul “Penetapan Kadar Alkali Bebas pada Sabun Mandi Sediaan Padat Secara Titrimetri“. Adapun pengujian dilakukan selama penulis melakukan praktek kerja lapangan di Balai Besar Pengawas Obat dan Makanan di
Medan.
Penetapan kadar alkali bebas pada sabun mandi sediaan padat dilakukan
secara Titrimetri. Titrimetri adalah pemeriksaan jumlah zat yang didasarkan pada
pengukuran volume larutan pereaksi yang dibutuhkan untuk bereaksi secara
1.2Tujuan
Adapun tujuan dari penetapan kadar alkali bebas pada sabun mandi
sediaan padat adalah untuk mengetahui apakah kadar alkali bebas yang terdapat
dalam sabun mandi sediaan padat memenuhi persyaratan kadar alkali bebas yang
ditetapkan dalam Standar Nasional Indonesia (SNI).
1.3Manfaat
Manfaat yang diperoleh dari penetapan kadar alkali bebas pada sabun
mandi sediaan padat adalah agar dapat mengetahui bahwa produk sabun yang
beredar di pasaran memenuhi persyaratan kadar alkali bebas Standar Nasional
BAB II
TINJAUAN PUSTAKA
2.1 Sabun
2.1.1 Pengertian Sabun
Sabun adalah bahan yang digunakan untuk mencuci dan mengemulsi,
terdiri dari dua komponen utama yaitu asam lemak dengan rantai karbon C16 dan
sodium atau potasium. Sabun merupakan pembersih yang dibuat dengan reaksi
kimia antara kalium atau natrium dengan asam lemak dari minyak nabati atau
lemak hewani. Sabun yang dibuat dengan NaOH dikenal dengan sabun keras
(hard soap), sedangkan sabun yang dibuat dengan KOH dikenal dengan sabun
lunak (soft soap). Sabun dibuat dengan dua cara yaitu proses saponifikasi dan
proses netralisasi minyak. Proses saponifikasi minyak akan memperoleh produk
sampingan yaitu gliserol, sedangkan proses netralisasi tidak akan memperoleh
gliserol. Proses saponifikasi terjadi karena reaksi antara trigliserida dengan alkali,
sedangkan proses netralisasi terjadi karena reaksi asam lemak bebas dengan alkali
(Qisti, 2009).
Sabun merupakan senyawa garam dari asam-asam lemak tinggi, seperti
natrium stearat, C17H35COO-Na+. Aksi pencucian dari sabun banyak dihasilkan
dari kekuatan pengemulsian dan kemampuan menurunkan tegangan permukaan
dari air. Konsep ini dapat di pahami dengan mengingat kedua sifat dari anion
2.1.2 Komposisi Sabun
Sabun konvensional yang dibuat dari lemak dan minyak alami dengan
garam alkali serta sabun deterjen saat ini yang dibuat dari bahan sintetik,
biasanya mengandung surfaktan, pelumas, antioksidan, deodorant, warna,
parfum, pengontrol pH, dan bahan tambahan khusus.
a. Surfaktan
Surfaktan adalah molekul yang memiliki gugus polar yang suka air
(hidrofilik) dan gugus non polar yang suka minyak (lipofilik) sehingga dapat
memperasatukan campuran yang terdiri dari minyak dan air yang bekerja
menurunkan tegangan permukaan. Surfaktan merupakan bahan terpenting dari
sabun. Lemak dan minyak yang dipakai dalam sabun berasal dari minyak kelapa
(asam lemak C12), minyak zaitun (asam lemak C16-C18), atau lemak babi.
Penggunaan bahan berbeda menghasilkan sabun yang berbeda, baik secara fisik
maupun kimia. Ada sabun yang cepat berbusa tetapi terasa airnya kasar dan tidak
stabil, ada yang lambat berbusa tetapi lengket dan stabil. Jenis bahan surfaktan
pada syndet dewasa ini mencapai angka ribuan (Anonima, 2013; Wasitaatmadja,
1997).
b. Pelumas
Untuk menghindari rasa kering pada kulit diperlukan bahan yang tidak saja
meminyaki kulit tetapi juga berfungsi untuk membentuk sabun yang lunak, misal:
asam lemak bebas, fatty alcohol, gliserol, lanolin, paraffin lunak, cocoa butter,
dan minyak almond, bahan sintetik ester asam sulfosuksinat, asam lemak
Bahan-bahan selain meminyaki kulit juga dapat menstabilkan busa dan berfungsi
sebagai peramas (plasticizers) (Wasitaatmadja, 1997).
c. Antioksidan dan Sequestering Agents
Antioksidan adalah senyawa atau zat yang dapat menghambat, menunda,
mencegah, atau memperlambat reaksi oksidasi meskipun dalam konsentrasi yang
kecil. Untuk menghindari kerusakan lemak terutama bau tengik, dibutuhkan
bahan penghambat oksidasi, misalnya stearil hidrazid dan butilhydroxy toluene
(0,02%-0,1%). Sequestering Agents dibutuhkan untuk mengikat logam berat yang
mengkatalis oksidasi EDTA. EHDP (ethanehidroxy-1-diphosphonate) (Anonimb,
2013; Wasitaatmadja, 1997).
d. Deodorant
Deodorant adalah suatu zat yang digunakan untuk menyerap atau
mengurangi bau menyengat. Deodorant dalam sabun mulai dipergunakan sejak
tahun 1950, namun oleh karena khawatir efek samping, penggunaannya dibatasi.
Bahan yang digunakan adalah TCC (trichloro carbanilide) dan 2-hidroxy
2,4,4-trichlodiphenyl ester (Anonimc, 2013; Wasitaatmadja, 1997).
e. Warna
Kebanyakan sabun toilet berwarna cokelat, hijau biru, putih, atau krem.
Pewarna sabun dibolehkan sepanjang memenuhi syarat dan peraturan yang ada,
pigmen yang digunakan biasanya stabil dan konsentrasinya kecil sekali
menimbulkan efek berkilau. Akhir-akhir ini dibuat sabun tanpa warna dan
transparan (Wasitaatmadja, 1997).
f. Parfum
Isi sabun tidak lengkap bila tidak ditambahkan parfum sebagai pewangi.
Pewangi ini harus berada dalam pH dan warna yang berbeda pula. Setiap pabrik
memilih bau dan warna sabunbergantung pada permintaan pasar atau masyarakat
pemakainya. Biasanya dibutuhkan wangi parfum yang tidak sama untuk
membedakan produk masing-masing (Wasitaatmadja, 1997).
g. Pengontrol pH
Penambahan asam lemak yang lemah, misalnya asam sitrat, dapat
menurunkan pH sabun (Wasitaatmadja, 1997).
h. Bahan tambahan khusus
Menurut Wasitaatmadja (1997), berbagai bahan tambahan untuk memenuhi
kebutuhan pasar, produsen, maupun segi ekonomi dapat dimasukkan ke dalam
formula sabun. Dewasa ini dikenal berbagai macam sabun khusus, misalnya:
1. Superfatty yang menambahkan lanolin atau paraffin.
2. Transparan yang menambahkan sukrosa dan gliserin.
3. Deodorant, yang menambahkan triklorokarbon, heksaklorofen, diklorofen,
triklosan, dan sulfur koloidal.
4. Antiseptik (medicated = carbolic) yang menambahkan bahan antiseptic,
misalnya: fenol, kresol, dan sebagainya.
6. Sabun netral, mirip dengan sabun bayi dengan konsentrasi dan tujuan yang
berbeda.
7. Apricot, dengan sabun menambahkan apricot atau monosulfiram.
2.1.3 Fungsi Sabun
Fungsi sabun dalam anekaragam cara adalah sebagai bahan pembersih.
Sabun menurunkan tegangan permukaan air, sehingga memungkinkan air itu
membasahi bahan yang dicuci dengan lebih efektif, sabun bertindak sebagai suatu
zat pengemulsi untuk mendispersikan minyak dan gemuk; dan sabun teradsorpsi
pada butiran kotoran (Keenan, 1980).
Kotoran yang menempel pada kulit umumnya adalah minyak, lemak dan
keringat. Zat-zat ini tidak dapat larut dalam air karena sifatnya yang non polar.
Sabun digunakan untuk melarutkan kotoran-kotoran pada kulit tersebut. Sabun
memiliki gugus non polar yaitu gugus –R yang akan mengikat kotoran, dan gugus
–COONa yang akan mengikat air karena sama-sama gugus polar. Kotoran tidak
dapat lepas karena terikat pada sabun dan sabun terikat pada air (Qisti, 2009).
2.1.4 Efek Samping Sabun pada Kulit
Sabun digunakan untuk membersihkan kotoran pada kulit baik berupa
kotoran yang larut dalam air maupun yang larut dalam lemak. Namun dengan
penggunaan sabun kita akan mendapatkan efek lain pada kulit, pembengkakan
dan pengeringan kulit, denaturasi protein dan ionisasi, antimikrobial,
a. Daya Alkalinisasi Kulit
Daya alkalinisasi sabun dianggap sebagai faktor terpenting dari efek
samping sabun. Reaksi basa yang terjadi pada sabun konvensional yang
melepaskan ion OH sehingga pH larutan sabun ini berada antara 9-12 dianggap
sebagai penyebab iritasi pada kulit. Bila kulit terkena cairan sabun, pH kulit akan
naik beberapa menit setelah pemakaian meskipun kulit telah dibilas dengan air.
Pengasaman kembali terjadi setelah 5-10 menit, dan setelah 30 menit pH kulit
menjadi normal kembali. Alkalinisasi dapat menimbulkan kerusakan kulit bila
kontak berlangsung lama, misalnya pada tukang cuci, dokter, pembilasan tidak
sempurna, atau pH sabun yang sangat tinggi. Efek alkalinisasi pada sabun
sintetik sudah jauh berkurang karena sabun sintetik memakai berbagai bahan
yang tidak alkalis. Berbagai penelitian mengenai daya iritasi sabun pada kulit
akibat pH sabun yang tinggi telah banyak dilakukan. Pada tahun-tahun terakhir
beberapa peneliti membuktikan bahwa sifat iritasi sabun berada di kulit setelah
dibilas dan bagaimana absorpsi kulit terhadap sabun (Wasitaatmadja, 1997).
b. Daya Pembengkakan dan Pengeringan Kulit
Kontak air (pH) pada kulit yang lama akan menyebabkan lapisan tanduk
kulit membengkak akibat kenaikan permeabilitas kulit terhadap air. Cairan yang
mengandung sabun dengan pH alkalis akan mempercepat hilangnya mantel asam
pada lemak kulit permukaan sehingga pembengkakan kulit akan terjadi lebih
cepat. Marchionini dan Schade (1928), yang meneliti hal tersebut menyatakan
bahwa kelenjar minyak kulit berperan dalam membentuk keasaman kulit dengan
sabun, deterjen sintetik juga dapat mengganggu lapisan lemak permukaan kulit
yang agak asam. Seperti air dan sabun, deterjen sintetik juga dapat mengganggu
lapisan lemak permukaan kulit dalam kapasitas yang lebih kecil. Besarnya
kerusakan lapisan lemak kulit yang terjadi bergantung pada: temperatur,
konsentrasi, waktu kontak, dan tipe kulit pemakai. Kerusakan lapisan lemak kulit
dapat meningkatkan permeabilitas kulit sehingga mempermudah benda asing
menembus ke dalamnya. Bergantung pada lama kontak dan intensitas
pembilasan, maka cairan sabun dapat diabsorpsi oleh lapisan luar kulit sehingga
dapat tetap berada di dalam kulit sesudah dibilas. Kerusakan lapisan lemak kulit
dapat menambah kekeringan kulit akibat kegagalan sel kulit mengikat air.
Pembengkakan kulit inisial akan menurunkan pula kapasitas sel untuk menahan
air sehingga kemudian terjadi pengeringan yang akan diikuti oleh kekenduran dan
pelepasan ikatan antarsel tanduk kulit. Kulit tampak kasar dan tidak elastis.
Terjadi pula peningkatan permeabilitas stratum korneum terhadap larutan kimia
yang iritan. Inilah yang sering dirasakan pada kulit oleh mereka yang sering dan
lama berhubungan dengan deterjen (rasa deterjen). Penambahan sabun/deterjen
dengan bahan-bahan pelumas (superfatty) dapat mengurangi efek ini
(Wasitaatmadja, 1997).
c. Daya Denaturasi Protein dan Ionisasi
Reaksi kimia sabun dapat mengendapkan ion kalsium (K) dan magnesium
(Mg) di lapisan atas kulit. Pada kulit yang kehilangan lapisan tanduk,
pengendapan K+ dan Mg+ akan mengakibatkan reaksi alergi. Pengendapan K+ dan
sehingga menimbulkan infeksi oleh kuman yang larut dalam minyak. Berbeda
dengan sabun, deterjen sintetik tidak menimbulkan pengendapan itu, namun
iritasi kulit dapat terjadi karena adanya gugus SH akibat denaturasi keratin. Pada
keratin normal tidak ada gugus merkapto (SH) bebas, dan adanya deterjen dapat
melepas gugus ini dari sistein dan sistin (Wasitaatmadja, 1997).
d. Daya Antimikrobial
Sabun yang mengandung surfaktan, terutama kation, mempunyai daya
antimikroba, apalagi bila ditambah bahan antimikroba. Daya antimikroba ini
terjadi pula akibat kekeringan kulit, pembersihan kulit, oksidasi di dalam sel
keratin, daya pemisah surfaktan, dan kerja mekanisme air (Wasitaatmadja, 1997).
e. Daya Antiperspirasi
Kekeringan kulit juga dibantu oleh penekanan perspirasi. Pada percobaan
dengan larutan natrium lauril sulfat, didapat penurunan produksi kelenjar keringat
antara 25-75% (Wasitaatmadja, 1997).
f. Lain-lain
Efek samping lain berupa dermatitis kontak iritan, dermatitis kontak
alergik, atau kombinasi keduanya. Sabun merupakan iritan lemah. Penggunaan
yang lama dan berulang akan menyebabkan iritasi, biasanya mulai di bawah
cincin yang tidak dicuci bersih, dan terjadi di dalam rumah tangga, bartender,
hairdresser, sehingga disebut sebagai soap atau housewife contact dermatitis.
Pembuktian efek iritasi sering kontroversial. Uji tempel konvensional dengan
dengan intensitas yang bervariasi. Reaksi alergi terhadap deterjen sintetik lebih
jarang, lebih mungkin terjadi secara kumulatif akibat penggunaan yang berulang
pada kulit yang sensitif (Wasitaatmadja, 1997).
2.1.5 Proses Pembuatan Sabun
Sabun dapat dibuat melalui dua proses, yaitu:
1. Saponifikasi
Saponifikasi melibatkan hidrolisis ikatan ester gliserida yang menghasilkan
pembebesan asam lemak dalam bentuk garam dan gliserol. Garam dari asam
lemak berantai panjang adalah sabun (Stephen, 2004).
Reaksi kimia pada proses saponifikasi adalah sebagai berikut:
2. Netralisasi
Netralisasi adalah proses untuk memisahkan asam lemak bebas dari minyak
atau lemak, dengan cara mereaksikan asam lemak bebas dengan basa atau
pereaksi lainnya sehingga membentuk sabun (Ketaren, 2008).
2.2 Sabun Mandi Padat
2.2.1 Pengertian Sabun Mandi Padat
Sabun mandi merupakan garam logam alkali (Na) dengan asam lemak dan
minyak dari bahan alam yang disebut trigliserida. Lemak dan minyak mempunyai
dua jenis ikatan, yaitu ikatan jenuh dan ikatan tak jenuh dengan atom karbon 8-12
yang berikatan ester dengan gliserin. Secara umum, reaksi antara kaustik dengan
gliserol dan sabun yang disebut dengan saponifikasi. Setiap minyak dan lemak
mengandung asam-asam lemak yang berbeda-beda. Perbedaan tersebut
menyebabkan sabun yang terbentuk mempunyai sifat yang berbeda. Minyak
dengan kandungan asam lemak rantai pendek dan ikatan tak jenuh akan
menghasilkan sabun cair. Sedangkan rantai panjang dan jenuh menghasilkan
sabun yang tak larut pada suhu kamar (Andreas, 2009).
Sabun mandi merupakan senyawa natrium atau kalium dengan asam
lemak yang digunakan sebagai bahan pembersih tubuh, berbentuk padat, berbusa,
dengan atau penambahan lain serta tidak menyebabkan iritasi pada kulit (SNI,
1994).
Menurut Keenan (1980), dalam pembuatan sabun, lemak dipanasi dalam
ketel besi yang besar dengan larutan natrium hidroksida dalam air, sampai lemak
itu terhidrolisis sempurna. Pereaksi semacam itu sering disebut penyabunan
(latin, sapo adalah sabun), karena reaksi itu telah digunakan sejak zaman Romawi
kuno untuk mengubah lemak dan minyak menjadi sabun. Persamaan untuk reaksi
itu adalah:
(RCO2)3C3H3 + 3NaOH 3RCO2Na + C3H5(OH)3
Jika lemak/minyak dihidrolisis, akan terbentuk gliserol dan asam lemak
yang dengan adanya Na(NaOH) akan terbentuk sabun karena sabun merupakan
garam Na atau K dari asam lemak. Sabun Na dan K larut dalam air, sedangkan
Ca dan Mg tidak larut. Sabun Na (sabun keras) digunakan untuk mencuci dan
sabun K (sabun lunak) digunakan untuk sabun mandi (Panil, 2008).
2.2.2 Syarat Mutu Sabun Mandi
Syarat mutu sabun mandi menurut Standar Nasional Indonesia
06-3235-1994 dapat dilihat pada Tabel 1.
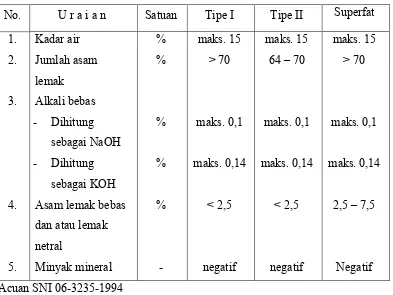
Tabel 1. Syarat Mutu Sabun Mandi
No. U r a i a n Satuan Tipe I Tipe II Superfat
Kadar air merupakan bahan yang menguap pada suhu dan waktu tertentu.
dihasilkan cukup keras sehingga lebih efisien dalam pemakaian dan sabun tidak
mudah larut dalam air. Kadar air akan mempengaruhi kekerasan dari sabun
(Qisti, 2009).
2. Jumlah Asam Lemak
Jumlah asam lemak merupakan jumlah total seluruh asam lemak pada
sabun yang telah atau pun yang belum bereaksi dengan alkali. Sabun yang
berkualitas baik mempunyai kandungan total asam lemak minimal 70%, hal ini
berarti bahan-bahan yang ditambahkan sebagai bahan pengisi dalam pembuatan
sabun kurang dari 30%. Tujuannya untuk meningkatkan efisiensi proses
pembersihan kotoran berupa minyak atau lemak pada saat sabun digunakan.
Bahan pengisi yang biasa ditambahkan adalah madu, gliserol, waterglass, protein
susu dan lain sebagainya. Tujuan penambahan bahan pengisi untuk memberikan
bentuk yang kompak dan padat, melembabkan, menambahkan zat gizi yang
diperlukan oleh kulit (Qisti, 2009).
3. Alkali Bebas
Alkali bebas merupakan alkali dalam sabun yang tidak diikat sebagai
senyawa. Kelebihan alkali bebas dalam sabun tidak boleh lebih dari 0,1% untuk
sabun Na, dan 0,14% untuk sabun KOH karena alkali mempunyai sifat yang
keras dan menyebabkan iritasi pada kulit. Kelebihan alkali bebas pada sabun
dapat disebabkan karena konsentrasi alkali yang pekat atau berlebih pada proses
penyabunan. Sabun yang mengandung alkali tinggi biasanya digunakan untuk
4. Asam Lemak Bebas
Asam lemak bebas merupakan asam lemak pada sabun yang tidak terikat
sebagai senyawa natrium atau pun senyawa trigliserida (lemak netral). Tingginya
asam lemak bebas pada sabun akan mengurangi daya membersihkan sabun,
karena asam lemak bebas merupakan komponen yang tidak diinginkan dalam
proses pembersihan. Sabun pada saat digunakan akan menarik komponen asam
lemak bebas yang masih terdapat dalam sabun sehingga secara tidak langsung
mengurangi kemampuannya untuk membesihkan minyak dari bahan yang
berminyak (Qisti, 2009).
5. Minyak Mineral
Minyak mineral merupakan zat atau bahan tetap sebagai minyak, namun
saat penambahan air akan terjadi emulsi antara air dan minyak yang ditandai
dengan kekeruhan. Minyak mineral adalah minyak hasil penguraian bahan
organik oleh jasad renik yang terjadi berjuta-juta tahun. Minyak mineral sama
dengan minyak bumi beserta turunannya. Contoh minyak mineral adalah: bensin,
minyak tanah, solar, oli, dan sebagainya. Kekeruhan pada pengujian minyak
mineral dapat disebabkan juga oleh molekul hidrokarbon dalam bahan (Qisti,
2009).
2.3 Alkali Bebas
2.3.1 Pengertian Alkali Bebas
Alkali bebas merupakan alkali dalam sabun yang tidak diikat sebagai
sabun Na dan 0,14% untuk sabun KOH karena alkali mempunyai sifat yang keras
dan menyebabkan iritasi pada kulit. Kelebihan alkali bebas pada sabun dapat
disebabkan karena konsentrasi alkali yang pekat atau berlebih pada proses
penyabunan. Sabun yang mengandung alkali tinggi biasanya digunakan untuk
sabun cuci (Qisti, 2009).
Mutu sabun sangat ditentukan oleh kadar alkali bebas di dalamnya. Jika
terlalu basa alkali bebas dapat merusak kulit bila dipakai. Oleh karena itu, kadar
alkali bebasnya tidak boleh lebih dari 0,1% untuk sabun Na dan 0,14% untuk
sabun KOH. Kadar alkali bebas juga dapat dipakai sebagai indikator dari tidak
sempurnanya proses penyabunan (Nandawai, 2009).
2.3.2 Efek Samping Alkali pada Kulit
Alkali juga dapat merusak kulit dibandingkan dengan menghilangkan
bahan berminyak dari kulit. Sungguh pun demikian dalam penggunaan sabun
dengan air akan terjadi proses hidrolis sehingga mendapatkan sabun yang baik
maka diukur sifat alkalisnya yakni pH 5,8-10,5. Pada kulit yang normal
kemungkinan pengaruh alkali lebih banyak. Beberapa penyakit kulit sensitif
terhadap reaksi alkalis, dalam hal ini pemakaian cairan sabun merupakan kontra
indikasi. pH kulit normal antara 3-6, tetapi bila dicuci dengan sabun pH menjadi
9, walaupun kulit cepat bertukar kembali menjadi normal mungkin ini tidak
2.3.3 Kandungan Alkali pada Sabun
Kandungan alkali yang cukup besar menandakan bahwa produk sabun
yang dihasilkan memiliki kualitas yang kurang baik, karena semakin besar
kandungan / kadar alkali dalam produk sabun yang dihasilkan maka kualitas
produk yang dihasilkan pun semakin menurun kualitasnya. Akan tetapi, produk
sabun yang bebas alkali pun tidak berarti bahwa kualitasnya lebih baik. Sabun
yang bebas alkali justru dapat menyebabkan kerusakan kulit (Zaelana, 2011).
2.4 Metode Titrimetri
Titrimetri atau analisis volumetri adalah pemeriksaan jumlah zat yang
didasarkan pada pengukuran volume larutan pereaksi yang dibutuhkan untuk
bereaksi secara stoikiometri dengan zat yang ditentukan (Rivai, 1995).
2.4.1 Penggolongan Titrimetri
Analisis secara titrimetri (volumetri) dapat digolongkan sebagai berikut:
a. Berdasarkan reaksi kimia
Berdasarkan reaksi yang terjadi selama titrasi, volumetri dapat
dikelompokkan menjadi 4 jenis:
1. Reaksi asam-basa (asidi-alkalimetri = netralisasi)
Penetapan kadar ini berdasarkan pada perpindahan proton dari zat
yang bersifat asam atau basa, baik dalam lingkungan air ataupun dalam
2. Reaksi oksidasi-reduksi (redoks)
Dasar yang digunakan adalah perpindahan elektron. Penetapan kadar
senyawa berdasarkan reaksi ini digunakan secara luas seperti
permanganometri, serimetri, iodi-iodometri, iodatometri, serta
bromatometri.
3. Reaksi pengendapan (presipitasi)
Penetapan kadar berdasarkan pada terjadinya endapan yang sukar larut
misalnya pada penetapan kadar secara argentometri.
4. Reaksi pembentukan kompleks
Dasar yang digunakan adalah terjadinya reaksi antara zat-zat
pengkompleks organik dengan ion logam menghasilkan senyawa
kompleks yang mantap. Penetapan kadar yang menggunakan prinsip ini
adalah metode kompleksometri.
b. Berdasarkan cara titrasi
Teknik volumetri berdasarkan cara titrasinya dapat dikelompokkan
menjadi:
1. Titrasi langsung
Cara ini dilakukan dengan melakukan titrasi langsung terhadap zat
yang akan ditetapkan. Cara ini mudah, cepat, dan sederhana.
2. Titrasi kembali
Dilakukan dengan cara penambahan titran dalam jumlah berlebihan,
kemudian kelebihan titran dititrasi dengan titran lain. Pada cara ini ada 2
menjadi lebih besar. Disamping itu cara ini juga memakan waktu yang
lama.
c. Berdasarkan jumlah sampel
Menurut Rohman (2007), berdasarkan jumlah sampel, teknik volumetri
dibedakan menjadi:
1. Titrasi makro
- Jumlah sampel : 100 – 1000 mg
- Volume titran : 10 – 100 ml
- Ketelitian buret : 0,02 ml
2. Titrasi semi mikro
- Jumlah sampel : 10 – 100 mg
- Volume titran : 1 – 10 ml
- Ketelitian buret : 0,001 ml
3. Titrasi mikro
- Jumlah sampel : 1 – 100 mg
- Volume titran : 0,1 – 1 ml
- Ketelitian buret : 0,001 ml
2.4.2 Asidimetri-Alkalimetri
Asidimetri dan alkalimetri termasuk reaksi netralisasi yakni reaksi antara
ion hidrogen yang berasal dari asam dengan ion hidroksida yang berasal dari basa
untuk menghasilkan air yang bersifat netral. Netralisasi dapat juga dikatakan
sebagai reaksi antara donor proton (asam) dengan penerima proton (basa)
Asidimetri merupakan penetapan kadar secara kuantitatif terhadap
senyawa-senyawa yang bersifat basa dengan menggunakan baku asam.
Sebaliknya alkalimetri adalah penetapan kadar senyawa-senyawa yang bersifat
asam dengan menggunakan baku basa (Rohman, 2007).
Titrasi Langsung Asam-Basa Dalam Larutan Air
1. Titrasi asam kuat/basa kuat
Pada awal titrasi perubahan nilai pH berlangsung lambat sampai
menjelang titik ekivalen. Pada saat titik ekivalen, nilai pH meningkat secara
drastis. Untuk mengamati titik akhir titrasi dapat digunakan indicator atau
menggunakan metode elektrokimia.
Suatu indikator merupakan asam atau basa lemah yang berubah warna
diantara bentuk terionisasinya dan bentuk tidak terionisasinya. Kisaran
penggunaan indikator adalah 1 unit pH disekitar nilai pKa-nya. Sebagai contoh
fenolftalein (pp), mempunyai pKa 9,4 (perubahan warna antara pH 8,4 – 10,4).
Struktur fenolftalein akan mengalami penataan ulang pada kisaran pH ini karena
proton dipindahkan dari struktur fenol dari pp sehingga pH-nya meningkat
akibatnya akan terjadi perubahan warna. Metil orange (MO) mempunyai pKa 3,7
(perubahan warna antara pH 2,7 dan pH 4,7), mengalami hal yang serupa terkait
dengan perubahan warna yang tergantung pada pH. Kedua indikator ini berada
pada kisaran titik balik (titik infeksi) pada titrasi asam kuat dan basa kuat.
2. Titrasi asam lemah dengan basa kuat dan titrasi basa lemah dengan asam kuat
Jika sejumlah kecil volume asam kuat atau basa kuat ditambahkan pada
1 unit pH, di bawah atau di atas nilai pKa. Seringkali pelarut organik yang dapat
campur dengan air, seperti etanol ditambahkan untuk melarutkan analit sebelum
dilakukan titrasi.
3. Titrasi tidak langsung dalam pelarut air
Titrasi tidak langsung ini dapat dilakukan untuk titrasi asam kuat/basa
kuat, titrasi asam lemah dengan basa kuat, ataupun titrasi basa lemah dengan
asam kuat. Contoh yang paling umum dilakukan adalah titrasi asam lemah
dengan basa kuat (Rohman, 2007; Watson, 2009).
BAB III
METODE PERCOBAAN
3.1Tempat Pengujian
Pengujian penetapan kadar alkali bebas pada sabun mandi padat secara
titrimetri dilakukan di Laboratorium Kosmetik, Balai Besar Pengawas Obat dan
Makanan di Medan yang berada di Jalan Willem Iskandar Pasar V Barat I No. 2
Medan.
3.2Alat
Alat yang digunakan pada pengujian ini adalah erlenmeyer, timbangan
analitik, mikoburet, beaker gelas, hot plate, pipet tetes, spatula, dan gelas ukur.
3.3Bahan
Bahan yang digunakan pada pengujian ini adalah alkohol netral, HCl 0,1 N
dalam alkohol, KOH 0,1 N dalam alkohol.
3.4 Sampel
Nama sampel : Herborist
Wadah/kemasan : Plastik
Pabrik : PT. Victoria Care Indonesia
Nomor bets : F0524A1
Nomor registrasi : POM NA 18100500004
Komposisi : Water, Coconut Oil, Palm Oil, Myristic Acid,
Sodium Hydroxide, Sodium Laureth Sulfate,
Stearic Acid, Lauryl Triethanolamine, Perfume,
BHT.
Kode sampel : 61/D1
3.5 Prosedur
3.5.1 Pembuatan Pereaksi
- Pembuatan Alkohol Netral
Siapkan alkohol netral 200 ml masukkan kedalam beaker gelas 300 ml.
Tambahkan 1 ml penunjuk fenolptalein. Kemudian netralkan dengan KOH 0,1 N
dalam alkohol.
- Pembakuan Larutan HCl 0,1 N (BM = 36,46)
Tiap 1000 ml larutan mengandung 36,46 gram HCl. Timbang seksama
lebih kurang 0,075 gram baku primer natrium karbonat anhidrat yang sebelumnya
telah dipanaskan pada suhu 270ºC selama 1 jam. Larutkan dalam 10 ml air dan
tambahkan 2 tetes merah metil LP. Tambahkan asam perlahan-lahan dari buret.
Sambil diaduk hingga larutan berwarna merah muda pucat. Panaskan larutan
hingga mendidih, dinginkan dan lanjutkan titrasi. Panaskan lagi hingga mendidih,
dan titrasi lagi bila perlu hingga warna merah muda pucat tidak hinag dengan
pendidihan lebih lanjut. Hitung normalitas larutan.
3.5.2 Persiapan Contoh Uji
Contoh sabun yang akan diuji dipotong-potong halus secepat mungkin
dan segara masukkan ke dalam botol bertutup asah dan campur serba sama dan
segera digunakan untuk pengujian untuk menghindari kemungkinan menguapnya
air.
3.5.3 Cara Uji Sampel
1. Siapkan alkohol netral dengan mendidihkan 100 ml alkohol dalam labu
erlenmeyer 250 ml, tambahkan 0,5 ml penunjuk fenolptalein dan dinginkan
sampai suhu 70ºC kemudian netralkan dengan KOH 0,1 N dalam alkohol.
2. Timbang dengan teliti lebih kurang 5 g contoh dan masukkan kedalam alkohol
netral diatas, tambahkan batu didih, pasang pendingin tegak dan panasi agar
cepat larut diatas penangas air, didihkan selama 30 menit. Bila contoh sabun
mengandung banyak bagian yang tidak larut, agar tidak mengganggu, saring
dahulu sebelum titrasi dilakukan.
3. Apabila petunjuk fenolptalein berwarna merah maka larutan tersebut bersifat
basa dan yang diperiksa adalah alkali bebas dengan menitarnya menggunakan
3.6Interpretasi Hasil
Kadar alkali bebas dalam sampel dihitung dengan menggunakan rumus:
Kadar alkali bebas dihitung NaOH = VxNx0,04
W x 100 %
Kadar alkali bebas dihitung KOH = VxNx0,0561
W x 100 %
Keterangan : V = HCl yang dipergunakan, ml
N = Normalitas HCl yang dipergunakan W = Berat contoh, gram
40 = berat setara NaOH
BAB IV
HASIL DAN PEMBAHASAN
4.1Hasil
Pada percobaan penetapan kadar alkali bebas pada sabun mandi sediaan
padat dengan metode titrimetri, diketahui bahwa sabun mandi sediaan padat yang
diuji mengandung alkali bebas dengan kadar 0,05%. Contoh perhitungan hasil
pengujian dapat dilihat pada Lampiran 2 halaman 33.
4.2Pembahasan
Dari hasil pengujian yang dilakukan, diketahui bahwa kadar alkali bebas
yang diperoleh pada sampel Herborist adalah 0,05%. Hasil ini masih memenuhi
persyaratan sesuai yang tertera pada Standar Nasional Indonesia 06–3532–1994
ditetapkan bahwa kadar alkali bebas pada sabun mandi padat yang dianalisis
tersebut tidak lebih dari 0,14%.
Pada pengujian kadar alkali bebas pada sampel Herborist menggunakan
metode titrimetri dengan pelarut alkohol netral, indikator yang digunakan
fenolfthalein dan pentiter yang digunakan HCl 0,1 N dalam alkohol. Sampai
BAB V
KESIMPULAN DAN SARAN
5.1 Kesimpulan
Dari hasil percobaan penetapan kadar alkali bebas pada sabun mandi
sediaan padat dengan metode titrimetri, diketahui bahwa sabun mandi sediaan
padat yang diuji mengandung alkali bebas dengan kadar 0,05%, memenuhi
persyaratan kadar alkali bebas sesuai dengan SNI 06–3532–1994 yaitu tidak lebih
dari 0,14%.
5.2. Saran
Disarankan kepada peneliti selanjutnya untuk melakukan penetapan kadar
alkali bebas pada produk sabun mandi lainnya agar dapat dijadikan perbandingan.
Sebaiknya dilakukan uji parameter lain agar kita dapat mengetahui apakah sabun
mandi yang beredar dipasaran telah memenuhi syarat mutu sabun mandi menurut
SNI 06-3532-1994. Hal tersebut sangat dibutuhkan untuk mengetahui layak atau
DAFTAR PUSTAKA
Achmad, R. (2004). Kimia Lingkungan. Jakarta: Universitas Negeri Jakarta. Hal. 111.
Andreas, H. (2009). Membuat Sabun 2 Laporan Ilmiah. Diakses pada tanggal 1 April 2013.
Anonima. Surfaktan. Available from: http://id.m.wikipedia.org. Diakses pada tanggal 16 April 2013.
Anonimb. Antioksidan. Available from: http://www.kampusku. Diakses pada tanggal 16 April 2013.
Anonimc. Deodoran. Available from: http//abdisr.blogspot.com. Diakses pada tanggal 16 April 2013.
Keenan, C.W., Donal, C.K., dan Jaesse, H.W. (1980). Kimia Untuk Universitas. Edisi keenam Jilid 2. Jakarta: Penerbit Erlangga. Hal. 198.
Ketaren, S. (2008). Minyak dan Lemak Pangan. Jakarta: UI-Press. Hal. 206.
Nandawai. Sabun Cair dengan Bahan Aktif Lidah Buaya. Available from:
Diakses pada tanggal 9 April 2013.
Panil, Z. (2008). Memahami Teori Dan Praktik Biokimia Dasar Medis. Padang: EGC. Hal. 28.
Qisti, R. (2009). Sifat Kimia Sabun Transparan dengan Penambahan Madu pada
Konsentrasi yang Berbeda. Available from:
23 Maret 2013.
Rivai, H. (1995). Asas Pemeriksaan Kimia. Jakarta: UI-Press. Hal. 49.
Rohman, A. (2007). Kimia Farmasi Analisis. Yogyakarta: Pustaka Pelajar. Hal. 124, 136, 140.
Sari, L. (2003). Sabun Obat. Available from:
Maret 2013
Wasitaatmadja, S. (1997). Penuntun Ilmu Kosmetik Medik. Jakarta: Penerbit Universitas Indonesia. Hal. 98-103.
Watson, D. (2009). Analisis Farmasi: Buku Ajar untuk Mahasiswa Farmasi dan
Praktisi Kimia Farmasi. Edisi 2. Jakarta: Penerbit Buku Kedokteran. Hal.
71-76.
Wilbraham, A. (1992). Pengantar Kimia Organik dan Hayati. Bandung: ITB. Hal. 143.
Zaelana, Y. Saponifikasi. Available from
LAMPIRAN
Lampiran 1
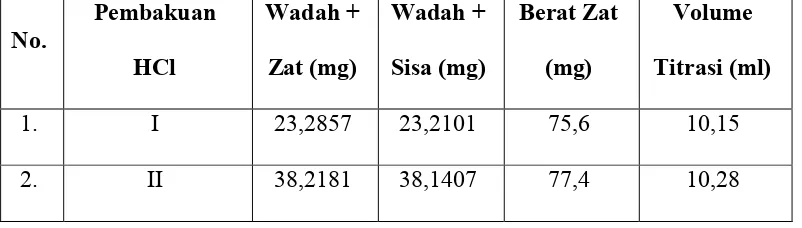
Data Penimbangan dan Perhitungan Pembakuan HCl dan KOH Tabel 2. Data Pembakuan HCl
No.
I. Perhitungan Pembakuan HCl
1. Diketahui : N HCl = 0,1 N
1 ml HCl 1N = 52,99 mg natrium karbonat anhidrat
Perhitungan :
1 ml HCl 1N = 52,99 mg natrium karbonat anhidrat
Perhitungan :
Vtitrasi x N = Berat Zat (mg)5
10,28 x N = 77,4
Normalitas HCl = 0,1414 N
Perhitungan:
Volume KOH x Normalitas KOH = Volume HCl x Normalitas HCl
10,76 x N.KOH = 5 x 0,1414 N
N.KOH = 0,0657 N
2. Diketahui: Volume HCl = 5 ml
Volume titrasi = 10,19 ml
Normalitas HCl = 0,1414 N
Perhitungan:
Volume KOH x Normalitas KOH = Volume HCl x Normalitas HCl
Lampiran 2
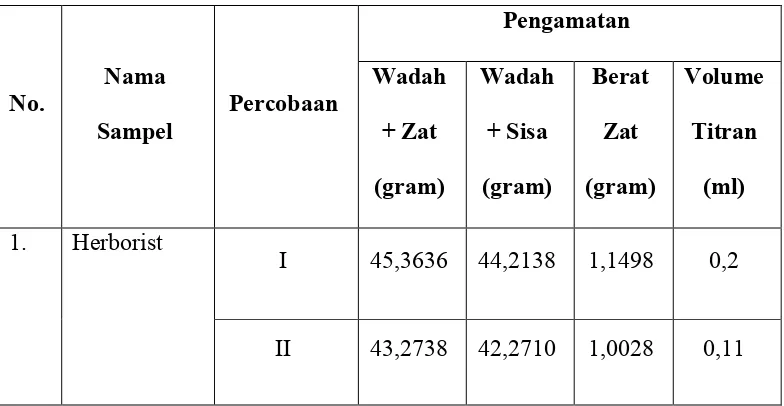
Tabel 3. Data Penetapan Kadar Alkali Bebas dalam Sabun Mandi Padat
No.
Perhitungan Kadar Alkali Bebas
Kadar Alkali Bebas Sabun Mandi Padat Herborist
Rata – rata Kadar Asam Lemak Bebas = 0,0658 % +0,0415 %