PENGARUH PENAMBAHAN PUPUK UREA TERHADAP
KANDUNGAN NITRIT PADA TANAMAN BAYAM
(
Amarantus Tricolor
) SETELAH DIMASAK
SELAMA LIMA MENIT
SKRIPSI
DANI EFENDI GIRSANG
080822043
DEPARTEMEN KIMIA
FAKULTAS MATEMATIKA DAN ILMU PENGETAHUAN ALAM
UNIVERSITAS SUMATERA UTARA
PENGARUH PENAMBAHAN PUPUK UREA TERHADAP
KANDUNGAN NITRIT PADA TANAMAN BAYAM
(
Amarantus Tricolor
) SETELAH DIMASAK
SELAMA LIMA MENIT
SKRIPSI
Diajukan untuk melengkapi tugas dan memenuhi syarat mencapai gelar Sarjana Sains
DANI EFENDI GIRSANG
080822043
DEPARTEMEN KIMIA
FAKULTAS MATEMATIKA DAN ILMU PENGETAHUAN ALAM
UNIVERSITAS SUMATERA UTARA
PERSETUJUAN
Judul : PENGARUH PENAMBAHAN PUPUK UREA TERHADAP KANDUNGAN NITRIT PADA TANAMAN BAYAM
(Amarantus Tricolor) SETELAH DI MASAK SELAMA LIMA MENIT
Kategori : SKRIPSI
Nama : DANI EFENDI GIRSANG NIM : 080822043
Program Studi : SARJANA (S1) KIMIA EKSTENSI Departemen : KIMIA
Fakultas : MATEMATIKA DAN ILMU PENGETAHUAN ALAM (FMIPA)
UNIVERSITAS SUMATERA UTARA
Disetujui
Medan , Desember 2011
Komisi Pembimbing
Dosen Pembimbing I Dosen Pembimbing II
Dr. Ribu Surbakti, MS Drs. Firman Sebayang, MS NIP : 194507061980031001 NIP : 195607261985031001
Diketahui / Disetujui oleh
Departemen Kimia FMIPA USU Ketua,
PERNYATAAN
PENGARUH PENAMBAHAN PUPUK UREA TERHADAP KANDUNGAN NITRIT PADA TANAMAN BAYAM (Amarantus Tricolor)
SETELAH DIMASAK SELAMA LIMA MENIT
SKRIPSI
Saya mengakui bahwa skripsi ini adalah hasil kerja saya sendiri, kecuali beberapa kutipan dan ringkasan yang masing- masing disebutkan sumbernya.
Medan, Desember 2011
PENGHARGAAN
Segala puji syukur penulis panjatkan kepada Tuhan Yang Maha Pengasih dan Penyayang atas berkat rahmatnya sehingga penulis dapat menyelesaikan penelitian dan penulisan skripsi dengan judul “ Pengaruh Penambahan Pupuk Urea Terhadap Kandungan Nitrit Pada Tanaman Bayam (Amarantus tricolor) Setelah di Masak selama 5 Menit ”,
yang merupakan salah satu syarat untuk memperoleh Gelar Sarjana di Fakultas MIPA- USU. Dengan penuh kasih sayang setulusnya penulis mengucapkan terimakasih yang tak terhingga kepada keluargaku tercinta, kedua orangtuaku, Bapak B. Girsang dan Mama M. Turnip atas kasih sayang, doa dan bantuan moril, material serta perhatian yang tulus kepada penulis selama perkuliahan sampai selesainya skripsi ini. Terimakasih juga buat kakak ku (Maria), adik- adikku (Suria, Junet, Talia) atas doa dan tawa yang selalu mengiringi langkah. Dengan segala kerendahan hati penulis juga mengucapkan terimakasih yang sebesar- besarnya kepada Dr. Ribu Surbakti MS dan Drs. Firman Sebayang MS (selaku Dosen pembimbing I dan II) yang dengan penuh kesabaran membimbing penulis selama melakukan penelitian hingga selesainya skripsi ini. Ucapan terimakasih juga ditujukan kepada Ketua Departemen Kimia, Dr. Rumondang Bulan Nst, MS, serta seluruh dosen Departemen Kimia FMIPA- USU, pegawai di FMIPA- USU dan rekan- rekan seperjuangan. Penulis menyadari sepenuhnya bahwa skripsi ini masih jauh dari sempurna oleh karena itu dengan segala kerendahan hati penulis mengharapkan kritik dan saran yang membangun demi kesempurnaan skripsi ini.
EFFECT OF UREA ADDITION ON NITRITE CONTENT IN SPINACH PLANE
ABSTRACT
Research on the analysis of levels of nitrite (NO2) on vegetable crops are needed to
determine the extent of the influence of nitrite on health.
Measurement of nitrite levels in kolorimetris with diazotisasi method using spectrophotometry equipment produces the purple dye reddish. The following color-beer lambert law and absorb light at a wavelength of 540 nm.
ABSTRAK
Penelitian tentang analisa kadar nitrit (NO2) pada tanaman sayur- sayuran sangat
dibutuhkan untuk mengetahui sejauh mana pengaruh nitrit terhadap kesehatan.
Pengukuran kadar nitrit secara kolorimetris dengan metode diazotisasi menggunakan alat spektrofotometri menghasilkan celupan yang berwarna ungu kemerah- merahan. Warna tersebut mengikuti hukum Lambert- Beer dan menyerap sinar pada panjang gelombang 540 nm.
DAFTAR ISI Bab 2. Tinjauan Pustaka
2.1. Sekilas Tentang Tanaman Bayam 4 2.2. Manfaat dan Bahaya Tanaman Bayam 7 2.3. Pupuk dan Pemupukan 8 2.4. Proses Kimia Pembuatan Urea 10 2.5. Kegunaan Pupuk Urea 11 2.6. Siklus Nitrogen di Alam 12 2.6.1. Sifat Fisik dan Struktur Kimia Senyawa Nitrat dan Nitrit 14 2.6.2. Dosis dan Kadar Normal 15 2.6.3. Analisa Nitrit dengan Metode Spektrofotometri 17 Bab 3. Alat dan Bahan
3.1. Alat- alat yang digunakan 19 3.2. Bahan- bahan yang digunakan 19 3.3. Prosedur Penelitian 20 3.3.1. Penyedian Larutan Pereaksi 20 3.3.2. Penyedian Larutan Stok Standart Nitrit 20 3.3.3. Pembuatan Kurva Kalibrasi 20 3.3.4. Prosedur Penanaman Bayam 21 3.3.5. Perlakuan Pada Sampel 21
3.4. Bagan Penelitian 22
Bab 4. Hasil dan Pembahasan 24
4.1. Hasil 24
4.2. Persamaan Garis Regresi untuk Kurva Kalibrasi
Larutan Standart Nitrit 25 4.3. Perhitungan Konsentrasi Nitrit Pada Sampel 26
4.4. Pembahasan 27
Bab 5. Kesimpulan dan Saran
5.1. Kesimpulan 28
5.2. Saran 28
Daftar Pustaka 29
DAFTAR TABEL
Halaman
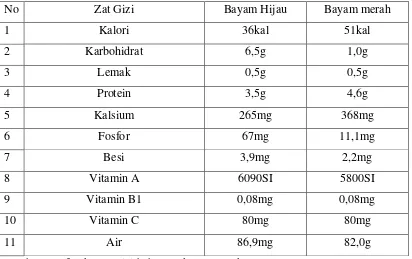
Tabel 2.1. Komposisi Zat Gizi 5
Tabel 4.1. Data Pengukuran Absorbansi Larutan Standar Nitrit (NO2) 12
Tabel 4.2. Data Perhitungan Garis Regresi Untuk Larutan Standar Nitrit (NO2) 25
Tabel 4.3. Data Perhitungan Konsentrasi Nitrit Pada Tanaman Bayam Yang di
DAFTAR GAMBAR
Halaman
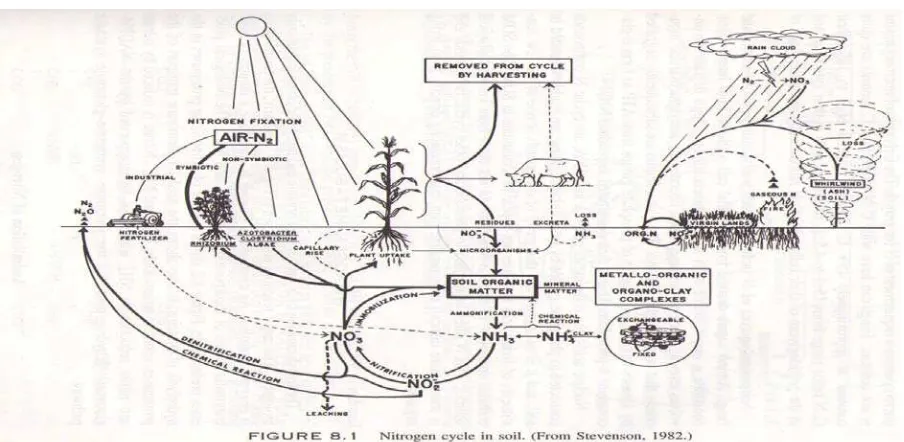
Gambar 2.1. Siklus Nitrogen 12
Gambar I. Kurva Kalibrasi Larutan Standar Nitrit (NO2-) 31
EFFECT OF UREA ADDITION ON NITRITE CONTENT IN SPINACH PLANE
ABSTRACT
Research on the analysis of levels of nitrite (NO2) on vegetable crops are needed to
determine the extent of the influence of nitrite on health.
Measurement of nitrite levels in kolorimetris with diazotisasi method using spectrophotometry equipment produces the purple dye reddish. The following color-beer lambert law and absorb light at a wavelength of 540 nm.
ABSTRAK
Penelitian tentang analisa kadar nitrit (NO2) pada tanaman sayur- sayuran sangat
dibutuhkan untuk mengetahui sejauh mana pengaruh nitrit terhadap kesehatan.
Pengukuran kadar nitrit secara kolorimetris dengan metode diazotisasi menggunakan alat spektrofotometri menghasilkan celupan yang berwarna ungu kemerah- merahan. Warna tersebut mengikuti hukum Lambert- Beer dan menyerap sinar pada panjang gelombang 540 nm.
BAB I
PENDAHULUAN
I.1. Latar Belakang
Pemberian kompos pada tanaman sayuran sangat penting untuk menyediakan hara yang
dibutuhkan tanaman. Sayuran memerlukan banyak sekali hara tanaman. Pemberian yang
terlalu banyak dapat mengakibatkan ketidakseimbangan hara pada tanaman, sehingga
mengakibatkan berlebihnya hara N dapat menjadi polusi lingkungan (Roostika,I,dkk. 2005)
Penelitian pemberian pupuk N pada tanaman bayam masih jarang dilakukan.
Bayam merupakan sayuran yang telah lama dikenal dan dibudidayakan secara luas oleh
petani di seluruh wilayah Indonesia, bahkan di negara lain. Hal ini terbukti dengan adanya
banyak nama untuk tanaman bayam ini.
Sosok tanaman bayam sangat mudah dikenali, yaitu berupa perdu yang tumbuh
tegak, batangnya tebal dan berserat dan sekulen, pada beberapa jenis mempunyai duri.
Daunnya bisa tebal atau tipis, besar atau kecil, berwarna hijau atau ungu kemerahan (pada
jenis bayam merah). Bunganya berrbentuk pecut, muncul di pucuk tanaman atau pada
ketiak daunnya. Bijinya berukuran sangat kecil berwarna hitam atau coklat dan mengkilap.
(Bandini Yusni. 2001)
Jangan pernah mengkonsumsi bayam lebih dari 5 jam, karena selain mengandung
zat Fe3+, bayam juga mengandung zat nitrat (NO3). Jika teroksidasi dengan udara, maka
akan menjadi nitrit (NO2). Nitrit adalah senyawa yang tidak berwarna, tidak berbau,
bersifat racun bagi tubuh manusia.
Menurut John S. Wishnok, bayam segar yang baru di cabut dari persemaiannya
telah mengandung senyawa nitrit kira- kira sebanyak 5 mg/ kg. Dengan kata lain, dalam 1
hari penyimpanan, senyawa nitrit akan meningkat 21mg/ kg (7%).
Nitrogen merupakan unsur hara yang paling sedikit terdapat dalam tanah. Tanaman
yang tumbuh ditanah yang kekurangan nitrogen menunjukan pertumbuhan yang lambat,
daunnya kuning, hasilnya rendah dan kadang- kadang kadar proteinnya rendah. Nitrat dan
nitrit merupakan bentuk nitrogen yang teroksidasi, dengan tingkat oksidasi masing- masing
+3 dan +5. Nitrit biasanya tidak bertahan lama dan merupakan keadaan sementara proses
oksidasi antara amoniak dan nitrat (Sianipar. 2001).
Penentuan kadar nitrat dan nitrit secara kolorimetris dengan menggunakan alat
spektrofotometri didasarkan pada reduksi nitrat menjadi nitrit. Senyawa nitrat di reduksi
menjadi nitrit oleh butiran cadmium yang di lapisi tembaga dalam suatu kolom. Senyawa
Nitrat yang terbentuk kemudian direaksikan dengan amin aromatik membentuk senyawa
diazo yang berwarna merah muda. Senyawa kompleks yang berwarna merah muda tersebut
kemudian ditentukan kadarnya dengan menggunakan spektrofotometer UV- Vis.
Dari keterangan diatas penulis tertarik mengamati “Pengaruh Penambahan Pupuk
Urea Terhadap Kandungan Nitrit Tanaman Bayam Dengan Perbandingan Variasi
Penambahan Pupuk Urea”.
1.2 Permasalahan
Apakah terdapat hubungan antara penambahan pupuk urea dengan kandungan nitrit pada
tanaman bayam setelah dimasak selama 5 menit.
1.3Pembatasan Masalah
Dalam Penelitian ini permasalahan dibatasi pada :
1. Pupuk yang digunakan adalah pupuk urea dengan penambahan variasi yang telah
ditentukan yaitu 0, 100, 200, 300, 400, 500/ 2m2
2. Parameter yang digunakan adalah kadar nitrit
3. Metode yang diguinakan adalah metode diazotisasi dengan menggunakan alat
spektrofotometer UV- Vis
1.4Tujuan Penelitian
Penelitian ini bertujuan untuk mengetahui pengaruh penambahan pupuk urea terhadap
1.5Manfaat Penelitian
Untuk memberikan informasi kepada masyrakat tentang pengaruh penambahan pupuk urea
terhadap kandungan nitrit pada tanaman bayam.
1.6 Lokasi Penelitian
Penelitian ini dilakukan :
1. Fakultas Pertanian USU
2. BTKL-PPM ( Balai Teknik Kesehatan Lingkungan - Pemberantasan Penyakit
Menular ), Jl. Wahid Hasyim.
1.7Metodologi Penelitian
Penelitian ini bersifat eksperimen laboratorium dimana metode penelitian dilakukan
dengan cara sebagai berikut
1. Sampel adalah bayam yang ditanam dengan penambahan pupuk urea yang telah
ditentukan.
2. Pengukuran nitrit (NO2) dalam bentuk N-NO2 dengan metode diazotisasi dimana
nitrit di komplekskan dengan pelarut nitrit yang terdiri dari sulfanil-amin dan naftil
BAB II
TINJAUAN PUSTAKA
2.1Sekilas Tentang Tanaman Bayam
Di Indonesia hanya dikenal dua jenis bayam budidaya, yaitu amaranthus tricolor
dan amarantus hybridus. Jenis amarantus tricolor biasa ditanam sebagai bayam
cabut dan terdiri dari dua varietas, yaitu bayam hijau (bayam putih, bayam sekul
atau bayam cina). Dan bayam merah karena tanamannya berwarna merah.
Amaranthus hybridus sering disebut bayam kakap, bayam tahun, atau bayam
bathok dan di tanam sebagai bayam petik. Di luar dari jenis bayam tersebut
merupakan bayam liar.
Berdasarkan cara penanamannya jenis bayam dibedakan menjadi bayam
cabut dan bayam petik. Bayam cabut adalah bayam yang di panen dengan cara di
cabut seluruh bagian tanaman beserta akar- akarnya. Bayam petik adalah bayam
yang pemanenannya di lakukan dengan cara dipetik daun atau pucuk daunnya saja
sehingga dapat dilakukan berulang kali sepanjang tanaman masih produktif.
Di tinjau dari segi kandungan gizinya, bayam merupakan jenis sayuran hijau
yang banyak manfaatnya bagi kesehatan dan pertumbuhan badan, terutama bagi
anak- anak dan para ibu yang sedang hamil. Di dalam daun bayam terdapat cukup
banyak kandungan protein, mineral kalsium, zat besi dan vitamin yang dibutuhkan
oleh tubuh manusia, Beberapa kegunaan gizi dalam daun bayam seperti vitamin B
dapat mencegah penyakit biri- biri, memperkuat syaraf, dan melenturkan otot
rahim. Dengan demikian konsumsi bayam sangat dianjurkan bagi ibu yang tengah
hamil untuk memudahkan persalinannya. Vitamin C sangat membantu
Manfat lain dari bayam yaitu akarnya dapat menjadi obat untuk
menghilangkan panas (antipretik), obat diare dan membersihkan darah.
Tabel 2.1. Komposisi zat gizi bayam per 100 g Bahan
No Zat Gizi Bayam Hijau Bayam merah
Sumber : Daftar komposisi bahan makanan, Depkes 1980
Bentuk tanaman bayam adalah terna (perdu), tinggi tanaman dapat mencapai 1,5 –
2 m, berumur semusin atau lebih. Sistem perakaran lebih menyebar dangkal pada
kedalaman antara 20 – 40 cm dan akar tunggang.
Daunnya berbentuk bulat telur dengan ujung agak meruncing mempunyai urat- urat
daun yang jelas.Warna daun variasi, mulai dari hijau muda, hijau tua, hijau keputih-
putihan, sampai berwarna merah. Daun bayam liar umumnya kasap (kasar) dan kadang
berduri.
Batang tumbuh tegak, tebal, berdaging dan banyak mengandung air, tumbuh tinggi
di atas permukaan tanah. Bayam tahunan mempunyai batang keras berkayu dan bercabang
banyak.
Bunga bayam berukuran kecil, berjumlah banyak, terdiri dari daun bunga 1- 5, dan
bakal buah 2- 3 buah. Bunga keluar dari ujung- ujung tanaman ketiak daun yang tersusun
Perkawinannya bersifat universal yaitu dapat menyerbuk sendiri maupun menyerbuk
silang. Penyerbukan berlangsung dengan bantuan angin.
Perkembangbiakan tanaman bayam umumya generatif (biji), biji berukuran sangat
kecil dan halus, berbentuk bulat, dan berwarna coklat tua mengkilap seperti hitam kelam.
Namun, ada beberapa jenis bayam yang mempunyai warna biji putih sampai merah,
misalnya bayam maksi yang bijinya merah. Setiap tanaman dapat menghasilkan biji kira-
kira 1200- 3000 biji/ gram. Pada tanaman bayam tahunan, perbanyakan dapat juga
dilakukan secara vegetatif dengan stek batang. Caranya potong bagian cabang muda
dengan panjang stek sekitar 15- 20 cm dan daun- daunnya di buang, kecuali yang masih
kuncup.
Penanaman
1. Waktu tanam
Tanaman bayam dapat tumbuh sepanjang musim. Namun, waktu tanam yang baik
untuk bayam cabut adalah awal musim hujan dan awal musim kemarau. Karena
pada saat itu, hama dan tanaman peyakit belum menyerang
2. Cara Tanam
Benih bayam disebar secara langsung di atas bendengan yang sudah di siapkan.
Kebutuhan benih untuk 1 Ha yaitu 5- 1 kg biji bayam atau sekitar , 5- 1 g/m2 lahan.
Benih disebar secara langsung dalam barisan dengan jarak antar barisan 20 cm agar
benih tidak terlalu rapat dan lebih teratur serta memudahkan penjarangan. Benih di
tanam pada kedalaman 1- 2 cm dan ditutup kembali dengan tanah tipis- tipis. Untuk
menjaga kelembapan tanah, lakukan penyiraman dengan hati- hati agar benih tidak
berantakan. Gunakan gembor yang siramannya halus. Bila tanah telah lembap,
penyiraman tidak perlu dilakukan. Benih akan berkecambah setelah 5-7 hari bila
persyaratan tumbuhnya terpenuhi
Untuk melindungi benih dari hujan deras dan hanyut bersama air maka benih
ditutup dengan mulsa jerami atau daun pisang. Jika tanaman sudah berkecambah
dan cukup kuat, mulsa dapat diangkat dari bendengan.
3. Pemeliharaan
a. Pemupukan
Salah satu usaha meningkatkan hasil dan kualitas tanaman bayam adalah
Pupuk organik merupakan pupuk alami yang berasal dari kotoran hewan,
kompos atau sisa- sisa tanaman hijau. Sedangkan pupuk anorganik merupakan
pupuk kimia seperti urea, TSP.
Dosis pupuk untuk tanaman bayam tiap hektarnya yaitu 100 kg urea. Pupuk
urea sebagai pupuk susulan diberikan setelah tanaman tumbuh setinggi 5cm.
Pemberian pupuk urea dapat dilakukan dengan cara dibenamkan atau disiram.
Pemupukan urea, sebaiknya dilakukan dengan cara dibenamkan atau disiram.
Pemupukan urea, sebaiknya dilakukan secara bertahap. Hal ini untuk mencegah
hilangnya pupuk nitrogen karena tercuci, menguap. Oleh karena itu, pada saat
musim hujan pemberian pupuk nitrogen dengan cara dibenamkan akan lebih
efektif agar tidak mudah terhanyut oleh air.
b. Pengairan
Pengairan merupakan syarat mutlak keberhasilan usaha tani tanaman bayam.
Tanaman bayam tidak menyukai keadaan tanah yang becek dan tergenang. Hal
ini akan menyebabkan akar menjadi busuk. Selain itu sirkulasi udara dalam
tanah menjadi kurang baik.
Pada musim hujan, penyiraman dapat di tiadakan karena kebutuhan air telah
terpenuhi melalui air hujan.
c. Penyiangan
Penyiangan dilakukan 2 minggu sekali, atau tergantung pada banyaknya gulma
yang tumbuh
d. Penjarangan
Penjarangan di lakukan setelah tanaman berumur 40 hari dan merupakan panen
pertama.
(Bandini Yusni. 2001)
2.2 Manfaat dan bahaya bayam
Bayam mengandung zat yang berupa Fe2+ (ferro), jikalau bayam terlalu lama berinteraksi
dengan O2 (oksigen), maka kandungan Fe2+ pada bayam akan teroksidasi menjadi Fe3+
(ferri). Meski sama- sama zat besi, yang bermanfaat untuk manusia adalah ferro, lain
halnya dengan ferri yang bersifat racun. Jadi jangan sekali- sekali untuk memanaskan sayur
Alangkah baiknya juga, kita harus segera mengkonsumsi bayam sesaat sudah
diolah, lebih baik hindari juga mengkonsumsi bayam yang sudah lebih dari 5 jam di atas
meja makan, karena selain mengandung zat ferri yang tadi disebutkan di atas, bayam
tersebut juga dapat mengandung zat nitrat (NO3) yang jika teroksidasi dengan udara juga
akan menjadi NO2 (nitrit) yang bersifat senyawa tidak berwarna, tidak berbau dan bersifat
racun.
Dalam proses penyimpanan di lemari es pun harus diperhatikan, karena semakin
lama bayam disimpan di dalam lemari es, senyawa nitrit pun akan terus meningkat
kadarnya. Efek racun pada nitrit menimbulkan reaksi dengan zat besi dalam sel darah
merah tepatnya di hemoglobin. Ikatan nitrit dengan hemoglobin disebut Methemoglobin
yang mengakibatkan hemoglobin tidak mampu mengikat oksigen. Jika jumlah
methemoglobin mencapai lebih dari 15% dari total hemoglobin, makan akan terjadi
Sianosis yang artinya keadaan dimana seluruh jaringan tubuh manusia kekurangan oksigen.
Secara umum, bayam dapat meningkatkan kinerja ginjal dan melancarkan
pencernaan. Daun bayam digunakan untuk membersihkan darah sehabis bersalin,
memperkuat akar rambut serta mengobati tekanan darah rendah, kurang darah (anemia)
dan gagal ginjal. Selain itu, sayur bayam memiliki khasiat untuk mencegah hilangnya
pengelihatan akibat usia yang menua (macular degeneration), penyakit kanker, katarak dan
bayi lahir cacat. Bayam adalah sumber lutein dan folate yang hebat, yang membantu
mencegah penyakit jantung & bayi yang lahir cacat.
Kandungan folic acid yang ada di bayam juga mampu melindungi otot jantung dari
meningkatnya kadar glukosa yang mudah larut dan mengandung B9. Vitamin ini biasanya
menjadi suplemen bagi perempuan yang mengandung untuk melindungi bayi dari cacat
pada bagian syaraf.
Manfaat Bayam lainnya, mengurangi pembentukan batu empedu sebab bayam kaya
magnesium di samping ikan, kacang almon kering, alpukat, pisang, kismis. Sayur bayam
juga memberikan zat besi pencegah anemia namun zat besi di dalam bayam tidak mudah
2.3 Pupuk dan Pemupukan
Pengertian pupuk secara umum adalah suatu bahan yang bersifat organik ataupun
anorganik, bila ditambahkan kedalam tanah atau tanaman, dapat memperbaiki sifat fisik,
kimia, biologi tanah dan dapat meningkatkan pertumbuhan tanaman.
Pemupukan berarti cara- cara atau metode serta usaha- usaha yang dilakukan dalam
pemberian pupuk atau unsur hara ke tanah atau tanaman yang sesuai dengan kebutuhan dan
pertumbuhan tanaman normal (Hasibuan. 2005)
Kita tidak mengharapkan bahwa pemberian pupuk, pada tanah yang kekurangan
unsur hara yang dibutuhkan untuk pertumbuhan dan perkembangan tanaman, dapat
memberikan pengaruh yang merugikan.
Kesimpang siuran pustaka tentang pengaruh pupuk terhadap kandungan zat gizi
sebagian besar disebabkan oleh keterkaitan yang rumit antar unsur dalam tanah. Pemberian
satu macam unsur dapat mempengaruhi ketersediaan unsur lain. Penambahan campuran
unsur dapat mengakibatkan berbagai pengaruh terhadap tanaman yang tumbuh pada tanah
itu. Karena sukarnya merancang percobaan dan bahkan lebih sukar lagi menafsirkan
hasilnya, masih belum jelas bahwa pupuk organik lebih baik dibandingkan pupuk
anorganik dalam menghasilkan makanan yang nilai gizinya lebih tinggi. (Endel karmas.
1989)
Sumber unsur nitrogen sebenarnya cukup banyak terdapat di atmosfir, yaitu lebih
kurang 79,2% dalanm bentuk N2 bebas, namun demikian unsur N ini baru dapat digunakan
oleh tanaman setelah mengalami perubahan kebentuk yang terikat yang kemudian dalam
bentuk pupuk.
Nitrogen memiliki jumlah yang sangat sedikit di dalam tanah, sehingga tanaman
sangat kesulitan untuk memperoleh nitrogen dalam bentuk nitrat dan asam amino untuk
pertumbuhan dan perkembangan tanaman itu sendiri. Untuk memenuhi kebutuhan nitrogen
bagi tanaman, maka dilakukan pemupukan nitrogen dengan menggunakan pupuk N yaitu
pupuk urea. Meski di dalam pupuk tersebut ada unsur yang lain akan tetapi nitrogen
mempunyai pengaruh yang paling menyolok dan cepat. Fungsi nitrogen bagi pertumbuhan
tanaman yaitu memperbaiki pertumbuhan vegetatif tanaman, tanaman berwarna hijau jika
tanaman memperoleh nitrogen yang cukup, dan pembentukan protein.
Tanaman tidak dapat membedakan dan tidak bisa memilih unsur hara yang diserap
sebagainya) melalui mekanisme pertukaran ion, dan dalam bentuk ion-ion anorganik. Agar
dapat diserap tanaman, pupuk organik harus melalui serangkaian proses perombakan oleh
mikroba dalam tanah menjadi ion-ion anorganik/kimia. Jadi yang diserap tanaman pada
akhirnya tetap saja berupa ion-ion anorganik / kimia. (Hardjowigeno 2007).
2.4 Proses kimia pembuatan urea
Pupuk urea yang dikenal dengan nama rumus kimianya NH2CONH2 pertama kali dibuat
secara sintetis oleh Frederich Wohler tahun 1928 dengan mereaksikan garam cianat dengan
ammonium hidroksida.
Pupuk urea yang dibuat PT Pusri merupakan reaksi antara karbon dioksida (CO2)
dan ammonia (NH3).Kedua senyawa ini berasal dari bahan gas bumi, air dan udara. Ketiga
bahan baku tersebut merupakan kekayaan alam yang terdapat di Sumatera Selatan.
Pada proses pembuatan amoniak dengan tekanan rendah dalam reaktor (±150
atmosfir) yaitu dengan reaksi reforming merubah CO menjadi CO2, penyerapan CO2 dan
metanasi. Reaksi reforming ini dilakukan dalam 2 tingkatan yaitu :
Gas bumi dan uap air direaksikan dengan katalis melalui piap-pipa vertikal dalam dapur
reforming pertama dan secara umum reaksi yang terjadi sebagai berikut:
Cn H2n + nH2O ---> NCO + (2n+1)H2 - panas
CH4 + H2O ---> CO + 3H2 - panas
Udara dialirkan dan bercampur dengan arus gas dari reformer pertama di dalam reformer
kedua, hal ini dimaksudkan untuk menyempurnakan reaksi reforming dan untuk
memperoleh campuran gas yang mengandung nitrogen (N)
2 CH4 + 3 O2 ---> 12 N2
2 CO + 4 H2O ---> 12 N2
lalu campuran gas sesudah reforming direaksikan dengan H2O di dalam converter CO
untuk mengubah CO menjadi CO2
CO + H2O ---> CO2 + H2
CO2 yang terjadi dalam campuran gas diserap dengan K2 CO3
K2 CO3 + CO2 + H2O ---> KHCO3
Setelah CO2 dipisahkan, maka sisa-sisa CO, CO2 dalam campuran gas harus dihilangkan
yaitu dengan cara mengubah zat-zat itu menjadi CH4 kembali
CO + 3H2 ---> CH4 + H2O
CO2 + 4H2 ---> CH4 + 2H2O
Lalu kita mensitesa nitrogen dengan hidrogen dalam suatu campuran ganda pada
tekanan 150 atmosfir dan kemudian dialirkan ke dalam converter amoniak.
N2 + 3H2 ---> 2NH3
Setelah didapatkan CO2 (gas) dan NH3 (cair), kedua senyawa ini direaksikan dalam
reaktor urea dengan tekanan 200-250 atmosfer.
2NH3 + CO2 ---> NH2COONH4 + Q
amoniak karbon dioksida ammonium karbamat
NH2COONH4 ---> NH2 CONH2 + H2O - Q
Reaksi ini berlangsung tanpa katalisator dalam waktu ±25 menit. Proses selanjutnya
adalah memisahkan urea dari produk lain dengan memanaskan hasil reaksi (urea, biuret,
ammonium karbamat, air dan amoniak kelebihan) dengan penurunan tekanan, dan
temperatur 120-165 derajat Celsius, sehingga ammonium karbamat akan terurai menjadi
NH3 dan CO2, dan kita akan mendapatkan urea berkonsentrasi 70-75%.
Untuk mendapatkan konsentrasi urea yang lebih tinggi maka dilakukan pemekatan dengan
cara:
1. Penguapan larutan urea di bawah vacuum (ruang hampa udara, tekanan 0,1 atmosfir
mutlak), sehingga larutan menjadi jenuh dan mengkristal.
2. Memisahkan kristal dari cairan induknya dengan centrifuge
3. Penyaringan kristal dengan udara panas
Untuk mendapatkan urea dalam bentuk butiran kecil, keras, padat maka kristal urea
dipanaskan kembali sampai meleleh dan urea cair lalu disemprotkan melalui nozzle-nozzle
kecil dari bagian atas menara pembutir (prilling tower).
Sementara tetesan urea yang jatuh melalui nozzle tersebut, dihembuskan udara
dingin ke atas sehingga tetesan urea akan membeku dan menjadi butir urea yang keras dan
2.5 Kegunaan pupuk urea
Unsur hara yang terkandung dalam pupuk urea sangat besar kegunaanya untuk
pertumbuhan dan perkembangan tanaman:
1. Membuat daun tanaman lebih hijau segar dan banyak mengandung butir hijau daun
(chlorophyl) yang mempunyai peranan sangat panting dalam proses fotosintesa
2. Mempercepat pertumbuhan tanaman (tinggi, jumlah anakan, cabang dan lain-lain)
3. Menambah kandungan protein tanaman
4. Dapat dipakai untuk semua jenis tanaman baik tanaman pangan, holtikultura, tanaman
perkebunan, usaha peternakan dan usaha perikanan.
Gejala kekurangan unsur hara nitrogen
1. Daun tanaman berwarna pucat kekuning-kunigan
2. Daun tua berwarna kekuning-kuningan dan pada tanaman padi warna ini dimulai
dari ujung daun menjalar ke tulang daun
3. Dalam keadaan kekurangan yang parah daun menjadi kering dimulai dari daun
bagian bawah terus ke bagian atas
4. Pertumbuhan tanaman lambat dan kerdil
5. Perkembangan buah tidak sempurna atau tidak baik, sering kali masak sebelum
waktunya.
2.6 Siklus Nitrogen di alam
Gas Nitrogen banyak terdapat di atmosfer, yaitu 80% dari udara. Nitrogen bebas
dapat ditambat difiksai terutama dari tumbuhan yang berbintil akar (misalnya jenis
polongan) dan beberapa jenis ganggang. Nitrogen bebas juga dapat bereaksi dengan
hidrogen ataupun oksigen dengan bantuan kilat petir. Nitrogen bebas mempunyai sifat
tidak mudah bereaksi, sehingga untuk memecahnya diperlukan energi yang tinggi seperti
contoh dengan bantuan kilat petir. Selain itu, nitrogen bebas ini diasimilasi oleh tumbuhan
lewat perakaran dalam bentuk nitrat.
Secara organik, nitrogen di udara dapat di ikat oleh beberapa mikroba (azotobacter,
rhizobium, dsb) menjadi bentuk nitrat yang dapat dimanfaatkan oleh tumbuhan. Nitrogen
yang diikat biasanya dalam bentuk amonia. Amonia di peroleh dari hasil penguraian
jaringan yang mati oleh bakteri. Amonia ini akan dinitrifikasi oleh bakteri nitrit yaitu
nitrosomonas dan nitrosococcus sehingga menghasilkan nitrat yang akan diserap oleh
tumbuhan. Selanjutnya oleh bakteri denitrifikan, nitrat diubah menjadi amonia kembali,
dan amonia diubah menjadi nitrogen yang dilepaskan ke udara. Dengan cara ini siklus
nitrogen akan berulang dalam ekosistem (Dwidjoseputro. 1987)
Nitrat (NO3-) dan nitrit (NO2-) adalah ion- ion organik alami yang merupakan
bagian dari siklus nitrogen. Aktifitas mikroba ditanah atau di air menguraikan sampah yang
mengandung nitrogen organik pertama- tama menjadi amonia, kemudian dioksidasikan
menjadi nitrit dan nitrat. Oleh karena nitrit dapat dengan mudah dioksidasikan menjadi
nitrat, maka nitrat adalah senyawa yang paling sering di temukan didalam air bawah tanah
maupun air yang terdapat dipermukaan. Pencemaran oleh pupuk nitrogen, termasuk
amonia anhidrat seperti juga sampah organik hewan maupun manusia, dapat meningkatkan
kadar nitrat didalam air.
Pada daerah dimana pupuk nitrogen secara luas digunakan, sumur-sumur
perumahan yang ada disana hampir pasti tercemar oleh nitrat. Diperkirakan 14 juta rumah
tangga di Amerika Serikat menggunakan sumur pribadi untuk memenuhi kebutuhan air
minumnya (Badan Sensus Amerika Serikat 1993). Pada daerah pertanian, pupuk nitrogen
merupakan sumber utama pencemaran terhadap air bawah tanah yang digunakan sebagai
air minum. Sebuah penelitian oleh United States Geological Survey menunjukkan bahwa >
8200 sumur di seluruh AS terkontaminasi oleh nitrat melebihi standar air minum yang
nitrat lainnya pada air sumur adalah pencemaran dari sampah organik hewan dan rembesan
dari septic tank.
Kandungan nitrat yang tinggi pada tanaman disebabkan oleh akumulasi nitrat dalam
jaringan pertumbuhan tanaman. Akumulasi nitrat pada bagian batang lebih tinggi daripada
dalam daun. Pada bagian batang, kandungan nitrat paling tinggi terdapat pada sepertiga
batang bagian bawah. Hal ini karena posisinya lebih dekat dengan permukaan tanah
sehingga akan lebih banyak mengabsorbsi nitrat. Pada musim kemarau, nitrat banyak yang
tidak terlarut atau tidak terbuang karena tidak ada hujan. Akibatnya, nitrat banyak yang
diserap tanaman. (Stoltenow dan lardy. 1998)
Nitrat dalam tanah diperlukan tanaman untuk pertumbuhan. Lebih dari 90% N
diserap tanaman dalam bentuk nitrat. Sumber N adalah pupuk, baik pupuk organik maupun
anorganik (pupuk kimia). Nitrogen dalam kedua jenis pupuk tersebut umumnya dalam
bentuk amonium (NH4+), yang kemudian dengan cepat diubah menjadi nitrat dalam tanah.
Oleh karena itu, pemberian pupuk yang berlebihan akan meningkatkan kandungan nitrat
dalam tanaman. Pembuangan kotoran kandang secara terus- menerus tanpa melalaui
saluran khusus kedalam tanah akan meningkatkan kandungan amonia dalam tanah.
Selanjutnya, melalui proses nitrifikasi, terjadi pembentukan nitrat- nitrit dari amonia dalam
tanah yang kemudian diserap oleh tanaman. (Cassel dan Barao. 2000)
2.6.1 Sifat Fisik dan Struktur Kimia Senyawa Nitrat dan Nitrit
Nitrat dibentuk dari asam nitrit yang berasal dari amonia melalui proses oksidasi katalitik,
Nitrit juga merupakan hasil metabolisme dari siklus nitrogen. Bentuk pertengahan dari
nitrifikasi dan denitrifikasi. Nitrat dan nitrit adalah komponen yang mengandung nitrogen
berikatan dengan atom oksigen, nitrat mengikat tiga atom oksigen sedangkan nitrit
mengikat dua atom oksigen. Di alam, nitrat sudah diubah menjadi bentuk nitrit atau bentuk
lainnya.
Pada kondisi yang normal baik nitrit maupun nitrat adalah komponen yang stabil,
tetapi dalam suhu yang tinggi akan tidak stabil dan dapat meledak pada suhu yang sangat
tinggi dan tekanan yang sangat besar. Biasanya, adanya ion klorida, bahan metal tertentu
dan bahan organik akan mengakibatkan nitrat dan nitrit menjadi tidak stabil. Jika terjadi
kebakaran, maka tempat penyimpanan nitrit maupun nitrat sangat berbahaya untuk didekati
garam dari nitrat dan nitrit tidak berwana dan tidak berbau serta tidak berasa, bersifat
higroskopis. (info.ag.uidaho.edu/pdf/CIS/CIS1099.pdf.Access on : December 1. 2006)
2.6.2 Dosis dan Kadar Normal
Dosis letal dari nitrat pada orang dewasa adalah sekitar 4 sampai 30 g (atau sekitar 40
sampai 300 mg NO3-kg). Dosis antara 2 sampai 9 gram NO3- dapat mengakibatkan
methemoglobinemia. Nilai ini setara dengan 33 sampai 150 mg NO3-/ kg.
Dosis letal dari nitrit pada orang dewasa bervariasi antara 0,7 dan 6 g NO2- (atau sekitar 10
sampai 100 mg NO2-/ kg.
Dengan dosis yang lebih kecil akan dapat menyebabkan neonatus karena belum
lengkapnya pembentukan dan regenerasi didalam tubuh mereka. Kebanyakan kasus
membuktikan bahwa neonatus langsung mengalami methemoglobinemia setelah minum air
formula yang tinggi nitrit atau nitrat. (Ruse M. 1999)
Bahan makanan yang tercemar oleh nitrit maupun bahan makanan yang di awetkan
menggunakan nitrit dan nitrat dapat menyebabkan methemoglobinemia siptomatik pada
anak- anak. Walaupun sayuran jarang menjadi sumber keracunan akut, sayuran memberi
kontribusi >70% nitrat dalam diet manusia tertentu. Kembang kol, bayam, brokoli, dan
umbi- umbian memiliki kandungan nitrat alami lebih banyak dari sayuran lainnya. Sisanya
berasal dari air minum (±21%) dan dari daging atau produk olahan daging (6%) yang
sering memakai natrium nitrat (NaNO3) sebagai pengawet maupun pewarna makanan.
(info.ag.uidaho.edu/pdf/CIS/CIS1099.pdf.Access on :December 1, 2006)
Penyalahgunaan inhalan nitrit yang mudah menguap dapat menyebabkan
methemoglobinemia berat dan kematian. Terpapar nitrit tak sengaja dalam laboratorium
kimia dan penghirupan pada usaha bunuh diri pernah terjadi. Penyalahgunaan nitrit volatile
atau mudah menguap (amyl, butyl, dan isobutyl nitrit) sebagai perangsang sering terjadi.
Terpapar nitrat atau nitrit juga dapat berasal dari obat-obatan tertentu. Bayi dan
anak-anak rentan terpapar oleh nitrat melalui perak nitrat topikal yang digunakan pada
terapi luka bakar. Obat-obatan lainnya yang diduga menyebabkan keracunan nitrat atau
nitrit adalah derivate quinone (antimalaria), nitrogliserin, bismuth subnitrit (antidiare),
ammonium nitrat (diuretik), amyl dan natrium nitrit (antidotum keracunan sianida dan
hidrogen sulfida), dan isosorbid dinitrat/tetranitrat (vasodilator untuk terapi penyakit arteri
koroner).
sumur di dekat pertanian juga sering menjadi sumber keracunan nitrat terbesar. Hal ini
sangat berbahaya bila kandungan nitrat ini dikonsumsi oleh anak bayi dan dapat
menimbulkan keracunan akut. Bayi yang baru berumur beberapa bulan belum mempunyai
keseimbangan yang baik antara usus dan bakteri usus. Sebagai akibatnya, nitrat yang
masuk dalam saluran pencernaan akan langsung diubah menjadi nitrit yang kemudian
berikatan dengan hemoglobin membentuk methemoglobin. Ketidak mampuan tubuh bayi
untuk mentoleransi adanya methemoglobin yang terbentuk dalam tubuh mereka akan
mengakibatkan timbulnya sianosis pada bayi. Pada bayi yang telah berumur enam bulan
atau lebih, bakteri pengubah nitrat di dalam tetap ada walau dalam jumlah sedikit. Pada
anak-anak dan orang dewasa, nitrat diabsorbsi dan di sekresikan sehingga resiko untuk
keracunan nitrat jauh lebih kecil. (Parrot K. 2002)
Menurut siklusnya, bakteri akan mengubah nitrogen menjadi nitrat yang kemudian
digunakan oleh tumbuh-tumbuhan. Hewan yang memakan tumbuh-tumbuhan kemudian
menggunakan nitrat untuk menghasilkan protein di dalam tubuh. Setelah itu, nitrat akan
dikeluarkan kembali ke lingkungan dari kotoran hewan tersebut. Mikroba pengurai
kemudian mengubah nitrat yang terdapat dalam bentuk amoniak menjadi nitrit. Selain itu,
nitrat juga diubah menjadi nitrit pada traktus digestivus manusia dan hewan. Setelah itu
bakteri dilingkungan akan mengubah nitrit menjadi nitrogen kembali.
Tetapi apabila jumlah nitrit ataupun nitrat yang berada di suatu lingkungan
melebihi kadar normal maka siklus ini tidak akan dapat berjalan sebagaimana mestinya.
Aktifitas pertanian yang dilakukan manusia telah banyak meningkatkan kadar nitrat
dilingkungan karena penggunaan pupuk yang berlebihan. Nitrat dan nitrit sangat mudah
bercampur dengan air dan terdapat bebas didalam lingkungan.
Hemoglobin adalah pigmen darah merah yang berfungsi untuk mengikat oksigen
dari paru-paru untuk dialirkan ke seluruh tubuh kita. Dalam proses ini akan terbentuk apa
yang disebut oksihemoglobin, sehingga darah segar terlihat berwarna merah cerah. Fungsi
oksigen sendiri adalah untuk melaksanakan proses metabolisme (oksidasi) dalam tubuh,
misalnya oksidasi gula untuk menghasilkan energi yang diperlukan oleh tubuh kita.
Apabila darah keluar dari urat darah (misalnya karena terluka), maka darah yang
tadinya berwarna merah cerah akan berubah menjadi kecoklatan karena adanya kontak
dengan oksigen dari udara. Dalam hal ini yang terjadi adalah oksidasi hemoglobin oleh
Apabila ke dalam tubuh kita masuk nitrit (melalui konsumsi makanan), maka di dalam
tubuh akan terbentuk NO seperti yang telah disebutkan di atas. Apabila nitrit yang
terkonsumsi jumlahnya banyak, maka NO yang terbentuk juga banyak. NO tersebut adalah
dapat bergabung dengan hemoglobin membentuk nitrosohemoglobin, seperti halnya yang
terjadi pada pigmen daging.
Akibatnya hemoglobin tersebut tidak mampu lagi mengikat oksigen, sebab telah mengikat
NO tersebut. Akibat lebih lanjut adalah tubuh kekurangan oksigen, sehingga akhirnya akan
mengakibatkan terjadinya kematian. Kekurangan oksigen tersebut nampak pada korban
yang menjadi kebiru-biruan. (Muchtadi Deddy. 2005)
Nitrit juga dapat mengakibatkan penurunan tekanan darah karena efek
vasodilatasinya.Gejala klinis yang timbul dapat berupa nausea, vomitus, nyeri abdomen,
nyeri kepala, pusing, penurunan tekananan darah dan takikardi, selain itu sianosis dapat
muncul dalam jangka waktu beberapa menit sampai 45 menit. Pada kasus yang ringan,
sianosis hanya tampak disekitar bibir dan membran mukosa. Adanya sianosis sangat
tergantung dari jumlah total hemoglobin dalam darah, saturasi oksigen, pigmentasi kulit
dan pencahayaan saat pemeriksaan. Bila mengalami keracunan yang berat, korban dapat
tidak sadar seperti stupor, koma atau kejang sebagai akibat hipoksia berat.
Mula-mula timbul gangguan gastrointestinal dan sianosis tanpa sebab akan sering
dijumpai. Pada kasus yang berat, koma dan kematian dapat terjadi dalam satu jam pertama
akibat timbulnya hipoksia dan kegagalan sirkulasi. Akibatnya, terjadi iskemia terutama
organ-organ yang vital. Efek vasodilatasi ini tidak dapat di blok oleh atropin atau
obat-obatan lain. Tubuh seharusnya mengkompensasinya dengan takikardi tetapi karena pada
korban dapat terjadi vasovagal reflex yang mengakibatkan bradikardi. Pada sistem
pernafasan mulai tampak takipneu dan hiperventilasi disertai dengan sianosis. Apabila
dibiarkan maka akan timbul koma dan kejang sebagai akibat anoksia serebri. (Ruse M.
1999)
2.6.3 Analisa Nitrit Dengan Metode Spektrofotometer
Nitrit (NO2) ditentukan secara kolorimetris dengan alat spektrofotometer. Pada pH 2,0
sampai 2,5 nitrit berikatan dengan hasil reaksi antara diazo asam sulfanik dan
berwarna ungu kemerah- merahan. Warna tersebut mengikuti hukum beer- lambert dan
menyerap sinar panjang gelombang 543 nm.
Metode kolorimetris tersebut sangat peka, sehingga biasanya perlu pengenceran sampel.
Selain dari metode ini, tidak ada cara analisa yang dapat dianggap bersifat baku. Karena
nitrit dioskidasi dengan cepat oleh oksigen terlarut dan bakteri- bakteri menjadi nitrat.
(Alerts G dan Sri S. 1984).
Spektrofotometer sesuai dengan namanya adalah alat yang terdiri dari
spektrofotometer dan fotometer. Spektrofotometer menghasilkan sinar dari spektrum
dengan panjang gelombang tertentu dan fotometer adalah alat pengukur intensitas cahaya
yang ditransmisikan atau yang diabsorpsi. Jadi spektrofotometer digunakan untuk
mengukur energi secara relatif jika energi tersebut ditransmisikan, direfleksikan atau
diemisikan sebagai fungsi dari panjang gelombang. (Khopkar SM. 1994)
Ada beberapa hal yang perlu diperhatikan dalam analisa dengan spektrofotometer
UV- Vis terutama untuk senyawa- senyawa yang semula tidak berwarna yang akan
dianalisa dengan spektrofotometri UV- Vis karena senyawa tersebut harus terlebih dahulu
diubah menjadi senyawa yang berwarna.
Sebagai contohnya adalah analisa obat- obatan golongan sulfonamid dengan cara
mengubahnya menjadi senyawa yang berwarna setelah sulfonamid tersebut di diazotasi dan
di kopling dengan naftil etilendiamin (NED).
Kelebihan asam nitrit dihilangkan dengan penambahan asam sulfamat karena kalau
tidak dihilangkan, senyawa yang sudah berwarna akan dirusak (dioksidasi) oleh asam
BAB III
METODOLOGI PENELITIAN
3.1. Alat- alat yang digunakan
1. Labu takar Pyrex
2. Gelas ukur Pyrex
3. Gelas beker Pyrex
4. Pipet volum Pyrex
5. Tabung reaksi Pyrex
6. Erlenmeyer Pyrex
7. Hotplate
8. Spektrofotometer DR 4000 seri OACH
9. Spatula
10. Pipet tetes
3.2. Bahan- bahan yang digunakan
1. Natrium nitrit (NaNO2) p.a (E Merck)
2. Asam sulfanilamida p.a (E Merck)
3. 1- naftilamin p.a (E Merck)
4. Asam klorida p.a (E Merck)
5. Asam asetat glasial p.a (E Merck)
3.3 Prosedur Penelitian
3.3.1 Penyedian larutan pereaksi
a. Larutan N- 1 naftiletilendiaminhidroklorida
Di dalam labu takar 100 ml yang telah berisi asam klorida (HCl) pekat ditambahkan 0,85 g
N- 1 naftiletilendiaminhidroklorida (C10H7-NHCH2CH2NH2.2HCl) kemudian diencerkan
sampai 100 ml dengan aquadest
b. Reagen sulfanilamid
Didalam labu ukur 100 ml ditambahkan 0,60 g asam sulfanilamide (C3H7O3NS) lalu
didinginkan kemudian ditambahkan 20 ml asam klorida pekat, dan diencerkan sampai 100
ml.
3.3.2 Penyedian larutan stok standart nitrit
Kedalam labu ukur 100 ml dilarutkan 0,15 g NaNO2 kemudian dilarutkan hingga 100 ml.
3.3.3 Pembuatan kurva kalibrasi
1. Dari larutan standart NaNO2 1000 ppm dipipet sebanyak 10 ml lalu dimasukkan
kedalam labu takar 100 ml kemudian diencerkan dengan aquadest hingga garis
batas sehingga diperoleh larutan standart NO2 100 ppm.
2. Dari larutan standart 100 ppm dipipet sebanyak 10 ml lalu dimasukkan kedalam
labu takar 100 ml kemudian diencerkan dengan aquadest hingga garis batas
sehingga diperoleh larutan standart NO2 10 ppm.
3. Dan dari larutan standart 10 ppm dipipet sebanyak 2,4,6,8,10 ml lalu masing-
masing dimasukkan kedalam labu takar 100 ml kemudian diencerkan dengan
aquadest hingga garis batas sehingga diperoleh larutan standart NO2
0,2;0,4;0,6;0,8;1 ppm.
4. Kemudian masing- masing larutan standart tersebut (0,2;0,4;0,6;0,8;1 ppm) diambil
25 ml kemudian dimasukkan kedalam elenmeyer, kemudian ditambahkan 2,5 ml
asam sulfanilamide dan 2,5 ml naftilamin, kemudian di diamkan selama 10 menit
3.3.4 Prosedur penanaman bayam dengan variasi penambahan pupuk
1. Lahan dibersihkan dari sisa- sisa akar tanaman lain dan gulma, kemudian diberi
pupuk kandang
2. Benih bayam disebar pada lahan yang telah disiapkan, ditanam pada kedalaman 1-2
cm
3. Dilakukan penyiraman pada pagi dan sore hari
4. Setelah tanaman berumur 7 hari diberikan pupuk dengan variasi yang telah di
tentukan yaitu (100,200,300,400,500 gr/ 2m)
5. Tanaman dapat di petik setelah berumur 3 minggu.
3.3.5 Perlakuan pada sampel
1. Sebanyak 100 g sampel bayam direbus dengan 500 ml air selama 5 menit
2. Kemudian dibiarkan beberapa menit lalu di saring
3. Kemudian sebanyak 25 ml filtrat dimasukkan kedalam labu elenmeyer
4. Kemudian ditambhakan 2,5 ml asam sulfanilamida dan 2,5 ml naftilamin,
kemudian didiamkan selama 10 menit lalu diukur absorbansinya dengan
3.4 Bagan Penelitian
3.4.1 Pembuatan kurva kalibrasi
3.4.1.1Kurva kalibrasi larutan standart nitrit
Dimasukkan sebanyak 25 ml kedalam elenmeyer
Ditambahkan 2,5 ml sulfanilamid
Ditambahkan 2,5 ml naftilamin
Didiamkan selama 10 menit
Diukur dengan spektrofotometer = 540 nm 25ml larutan standart nitrit
(0,2;0,4;0,6;0,8;1 ppm)
Larutan merah muda
Larutan merah lembayung
3.4.2 Pengukuran nitrit pada sampel
NB: Sampel bayam adalah sampel yang ditanam dengan penambahan variasi pupuk urea
masing- masing sebanyak 0,100,200,300,400,500 g
100 g sampel Bayam
Sayuran Bayam
Dibiarkan beberapa menit
Disaring
Filtrat Residu
Direbus dengan 500 ml air
Dimasukkan sebanyak 25 ml kedalam elenmeyer
Ditambahkan 2,5 ml asam sulfanilamida
Ditambah 2,5 ml -Naftilamin
Larutan merah muda
Didiamkan selama 10 menit
Larutan merah lembayung
Diukur dengan Spektrofotometer λ = 540 nm
BAB IV
HASIL DAN PEMBAHASAN
4.1 Hasil
4.1.1 Pengukuran absorbansi larutan standar nitrit (NO2)
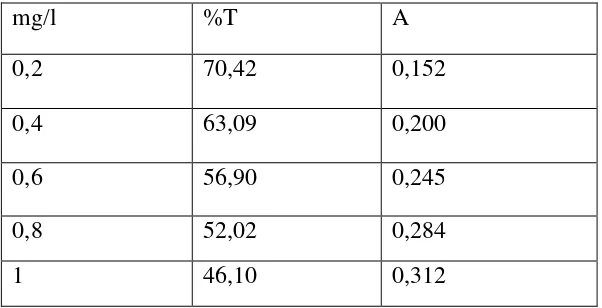
Tabel 4.1 Data pengukuran absorbansi larutan standar nitirt (NO2)
mg/l %T A
0,2 70,42 0,152
0,4 63,09 0,200
0,6 56,90 0,245
0,8 52,02 0,284
1 46,10 0,312
Penurunan persamaan garis regresi untuk kurva kalibrasi larutan standart nitrit
Hasil pengukuran absorbansi dari suatu larutan seri standart nitrit diplotkan terhadap
konsentrasi larutan standart sehingga di peroleh kurva kalibrasi berupa garis linear.
Persamaan garis regresi untuk kurva kalibrasi ini dapat diturunkan dengan
menggunakan metode least square dimana konsentrasi dinyatakan sebagai Xi dan
4.2 Persamaan garis regresi untuk kurva kalibrasi larutan standart nitrit
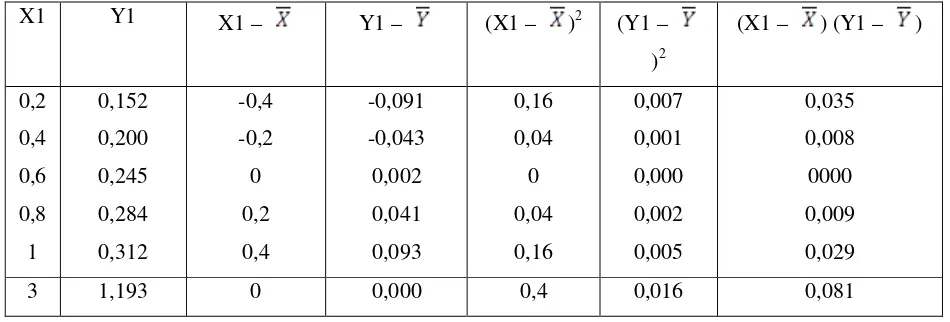
Tabel 4.2 Data perhitungan garis regresi untuk larutan standar nitrit (NO2)
X1 Y1 X1 – Y1 – (X1 – )2
Persamaan garis regersi untuk kurva kalibrasi di nyatakan dengan y = ax + b, dimana
a = slope
b = intersept
Harga slope (a) dapat di peroleh dari persamaan sebagai berikut :
Sedangkan harga intersept (b) dapat di peroleh melalui persamaan
= 0,239 – (0,202)(0,6)
= 0,239 – 0,1212
Persamaan garis regresi untuk kurva kalibrasi nitrit
Y = ax + b
Y = 0,202x – 0,117
4.3 Perhitungan konsentrasi nitrit pada sampel
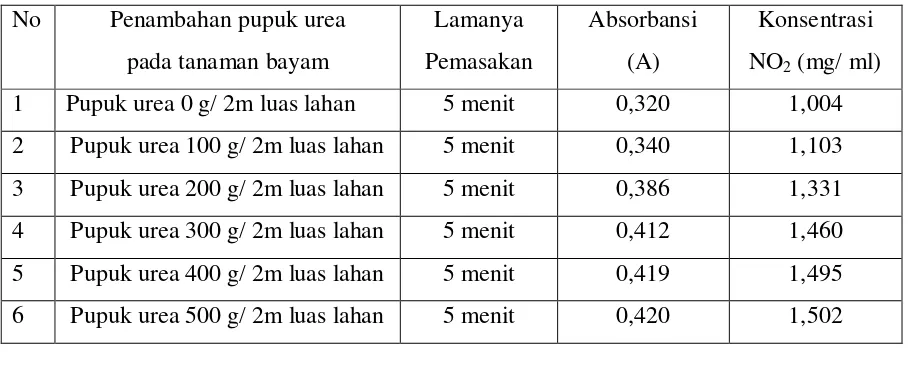
Tabel 4.3 Data perhitungan konsentrasi nitrit pada tanaman bayam yang dimasak selama 5
menit
No Penambahan pupuk urea
pada tanaman bayam
Lamanya
X = (X= konsentrasi nitrit dalam sampel; Y= absorbansi)
Sampel 1 (bayam yang menggunakan 0 gr pupuk urea/ 2m luas lahan)
Y = ax + b
Sampel 2 (bayam yang menggunakan 100 gr pupuk urea/ 2m luas lahan) = 1,103 mg/ml
Sampel 2 (bayam yang menggunakan 200 gr pupuk urea/ 2m luas lahan) = 1,331 mg/ml
Sampel 2 (bayam yang menggunakan 300 gr pupuk urea/ 2m luas lahan) = 1,460 mg/ml
Sampel 2 (bayam yang menggunakan 400 gr pupuk urea/ 2m luas lahan) = 1,495 mg/ml
4.4 Pembahasan
Dari hasil penelitian, hasil reaksi antara diazo asam sulfamil dan
N-1-naftil-etilendehidroklorida (NED-dehidroklorida), maka akan terbentuk celupan berwarna ungu
kemerah- merahan. Warna tersebut mengikuti hukum Lambert- beer dan menyerap sinar
pada panjang gelombang 540 nm.
Pengukuran dengan spektrofotometer sinar tampak perlu dilakukan pengukuran khusus
untuk menentukan waktu operasi yaitu pada saat mana suatu larutan berwarna mencapai
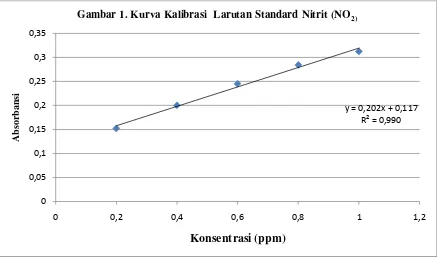
titik transmisi minimum atau absorbansi maksimun. Kurva kalibrasi larutan standar nitrit
(tabel 4.2) dibuat dengan memvariasikan konsentrasi larutan satandar nitrit dan dengan
menggunakan persamaan least square diperoleh persamaan garis linear yaitu Y= 0,202 x –
0,117 dengan grafik pada gambar 1.
Dari analisa stasistik pada keenam penanaman bayam menunjukkan bahwa
tanaman bayam dipengaruhi secara nyata oleh pemberian pupuk urea. Tanaman bayam
yang tidak menggunakan pupuk urea memiliki konsentrasi nitrit sebesar 1,004 mg/ml, dan
berangsur- angsur meningkat dengan penambahan pupuk urea yaitu 1,103; 1,331; 1,460;
1,495; 1,502 mg/ml untuk penambahan pupuk urea masing- masing 100; 200; 300; 400 dan
500 g/2m
Peningkatan konsentrasi dan jumlah kadar nitrit tergantung pada jenis sayuran,
suhu yang ditanam, paparan sinar matahari, tingkat kelembaban tanah.
Peningkatan kadar nitrit yang tidak terlalu signifikan mungkin disebabkan oleh pengaruh
curah hujan yang sangat tinggi pada saat penanaman bayam. Sehingga pupuk yang
ditambahkan pada tanaman lebih banyak terbawa oleh air dibandingkan dengan yang di
serap oleh tanaman. Kandungan nitrit yang tinggi pada tanaman disebabkan oleh akumulasi
nitrit dalam jaringan pertumbuhan tanaman. Akumulasi nitrit pada bagian batang lebih
tinggi daripada dalam daun. Pada bagian batang, kandungan nitrit paling tinggi terdapat
pada sepertiga batang bagian bawah. Hal ini karena posisinya lebih dekat dengan
permukaan tanah sehingga akan lebih banyak mengabsorbsi nitrit. Pada musim penghujan
BAB V
KESIMPULAN DAN SARAN
5.1 Kesimpulan
1. Peningkatan dosis urea sebagai sumber N dapat meningkatkan hasil tanaman. Hal
ini disebabkan karena fungsi N secara langsung berperan dalam pembentukan dan
perbaikan pertumbuhan vegetatif tanaman, dimana tanaman yang tumbuh pada
tanah yang cukup N, berwarna lebih hijau.
2. Adanya korelasi antara penambahan pupuk urea dengan kadar nitrit pada bayam
setelah dimasak.
3. Semakin besar kadar ammonium maka kadar nitritnya juga semakin besar
5.2 Saran
1. Para petani sebaiknya mencari terobosan baru untuk meningkatkan hasil pertanian
2. Perlu dilakukan penelitian lebih lanjut tentang pengaruh pupuk terhadap
DAFTAR PUSTAKA
Alerts, G, dan Santika,S.S, (1978), Metode penelitian Air, Usaha Nasional, Surabaya
Abdul Rahman, (2007), Kimia Farmasi Analisis, cetakan II, Pustaka Pelajar, Yogyakarta
Bandini, Y, (2001), Bayam, Cetakan Kelima, Jakarta, Penebar Swadaya
Cassel, K, and Barao, (2000), Causes and Prevention: nitrate Poisioning of livestock, College of Agriculture and Natural Resources, University
Khopkar SM, (2008), Konsep Dasar Kimia Analitik, UI-Press, Jakarta
Maryland.http://www.agnr.umd.edu/MCE/Publications.4 september 2007
Muchtadi Deddy, (2005), Keracunan Sodium Nitrit, Departement of Food Science and Technology, Bogor, IPB
Parrot K, Woodard J,Ross B. Household Water Quality. “Nitrates in Household Water”. Virginia polytechnic institute and state university. Virginia State University. Virginia. 2002. Available from: info.ag.uidaho.edu/pdf/CIS/CIS1099.pdf. Access on: December 1, 2006.
Roostika Ika, dkk, (2005), Pengaruh Tiga Jenis Pupuk Nitrogen Terhadap Tanaman Sayuran, Balai Besar Penelitian dan Pengembangan Teknologi dan sumberdaya Genetik Pertanian (Balitbiogen), Bogor 16111
Roberts S. Harris, (1989), Evaluasi Gizi Pada Pengolahan Bahan Pangan, Bandung: ITB
Ruse M, Nitrates and Nitrites. IPCS, Newcastle. United Kingdom, (1999), Available from:
Sianipar A, (2001), Penentuan Kadar Nitrat di Beberapa Kerambahan Ikan di Sekitar Perairan Danau Toba, Skripsi Jurusan Kimia, FMIPA USU, Medan
y = 0,202x + 0,117 R² = 0,990
0 0,05 0,1 0,15 0,2 0,25 0,3 0,35
0 0,2 0,4 0,6 0,8 1 1,2
Abso
r
ba
nsi
Konsentrasi (ppm)
0 200 400 600 800 1.000 1.200 1.400 1.600
0 100 200 300 400 500
K
a
ndung
a
n
N
it
ri
t
(N
O
2
)