KARAKTERISASI PRODUK BIOSOLUBILISASI BATUBARA
LIGNIT OLEH KAPANG INDIGENOUS DARI TANAH
PERTAMBANGAN SUMATERA SELATAN
MIFTAHUL JANNAH
PROGRAM STUDI KIMIA
FAKULTAS SAINS DAN TEKNOLOGI
UNIVERSITAS ISLAM NEGERI SYARIF HIDAYATULLAH
JAKARTA
KARAKTERISASI PRODUK BIOSOLUBILISASI BATUBARA
LIGNIT OLEH KAPANG INDIGENOUS DARI TANAH
PERTAMBANGAN SUMATERA SELATAN
SKRIPSI
Sebagai Salah Satu Syarat untuk Memperoleh Gelar Sarjana Sains Pada Program Studi Kimia Fakultas Sains dan Teknologi
Universitas Islam Negeri Syarif Hidayatullah Jakarta
MIFTAHUL JANNAH 106096003229
PROGRAM STUDI KIMIA
FAKULTAS SAINS DAN TEKNOLOGI
UNIVERSITAS ISLAM NEGERI SYARIF HIDAYATULLAH
JAKARTA
KARAKTERISASI PRODUK BIOSOLUBILISASI BATUBARA
LIGNIT OLEH KAPANG INDIGENOUS DARI TANAH
PERTAMBANGAN SUMATERA SELATAN
SKRIPSI
Sebagai Salah Satu Syarat untuk Memperoleh Gelar Sarjana Sains Pada Program Studi Kimia Fakultas Sains dan Teknologi
Universitas Islam Negeri Syarif Hidayatullah Jakarta
MIFTAHUL JANNAH 106096003229
Menyetujui,
Pembimbing I Pembimbing II
Irawan Sugoro, M.Si Sandra Hermanto, M.Si NIP. 19761018 20001 2 1001 NIP. 19750810 200501 1 005
Mengetahui,
Ketua Program Studi Kimia
PENGESAHAN UJIAN
Skripsi berjudul “Karakterisasi Produk Biosolubilisasi Batubara Lignit oleh Kapang
Indigenous dari Tanah Pertambangan Sumatera Selatan” yang ditulis oleh Miftahul Jannah NIM 106096003229 telah diuji dan dinyatakan LULUS dalam sidang munaqosyah Fakultas Sains dan Teknologi Universitas Islam Negeri Syarif Hidayatullah Jakarta pada tanggal 10 Desember 2010. Skripsi ini telah diterima sebagai salah satu syarat untuk memperoleh gelar Sarjana Strata Satu (S1) Program Studi Kimia.
Menyetujui
Penguji I, Penguji II,
La Ode Sumarlin, M.Si Anna Muawanah, M.Si NIP. 150 408 693 NIP. 19740508 199903 2 002
Pembimbing I, Pembimbing II,
Irawan Sugoro, M.Si Sandra Hermanto, M.Si NIP. 19761018 20001 2 1001 NIP. 19750810 200501 1 005
Mengetahui,
Dekan
Fakultas Sains dan Teknologi Ketua Program Studi Kimia
PERNYATAAN
DENGAN INI SAYA MENYATAKAN BAHWA SKRIPSI INI ADALAH HASIL KARYA SENDIRI YANG BELUM PERNAH DIAJUKAN SEBAGAI SKRIPSI ATAU KARYA ILMIAH PADA PERGURUAN TINGGI ATAU LEMBAGA MANAPUN.
Jakarta, Desember 2010
MIFTAHUL JANNAH
KARAKTERISASI PRODUK BIOSOLUBILISASI BATUBARA
LIGNIT OLEH KAPANG INDIGENOUS DARI TANAH
PERTAMBANGAN SUMATERA SELATAN
MIFTAHUL JANNAH
PROGRAM STUDI KIMIA
FAKULTAS SAINS DAN TEKNOLOGI
UNIVERSITAS ISLAM NEGERI SYARIF HIDAYATULLAH
JAKARTA
2010 M / 1431 H
KARAKTERISASI PRODUK BIOSOLUBILISASI BATUBARA
LIGNIT OLEH KAPANG INDIGENOUS DARI TANAH
PERTAMBANGAN SUMATERA SELATAN
SKRIPSI
Sebagai Salah Satu Syarat untuk Memperoleh Gelar Sarjana Sains Pada Program Studi Kimia Fakultas Sains dan Teknologi
Universitas Islam Negeri Syarif Hidayatullah Jakarta
MIFTAHUL JANNAH 106096003229
PROGRAM STUDI KIMIA
FAKULTAS SAINS DAN TEKNOLOGI
UNIVERSITAS ISLAM NEGERI SYARIF HIDAYATULLAH
JAKARTA
2010 M / 1431 H
KARAKTERISASI PRODUK BIOSOLUBILISASI BATUBARA
LIGNIT OLEH KAPANG INDIGENOUS DARI TANAH
PERTAMBANGAN SUMATERA SELATAN
SKRIPSI
Sebagai Salah Satu Syarat untuk Memperoleh Gelar Sarjana Sains Pada Program Studi Kimia Fakultas Sains dan Teknologi
Universitas Islam Negeri Syarif Hidayatullah Jakarta
MIFTAHUL JANNAH 106096003229
Menyetujui,
Pembimbing I Pembimbing II
Irawan Sugoro, M.Si Sandra Hermanto, M.Si NIP. 19761018 20001 2 1001 NIP. 19750810 200501 1 005
Mengetahui,
Ketua Program Studi Kimia
Sri Yadial Chalid, M.Si NIP. 19680313 20031 2 2001
PENGESAHAN UJIAN
Skripsi berjudul “Karakterisasi Produk Biosolubilisasi Batubara Lignit oleh Kapang
Indigenous dari Tanah Pertambangan Sumatera Selatan” yang ditulis oleh Miftahul Jannah NIM 106096003229 telah diuji dan dinyatakan LULUS dalam sidang munaqosyah Fakultas Sains dan Teknologi Universitas Islam Negeri Syarif Hidayatullah Jakarta pada tanggal 10 Desember 2010. Skripsi ini telah diterima sebagai salah satu syarat untuk memperoleh gelar Sarjana Strata Satu (S1) Program Studi Kimia.
Menyetujui
Penguji I, Penguji II,
La Ode Sumarlin, M.Si Anna Muawanah, M.Si NIP. 150 408 693 NIP. 19740508 199903 2 002
Pembimbing I, Pembimbing II,
Irawan Sugoro, M.Si Sandra Hermanto, M.Si NIP. 19761018 20001 2 1001 NIP. 19750810 200501 1 005
Mengetahui,
Dekan
Fakultas Sains dan Teknologi Ketua Program Studi Kimia
DR. Syopiansyah Jaya Putra, M. Sis. Sri Yadial Chalid, M.Si NIP. 19680117 20011 2 1001 NIP. 19680313 20031 2 2001
PERNYATAAN
DENGAN INI SAYA MENYATAKAN BAHWA SKRIPSI INI ADALAH HASIL KARYA SENDIRI YANG BELUM PERNAH DIAJUKAN SEBAGAI SKRIPSI ATAU KARYA ILMIAH PADA PERGURUAN TINGGI ATAU LEMBAGA MANAPUN.
Jakarta, Desember 2010
MIFTAHUL JANNAH
106096003229
KATA PENGANTAR
Bismillahirrahmanirrahiim…
Segala puji bagi Allah yang telah memberikan banyak kenikmatan yang tidak akan pernah habis, nikmat yang patut selalu kita syukuri sehingga skripsi yang berjudul “Karakterisasi Produk Biosolubilisasi Batubara Lignit oleh Kapang
Indigenous dari Tanah Pertambangan Sumatera Selatan” dapat diselesaikan
dengan baik. Skripsi ini disusun sebagai salah satu syarat dalam menyelesaikan program studi S1 pada Program Studi Kimia Fakultas Sains dan Teknologi Universitas Islam Negeri Syarif Hidayatullah Jakarta.
Penulis menyadari bahwa isi maupun materi skripsi ini masih banyak kekurangannya, walaupun sudah diupayakan semaksimal mungkin oleh karena itu kritik dan saran yang bersifat konstruktif guna kesempurnaan dalam penulisan skripsi ini sangat diperlukan.
Pada kesempatan ini penulis tidak lupa mengucapkan terimakasih yang sebesar-besarnya atas bimbingan dan saran serta dukungannya kepada:
1. DR. Syopiansyah Jaya Putra, M.Sis selaku Dekan Fakultas Sains dan Teknologi UIN Syarif Hidayatullah Jakarta.
2. Sri Yadial Chalid, M.Si selaku Ketua Program Studi Kimia UIN Syarif Hidayatullah Jakarta.
3. Irawan Sugoro, M.Si. selaku pembimbing I yang telah banyak meluangkan waktunya, memberi saran, bimbingan dan motivasi dalam melaksanakan kegiatan penelitian dan penulisan skripsi ini.
4. Sandra Hermanto, M.Si. selaku pembimbing II atas kesabarannya dalam membimbing dan terimakasih atas masukan-masukan yang tentunya membantu untuk kedepannya agar lebih maju.
5. La Ode Sumarlin, M.Si dan Anna Muawanah, M.Si selaku dosen penguji sidang, terimakasih penulis ucapkan atas saran, masukan, serta nasihat yang membangun semangat bagi penulis.
6. Para Dosen Program Studi Kimia atas sumbangsih Ilmunya.
7. Kedua Orang Tuaku tercinta, Ayahanda Rusdi Usman, M.M.Pd dan Ibunda Nurhaidah yang memberikan kasih sayang yang luar biasa, kesabaran, dukungan dan doa yang tiada henti untuk ananda serta adik-adikku tersayang (abdul, awa, umi).
8. Dodi yang telah meluangkan waktunya, bersedia mendegar keluh kesah penulis, dan selalu ada ketika penulis butuhkan.
9. Teman-teman seperjuangan selama penelitian (dede, riska, diyah, yelvi, noet, dan ryan) terimakasih atas bantuan dan sharingnya.
10.Teman-temanku semua terutama anak Kimia angkatan 2006
11.Pihak-pihak lain yang tidak bisa saya sebutkan satu persatu, tapi saya ucapkan sekali lagi banyak terimakasih karena dengan bantuan semuanya segala masalah dapat terselesaikan dengan lebih mudah dan mendapatkan hasil yang lebih baik.
Jakarta, Desember 2010
Miftahul Jannah
DAFTAR ISI
Halaman
KATA PENGANTAR... vi
DAFTAR ISI... viii
DAFTAR GAMBAR ... xi
DAFTAR TABEL ... xiii
DAFTAR LAMPIRAN... xiv
ABSTRAK ... xv
ABSTRACT... xvi
BAB I PENDAHULUAN... 1
1.1. Latar Belakang ... 1
1.2. Perumusan Masalah ... 3
1.3. Hipotesis ... 4
1.4. Tujuan Penelitian ... 4
1.5. Manfaat Penelitian ... 4
BAB II TINJAUAN PUSTAKA... 5
2.1. Batubara ... 5
2.1.1. Pembentukan Batubara... 7
2.1.2. Klasifikasi Batubara ... 9
2.1.3. Substansi Humik dalam Batubara ... 13
2.2. Biosolubilisasi Batubara ... 14
2.2.1. Mikroorganisme Pensolubilisasi Batubara ... 15
2.2.2. Solubilisasi Batubara oleh Kapang... 18
2.2.3. Faktor-Faktor yang Berpengaruh Terhadap Biosolubilisasi Batubara ... 22
2.3. Analisis Kimia Terhadap Produk Solubilisasi Batubara... 24
2.3.1. Spektrofotometer UV-Vis... 24
2.3.2. Spektrofotometer Fourier Transform Infra Red (FTIR)... 26
2.3.3. Gas Chromatography Mass Spectrometry (GCMS)... 30
BAB III METODOLOGI PENELITIAN... 34
3.1. Waktu dan Tempat Penelitian... 34
3.2. Alat dan Bahan... 34
3.2.1. Alat ... 34
3.2.2. Bahan ... 34
3.3. Prosedur Kerja ... 35
3.3.1. Persiapan dan Sterilisasi Alat... 35
3.3.2. Persiapan Serbuk Batubara ... 35
3.3.3. Pembuatan Medium Minimal Salt (MS) ... 36
3.3.4. Pembuatan Medium MSSA ... 36
3.3.5. Peremajaan Kultur Spora Kapang... 36
3.3.6. Kultur Inokulum Spora ... 36
3.3.7. Pembuatan Medium MSS ... 37
3.3.8. Biosolubilisasi Batubara ... 37
3.3.9. Pengukuran pH Medium ... 38
3.3.10. Pengukuran Aktivitas Enzim ... 38
3.3.11. Pengukuran Asam Humat dan Fulvat ... 38
3.3.12. Pengukuran Solubilisasi dengan Spektrofotometer UV-Vis... 39
3.3.13. Analisis Hasil Solubilisasi Batubara oleh Kapang dengan Menggunakan GCMS ... 39
3.3.14. Analisis Sample dengan Menggunakan FTIR ... 40
3.4. Skema Kerja... 41
BAB IV HASIL DAN PEMBAHASAN... 42
4.1. Perubahan Nilai Derajat Keasaman (pH) pada Medium... 42
4.2. Analisis Aktivitas Enzim dengan FDA... 44
4.3. Solubilisasi Batubara ... 47
4.4. Asam Humat dan Asam Fulvat pada Produk Solubilisasi Batubara ... 51
4.5. Analisa Spektrum IR Produk Biosolubilisasi Batubara ...54
4.6. Analisis GC-MS Hasil Solubilisasi Batubara oleh Kapang... 55
BAB V KESIMPULAN DAN SARAN... 60
5.1. Kesimpulan ... 60
5.2. Saran ... 60
DAFTAR PUSTAKA... 61
LAMPIRAN ... 65
DAFTAR GAMBAR
Halaman
Gambar 1. Proses Pembentukan Batubara ... 7
Gambar 2. Struktur Kimia dan Bentuk Batubara Lignit ... 10
Gambar 3. Struktur Kimia dan Bentuk Batubara Subbituminus... 11
Gambar 4. Struktur Kimia dan Bentuk Batubara Bituminus ... 12
Gambar 5. Struktur Kimia dan Bentuk Batubara Antrasit ... 12
Gambar 6. Struktur Asam Humat ... 13
Gambar 7. Struktur Asam Fulvat ... 14
Gambar 8. (a) Struktur lignin, (b) hemiselulosa dan (c) selulosa ... 19
Gambar 9. Spektrofotometer UV-vis ... 25
Gambar 10. Vibrasi Renggangan ... 27
Gambar 11. Vibrasi Bengkokan... 28
Gambar 12. Instrumentasi FTIR ... 29
Gambar 13. Instrumentasi GCMS... 31
Gambar 14. Nilai pH Medium pada Berbagai kapang... 42
Gambar 15. Reaksi Penguraian Piridin Menjadi Amonia dan Terbentuknya Amonium Hidroksida ... 43
Gambar 16. Reaksi Hidrolisis FDA Oleh Enzim Esterase ... 44
Gambar 17. Aktivitas Enzim pada Produk Biosolubilisasi Batubara denganKapang Yang Berbeda... 45
Gambar 18. Reaksi Enzim dan Substrat pada Pembentukan Produk... 46
Gambar 19. Pengaruh (S) Terhadap Aktivitas katalitik Enzim ... 47
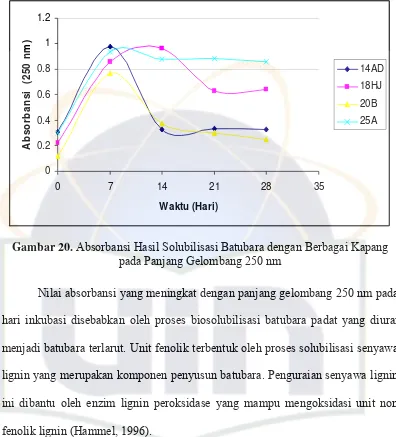
Gambar 20. Absorbansi Hasil Solubilisasi Batubara pada Berbagai
Kapang dengan Panjang Gelombang 250 nm... 48
Gambar 21. Reaksi Degradasi Lignin Oleh Enzim Lignin Peroksidase... 48
Gambar 22. Reaksi oksidasi unit fenolik oleh Enzim Laccase dan Mangan .. 49
Gambar 23. Absorbansi Hasil Solubilisasi Batubara pada Berbagai
Kapang dengan Panjang Gelombang 450 nm... 49
Gambar 24. Reaksi Degradasi Poli Aromatik Hidrokarbon (PAH)... 50
Gambar 25. Perbandingan Asam Humat dan Asam Fulvat pada Produk
Solubilisasi Batubara dengan Jenis Kapang yang Berbeda. ... 52
Gambar 26. Reaksi Degradasi Naftasena... 53
Gambar 27. Spektrum Hasil Analisa FTIR Terhadap Sisa Endapan Hasil Biosolubilisasi Batubara oleh Kapang 14AD, 20B, 25A, 18HJ dan kontrol ... 54
Gambar 28. Persentase Area Senyawa hidrokarbon Komponen Bensin dan Solar Hasil Biosolubilisasi Batubara oleh
Berbagai Kapang... 58
DAFTAR TABEL
Halaman
Tabel 1. Bahan Mineral yang Biasa Terdapat dalam Batubara ... 6
Tabel 2. Unsur-Unsur Yang Terdapat pada Setiap Tahapan Pembentukan Batubara ... 8
Tabel 3. Persentase Senyawa Sulfur dalam Batubara ... 9
Tabel 4. Enzim ekstraseluler pendegradasi lignin dari kapang pelapuk putih... 21
Tabel 5. Beberapa Contoh Nilai Frekuensi Gugus Fungsi ... 30
Tabel 6. Komposisi Medium... 35
Tabel 7. Kondisi Optimum GC-MS... 40
Tabel 8. Senyawa Hasil Biosolubilisasi Batubara Menggunakan GC-MS... 56
DAFTAR LAMPIRAN
Halaman
Lampiran 1. Komposisi Medium ... 65
Lampiran 2. Skema Kerja ... 66
Lampiran 3. Parameter Pengujian pada Berbagai Kapang ... 67
Lampiran 4. Senyawa Komponen Bensin dan Solar Hasil Biosolubilisasi Batubara ... 69
Lampiran 5. Spektrum Hasil FTIR Batubara Lignit ... 71
Lampiran 6. Kromatogram Hasil GC-MS Kontrol ... 74
Lampiran 7. Kromatogram Hasil GC-MS Solubilisasi Batubara oleh Kapang ... 75
Lampiran 8. Komponen Senyawa Solar ... 79
Lampiran 8. Batubara lignit ... 80
Lampiran 9. Hasil Biosolubilisasi Batubara ... 81
Lampiran 10. Endapan Batubara Lignit Hasil Saring Sampel ... 82
ABSTRAK
Karakterisasi Produk Biosolubilisasi Batubara Lignit oleh Kapang Indigenous
dari Tanah Pertambangan Sumatera Selatan. Di bawah bimbingan Irawan Sugoro, M.Si dan Sandra Hermanto, M.Si
Biosolubilisasi batubara adalah proses pelarutan batubara dalam suatu medium dengan bantuan mikroorganisme. Mikroorganisme yang digunakan pada penelitian ini terdiri dari 4 isolat kapang indigenous yang merupakan hasil isolasi dari tanah pertambangan batubara di Sumatera Selatan. Tujuan dari penelitian ini adalah mengetahui kemampuan kapang indigenous hasil isolasi dari tanah pertambangan batubara Sumatera Selatan dalam mensolubilisasi batubara lignit dan karakteristik produk yang dihasilkan. Medium yang digunakan adalah minimal salt sugar (MSS) dengan penambahan batubara lignit Sumatera Selatan 5 %, kemudian diinokulasikan spora kapang sebanyak 5 % dengan pencuplikan pada hari 7, 14, 21, dan 28. Hasilnya menunjukkan bahwa kapang indigenous memiliki kemampuan yang berbeda dalam mensolubilisasi batubara dimana kapang 14AD pada hari ke 7 inkubasi menunjukan solubilisasi terbesar. Hasil analisis GCMS menunjukkan bahwa kapang 25A pada hari ke 7 inkubasi menghasilkan persentase senyawa hidrokarbon terbesar dengan komposisi karbon yang setara dengan bensin dan solar.
Kata kunci : Biosolubilisasi, Batubara, kapang, lignit
xv i ABSTRACT
Characterization of Lignite Coal Biosolubilization Products by Indigenous Molds from Mining Land in South Sumatera. Under direction of Irawan Sugoro, M.Si and Sandra Hermanto, M.Si
Coal Biosolubilization is the coal dissolution process in a medium by microorganisms. The microorganism this research was 4 isolates of indigenous moulds result isolated from mining land in South Sumatera. The purpose of this research was to determine the ability of indigenous moulds in solubilization lignite and characterization of the products. The medium was minimal salt sugar (MSS) + 5 % of South Sumatra lignite and 5 % mould spores and sampling times were done at 7, 14, 21, and 28 days. The result showed that Indigenous moulds have different ability in solubilization of lignite and the highest solubilization occurred was 14AD after 7 days incubation. GCMS analysis showed the largest percentage of hydrocarbon compound which is equivalent to gasoline and diesel was 25A after 7 days incubation.
1
BAB I
PENDAHULUAN
1.1. Latar Belakang
Cadangan sumber daya energi di Indonesia semakin menipis. Saat ini
Indonesia hanya memiliki 4.300 juta ton cadangan minyak dari total cadangan
minyak dunia tahun 2006 sebesar 1.208.200 ton, dengan tingkat produksi sebesar
390 juta ton per tahun, dan hanya dapat bertahan dalam 11 tahun ke depan.
Sementara itu, gas alam hanya memiliki cadangan yang ekuivalen dengan masa
produksi selama 35,54 tahun. Oleh karena itu perlu dicari bahan bakar alternatif
pengganti minyak bumi dan gas yang keberadaannya melimpah, salah satunya
adalah batubara (Jauhary, 2007).
Berdasarkan laporan Departemen Energi dan Sumber Daya Mineral
(2008), potensi sumber daya batubara di Indonesia pada akhir tahun 2008
sebanyak 105 miliar ton yang berasal dari tiga daerah, yaitu Sumatera Selatan,
Kalimantan Timur dan Kalimantan Selatan. Batubara sebagai bahan bakar
alternatif diperkirakan dapat menjadi solusi dari krisis kelangkaan BBM sampai
ratusan tahun mendatang (Calvin, 2007). Sehingga batubara merupakan kandidat
yang sesuai sebagai alternatif untuk menggantikan energi minyak bumi.
Cadangan batubara di dunia pada umumnya tidak berkualitas baik, bahkan
setengahnya merupakan batubara dengan kualitas rendah, seperti: lignit dan
subituminus. Batubara jenis ini memiliki tingkat kelembaban yang tinggi dan
2
harganya pun sangat murah (Sukandarrumidi, 1995). Di Indonesia, lebih dari
46 % merupakan batubara kualitas rendah dari jenis lignit (Beyond, 2009). Oleh
karena itu perlu ada upaya solusi untuk meningkatkan kualitas batubara agar
bernilai ekonomis. Salah satu upaya yang dapat dilakukan adalah dengan cara
pencairan (solubilisasi) batubara.
Pencairan batubara dapat dilakukan dengan metode fisika dan biologi.
Metode fisika yaitu dengan proses sintesis fischer-Tropsch dan Brown Coal
Liquefaction Technology (BCL). Pencairan batubara dengan metode tersebut
memakan biaya operasional yang cukup tinggi dan memerlukan instalasi yang
cukup rumit serta menghasilkan produk sampingan yang berbahaya. Sehingga
perlu dikembangkan suatu teknologi pengolahan batubara menjadi energi
alternatif yang efisien (Natural Resources Defense Council, 2007).
Salah satu metode pencairan batubara yang bisa dikembangkan adalah
secara biologis dengan bantuan mikroorganisme yang disebut biosolubilisasi.
Pencairan batubara dengan metode biologi relatif dapat menekan biaya
operasional karena tidak dilakukan dalam tekanan dan temperatur yang tinggi
serta lebih ramah lingkungan karena tidak menghasilkan produk sampingan yang
berbahaya (Shi, 2009).
Sejumlah jamur dan bakteri diketahui mampu berinteraksi dengan
batubara kualitas rendah pada enzim ekstraseluler. Kapang memiliki kemampuan
untuk mensolubilisasi batubara karena aktivitas enzim lignoselulasenya (Cohen et
al, 1990). Proses ini mampu mensolubilisasi polimer organik berupa karbohidrat
3
menyusun batubara. Hasil penelitian sebelumnya yang dilakukan oleh Selvi et al,
2009 menyatakan bahwa kapang Aspergillus sp. mampu mensolubilisasi batubara
subituminus. Kapang Trichoderma sp. dan Penicillium sp. yang diisolasi dari
sampel batubara subituminus Sumetera Selatan mampu mensolubilisasi batubara
subituminus (Sugoro et al., 2009).
Sampel batubara yang digunakan dalam penelitian ini adalah batubara
jenis lignit yang berasal dari Lahat Sumatera Selatan, dengan kapang indigenous
sebagai mikroorganisme yang membantu proses biosolubilisasi. Kapang
indigenous tersebut merupakan kapang penghuni asli suatu habitat atau substrat.
Kapang ini diisolasi langsung dari tanah pertambangan batubara tersebut,
sehingga dapat memudahkan saat pengaplikasian karena secara alami telah
teradaptasi dengan substrat batubara (Sugoro et al., 2009). Pada akhirnya
diharapkan proses biosolubilisasi ini dapat meningkatkan kualitas batubara lignit
dan menghasilkan senyawa potensial sebagai pengganti Bahan Bakar Minyak.
1.2. Perumusan Masalah
1. Apakah kapang indigenous hasil isolasi dari tanah pertambangan
batubara memiliki kemampuan solubilisasi batubara lignit?
2. Bagaimanakah karakteristik produk biosolubilisasi batubara lignit
Sumatera Selatan oleh kapang indigenous hasil isolasi dari tanah
4 1.3. Hipotesis
1. Kapang indigenous hasil isolasi dari tanah pertambangan batubara
Sumatera Selatan dapat mensolubilisasi batubara lignit dengan
kemampuan yang berbeda-beda pada setiap isolat.
2. Senyawa Hasil biosolubilisasi lignit oleh kapang indigenous merupakan
senyawa hidrokarbon yang memiliki karakteristik bensin dan solar.
1.4. Tujuan Penelitian
1. Mengetahui kemampuan kapang indigenous hasil isolasi dari tanah
pertambangan batubara Sumatera Selatan dalam mensolubilisasi
batubara lignit
2. Mengetahui karakteristik produk batubara cair hasil biosolubilisasi
kapang indigenous batubara lignit Sumatera Selatan sebagai energi
alternatif.
1.5. Manfaat Penelitian
Hasil penelitian ini diharapkan dapat memberikan informasi mengenai
potensi kapang indigenous yang berasal dari tanah pertambangan batubara lignit
Sumatera Selatan dalam proses biosolubilisasi dan karakteristik produk
biosolubilisasi batubara yang dihasilkan untuk bahan bakar alternatif pengganti
5
BAB II
TINJAUAN PUSTAKA
2.1. Batubara
Batubara adalah mineral organik yang terbentuk dari endapan, dan
merupakan batuan organik yang terutama terdiri dari karbon, hidrogen, dan oksigen.
Batubara terbentuk dari tumbuhan yang telah bersatu antara strata batuan lainnya
dan diubah oleh kombinasi pengaruh tekanan dan panas selama jutaan tahun
sehingga membentuk lapisan batubara. Proses yang mengubah tumbuhan menjadi
batubara tadi disebut dengan pembatubaraan atau coalification (Speight, 1994).
Bahan mineral di dalam batubara berasal dari unsur organik yang terdapat
dalam tumbuhan pembentuk batubara dan dari bahan mineral yang berasal dari
luar yang tergabung dalam proses pembentukan batubara. Jumlah dan tipe mineral
yang ditemukan dalam batubara sangat bervariasi, bergantung pada sejarah
pembentukan batubara tersebut. Mineral yang ditemukan dalam jumlah yang
melimpah adalah clay mineral dengan illite, kaolinite dan montmorillonite sebagai
jenis yang sering ditemukan (speight, 1994). Mineral utama yang ditemukan
dalam batubara dapat diklasifikasikan sebagai shale, kaolin, sulfida, karbonat,
klorida atau accessory mineral. Beberapa kelompok mineral yang terkandung
6
Tabel 1. Bahan Mineral yang Biasa Terdapat dalam Batubara
Kelompok Senyawa Formula
Muscovite KAI3Si3O10(OHF)2
Pyrophillite Al2O3
2.1.1. Pembentukan Batubara
Penimbunan pasir dan sedimen lainnya, bersama dengan pergeseran kerak
bumi (dikenal sebagai pergeseran tektonik) mengubur rawa dan gambut yang
seringkali sampai kedalaman yang sangat dalam. Penimbunan tersebut
menyebabkan material tumbuhan terkena suhu dan tekanan yang tinggi. Suhu dan
tekanan yang tinggi menyebabkan tumbuhan tersebut mengalami proses
perubahan fisika dan kimiawi yang mengubah tumbuhan tersebut menjadi gambut
dan kemudian batubara (Sukandarrumidi, 1995). Proses pembentukan batubara
dapat digambarkan sebagai berikut:
Gambar 1. Proses Pembentukan Batubara (Sukandarrumidi, 1995)
Proses pembentukan batubara terdiri dari dua tahap, yaitu tahap
penggambutan dan tahap pembatubaraan. Tahap penggambutan dimana sisa-sisa
tumbuhan yang terakumulasi tersimpan dalam kondisi reduksi di daerah rawa
dengan sistem pengeringan yang buruk dan selalu tergenang air pada kedalaman
0,5 – 10 meter. Material tumbuhan yang busuk ini melepaskan H, N, O, dan C
dalam bentuk senyawa CO2, H2O, dan NH3 untuk menjadi humus. Bakteri
8
anaerobik dan fungi akan merubah material tersebut menjadi gambut
(Sukandarrumidi, 1995).
Pada proses pembatubaraan gambut akan terkubur dengan sedimen lain, di
bawah pemanasan dan tekanan mengubah gambut menjadi batubara tingkat
rendah yaitu lignit. Batubara di bawah pemanasan dan tekanan yang terus
menerus selama jutaan tahun, mengalami perubahan yang secara bertahap
sehingga menambah maturitas organiknya dan mengubah batubara muda menjadi
batubara subituminus. Pada pemanasan dan tekanan yang lebih tinggi batubara
lignit berubah menjadi batubara bituminus. Bahkan pada pemanasan dan tekanan
yang lebih tinggi lagi dapat mengubah batubara bituminus menjadi batubara
antrasit yang lebih keras dan mengkilap (Sukandarrumidi, 1995). Berikut ini
contoh analisis dari masing – masing unsur yang terdapat dalam setiap tahapan
pembatubaraan pada Tabel 2.
Tabel 2.Unsur-Unsur Yang Terdapat pada Setiap Tahapan Pembentukan Batubara
Jenis Batubara C (%) H (%) O (%) N (%) C/O
Semakin tinggi tingkat pembatubaraan, kadar karbon akan meningkat
sedangkan hidrogen dan oksigen berkurang. Batubara dengan tingkat
pembatubaraan rendah disebut pula batubara bermutu rendah, contohnya lignit
9
berwarna suram seperti tanah, memiliki tingkat kelembaban (moisture) yang
tinggi dan kadar karbon yang rendah, sehingga kandungan energinya juga rendah.
Semakin tinggi mutu batubara, umumnya akan semakin keras dan kompak, serta
warnanya akan semakin hitam mengkilat (Sukandarrumidi, 1995).
Selain unsur karbon, hidrogen, oksigen dan nitrogen, di dalam batubara
terdapat sulfur. Sulfur berada dalam bentuk senyawa organik dan anorganik.
Sulfur anorganik sebagian besar terdiri dari bentuk sulfit dan sulfat. Kandungan
sulfur dalam batubara bervariasi tergantung wilayah batubara tersebut berasal
(Speight, 1994). Berikut persentase senyawa sulfur dalam batubara:
Tabel 3. Persentase Senyawa Sulfur dalam Batubara
Unsur Rentang
Sulfur organik 0,31-3,09 %
Sulfur pirit 0,06-3,78 %
Sulfur sulfat 0,01-1,06 %
Total sulfur 0,42-6,47 %
(Speight, 1994).
2.1.2. Klasifikasi Batubara
Faktor tumbuhan purba yang jenisnya berbeda-beda sesuai dengan zaman
geologi dan lokasi tempat tumbuh dan berkembangnya, ditambah dengan lokasi
pengendapan (sedimentasi) tumbuhan, pengaruh tekanan batuan dan panas bumi
serta perubahan geologi yang berlangsung kemudian, akan menyebabkan
batubara berdasarkan tingkat pembatubaraan ini dapat dikelompokkan sebagai
berikut :
1. Lignit
Lignit merupakan jenis batubara yang secara geologis tergolong jenis
batubara yang paling muda yang mengandung karbon sebanyak 25-35%.
Pada umumnya warna lignit mulai dari coklat hingga hitam kecoklatan
(Gambar 3). Lignit sebagian besar terdiri dari material kayu kering yang
terkena tekanan tinggi. Lignit bersifat rapuh serta memiliki kandungan air
yang sangat tinggi sehingga perlu dikeringkan terlebih dahulu sebelum
dibakar. Sebagian besar lignit digunakan untuk pembangkit listrik. Struktur
kimia dan bentuk batubara lignit dapat dilihat pada gambar 2 (Speight,
1994).
(a) (b)
Gambar 2 . (a) Struktur Kimia Batubara Lignit (Schumacher,1997), (b) Bentuk Batubara Lignit (Bryant, 2005)
2. Subituminus
Batubara jenis subbituminus memiliki warna hitam. Kandungan karbon di
dalam batubara ini berkisar 35-45%. Batubara subbituminus memiliki nilai
kalor yang lebih rendah dari pada batubara bituminus. Batubara ini
merupakan batubara yang sering digunakan dalam industri karena di
Indonesia jumlahnya sangat melimpah. Struktur dan bentuk batubara
Subbituminus dapat dilihat pada gambar 3 (Speight, 1994)..
(a) (b)
Gambar 3. (a) Struktur Kimia Batubara Subbituminus (Schumacher,1997), (b) Bentuk Batubara Subbituminus (Bryant, 2005)
3. Bituminus
Batubara jenis bituminus dapat diperoleh dengan menambahkan panas
serta tekanan pada lignit. Batubara Bituminus mengandung karbon
sebanyak 45-86%. Penggunaan terbesar batubara bituminus terdapat di
pembangkit listrik serta industri baja. Bentuk batubara bituminus dapat dilihat
pada gambar 4 (Speight, 1994).
(a) (b)
Gambar 4 . (a) Struktur Kimia Batubara Bituminus (Schumacher,1997), (b) Bentuk Batubara Bituminus ((Bryant, 2005)
4. Antrasit
Antrasit merupakan golongan batubara yang paling tinggi, memiliki tampilan
yang hitam mengkilat seperti permukaan logam. Antrasit mengandung
karbon sebanyak 86-97%. Bentuk batubara Antrasit dapat dilihat pada
gambar 5 (Speight, 1994)
(a) (b)
Gambar 5. (a) Struktur Kimia Batubara Antrasit (Schumacher,1997), (b) Bentuk Batubara Antrasit (Bryant, 2005)
12
Dari keempat jenis batubara tersebut, masing-masing memiliki kualitas
airnya yang sangat tinggi harga lignit pun sangat murah. Oleh karena itu, untuk
pengolahan batubara menjadi energi alternatif, jenis yang banyak dipakai adalah
lignit karena cost effective (Speight, 1994).
2.1.3. Substansi Humik dalam Batubara
Substansi humik (HSs) merupakan produk organik yang berwarna coklat
sampai hitam dengan banyak pengaruhnya terhadap agrikultural dan lingkungan.
HSs merupakan karbon terkaya di bumi. HSs juga merupakan makromolekul
aromatik yang kompleks dengan variasi ikatan diantara gugus aromatik. Ikatan
yang berbeda termasuk diantaranya asam amino, peptida, asam alifatik, dan
senyawa alifatik lainnya. Gugus fungsional dalam sustansi humat termasuk gugus
asam karboksil (COOH), fenolik, alifatik, dan enolik-OH dan struktur karbonil
(C=O) dalam berbagai tipe yang bervariasi (Arianto et al., 2005).
Menurut Arianto et al., (2005), subtansi humik terdiri atas fraksi asam
humat, asam fulvat dengan klasifikasi sebagai berikut :
1. HumicAcid (Asam humat)
Warna gelap, amorf, dapat diekstraksi pada pH 4 keatas, tidak larut dalam
asam, mengandung gugus fungsional asam seperti fenolik dan karboksilik,
berat molekul (BM) 20000 hingga 1360000.
Gambar 6. Struktur Asam Humat (Stevenson, 1982)
2. Fulvic Acid (Asam fulvat)
Dapat diekstraksi dengan basa kuat, larut juga dalam asam, berat molekul
(BM) 275-2110.
Gambar 7 . Struktur Asam Fulvat (Stevenson, 1982)
2.2. Biosolubilisasi Batubara
Biosolubilisasi adalah proses pelarutan batubara dalam suatu medium
dengan bantuan mikroorganisme. Biosolubilisasi dapat berupa upaya untuk
mencairkan batubara atau bioliquifaksi yang nantinya dapat digunakan sebagai
bahan bakar pengganti minyak bumi. Disamping untuk mencairkan batubara,
biosolubilisasi dapat pula digunakan untuk mengurangi kandungan sulfur atau
logam toksik pada batubara (Faison et al.,1989).
Pencairan batubara dengan metode biologi dapat menekan biaya
operasional karena tidak dilakukan dalam tekanan dan temperatur yang tinggi
serta lebih ramah lingkungan karena tidak menghasilkan produk samping
berbahaya. Meskipun teknologi ini memiliki potensi besar, tetapi masih ada
sejumlah masalah yang harus dipecahkan. Tanpa adanya pelarut yang cocok,
produk yang dihasilkan tetap padat.
Meskipun produk terlarut memiliki kandungan energi tinggi dan
15
memungkinkan digunakan sebagai bahan bakar, tapi belum dapat digunakan
sebagai bahan bakar sarana transportasi. Selain itu, kebanyakan mikroorganisme
membutuhkan gula dan media pertumbuhan untuk pertumbuhan lebih dari 2
minggu. Media murah yang mampu mempercepat pertumbuhan mikroorganisme
dibutuhkan untuk aplikasi komersial. Masalah ekonomis lainnya yang
berhubungan adalah dibutuhkannya pra-perlakuan untuk menghasilkan produk
berkualitas (Liu et al., 1989).
Produksi batubara cair dapat juga dilakukan dengan memanfaatkan enzim
hasil isolasi dari mikroorganisme. Biosolubilisasi batubara dengan bantuan
mikroorganisme dapat menghasilkan produk yang setara dengan komponen
minyak bumi. Produk biosolubilisasi yang setara dengan senyawa yang terdapat
dalam bensin mempunyai rantai atom karbon yang pendek yaitu C4 sampai C12,
sedangkan untuk komponen minyak solar mempunyai atom karbon C10 sampai
C13 (American Petroleum Institute, 2001).
2.2.1. Mikroorganisme Pensolubilisasi Batubara
Terdapat beberapa jenis mikroorganisme dari jenis bakteri maupun jamur
yang dapat mengubah batubara padat menjadi produk cair. Batubara cair yang
dihasilkan dari proses biosolubilisasi adalah berupa campuran senyawa yang larut
dalam air, senyawa-senyawa polar dengan berat molekul relatif tinggi. Contoh
bakteri yang dapat dimanfaatkan untuk proses ini adalah Thiobacillus
Ferroxidans, Leptospirillum Ferroxidansdan Rhodococcus erythropolis.
Sementara itu contoh fungi yang dapat dimanfaatkan untuk proses ini diantaranya
16
Kapang adalah kelompok mikroorganisme yang tergolong dalam fungi.
Selain kapang, organisme lainnya yang termasuk ke dalam fungi adalah khamir
dan cendawan (mushroom). Kapang merupakan organisme multiseluler,
eukariotik, tidak berklorofil, dinding selnya tersusun dari kitin, bersifat heterotrof,
menyerap nutrient melalui dinding selnya, mengeksresikan enzim ekstraseluler ke
lingkungan, menghasilkan spora atau konidia, bereproduksi seksual dan atau
aseksual. Tubuh kapang terdiri dari hifa, hifa berfungsi menyerap nutrien dari
lingkungan serta membentuk struktur reproduksi (Hidayat et al, 2006).
Hifa adalah suatu struktur berbentuk tabung menyerupai seuntai benang
panjang yang terbentuk dari pertumbuhan spora atau konidia. Kumpulan hifa yang
bercabang-cabang membentuk suatu jala dan umumnya berwarna putih disebut
miselium. Ada beberapa kapang dengan miselia longgar atau seperti bulu kapas
sedangkan yang lainnya kompak. Penampakan miselia ada yang seperti beludru
(velvet) pada permukaan atasnya, beberapa kering seperti bubuk, basah atau
memiliki massa seperti gelatin (Hidayat et al, 2006).
Kapang saprofit adalah kapang yang memanfaatkan atau menyerap nutrien
dari benda mati. Pada umumnya, kapang mengekskresikan enzim ekstraseluler ke
lingkungan. Enzim ekstraseluler tersebut menguraikan komponen-komponen
kompleks pada substrat menjadi komponen-komponen sederhana yang dapat
dengan mudah diserap kapang untuk mensintesis berbagai bagian sel, dan
digunakan sebagai sumber energinya. Keberadaan kapang pada suatu substrat
dapat diketahui dengan adanya perubahan warna atau kekeruhan pada substrat
17
mengindikasikan adanya pertumbuhan kapang berupa pertambahan massa sel atau
volume sel (Gandjar et al, 2006).
Sifat-sifat fisiologi kapang sangat penting dipenuhi agar pertumbuhan
kapang menjadi optimal. Gandjar et al., (2006) menerangkan sifat-sifat fisiologi
kapang sebagai berikut :
1. Kebutuhan air
Pada umumnya, fungi tingkat rendah seperti Rhizopus sp. dan Mucor sp.
memerlukan lingkungan dengan kelembaban nisbi 90 %, kapang Aspergillus
sp, Penicillium sp, Fusarium sp. dan banyak hypomycetes lainnya dapat
hidup pada kelembaban yang lebih rendah yaitu 80 % sedangkan kapang
xerofilik mampu hidup pada kelembaban 70 %.
2. Suhu
Kebanyakan kapang bersifat mesofilik yaitu tumbuh baik pada suhu kamar.
Suhu optimum pertumbuhan untuk kebanyakan kapang adalah sekitar 25-30°
C, tetapi beberapa kapang dapat tumbuh pada suhu 35-37° C atau lebih tinggi
seperti Aspergillus sp. Beberapa kapang mampu tumbuh pada suhu dingin
(bersifat psikrotrofik) dan juga pada suhu tinggi (termofilik).
4. Derajat keasaman (pH)
Kebanyakan kapang mampu tumbuh pada kisaran pH yang luas yaitu 2 - 8,5
akan tetapi pertumbuhannya akan lebih baik pada kondisi asam atau pH
18 5. Substrat
Substrat merupakan sumber nutrien utama bagi kapang. Nutrien dalam
substrat baru dapat dimanfaatkan apabila kapang telah mengekskresikan
enzim-enzim ekstraseluler untuk menguraikan senyawa kompleks menjadi
sederhana.
6. Komponen penghambat
Beberapa kapang mengeluarkan komponen yang dapat menghambat
organisme lainnya seperti bakteri, komponen tersebut disebut antibiotik.
2.2.2. Solubilisasi Batubara oleh Kapang
Batubara diperkaya dengan berbagai macam polimer organik yang berasal
dari karbohidrat dan lignoselulosa yang terdiri dari selulosa, hemiselulosa dan
lignin. Selulosa merupakan komponen utama penyusun dinding sel tanaman, dan
salah satu komponen pembangun tumbuhan. Selulosa adalah polimer yang
tersusun atas unit-unit glukosa melalui ikatan α-1,4-glikosida. Enzim yang dapat
mengurai selulosa adalah selulase dan merupakan enzim kompleks yang terdiri
dari tiga komponen. Endoglukanase, mengurai polimer selulosa secara random
pada ikatan internal α-1,4-glikosida untuk menghasilkan oligodekstrin dengan
panjang rantai bervariasi. Eksoglukanase, mengurai selulosa dari ujung pereduksi
dan nonpereduksi untuk menghasilkan selobiosa/glukosa. Enzim α-glukosidase,
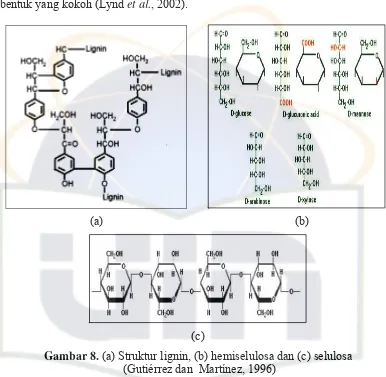
mengurai selobiosa untuk menghasilkan glukosa (Lynd et al., 2002).
Hemiselulosa merupakan kelompok polisakarida heterogen dengan berat
molekul rendah, relatif lebih mudah dihidrolisis dengan asam menjadi monomer
merupakan polimer dengan struktur aromatik yang terbentuk melalui unit-unit
penilpropan. Lebih dari 30 % tanaman tersusun atas lignin yang memberikan
bentuk yang kokoh (Lynd et al., 2002).
(a) (b)
(c)
Gambar 8. (a) Struktur lignin, (b) hemiselulosa dan (c) selulosa (Gutiérrez dan Martínez, 1996)
Lignin sulit disolubilisasi karena strukturnya kompleks dan heterogen
yang berikatan dengan selulosa dan hemiselulosa dalam jaringan tanaman
(Orth et al, 1993). Lignin merupakan suatu unsur yang memegang peranan
penting dalam merubah susunan sisa tumbuhan menjadi batubara. Sebagian besar
mikroorganisme yang mampu mensolubilisasi lignin dapat diaplikasikan juga
untuk mensolubilisasi batubara (Cohen et al., 1990).
20
Enzim pensolubilisasi lignin secara umum terdiri dari dua kelompok
utama yaitu laccase (Lac) dan peroksidase yang terdiri dari lignin peroksidase
(LiP) dan mangan peroksidase (MnP) (Chahal dan Chahal, 1998). Ketiga enzim
tersebut bertanggung jawab terhadap pemecahan awal polimer lignin (Akhtar et
al., 1997). Mangan peroksidase (MnP), lignin peroksidase (LiP) atau laccase
mampu mensolubilisasi komponen aromatik pada batubara dan
mendepolimerisasinya menjadi komponen yang kaya oksigen dan dapat melarut
ke dalam air (Holker et al., 2002).
Enzim pendegradasi lignin secara umum terdiri dari dua kelompok utama
yaitu laccase (Lac) dan peroksidase yang terdiri dari lignin peroksidase (LiP) dan
mangan peroksidase (MnP) (Chahal and Chahal, 1998). Ketiga enzim tersebut
bertanggung jawab terhadap pemecahan awal polimer lignin dan menghasilkan
produk dengan berat molekul rendah, larut dalam air dan CO2 (Akhtar et al.,
1997).
Lignin peroksidase (LiP) merupakan enzim utama dalam proses
degaradasi lignin karena mampu mengoksidasi unit non fenolik lignin. Unit non
fenolik merupakan penyusun sekitar 90 persen struktur lignin. Oksidasi
substruktur lignin yang dikatalis oleh LiP dimulai dengan pemisahan satu elektron
cincin aromatik substrat donor dan menghasilkan radikal aril. LiP memotong
ikatan Cα-Cβ molekul lignin, pemotongan tersebut merupakan jalur utama
perombakan lignin oleh berbagai kapang pelapuk putih (Hammel, 1996).
Mangan peroksidase (MnP) berperan dalam oksidasi unit fenolik, sehingga
21
pengikatan H2O2 atau peroksida organik dengan enzim ferric alami dan
pembentukan kompleks peroksida besi. Pemecahan ikatan oksigen peroksida
membutuhkan Fe oxo-porphyrin-radikal kompleks dalam pembentukan
MnP-komponen I, kemudian ikatan dioksigen dipecah dan dikeluarkan satu molekul air.
Reaksi berlangsung sampai terbentuk MnP-komponen II, ion Mn2+ bekerja
sebagai donor 1-elektron untuk senyawa antara porfirin dan dioksidasi menjadi
Mn3+. Mn3+ merupakan oksidasi kuat yang dapat mengoksidasi senyawa fenolik
tetapi tidak dapat menyerang unit non fenolik lignin (Perez et al., 2002).
Laccase ditemukan pada kapang, khamir, dan bakteri. Enzim ini tidak
membutuhkan H2O2 tetapi menggunakan molekul oksigen. Laccase mereduksi
oksigen menjadi H2O dalam substrat fenolik melalui reaksi satu elektron
membentuk radikal bebas yang dapat disamakan dengan radikal kation yang
terbentuk pada reaksi MnP (Kersten et al., 1990).
Tabel 4. Enzim ekstraseluler pendegradasi lignin dari kapang pelapuk putih (Akhtar et al.,1997).
Enzim Tipe Enzim Peran dalam Degradasi
Peroksidase Degradasi unit non fenolik
H2O2 2,5-3,0
Mangan peroksi dase
22
Kapang yang memiliki kemampuan paling baik dalam proses
biosolubilisasi batubara adalah Trametes versicolor, Pleurotus florida, P.
ostreatus and P. sajorcaju. Kapang lain yang juga mampu mensolubilisasi
batubara seperti Trichoderma atroviride, Fusarium oxysporum, Penicillium sp.,
Candida sp., Aspergillus sp., Mucor sp. dan Sporothrix sp. namun dengan
kemampuan yang lebih kecil. Kapang tersebut mensolubilisasi batubara
menggunakan enzim ekstraseluler (Reiss, 1992).
Enzim ekstraseluler adalah enzim yang diekskresikan oleh kapang ke luar
tubuhnya untuk mensolubilisasi substrat. Enzim ekstraseluler tersebut akan
menghasilkan medium yang lebih gelap akibat dari solubilisasi batubara selama
proses kultur cair atau cairan gelap pada permukaan kultur ketika ditumbuhkan
pada permukaan kultur agar (Faison et al, 1989).
2.2.3. Faktor-Faktor yang Berpengaruh Terhadap Biosolubilisasi Batubara
Di dalam proses biodegradasi terdapat beberapa faktor yang berpengaruh
terhadap kerja mikroorganisme yang digunakan. Faktor-faktor tersebut dapat
berupa kondisi lingkungan, ataupun perlakuan awal terhadap batubara. Beberapa
faktor yang berpengaruh terhadap proses biosolubilisasi diantaranya:
A. Temperatur
Secara umum kenaikan temperatur akan meningkatkan laju reaksi kimia,
termasuk reaksi yang dilakukan oleh mikroorganisme. Temperatur proses
biodegradasi harus dikendalikan agar tetap berada pada temperatur optimum
mikroorganisme yang digunakan serta tidak melewati temperatur minimum
23
temperatur optimum dan temperatur maksimum yang berbeda-beda. Oleh
karena itu, temperatur optimum biodegradasi akan sangat bergantung pada
mikroorganisme yang digunakan. Temperatur optimum pada kapang adalah
22-30 oC (Pelzar dan Chan, 2005).
B. pH
Seperti halnya temperatur, pH juga sangat berpengaruh terhadap proses
biosolubilisasi. Setiap mikroorganisme memiliki pH optimum yang berlainan
oleh karena itu biodegradasi harus dilakukan pada pH optimum sesuai dengan
mikroorganisme yang digunakan. Jika pH yang digunakan terlalu asam atau
basa maka proses biodegradasi akan mengalami inhibisi. Inhibisi ini terjadi
akibat pengaruh buruk lingkungan yang terlalu asam terhadap metabolisme
mikroorganisme yang menyebabkan aktivitas metaboliknya menurun. pH
optimum kapang adalah 3,8-5,6 (Pelzar dan Chan, 2005).
C. Ukuran Partikel
Ukuran partikel batubara memberikan pengaruh terhadap persentase
pengurangan sulfur dalam proses biodegradasi batubara. Semakin kecil
ukuran partikel batubara maka persentase pengurangan sulfur akan semakin
besar. Ukuran partikel yang kecil menyebabkan luas pemukaan kontak antara
sel bakteri dengan batubara semakin besar. Akibatnya reaksi oksidasi
senyawa sulfur yang terjadi akan semakin banyak pula. Ukuran batubara
24 D. Konsentrasi Mikroorganisme
Semakin sedikit konsentrasi sel mikroorganisme, maka efisiensi biodegradasi
akan semakin berkurang. Pada umumnya konsentrasi mikroorganisme yang
digunakan adalah 5 % (Scott dan lewis, 1990).
2.3. Analisis Kimia Terhadap Produk Solubilisasi Batubara
Produk biosolubilisasi batubara dikarakterisasi menggunakan
Spektrofotometer UV-Vis, Spektrofotometer infra merah (FTIR), dan
Kromatografi Gas - Spektroskopi Massa (GC-MS) sebagaimana yang telah
dilakukan oleh Shi, et al., (2009).
2.3.1. Spektrofotometer UV-Vis
Spektrofotometer sesuai dengan namanya adalah alat yang terdiri dari
spektrometer dan fotometer. Spektrometer menghasilkan sinar dari spektrum
dengan panjang gelombang tertentu dan fotometer adalah alat pengukur intensitas
cahaya yang ditransmisikan atau yang diabsorpsi. Jadi spektrofotometer
digunakan untuk mengukur energi secara relatif jika energi tersebut
ditransmisikan, direfleksikan atau diemisikan sebagai fungsi dari panjang
gelombang (Underwood dan Day, 2002).
Semua molekul dapat mengabsorpsi radiasi dalam daerah UV-Vis karena
mengandung elektron, baik sekutu maupun menyendiri, yang dapat dieksitasikan
ke tingkat yang lebih tinggi. Panjang gelombang di mana absorpsi itu terjadi,
bergantung pada berapa kuat elektron itu terikat dalam molekul itu (Underwood
Gambar 9. Spektrofotometer UV-vis (Dokumen Pribadi,2010)
Kebanyakan penerapan spektrofotometri ultraviolet dan cahaya tampak
pada senyawa organik didasarkan pada transisi n-π* ataupun π-π* dan karenanya
memerlukan hadirnya gugus kromofor dalam molekul itu. Transisi itu terjadi
dalam daerah spektrum (sekitar 200 nm hingga 700 nm) yang praktis untuk
digunakan dalam eksperimen. Identifikasi kualitatif senyawa organik dalam
daerah ini jauh lebih terbatas daripada dalam daerah inframerah. Ini karena pita
absorpsi terlalu lebar dan kurang terinci. Tetapi gugus-gugus fungsional tertentu
seperti karbonil, nitro, dan sistem terkonjugasi, benar-benar menunjukkan puncak
karakteristik, dan sering dapat diperoleh informasi yang berguna mengenai ada
atau tidaknya gugus semacam itu dalam molekul tersebut (Underwood dan Day,
2002).
Pada penelitian ini analisis produk biosolubilisasi batubara dilakukan
dengan menggunakan spektroskopi sinar ultraviolet-visible (UV-Vis).
Spektroskopi UV-Vis dapat menentukan adanya ikatan tak jenuh dalam produk
biosolubilisasi (Shi et al., 2009). Panjang gelombang yang digunakan yaitu 250
dan 450 nm.
26
2.3.2. Spektrofotometer Fourier Transform Infra Red (FTIR)
Spektrofotometri infra merah merupakan teknik yang di dasarkan pada
vibrasi (pergerakan) atom-atom dalam molekul. Spektrum infra merah pada
umumnya dihasilkan melalui sampel dan penentuan fraksi akibat dari sinar yang
diabsorbsi pada energi tertentu. Energi tempat munculnya peak absorpsi
berhubungan dengan frekuensi vibrasi suatu gugus fungsi atau kromofor yang
terdapat dalam suatu molekul. Spektrofotometri IR ditujukan untuk penentuan
gugus-gugus fungsi molekul pada analisis kualitatif (Giwangkara, 2006).
Energi dari kebanyakan vibrasi molekul berhubungan dengan daerah infra
merah. Vibrasi molekul dapat dideteksi dan diukur pada spektrum infra merah,
penggunaan spektrum infra merah untuk penentuan struktur senyawa organik
biasanya antara 650-4000 cm-1 (15,4-2,5 µm). Daerah di bawah frekuensi
650 cm-1 dinamakan infra merah jauh dan daerah di atas frekuensi 4000 cm-1
dinamakan infra merah dekat. Letak puncak serapan dapat dinyatakan dalam
satuan frekuensi (µm) atau bilangan gelombang (cm-1 ) (Sudjadi, 1985).
Atom-atom di dalam molekul tidak dalam keadaan diam, tetapi biasanya
terjadi peristiwa vibrasi. Hal ini bergantung pada atom-atom dan kekuatan ikatan
yang menghubungkannya. Vibrasi dapat digolongkan atas dua golongan besar,
yaitu : vibrasi renggangan (stretching) dan vibrasi bengkokan (bending)
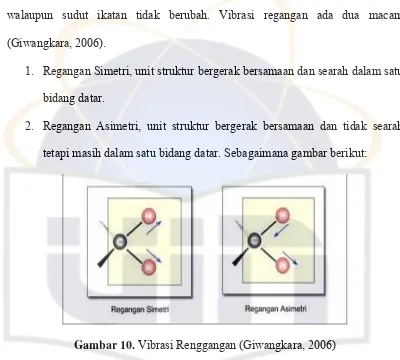
A. Vibrasi Regangan (Streching)
Dalam vibrasi ini atom bergerak terus sepanjang ikatan yang
menghubungkannya sehingga akan terjadi perubahan jarak antara keduanya,
walaupun sudut ikatan tidak berubah. Vibrasi regangan ada dua macam
(Giwangkara, 2006).
1. Regangan Simetri, unit struktur bergerak bersamaan dan searah dalam satu
bidang datar.
2. Regangan Asimetri, unit struktur bergerak bersamaan dan tidak searah
tetapi masih dalam satu bidang datar. Sebagaimana gambar berikut:
Gambar 10. Vibrasi Renggangan (Giwangkara, 2006)
B. Vibrasi Bengkokan (Bending)
Jika sistem tiga atom merupakan bagian dari sebuah molekul yang lebih
besar, maka dapat menimbulkan vibrasi bengkokan atau vibrasi deformasi yang
mempengaruhi osilasi atom atau molekul secara keseluruhan. Vibrasi bengkokan
ini terbagi menjadi empat jenis (Giwangkara, 2006).
1. Vibrasi Goyangan (Rocking), unit struktur bergerak mengayun asimetri
tetapi masih dalam bidang datar.
2. Vibrasi Guntingan (Scissoring), unit struktur bergerak mengayun simetri
dan masih dalam bidang datar.
3. Vibrasi Kibasan (Wagging), unit struktur bergerak mengibas keluar dari
bidang datar.
4. Vibrasi Pelintiran (Twisting), unit struktur berputar mengelilingi ikatan
yang menghubungkan dengan molekul induk dan berada di dalam bidang
datar.
Gambar 11. Vibrasi Bengkokan (Giwangkara, 2006)
Jika suatu senyawa organik disinari dengan sinar infra-merah yang
mempunyai panjang gelombang tertentu, akan didapatkan bahwa beberapa
frekuensi tersebut diserap oleh senyawa tersebut. Sebuah alat pendetektor yang
diletakan di sisi lain senyawa tersebut akan menunjukkan bahwa beberapa
frekuensi melewati senyawa tersebut tanpa diserap sama sekali, tapi frekuensi
lainya banyak diserap. Beberapa banyak frekuensi tertentu yang melewati
senyawa tersebut diukur sebagai persen transmitan (Sudjadi, 1985).
Gambar 12. Instrumentasi FTIR (Dokumen Pribadi, 2010)
Pada sistem optik FTIR digunakan radiasi LASER (Light Amplification By
Stimulated Emmission of Radiation) yang berfungsi sebagai radiasi yansg
diinterferensikan dengan radiasi infra merah agar sinyal radiasi infra merah yang
diterima oleh detektor secara utuh dan lebih baik. Detektor yang digunakan dalam
spektrofotometer FTIR adalah TGS ( Tetra Glycerine Sulphate) atau MCT
(Mercury Cadmium Telluride). Detektor MCT lebih banyak digunakan karena
memiliki beberapa kelebihan dibandingkan detektor TGS yaitu memberikan
respon yang lebih baik pada frekuensi modulasi tinggi, lebih sensitif, cepat tidak
dipengaruhi oleh temperatur, sangat selektif terhadap energi vibrasi yang diterima
dari radiasi infra merah (Giwangkara, 2006).
30
Tabel 5. Beberapa Contoh Nilai Frekuensi Gugus Fungsi
Gugus Fungsi Panjang Gelombang Frekuensi (cm-1)
O-H Alkohol/fenol bebas
Asam karboksilat
sekunder dan amida
6,10-6,45 3140-3320
2.3.3. Gas Chromatography Mass Spectrometry (GC-MS)
Kromatografi Gas-Spektroskopi Massa atau sering disebut GC-MS (Gass
Chromatography Mass Spectrometry) adalah teknik analisis yang
Massa. Kromatografi gas adalah metode analisis, dimana sampel terpisahkan
secara fisik menjadi bentuk molekul-molekul yang lebih kecil (hasil pemisahan
dapat dilihat berupa kromatogram). Sedangkan spektroskopi massa adalah metode
analisis, dimana sampel yang dianalisis akan diubah menjadi ion-ion gasnya, dan
massa dari ion-ion tersebut dapat diukur berdasarkan hasil deteksi berupa
spektrum massa (Underwood dan Day, 2002).
Gambar 13. Instrumentasi GC-MS (Dokumen Pribadi, 2010)
Pada GC hanya terjadi pemisahan untuk mendapatkan komponen yang
diinginkan, sedangkan bila dilengkapi dengan MS (berfungsi sebagai detector)
komponen tersebut dapat teridentifikasi, karena Spektrum Bobot Molekul pada
suatu komponen dapat dilihat, serta dapat juga dibandingkan dengan LIBRARY
(reference) pada software (Hermanto, 2008).
Pemisahan komponen senyawa dalam GC-MS terjadi di dalam kolom
(kapiler) GC dengan melibatkan dua fase, yaitu fase diam dan fase gerak. Fase
diam adalah zat yang ada di dalam kolom, sedangkan fase gerak adalah gas
pembawa (Helium maupun Hidrogen dengan kemurnian tinggi, yaitu ± 99,995%).
Proses pemisahan dapat terjadi karena terdapat perbedaan kecepatan alir dari tiap
32
molekul di dalam kolom. Perbedaan tersebut dapat disebabkan oleh perbedaan
afinitas antar molekul dengan fase diam yang ada di dalam kolom.
Komponen-komponen yang telah dipisahkan tersebut masuk ke dalam ruang MS yang
berfungsi sebagai detektor secara instrumentasi (Hermanto, 2008).
Injeksi sampel berupa cairan adalah teknik memasukkan sampel yang
paling umum. Sampel langsung dimasukkan atau diinjeksi setelah mendapat
preparasi. Direct Inlet Probe digunakan untuk sampel yang memilki titik uap yang
lebih tinggi dari kemampuan injector GC atau untuk analisis sampel yang tidak
stabil secara termal. Sampel langsung dimasukkan ke dalam MS tanpa melalui
GC. Teknik Headspace digunakan untuk sampel hasil ekstraksi dari
senyawa-senyawa organik yang mudah menguap. Senyawa-senyawa-senyawa tersebut terdapat di
dalam produk berbentuk cair atau padat. Misalnya, senyawa yang mudah
menguap di dalam air, aroma di dalam produk makanan dan sebagainya. Sampel
dimasukkan ke dalam wadah khusus, lalu diinkubasi. Setelah terjadi ekuilibrium
gas yang berada di atas diambil oleh syringe. Lalu sampel dimasukkan ke dalam
GC. Teknik sampling ini menggunakan alat khusus yang terpisah dari instrumen
GC-MS, sedangkan pirolis digunakan untuk sampel yang tidak dapat diuapkan
oleh injector GC, misalnya polimer-polimer.
Sampel pertama kali diuraikan terlebih dahulu oleh pemanasan dalam alat
khusus, hasil dekomposisi dapat dianalisis oleh GC. Purge dan Trap, digunakan
untuk sampel hasil ekstraksi dari senyawa-senyawa organik yang mudah
menguap. Zat yang mudah menguap (zat volatil) pertama kali dikeluarkan dari
33
oleh zat khusus untuk meng-absorb seperti karbon aktif. Kemudian absorben
dipanaskan untuk melepaskan senyawa yang diinginkan ke dalam GC untuk
34
BAB III
METODE PENELITIAN
3.1. Waktu dan Tempat Penelitian
Penelitian ini dilaksanakan pada bulan April - Juni 2010. Bertempat di
Badan Tenaga Nuklir Nasional (BATAN) Pasar Jumat, Lebak Bulus, Jakarta
Selatan dan Pusat Laboratorium Terpadu UIN Syarif Hidayatullah Jakarta.
3.2. Alat dan Bahan 3.2.1. Alat
Alat - alat yang digunakan adalah Gas Chromatograph Mass Spectrometer
(GC-MS) Shimadzu QP 2010, Fourier Transform Infra Red (FTIR) Spectrum One
Perkin Elmer, Spektrofotometer Spectronic Genesys, mikroskop, Laminar Air
Flow Cabinet (LAFC), Shaker, autoklaf, refrigerator, inkubator, pH meter
HANNA Instruments HI 8520, saringan berukuran 100 mesh, desikator, oven,
vortex Heidolph REAX 2000, hot plate, magnetic stirrer, kuvet, Erlenmeyer,
spatula, pinset, ose, bunsen, gelas ukur, mortal, Handy Press, sel KBr, botol
semprot, corong buchner, pipet tetes, parafilm, mikropipet, cawan Petri, kaca
objek, cover glass, tabung reaksi, dan rak tabung.
3.2.2. Bahan
Bahan – bahan yang digunakan adalah batubara jenis lignit dengan ukuran
100 mesh yang berasal dari daerah pertambangan Lahat Sumatera Selatan, 4 jenis
isolat kapang yang berasal dari tanah pertambangan Lahat Sumatera Selatan (kode
35
(MSS), Minimalt Salt Sugar Agar (MSSA), agar bakto, larutan fisiologis (NaCl
0.85%), sukrosa 0,1 %, yeast ekstrak, Flourescein Diacetate (FDA), aseton (pa),
KH2PO4 (pa), alumunium foil, aquadest, alkohol 70%, benzen, heksana, dietil
eter, serbuk KBr kering.
Tabel 6. Komposisi Medium
Nama
3.3.1. Persiapan dan Sterilisasi Alat
Alat – alat gelas yang akan digunakan dibersihkan terlebih dahulu.
Alat-alat yang telah dibersihkan, disterilkan dengan autoklaf pada suhu 121oC selama
15 menit. Peralatan yang tidak tahan panas disterilkan dengan menggunakan
alkohol 70% (Waluyo, 2008).
3.3.2. Persiapan Serbuk Batubara
Batubara digerus dengan mortal secara aseptik di dalam LAFC hingga
berukuran kecil. Batubara yang telah digerus, disaring menggunakan penyaring
dengan ukuran 100 mesh dan diayak sampai halus. Sampel batubara yang sudah
36 3.3.3. Pembuatan Medium Minimal Salt (MS)
Medium MSS dibuat dengan cara menimbang sebanyak 0,52 g
MgSO4.7H2O ; 0,003 g ZnSO4.7H2O ; 5 g KH2PO4 ; 0,005 g FeSO4, dan 1 g
NH4(SO4). Bahan-bahan tersebut dilarutkan dengan 1 liter aquades. Campuran
tersebut dilarutkan sampai homogen (Silva et al, 2007).
3.3.4. Pembuatan Medium Minimal Salt + Sugar + Agar (MSSA)
Medium MSSA dibuat dengan sebanyak 100 ml MS, ditambahkan
batubara 1 % (2 g) dan dimasukan ke dalam Erlenmeyer 1, ditutup dengan
alumunium foil, kemudian 100 ml aquadest dimasukan ke dalam Erlenmeyer 2
yang berbeda lalu ditambahkan 1,5 g agar, 1 g sukrosa, dan 0,2 g ekstrak ragi
setelah itu dipanaskan dan ditutup dengan alumunium foil. Kedua Erlenmeyer
diautoklaf dengan tekanan 1 atm, suhu 121oC selama 15 menit. Kedua larutan
yang berada di Erlenmeyer berbeda tersebut dicampur, dihomogenkan, dan
dituang ke dalam cawan petri yang telah diautoklaf.
3.3.5. Peremajaan Kultur Spora Kapang
Empat jenis Kultur kapang hasil isolasi dari tanah pertambangan diambil
menggunakan ose steril, kemudian diinokulasi ke dalam 4 cawan petri yang berisi
15 ml medium MSSA. Medium MSSA direkatkan menggunakan parafilm dan
diberi label sesuai kode isolatnya. Cawan petri yang berisi kultur kapang tersebut
diinkubasi pada suhu ruang 5-7 hari sampai kapang menghasilkan spora.
3.3.6. Kultur Inokulum Spora
Isolat kapang hasil peremajaan dengan medium MSSA, dimasukkan 10 ml
37
ose steril hingga larut. Larutan spora dituang ke dalam yellow tube, diberi label
sesuai kode isolatnya dan divorteks (Fardiaz, 1992).
3.3.7. Pembuatan Medium Minimal Salt + Sugar (MSS)
Medium MSS dibuat dengan sebanyak 600 ml MS, ditambahkan sukrosa
0,1 % (0,6 g) dan ekstrak ragi 0,1 % (0,6 g). Campuran tersebut dihomogenkan
dan dimasukan ke dalam 20 tabung Erlenmeyer masing-masing 30 ml, kemudian
ditambahkan 5% serbuk batubara (1,5 g) ke dalam 20 Erlenmeyer tersebut.
Erlenmeyer ditutup rapat dengan alumunium foil dan diautoklaf dengan suhu
121oC selama 15 menit.
3.3.8. Biosolubilisasi Batubara
Keempat kultur inokulum spora sebanyak 5 % diinokulasikan ke dalam
30 ml medium MSS yang telah ditambahkan batubara 1,5 g. Medium MSS
tersebut diinkubasi menggunakan shaking incubator dengan kecepatan 150 rpm,
pada suhu ruang, selama 28 hari. Pencuplikan sampel kultur dilakukan pada hari
ke 0, 7, 14, 21, dan 28 menurut metode Scott dan Lewis, 1990.
Sampel kultur dimasukan ke dalam yellow tube dan diberi label, kemudian
disentrifugasi untuk memisahkan endapan dari supernatannya. Sampel selanjutnya
disaring dengan kertas whatman No.1. Supernatan yang didapatkan dianalisis pH,
aktivitas enzim, asam humat dan fulvat, dan solubilisasi batubara dengan
spektrofotometer UV-Vis dan GC-MS. Endapan batubara yang telah terpisah
38 3.3.9. Pengukuran pH Medium Sampel
Supernatan dari masing-masing sampel diukur nilai pH nya menggunakan
pH meter yang telah dikalibrasi.
3.3.10. Pengukuran Aktivitas Enzim
Supernatan dimasukan 1 ml ke dalam tabung reaksi, kemudian
ditambahkan 4 ml KH2PO4. Reaksi dimulai dengan menambahkan 40 g FDA
kemudian divortex dan inkubasi selama 20 menit. Setelah penginkubasian segera
ditambahkan aseton sebanyak 4 ml untuk menghentikan reaksi kemudian tutup
dengan alumunium foil. Suspensi disaring dengan kertas whatman N0. 1. Filtrat
dimasukan ke dalam tabung reaksi , ditutup dengan kertas parafilm dan disimpan
dalam es batu untuk menguapkan aseton. Nilai absorbansi diukur dengan
menggunakan spektrofotometer pada panjang gelombang 490 nm (Breeuwer,
1996).
3.3.11. Pengukuran Asam Fulvat dan Asam Humat • Asam Fulvat
Terhadap setiap sampel dilakukan perlakuan asam yakni dengan
menambahkan asam klorida (HCl) 4 N hingga pH mencapai 1, setelah pH
mencapai nilai yang diinginkan kemudian dilakukan sentrifugasi selama 20 menit
dengan kecepatan 8000 rpm. Dari proses tersebut didapatkan supernatan dan
pellet yang terpisah di dasar tabung sentrifugasi. Supernatan yang didapatkan
kemudian dipindahkan ke dalam tabung terpisah dan diukur absorbansinya
menggunakan spekrofotometer pada panjang gelombang 280 nm (Fakuosa dan
39 • Asam Humat
Setelah proses asidifikasi menggunakan HCl 4 N, maka endapan yang
didapatkan dari hasil sentrifugasi diperlakukan lebih lanjut yakni dengan
membilasnya menggunakan aquadest hingga pH nya mencapai nilai 4. Setelah itu
dilakukan pengukuran absorbansinya dengan menggunakan spektrofotometer
pada panjang gelombang 450 nm (Fakuosa dan Frost, 1998).
3.3.12. Pengukuran Solubilisasi dengan Spektrofotometer UV-Vis
Supernatan hasil solubilisasi disentrifugasi 5400 rpm selama 15 menit
kemudian diukur nilai absorbansinya menggunakan Spektrofotometer UV-Vis
pada panjang gelombang 250 nm dan 450 nm untuk mengetahui tingkat
solubilisasi batubara. Nilai absorbansi yang tinggi berbanding lurus dengan
tingkat solubilisasi batubara yang tinggi pula, data tersebut digunakan sebagai
dasar untuk menyeleksi isolat kapang. Supernatan (sampel) dengan nilai absorbsi
(biosolubilisasi) tertinggi akan diuji lanjut menggunakan GC-MS (Selvi dan
Banerje, 2007).
3.3.13. Analisis Sample dengan Menggunakan FTIR
Endapan batubara dianalisis dengan FTIR pada range frekuensi 4000- 450
cm-1 dengan resolusi 4 cm-1. Endapan batubara hasil biosolubilisasi terlebih
dahulu dioven pada suhu 55 oC. Sebanyak 0,2 g sampel dibuat pellet dalam KBr
dengan rasio 1:100. Sampel dicampurkan dengan serbuk KBr kering dengan
lumpang agate atau vibrating Ball Mill hingga benar-benar homogen. Campuran
tersebut dicetak dengan handy press. Cakram KBr yang sudah terbentuk
40
FTIR (Shi et al., 2009). Kontrol yang digunakan adalah batubara lignit yang
belum diberi perlakuan biosolubilisasi.
3.3.14. Analisis Hasil Solubilisasi Batubara oleh Kapang dengan Menggunakan GC-MS
Supernatan hasil solubilisasi dan pelarut dicampur dengan perbandingan
1:1. Pelarut yang digunakan adalah benzena : heksana : dietil eter dengan
perbandingan 3:1:1. campuran lalu diaduk, didiamkan beberapa saat sampai
terbentuk fase atas dan bawah. Fase atas selanjutnya dimasukan ke dalam vial
untuk dianalisis dengan alat GC-MS. Kontrol yang digunakan adalah batubara
yang dilarutkan dalam medium minimal salt, kemudian diekstrak dengan pelarut
yang sama. Kondisi optimum GC-MS yang digunakan sebagai berikut (Silva et
al., 2007).
Tabel 7 . Kondisi Optimum GC-MS
Spesifikasi Keterangan
Nama kolom (RTX-1MS) Restax
Panjang kolom 30 m
Diameter kolom 0,25 mm
Ketebalan kolom 0,25 m df
Jenis kolom Non polar
Suhu kolom oven 50 oC
Suhu injeksi 280 oC
Cara injeksi Split
Cara kontrol aliran Kecepatan linear
Tekanan 90,7 kPa
Total aliran 19,9 mL/menit
Aliran kolom 1,54 mL/menit
Kecepatan linear 45 cm/detik
Jumlah sampel 5 l
Fase diam Polimethyl siloxane
Fase gerak Gas helium
3.4. Skema Kerja
Produk biosolubilisasi
BAB IV
HASIL DAN PEMBAHASAN
4.1. Perubahan Nilai Derajat Keasaman (pH) pada Medium
Perubahan pH merupakan hal yang menjadi salah satu faktor pengukuran
dalam proses solubilisasi batubara. Solubilisasi yang dilakukan oleh seluruh
kapang pada penelitian ini menghasilkan pH yang asam. pH awal seluruh kapang
pada hari ke-0, yaitu berkisar antara 4,25 – 4,5, pada hari ke-7,14 dan 21 inkubasi,
pH mengalami penurunan yang berkisar antara 3,31 - 4,5. Setelah hari ke-28
inkubasi seluruh kapang cendrung mengalami sedikit peningkatan berkisar antara
3,49 - 3,55 (Gambar 14).
Gambar 14. Nilai pH Medium pada Berbagai kapang
Penurunan pH yang terjadi dapat disebabkan terbentuknya asam-asam
organik dan juga dapat disebabkan telah terjadinya desulfurisasi, dimana sulfur
dalam batubara terlarut ke dalam medium cair dalam bentuk ion sulfat (SO42-)