SUAEDAH
SEKOLAH PASCASARJANA
INSTITUT PERTANIAN BOGOR
PERNYATAAN MENGENAI TESIS
DAN SUMBER INFORMASI
Dengan ini saya menyatakan bahwa tesis dengan judul model SEIRS-LSEI pada penyakit chikungunya adalah karya saya sendiri dengan arahan dari komisi pembimbing dan belum diajukan dalam bentuk apapun kepada perguruan tinggi manapun. Sumber informasi yang berasal atau dikutip dari karya yang diterbitkan maupun tidak diterbitkan dari penulis lain telah disebutkan dalam teks dan dicantumkan dalam daftar pustaka di bagian akhir tesis ini.
Bogor, Juli 2012
BAKHTIAR and ALI KUSNANTO.
Chikungunya is a disease caused by the chikungunya virus. It is spread to human through the bites of Aedes aegypti and Aedes albopictus mosquitoes. A SEIRS-LSEI model is proposed to formulate the dynamic of chikungunya disease from mosquito to human. SEIRS-LSEI model of chikungunya has four equilibrium points, i.e. two disease free and two endemic points. The stability of those points are determined according to the eigen values of Jacobi matrix. The existence of the disease are controlled by the basic reproduction number
In this thesis, the dynamical analysis of interaction between human and mosquito is given by some illustrative examples. We consider two policies in controlling mosquito population, i.e. spraying and using antimosquito lotion. Mosquito spraying will increase the parameter of mosquito mortality, while spraying antimosquito lotion will decrease the parameter of average daily biting. The dynamics of the disease is mainly determined by the intensity of interaction of human susceptible with infected mosquito. Simulation results confirm that, if the rate of mosquito mortality increases by spraying, then the population of infected human decreases, such that the population of suscepted human increases. The same situation happens when the average daily biting of infected mosquito decreases by lotion usage.
. If the number is less than one, then the disease can be removed from the population. On the other hand, if the number is greater than one, then the disease remains in the population.
RINGKASAN
SUAEDAH. Model SEIRS-LSEI pada Penyakit Chikungunya. Di bawah bimbingan TONI BAKHTIAR dan ALI KUSNANTO.
Chikungunya adalah penyakit yang disebabkan oleh virus chikungunya yang disebarkan ke manusia melalui gigitan nyamuk Aedes aegypti dan nyamuk Aedes albopictus (Pialoux et al., 2007). Model matematika penyebaran penyakit chikungunya yang diperkenalkan oleh Dumont et al., 2008, dengan mengklasifikasikan menjadi dua populasi yaitu populasi manusia berbentuk SEIR (Susceptible-Exposed-Infected-Resistant) dan populasi nyamuk berbentuk LSEI (Larvae-Susceptible-Exposed-Infected). Dalam tulisan ini dikembangkan model SEIR (Dumont et al., 2008) pada penyakit chikungunya dengan menambahkan asumsi bahwa individu yang mempunyai kekebalan tubuh setelah terserang penyakit menjadi rentan kembali walaupun peluangnya sangat kecil, sehingga model ini disebut model SEIRS (Susceptible-Exposed-Infected-Resistant- Susceptible).
Tujuan utama dalam penulisan ini adalah (1) Mengkonstruksi model penyebaran penyakit chikungunya model SEIRS-LSEI, (2) Melakukan analisis kestabilan model penyebaran penyakit chikungunya, (3) Melakukan simulasi numerik terhadap model SEIRS untuk melihat pengaruh perubahan nilai parameter, yakni laju kematian nyamuk dan rata-rata gigitan nyamuk terinfeksi terhadap dinamika populasi manusia rentan per hari.
Dari model SEIRS-LSEI pada penyakit chikungunya yang dilakukan secara simultan maka didapat 4 (empat) titik tetap yaitu: dua titik tetap tanpa penyakit dan dua titik tetap endemik di mana kestabilannya dipengaruhi oleh nilai eigen dan bilangan reproduksi dasar (R0). Jika R0 ˂ 1, maka penyakit chikungunya
akan menghilang dari populasi dan jika R0
Simulasi yang dilakukan yaitu melalui penyemprotan dan penggunaan obat anti nyamuk, dengan mengubah-ubah laju kematian nyamuk (µ
≥ 1, maka penyakit chikungunya akan
menetap di dalam populasi.
m
Dinamika populasi ketika bilangan reproduksi dasar kurang dari satu lebih cepat menuju kestabilan dibandingkan ketika bilangan reproduksi dasar lebih besar dari satu. Semakin kecil bilangan reproduksi dasar maka populasi semakin cepat menuju kestabilan.
manusia rentan yang menjadi terekspos dan selanjutnya terinfeksi semakin sedikit. Jika rata-rata gigitan nyamuk terinfeksi naik, maka jumlah subpopulasi manusia rentan semakin berkurang sedangkan subpopulasi lainnya semakin bertambah. Artinya, semakin besar rata-rata gigitan nyamuk terinfeksi maka jumlah manusia rentan yang menjadi terekspos dan selanjutnya terinfeksi semakin banyak.
Pada populasi nyamuk, jika laju kematian nyamuk naik, maka jumlah subpopulasi nyamuk rentan semakin bertambah sedangkan subpopulasi lainnya semakin berkurang. Artinya, semakin besar laju kematian nyamuk maka jumlah nyamuk rentan yang menjadi terekspos dan selanjutnya terinfeksi semakin sedikit. Jika rata-rata gigitan nyamuk terinfeksi naik, maka jumlah subpopulasi nyamuk rentan semakin berkurang sedangkan subpopulasi lainnya semakin bertambah. Artinya, semakin besar rata-rata gigitan nyamuk terinfeksi maka jumlah nyamuk rentan yang menjadi terekspos dan selanjutnya terinfeksi semakin banyak.
Kata kunci: Chikungunya, model SEIRS-LSEI, bilangan reproduksi, interaksi populasi manusia dengan populasi nyamuk.
Hak cipta milik Institut Pertanian Bogor, tahun 2012
Hak cipta dilindungi Undang-undang
1. Dilarang mengutip sebagian atau seluruh karya tulis ini tanpa mencantumkan atau menyebutkan sumber
a. Pengutipan hanya untuk kepentingan pendidikan, penelitian, penulisan karya ilmiah, penyusunan laporan, penulisan kritik atau tinjauan suatu masalah.
b. Pengutipan tidak merugikan kepentingan yang wajar Institut Pertanian Bogor.
SUAEDAH
Tesis
sebagai salah satu syarat untuk memperoleh gelar Magister Sains pada
Program Studi Matematika Terapan
SEKOLAH PASCASARJANA
INSTITUT PERTANIAN BOGOR
Program Studi : Matematika Terapan
Disetujui
Komisi Pembimbing
Dr. Toni Bakhtiar, M.Sc. Drs. Ali Kusnanto, M.Si.
Ketua Anggota
Diketahui
Ketua Program Stuti Dekan Sekolah Pascasarjana
Matematika Terapan
Dr. Ir. Endar H. Nugrahani, M.S. Dr. Ir. Dahrul Syah, M.Sc.Agr.
PRAKATA
Puji syukur kehadirat Allah SWT atas segala karunia-Nya sehingga karya ilmiah ini dapat dilaksanakan dan diselesaikan dengan baik.
Penelitian ini diberi judul Model SEIRS-LSEI pada Penyakit Chikungunya. Karya ilmiah ini tidak akan mungkin terselesaikan tanpa adanya dorongan, bantuan dan kritikan membangun dari berbagai pihak. Terimakasih penulis ucapkan kepada Dr. Toni Bakhtiar, M.Sc. dan Drs. Ali Kusnanto, M.Si. selaku pembimbing serta Dr. Ir. Hadi Sumarno, M.S. selaku penguji yang banyak memberikan saran.
Demikian pula, penulis mengucapkan terimakasih kepada Kementerian Agama Republik Indonesia yang telah memberikan beasiswa. Ungkapan terima kasih juga disampaikan kepada ibu, bapak, suami dan anakku, serta rekan-rekan seperjuangan di S2 angkatan 2009, Keluarga besar MTsN Kandanghaur, Indramayu serta berbagai pihak yang tak dapat penulis sebutkan satu per satu, penulis mengucapkan banyak terima kasih, dan semoga Allah SWT melimpahkan keberkahan serta kemanfaatan atas keberhasilan ini. Amien.
Penulis menyadari bahwa karya ilmiah ini masih jauh dari sempurna, walaupun demikian penulis tetap berharap semoga karya ilmiah ini dapat memberikan kontribusi pada bidang matematika dan bidang-bidang lainnya.
Penulis dilahirkan di Indramayu pada tanggal 07 Maret 1972 dari Bapak Sokhibi dan Ibu Daerih. Penulis merupakan anak keenam dari sembilan bersaudara.
Tahun 1991 penulis lulus dari SMAN Kandanghaur Indramayu. Pada Tahun 1997 penulis melanjutkan kuliah di Sekolah Tinggi Agama Islam Negeri Cirebon, mengambil program studi Matematika dan lulus pada tahun 2003. Tahun 2005 mendapat SK CPNS sebagai guru di Madrasah Tsanawiyah Negeri (MTsN) Kandanghaur, Indramayu.
DAFTAR ISI
2.1.1 Sistem Persamaan Diferensial Linear (SPDL) ... 3
2.1.2 Sistem Persamaan Diferensial Taklinear (SPDTL) ... 3
2.1.3 Sistem Persamaan Diferensial Mandiri ... 3
2.2 Titik Tetap ... 4
III MODEL PENYEBARAN PENYAKIT CHIKUNGUNYA ... 7
3.1 Model SEIRS……….. 7
3.2 Kerangka Analisis ... 12
IV HASIL DAN PEMBAHASAN……….………. 13
4.1 Penentuan Titik Tetap ... 13
4.2 Analisis Kestabilan Titik Tetap ... 15
4.2.1 Kestabilan Titik Tetap T1 4.2.2 Kestabilan Titik Tetap T ... 16
2 ... 17
V SIMULASI ... 21
5.1 Parameter Yang Ditetapkan ... 21
5.2 Simulasi Analisis Kestabilan ... 22
5.2.2.1 Populasi manusia……… 28
5.2.2.2 Populasi nyamuk……… 30
VI SIMPULAN DAN SARAN……… 34
DAFTAR GAMBAR
1 Model kompartemen penyakit chikungunya……… 8 2 Bagan kerangka analisis………... 12 3 Dinamika populasi manusia rentan terhadap waktu t untuk kondisi
R0
4 Dinamika populasi manusia terekspos terhadap waktu t untuk kondisi
˂ 1……….
22
R0
5 Dinamika populasi manusia terinfeksi terhadap waktu t untuk kondisi
˂ 1………...
23
R0
6 Dinamika populasi manusia sembuh terhadap waktu t untuk kondisi
˂ 1………...
24
R0
7 Dinamika populasi nyamuk berupa larva terhadap waktu t untuk kondisi
˂ 1………...
24
R0
8 Dinamika populasi nyamuk rentan terhadap waktu t untuk kondisi
˂ 1………...
25
R0
9 Dinamika populasi nyamuk terekspos terhadap waktu t untuk kondisi
˂ 1………...
26
R0
10 Dinamika populasi manusia terinfeksi terhadap waktu t untuk kondisi
˂ 1...………
26
R0
11 Dinamika populasi manusia rentan terhadap waktu t untuk kondisi
˂ 1………
27
R0
12 Dinamika populasi manusia terekspos terhadap waktu ˃ t untuk kondisi
1.………. 28
R0
13 Dinamika populasi manusia terinfeksi terhadap waktu t untuk kondisi
˃ 1.………..
29
R0
14 Dinamika populasi manusia sembuh terhadap waktu t untuk kondisi
˃ 1..……….
29
R0
15 Dinamika populasi nyamuk berupa larva terhadap waktu t untuk kondisi
˃ 1..……….
30
R0
16 Dinamika populasi nyamuk rentan terhadap waktu t untuk kondisi
˃ 1...……….
30
R0
17 Dinamika populasi manusia terekspos terhadap waktu t untuk kondisi
˃ 1..……….
R0˃ 1..……….
32
DAFTAR TABEL
DAFTAR LAMPIRAN
1 Menentukan titik tetap……… 37 2 Penentuan bilangan reproduksi dasar………... 38
3 Bukti Teorema 1………. 39 4 Membuat program simulasi untuk kondisi R0
5 Membuat program simulasi untuk kondisi R
˂ 1………. 48
0˃ 1....……….
1
I PENDAHULUAN
1.1 Latar Belakang
Chikungunya adalah penyakit yang disebabkan oleh virus chikungunya
yang disebarkan ke manusia melalui gigitan nyamuk Aedes aegypti dan nyamuk
Aedes albopictus (Pialouk et al., 2007). Nyamuk yang menggigit manusia
penderita chikungunya akan terinfeksi oleh virus chikungunya dan setelah sekitar
seminggu, nyamuk tersebut dapat menularkan virus pada manusia lain yang sehat.
Kondisi iklim dari satu tempat ke tempat lain bisa berubah cepat. Ini merupakan
fakta penting karena hidup nyamuk ini sangat terkait dengan suhu dan
kelembaban (Dumont et al., 2008). Pada musim hujan, tempat perkembangbiakan
Aedes aegypti yang pada musim kemarau tidak terisi, mulai terisi oleh air. Selain
itu pada musim hujan semakin banyak tempat-tempat penampungan air alamiah
yang terisi air hujan yang dapat digunakan sebagai tempat perkembangan nyamuk
ini. Karena itu, pada musim penghujan populasi nyamuk Aedes aegypti
meningkat, sehingga bertambahnya populasi nyamuk menyebabkan faktor
peningkatan penyakit chikungunya jika dalam daerah tersebut ada penderitanya.
Gejala chikungunya muncul antara 2 sampai 4 hari setelah gigitan dan
ditandai oleh demam tinggi, sakit kepala, dan arthritis pada beberapa sendi
(seperti pergelangan kaki dan pergelangan tangan). Manifestasi penyakit
berlangsung tiga sampai sepuluh hari. Virus ini bersifat self limiting disease, yaitu
hilang dengan sendirinya. Namun, rasa nyeri masih tertinggal dalam hitungan
minggu sampai bulan. Tidak ada vaksin maupun obat, penderita biasanya cukup
minum obat penurun panas dan penghilang rasa sakit. Yang penting penderita
cukup istirahat, minum, dan makan makanan bergizi (Pialouk et al., 2007).
Satu-satunya cara mencegah penularan penyakit ini adalah dengan memutus rantai
penularan dengan cara memberantas nyamuk tersebut, sebagaimana sering
disarankan dalam pemberantasan penyakit demam berdarah dengue, yaitu dengan
cara menguras tempat penampungan air bersih, bak mandi, vas bunga, dan
sebagainya (Chandra, 2006).
Dalam penelitian ini akan dibahas sebuah model matematika penyebaran
merupakan modifikasi dari Model SEIR. Modifikasi dilakukan dengan
menambahkan asumsi bahwa individu yang memunyai kekebalan tubuh setelah
terserang penyakit dapat menjadi rentan kembali walaupun peluangnya sangat kecil
(Labadie et al., 2010), sehingga model ini disebut model SEIRS
(Susceptible-Exposed-Infected-Resistant-Susceptible). Selanjutnya, dilakukan analisis kestabilan
dan simulasi numerik pada model-model tersebut. Perhitungan dalam analisis
kestabilan dan simulasi numerik dilakukan dengan pemrograman berbasis
fungsional
1.2 Tujuan Penelitian .
Penelitian ini bertujuan untuk:
1. Mengkonstruksi model penyebaran penyakit chikungunya pada
model SEIRS-LSEI,
2. Melakukan analisis kestabilan model penyebaran penyakit
Chikungunya,
3. Melakukan simulasi numerik untuk melihat seberapa besar pengaruh
parameter tertentu yaitu laju kematian nyamuk , dan rata-rata gigitan
3
II LANDASAN TEORI
2.1 Sistem Persamaan Diferensial
Definisi 1 (Sistem Persamaan Diferensial)
Sistem persamaan diferensial (SPD) adalah suatu persamaan yang
dinyatakan sebagai:
(1)
dengan
, dan
Jika taklinear terhadap sistem (1) disebut SPD taklinear dan jika
linear maka SPD (1) disebut linear.
(Braun, 1983)
Definisi 2 (Sistem Persamaan Diferensial Linear Orde Satu)
SPD linear dapat dinyatakan sebagai:
(2)
dengan adalah matriks koefisien konstan berukuran dan adalah vektor
konstan. Sistem tersebut dinamakan SPD linear orde satu dengan kondisi awal .
Jika , maka sistem dikatakan homogen dan jika , maka sistem
Definisi 3 (Sistem Persamaan Diferensial Mandiri)
Misalkan suatu sistem persamaan diferensial dinyatakan sebagai berikut:
(3)
dengan merupakan fungsi kontinu bernilai real dari dan memunyai turunan
parsial kontinu. Sistem (3) disebut sistem persamaan diferensial mandiri
(autonomous) karena tidak memuat t secara eksplisit didalamnya.
(Tu, 1994)
2.2 Titik Tetap
Definisi 4 (Titik Tetap)
Misalkan diberikan sistem persamaan diferensial mandiri (3). Titik
disebut titik tetap atau titik kritis atau titik kesetimbangan jika .
(Tu, 1994)
Definisi 5 (Titik Tetap Stabil)
Misalkan adalah titik tetap sebuah SPD dan x(t) adalah solusi yang memenuhi
kondisi awal x(0) = dengan . Titik dikatakan titik tetap stabil jika
untuk sembarang terdapat r sedemikian sehingga jika posisi awal
memenuhi maka solusi x(t) memenuhi , untuk
t .
(Verhulst, 1990)
Definisi 6 (Titik Tetap Takstabil)
Misalkan dan x(t) adalah sebuah solusi SPD
dengan nilai awal x(0) = dengan Titik dikatakan titik tetap
takstabil jika terdapat > 0 dan untuk sebarang r > 0 terdapat nilai awal yang
memenuhi sehingga solusi x(t) memenuhi , untuk
t > 0.
5
Untuk menganalisis kestabilan titik tetap dari suatu SPD taklinear dapat dilakukan
dengan pelinearan pada sistem persamaan diferensialnya.
2.3 Pelinearan
Analisis kestabilan sistem persamaan diferensial taklinear dapat dilakukan
melalui analisis sistem linear padanannya. Misalkan diberikan sistem persamaan
diferensial taklinear sebagai berikut:
. (4)
Dengan menggunakan ekspansi Taylor di sekitar titik tetap , maka sistem
persamaan (4) dapat ditulis:
(5)
dengan adalah matriks Jacobi, yaitu
A , (6)
dan adalah suku berorde tinggi yang bersifat . Selanjutnya,
pada persamaan (5) disebut pelinearan dari sistem persamaan diferensial
taklinear pada persamaan (4) dan ditulis dalam bentuk (Tu, 1994).
2.4 Nilai Eigen dan Vektor Eigen
Diberikan matriks koefisien konstan berukuran n × n, dan SPD homogen
berikut:
, (7)
Suatu vektor taknol xdalam ruang disebut vektor eigen dari jika untuk suatu
skalar λ berlaku:
Nilai skalar λ dinamakan nilai eigen dari . Untuk mencari nilai λ dari matriks ,
maka persamaan (8) dapat ditulis kembali sebagai berikut:
(9)
dengan I matriks identitas. Persamaan (9) memunyai solusi taknol jika dan hanya
jika
Persamaan (10) disebut persamaan karakteristik dari matriks .
(Anton, 1997)
Analisis Kestabilan Titik Tetap
Kestabilan titik tetap dari sistem ditentukan berdasarkan tanda nilai
eigen matriks A sebagai berikut:
1. Sistem adalah stabil jika dan hanya jika setiap nilai eigen adalah
bernilai negatif.
2. Sistem adalah takstabil jika dan hanya jika minimal satu nilai eigen
dari bernilai taknegatif.
(Borrelli dan Coleman 1998)
2.5 Bilangan Reproduksi Dasar
Bilangan reproduksi dasar, dinotasikan dengan R
Kondisi yang akan timbul adalah:
0 ialah nilai harapan
terjadinya infeksi per satuan waktu. Infeksi ini terjadi pada suatu populasi yang
seluruhnya rentan yang dihasilkan oleh satu jenis individu yang sudah terinfeksi.
1 Jika R0 1, penyakit chikungunya akan hilang dari populasi.
2 Jika R0 1, penyakit chikungunya akan menetap di dalam populasi.
R0 dalam penelitian ini ditentukan dengan menggunakan metode yang
dikenalkan oleh Watmough (2008) dan van den Driessche dan Watmough (2005)
7
yang menyebabkan infeksi saja. Matriks tersebut dinamakan dengan the next
generation matrix. Nilai eigen taknegatif dengan modulus terbesar matriks ini
yang nantinya digunakan sebagai nilai R0.
III MODEL PENYEBARAN PENYAKIT CHIKUNGUNYA
3.1 Model SEIRS-LSEI
Model SEIR (Susceptible-Eexposed-Infected-Resistant) pada penyakit
chikungunya dikenalkan oleh Dumont et al., (2008) dengan mengklasifikasikan
total populasi manusia sebagai host ke dalam empat kelas, yaitu manusia yang
rentan (susceptible) , manusia yang terekspos (exposed) , manusia yang
terinfeksi (infected) , dan manusia yang sembuh (resistant) . Manusia yang
rentan adalah manusia yang tidak terkena infeksi dan bukan imun. Manusia yang
terekspos adalah manusia yang telah diinfeksi oleh virus ketika masa inkubasi
intrinsik dalam tubuh manusia sedang berlangsung. Manusia yang terinfeksi
adalah manusia yang tertular virus chikungunya dan dapat menularkan virus
tersebut kepada individu lain dengan perantara nyamuk. Manusia sembuh adalah
manusia yang telah sembuh dari penyakit chikungunya. Dapat juga ditulis:
Sedangkan total populasi nyamuk sebagai vektor dibagi menjadi
empat kelas, yaitu larva (larvae) , nyamuk yang rentan (susceptible) ,
nyamuk yang terekspos (exposed) , dan nyamuk yang terinfeksi (infected) .
Larva adalah jentik-jentik nyamuk atau anak nyamuk yang baru lahir. Nyamuk
yang rentan adalah nyamuk yang belum tertular virus. Nyamuk yang terekspos
adalah nyamuk yang diinfeksi oleh virus ketika masa inkubasi ekstrinsik dalam
tubuh nyamuk sedang berlangsung. Sedangkan nyamuk yang terinfeksi adalah
nyamuk yang tertular virus dan dapat menularkan virus tersebut kepada individu
lain. Dapat juga ditulis:
9
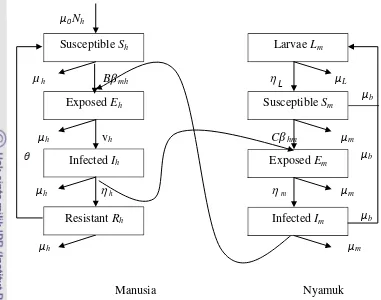
Gambar 1 Model kompartemen penyakit chikungunya. Manusia Nyamuk
Model SEIR ini selanjutnya dimodifikasi dengan menambahkan asumsi
bahwa individu yang mempunyai kekebalan tubuh setelah terserang penyakit
menjadi rentan kembali walaupun peluangnya sangat kecil (Labadie et al., 2010),
sehingga model ini disebut model SEIRS
(Susceptible-Exposed-Infected-Resistant-Susceptible).
Secara skematis, pola penyebaran penyakit chikungunya dapat
digambarkan dalam bentuk bagan seperti yang diperlihatkan pada Gambar 1.
Model SEIRS pada Gambar 1 menjelaskan laju perpindahan individu antara
kelas S, E, I, R dan S. Diasumsikan bahwa laju kelahiran (µ0) dan laju kematian
(µh) di setiap kelas adalah sama, yaitu µ0 = µh. Model penyebaran virus
chikungunya sebelumnya menggunakan asumsi semua telur nyamuk sehat. Individu
lahir di kelas rentan (Sh) dengan laju kelahiran sebesar µ0. Manusia yang berada di
kelas rentan akan mati dengan laju kematian sebesar µh, atau masuk ke kelas
terekspos (Eh) karena terjangkit penyakit dengan laju penularan sebesar βmh Jadi
βmh merupakan tingkat interaksi antara nyamuk yang terinfeksi dengan manusia yang rentan sehingga menjadi manusia yang terekspos artinya tidak ada kontak
langsung dari kelas rentan (Sh) ke kelas terekspos (Eh). Selanjutnya manusia yang
berada di kelas terekspos akan mati dengan laju kematian sebesar µh, atau masuk ke
kelas terinfeksi (Ih) dengan laju perubahan sebesar νh. Selanjutnya manusia yang
berada di kelas terinfeksi akan mati dengan laju kematian sebesar µh, atau sembuh
dengan laju penyembuhan sebesar ηh sehingga dimasukkan ke kelas sembuh (Rh).
Kemudian manusia di kelas sembuh akan mati dengan laju kematian sebesar µh
Dari penjelasan di atas dapat dituliskan dalam bentuk persamaan-persamaan
berikut:
,
atau menjadi rentan kembali karena sistem kekebalan tubuh dapat hilang sehingga
kembali masuk ke kelas rentan dengan laju hilangnya kekebalan sebesar θ.
Persamaan untuk populasi manusia
B adalah rata-rata gigitan nyamuk terinfeksi pada manusia terekspos (per hari),
adalah peluang transmisi dari nyamuk yang terinfeksi ke manusia (per gigitan),
adalah laju kematian manusia secara alami (per hari),
adalah rata-rata rentang hidup manusia,
11
tersebut akan tertular (per hari),
adalah periode inkubasi intrinsik (proses masuknya virus dalam tubuh manusia) per hari,
adalah laju hilangnya kekebalan tubuh,
adalah merupakan laju terjadinya interaksi antara nyamuk yang terinfeksi dengan manusia rentan,
adalah laju kelahiran manusia secara alami (per hari), dengan µ0 = µh
Model LSEI pada Gambar 1 menjelaskan laju perpindahan nyamuk antara
kelas L, S, E, dan I. Nyamuk berupa larva ( mati dengan laju kematian
sebesar atau tumbuh menjadi nyamuk dewasa dengan laju sebesar Nyamuk
dewasa di kelas SEI di asumsikan dapat menghasilkan larva dengan laju atau
mati dengan laju , atau terjangkit penyakit dengan laju penularan sebesar
Jadi merupakan tingkat interaksi antara manusia yang terinfeksi dengan
nyamuk yang rentan, artinya nyamuk yang rentan menjadi terekspos karena
pengaruh gigitan dari manusia yang terinfeksi dalam arti tidak ada kontak langsung
antara kelas nyamuk yang rentan ( ) dan kelas terekspos ( ). Nyamuk yang baru
lahir digolongkan ke kelas terekspos ( ) dengan laju kelahiran sebesar ,
selanjutnya laju perubahan dari nyamuk yang terekspos menjadi terinfeksi
sebesar . Nyamuk di kelas terinfeksi ( ) akan mati dengan laju kematian
sebesar . Keadaan populasi nyamuk mengalami perubahan karena asumsi
sebagian telur nyamuk terinfeksi. Jumlah nyamuk yang rentan ( ) akan meningkat
karena bertambahnya kelahiran nyamuk sehat dan akan berkurang karena gigitan
nyamuk kepada populasi manusia terinfeksi serta karena kematian alami. Populasi
nyamuk yang terkena infeksi ( ) akan meningkat karena kelahiran nyamuk
terinfeksi, gigitan nyamuk kepada populasi manusia terinfeksi dan berkurang
karena kematian alami. Perubahan musim membuat perubahan suhu, sehingga pola
musiman mempengaruhi di dalam penyebaran penyakit chikungunya. Variasi di
dalam masa inkubasi ekstrinsik disebabkan oleh perubaha-perubahan suhu, semakin
rendah suhu masa inkubasi semakin lama.
.
Garis yang menghubungkan model SEIRS dan LSEI pada gambar
yang terinfeksi dengan manusia yang terekspos adalah awal penyebaran penyakit
chikungunya dari dunia nyamuk ke dunia manusia.
Dari penjelasan di atas dapat dituliskan dalam bentuk persamaan-persamaan
berikut:
Persamaan untuk populasi nyamuk
dengan kondisi dan + =
di mana
Nm
C adalah rata-rata gigitan individu nyamuk pada manusia (per hari), adalah total populasi nyamuk (ekor),
adalah peluang transmisi dari manusia yang terinfeksi ke nyamuk (per gigitan),
adalah laju kelahiran nyamuk secara alami (per hari), adalah laju kematian tahap larva (per hari),
adalah rata-rata rentang hidup nyamuk dewasa,
adalah laju kematian alami larva (per hari),
adalah tingkat transisi (pematangan) dari larva menjadi dewasa (per hari),
adalah masa inkubasi ekstrinsik (proses masuknya virus ketubuh nyamuk)
per hari,
adalah kapasitas maksimal larva yang hidup,
13
Jika faktor lingkungan (musim) dipertimbangkan maka dapat dilakukan
penyesuaian terhadap total populasi nyamuk dan laju kelahiran nyamuk. Misalnya
dengan menjadikan kedua parameter tersebut sebagai fungsi dari waktu, yaitu
dan Nilai parameter-parameter yang lain pun dapat
disesuaikan dengan lokasi di mana model akan diterapkan.
Model ini menggunakan beberapa asumsi sebagai berikut:
1 Total populasi adalah konstan,
2 manusia dan nyamuk diasumsikan lahir rentan,
3 nyamuk tidak pernah sembuh setelah terinfeksi virus,
4 larva diasumsikan sehat.
Selanjutnya dilakukan analisis kestabilan model penularan penyakit
chikungunya yang menghasilkan beberapa titik tetap. Analisis titik tetap tersebut
nantinya akan dihasilkan syarat kestabilan untuk masing-masing titik tetap.
3.2 Kerangka Analisis
Adapun kerangka analisis yang akan dikaji dan diterapkan pada model
adalah sebagai berikut:
1 Menentukan titik tetap dari persamaan (1)–(8),
2 melakukan pelinearan di sekitar titik tetap terhadap model taklinear (1)-(8),
3 menentukan nilai eigen,
4 menentukan bilangan reproduksi dasar (R0
5 menganalisis kestabilan dengan simulasi. ),
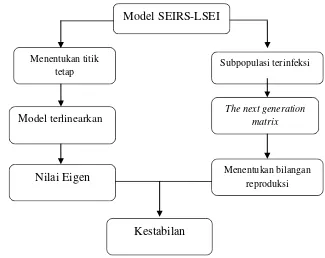
Secara skematis, kerangka analisis dapat digambarkan dalam bentuk bagan
Gambar 2 Bagan kerangka analisis. Model SEIRS-LSEI
Menentukan titik
tetap Subpopulasi terinfeksi
The next generation matrix
Menentukan bilangan reproduksi
Model terlinearkan
Nilai Eigen
15
IV HASIL DAN PEMBAHASAN
4.1 Penentuan Titik TetapDalam menentukan suatu solusi yang tidak berubah menurut waktu sering
digunakan analisis titik tetap pada sistem persamaan diferensial. Untuk sistem
persamaan (1)–(8), titik tetap diperoleh pada saat , , ,
, , , , dan sehingga sistem persamaan
tersebut dapat ditulis sebagai berikut:
= 0
Sistem persamaan (4.1) di atas memiliki empat titik tetap, yaitu:
4 Titik tetap T4
( , , , , , , , ) dengan,
17
Penentuan titik tetap ini dapat dilihat pada Lampiran 1.
4.2. Analisis Kestabilan Titik Tetap
Misalkan dari model (4.1) didefinisikan fungsi-fungsi sebagai berikut:
�5[�ℎ,
�
ℎ,�ℎ,�ℎ,��,��,��,��] =���1−����(�� +�� +��)− ���� −����
(4.3)
Dengan menggunakan (6) terhadap (4.3) diperoleh matriks Jacobi sebagai
berikut:
(4.4)
Penentuan matriks Jacobi ini dapat dilihat pada Lampiran 2.
4.2.1 Kestabilan titik tetap T1
Untuk menentukan kestabilan titik tetap T
1 ( , 0, 0, 0, 0, 0, 0, 0) yaitu
dengan melakukan pelinearan pada (4.1) di atas. Titik T1
(4.5) ( , 0, 0, 0, 0, 0, 0)
disubstitusi ke matriks Jacobi (4.4), sehingga diperoleh:
Dengan menyelesaikan persamaan karakteristik diperoleh
19
– .
Karena semua parameter yang terlibat bernilai positif, maka ,
, , , , dan . Untuk akan bernilai negatif
jika . Untuk akan
bernilai negatif jika maka
jadi titik tetap T1 stabil. Tetapi untuk akan
bernilai positif jika , maka
jadi titik tetap T1 sadel. Jadi T1 dapat dikatakan
stabil dan juga T1 dapat dikatan sadel.
4.2.2 Kestabilan titik tetap T
Kestabilan titik tetap tanpa penyakit ini diberikan oleh teorema berikut.
2
Teorema 1. Jika , maka (Nh, 0, 0, 0, Lm0, Sm0, 0, 0) adalah
titik tetap bebas penyakit sistem (1) (2), yang stabil asimtotik lokal jika
R0 < 1 dan tidak stabil asimtotik lokal jika R0
Bukti :
> 1.
Dari persamaan (4.1) titik tetap diperoleh pada pada saat , ,
, , , , , dan dengan:
,
,
Dengan pemrograman berbasis fungsional diperoleh titik tetap = ( , 0,
0, 0, , . Menyimpulkan bahwa
atau , Kemudian dan ini
bahwa dan Karena , maka
akibatnya adalah equilibrium bebas penyakit. (lihat lampiran 3)
Dengan mengambil sistem persamaan (4.1) dan menyusunnya kembali
dalam urutan subpopuasi-subpopulasi yang menyebabkan infeksi saja, yaitu ,
, , dan
diperoleh sistem persamaan sebagai berikut :
21
Dari sistem di atas, diperoleh matriks-matriks
Φ = , ς =
sehingga,
F = , V = .
Selanjutnya, dihitung matriks K = FV-1 sebagai berikut:
K =
.
Berdasarkan Van den Driessche dan Watmough 2005, bilangan reproduksi
dasar R0
) = R
merupakan nilai eigen dengan modulus terbesar matriks K, ditulis:
0
Selanjutnya diperoleh : 0
R0
Terlihat bahwa R
= .
0 dipengaruhi oleh banyak parameter. Sebagai contoh jika
rata-rata gigitan nyamuk (B) diperbesar, maka R0 akan membesar. Artinya,
peluang penyakit akan menetap di dalam populasi juga semakin besar. Untuk
meperkecil R0
Berikut adalah tabel kondisi kestabilan dari kedua titik tetap yang diperoleh. , maka laju kematian nyamuk diperbesar. Akibatnya, penyakit
akan menghilang dari populasi.
Tabel 1 Kondisi kestabilan titik tetap
Kondisi T1 T2
dan Sadel Stabil
dan Sadel Tidak Stabil
Dari Tabel 1 dapat dilihat bahwa kondisi kestabilan dari titik tetap yang diperoleh
saling bertentangan. Ketika titik tetap pertama stabil, titik tetap yang kedua tidak
stabil dan ketika titik tetap yang pertama sadel, titik tetap dua stabil.
Titik tetap T3 dan titik tetap T4 akan di cari dengan melakukan simulasi.
Hal ini dilakukan karena kedua titik tetap tersebut sulit ditentukan secara analitik.
23
5.1 Parameter yang Ditetapkan
Misalkan dalam suatu pengamatan diperoleh parameter-parameter seperti
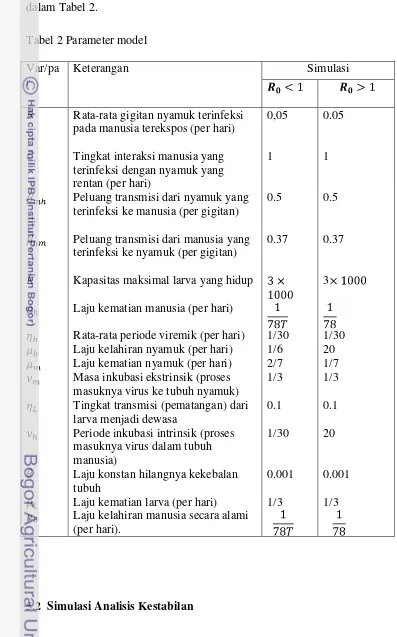
dalam Tabel 2.
Tabel 2 Parameter model
Var/pa r
Keterangan Simulasi
B Rata-rata gigitan nyamuk terinfeksi pada manusia terekspos (per hari)
0,05 0.05
C Tingkat interaksi manusia yang terinfeksi dengan nyamuk yang rentan (per hari)
1 1
Peluang transmisi dari nyamuk yang terinfeksi ke manusia (per gigitan)
0.5 0.5
Peluang transmisi dari manusia yang terinfeksi ke nyamuk (per gigitan)
0.37 0.37
K Kapasitas maksimal larva yang hidup
Masa inkubasi ekstrinsik (proses
masuknya virus ke tubuh nyamuk)
1/3 1/3
Tingkat transmisi (pematangan) dari larva menjadi dewasa
0.1 0.1
Periode inkubasi intrinsik (proses masuknya virus dalam tubuh manusia)
1/30 20
θ Laju konstan hilangnya kekebalan tubuh
0.001 0.001
Laju kematian larva (per hari) Laju kelahiran manusia secara alami (per hari).
1/3 1/3
5.2.1 Populasi untuk Kondisi
5.2.1.1 Populasi Manusia
Kondisi adalah kondisi di mana populasi akan stabil menuju
musnahnya virus dari populasi.
Berdasarkan nilai-nilai parameter yang ada pada Tabel 2 dan dengan mengambil nilai dan B yang sudah ditetapkan, diperoleh gambar dinamika
populasi di bawah ini untuk nilai dan B dengan nilai .
Nilai awal total populasi manusia yang seluruhnya rentan adalah 1000.
Nilai awal total populasi nyamuk yang berupa larva adalah 3000 dengan jumlah
nyamuk yang terinfeksi 20%.
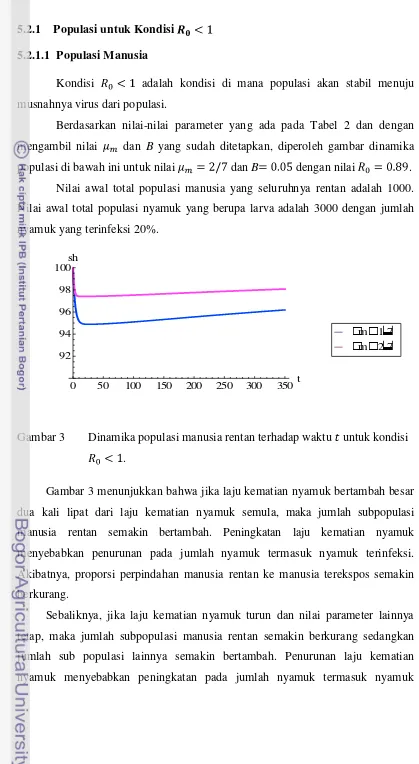
Gambar 3 Dinamika populasi manusia rentan terhadap waktu untuk kondisi
.
Gambar 3 menunjukkan bahwa jika laju kematian nyamuk bertambah besar
dua kali lipat dari laju kematian nyamuk semula, maka jumlah subpopulasi
manusia rentan semakin bertambah. Peningkatan laju kematian nyamuk
menyebabkan penurunan pada jumlah nyamuk termasuk nyamuk terinfeksi.
Akibatnya, proporsi perpindahan manusia rentan ke manusia terekspos semakin
berkurang.
Sebaliknya, jika laju kematian nyamuk turun dan nilai parameter lainnya
tetap, maka jumlah subpopulasi manusia rentan semakin berkurang sedangkan
jumlah sub populasi lainnya semakin bertambah. Penurunan laju kematian
nyamuk menyebabkan peningkatan pada jumlah nyamuk termasuk nyamuk
25
terinfeksi. Akibatnya, proporsi perpindahan manusia rentan ke manusia terekspos
semakin bertambah. Gambar 3 menunjukkan bahwa pada subpopulasi manusia
rentan ( ), di awal simulasi mengalami penurunan kemudian meningkat hingga
stabil ke .
Gambar 4 Dinamika populasi manusia terekspos terhadap waktu untuk
kondisi .
Gambar 4 menunjukkan bahwa jika laju kematian nyamuk bertambah besar
dua kali lipat dari laju kematian nyamuk semula, maka jumlah subpopulasi
manusia terekspos mengalami penurunan karena virus tidak dapat bertahan dalam
populasi. Peningkatan laju kematian nyamuk menyebabkan penurunan pada jumlah
nyamuk termasuk nyamuk terinfeksi. Akibatnya, proporsi perpindahan manusia
rentan ke manusia terekpos semakin berkurang.
Sebaliknya, jika laju kematian nyamuk turun dan nilai parameter lainnya
tetap, maka jumlah subpopulasi manusia terekspos semakin bertambah.
Penurunan laju kematian nyamuk menyebabkan peningkatan pada jumlah nyamuk
termasuk nyamuk terinfeksi. Akibatnya, proporsi perpindahan manusia rentan ke
manusia terekspos semakin berkurang. Pada subpopulasi manusia terekspos ( ),
awalnya mengalami peningkatan kemudian menurun hingga stabil ke
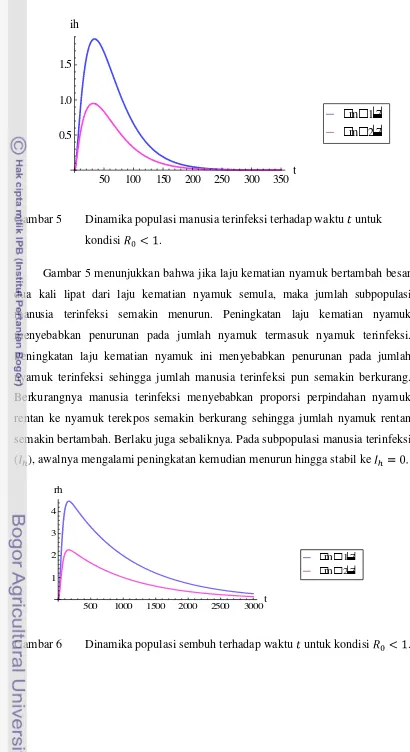
Gambar 5 Dinamika populasi manusia terinfeksi terhadap waktu untuk
kondisi .
Gambar 5 menunjukkan bahwa jika laju kematian nyamuk bertambah besar
dua kali lipat dari laju kematian nyamuk semula, maka jumlah subpopulasi
manusia terinfeksi semakin menurun. Peningkatan laju kematian nyamuk
menyebabkan penurunan pada jumlah nyamuk termasuk nyamuk terinfeksi.
Peningkatan laju kematian nyamuk ini menyebabkan penurunan pada jumlah
nyamuk terinfeksi sehingga jumlah manusia terinfeksi pun semakin berkurang.
Berkurangnya manusia terinfeksi menyebabkan proporsi perpindahan nyamuk
rentan ke nyamuk terekpos semakin berkurang sehingga jumlah nyamuk rentan
semakin bertambah.Berlaku juga sebaliknya. Pada subpopulasi manusia terinfeksi
( ), awalnya mengalami peningkatan kemudian menurun hingga stabil ke
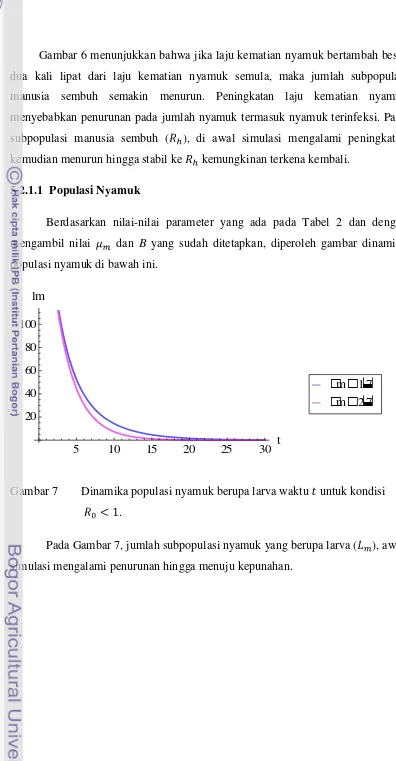
Gambar 6 Dinamika populasi sembuh terhadap waktu untuk kondisi . 50 100 150 200 250 300 350 t
27
Gambar 6 menunjukkan bahwa jika laju kematian nyamuk bertambah besar
dua kali lipat dari laju kematian nyamuk semula, maka jumlah subpopulasi
manusia sembuh semakin menurun. Peningkatan laju kematian nyamuk
menyebabkan penurunan pada jumlah nyamuk termasuk nyamuk terinfeksi. Pada
subpopulasi manusia sembuh ( ), di awal simulasi mengalami peningkatan
kemudian menurun hingga stabil ke kemungkinan terkena kembali.
5.2.1.1 Populasi Nyamuk
Berdasarkan nilai-nilai parameter yang ada pada Tabel 2 dan dengan
mengambil nilai dan B yang sudah ditetapkan, diperoleh gambar dinamika
populasi nyamuk di bawah ini.
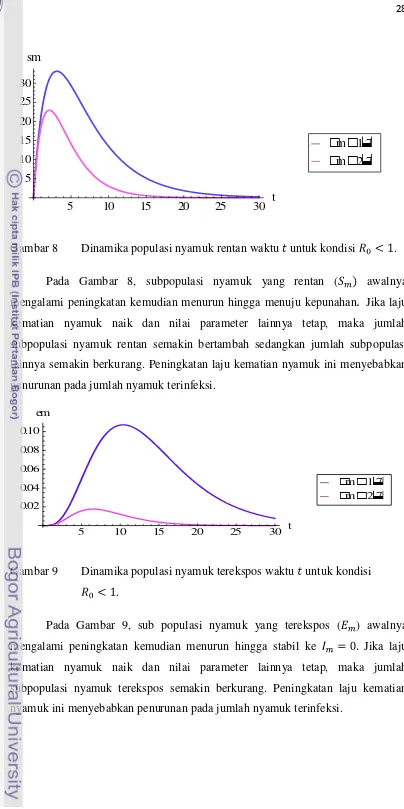
Gambar 7 Dinamika populasi nyamuk berupa larva waktu untuk kondisi
.
Pada Gambar 7, jumlah subpopulasi nyamuk yang berupa larva ( ), awal
simulasi mengalami penurunan hingga menuju kepunahan.
Gambar 8 Dinamika populasi nyamuk rentan waktu untuk kondisi .
Pada Gambar 8, subpopulasi nyamuk yang rentan ( awalnya
mengalami peningkatan kemudian menurun hingga menuju kepunahan Jika laju
kematian nyamuk naik dan nilai parameter lainnya tetap, maka jumlah
subpopulasi nyamuk rentan semakin bertambah sedangkan jumlah subpopulasi
lainnya semakin berkurang. Peningkatan laju kematian nyamuk ini menyebabkan
penurunan pada jumlah nyamuk terinfeksi.
Gambar 9 Dinamika populasi nyamuk terekspos waktu untuk kondisi
.
Pada Gambar 9, sub populasi nyamuk yang terekspos ( ) awalnya
mengalami peningkatan kemudian menurun hingga stabil ke Jika laju
kematian nyamuk naik dan nilai parameter lainnya tetap, maka jumlah
subpopulasi nyamuk terekspos semakin berkurang. Peningkatan laju kematian
nyamuk ini menyebabkan penurunan pada jumlah nyamuk terinfeksi.
29
Gambar 10 Dinamika populasi nyamuk terinfeksi waktu untuk kondisi
.
Pada Gambar 10, subpopulasi nyamuk yang terinfeksi ( ), dari awal
simulasi mengalami penurunan hingga stabil ke . Jika laju kematian
nyamuk naik dan nilai parameter lainnya tetap, maka jumlah subpopulasi nyamuk
terinfeksi semakin berkurang. Peningkatan laju kematian nyamuk ini
menyebabkan penurunan pada jumlah nyamuk terinfeksi sehingga jumlah
manusia terinfeksi pun semakin berkurang.
Dengan demikian, dapat dikatakan bahwa jumlah tiap subpopulasi stabil ke
titik tetap tanpa penyakit
Ini menunjuk-kan bahwa sub-sub populasi manusia terekpos dan terinfeksi serta
nyamuk terekpos dan terinfeksi menuju nol.
Dari gambar 3-6 dapat disimpulkan bahwa jika laju kematian nyamuk
bertambah besar dua kali lipat dari laju kematian nyamuk semula, maka jumlah
sub populasi manusia rentan semakin bertambah sedangkan jumlah subpopulasi
lainnya semakin berkurang. Peningkatan laju kematian nyamuk menyebabkan
penurunan pada jumlah nyamuk termasuk nyamuk terinfeksi. Akibatnya, proporsi
perpindahan manusia rentan ke manusia terekpos semakin berkurang.
Pada populasi nyamuk sebagaimana ditunjukkan oleh Gambar 7-10 jika
laju kematian nyamuk naik dan nilai parameter lainnya tetap, maka jumlah
subpopulasi nyamuk rentan semakin bertambah sedangkan jumlah subpopulasi
lainnya semakin berkurang. Peningkatan laju kematian nyamuk ini menyebabkan
penurunan pada jumlah nyamuk terinfeksi sehingga jumlah manusia terinfeksi pun
semakin berkurang.
5.2.2 Populasi untuk Kondisi
5.2.2.1 Populasi Manusia
Kondisi akan dianalisis untuk satu kondisi yaitu .
Berdasarkan nilai-nilai parameter yang ada pada Tabel 2 dan dengan mengambil
nilai-nilai parameter dan B pada interval yang sudah ditetapkan, diperoleh
gambar dinamika populasi di bawah ini untuk nilai dan B .
Nilai awal total populasi manusia yang seluruhnya rentan adalah 1000. Nilai
awal total populasi nyamuk yang berupa larva adalah 3000 dengan jumlah
nyamuk yang terinfeksi 20%.
Gambar 11 Dinamika populasi manusia rentan terhadap waktu untuk kondisi .
Gambar 11 menunjukkan bahwa jumlah subpopulasi manusia rentan ( )
setelah tertular virus, dari awal simulasi mengalami penurunan hingga stabil ke .
Jika rata-rata gigitan nyamuk bertambah besar dari rata-rata gigitan nyamuk
semula, maka jumlah subpopulasi manusia rentan semakin berkurang sedangkan
jumlah sub populasi lainnya semakin bertambah. Peningkatan rata-rata gigitan
nyamuk terinfeksi dapat meningkatkan nilai peluang kontak antara nyamuk
terinfeksi dengan manusia rentan. Akibatnya, proporsi perpindahan manusia
rentan ke manusia terekspos semakin bertambah.
31
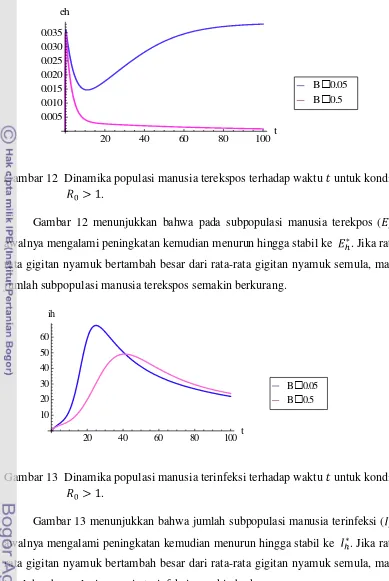
Gambar 12 Dinamika populasi manusia terekspos terhadap waktu untuk kondisi .
Gambar 12 menunjukkan bahwa pada subpopulasi manusia terekpos ( ),
awalnya mengalami peningkatan kemudian menurun hingga stabil ke . Jika
rata-rata gigitan nyamuk bertambah besar dari rata-rata-rata-rata gigitan nyamuk semula,maka
jumlah subpopulasi manusia terekspos semakin berkurang.
Gambar 13 Dinamika populasi manusia terinfeksi terhadap waktu untuk kondisi .
Gambar 13 menunjukkan bahwa jumlah subpopulasi manusia terinfeksi ( ),
awalnya mengalami peningkatan kemudian menurun hingga stabil ke . Jika
rata-rata gigitan nyamuk bertambah besar dari rata-rata-rata-rata gigitan nyamuk semula,maka
jumlah subpopulasi manusia terinfeksi semakin berkurang.
Gambar 14 Dinamika populasi manusia sembuh terhadap waktu untuk kondisi .
Gambar 14 menunjukkan bahwa jumlah subpopulasi manusia sembuh ( ),
di awal simulasi mengalami peningkatan kemudian menurun hingga stabil ke
. Jika rata-rata gigitan nyamuk bertambah besar
dari rata-rata gigitan nyamuk semula, maka jumlah subpopulasi manusia sembuh
semakin berkurang.
5.2.2.2 Populasi Nyamuk
Berdasarkan nilai-nilai parameter yang ada pada Tabel 2 dan dengan
mengambil nilai dan B yang sudah ditetapkan, diperoleh gambar dinamika
populasi nyamuk di bawah ini.
Gambar 15 Dinamika populasi nyamuk yang berupa larva terhadap waktu untuk kondisi .
Pada Gambar 15, jumlah subpopulasi nyamuk yang berupa larva, awalnya
33
Gambar 16 Dinamika populasi nyamuk yang rentan terhadap waktu untuk kondisi .
Pada Gambar 16, Pada subpopulasi nyamuk rentan ( ), mengalami
peningkatan hingga stabil ke . Jika rata-rata gigitan
nyamuk terinfeksi naik dan nilai parameter lainnya tetap, maka jumlah
subpopulasi nyamuk rentan semakin berkurang sedangkan jumlah subpopulasi
lainnya semakin bertambah. Hal ini disebabkan karena meningkatnya nilai
peluang kontak antara nyamuk rentan dengan manusia terinfeksi, sehingga
proporsi perpindahan nyamuk rentan ke nyamuk terekspos semakin bertambah.
Gambar 17 Dinamika populasi nyamuk yang terekspos terhadap waktu untuk kondisi .
Pada Gambar 17, jumlah subpopulasi nyamuk terekspos ( ), awalnya
mengalami peningkatan kemudian menurun hingga stabil ke . Jika rata-rata
gigitan nyamuk terinfeksi naik dan nilai parameter lainnya tetap, maka jumlah
subpopulasi nyamuk terekspos semakin bertambah. Hal ini disebabkan karena
meningkatnya nilai peluang kontak antara nyamuk rentan dengan manusia
terinfeksi, sehingga proporsi perpindahan nyamuk rentan ke nyamuk terekspos
semakin bertambah.
Gambar 18 Dinamika populasi nyamuk yang terinfeksi terhadap waktu untuk kondisi .
Pada Gambar 18, Jumlah subpopulasi nyamuk terinfeksi ( ), dari awal
simulasi mengalami penurunan hingga stabil ke .
Jadi, dapat dikatakan bahwa jumlah tiap subpopulasi stabil ke titik tetap
endemik , , , , , , , .
Dari Gambar 11-14 di atas dapat disimpulkan bahwa jika rata-rata gigitan
nyamuk bertambah besar dari rata-rata gigitan nyamuk semula, maka jumlah sub
populasi manusia rentan semakin berkurang sedangkan jumlah subpopulasi
lainnya semakin bertambah. Peningkatan rata-rata gigitan nyamuk terinfeksi dapat
meningkatkan nilai peluang kontak antara nyamuk terinfeksi dengan manusia
rentan. Akibatnya, proporsi perpindahan manusia rentan ke manusia terekspos
semakin bertambah.
Ini menunjukkan bahwa sub-sub
populasi manusia terekspos dan terinfeksi serta nyamuk terekspos dan terinfeksi
menuju ke nilai yang tidak nol.
Sedangkan pada populasi nyamuk, jika rata-rata gigitan nyamuk terinfeksi
naik dan nilai parameter lainnya tetap, maka jumlah subpopulasi nyamuk rentan
semakin berkurang sedangkan jumlah subpopulasi lainnya semakin bertambah.
Hal ini disebabkan karena meningkatnya nilai peluang kontak antara nyamuk
35
rentan dengan manusia terinfeksi, sehingga proporsi perpindahan nyamuk rentan
VI KESIMPULAN DAN SARAN
6.1 KesimpulanDalam tulisan ini telah diberikan model SEIRS-LSEI pada penyakit
chikungunya. Dari model tersebut dihasilkan empat titik tetap, yaitu dua titik tetap
tanpa penyakit dan dua titik tetap endemik. Secara umum model yang dihasilkan
dapat menunjukkan adanya endemi di suatu daerah untuk nilai parameter tertentu.
Secara simulasi numerik dari grafik bidang solusi dapat dilihat, bahwa:
a. Jika laju kematian nyamuk naik, maka jumlah subpopulasi manusia rentan
semakin bertambah sedangkan subpopulasi lainnya semakin berkurang.
Artinya, semakin besar laju kematian nyamuk maka jumlah manusia rentan
yang menjadi terekspos dan selanjutnya terinfeksi semakin sedikit.
b. Jika rata-rata gigitan nyamuk terinfeksi naik, maka jumlah subpopulasi
manusia rentan semakin berkurang sedangkan subpopulasi lainnya semakin
bertambah. Artinya, semakin besar rata-rata gigitan nyamuk terinfeksi maka
jumlah manusia rentan yang menjadi terekspos dan selanjutnya terinfeksi
semakin banyak.
c. Jika laju kematian nyamuk naik, maka jumlah subpopulasi nyamuk rentan
semakin bertambah sedangkan subpopulasi lainnya semakin berkurang.
Artinya, semakin besar laju kematian nyamuk maka jumlah nyamuk rentan
yang menjadi terekspos dan selanjutnya terinfeksi semakin sedikit.
d. Jika rata-rata gigitan nyamuk terinfeksi naik, maka jumlah subpopulasi
nyamuk rentan semakin berkurang sedangkan subpopulasi lainnya semakin
bertambah. Artinya, semakin besar rata-rata gigitan nyamuk terinfeksi maka
jumlah nyamuk rentan yang menjadi terekspos dan selanjutnya terinfeksi
37
6.2 Saran
Dalam upaya penanggulangan wabah penyakit chikungunya, disarankan
untuk meningkatkan laju kematian nyamuk ( ) dan menurunkan rata-rata gigitan
nyamuk terinfeksi (B). Peningkatan laju kematian nyamuk dapat dilakukan antara
lain dengan cara pemberantasan sarang nyamuk melalui penyemprotan dan
pemakaian obat anti nyamuk. Untuk menurunkan rata-rata gigitan nyamuk
terinfeksi dapat dilakukan dengan menggunakan lotion dan memasang kelambu
38
DAFTAR PUSTAKA
Anderson, May R. M. (1991), Infectiaus Diseases of Humans: Dynamics and
Control, Oxford University Press, Oxpord.
Anton Howard. 1997. Aljabar Linear Elementer. Jakarta: Penerbit Erlangga.
Braun, M. 1983. Differential Equations and Their Applications. New York :
Springer-Verlag
Borelli RL, Coleman CS. 1998. Differential Equations. USA: John Wiley and Sons, INC.
Chandra B. 2006. Pengantar Kesehatan Lingkungan. Jakarta: Penerbit Buku Kedokteran EGC
Dumont Y, Chiroleu F, Domerg C (2008). On a temporal model for the Chikungunya disease: Modelling, theory and numerics. Mathematical Biosciences, 213:80-91.
Edelstein-Keshe L. 1988. Mathematical Models in Biology. New York : Random
House.
Labadie et al (2010). Chikungunya disease in nonhuman primates involves long-term viral persistence in macrophages. The Journal of Clinikal Investigation, 120(3):894-906
Pialoux G, Gauzere B. A, Jaureguiberry S, Strobel M (2007). Chikungunya, an epidemic arbovirosis. Lancet Infect. Dis. 7:319.
Szidarovszky F. dan AT.Bahill. 1998. Linear System Theory. CRC Press. Florida.
Tu PNV. 1994. Dinamical System, An Introduction with Applications in
Economics and Biology. New York : Springer-Verlag.
van den Driessche, P., Watmough, J., 2005. Reproduction numbers and sub-threshold endemic equilibria for compartmental models of disease transmission. Mathematical Biosciences. 180 (2002) 29.
van den Driessche, P., Watmough, J., 2008. Chapter 5: Further Notes on the Basic
Mathematical Epidemiology, Vol. 1945. Lecture Notes in Mathematics,
Springer, pp. 159–178.
Verhulst F. 1990. Nonlinear Differential Equation and Dynamical System.
40
Lampiran 1. Penentuan Titik Tetap
Clear[f1,f2,f3,f4,f5,f6,f7,sh,eh,ih,rh,lm,sm,em,im,µh,b,βmh,θ,νh,ηh,µb,k,ηl,µl,c, βhm,µm,ηm,sol]
f1[sh_,eh_,ih_,rh_,lm_,sm_,em_,im_]:=µh nh-b βmh im/nh sh-µh sh+θ rh;
f2[sh_,eh_,ih_,rh_,lm_,sm_,em_,im_]:=b βmh im/nh sh-νh eh-µh eh;
f3[sh_,eh_,ih_,rh_,lm_,sm_,em_,im_]:=νh eh-ηh ih-µh ih;
f4[sh_,eh_,ih_,rh_,lm_,sm_,em_,im_]:=ηh ih-µh rh-(θ+µh)rh;
f5[sh_,eh_,ih_,rh_,lm_,sm_,em_,im_]:=µb (1-lm/k)(sm+em+im)-ηl lm-µl lm;
f6[sh_,eh_,ih_,rh_,lm_,sm_,em_,im_]:=-c βhm ih/nh sm-µm sm+ηl lm;
f7[sh_,eh_,ih_,rh_,lm_,sm_,em_,im_]:=c βhm ih/nh sm-µm em-ηm em;
Lampiran 2. Penentuan Bilangan Reproduksi Dasar (R0)
Dengan mengambil sistem persamaan (4.1) dan menyusunnya kembali dalam urutan sub-sub populasi yang menyebabkan infeksi saja, yaitu , , , dan diperoleh sistem persamaan sebagai berikut:
Dari sistem di atas, diperoleh matriks-matriks
Φ = dan ς =
Sehingga,
F = dan V =
42
sehingga bilangan reproduksi dasar adalah
=
Populasi manusia
(1)
(2)
( (
44
(1) (3)
(2) = (6)
Populasi Nyamuk
46
atau
jika
Dan
48
Lanjutan teorema I
Bilangan Reproduksi
Dengan mengambil sistem persamaan (4.1) dan menyusunnya kembali dalam urutan sub-sub populasi yang menyebabkan infeksi saja, yaitu , , , dan diperoleh sistem persamaan sebagai berikut:
Dari sistem di atas, diperoleh matriks-matriks
sehingga,
50
Selanjutnya, dihitung matriks K = FV-1 sebagai berikut:
rh'[t]ηh ih[t]-µh rh[t]-(θ+µh)rh[t],
sm[t0]0,em[t0]0,im[t0]60},{sh[t],eh[t],ih[t],rh[t],lm[t],sm[t],em[t],im[t]},{t,t0,T}]
54
fsm[i_]:=sol1[i][[1,6,2]];
Plot[Evaluate[Table[fsm[i],{i,µm1,2*µm1,µm1}]],{t,0,T},PlotLegend→{"µm = 1/7","µm =
2/7"},LegendPosition→{1,0.3},LegendTextSpace→3,LegendSize→0.5, ShadowBackground→White,AxesLabel→{"t","sm"},AxesOrigin→{0,0}]
fem[i_]:=sol1[i][[1,7,2]];
Plot[Evaluate[Table[fem[i],{i,µm1,2*µm1,µm1}]],{t,0,T},PlotLegend→{"µm = 1/7","µm =
2/7"},LegendPosition→{1,0.3},LegendTextSpace→3,LegendSize→0.5, ShadowBackground→White,AxesLabel→{"t","em"},AxesOrigin→{0,0}]
fim[i_]:=sol1[i][[1,8,2]];
eh'[t]b βmh im[t]/nh[t] sh[t]-νh eh[t]-µh eh[t],
sm[t0]0,em[t0]0,im[t0]60},{sh[t],eh[t],ih[t],rh[t],lm[t],sm[t],em[t],im[t]},{t,t0,T}]
Plot[Evaluate[Table[flm[i],{i,µm1,2*µm1,µm1}]],{t,0,T},PlotLegend→{"B = 0.05","B =
0.5"},LegendPosition→{1,0.3},LegendTextSpace→3,LegendSize→0.5, ShadowBackground→White,AxesLabel→{"t","lm"},AxesOrigin→{0,0}]
fsm[i_]:=sol1[i][[1,6,2]];
Plot[Evaluate[Table[fsm[i],{i,µm1,2*µm1,µm1}]],{t,0,T},PlotLegend→{"B = 0.05","B =
0.5"},LegendPosition→{1,0.3},LegendTextSpace→3,LegendSize→0.5, ShadowBackground→White,AxesLabel→{"t","sm"},AxesOrigin→{0,0}]
fem[i_]:=sol1[i][[1,7,2]];
Plot[Evaluate[Table[fem[i],{i,µm1,2*µm1,µm1}]],{t,0,T},PlotLegend→{"B = 0.05","B =
0.5"},LegendPosition→{1,0.3},LegendTextSpace→3,LegendSize→0.5, ShadowBackground→White,AxesLabel→{"t","em"},AxesOrigin→{0,0}]
fim[i_]:=sol1[i][[1,8,2]];
Plot[Evaluate[Table[fim[i],{i,µm1,2*µm1,µm1}]],{t,0,T},PlotLegend→{"B = 0.05","B = 0.5"},LegendPosition→