Lampiran 2. Tumbuhan Pecut Kuda
Lampiran 3. Hasil Mikroskopik dengan Perbesaran 10 × 40
Keterangan:
1. Stomata tipe diasitik
2. Pembuluh kayu dengan penebalan jala 3. Serat sklerenkim
Lampiran 4. Perhitungan Hasil Karakterisasi Simplisia dan Ekstrak n-Heksan Pecut Kuda
Perhitungan Hasil Karakterisasi Simplisia Pecut Kuda 1. Perhitungan Penetapan Kadar Air
% Kadar Air = volumeair (ml )
beratsampel (g) x 100%
a. Berat sampel = 5,011 g Volume air = 0,4 ml
% Kadar Air =0,4 ml
5,011 g x 100% = 7,98 %
b. Berat sampel = 5,012 g Volume air = 0,5 ml
% Kadar Air = 0,5 ml
5,012 g x 100% = 9,97 %
c. Berat sampel = 5,004 g Volume air = 0,4 ml
% Kadar Air = 0,4 ml
5,004 g x 100% = 7,99 %
% Kadar Air Rata-Rata = 7,98%+9,97%+7,99%
3 = 6,65%
2. Perhitungan Penetapan Kadar Sari Larut dalam Air % Kadar sari larut dalam air = berat sari (g)
berat sampel (g) x 100
20 ×100%
a. Berat sampel = 5,0193 g Berat sari = 0,2042g
% Kadar sari larut dalam air =0,2042 g
5,0193 g x 100
20 ×100% = 20,34%
% Kadar sari larut dalam air =0,2021 g
5,0190 g x 100
20 ×100% = 20,13%
c. Berat sampel = 5,0187 g Berat sari = 0,201g
% Kadar sari larut dalam air = 0,201 g
5,0187 g x 100
20 ×100% = 20,02%
% Kadar sari larut dalam air rata-rata = 20,34%+20,13%+20,02%
3 = 20,16%
3. Perhitungan Penetapan Kadar Sari Larut dalam Etanol % Kadar sari larut dalam etanol = berat sari (g)
berat sampel (g) x 100
20 ×100%
a. Berat sampel = 5,0092 g Berat sari = 0,284g
% Kadar sari larut dalam etanol = = 0,284 g
5,0092 g x 100
20 ×100% = 28,34%
b. Berat sampel = 5,010 g Beratsari = 0,294g
% Kadar sari larut dalam etanol =0,294 g
5,010 g x 100
20 ×100% = 29,34%
c. Berat sampel = 5,0086 g Berat sari = 0,273g
% Kadar sari larut dalam etanol = 0,273 g
5,0086 g x 100
20 ×100% = 27,25%
% Kadar sari larut dalam etanol rata-rata = 28,34%+29,34%+27,25%
3 =
28,31%
4. Perhitungan Penetapan Kadar Abu Total % Kadar abu total = berat abu (g)
a. Berat sampel = 3,06 g Berat abu = 0,16g % Kadar abu total = 0,16 g
3,06 g×100% = 5,22%
b. Berat sampel = 3,08 g Beratabu = 0,18g
% Kadar abu total =0,18 g
3,08 g×100% = 5,84%
c. Berat sampel = 3,04 g Berat abu = 0,16g
% Kadar abu total = 0,16 g
3,04 g×100% = 5,26%
% Kadar abu total rata-rata = 5,22%+5,84%+5,26%
3 = 5,44%
5. Perhitungan Penetapan Kadar Abu Tidak Larut Asam % Kadar abu tidak larut asam = berat abu (g)
berat sampel (g)×100%
a. Berat sampel = 3,06 g Berat abu = 0,01g
% Kadar abu tidak larut asam = 0,01 g
3,06 g×100% = 0,32%
b. Berat sampel = 3,08 g Beratabu = 0,02g
% Kadar abu tidak larut asam =0,02 g
3,08 g×100% = 0,64%
c. Berat sampel = 3,04 g Berat abu = 0,01g
% Kadar abu tidak larut asam = 0,01 g
% Kadar abu tidak larut asam rata-rata = 0,32%+0,64%+0,52%
3 = 0,42%
Perhitungan Hasil Karakterisasi Ekstrak n-Heksan Pecut Kuda 1. Perhitungan Penetapan Kadar Air
% Kadar Air = volumeair (ml )
beratsampel (g) x 100%
Berat sampel = 1,002 g Volume air = 0,05 ml
% Kadar Air =0,05 ml
1,002 g x 100% = 4,99 %
2. Perhitungan Penetapan Kadar Abu Total % Kadar abu total = berat abu (g)
berat sampel (g)×100%
Berat sampel = 1,005 g Berat abu = 0,015g
% Kadar abu total = 0,015 g
1,005 g×100% = 1,49% 3. Perhitungan Penetapan Kadar Abu Tidak Larut Asam % Kadar abu tidak larut asam = berat abu (g)
berat sampel (g)×100%
Berat sampel = 1,005 g Berat abu = 0,004g
% Kadar abu tidak larut asam = 0,004 g
Lampiran 6. Alat yang Digunakan
Modifikasi alat penampung urin
Lampiran 7. Hasil Pengujian Dari AAS
Kelompok Dosis
Absorbansi
Natrium Kalium
Na CMC 0.5%
0.2424 0.1843
0.2527 0.1297
0.2099 0.1521
0.2729 0.1048
0.2328 0.0879
Furosemid 10 mg/kg bb
0.5896 0.3425
0.6097 0.3196
0.5032 0.3063
0.5568 0.2821
0.6302 0.2941
EnHPK 100 mg/kg bb
0.1898 0.1590
0.1702 0.1475
0.1475 0.1346
0.1544 0.1046
0.1388 0.1236
EnHPK 150 mg/kg bb
0.3924 0.1966
0.5097 0.2792
0.3481 0.2469
0.4268 0.2206
0.5424 0.1596
EnHPK 200 mg/kg bb
0.3725 0.1348
0.4817 0.1853
0.4559 0.2045
0.2730 0.1253
Lampiran 8. Data Volume Urin Tiap Jam (ml), Volume Total Urin Rata-rata (ml), Kadar Natrium (meq/l), dan Kadar Kalium (meq/l)
Data Volume Urin Tiap Jam
Kelompok Pengujian Rata-rata volume urin tiap jam (ml)
1 2 3 4 5
CMC-Na 0.5% 0,18 0,18 0,2 0,28 0,29
Furosemid 10 mg/kg bb 0,54 0,56 0,59 0,74 0,82
EnHPK 100 mg/kg bb 0,22 0,27 0,39 0,41 0,49
EnHPK 150 mg/kg bb 0,49 0,52 0,55 0,56 0,84
EnHPK 200 mg/kg bb 0,18 0,38 0,5 0,58 0,63
Data Volume Total Urin Rata-rata, Kadar Natrium dan Kadar Kalium
No Parameter Kontrol Na-CMC 0,5%
Furosemid 10 mg/kg bb
Ekstrak n-heksan Pecut Kuda
Dosis 100 mg/kg bb Dosis 150 mg/kg bb Dosis 200 mg/kg bb 1
Volume Total Urin Rata-rata (ml)
1,1 3,3 1,85
2,9 1,95
1,3 3,45 1,8
3,1 2,9
1 2,8 1,65
3 2,5
1,2 3 2,1
2,5 1,8
1,05 3,7 1,5
3,3 2,2
Rata-rata ± SD 1,13 ± 0,120 3,25 ± 0,357 1,78 ± 0,224
2,96 ± 0,297 2,27 ± 0,441 2 Kadar Natrium (meq/l)
37,66 91,01 29,58
60,71 57,65
39,24 94,10 26,57
78,73 74,43
32,67 77,73 23,08
53,90 70,47
42,35 85,97 24,14
65,99 42,36
36,18 97,25 21,74
83,76 45,51
Rata-rata ± SD 37,62 ± 3,59 89,21 ± 7,65 25,02 ± 3,10
68,62 ± 12,42 58,08 ±14,37 3 Kadar Kalium (meq/l)
27,49 50,66 23,79
29,30 20,25
19,49 47,31 22,11
41,39 27,64
22,78 45,36 20,22
36,66 30,45
15,85 41,82 15,82
32,81 18,85
13,38 43,57 18,60
23,88 15,85
Rata-rata ± SD 19,80 ± 5,59 45,75 ± 3,42 20,11 ± 3,09
32,81 ± 6,72
Lampiran 9. Contoh perhitungan kadar elektrolit
Kadar Na = Konsentrasi (mcg /ml )
Volume sampel x 2500
Pembacaan pada AAS = 0,3988 mcg/ml
Kadar Na = 0,3988 mcg /ml
1 ml x 2500 = 997 mcg/ml
= 0,997 mg/ml
meq/L = Kadar Na (mg /ml )
BM Na x 1 meq
= 0,997 mg /ml
123 x 1 meq = 0,04334 meq/ml
Lampiran 10. Data Kalibrasi Natrium Kalibrasi Natrium
Konsentrasi Absorbansi
0.0000 -0.0002
1.0000 0.1385
2.0000 0.2793
3.0000 0.4145
4.0000 0.5693
5.0000 0.7046
Penentuan Persamaan Regresi
Konsentrasi ( X )
Absorbansi
( Y ) XY X2 Y2
0.0000 -0.0002 0 0 0.00000004
1.0000 0.1385 0.1385 1 0.01918225
2.0000 0.2793 0.5586 4 0.07800849
3.0000 0.4145 1.2435 9 0.17181025
4.0000 0.5693 2.2772 16 0.32410249
5.0000 0.7046 3.523 25 0.49646116
ΣX= 15 ΣY=2.106
ΣXY= 7.7408 ΣX2=55 ΣY 2
=1.08956468
x =2.5 y =0.351
-0,2 0 0,2 0,4 0,6 0,8
0 1 2 3 4 5
A
b
s
o
rb
a
n
s
i
Konsentrasi
Kurva Kalibrasi Natrium
a=
∑ �� −(∑ �)(∑ �)
�
∑ �2−(∑ �)2
�
=
7.7408−(15)(2.106 ) 6
55−(15)2
6
a =
7.7408−31.59 6
55−2256
a =
7.7408−5.26555−37.5
a =
2.475817.5
a= 0.141474
b = y – ax = 0.351 – (0.141474) (2.5
)
b
=
0.351 – 0.353686
b = -0.00269
Persamaan Regresi Y = aX + b
Y = 0.141474X – 0.00269
r =
∑ �� −(∑ �)(∑ �)
�
��∑ �2
–(∑ ��)2��∑ �2−(∑ ��)2�
=
7.7408−(15)(2.106 ) 6
��55–(15)26 ��1.08956468−(2.106 )26 �
=
7.7408−31.59 6
��55–225
6 ��1.08956468−
4.435236
6 �
=
7.7408−5.265��55–37.5�[1.08956468−0.739206 ]
=
2.4758�[17.5][0.350359 ]
=
2.4758√6.131277
=
2.47582.4761
Lampiran 11. Hasil Kalibrasi Kalium Kalibrasi Kalium
Konsentrasi Absorbansi
0.0000 0.0003
2.0000 0.0842
4.0000 0.1710
6.0000 0.2488
8.0000 0.3502
10.0000 0.4379
Penentuan Persamaan Regresi
Konsentrasi ( X )
Absorbansi
( Y ) XY X2 Y2
0.0000 0.0003 0 0 0.00000009
2.0000 0.0842 0.1684 4 0.00708964
4.0000 0.171 0.684 16 0.029241
6.0000 0.2488 1.4928 36 0.06190144
8.0000 0.3502 2.8016 64 0.12264004
10.0000 0.4379 4.379 100 0.19175641
ΣX= 30 ΣY=1.2924
ΣXY=9.5258 ΣX2=220 ΣY2= 0.41262862 x =5 y =0.2154
0 0,1 0,2 0,3 0,4 0,5
0 2 4 6 8 10
A
b
s
o
rb
a
n
s
i
Konsentrasi
Kurva Kalibrasi Kalium
A =
∑ �� −(∑ �)(∑ �)
�
∑ �2−(∑ �)2
�
=
9.5258−(30)(1.2924 ) 6
220−(30)2
6
a =
9.5258−38.772 6
220−900
6
a =
9.5258−6.462220−150
a =
3.063870
a=
0.043769b = y – ax = 0.2154 – (0.043769) (5
)
b
=
0.2154 – 0.218843
b =
-
0.00344Persamaan Regresi
Y = aX + bY = 0.043769X - 0.00344
r =
∑ �� −(∑ �)(∑ �)
�
��∑ �2
–(∑ ��)2��∑ �2−(∑ ��)2�
=
9.5258−(30)(1.2924 ) 6
��220–(30)2
6 ��0.41262862−
(1.2924 )2
6 �
=
9.5258−38.772 6
��220−900
6 ��0.41262862−
1.670298
6 �
=
9.5258−6.462�[220−150][0.41262862−0.278383 ]
=
3.0638�[70][0.134246 ]
=
3.0638√9.397196
=
3.06383.0654
Lampiran 12. Hasil data statistik ANAVA dengan Uji Tukey Descriptives
Volume Urin Jam ke-1
N Mean Std.
Deviation Std. Error
95% Confidence Interval for Mean
Min Max Lower
Bound
Upper Bound
Na-CMC 0,5% 5 .1800 .24900 .11136 -.1292 .4892 .00 .50 Furosemid 10 mg/kg
bb 5 .5400 .53080 .23738 -.1191 1.1991 .00 1.20 EnHPK 100 mg/kg bb
5 .2200 .31937 .14283 -.1766 .6166 .00 .70 EnHPK 150 mg/kg bb
5 .4700 .53572 .23958 -.1952 1.1352 .00 1.30 EnHPK 200 mg/kg bb
5 .1800 .40249 .18000 -.3198 .6798 .00 .90 Total 25 .3180 .41730 .08346 .1457 .4903 .00 1.30
Multiple Comparisons
Volume Urin Jam ke-1 Tukey HSD (I)Kelompok Pengujian (J)Kelompok Pengujian Mean Difference (I-J) Std.
Error Sig.
95% Confidence Interval Lower Bound Upper Bound
Na-CMC 0,5% Furosemid 10
mg/kg bb -.36000 .26754 .667 -1.1606 .4406 EnHPK 100
mg/kg bb -.04000 .26754 1.000 -.8406 .7606 EnHPK 150
mg/kg bb -.29000 .26754 .813 -1.0906 .5106 EnHPK 200
mg/kg bb .00000 .26754 1.000 -.8006 .8006 Furosemid 10 mg/kg
bb
Na-CMC 0,5%
.36000 .26754 .667 -.4406 1.1606 EnHPK 100
mg/kg bb .32000 .26754 .754 -.4806 1.1206 EnHPK 150
mg/kg bb .07000 .26754 .999 -.7306 .8706 EnHPK 200
Deskriptive
Volume Urin Jam ke-2
N Mean Std. Deviation
Std. Error
95% Confidence Interval for Mean
Min Max Lower
Bound
Upper Bound
Na-CMC 0,5% 5 .3600 .49800 .22271 -.2583 .9783 .00 1.00 Furosemid 10
mg/kg bb 5 1.1000 1.08570 .48554 -.2481 2.4481 .00 2.35 EnHPK 100 mg/kg
bb 5 .4900 .46152 .20640 -.0831 1.0631 .00 1.00 EnHPK 150 mg/kg
bb 5 1.0100 .86342 .38613 -.0621 2.0821 .00 2.00 EnHPK 200 mg/kg
bb 5 .5600 .56833 .25417 -.1457 1.2657 .00 1.30
Total 25 .7040 .73625 .14725 .4001 1.0079 .00 2.35
Multiple Comparisons
Volume Urin Jam ke-2 Tukey HSD
(I) Kelompok Pengujian (J) Kelompok Pengujian
Mean Difference (I-J)
Std. Error Sig.
95% Confidence Interval Lower Bound Upper Bound
Na-CMC 0,5% Furosemid 10
mg/kg bb -.74000 .46547 .520 -2.1329 .6529 EnHPK 100
mg/kg bb -.13000 .46547 .999 -1.5229 1.2629 EnHPK 150
mg/kg bb -.65000 .46547 .637 -2.0429 .7429 EnHPK 200
mg/kg bb -.20000 .46547 .992 -1.5929 1.1929
Furosemid 10 mg/kg bb Na-CMC 0,5% .74000 .46547 .520 -.6529 2.1329 EnHPK 100
mg/kg bb .61000 .46547 .688 -.7829 2.0029 EnHPK 150
mg/kg bb .09000 .46547 1.000 -1.3029 1.4829 EnHPK 200
Descriptives
Volume Urin Jam ke-3
N Mean Std. Deviation
Std. Error
95% Confidence Interval for Mean
Min Max Lower
Bound
Upper Bound
Na-CMC 0,5% 5 .5600 .38471 .17205 .0823 1.0377 .00 1.00
Furosemid 10
mg/kg bb 5 1.6900 .80808 .36139 .6866 2.6934 1.10 3.00 EnHPK 100
mg/kg bb 5 .8800 .33653 .15050 .4621 1.2979 .45 1.35 EnHPK 150
mg/kg bb 5 1.5600 .88487 .39573 .4613 2.6587 .80 2.90 EnHPK 200
mg/kg bb 5 1.0600 .65803 .29428 .2430 1.8770 .00 1.70 Total
25 1.1500 .73499 .14700 .8466 1.4534 .00 3.00
Multiple Comparisons
Volume Urin Jam ke-3
Tukey HSD
(I) Kelompok Pengujian (J)Kelompok Pengujian
Mean Difference (I-J)
Std. Error Sig.
95% Confidence Interval Lower Bound Upper Bound
Na-CMC 0,5% Furosemid 10
mg/kg bb -1.13000 .41282 .083 -2.3653 .1053
EnHPK 100
mg/kg bb -.32000 .41282 .935 -1.5553 .9153
EnHPK 150
mg/kg bb -1.00000 .41282 .150 -2.2353 .2353
EnHPK 200
mg/kg bb -.50000 .41282 .745 -1.7353 .7353
Furosemid 10 mg/kg bb Na-CMC 0,5% 1.13000 .41282 .083 -.1053 2.3653
EnHPK 100
mg/kg bb .81000 .41282 .319 -.4253 2.0453
EnHPK 150
mg/kg bb .13000 .41282 .998 -1.1053 1.3653
EnHPK 200
Descriptives
Volume Urin Jam ke-4
N Mean Std.
Deviation Std. Error
95% Confidence Interval for Mean
Min Max Lower
Bound
Upper Bound Na-CMC 0,5%
5 .8400 .35071 .15684 .4045 1.2755 .40 1.30 Furosemid 10 mg/kg
bb 5 2.4300 .76616 .34264 1.4787 3.3813 1.60 3.45 EnHPK 100 mg/kg bb
5 1.2900 .51039 .22825 .6563 1.9237 .70 1.85 EnHPK 150 mg/kg bb
5 2.1200 .44385 .19849 1.5689 2.6711 1.80 2.90 EnHPK 200 mg/kg bb
5 1.6400 .68044 .30430 .7951 2.4849 .90 2.50 Total 25 1.6640 .77976 .15595 1.3421 1.9859 .40 3.45
Multiple Comparisons
Volume Urin Jam ke-4
Tukey HSD
(I) Kelompok Pengujian (J) Kelompok
Pengujian
Mean Difference (I-J)
Std. Error Sig.
95% Confidence Interval Lower Bound Upper Bound
Na-CMC 0,5% Furosemid 10
mg/kg bb -1.59000
*
.36116 .002 -2.6707 -.5093
EnHPK 100
mg/kg bb -.45000 .36116 .725 -1.5307 .6307
EnHPK 150
mg/kg bb -1.28000
*
.36116 .015 -2.3607 -.1993
EnHPK 200
mg/kg bb -.80000 .36116 .215 -1.8807 .2807
Furosemid 10 mg/kg bb Na-CMC 0,5% 1.59000* .36116 .002 .5093 2.6707
EnHPK 100
mg/kg bb 1.14000
*
.36116 .036 .0593 2.2207
EnHPK 150
mg/kg bb .31000 .36116 .909 -.7707 1.3907
EnHPK 200
mg/kg bb .79000 .36116 .225 -.2907 1.8707
Descriptives
Volume Urin Jam ke-5
N Mean Std.
Deviation Std. Error
95% Confidence Interval for Mean
Min Max
Lower Bound
Upper Bound
Na-CMC 0,5% 5 1.1300 .12042 .05385 .9805 1.2795 1.00 1.30
Furosemid 10
mg/kg bb 5 3.2500 .35707 .15969 2.8066 3.6934 2.80 3.70
EnHPK 100 mg/kg
bb 5 1.7800 .22528 .10075 1.5003 2.0597 1.50 2.10
EnHPK 150 mg/kg
bb 5 2.9600 .29665 .13266 2.5917 3.3283 2.50 3.30
EnHPK 200 mg/kg
bb 5 2.2700 .44102 .19723 1.7224 2.8176 1.80 2.90
Total
25 2.2780 .83617 .16723 1.9328 2.6232 1.00 3.70
Multiple Comparisons
Volume Urin Jam ke-5
Tukey HSD
(I) Kelompok Pengujian (J) Kelompok
Pengujian
Mean Difference (I-J)
Std. Error Sig.
95% Confidence Interval Lower Bound Upper Bound
Na-CMC 0,5% Furosemid 10
mg/kg bb -2.12000
*
.19499 .000 -2.7035 -1.5365
EnHPK 100
mg/kg bb -.65000
*
.19499 .024 -1.2335 -.0665
EnHPK 150
mg/kg bb -1.83000
*
.19499 .000 -2.4135 -1.2465
EnHPK 200
mg/kg bb -1.14000
*
.19499 .000 -1.7235 -.5565
Furosemid 10 mg/kg bb Na-CMC 0,5%
2.12000* .19499 .000 1.5365 2.7035
EnHPK 100
mg/kg bb 1.47000
*
.19499 .000 .8865 2.0535
EnHPK 150
mg/kg bb .29000 .19499 .582 -.2935 .8735
EnHPK 200
mg/kg bb .98000
*
.19499 .001 .3965 1.5635
Descriptives Volume total urin
N Mean
Std. Deviati-on Std. Error 95% Confidence Interval for Mean
Min Max Lower
Bound
Upper Bound
CMC-Na 0.5% 5 1.1300 .12042 .05385 .9805 1.2795 1.00 1.30 Furosemid 10
mg/kgbb 5 3.2500 .35707 .15969 2.8066 3.6934 2.80 3.70 EnHPK 100
mg/kgbb 5 1.7780 .22454 .10042 1.4992 2.0568 1.50 2.10 EnHPK 150
mg/kgbb 5 2.9600 .29665 .13266 2.5917 3.3283 2.50 3.30 EnHPK 200
mg/kgbb 5 2.2700 .44102 .19723 1.7224 2.8176 1.80 2.90 Total 25 2.2776 .83639 .16728 1.9324 2.6228 1.00 3.70
Multiple Comparisons Volume total urin
Tukey HSD
(I) Kelompok uji (J) Kelompok uji Mean Difference (I-J) Std.
Error Sig.
95% Confidence Interval Lower Bound Upper Bound
CMC-Na 0.5% Furosemid 10 mg/kgbb
-2.12000* .19492 .000 -2.7033 -1.5367
EnHPK 100 mg/kgbb
-.64800* .19492 .025 -1.2313 -.0647
EnHPK 150 mg/kgbb
-1.83000* .19492 .000 -2.4133 -1.2467
EnHPK 200 mg/kgbb
-1.14000* .19492 .000 -1.7233 -.5567
Furosemid 10 mg/kgbb
CMC-Na 0.5%
2.12000* .19492 .000 1.5367 2.7033
EnHPK 100 mg/kgbb
1.47200* .19492 .000 .8887 2.0553
EnHPK 150 mg/kgbb
.29000 .19492 .582 -.2933 .8733
EnHPK 200 mg/kgbb
.98000* .19492 .001 .3967 1.5633
Descriptives
Kadar Natrium
N Mean Std. Deviation
Std. Error
95% Confidence Interval for Mean
Min Max Lower
Bound
Upper Bound
Na-CMC
0,5% 5 37.6210 3.59090 1.60590 33.1623 42.0797 32.67 42.35 Furosemid
10 mg/kg bb 5 89.2144 7.64794 3.42026 79.7183 98.7106 77.74 97.25 EnHPK 100
mg/kg bb 5 25.0207 3.10099 1.38680 21.1703 28.8711 21.74 29.58 EnHPK 150
mg/kg bb 5 68.6207 12.42528 5.55675 53.1927 84.0487 53.90 83.76 EnHPK 200
mg/kg bb 5 58.0856 14.36997 6.42645 40.2430 75.9283 42.36 74.43
Total 25 55.7125 24.65355 4.93071 45.5360 65.8890 21.74 97.25
Multiple Comparisons
Kadar Natrium Tukey HSD
(I) Kelompok uji
(J) Kelompok uji
Mean Difference
(I-J) Std. Error Sig.
95% Confidence Interval Lower Bound Upper Bound CMC-Na 0.5% Furosemid 10
mg/kgbb
-48.34376* 6.53676 .000 -67.9042 -28.7833
EnHPK 100 mg/kgbb
15.51752 6.53676 .164 -4.0429 35.0779
EnHPK 150 mg/kgbb
-29.31686* 6.53676 .002 -48.8773 -9.7564
EnHPK 200 mg/kgbb
-16.11776 6.53676 .139 -35.6782 3.4427
Furosemid 10 mg/kgbb CMC-Na 0.5% 48.34376* 6.53676 .000 28.7833 67.9042
EnHPK 100 mg/kgbb
63.86128* 6.53676 .000 44.3008 83.4217
EnHPK 150 mg/kgbb
19.02690 6.53676 .059 -.5335 38.5873
EnHPK 200 mg/kgbb
32.22600* 6.53676 .001 12.6656 51.7864
Descriptives
Kadar Kalium
N Mean Std.
Deviation Std. Error
95% Confidence Interval for Mean
Min Max Lower
Bound
Upper Bound
Na-CMC 0,5% 5 19.8009 5.59080 2.50028 12.8590 26.7428 13.38 27.50
Furosemid 10
mg/kg bb 5 45.7472 3.42493 1.53167 41.4946 49.9998 41.82 50.67 EnHPK 100
mg/kg bb 5 20.1085 3.08953 1.38168 16.2723 23.9446 15.82 23.79 EnHPK 150
mg/kg bb 5 32.8092 6.72052 3.00551 24.4646 41.1538 23.88 41.39 EnHPK 200
mg/kg bb 5 22.6100 6.16863 2.75869 14.9506 30.2693 15.85 30.45 Total 25 28.2151 11.22694 2.24539 23.5809 32.8494 13.38 50.67
Multiple Comparisons Kadar Kalium Tukey HSD (I)Kelompok Pengujian (J)Kelompok Pengujian Mean Difference
(I-J) Std. Error Sig.
95% Confidence Interval Lower Bound Upper Bound Na-CMC 0,5% Furosemid 10 mg/kg
bb -25.94624
*
3.29545 .000 -35.8075 -16.0850
EnHPK 100 mg/kg
bb -.30756 3.29545 1.000 -10.1688 9.5537 EnHPK 150 mg/kg
bb -13.00827
*
3.29545 .006 -22.8695 -3.1471
EnHPK 200 mg/kg
bb -2.80904 3.29545 .911 -12.6703 7.0522
Furosemid 10 mg/kg bb Na-CMC 0,5% 25.94624* 3.29545 .000 16.0850 35.8075 EnHPK 100 mg/kg
bb 25.63868
*
3.29545 .000 15.7775 35.4999
EnHPK 150 mg/kg
bb 12.93797
*
3.29545 .007 3.0768 22.7992
EnHPK 200 mg/kg
bb 23.13720
*
3.29545 .000 13.2760 32.9984
DAFTAR PUSTAKA
Asif, M., Jabeen, Q., Atif, M., Majid, A. M. S. A., dan Zaman, M. Q. (2014). Diuretic Activity of Achyranthes aspera Linn Crude Aqueous Extract in Albino Rats. Tropical Journal of Pharmaceutical Research. 13(12): 2039-2045.
Basset, J., Denney, R. C., Jeffery, G. H., dan Mendham, J. (1994). Buku Ajar Vogel: Kimia Analisis Kuantitatif Anorganik. Penerjemah: Hadyana, A dan Setiono, L. Jakarta: EGC. Halaman 234-245.
Bhadoriya, U., Tiwari, S., Sharma, P., Bankey, S., dan Mourya, M. (2011). Diuretic Activity of Extract of Salvia officinalis L. Asian Journal of Pharmacy and Life Science. 1(1): 24-28.
Bourne, R. H. dan Zastrow, V. M. (2001). Reseptor dan Farmakodinamika Obat. Dalam: Farmakologi Dasar dan Klinik. Edisi I. Jakarta: Salemba Medika. Halaman 30-31.
BPOM, RI. (2012). Pedoman Teknologi Formulasi Sediaan Berbasis Ekstrak. Volume 1. Jakarta: Badan Pengawasan Obat dan Makanan RI. Halaman 6, 12, 14.
Calista. (2010). Ekstraksi Senyawa Aktif Dari Tumbuhan Liar Pecut Kuda Sebagai Obat Herbal Antikanker Menggunakan Metode Ramah Lingkungan. Skripsi. Surabaya: Universitas Katolik Widya Mandala.
Dalimartha, S. (2000). Atlas Tumbuhan Obat Indonesia. Jilid 2. Jakarta: Pustaka Bunda. Halaman 146-148.
Darwis, W., Hafiedzani, M., dan Astuti, R. R. S. (2012). Efektivitas Ekstrak Akar dan Daun Pecut Kuda Stachytarpetha jamaicensis (L.) Vahl Dalam Menghambat Pertumbuhan Jamur Candida albicans Penyebab Kandidiasis Vaginalis. Jurnal Ilmiah. 8(2).
Depkes, RI. (1995). Farmakope Indonesia. Edisi Keempat. Jakarta: Departemen Kesehatan RI. Halaman 29-31, 33, 649, 748, 970.
Depkes, RI. (1979). Farmakope Indonesia. Edisi Ketiga. Jakarta: Departemen Kesehatan RI. Halaman 7, 744,748.
Ditjend, POM. (1989). Materia Medika Indonesia. Jilid V. Jakarta: Departemen Kesehatan RI. Halaman 169-171, 300-337.
Farnsworth, N. R. (1966). Biological and Phytochemical Screenning of Plants. Journal of Pharmaceutical Science. 55(3): 256-263.
Foye, W. O. (1995). Prinsip-Prinsip Kimia Medisinal. Jilid II. Yogyakarta: UGM Press. Halaman 145-150.
Ganong, W. F. (2002). Buku Ajar Fisiologi Kedokteran. Edisi 20. Jakarta: EGC. Halaman 671-680.
Gandasoebrata. (1992). Penuntun Laboratorium Klinik. Jakarta: PT. Dian Rakyat. Guyton, A. C. (1997). Fisiologi Manusia dan Mekanisme Penyakit III.
Terjemahan: P. Andrianto.Jakarta : EGC
Guyton dan Hall. (1997). Buku Ajar Fisiologi Kedokteran. Edisi IX. Jakarta: EGC. Halaman 289-345.
Harborne, J. B. (1987). Metode Fitokimia Penuntun cara Modern Menganalisa Tumbuhan. Edisi II. Penerjemah: Kosasih Padmawinata dan Iwang Soediro. Bandung: ITB. Halaman 94-97, 152.
Hastuti, A. (2013). Uji Efek Diuretik Ekstrak Etanol Daun Kersen (Muntingia calabura L.) Terhadap Kadar Natrium dan Kalium Pada Urin Tikus Putih Jantan Galur Wistar. Skripsi. Jurusan Farmasi. Sekolah Tinggi Ilmu Kesehatan Ngudi Waluyo. Ungaran.
Indrayani, L. (2006). Skrining Fitokimia dan Uji Toksisitas Ekstrak Etanol Pecut Kuda (Stachytarpetha jamaicensis L.Vahl) Terhadap Larva Udang (Artemia salina Leach). Berk. Penel. Hayati: 12: 57-61.
Isnania, Fatimawali, dan Wehantouw, F. (2014). Aktivitas Diuretik dan Skrining Fitokimia Ekstrak Etanol Biji Pepaya (Carica papaya L.)Pada Tikus Putih Jantan Galur Wistar (Rattus norvegicus). Jurnal Ilmiah Farmasi. 3(3): 188-195.
Jannah, H., Sudarma, I. M., Andayani, Y. (2013). Analisis Senyawa Fitosterol Dalam Ekstrak Buah Buncis (Phaseolus vulgaris L.). Chem. Prog. 6(2): 70.
Lingga, I. S., Citraningtyas, G., Lolo, W. A. (2014). Uji Efek Ekstrak Etanol Patikan Kebo (Euphorbia hirta Linn.) Sebagai Diuretik pada Tikus Putih Jantan Galur Wistar (Rattus norvegicus sp.). Jurnal Ilmiah Farmasi. 3(3) : 288.
Mamoon, S. A., dan Azam, M. G. (2011). Diuretic Activity and Brine Shrimp Toxicity of Derris trifoliate Lour. International Journal of Pharmacy and Life Science. 2(9): 1029-1032.
Masroh, L. (2010). Isolasi dan Uji Toksisitas Senyawa Aktif Ekstrak Heksana Daun Pecut Kuda (Stachytarpetha jamaicensis L.Vahl). Skripsi. Jurusan Kimia. Fakultas Sains dan Teknologi.Universitas Islam Negeri (AIN). Maulana Malik Ibrahim. Malang.
Mutschler. E. (1991). Dinamika Obat. Edisi V. Bandung: Institut Teknologi Bandung. Halaman 565-568.
Nafrialdi. (2007). Diuretik dan Antidiuretik. Dalam: Farmakologi dan Terapi. Editor: Sulistia Gan Gunawan. Edisi V. Jakarta: Departemen Farmakologi dan Terapeutik FKUI. Halaman 345, 389-400.
Nessa., Arifin, H., Muchtar, H. (2013). Efek Diuretik dan Daya Larut Batu Ginjal Dari Ekstrak Etanol Rambut Jagung (Zea mays L.). Prosiding Seminar Nasional Perkembangan Terkini Sains Farmasi dan Klinik III.
Parmar, N. S., dan Prakash, S. (2006). Screening Methods in Pharmacology. Kawali: Institute of Pharmacheutical Science and Technology. Halaman 241-245.
Permadi, A. (2006). Tanaman Obat Pelancar Air Seni. Cetakan I. Jakarta: Penebar Swadaya. Halaman 16-20.
Putera, K. A. S. BT. I. (2010). Antimicrobial Activity and Cytotoxic Effects of Stachytarpheta jamaicensis (L.) Vahl Crude Plant Extracts. Dissertation. Malaysia: Faculty of Biosciences and Bioengineering University Teknologi Malaysia. Halaman 6.
Rasyid, A. (2011). Ketidakseimbangan Cairan, Elektrolit dan Eliminasi. Tanggal akses: 4 Januari 2014. http://www.sisrom.blogspot.com/2006/ 05/kebutuhan-cairan-dan elektrolit. html.
Retnowati, K. (2012). Uji Aktivitas Antibakteri Ekstrak dan Fraksi Daun Pecut Kuda (Stachytarpetha jamaicensis (L.)Vahl) Terhadap Isolat Klinis Methicillin Resistant Staphylococcus Aureus. Skripsi. Jatinangor: Fakultas Farmasi. Universitas Padjadjaran.
Sinaga, T. I. F. (2014). Uji Efek Diuretik Ekstrak Etanol Buah Inggir-inggir (Solanum sanitwongsei Craib) Pada Tikus Putih Jantan. Skripsi. Fakultas Farmasi. Universitas Sumatera Utara. Medan.
Syamsuni, H. A. (2006). Ilmu Resep. Jakarta: Penerbit Buku Kedokteran EGC. Halaman 263-264.
Tjay, T. H., dan Rahardja, K. (2002). Obat-Obat Penting (Khasiat,Penggunaan, dan Efek-Efek Samping). Edisi V. Ditjen PCMRI, Jakarta. Halaman 372-381.
BAB III
METODE PENELITIAN
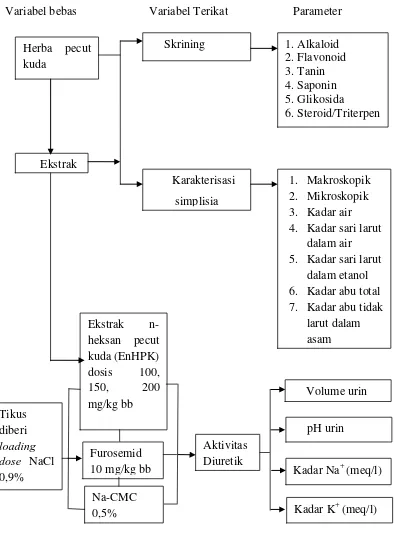
Penelitian ini bersifat eksperimental yang terdiri dari beberapa tahapan meliputi: pengumpulan tumbuhan pecut kuda, identifikasi tumbuhan, pembuatan simplisia pecut kuda, karakterisasi simplisia, skrining fitokimia, pembuatan ekstrak n-heksan pecut kuda, dan pengujian efek diuretik menggunakan rancangan acak lengkap (RAL). Data yang diperoleh di analisis secara ANAVA (analisis variansi) dan dilanjutkan dengan uji beda rata-rata Tukey menggunakan program statistical and product service solution (SPSS) 17.0.
3.1 Alat dan Bahan 3.1.1 Alat-alat
Alat-alat yang digunakan dalam penelitian ini adalah alat-alat gelas laboratorium, neraca listrik (Chyo JP2-6000), timbangan hewan (Chyo JP2-6000), rotary evaporator (Heidolph vv-2000), freeze dryer (Modulyo, Edwards serial no: 3985), mortir dan stamper, oral sonde, aluminium foil, waterbath, mikroskop, seperangkat alat pengujian diuresis berupa modifikasi kandang metabolik, AAS (Shimadzu AA 6200).
3.1.2 Bahan-bahan
3.2 Pengumpulan Tumbuhan Pecut Kuda
Pengumpulan tumbuhan dilakukan secara purposif, yaitu tanpa membandingkan dengan daerah lain. Tumbuhan yang digunakan dalam penelitian ini adalah pecut kuda yang diambil dari daerah Bukit Simarsayang, Kota Padang Sidempuan, Provinsi Sumatera Utara.
3.3 Identifikasi Tumbuhan
Identifikasi tumbuhan dilakukan oleh Lembaga Ilmu Pengetahuan Indonesia (LIPI) Pusat Penelitian dan Pengembangan Biologi Bogor. Sampel yang digunakan pada penelitian ini adalah sama dengan yang digunakan oleh Melida Kristina Baringbing seperti tertera pada lampiran 1.
3.4 Pembuatan Simplisia
Tumbuhan yang digunakan pada penelitian ini adalah pecut kuda yang masih segar. Tumbuhan dibersihkan dari pengotor lain seperti tanah dan serangga, lalu dicuci hingga bersih kemudian ditiriskan, dipotong-potong dan ditimbang, diperoleh berat basah sebesar 3,6 kg. Tumbuhan tersebut kemudian dikeringkan dalam lemari pengering pada temperatur ± 40ºC sampai tumbuhan kering. Simplisia yang telah kering diblender menjadi serbuk, ditimbang dan diperoleh berat simplisia sebesar 1,5 kg, lalu dimasukkan ke dalam wadah plastik bertutup rapat dan disimpan pada suhu kamar (Ditjend, POM., 1989).
3.5 Karakterisasi Simplisia
penetapan kadar sari larut dalam etanol, penetapan kadar abu total, penetapan kadar abu tidak larut dalam asam (Ditjend, POM., 1989).
3.5.1 Pemeriksaan makroskopik dan organoleptik
Pemeriksaan makroskopik dan organoleptik dilakukan dengan mengamati bentuk, rasa, bau, dan warna dari simplisia pecut kuda.
3.5.2 Pemeriksaan mikroskopik
Pemeriksaan mikroskopik terhadap simplisia dilakukan dengan cara menaburkan serbuk simplisia diatas kaca objek yang telah ditetesi dengan larutan kloralhidrat dan ditutup dengan kaca penutup kemudian diamati dibawah mikroskop (Ditjend, POM., 1989).
3.5.3 Penetapan kadar air
Penetapan kadar air dilakukan dengan metode Azeotropi (destilasi toluen). Alat terdiri dari labu kaca, tabung silinder, tabung pendingin, tabung penyambung dan tabung penerima. Caranya:
a. destilasi pertama
Dibersihkan tabung penerima dan pendingin pada alat, dibilas dengan air dan dikeringkan. Masukkan 200 ml toluena dan 2 ml air ke dalam labu yang kering. Dipanaskan alat untuk mendestilasi cairan selama 2 jam. Dibiarkan dingin selama 30 menit dan dibaca volume air dengan ketelitian 0,05 ml.
b. destilasi kedua
dinaikkan sampai 4 tetes tiap detik. Setelah semua air terdestilasi, dibilas bagian dalam tabung pendingin dengan toluen. Destilasi dilanjutkan selama 5 menit, hentikan pemanasan, dibiarkan tabung penerima dingin pada suhu kamar dan keluarkan tetesan air yang menempel pada dinding tabung penerima dengan menepuk tabung. Dibiarkan lapisan air dan toluen memisah dan baca volume airnya (WHO, 1998).
3.5.4 Penetapan kadar sari larut dalam air
Sebanyak 5 g serbuk dimaserasi selama 24 jam dalam 100 ml air kloroform (2,5 ml kloroform dalam air suling sampai 1000 ml) dalam labu bersumbat sambil sesekali dikocok selama 6 jam pertama kemudian dibiarkan selama 18 jam dan disaring. Sejumlah 20 ml filtrat pertama diuapkan sampai kering dalam cawan dangkal berdasar rata yang telah ditara. Sisa dipanaskan dalam oven pada suhu 105ºC sampai diperoleh bobot konstan. Kadar sari yang larut di dalam air dihitung terhadap bahan yang telah dikeringkan di udara (Depkes, RI., 1995).
3.5.5 Penetapan kadar sari larut dalam etanol
3.5.6 Penetapan kadar abu total
Timbang saksama dalam kurs porselin yang telah ditara sejumlah contoh setara dengan 2 g sampai 4 g bahan yang telah dikeringkan di udara, pijarkan perlahan-lahan, kemudian naikkan suhu secara bertahap hingga 675°C ± 25°C sampai bebas karbon dan tetapkan bobot abu. Jika abu bebas karbon tidak dapat diperoleh dengan cara tersebut, lakukan penyarian dengan air panas, tampung sisa yang tidak larut pada kertas saring bebas abu, pijarkan residu dan kertas saring sampai abu berwarna putih atau hampir putih, kemudian tambahkan filtrat, uapkan sampai kering, dan panaskan hingga suhu 675°C ± 25°C. Jika abu bebas karbon tidak dapat diperoleh dengan cara ini, dinginkan kurs porselin, tambahkan 15 ml etanol pekat, lepaskan abu dengan pengaduk gelas, bakar etanol dan panaskan lagi isi kurs porselin hingga suhu 675°C ± 25°C. Dinginkan dalam desikator, timbang abu dan hitung kadar abu dalam persen terhadap bobot contoh yang digunakan (Depkes, RI., 1995).
3.5.7 Penetapan kadar abu tidak larut asam
Didihkan abu yang diperoleh seperti yang tertera pada penetapan kadar abu dengan 25 ml asam klorida selama 5 menit, kumpulkan bagian tidak larut pada kurs yang telah ditara atau kertas saring bebas abu, cuci dengan air panas, pijarkan dan timbang. Hitung kadar abu tidak larut dalam asam dalam persen, dihitung terhadap bobot contoh yang digunakan (Depkes, RI., 1995).
3.6 Skrining Fitokimia
dilakukan meliputi skrining terhadap golongan alkaloid, flavonoid, tanin, saponin, glikosida, dan steroid/triterpen (Depkes, RI., 1995; Harborne, 1987).
3.6.1 Pemeriksaan alkaloida
Simplisia atau ekstrak n-heksan pecut kuda ditimbang sebanyak 0,5 g kemudian ditambahkan 1 ml asam klorida 2 N dan 9 ml air suling, dipanaskan di atas penangas air selama 2 menit, didinginkan dan disaring. Filtrat yang diperoleh dipakai untuk uji alkaloida: diambil 3 tabung reaksi, lalu kedalamannya dimasukkan 0,5 ml filtrat. Pada masing-masing tabung reaksi ditambahkan 2 tetes pereaksi Mayer, 2 tetes pereaksi Bouchardat, 2 tetes pereaksi Dragendroff. Alkaloida positif jika terjadi endapan atau kekeruhan paling sedikit dua dari tiga percobaan diatas (Depkes, RI., 1979).
3.6.2 Pemeriksaan flavonoida
Sebanyak 10 g simplisia atau ekstrak n-heksan pecut kuda ditambahkan 10 ml air panas, dididihkan selama 5 menit dan disaring dalam keadaan panas, ke dalam 5 ml filtrat ditambahkan 0,1 g serbuk magnesium dan 1 ml asam klorida pekat dan 2 ml amil alkohol, dikocok dan dibiarkan memisah. Flavonoida positif jika warna merah atau kuning atau jingga pada lapisan amil alkohol (Farnsworth, 1966).
3.6.3 Pemeriksaan glikosida
dan kloroform (2:3), dilakukan berulang kali sebanyak 3 kali. Sari air dikumpulkan dan diuapkan pada temperatur tidak lebih dari 50ºC. Sisanya dilarutkan dalam 2 ml air dan 5 tetes pereaksi Molish. Kemudian secara perlahan-lahan ditambahkan 2 ml asam sulfat pekat melalui dinding tabung, terbentuknya cincin berwarna ungu pada batas kedua cairan menunjukkan ikatan gula (Depkes, RI., 1979).
3.6.4 Pemeriksaan saponin
Simplisia atau ekstrak n-heksan pecut kuda ditimbang sebanyak 0,5 g dan dimasukkan ke dalam tabung reaksi, lalu ditambahkan 10 ml air panas, dinginkan kemudian dikocok kuat-kuat selama 10 detik. Jika terbentuk busa setinggi 1 - 10 cm yang stabil tidak kurang dari 10 menit dan tidak hilang dengan penambahan 1 tetes asam klorida 2 N menunjukkan adanya saponin (Depkes, RI., 1995).
3.6.5 Pemeriksaan tanin
Simplisia atau ekstrak n-heksan pecut kuda ditimbang sebanyak 1 g, dididihkan selama 30 menit dalam 100 ml air suling lalu didinginkan dan disaring. Pada filtrat ditambahkan 1 - 2 tetes pereaksi besi (III) klorida 1%. Jika terjadi warna biru kehitaman atau hijau kehitaman menunjukkan adanya tannin (Farnsworth, 1966).
3.6.6 Pemeriksaan steroida/triterpenoida
3.7 Pembuatan Ekstrak n-Heksan Pecut Kuda
Pembuatan ekstrak n-heksan pecut kuda dilakukan secara maserasi dengan menggunakan pelarut n-heksan. Caranya, sebanyak 1200 g serbuk simplisia pecut kuda dimasukkan ke dalam bejana kaca kemudian dituangi cairan penyari sebanyak 75 bagian cairan penyari n-heksan (9 liter), ditutup dan dibiarkan selama 5 hari terlindung dari cahaya sambil sering diaduk, lalu disaring, di remaserasi ampas dengan cairan penyari secukupnya hingga diperoleh 100 bagian (12 liter), maserat dipindahkan kedalam bejana tertutup, dibiarkan di tempat yang sejuk, terlindung dari cahaya selama 2 hari, lalu di enaptuangkan atau disaring. Maserat yang diperoleh dipekatkan dengan alat rotary evaporator. Kemudian dikeringkan dengan freeze dryer sehingga diperoleh ekstrak kental (Depkes, RI., 1979).
3.8 Penyiapan Bahan Uji, Obat Pembanding dan Kontrol
Ekstrak n-heksan pecut kuda dibuat dalam bentuk suspensi menggunakan Na-CMC 0,5%. Obat pembanding furosemid dibuat dalam bentuk suspensi menggunakan Na-CMC 0,5%. Kontrol negatif yang digunakan adalah suspensi Na-CMC 0,5%.
3.8.1 Pembuatan suspensi Na-CMC 0,5%
3.8.2 Pembuatan suspensi furosemid
Satu tablet yang mengandung 40 mg furosemid digerus dan ditambahkan larutan Na-CMC 0,5% sedikit demi sedikit sambil digerus dan diencerkan dengan sedikit air. Dimasukkan ke dalam labu tentukur 10 ml, volumenya dicukupkan dengan akuades hingga 10 ml.
3.9 Penyiapan Hewan Percobaan
Hewan percobaan yang digunakan dalam penelitian ini adalah tikus putih jantan dengan berat 150 - 200 g. Sebelum pengujian dikondisikan terlebih dahulu selama satu minggu dengan kondisi lingkungan, makanan, dan minuman yang sama. Setelah satu minggu, dipilih tikus yang sehat ditandai dengan berat badan yang stabil atau meningkat.
3.10 Pengujian Efek Diuretik Pecut Kuda
3.11 Pembuatan Kurva Kalibrasi Kalium
Larutan baku kalium (konsentrasi 1000 μg/ml) dipipet sebanyak 1 ml,
dimasukkan ke dalam labu tentukur 100 ml dan dicukupkan hingga garis tanda dengan akuabides (konsentrasi 10 μg/ml).
Larutan untuk kurva kalibrasi kalium dibuat dengan memipet (10; 20; 30; 40; 50) ml dari larutan baku 10 μg/ml, masing-masing dimasukkan ke dalam labu tentukur 50 ml dan dicukupkan hingga garis tanda dengan akuabides larutan ini mengandung (2,0; 4,0; 6,0; 8,0; 10,0) μg/ml dan diukur absorbansinya pada panjang gelombang 766,5 nm dengan nyala udara-asetilen.
3.12 Pembuatan Kurva Kalibrasi Natrium
Larutan baku natrium (konsentrasi 1000 μg/ml) dipipet sebanyak 1 ml,
dimasukkan ke dalam labu tentukur 100 ml dan dicukupkan hingga garis tanda dengan akuabides (konsentrasi 10 μg/ml). Larutan induk baku II dibuat dengan
memipet larutan 10 μg/ml sebanyak 25 ml dimasukkan ke dalam labu tentukur
100 ml dan dicukupkan hingga garis tanda dengan akuabides (konsentrasi 2,5 μg/ml).
3.13 Penentuan Kadar Natrium dan Kalium dengan Spektrofotometer Serapan Atom
Sebanyak 1 ml urin dimasukkan ke dalam labu tentukur 50 ml kemudian dicukupkan dengan akuades sampai 50 ml. Dipindahkan ke dalam erlemeyer dan ditambahkan 5 ml HNO3 pekat dan beberapa batu didih. Didihkan secara
perlahan-lahan kemudian diuapkan dengan hotplate hingga volume urin total tinggal 20 ml, saring. Filtrat dimasukkan ke dalam labu tentukur 100 ml dicukupkan dengan akuades sampai garis tanda. Faktor pengenceran untuk penentuan kadar natrium pada urin adalah 5 kali, faktor pengenceran untuk penentuan kadar kalium urin adalah 2,5 kali. Selanjutnya diukur menggunakan alat SSA (SNI, 2004).
3.14 Analisis Data
BAB IV
HASIL DAN PEMBAHASAN
4.1 Hasil Identifikasi Tumbuhan
Tumbuhan yang digunakan telah diidentifikasi di Lembaga Ilmu Penelitian Indonesia (LIPI) – Bogor menunjukkan bahwa tumbuhan yang digunakan adalah pecut kuda (Stachytarpheta jamaicencis (L.) Vahl). Suku Verbenaceae. Hasil identifikasi dapat dilihat pada Lampiran 1.
4.2 Hasil Karakterisasi Simplisia Pecut Kuda
Hasil pemeriksaan makroskopik simplisia pecut kuda menunjukkan simplisia berwarna hijau, tekstur rapuh, aroma yang khas, rasa sepat, sifatnya dingin dan pahit. Hasil pemeriksaan mikroskopik serbuk simplisia memperlihatkan adanya rambut biasa, rambut kelenjar, epidermis, serabut sklerenkim, pembuluh kayu dengan penebalan jala, jaringan gabus dan fragmen mesofil.
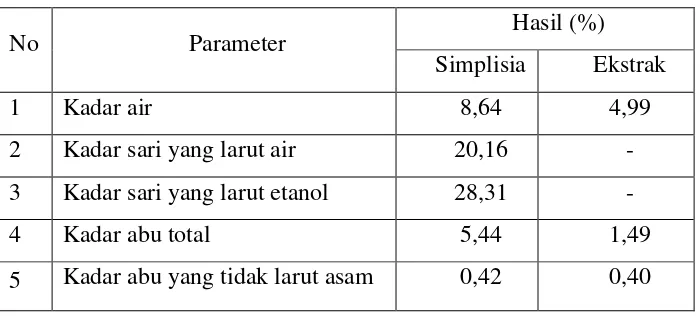
Tabel 4.1 Hasil Karakterisasi simplisia dan ekstrak n-heksan pecut kuda (Stachytarpheta jamaicensis L. Vahl)
No Parameter Hasil (%)
Simplisia Ekstrak
1 Kadar air 8,64 4,99
2 Kadar sari yang larut air 20,16 -
3 Kadar sari yang larut etanol 28,31 -
4 Kadar abu total 5,44 1,49
5 Kadar abu yang tidak larut asam 0,42 0,40
Hasil penetapan kadar air simplisia dan ekstrak n-heksan pecut kuda diperoleh 8,64% dan 4,99%. Hal ini sesuai dengan standarisasi kadar air simplisia secara umum dengan syarat yaitu tidak lebih dari 10% (Depkes, RI., 1995). Penetapan kadar air dilakukan untuk memberikan batasan minimal atau rentang tentang besarnya kandungan air dalam ekstrak karena tingginya kandungan air dapat menyebabkan ketidakstabilan sediaan obat, bakteri dan jamur cepat tumbuh dan bahan aktif yang terkandung didalamnya dapat terurai.
Penetapan kadar abu dimaksudkan untuk mengetahui kandungan mineral internal yang terdapat dalam simplisia yang diteliti serta senyawa organik yang tersisa selama pembakaran. Abu total terbagi dua, yang pertama abu fisiologis adalah abu yang berasal dari jaringan tumbuhan itu sendiri dan abu non fisiologis adalah sisa setelah pembakaran yang berasal dari bahan-bahan dari luar yang terdapat pada permukaan simplisia. Kadar abu tidak larut asam untuk menentukan jumlah silika, khususnya pasir yang ada pada simplisia dengan cara melarutkan abu total dalam asam klorida (WHO, 1998).
4.3 Hasil Skrining Fitokimia Simplisia dan EnHPK
[image:42.595.113.491.483.600.2]Skrining fitokimia serbuk simplisia dan ekstrak n-heksan pecut kuda dilakukan untuk mengetahui golongan senyawa metabolit sekunder yang terdapat di dalamnya. Hasil skrining fitokimia serbuk simplisia dan ekstrak dapat dilihat pada Tabel 4.2.
Tabel 4.2 Hasil skrining fitokimia serbuk simplisia dan ekstrak n-heksan pecut kuda (EnHPK)
No Parameter Tumbuhan Pecut Kuda
Simplisia Ekstrak n-Heksan
1 Alkaloid + +
2 Flavonoid + -
3 Saponin - -
4 Tanin + -
5 Glikosida + -
6 Steroid/Triterpenoid + +
Keterangan: + = mengandung golongan senyawa; - = tidak mengandung golongan senyawa
mengandung satu atau lebih atom nitrogen. Alkaloid merupakan suatu golongan senyawa organik yang terbanyak ditemukan di alam. Hampir seluruh alkaloid berasal
dari berbagai jenis tumbuhan. Semua alkaloid mengandung atom nitrogen yang
bersifat basa dan merupakan bagian dari cincin heterosiklik. Pada umumnya, basa bebas alkaloid hanya larut dalam pelarut organik dan juga diekstraksi dengan pelarut organik seperti kloroform, eter, dan sebagainya. Salah satu contoh alkaloid yang bersifat basa yaitu alkaloid steroid (solanidin, veratramin, dan sebagainya) (Robinson, 1995).
Steroid adalah triterpen yang mempunyai kerangka dasar system cincin siklopentana perhidrofenantren. Steroid adalah senyawa nonpolar yang dapat diekstraksi dengan pelarut organik yang bersifat nonpolar seperti eter atau heksana. Steroid yang terdapat dalam tumbuhan disebut fitosterol. Tiga senyawa yang biasa disebut fitosterol terdapat pada hampir setiap tumbuhan tinggi yaitu: sitosterol, stigmasterol, dan kampesterol (Harborne, 1987).
4.4 Hasil Pengujian Efek Diuretik
Pengujian efek diuretik ekstrak n-heksan pecut kuda dilakukan dengan parameter volume urin, pH urin, kadar natrium dan kadar kalium dalam urin terhadap tikus putih jantan.
4.4.1 Hasil volume urin
pertama menunjukkan adanya penambahan volume urin yang diproduksi dan yang kedua menunjukkan pengeluaran zat-zat terlarut dalam urin. Hasil pengukuran volume urin tikus setelah pemberian ekstrak n-heksan pecut kuda dapat dilihat pada Tabel 4.3.
Tabel 4.3 Hasil pengukuran volume urin rata-rata tiap jam selama 5 jam
Kelompok Pengujian
Rata-rata volume urin tiap jam (ml)
1 p 2 P 3 p 4 p 5 p
Na-CMC
0.5% 0,18 0,667 0,36 0,520 0,56 0,83 0,84 0,002 #
1,13 0,00#
Furosemid 10 mg/kg
bb
0,54 0,667 1,1 0,520 1,69 0,83 2,43 0,002* 3,25 0,00*
EnHPK 100 mg/kg
bb
0,22 1,00 0,49 0,999 0,88 0,935 1,29 0,725 1,78 0,024 *
0,754 0,688 0,319 0,036# 0,00#
EnHPK 150 mg/kg
bb
0,49 0,813 1,01 0,637 1,56 0,150 2,12 0,015 *
2,96 0,00 *
0,999 1,00 0,998 0,909 0,582
EnHPK 200 mg/kg
bb
0,18 1,00 0,56 0,992 1,06 0,745 1,64 0,215 2,27 0,00 *
0,667 0,773 0,558 0,225 0,001#
Keterangan: *= Berbeda signifikan terhadap Kontrol Na-CMC 0,5%
#
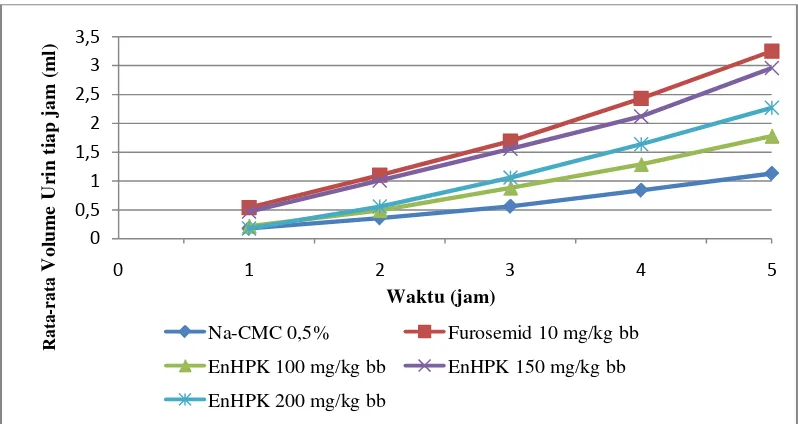
= Berbeda signifikan terhadap Furosemid 10 mg/kg bb Profil volume urin terhadap waktu ditunjukkan pada Gambar 4.1.
Gambar 4.1 Rata-rata volume urin terhadap waktu setiap jam selama 5 jam 0 0,5 1 1,5 2 2,5 3 3,5
0 1 2 3 4 5
R at a -r at a V o lu m e U r in t ia p j a m ( m l) Waktu (jam)
[image:44.595.128.527.520.732.2]Pada Tabel 4.3 dan Gambar 4.1 menunjukkan bahwa semua sediaan uji dan kelompok pembanding sudah menunjukkan efek diuretik. Kelompok pembanding furosemid menunjukkan rata-rata volume urin tiap jam paling tinggi dibandingkan dengan kelompok dosis ekstrak. Menurut Khan (2005), furosemid memiliki waktu paruh yang singkat (15 menit) dengan onset 1-2 jam setelah pemberian secara peroral serta durasi 2-6 jam. EnHPK dosis 100 dan 200 mg/kg bb pada jam ke-1 belum terlihat adanya peningkatan volume urin, tetapi pada jam ke-2 hingga jam ke-5 volume urin meningkat. Volume urin EnHPK dosis 100 dan 200 mg/kg bb lebih rendah dari furosemid dan EnHPK dosis 150 mg/kg bb tetapi lebih tinggi dari Na-CMC 0,5%. Peningkatan volume urin EnHPK dosis 150 mg/kg bb sudah terlihat mulai dari jam ke-1 dan terus meningkat hingga jam ke-5. Volume urin EnHPK dosis 150 mg/kg bb lebih tinggi dari Na-CMC 0,5% dan EnHPK dosis 100, 200 mg/kg bb tetapi lebih rendah dari furosemid. Pemberian ekstrak dosis 100, 150, dan 200 mg/kg bb mengalami peningkatan volume urin yang disebabkan karena adanya kandungan alkaloid dan steroid yang berperan dalam meningkatkan volume urin (diuresis).
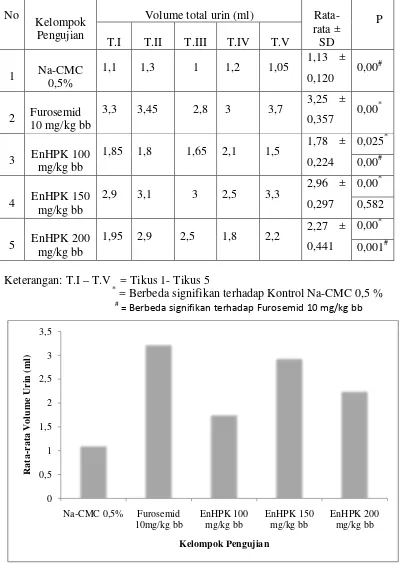
Tabel 4.4 Hasil pengukuran volume total urin tikus pada kelompok uji
No
Kelompok Pengujian
Volume total urin (ml) Rata-rata ±
SD
P T.I T.II T.III T.IV T.V
1 Na-CMC 0,5%
1,1 1,3 1 1,2 1,05 1,13 ± 0,120 0,00
#
2 Furosemid 10 mg/kg bb
3,3 3,45 2,8 3 3,7 3,25 ±
0,357 0,00
*
3 EnHPK 100 mg/kg bb
1,85 1,8 1,65 2,1 1,5 1,78 ± 0,224
0,025* 0,00#
4 EnHPK 150 mg/kg bb
2,9 3,1 3 2,5 3,3 2,96 ± 0,297
0,00* 0,582
5 EnHPK 200 mg/kg bb
1,95 2,9 2,5 1,8 2,2 2,27 ±
0,441
0,00* 0,001#
Keterangan: T.I – T.V = Tikus 1- Tikus 5
*
= Berbeda signifikan terhadap Kontrol Na-CMC 0,5 %
#
= Berbeda signifikan terhadap Furosemid 10 mg/kg bb
Gambar 4.2 Volume total urin pada tikus putih jantan
Pada Tabel 4.4 dan Gambar 4.2 dapat dilihat bahwa rata-rata volume total urin untuk Na-CMC 1,13 ± 0,120 ml, furosemid 3,25 ± 0,357 ml, EnHPK dosis
0 0,5 1 1,5 2 2,5 3 3,5
[image:46.595.109.512.117.685.2]100 mg/kg bb 1,78 ± 0,224 ml, EnHPK dosis 150 mg/kg bb 2,96 ± 0,297 ml, EnHPK dosis 200 mg/kg bb 2,27 ± 0,441 ml.
Berdasarkan hasil yang diperoleh, EnHPK dengan dosis 100 mg/kg bb, 150 mg/kg bb, dan 200 mg/kg bb menunjukkan efek diuretik terhadap volume total urin. Hasil analisis secara statistik menunjukkan bahwa terdapat perbedaan yang signifikan volume total urin antara kelompok Na-CMC 0,5% dengan kelompok EnHPK dosis 100 mg/kg bb dengan nilai signifikansi 0,025 (p < 0,05), kelompok EnHPK dosis 150 mg/kg bb dengan nilai signifikansi 0,00 (p < 0,05), dan kelompok EnHPK dosis 200 mg/kg bb dengan nilai signifikansi 0,00 (p < 0,05).
Hasil statistik juga menunjukkan bahwa terdapat perbedaan yang signifikan volume total urin kelompok furosemid dengan kelompok EnHPK dosis 100 mg/kg bb dengan nilai signifikansi 0,00 (p < 0,05) dan kelompok EnHPK dosis 200 mg/kg bb dengan nilai signifikansi 0,01 (p < 0,05), tetapi tidak terdapat perbedaan yang signifikan dengan kelompok EnHPK dosis 150 mg/kg bb dengan nilai signifikansi 0,582 (p > 0,05), dengan demikian dapat disimpulkan bahwa EnHPK dengan dosis 150 mg/kg bb mempunyai efek diuretik yang paling baik terhadap volume total urin. Peningkatan pemberian dosis EnHPK dapat meningkatkan pengeluaran volume urin terhadap tikus putih jantan.
4.4.2 pH Urin
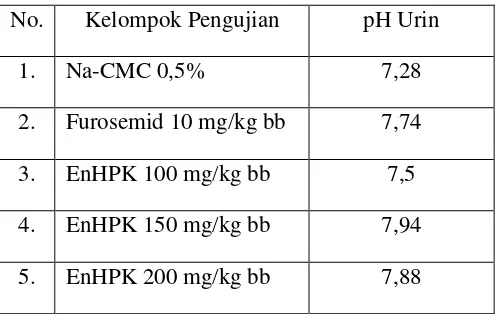
[image:48.595.143.391.160.320.2]Hasil pengujian terhadap pH urin terlihat pada Tabel 4.5. Tabel 4.5 Hasil penetapan pH Urin
No. Kelompok Pengujian pH Urin
1. Na-CMC 0,5% 7,28
2. Furosemid 10 mg/kg bb 7,74
3. EnHPK 100 mg/kg bb 7,5
4. EnHPK 150 mg/kg bb 7,94
5. EnHPK 200 mg/kg bb 7,88
Berdasarkan hasil pengukuran pH urin tikus putih setelah pemberian perlakuan ternyata relatif normal, yaitu berkisar antara 7,0 – 8,0. Menurut Gandasoebrata (1992), batas-batas normal pH urin adalah berkisar 4,6 – 8,5, hasil pengukuran yang cenderung basa dapat disebabkan urin menjadi bersifat lebih alkali setelah dibiarkan selama 5 jam karena urea akan berubah menjadi ammonia dan akan kehilangan CO. Derajat keasaman (pH) menyatakan konsentrasi ion hidrogen (H+) yang berhubungan dengan pengaturan keseimbangan asam dan basa
di dalam cairan tubuh. Guyton (1997) mengemukakan bahwa pengaturan keseimbangan asam-basa berhubungan dengan pengaturan konsentrasi ion H+ di
dalam cairan tubuh. Apabila konsentrasi H+berubah dari normal, maka ginjal akan
mengekskresikan urin yang asam/ basa, dengan demikian juga dapat membantu menyesuaikan konsentrasi ion H+cairan tubuh kembali normal.
4.4.3 Hasil kadar natrium
tubuh secara keseluruhan. Natrium adalah kation utama dalam darah dan cairan ekstraseluler. Elektrolit natrium ini akan membantu pengeluaran air seni yang disebut efek diuresis (Rasyid, 2011).
[image:49.595.107.514.330.611.2]Dari pengukuran kurva kalibrasi untuk natrium diperoleh persamaaan garis regresi yaitu Y = 0,141474X – 0,00269 dengan nilai r = 0,9998. Hal ini menunjukkan adanya korelasi linier yang menyatakan adanya hubungan antara X (konsentrasi) dan Y (absorbansi). Hasil pengukuran kadar natrium dapat dilihat pada Tabel 4.6 dan Gambar 4.3.
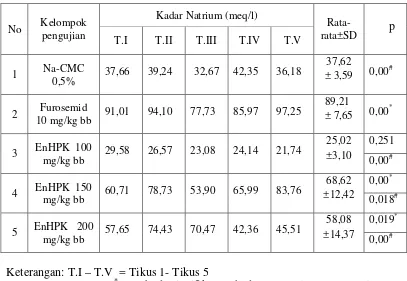
Tabel 4.6 Kadar natrium dalam urin tikus pada kelompok uji
No Kelompok pengujian
Kadar Natrium (meq/l)
Rata-rata±SD p T.I T.II T.III T.IV T.V
1 Na-CMC
0,5% 37,66 39,24 32,67 42,35 36,18
37,62
± 3,59 0,00 #
2 Furosemid
10 mg/kg bb 91,01 94,10 77,73 85,97 97,25
89,21
± 7,65 0,00 *
3 EnHPK 100
mg/kg bb 29,58 26,57 23,08 24,14 21,74
25,02 ±3,10
0,251
0,00#
4 EnHPK 150
mg/kg bb 60,71 78,73 53,90 65,99 83,76
68,62 ±12,42
0,00*
0,018#
5 EnHPK 200
mg/kg bb 57,65 74,43 70,47 42,36 45,51
58,08 ±14,37
0,019*
0,00#
Keterangan: T.I – T.V = Tikus 1- Tikus 5
*
= Berbeda signifikan terhadap Kontrol Na-CMC 0,5%
#
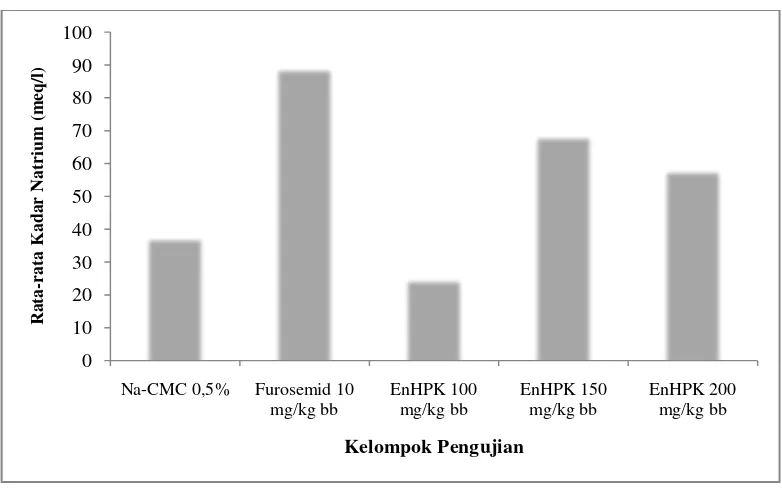
Gambar 4.3 Kadar natrium pada urin tikus putih jantan
Pada Tabel 4.6 dan Gambar 4.3 dapat dilihat bahwa dari hasil rata-rata yang diperoleh untuk Na-CMC 0,5% 37,62 ± 3,59 meq/l; furosemid dosis 10 mg/kg bb 89,21 ± 7,65 meq/l, EnHPK dosis 100 mg/kg bb 25,02 ± 3,10 meq/l, EnHPK dosis 150 mg/kg bb 68,62 ± 12,42 meq/l, dan EnHPK dosis 200 mg/kg bb 58,08 ± 14,37 meq/l.
Berdasarkan hasil yang diperoleh, EnHPK dengan dosis 100 mg/kg bb, 150 mg/kg bb, dan 200 mg/kg bb menunjukkan efek diuretik terhadap pengeluaran kadar natrium. Hasil analisis secara statistik menunjukkan bahwa tidak terdapat perbedaan yang signifikan pengeluaran kadar natrium antara kelompok Na-CMC 0,5% dengan kelompok EnHPK dosis 100 mg/kg bb dengan nilai signifikansi 0,251 (p > 0,05), tetapi terdapat perbedaan yang signifikan dengan kelompok EnHPK dosis 150 mg/kg bb dengan nilai signifikansi 0,00 (p < 0,05) dan kelompok EnHPK dosis 200 mg/kg bb dengan nilai signifikansi 0,019 (p < 0,05).
0 10 20 30 40 50 60 70 80 90 100
Hasil statistik juga menunjukkan bahwa terdapat perbedaan yang signifikan pengeluaran kadar natrium kelompok furosemid dengan kelompok EnHPK dosis 100 mg/kg bb dengan nilai signifikansi 0,00 (p < 0,05), kelompok EnHPK dosis 150 mg/kg bb dengan nilai signifikansi 0,018 (p < 0,05) dan kelompok EnHPK dosis 200 mg/kg bb dengan nilai signifikansi 0,00 (p < 0,05). Pemberian dosis EnHPK dapat meningkatkan pengeluaran kadar natrium terhadap tikus putih jantan. Peningkatan pengeluaran natrium dalam urin mengindikasikan adanya efek diuretik yang dihasilkan dari ekstrak tumbuhan pecut kuda.
4.4.4 Hasil kadar kalium
Kalium merupakan salah satu mineral makro yang berperan dalam pengaturan keseimbangan cairan tubuh. Masukan natrium yang tinggi dapat meningkatkan ekskresi kalium. Hubungan ini diperkirakan disebabkan sebagian oleh reabsorbsi kalium secara pasif mengikuti natrium dan air pada tubulus proksimal dan sepanjang lengkung Henle.
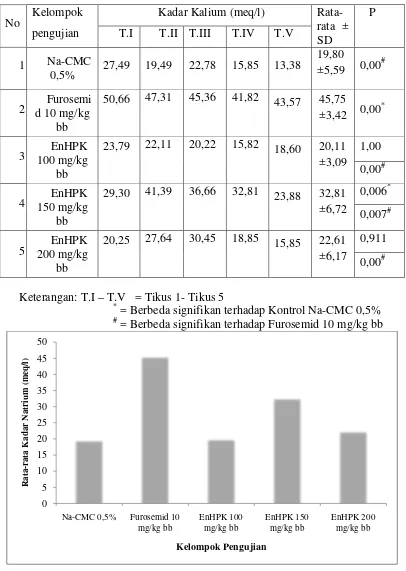
Tabel 4.7 Kadar kalium dalam urin tikus pada kelompok uji
No Kelompok pengujian
Kadar Kalium (meq/l) Rata-rata ± SD
P T.I T.II T.III T.IV T.V
1 Na-CMC
0,5% 27,49 19,49 22,78 15,85 13,38
19,80
±5,59 0,00
#
2 d 10 mg/kg Furosemi bb
50,66 47,31 45,36 41,82 43,57 45,75 ±3,42 0,00
*
3 100 mg/kg EnHPK bb
23,79 22,11 20,22 15,82 18,60 20,11 ±3,09
1,00 0,00#
4 150 mg/kg EnHPK bb
29,30 41,39 36,66 32,81 23,88 32,81 ±6,72
0,006* 0,007#
5 200 mg/kg EnHPK bb
20,25 27,64 30,45 18,85 15,85 22,61 ±6,17
0,911 0,00#
Keterangan: T.I – T.V = Tikus 1- Tikus 5
* = Berbeda signifikan terhadap Kontrol Na-CMC 0,5%
#
= Berbeda signifikan terhadap Furosemid 10 mg/kg bb
Gambar 4.4 Kadar kalium pada urin tikus putih jantan
Pada Tabel 4.7 dan Gambar 4.4 dapat dilihat bahwa dari perolehan hasil rata-rata kadar kalium untuk Na-CMC 0,5% 19,80 ± 5,59 meq/l, furosemid 10 mg/kg
0 5 10 15 20 25 30 35 40 45 50
bb 45,74 ± 3,42 meq/l, EnHPK dosis 100 mg/kg bb 20,10 ± 3,08 meq/l, EnHPK dosis 150 mg/kg bb 32,81 ± 6,72 meq/l, EnHPK dosis 200 mg/kg bb 22,61 ± 6,17 meq/l.
Berdasarkan hasil yang diperoleh, EnHPK dengan dosis 100 mg/kg bb, 150 mg/kg bb, dan 200 mg/kg bb menunjukkan efek diuretik terhadap pengeluaran kadar kalium. Dari ketiga dosis tersebut, EnHPK dosis 150 mg/kg bb mempunyai efek pengeluaran kalium yang lebih tinggi dibandingkan dengan dosis 100 dan 200 mg/kg bb. Hasil analisis secara statistik menunjukkan bahwa terdapat perbedaan yang signifikan pengeluaran kadar kalium antara kelompok Na-CMC 0,5% dengan kelompok EnHPK dosis 150 mg/kg bb dengan nilai signifikansi 0,006 (p < 0,05), tetapi tidak terdapat perbedaan dengan kelompok EnHPK dosis 100 mg/kg bb dengan nilai signifikansi 1,00 (p > 0,05) dan kelompok EnHPK dosis 200 mg/kg bb dengan nilai signifikansi 0,911 (p > 0,05).
Hasil statistik juga menunjukkan bahwa terdapat perbedaan yang signifikan pengeluaran kadar kalium kelompok furosemid dengan kelompok EnHPK dosis 100 mg/kg bb dengan nilai signifikansi 0,00 (p < 0,05), kelompok EnHPK dosis 150 mg/kg bb dengan nilai signifikansi 0,007 (p < 0,05) dan kelompok EnHPK dosis 200 mg/kg bb dengan nilai signifikansi 0,00 (p < 0,05).
meningkatkan respon yang sebanding dengan dosis yang ditingkatkan, namun dengan peningkatan dosis, peningkatan respon akhirnya akan menurun. Hal ini dapat terjadi pada obat bahan alam karena senyawa yang dikandungnya tidak tunggal melainkan terdiri dari berbagai senyawa kimia. EnHPK dosis 200 mg/kg bb kurang efektif sebagai diuretik dibandingkan dengan EnHPK dosis 150 mg/kg bb. EnHPK 200 mg/kg bb merupakan konsentrasi ekstrak yang paling tinggi, sehingga memungkinkan peningkatan jumlah zat aktif yang bersifat antagonis terhadap zat aktif EnHPK yang berkhasiat sebagai diuretik.
BAB V
KESIMPULAN DAN SARAN
5.1 Kesimpulan
Berdasarkan penelitian ini dapat disimpulkan bahwa:
a. pelarut n-heksan dapat menarik senyawa kimia tumbuhan yang merangsang pengeluaran urin yaitu senyawa golongan alkaloid dan steroid/triterpenoid. b. ekstrak n-heksan pecut kuda mempunyai aktivitas diuretik dengan
meningkatnya volume urin, kadar natrium dan kadar kalium dalam urin tikus putih jantan.
5.2 Saran
BAB II
TINJAUAN PUSTAKA
2.1 Uraian Tumbuhan
Pecut kuda tumbuh liar di tepi jalan, tanah lapang dan tempat-tempat terlantar lainnya. Tanaman yang berasal dari Amerika ini dapat ditemukan di daerah cerah, sedang, terlindung dari sinar matahari dan pada ketinggian 1-1500 m dpl. Pecut kuda merupakan terna tahunan, tumbuh tegak, tinggi ± 50 cm, tumbuh liar di sisi jalan daerah pinggir kota, tanah kosong yang tidak terawat. Daun letak berhadapan, bentuk bulat telur, tepi bergerigi, tidak berambut. Bunga duduk tanpa tangkai pada bulir-bulir yang berbentuk pecut, panjang 4-20 cm, bunga mekar tidak berbarengan, kecil-kecil, berwarna ungu dan putih (Dalimartha, 2000).
2.1.1 Sistematika Tumbuhan
Kedudukan kategori taksa untuk jenis pecut kuda di dalam sistematika tumbuhan adalah sebagai berikut (Ditjend, POM., 2000):
Divisi : Spermatophyta Sub divisi : Angiospermae Class : Dicotyledoneae
Ordo : Lamiales
Famili : Verbenaceae
Genus : Stachytarpheta
Spesies : Stachytarpheta jamaicensis (L.) Vahl
2.1.2 Sinonim
2.1.3 Nama Lokal
Jawa: jarong (Sunda), biron, karomenal, sekar laru, ngadirenggo (Jawa) (Dalimartha, 2000).
2.1.4 Nama Asing
Yu long bian (Cina), Snakeweed (Inggris) (Dalimartha, 2000). 2.1.5 Kandungan Kimia
Pecut kuda mengandung glikosida, flavonoid dan alkaloid (Dalimartha, 2000).
2.1.6 Khasiat Tumbuhan
Herba pecut kuda (Stachytarpheta jamaicensis (L.) Vahl) digunakan sebagai obat infeksi dan batu saluran kemih, rematik, sakit tenggorokan, pembersih darah, haid tidak teratur, keputihan, hepatitis A. Bunga dan tangkainya untuk pengobatan radang hati sedangkan akarnya untuk pengobatan keputihan (Dalimartha, 2000).
2.2 Metode Ekstraksi
Ekstrak adalah sediaan pekat yang diperoleh dengan mengekstraksi zat aktif dari simplisia nabati atau hewani menggunakan pelarut yang sesuai, kemudian semua atau hampir semua pelarut diuapkan (Ditjend, POM., 2000). Ekstrak adalah sediaan kering, kental atau cair dibuat dengan menyari simplisia nabati atau hewani menurut cara yang sesuai, diluar pengaruh cahaya matahari langsung (BPOM, 2012).
digolongkan ke dalam golongan minyak atsiri, alkaloid, flavonoid dan lain-lain (Ditjend, POM., 2000). Tujuan utama ekstraksi adalah untuk mendapatkan atau memisahkan sebanyak mungkin zat-zat yang memiliki khasiat pengobatan (Syamsuni, 2006).
Metode ekstraksi yang umum digunakan antara lain yaitu: a. Maserasi
Maserasi adalah proses penyarian simplisia menggunakan pelarut dengan beberapa kali pengocokan atau pengadukan pada temperatur ruangan, sedangkan remaserasi merupakan pengulangan penambahan pelarut setelah dilakukan penyaringan maserat pertama, dan seterusnya (Ditjend, POM., 2000).
b. Perkolasi
Perkolasi adalah proses penyarian simplisia dengan pelarut yang selalu baru sampai sempurna yang umumnya dilakukan pada temperatur ruangan. Serbuk simplisia yang akan diperkolasi tidak langsung dimasukkan kedalam bejana perkolator, tetapi dibasahi atau dimaserasi terlebih dahulu dengan cairan penyari sekurang-kurangnya selama 3 jam (Ditjend, POM., 2000).
c. Refluks
Refluks adalah proses penyarian simplisia dengan menggunakan alat pada temperatur titik didihnya dalam waktu tertentu dimana pelarut akan terkondensasi menuju pendingin dan kembali ke labu (Ditjend, POM., 2000).
d. Sokletasi
terkondensasi dari labu menuju pendingin, kemudian jatuh membasahi sampel (Ditjend, POM., 2000).
e. Digesti
Digesti adalah proses penyarian dengan pengadukan kontinu pada temperatur lebih tinggi dari temperatur kamar, yaitu secara umum dilakukan pada temperatur 40-50°C (Ditjend, POM., 2000).
f. Infundasi
Infundasi adalah proses penyarian dengan menggunakan pelarut air pada temperatur 90°C selama 15 menit (Ditjend, POM., 2000).
g. Dekoktasi
Dekoktasi adalah proses penyarian dengan menggunakan pelarut air pada temperatur 90°C selama 30 menit (Ditjend, POM., 2000).
2.3 Ginjal
Ginjal merupakan organ utama untuk membuang produk sisa metabolisme yang tidak diperlukan tubuh. Peran penting ginjal adalah membuang sisa metabolit tubuh dari hasil pencernaan dan fungsi lainnya mengontrol volume dan komposisi cairan tubuh. Fungsi pengaturan ginjal ini untuk memelihara kestabilan lingkungan sel-sel yang diperlukan untuk melakukan berbagai aktivitas (Guyton dan Hall, 1997).
asam urat dan ion-ion natrium, kalium, klorida serta ion-ion hidrogen dalam jumlah yang berlebihan (Guyton, 1997).
2.4 Diuretik
Dalam istilah diuresis ada dua pengertian yaitu adanya penambahan volume urin dan pengeluaran keseluruhan dari pada zat terlarut dalam air. Kegunaan terpenting diuretik adalah untuk memobilisasi air dan elektrolit dalam tubuh. Indikasi utama diuretik adalah pada edema akut/kronis, hipertensi dan insufisiensi jantung. Tempat kerja diuretik umumnya terletak pada sepanjang nefron yaitu pada tubulus proksimal, jerat henle, tubulus distal atau pada tubulus penampung. Nefron merupakan suatu kesatuan fungsional yang membentuk ginjal. Mengetahui tempat kerja diuretik sangat bermanfaat karena yang menentukan potensi kerja dan efek samping diuretik adalah tempat kerja.
Diuretik selain memperbanyak pengeluaran air juga dapat menambah pengeluaran elektrolit. Maka diuretik dapat menyebabkan gangguan keseimbangan elektrolit dan air. Secara umum diuretik dapat dibagi menjadi dua golongan besar yaitu diuretik osmotik dan penghambat transport elektrolit di tubuli ginjal (Ganong, 2002).
Penggolongan diuretik berdasarkan tempat dan mekanisme kerja menurut Nafrialdi (2007) antara lain:
a. Diuretik kuat
etakrinat. Waktu paruh diuretik kuat umumnya pendek sehingga diperlukan pemberian 2 atau 3 kali sehari. Efek samping diuretik kuat yaitu menimbulkan hiperkalsiuria dan menurunkan kalsium darah.
b. Diuretik tiazid
Diuretik tiazid bekerja menghambat simporter Na+ dan Cl- di hulu tubulus distal sehingga meningkatkan ekskresi natrium, klorida dan sejumlah air. Laju ekskresi natrium yang ditimbulkan oleh tiazid lebih rendah dibandingkan dengan diuretik lain. Beberapa obat yang termasuk golongan tiazid antara lain hidroklorotiazid, bendroflumetiazid dan klorotiazid.
c. Diuretik hemat kalium
Diuretik hemat kalium bekerja di hilir tubulus distal dan duktus koligentes dengan menghambat reabsorpsi natrium dan sekresi kalium sehingga ekskresi natrium meningkat sedangkan ekskresi kalium berkurang. Yang termasuk golongan diuretik hemat kalium ialah antagonis aldosteron, triamteren dan amilorid.
d. Diuretik osmotik
Mekanisme kerja diuretik osmotik adalah menghambat reabsorpsi natrium dan air dengan meningkatkan tekanan osmotik sehingga jumlah air dan elektrolit yang diekskresi bertambah. Diuretik osmotik bekerja di tubulus proksimal dan ansa henle desenden tipis. Contoh golongan obat ini adalah manitol, urea, gliserin dan isosorbid.
e. Penghambat karbonik anhidrase
sehingga pembentukan HCO3- dan H+ berkurang. Jumlah H+ yang disekresi dan
ditukarkan dengan Na+ juga berkurang sehingga ekskresi Na+ meningkat. HCO3
-yang tidak digabung dengan H+ akan diekskresi ke urin dan mengakibatkan meningkatnya ekskresi bikarbonat, natrium dan kalium melalui urin. Bertambahnya ekskresi kalium disebabkan pertukaran Na+ dan K+ lebih aktif, menggantikan pertukaran dengan H+. meningkatnya ekskresi elektrolit menyebabkan bertambahnya ekskresi air.
2.5 Mekanisme Pembentukan Urin
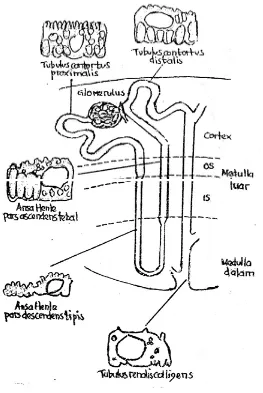
Gambar 2.1 Diagram nefron yang membentuk jukstamedularis (Ganong, 2002)
[image:63.595.118.381.96.489.2]spesifik yang kembali ke dalam darah atau oleh sekresi zat-zat lain dari kapiler peritubulus ke dalam tubulus (Guyton dan Hall, 1997).
Filtrat hasil dari glomerolus saat memasuki tubulus ginjal akan melalui bagian-bagian tubulus sebagai berikut; tubulus proksimal, ansa Henle, tubulus distal, tubulus kolingentes, dan duktus kolingentes, sebelum akhirnya dieksresikan sebagai urin. Di sepanjang perjalanannya, beberapa zat direabsorbsi kembali secara selektif dari tubulus dan kembali ke dalam darah, sedangkan yang lain disekresikan dari darah ke dalam lumen tubulus. Hasil dari urin yang terbentuk dan semua zat yang terdapat dalam urin akan menggambarkan penjumlahan dari tiga proses dasar ginjal; filtrasi glomerolus, reabsorbsi tubulus, dan sekresi tubulus. Kecepatan ekskresi urin suatu zat sama dengan laju dimana zat tersebut difiltrasi dikurangi laju reabsorbsinya ditambah laju dimana zat tersebut diekskresi dari kapiler peritubular darah ke dalam tubulus (Guyton dan Hall, 1997).
2.6 Furosemid
Furosemid adalah turunan sulfonamida yang berdaya diuretik kuat dan bertitik kerja di lengkung Henle bagian menaik. Sangat efektif pada keadaan udema di otak dan paru – paru yang akut.
Kelarutan praktis tidak larut dalam air dan dalam kloroform, larut dalam 75 bagian etanol (95%) dan dalam 850 bagian eter, larut dalam larutan alkali hidroksida (Depkes, RI., 1979).
Efek sampingnya secara umum, pada injeksi i.v terlalu cepat dan terjadi ketulian (reversibel) dan hipotensi, hipokalemia reversibel dapat terjadi pula. Dosis pada udema: oral 40 – 80 mg pagi p.c., jika perlu atau insufisiensi ginjal jarang s