AN
KAL
TO
S
DiaPR
NALISIS
LSIUM,
OMAT (
SPEKTR
ajukan untu gelarROGRA
UNIV
S KANDU
NATRI
(Solanum
ROFOTO
uk melengk r Sarjana F UnivePIN
N
AM EKS
FAKU
VERSITA
UNGAN
IUM DA
m lycoper
OMETR
SKRIP
kapi salah s Farmasi pa ersitas Sum
OLEH
NGSI HA
NIM 0815
STENSI S
ULTAS F
AS SUM
MEDA
2013
N MINER
AN MAG
rsicum M
RI SERA
PSI
satu syarat ada Fakulta matera UtarH:
ARLINA
524005
SARJAN
FARMA
MATERA
AN
3
RAL KA
GNESIUM
Mill.) SE
APAN AT
AN
KAL
TO
S
DiaPR
NALISIS
LSIUM,
OMAT(S
SPEKTR
ajukan untu gelarROGRA
UNIV
S KANDU
NATRI
Solanum
ROFOTO
uk melengk r Sarjana F UnivePIN
N
AM EKS
FAKU
VERSITA
UNGAN
IUM DA
m lycoper
OMETR
SKRIP
kapi salah s Farmasi pa ersitas Sum
OLEH
NGSI HA
NIM 0815
STENSI S
ULTAS F
AS SUM
MEDA
2013
N MINER
AN MAG
rsicum M
RI SERA
PSI
satu syarat ada Fakulta matera UtarH:
ARLINA
524005
SARJAN
FARMA
MATERA
AN
3
RAL KA
GNESIUM
Mill.) SEC
APAN AT
PENGESAHAN SKRIPSI
ANALISIS KANDUNGAN MINERAL KALIUM,
KALSIUM, NATRIUM DAN MAGNESIUM PADA
TOMAT (Solanum lycopersicum Mill.) SECARA
SPEKTROFOTOMETRI SERAPAN ATOM
OLEH: PINGSI HARLINA
NIM 081524005
Dipertahankan di Hadapan Panitia Penguji Skripsi Fakultas Farmasi Universitas Sumatera Utara
Pada Tanggal: 26 Oktober 2013 Disetujui Oleh:
Pembimbing I, Panitia Penguji,
Drs. Ismail, M.Si., Apt. Dr. Ginda Haro, M.Sc., Apt. NIP 195006141980031001 NIP 195108161980031002
Pembimbing II
Drs. Ismail, M.Si., Apt. NIP 195006141980031001 Dr. Muchlisyam, M.Si., Apt.
NIP 195006221980021001 Drs. Syahrial Yoenoes, S.U., Apt. NIP 195112061983031001
Drs. Immanuel S. Meliala, M.Si., Apt. NIP 195001261983031002
Medan, November 2013 Fakultas Farmasi
Universitas Sumatera Utara Dekan,
KATA PENGANTAR
Alhamdulillah, penulis haturkan ke hadirat Allah Yang Maha Kuasa yang telah melimpahkan rahmat, hidayah dan kemudahan kepada penulis sehingga dapat menyelesaikan penelitian dan penulisan skripsi ini.
Skripsi ini disusun untuk melengkapi salah satu syarat mencapai gelar Sarjana Farmasi pada Fakultas Farmasi Universitas Sumatera Utara, dengan judul Analisis Kandungan Mineral Kalium, Kalsium, Natrium, dan Magnesium Pada Tomat (Solanum lycopersicum Mill.) Secara Spektrofotometri Serapan Atom.
Apt., selaku Koordinator Laboratorium Penelitian Fakultas Farmasi USU yang telah memberikan izin dan fasilitas untuk penulis sehingga dapat mengerjakan dan menyelesaikan penelitian.
Penulis juga mengucapkan terima kasih dan penghargaan yang tiada terhingga kepada Ayahanda H. Yushar, M.Pd., Ibunda Hj. Amrina, Ama.Pd., suamiku Irwan Saputra, S.E., dan anakkku Mazaya Rinjani Irwan serta saudaraku Aprian Doni Faizal, S.E., Risda Nursah, S.E., Yessy Sistriana, S.Sos., Muhammad Fikri, S.Ked., yang telah memberikan cinta kasih yang tidak ternilai dengan apapun, doa yang tulus serta pengorbanan baik materi maupun non-materi. atas segala doa, kasih sayang, dan memberikan semangat. Buat sahabatku Lisa Helmita, S.Farm., Apt., dan Teman-Teman Ekstensi Farmasi USU 2008, terima kasih untuk perhatian, semangat, doa, dan kebersamaannya selama ini, serta seluruh pihak yang telah ikut membantu penulis yang tidak dapat disebutkan satu persatu.
Penulis menyadari sepenuhnya bahwa dalam penulisan skripsi ini masih jauh dari kesempurnaan, oleh karena itu penulis menerima kritik dan saran demi kesempurnaan skripsi ini. Akhirnya, penulis berharap semoga skripsi ini dapat memberi manfaat bagi kita semua.
Medan, November 2013 Penulis
ANALISIS KANDUNGAN MINERAL KALIUM, KALSIUM, NATRIUM, DAN MAGNESIUM PADA TOMAT (Solanum lycopersicum Mill.)
SECARA SPEKTROFOTOMETRI SERAPAN ATOM
ABSTRAK
Tomat merupakan tanaman yang dapat tumbuh dilahan perkebunan dan dipekarangan. Tanaman ini sangat bermanfaat bagi tubuh karena mengandung vitamin dan mineral yang diperlukan untuk pertumbuhan dan kesehatan. Tanaman ini mengandung mineral antara lain kalium, kalsium, natrium, dan magnesium. Tujuan penelitian ini untuk mengetahui kadar mineral kalium, kalsium, natrium, dan magnesium pada tomat (Solanum lycopersicum Mill.).
Metode penelitian yang dilakukan secara destruksi kering terhadap tomat plum dan penetapan kadar mineral kalium, kalsium, natrium, dan magnesium dilakukan dengan menggunakan spektrofotometer serapan atom dengan panjang gelombang 766,50 nm untuk kalium, pada panjang gelombang 422,7 nm untuk kalsium pada panjang gelombang 589,00 nm untuk natrium, dan pada panjang gelombang 285,20 nm untuk magnesium.
Dari hasil penelitian dapat disimpulkan bahwa tomat plum menunjukkan hasil positif untuk uji kualitatif dan mengandung mineral dengan kadar (263,67 ± 3,0418) mg/100 g untuk kalium; (25,0842 ± 0,4556) mg/100 g untuk kalsium; (8,4679 ± 0,1777) mg/100 g untuk natrium dan (13,1182 ± 0,6364) mg/100 g untuk magnesium.
Kata kunci: Tomat (Solanum lycopersicum Mill.), Kalium (K), Kalsium (Ca)
Natrium (Na), Magnesium (Mg), Spektrofotometer Serapan Atom.
THE ANALYSIS OF MINERALS CONTENT OF POTASSIUM, CALCIUM SODIUM, AND MAGNESIUM IN TOMATO(Solanum
lycopersicum Mill.) BY ATOMIC ABSORPTION
SPECTROPHOTOMETRY
ABSTRACT
Tomato is a plant that can grow in plantation and kitchen garden. This plant is very beneficial for the body because it contains vitamins and minerals needed for growth and health. It contains minerals such as potassium, calcium, sodium, and magnesium. The purpose of this study is to determine the mineral content of potassium, calcium, sodium, and magnesium in tomato (Solanum lycopersicum Mill.).
This research was by using the with dry destruction of plum tomato and the determination of potassium, calcium, sodium, and magnesium were by using the atomic absorption spectrophotometer with 766.50 nm for potassium, 422.7 nm for calcium, 589.00 nm for sodium, and 285.20 nm for magnesium.
Of the results of this research conclude that the plum tomato in a test by qualitative reactions showed positive and containing minerals with high levels of (263.67 ± 3.0418) mg/100 g for potassium; (25.0842 ± 0.4556) mg/100 g for calcium; (8.4679 ± 0.1777) mg/100 g for sodium and (13.1182 ± 0.6364) mg/100 g for magnesium.
Key word: Tomato (Solanum lycopersicum Mill.), Potassium (K), Calcium (Ca), Sodium (Na), Magnesium (Mg), Atomic Absorption Spectrophoto
DAFTAR ISI
Halaman
JUDUL ... i
HALAMAN PENGESAHAN ... iii
KATA PENGANTAR ... iv
ABSTRAK ... vi
ABSTRACT ... vii
DAFTAR ISI ... viii
DAFTAR TABEL ... xii
DAFTAR GAMBAR ... xiii
DAFTAR LAMPIRAN ... xiv
BAB I PENDAHULUAN ... 1
1.1 Latar Belakang ... 1
1.2 Perumusan Masalah ... 2
1.3 Hipotesis ... 2
1.4 Tujuan Penelitian ... 3
1.5 Manfaat Penelitian ... 3
BAB II TINJAUAN PUSTAKA ... 4
2.1 Uraian Sampel ... 4
2.1.1 Tomat (Solanum lycopersicum Mill.) ... 4
2.1.2 Deskripsi Tanaman Tomat ... 5
2.1.3 Kandungan Gizi Tomat ... 5
2.2.1 Kalium ... . 6
2.2.2 Kalsium ... 7
2.2.3 Natrium ... 7
2.2.4 Magnesium ... 7
2.3 Spektrofotometri Serapan Atom ... 8
2.4 Validasi Metode Analisis ... 12
BAB III METODE PENELITIAN ... 15
3.1 Tempat dan Waktu Penelitian ... 15
3.2 Bahan-Bahan ... 15
3.2.1 Sampel ... 15
3.2.2 Pereaksi ... 15
3.3 Alat-Alat ... 15
3.4 Pembuatan Pereaksi ... 16
3.4.1 Larutan Asam Pikrat 1% b/v ... 16
3.4.2 Larutan Kuning Titan 0,1% b/v ... 16
3.4.3 Larutan Natrium Hidroksida 2 N ... 16
3.4.4 Larutan Asam Nitrat 5 N ... 16
3.4.5 Larutan Asam Sulfat 1 N ... 16
3.5 Prosedur Penelitian ... 16
3.5.1 Pengambilan Sampel ... 16
3.5.2 Penyiapan Sampel ... 17
3.5.3 Proses Destruksi Kering ... 17
3.5.4 Pembuatan Larutan Sampel ... 17
3.5.5.1 Kalium ... 18
3.5.5.1.1 Uji Nyala Ni/Cr ... 18
3.5.5.1.2 Uji Kristal Kalium Dengan Larutan Asam Pikrat ... 18
3.5.5.2 Kalsium ... 18
3.5.5.2.1 Uji Nyala Ni/Cr ... 18
3.5.5.2.2 Uji Kristal Kalsium Dengan Larutan Asam Sulfat ... 19
3.5.5.3 Natrium ... 19
3.5.5.3.1 Uji Nyala Ni/Cr ... 19
3.5.5.3.2 Uji Kristal Natrium Dengan larutan Asam Pikrat ... 19
3.5.5.4 Magnesium ... 19
3.5.5.4.1 Reaksi Kualitatif Dengan Larutan Kuning Titan 0,1% b/v ... 19
3.5.6 Analisis Kuantitatif ... 20
3.5.6.1 Pembuatan Kurva Kalibrasi ... 20
3.5.6.1.1 Pembuatan Kurva Kalibrasi Kalium ... 20
3.5.6.1.2 Pembuatan Kurva Kalibrasi Kalsium .. 20
3.5.6.1.4 Pembuatan Kurva Kalibrasi Natrium . 21
3.5.6.1.3 Pembuatan Kurva Kalibrasi Magnesium ... 21
3.5.6.2 Penetapan Kadar Mineral dalam Sampel ... 22
3.5.6.2.1 Penetapan Kadar Kalium ... 22
3.5.6.2.2 Penetapan Kadar Kalsium ... 22
3.5.6.2.3 Penetapan Kadar Natrium ... 22
3.5.6.3 Perhitungan Kadar Kalium, Kalsium, Natrium,
Dan Magnesium Dalam Sampel ... 23
3.5.7 Analisis Data Secara Statistik ... 24
3.5.7.1 Penolakan Hasil Pengamatan ... 24
3.5.8 Validasi Metode Analisis ... 25
3.5.8.1 Uji Perolehan Kembali (Recovery) ... 25
3.5.8.2 Simpangan Baku Relatif ... 26
3.5.8.3 Penentuan Batas Deteksi dan Batas Kuantitasi .. 27
BAB IV HASIL DAN PEMBAHASAN ... 28
4.1 Identifikasi Kalium, Kalsium, Natrium, dan Magnesium Pada Sampel ... 28
4.2 Penetapan Kadar Kalium, Kalsium, Natrium, dan Magnesium Pada Sampel ... 29
4.2.1 Kurva Kalibrasi Kalium, Kalsium, Natrium, dan Magnesium ... ... 29
4.2.2 Pengukuran Kadar Kalium, Kalsium, Natrium, dan Magnesium Dalam Sampel ... 32
4.3 Validasi Metode Analisis ... 34
4.3.1 Uji Perolehan Kembali (Recovery) ... 34
4.3.2 Simpangan Baku Relatif ... 35
4.3.3 Batas Deteksi dan Batas Kuantitasi ... 35
BAB V KESIMPULAN DAN SARAN ... 36
5.1 Kesimpulan ... 36
5.2 Saran ... 36
DAFTAR PUSTAKA ... 37
DAFTAR TABEL
Halaman Tabel 3.1 Nilai Q kritis Pada Taraf Kepercayaan 95% ... 25 Tabel 4.1 Hasil Analisis Kualitatif Kalium, Kalsium Natrium, dan
Magnesium pada Tomat ... 28 Tabel 4.2 Hasil Analisis Kuantitatif Kalium, Kalsium, Natrium, dan
Magnesium pada Tomat ... 33 Tabel 4.3 Persen Uji Perolehan Kembali (Recovery) Kalium, Kalsium,
DAFTAR GAMBAR Halaman
Gambar 2.1 Komponen Spektrofotometer Serapan Atom ... 11
Gambar 4.1 Kurva Kalibrasi Kalium ... 30
Gambar 4.2 Kurva Kalibrasi Kalsium ... 31
Gambar 4.3 Kurva Kalibrasi Natrium ... 31
DAFTAR LAMPIRAN
Halaman Lampiran 1. Surat Hasil Identifikasi ... 39 Lampiran 2. Sampel yang digunakan ... 40 Lampiran 3. Hasil Analisis Kualitatif Kalium, Kalsium, Natrium dan
Magnesium PadaTomat ... 41 Lampiran 4. Bagan Alir Proses Destruksi Kering ... 43
Lampiran 5. Bagan Alir proses Pembuatan Larutan Sampel ... 44 Lampiran 6. Data Kalibrasi Kalium Pada Tomat Plum Dengan
Spektrofotometer Serapan Atom ... 45 Lampiran 7. Data Kalibrasi Kalium Dengan Spektrofotometer Serapan
Atom, Perhitungan Persamaan Garis Regresi dan
Koefisien Korelasi ... 47 Lampiran 8. Data Kalibrasi Kalsium Pada Tomat Plum Dengan
Spektrofotometer Serapan Atom ... 48 Lampiran 9. Data Kalibrasi Kalsium Dengan Spektrofotometer Serapan
Atom, Perhitungan Persamaan Garis Regresi
Koefisien Korelasi ... 50 Lampiran 10. Data Kalibrasi Natrium Pada Tomat Plum Dengan
Spektrofotometer Serapan Atom ... 51 Lampiran 11. Data Kalibrasi Natrium Dengan Spektrofotometer Serapan
Atom, Perhitungan Persamaan Garis Regresi
Koefisien Korelasi ... 53 Lampiran 12. Data Kalibrasi Magnesium Pada Tomat Plum Dengan
Spektrofotometer Serapan Atom ... 54 Lampiran 13. Data Kalibrasi Magnesium Dengan Spektrofotometer
Serapan Atom, Perhitungan Persamaan Garis Regresi
Koefisien Korelasi ... 56 Lampiran 14. Hasil Analisis Kadar Kalium, Kalsium, Natrium dan
Magnesium pada Tomat ... 57 Lampiran 15. Contoh Perhitungan Kadar Mineral Kalium, Kalsium,
Lampiran 16. Perhitungan Statistik Kadar Mineral Kalium, Kalsium,
Natrium dan Magnesium pada Tomat ... 61
Lampiran 17. Perhitungan Simpangan Baku Relatif Kadar Mineral Kalium, Kalsium, Natrium dan Magnesium pada Tomat ... 65
Lampiran 18. Perhitungan Batas Deteksi dan Batas Kuantitas ... 69
Lampiran 19. Hasil Uji Perolehan Kembali Kalium, Kalsium, Natrium dan Magnesium Setelah Penambahan Masing-masing Larutan Baku pada Tomat ... 73
Lampiran 20. Contoh Perhitungan Uji Uji Perolehan Kembali Kalium, Kalsium, Natrium dan Magnesium pada Tomat ... 75
Lampiran 21. Gambar Alat-Alat Yang Digunakan ... 79
Lampiran 22. Tabel Distribusi t ... 80
ANALISIS KANDUNGAN MINERAL KALIUM, KALSIUM, NATRIUM, DAN MAGNESIUM PADA TOMAT (Solanum lycopersicum Mill.)
SECARA SPEKTROFOTOMETRI SERAPAN ATOM
ABSTRAK
Tomat merupakan tanaman yang dapat tumbuh dilahan perkebunan dan dipekarangan. Tanaman ini sangat bermanfaat bagi tubuh karena mengandung vitamin dan mineral yang diperlukan untuk pertumbuhan dan kesehatan. Tanaman ini mengandung mineral antara lain kalium, kalsium, natrium, dan magnesium. Tujuan penelitian ini untuk mengetahui kadar mineral kalium, kalsium, natrium, dan magnesium pada tomat (Solanum lycopersicum Mill.).
Metode penelitian yang dilakukan secara destruksi kering terhadap tomat plum dan penetapan kadar mineral kalium, kalsium, natrium, dan magnesium dilakukan dengan menggunakan spektrofotometer serapan atom dengan panjang gelombang 766,50 nm untuk kalium, pada panjang gelombang 422,7 nm untuk kalsium pada panjang gelombang 589,00 nm untuk natrium, dan pada panjang gelombang 285,20 nm untuk magnesium.
Dari hasil penelitian dapat disimpulkan bahwa tomat plum menunjukkan hasil positif untuk uji kualitatif dan mengandung mineral dengan kadar (263,67 ± 3,0418) mg/100 g untuk kalium; (25,0842 ± 0,4556) mg/100 g untuk kalsium; (8,4679 ± 0,1777) mg/100 g untuk natrium dan (13,1182 ± 0,6364) mg/100 g untuk magnesium.
Kata kunci: Tomat (Solanum lycopersicum Mill.), Kalium (K), Kalsium (Ca)
Natrium (Na), Magnesium (Mg), Spektrofotometer Serapan Atom.
THE ANALYSIS OF MINERALS CONTENT OF POTASSIUM, CALCIUM SODIUM, AND MAGNESIUM IN TOMATO(Solanum
lycopersicum Mill.) BY ATOMIC ABSORPTION
SPECTROPHOTOMETRY
ABSTRACT
Tomato is a plant that can grow in plantation and kitchen garden. This plant is very beneficial for the body because it contains vitamins and minerals needed for growth and health. It contains minerals such as potassium, calcium, sodium, and magnesium. The purpose of this study is to determine the mineral content of potassium, calcium, sodium, and magnesium in tomato (Solanum lycopersicum Mill.).
This research was by using the with dry destruction of plum tomato and the determination of potassium, calcium, sodium, and magnesium were by using the atomic absorption spectrophotometer with 766.50 nm for potassium, 422.7 nm for calcium, 589.00 nm for sodium, and 285.20 nm for magnesium.
Of the results of this research conclude that the plum tomato in a test by qualitative reactions showed positive and containing minerals with high levels of (263.67 ± 3.0418) mg/100 g for potassium; (25.0842 ± 0.4556) mg/100 g for calcium; (8.4679 ± 0.1777) mg/100 g for sodium and (13.1182 ± 0.6364) mg/100 g for magnesium.
Key word: Tomato (Solanum lycopersicum Mill.), Potassium (K), Calcium (Ca), Sodium (Na), Magnesium (Mg), Atomic Absorption Spectrophoto
BAB I
PENDAHULUAN
1.1 Latar Belakang
Tomat merupakan tanaman yang dapat tumbuh dilahan perkebunan dan dipekarangan. Tanaman ini sangat bermanfaat bagi tubuh karena mengandung vitamin (B1, B2, B6, C, E) dan mineral (Ca, Mg, P, K, Na, Fe) yang diperlukan untuk pertumbuhan dan kesehatan (Fitriani, 2012). Beberapa jenis tomat yang lazim dikenal di masyarakat antara lain tomat plum, tomat beef, tomat chery, tomat hijau, tomat anggur dan tomat pear (Anonim¹, 2012).
Kemampuan tanaman tomat untuk dapat menghasilkan buah sangat tergantung pada interaksi antara pertumbuhan tanaman dan kondisi lingkungannya. Upaya untuk menanggulangi kendala tersebut adalah dengan perbaikan teknik budidaya. Salah satu teknik budidaya tanaman yang diharapkan dapat meningkatkan hasil dan kualitas tomat adalah hidroponik (Wijayani dan Wahyu, 2005).
Natrium dalam tubuh berperan untuk mempertahankan keseimbangan tubuh (Budiyanto, 2001). Kalsium mempunyai peranan penting dalam pembentukan tulang dan gigi (Barasi, 2007). Kalium adalah mineral penting yang diperlukan tubuh dalam pengaturan keseimbangan cairan tubuh (Winarno, 1995). Kadar magnesium yang normal dapat mempertahankan tonus otot polos, dan berimplikasi terhadap kontrol tekanan darah. Penting pula bagi absorpsi kalsium dam kalium (Tan dan Rahardja, 2007).
Penetapan kadar kalsium dan magnesium dapat dilakukan dengan gravimetri, kompleksometri dan spektofotometri serapan atom, sedangan penetapan kadar kalium dan natrium dapat dilakukan dengan gravimetri dan spektrofotometri serapan atom (Khopkar, 1985). Dalam hal ini, peneliti memilih menggunakan spektrofometri serapan atom karena pelaksanaannya relatif cepat (Rohman dan Ganjar, 2007). bahan yang digunakan sedikit dan spesifik untuk setiap logam tanpa dilakukan pemisahan pendahuluan (Khopkar, 1985).
1.2 Perumusan Masalah
1. Apakah kandungan mineral kalium, kalsium, natrium dan magnesium pada tomat dapat diidentifikasi dengan reaksi kimia kualitatif?
2. Apakah kadar mineral kalium, kalsium, natrium dan magnesium pada tomat berbeda dengan literatur?
1.3Hipotesis
1. Kandungan mineral kalium, kalsium, natrium dan magnesium pada tomat dapat diidentifikasi dengan reaksi kimia kualitatif.
1.4Tujuan Penelitian
1. Untuk mengidentifikasi apakah tomat mengandung kalium, kalsium, natrium dan magnesium dengan reaksi kimia.
2. Untuk mengetahui kadar mineral kalium, kalsium, natrium dan magnesium
pada tomat. 1.5 Manfaat Penelitian
BAB II
TINJAUAN PUSTAKA
2.1 Uraian Sampel
2.1.1 Tomat
Menurut Fitriani (2012) tomat dikenal dengan berbagai nama lokal, antara lain tomat (Jawa), tamato (sulawesi), terong kaluwat (sumatera), dan lain-lain. Tomat termasuk famili Solanaceae yang banyak varietasnya. Dalam sistematika tumbuh-tumbuhan (taksonomi) tomat diklasifikasikan sebagai berikut:
Kingdom : Plantae
Divisi : Spermatophyta
Class : Dicotyledoneae
Ordo : Solanales
Famili : Solanaceae
Genus : Solanum
Spesies : Solanum lycopersicum Mill.
Buat tomat merupakan salah satu jenis sayuran buah yang sangat dikenal oleh masyarakat, rasa buah tomat adalah manis-manis segar yang dapat memberikan kesegaran pada tubuh kita (Fitriani, 2012).
2.1.2 Deskripsi Tanaman Tomat
Tanaman tomat termasuk tanaman semusim (berumur pendek). Artinya, tanaman hanya satu kali produksi dan setelah itu mati. Tanaman tomat berbentuk perdu yang panjangnya mencapai ± 2 meter. Tanaman tomat memiliki akar tunggang yang tumbuh menembus kedalam tanah dan akar serabut yang tumbuh ke arah samping tetapi dangkal. Batang tanaman tomat berbentuk persegi empat hingga bulat, berbatang lunak tetapi cukup kuat, berbulu atau berambut halus diantara bulu-bulu itu terdapat kelenjar. Batang tanaman tomat berwarna hijau, pada ruas-ruas batang mengalami penebalan dan pada ruas bagian bawah tumbuh akar-akar pendek. Daun tanaman tomat berbentuk oval, bagian tepinya bergerigi dan membentuk celah-celah menyirip agak melengkung ke dalam, daun berwarna hijau dan merupakan daun majemuk ganjil yang berjumlah 5-7 (Fitriani, 2012).
Buah tomat memiliki bentuk dan ukuran yang bervariasi, buah yang masih muda berwarna hijau muda bila sudah matang warnanya menjadi merah. Buah tomat banyak mengandung biji lunak berwarna putih kekuning-kuningan yang tersusun secara berkelompok dan dibatasi oleh daging buah (Fitriani, 2012).
2.1.3 Kandungan gizi tomat
2.2 Mineral
Mineral merupakan bagian dari tubuh dan memegang peranan penting dalam pemeliharaan fungsi tubuh, baik pada tingkat sel, jaringan, organ, maupun fungsi tubuh secara keseluruhan. Mineral digolongkan ke dalam mineral makro dan mineral mikro. Mineral makro adalah mineral yang dibutuhkan tubuh dalam jumlah lebih dari 100 mg sehari, sedangkan mineral mikro adalah mineral yang dibutuhkan tubuh dalam jumlah kurang dari 100 mg sehari. Yang termasuk mineral makro antara lain natrium, klorida, kalium, kalsium, fosfor, dan magnesium. Sedangkan yang termasuk mineral mikro antara lain besi, mangan zink, dan tembaga (Almatsier, 2004).
2.2.1 Kalium
Kalium merupakan salah satu mineral makro yang berperan dalam pengaturan keseimbangan cairan tubuh. Sebanyak 95% kalium berada di dalam cairan intraseluler (Almatsier, 2004). Bahan pangan yang mengandung kalium baik dikonsumsi penderita tekanan darah tinggi. Konsumsi kalium yang banyak akan meningkatkan konsentrasinya didalam cairan intraselular, sehingga cenderung menarik cairan dari bagian ekstraselular dan menurunkan tekanan darah (Astawan, 2008).
2.2.2 Kalsium
Kalsium merupakan mineral yang paling banyak terdapat di dalam tubuh, yaitu 1,5 – 2% dari berat badan orang dewasa atau kurang lebih sebanyak 1 kg (Barasi, 2007). Dari jumlah ini, 99% berada didalam jaringan keras, yaitu tulang dan gigi terutama dalam bentuk hidroksiapatit; selebihnya kalsium tersebar luas di dalam tubuh. Peningkatan kebutuhan akan kalsium terjadi pada masa pertumbuhan, kehamilan, dan menyusui. Jumlah kalsium yang dianjurkan per hari untuk anak-anak adalah 300-400 mg, remaja 600-700 mg, dewasa 500-800 mg, dan ibu hamil dan menyusui sebesar 1200 mg (Almatsier, 2004).
Konsumsi kalsium yang banyak dapat menyebabkan batu ginjal. Kekurangan kalsium pada masa pertumbuhan dapat menyebabkan gangguan pertumbuhan seperti tulang kurang kuat, mudah bengkok dan rapuh. Pada orang dewasa, terutama sesudah usia 50 tahun akan kehilangan kalsium dari tulangnya. Ini yang dinamakan osteoporosis (Almatsier, 2004).
2.2.3 Natrium
Natrium berguna untuk fungsi syaraf dan otot. Selain itu, berguna juga bagi keseimbangan asam basa tubuh, pengantar implus syaraf, aktifitas sel, sedangkan kelebihan mineral ini dapat mengakibatkan tekanan darah tinggi serta hilangnya kalium. Kekurangan natrium menyebabkan kejang, kehilangan nafsu makan (Tan dan Rahardja, 2007). Kebutuhan natrium untuk orang dewasa ditaksir sebanyak 1600 mg sehari (Barasi, 2007).
2.2.4 Magnesium
memegang peranan penting dalam lebih dari tiga ratus sistem enzim di dalam tubuh (Almatsier, 2004).
Di dalam cairan sel ekstraseluler, magnesium memegang peranan penting dalam relaksasi otot. Kadar magnesium yang normal dapat mempertahankan tonus otot polos, dan berimplikasi terhadap kontrol tekanan darah (Barasi, 2007). Kekurangan magnesium karena makanan dapat menyebabkan kejang, halusinasi tetapi jarang terjadi. Konsumsi magnesium dengan banyak dapat menyebabkan gagal ginjal. Orang dewasa membutuhkan magnesium sekitar 250-280 mg sehari (Almatsier, 2004).
2.3 Spektrofotometri Serapan Atom
Spektrofotometri serapan atom adalah suatu metode yang digunakan untuk mendeteksi atom-atom logam dalam fase gas. Metode ini seringkali mengandalkan nyala untuk mengubah logam dalam larutan sampel menjadi atom-atom logam berbentuk gas yang digunakan untuk analisis kuantitatif dari logam dalam sampel (Bender, 1987).
Metode spektrofotometri serapan atom berdasarkan pada absorbsi cahaya oleh atom. Atom- atom akan menyerap cahaya pada panjang gelombang tertentu, tergantung pada sifat unsurnya. Dasar analisis menggunakan teknik spektrofotometri serapan atom adalah bahwa dengan mengukur besarnya absorbsi oleh atom analit, maka konsentrasi analit tersebut dapat ditentukan (Ganjar dan Rohman, 2007).
Cara ini cocok untuk analisis sekelumit logam karena mempunyai kepekaan yang tinggi, pelaksanaanya relatif sederhana, dan interferensinya sedikit. Spektrofotometri serapan atom didasarkan pada penyerapan energi sinar oleh atom-atom netral dalam bentuk gas (Ganjar dan Rohman, 2007).
Proses yang terjadi ketika dilakukan analisis dengan menggunakan spektrofotometri serapan atom dengan cara absorbsi yaitu penyerapan energi radiasi oleh atom-atom yang berada pada tingkat dasar. Atom-atom tersebut menyerap radiasi pada panjang gelombang tertentu, tergantung pada sifat atom tersebut. Sebagai contoh kalium menyerap radiasi pada panjang gelombang 766,50 nm, kalsium pada 422,7 nm, natrium pada 589 nm, dan magnesium menyerap radiasi pada panjang gelombang 285,20 nm. Dengan menyerap radiasi, maka atom akan memperoleh energi sehingga suatu atom pada keadaan dasar dapat ditingkatkan menjadi ke tingkat eksitasi (Ganjar dan Rohman, 2007).
Secara eksperimental akan diperoleh puncak-puncak serapan sinar oleh atom-atom yang dianalisis. Garis-garis spektrum serapan atom yang timbul karena serapan radiasi yang menyebabkan eksitasi atom dari keadaan azas ke salah satu tingkat energi yang lebih tinggi disebut garis-garis resonansi (Resonance line). Garis-garis resonansi ini akan dibaca dalam bentuk angka oleh Readout (Ganjar dan Rohman, 2007).
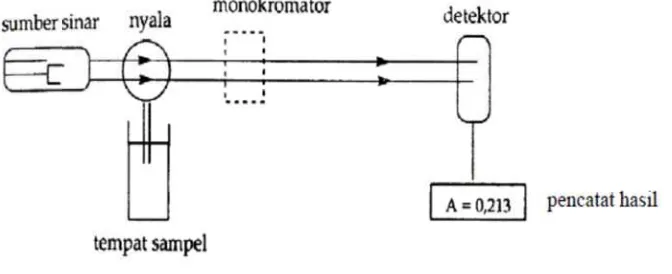
Adapun instrumentasi spektrofotometer serapan atom adalah sebagai berikut (Ganjar dan Rohman, 2007):
a. Sumber Radiasi
suatu katoda dan anoda. Katoda berbentuk silinder berongga yang dilapisi dengan logam tertentu sesuai dengan logam yang diperiksa.
b. Sumber atomisasi
Sumber atomisasi dibagi menjadi dua yaitu sistem nyala dan sistem tanpa nyala. Kebanyakan instrumen sumber atomisasinya adalah nyala dan sampel diintroduksikan dalam bentuk larutan. Sampel masuk ke nyala dalam bentuk aerosol. Aerosol biasa dihasilkan oleh nebulizer (pengabut) yang dihubungkan ke nyala oleh ruang penyemprot (chamber spray).
1. Dengan nyala (Flame)
Nyala digunakan untuk mengubah sampel yang berupa cairan menjadi bentuk uap atomnya dan untuk proses atomisasi. Suhu yang dapat dicapai oleh nyala tergantung pada gas yang digunakan, misalnya untuk gas asetilen-udara suhunya sebesar 2200ºC. Sumber nyala asetilen-udara ini merupakan sumber nyala yang paling banyak digunakan. Pada sumber nyala ini asetilen sebagai bahan pembakar, sedangkan udara sebagai bahan pengoksidasi.
2. Tanpa nyala (Flameless)
c. Monok Mo sesuai den lampu kat d. Detekto De tempat pen e. Amplifie Am
dari detekt e. Readou
Re
pencatat h menggamb Me pada saat itu antara kromator onokromato ngan panjan oda berong or etektor digu ngatoman. er
mplifier mer tor sehingg t
eadout meru hasil. Hasil barkan abso Gambar enurut Gan dilakukan a lain adalah: or merupaka ng gelomban ga. unakan unt rupakan su a dapat diba
upakan suat l pembacaa orbansi atau
2.1. Komp njar dan Ro
analisis deng :
an alat unt ng yang dig
tuk menguk
uatu alat un aca alat pen
tu alat penu an dapat be u intensitas
ponen Spekt ohman (200
gan alat spe
tuk memisah gunakan dal
kur intensi
ntuk mempe ncatat hasil (
unjuk atau d erupa angk emisi.
trofotometer 07), ganggu ektrofotome
hkan dan m am analisis
tas cahaya
erkuat signa (Readout).
dapat juga d ka atau beru
r Serapan A uan-ganggu eter serapan
memilih spek s yang dihas
yang mel
al yang dit
diartikan se rupa kurva
Atom
uan dapat te n atom, gang
a. Gangguan oleh penyerapan non-atomik
Gangguan ini terjadi akibat penyerapan cahaya dari sumber sinar yang bukan berasal dari atom-atom yang akan dianalisis. Penyerapan non-atomik dapat disebabkan adanya penyerapan cahaya oleh partikel-partikel pengganggu yang berada di dalam nyala. Cara mengatasi penyerapan non-atomik ini adalah bekerja pada panjang gelombang yang lebih besar.
b. Gangguan kimia yang dapat mempengaruhi jumlah atau banyaknya atom di dalam nyala
Pembentuk atom-atom netral dalam keadaan azas di dalam nyala sering terganggu oleh dua peristiwa kimia, yaitu:
- Disosiasi senyawa-senyawa yang tidak sempurna disebabkan terbentuknya
senyawa refraktorik (sukar diuraikan dalam api), sehingga akan mengurangi
jumlah atom netral yang ada di dalam nyala.
- Ionisasi atom-atom di dalam nyala akibat suhu yang digunakan terlalu tinggi. Prinsip analisis dengan spektrofotometer serapan atom adalah mengukur absorbansi atom-atom netral yang berada dalam keadaan azas. Jika terbentuk ion maka akan mengganggu pengukuran absorbansi atom netral karena spektrum absorbansi atom-atom yang mengalami ionisasi tidak sama dengan spektrum atom dalam keadaan netral sehingga akan mempengaruhi hasil.
2.4 Validasi Metode Analisis
parameter analisis yang harus dipertimbangkan dalam validasi metode analisis adalah sebagai berikut (Harmita, 2004):
a. Kecermatan
Kecermatan adalah ukuran yang menunjukkan derajat kedekatan hasil analisis dengan kadar analit yang sebenarnya. Kecermatan dinyatakan sebagai persen perolehan kembali (recovery) analit yang ditambahkan. Kecermatan ditentukan dengan dua cara, yaitu:
- Metode simulasi
Metode simulasi (Spiked-placebo recovery) merupakan metode yang dilakukan dengan cara menambahkan sejumlah analit bahan murni ke dalam suatu bahan pembawa sediaan farmasi (plasebo), lalu campuran tersebut dianalisis dan hasilnya dibandingkan dengan kadar analit yang ditambahkan (kadar yang sebenarnya).
- Metode penambahan baku
Metode penambahan baku (standard addition method) merupakan metode yang dilakukan dengan cara menambahkan sejumlah baku dengan konsentrasi tertentu pada sampel yang diperiksa, lalu dianalisis dengan metode yang akan divalidasi. Hasilnya dibandingkan dengan sampel yang dianalisis tanpa penambahan sejumlah baku. Persen perolehan kembali ditentukan dengan menentukan berapa persen baku yang ditambahkan ke dalam sampel dapat ditemukan kembali.
b. Keseksamaan (presisi)
Keseksamaan atau presisi diukur sebagai simpangan baku relatif atau
koefisien variasi. Keseksamaan atau presisi merupakan ukuran yang menunjukkan derajat kesesuaian antara hasil uji individual ketika suatu metode dilakukan secara berulang untuk sampel yang homogen. Nilai simpangan baku relatif yang memenuhi persyaratan menunjukkan adanya keseksamaan metode yang dilakukan. Nilai simpangan baku relatif dikatakan memenuhi kriteria seksama dan teliti jika RSDnya tidak lebih dari 2%.
c. Selektivitas (Spesifisitas)
Selektivitas atau spesifisitas suatu metode adalah kemampuannya yang hanya mengukur zat tertentu secara cermat dan seksama dengan adanya komponen lain yang ada di dalam sampel.
d. Linearitas dan rentang
Linearitas adalah kemampuan metode analisis yang memberikan respon baik secara langsung maupun dengan bantuan transformasi matematika, menghasilkan suatu hubungan yang proporsional terhadap konsentrasi analit dalam sampel. Rentang merupakan batas terendah dan batas tertinggi analit yang dapat ditetapkan secara cermat, seksama dan dalam linearitas yang dapat diterima. e. Batas deteksi dan batas kuantitasi
BAB III
METODE PENELITIAN
3.1 Tempat dan Waktu Penelitian
Penelitian ini dilakukan di Laboraturium Kimia Farmasi Kualitatif Fakultas Farmasi Universitas Sumatera Utara dan di Laboraturium Penelitian Fakultas Farmasi Universitas Sumatera Utara Medan pada bulan Maret 2013 - Juni 2013.
3.2 Bahan-bahan
3.2.1 Sampel
Sampel yang digunakan dalam penelitian ini adalah buah tomat Plum yang diambil di daerah Brastagi, Provinsi Sumatera Utara (Gambar Sampel dapat dilihat pada Lampiran 2, halaman 40).
3.2.2 Pereaksi
Bahan yang digunakan adalah pro analisis keluaran E. Merck yaitu asam nitrat pekat 65% b/v, asam pikrat 99% b/v, kuning titan 8% b/v, natrium hidroksida 99% b/v, aquabides (Ikapharmindo Putramas), larutan baku kalium 1000 mcg/ml, larutan baku kalsium 1000 mcg/ml larutan baku natrium 1000 mcg/ml, dan larutan baku magnesium 1000 mcg/ml (Laboratorium Penelitian Fakultas Farmasi USU).
3.3 Alat-alat
plate, kertas saring Whatman no. 42, neraca analitik, pisau stainless stell, krus porselen dan spatula.
3.4 Pembuatan Pereaksi
3.4.1 Asam Pikrat 1% b/v
Sebanyak 1 gram asam pikrat dilarutkan dalam aquabides hingga 100 ml.
3.4.2 Titan Yellow 0,1% b/v
Larutan titan yellow 0,1% b/v dibuat dengan cara melarutkan 0,1 g titan yellow dalam 100 ml aquabides.
3.4.3 Larutan Natrium Hidroksida 2 N
Sebanyak 80,02 gram natrium hidroksida dilarutkan dengan aquabides hingga 1000 ml (Ditjen POM, 1979).
3.4.4 Larutan HNO3 (1:1)
Larutan HNO3 (1:1) dibuat dengan mengencerkan 250 ml HNO3 65% b/v dengan akuabides hingga 500 ml (Horwitz, 2000).
3.4.5 Larutan H2SO4 1 N
Larutan H2SO4 1 N dibuat dengan mengencerkan larutan H2SO4 96% v/v sebanyak 3 ml dengan aquabides hingga 100 ml (Ditjen POM, 1979).
3.5 Prosedur Penelitian
3.5.1 Pengambilan sampel
3.5.2 Penyiapan Sampel
Tomat Plum dicuci bersih, lalu ditimbang ± 500 mg kemudian di blender sampai halus.
3.5.3 Proses Destruksi
3.5.3.1 Proses Destruksi Kering
Sampel yang telah dihaluskan ditimbang sebanyak 10 gram dimasukkan ke dalam krus porselen, lalu diabukan di tanur dengan temperatur awal 100oC dan perlahan-lahan temperatur dinaikkan menjadi 500oC dengan interval 25oC setiap 5 menit. Pengabuan dilakukan selama 24 jam dan dibiarkan dingin lalu dipindahkan ke desikator. Abu dibasahi dengan 10 tetes akuabides dan ditambahkan 5 ml HNO
3 (1:1) secara hati-hati. Kemudian kelebihan HNO3 diuapkan pada hot plate dengan suhu 100-120oC sampai kering. Krus porselen dimasukkan kembali ke dalam tanur dan diabukan selama 1 jam dengan suhu 500oC, kemudian didinginkan (Horwitz, 2000). (Bagan alir proses destruksi kering pada sampel dapat dilihat pada Lampiran 4, halaman 43).
3.5.4 Pembuatan Larutan Sampel
kasium, kalium, natrium dan magnesium. (Bagan alir prosedur destruksi kering dapat dilihat pada Lampiran 5, halaman 44).
3.5.5 Analisis Kualitatif
3.5.5.1 Kalium
3.5.5.1.1 Uji nyala Ni/Cr
Bersihkan kawat Ni/Cr dengan HCl pekat lalu dipijar pada api bunsen sampai tidak memberikan warna khusus pada nyala bunsen. Kemudian celupkan kawat pada sampel lalu dipijar pada api bunsen, amati warna yang terjadi pada nyala bunsen. Jika terdapat kalium akan terbentuk warna merah ungu pada nyala bunsen.
3.5.5.1.2 Uji Kristal Kalium dengan Asam Pikrat
Larutan sampel diteteskan 1-2 tetes pada object glass kemudian ditetesi dengan larutan asam pikrat, dibiarkan ± 5 menit lalu diamati di bawah mikroskop. Jika terdapat kalium, akan terlihat kristal berbentuk jarum kasar (Vogel, 1979). (Gambar kristal dapat dilihat pada Lampiran 3, halaman 41).
3.5.5.2 Kalsium
3.5.5.2.1 Uji nyala Ni/Cr
3.5.5.2.2 Uji Kristal Kalsium dengan Asam Sulfat 1 N
Larutan sampel diteteskan 1-2 tetes pada object glass kemudian ditetesi dengan larutan asam sulfat akan terbentuk endapan putih lalu diamati di bawah mikroskop. Jika terdapat kalsium, akan terlihat kristal berbentuk jarum (Vogel, 1979). (Gambar kristal dapat dilihat pada Lampiran 3, halaman 41).
3.5.5.3 Natrium
3.5.5.3.1 Uji nyala Ni/Cr
Bersihkan kawat Ni/Cr dengan HCl pekat lalu dipijar pada api bunsen sampai tidak memberikan warna khusus pada nyala bunsen. Kemudian celupkan kawat pada sampel lalu dipijar pada api bunsen, amati warna yang terjadi pada nyala bunsen. Jika terdapat natrium akan terbentuk warna kuning pada nyala bunsen.
3.5.5.3.2 Uji Kristal dengan Asam Pikrat
Larutan sampel diteteskan 1-2 tetes pada object glass kemudian ditetesi dengan 5 menit, lalu amati dibawah mikroskop. Jika terdapat natrium akan terbentuk jarum-jarum halus tersusun dipinggir. (Gambar kristal dapat dilihat pada Lampiran 3, halaman 42).
3.5.5.4 Magnesium
3.5.5.4.1 Reaksi Kualitatif dengan Larutan Kuning Titan 0,1% b/v
3.5.6 Analisis Kuantitatif
3.5.6.1 Pembuatan Kurva Kalibrasi
3.5.6.1.1 Pembuatan Kurva Kalibrasi Kalium
Larutan baku kalium (1000 µg/ml) dipipet sebanyak 5 ml, dimasukkan ke dalam labu tentukur 50 ml dan dicukupkan hingga garis tanda dengan akuabides (konsentrasi 100 µg/ml), kemudian dipipet 5 ml dimasukkan ke dalam labu tentukur 50 ml dan dicukupkan hingga garis tanda dengan akuabides (konsentrasi 10 µg/ml).
Larutan untuk kurva kalibrasi kalium dibuat dengan memipet (1,25; 2,5; 5,0; 7,5; dan 10) ml larutanbaku 10 µg/ml, masing-masing dimasukkan ke dalam labu tentukur 25 ml dan dicukupkan hingga garis tanda dengan akuabides (larutan ini mengandung 0,5; 1,0; 2,0; 3,0 dan 4,0 µg/ml) dan diukur pada panjang gelombang 766,5 nm dengan nyala udara-asetilen.
3.5.6.1.2 Pembuatan Kurva Kalibrasi Kalsium
Larutan baku kalsium (1000 µg/ml) dipipet sebanyak 5 ml, dimasukkan ke dalam labu tentukur 50 ml dan dicukupkan hingga garis tanda dengan akuabides (konsentrasi 100 µg/ml), kemudian dipipet 5 ml dimasukkan ke dalam labu tentukur 50 ml dan dicukupkan hingga garis tanda dengan akuabides (konsentrasi 10 µg/ml).
3.5.6.1.3 Pembuatan Kurva Kalibrasi Natrium
Larutan baku natrium (1000 µg/ml) dipipet sebanyak 1 ml, dimasukkan ke dalam labu tentukur 100 ml dan dicukupkan hingga garis tanda dengan akuabides (konsentrasi 10 µg/ml).
Larutan untuk kurva kalibrasi natrium dibuat dengan memipet (0,75; 1; 1,5; 2 dan 2,5) ml larutan baku 10 µg/ml, masing-masing dimasukkan ke dalam labu tentukur 50 ml dan dicukupkan hingga garis tanda dengan akuabides (larutan ini mengandung 0,15; 0,2; 0,3; 0,4; dan 0,5 µg/ml) dan diukur pada panjang gelombang 589,0 nm dengan nyala udara-asetilen.
3.5.6.1.4 Pembuatan Kurva Kalibrasi Magnesium
Larutan baku magnesium (1000 µg/ml) dipipet sebanyak 5 ml, dimasukkan ke dalam labu tentukur 50 ml dan dicukupkan hingga garis tanda dengan akuabides (konsentrasi 100 µg/ml), kemudian dipipet 5 ml dimasukkan ke dalam labu tentukur 50 ml dan dicukupkan hingga garis tanda dengan akuabides (konsentrasi 10 µg/ml), kemudian dipipet 5 ml dimasukkan ke dalam labu tentukur 50 ml dan dicukupkan hingga garis tanda dengan akuabides (konsentrasi 1 µg/ml).
3.5.6.2 Penetapan Kadar Mineral dalam Sampel
3.5.6.2.1 Penetapan Kadar Kalium
Larutan sampel tomat di ambil sebanyak 0,2 ml dimasukkan kedalam labu tentukur 25 ml dan diencerkan dengan akuabides hingga garis tanda (Faktor Pengenceran = 25/0,2 = 125 kali). Diukur absorbansinya dengan menggu nakan spektrofotometer serapan atom pada panjang gelombang 766,5 nm. Nilai absorbansi yang diperoleh harus berada dalam rentang kurva kalibrasi larutan baku kalium. Konsentrasi kalium dalam sampel ditentukan berdasarkan persamaan garis regresi dari kurva kalibrasi.
3.5.6.2.2 Penetapan Kadar Kalsium
Larutan sampel tomat di ambil sebanyak 2,5 ml dimasukkan kedalam labu tentukur 25 ml dan diencerkan dengan akuabides hingga garis tanda (Faktor Pengenceran = 25/2,5 = 10 kali). Diukur absorbansinya dengan menggunakan spektrofotometer serapan atom pada panjang gelombang 422,7 nm. Nilai absorbansi yang diperoleh harus berada dalam rentang kurva kalibrasi larutan baku kalsium. Konsentrasi kalsium dalam sampel ditentukan berdasarkan persamaan garis regresi dari kurva kalibrasi.
3.5.6.2.3 Penetapan Kadar Natrium
larutan baku natrium. Konsentrasi natrium dalam sampel ditentukan berdasarkan persamaan garis regresi dari kurva kalibrasi.
3.5.6.2.4 Penetapan Kadar Magnesium
Larutan sampel tomat diambil sebanyak 0,2 ml dimasukkan kedalam labu tentukur 25 ml dan diencerkan dengan akuabides hingga garis tanda (Faktor Pengenceran = 25/0,2 = 125 kali). Diukur absorbansi dengan menggu nakan spektrofotometer serapan atom pada panjang gelombang 285,2 nm. Nilai absorbansi yang diperoleh harus berada dalam rentang kurva kalibrasi larutan baku magnesium. Konsentrasi magnesium dalam sampel ditentukan berdasarkan persamaan garis regresi dari kurva kalibrasi.
3.5.6.3 Perhitungan Kadar Kalium, Kalsium, Natrium dan Magnesium dalam sampel
Menurut Harmita (2004), kadar kalium, kalsium, natrium, dan magnesium dihitung dengan mensubstitusikan absorbansi ke dalam persamaan regresi yang diperoleh dari kurva kalibrasi dengan menggunakan rumus dibawah ini:
Y = aX + b Keterangan:
Y = Absorbansi Sampel a = Slope X = Konsentrasi sampel b = Intersep
Menurut Harmita (2004), kadar kalium, kalsium, natrium, dan magnesium dalam sampel dapat dihitung dengan cara sebagai berikut:
(g) Sampel Berat
n pengencera Faktor
x (ml) Volume x
(mcg/ml) i
Konsentras (mcg/g)
Atom
3.5.7 Analisis Data Secara Statistik 3.5.7.1 Penolakan Hasil Pengamatan
Kadar kalium, kalsium, natrium, dan magnesium yang diperoleh dari hasil pengukuran masing-masing larutan sampel dianalisis secara statistik.
Menurut Sudjana (2005), standar deviasi dapat dihitung dengan rumus:
SD =
1 -n
X -Xi 2
Keterangan:
Xi = Kadar sampel
X = Kadar rata-rata sampel n = Jumlah pengulangan
Kadar kalium, kalsium, natrium, dan magnesium yang diperoleh dari hasil pengukuran masing-masing ke enam larutan sampel, diuji secara statistik dengan uji Q.
Q =
terendah Nilai
tertinggi Nilai
terdekat yang
Nilai dicurigai
yang Nilai
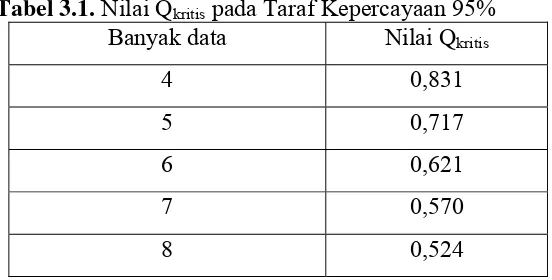
[image:41.595.116.392.567.707.2]Hasil pengujian atau nilai Q yang diperoleh ditinjau terhadap daftar harga Q pada Tabel 3.1 apabila Q>Qkritis maka data tersebut ditolak (Rohman dan Gandjar, 2007).
Tabel 3.1. Nilai Qkritis pada Taraf Kepercayaan 95% Banyak data Nilai Qkritis
Menurut Sudjana (2005), Untuk menentukan kadar kalium, kalsium, natrium, dan magnesium di dalam sampel dengan interval kepercayaan 95%; α = 0.05; dk = n - 1, dapat digunakan rumus:
µ = X ± (t(α/2, dk) x SD/√n Keterangan :
µ = Interval kepercayaan X = Kadar rata-rata sampel dk = Derajat kebebasan (dk = n-1) t = Harga t tabel sesuai dengan dk = n-1 α = Tingkat kepercayaan
SD = Standar deviasi n = Jumlah pengulangan
3.5.8 Validasi Metode Analisis
3.5.8.1 Uji Perolehan Kembali (Recovery)
Uji perolehan kembali (recovery) dilakukan dengan metode penambahan larutan standar (standard addition method). Dalam metode ini, kadar mineral dalam sampel ditentukan terlebih dahulu, selanjutnya dilakukan penentuan kadar mineral dalam sampel setelah penambahan larutan baku dengan konsentrasi tertentu (Ermer, 2005).
Menurut Harmita (2004), persen perolehan kembali dapat dihitung dengan rumus di bawah ini:
% Perolehan Kembali = A
A F
C C C
*
x 100% Keterangan:
CA = Kadar logam dalam sampel sebelum penambahan baku CF = Kadar logam dalam sampel setelah penambahan baku C*A = Kadar larutan baku yang ditambahkan
3.5.8.2 Simpangan Baku Relatif
Keseksamaan atau presisi merupakan ukuran yang menunjukkan derajat kesesuaian antara hasil uji individual ketika suatu metode dilakukan secara berulang untuk sampel homogen. Adapun uji ketelitian yaitu koefisien variasi atau Relative Standard Deviation (%RSD) (Harmita, 2004).
Menurut Harmita (2004), harga persentase koefisien variasi (%RSD) ditentukan dengan rumus sebagai berikut:
RSD = x100%
x SD
Keterangan:
X = Kadar rata-rata sampel SD = Standar Deviasi
RSD = Relative Standard Deviation
3.5.8.3 Penentuan Batas Deteksi dan Batas Kuantitasi
Batas deteksi merupakan jumlah terkecil analit dalam sampel yang dapat dideteksi yang masih memberikan respon signifikan. Sedangkan batas kuantitasi merupakan kuantitas terkecil analit dalam sampel yang masih dapat memenuhi kriteria cermat dan seksama (Harmita, 2004).
Simpangan Baku (SB) =
2 2
n Yi Y
Batas deteksi (LOD) =
slope SB x
3
Batas kuantitasi (LOQ) =
slope SB x
BAB IV
HASIL DAN PEMBAHASAN
4.1 Identifikasi Kalium, Kalsium, Natrium, dan Magnesium pada Sampel
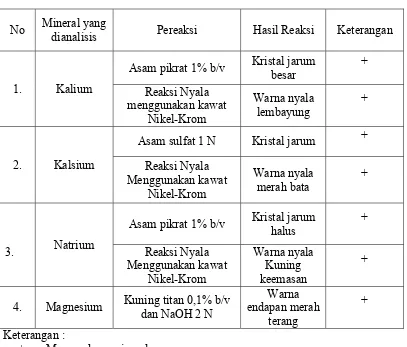
[image:45.595.110.517.366.713.2]Analisis kualitatif dilakukan sebagai analisis pendahuluan untuk mengetahui ada atau tidaknya mineral kalium, kalsium, natrium, dan magnesium dalam sampel yang akan dianalisis secara kuantitatif dengan menggunakan spektrofotometer serapan atom. Hasil analisis kualitatif kalium, kalsium, natrium, dan magnesium dapat dilihat pada Tabel 4.1.
Tabel 4.1. Hasil Analisis Kualitatif Kalium, Kalsium, Natrium, dan Magnesium Pada Tomat
No Mineral yang
dianalisis Pereaksi Hasil Reaksi Keterangan
1. Kalium
Asam pikrat 1% b/v Kristal jarum besar
+ Reaksi Nyala
menggunakan kawat Nikel-Krom
Warna nyala lembayung
+
2. Kalsium
Asam sulfat 1 N Kristal jarum + Reaksi Nyala
Menggunakan kawat Nikel-Krom
Warna nyala merah bata
+
3. Natrium
Asam pikrat 1% b/v Kristal jarum halus
+ Reaksi Nyala
Menggunakan kawat Nikel-Krom
Warna nyala Kuning keemasan
+
4. Magnesium Kuning titan 0,1% b/v dan NaOH 2 N
Warna endapan merah
terang
+ Keterangan :
Pada Tabel 4.1 menunjukkan bahwa tomat mengandung mineral kalium, kalsium, natrium, dan magnesium. Sampel dikatakan positif mengandung mineral kalium karena menghasilkan kristal jarum besar kalium pikrat pada saat penambahan asam pikrat 1% b/v serta memberikan warna nyala lembayung pada uji nyala dengan kawat nikel-krom. Sampel dikatakan positif mengandung mineral kalsium karena menghasilkan kristal jarum kalsium sulfat pada saat penambahan asam sulfat 1 N serta memberikan warna nyala merah bata pada uji nyala dengan kawat nikel-krom Sampel dikatakan positif mengandung mineral natrium karena menghasilkan kristal jarum halus natrium pikrat pada saat penambahan asam pikrat 1% b/v serta dikatakan positif mengandung mineral natrium karena memberikan warna nyala kuning keemasan pada uji nyala dengan kawat nikel-krom. Dikatakan positif mengandung mineral magnesium karena menghasilkan endapan merah terang dengan penambahan larutan kuning titan 0,1% b/v dan natrium hidroksida 2 N (Vogel, 1979).
Hasil absorbansi dengan spektrofotometer serapan atom menunjukkan adanya absorbansi pada panjang gelombang 766,50 nm untuk kalium, 422,7 nm untuk kalsium, 589,00 nm untuk natrium dan 285,20 nm untuk magnesium, Hal ini juga membuktikan secara kualitatif bahwa sampel mengandung ion kalium, kalsium, natrium, dan magnesium.
4.2 Penetapan Kadar Kalium, Kalsium, Natrium, dan Magnesium pada
Sampel
4.2.1 Kurva Kalibrasi Kalium, Kalsium, Natrium, dan Magnesium
Kurva kalibrasi kalium diperoleh dengan cara mengukur absorbansi dari
persamaan 0,9995 (K Lampiran Be baku kaliu Ku larutan ba persamaan 0,9985 (K Lampiran Be baku kalsi
n garis regr
Kurva, data
6, halaman
erdasarkan h
um yang dap
Gamb
urva kalibra
aku kalsium n garis regr
Kurva, data
8, halaman
erdasarkan h
ium yang da
resi Y = 0,
dan perhitu
n 45, Lampir
hasil pengu
pat dilihat p
bar 4.1 Kur
asi kalsium
m pada pan resi Y = 0,
dan perhitu
n 48, Lampir
hasil pengu
apat dilihat
0347X + 0
ungan persa ran 7, halam
ukuran terse
pada Gamba
rva Kalibras
diperoleh d
njang gelom
0306X + 0
ungan persa ran 9, halam
ukuran terse
pada Gamb
0,0012 deng
amaan garis man 47 ).
ebut dipero
ar 4.1.
si Larutan B
dengan cara mbang 422 0,0027 deng amaan garis man 50). ebut dipero bar 4.2. gan koefisie
s regresi da
oleh kurva
Baku Kalium
a mengukur
2,7 nm seh
gan koefisie
s regresi da
Kurv larutan ba persamaan 0,9992. (K Lampiran Ber baku natri Kur dari larut Gamb va kalibrasi aku natrium
n garis regr
Kurva, data
10, halama
rdasarkan h
ium yang da
Gamb
rva kalibras
an baku m
bar 4.2 Kurv
i natrium d
m pada pan
resi Y = 0,
dan perhitu
an 51, Lamp
hasil pengu
apat dilihat
bar 4.3 Kurv
si magnesiu
magnesium
va Kalibras
diperoleh de
njang gelom
,3655X - 0
tungan pers piran 11, hal
ukuran terse
pada Gamb
va Kalibras
um diperole
pada panja
si Larutan B
engan cara mbang 589, 0,0029 deng amaan gari laman 53). ebut dipero bar 4.3.
si Larutan B
eh dengan
ang gelomb
Baku Kalsium
mengukur
,00 nm seh
gan koefisie
s regresi da
leh kurva k
Baku Natrium cara meng bang 285,2 m absorbansi hingga dipe en korelasi apat dilihat kalibrasi la m gukur absor
diperoleh korelasi (r dilihat pad Be baku magn Be hubungan korelasi (r natrium s menunjuk (konsentra 4.2.2 Peng Sa Pa atom, terl dilakukan yang cuku rentang k
persamaan
r) = 0,9996
da Lampiran
erdasarkan h
nesium yan
Gamba
erdasarkan yang linea r) untuk ka ebesar 0,99 kkan adanya asi) dan Y (
gukuran K ampel
da penguku lebih dahul pengencera up tinggi se kalibrasi ma
n garis reg
(Kurva, da
n 12, halam
hasil pengu
ng dapat dili
r 4.4 Kurva
kurva kal ar antara k alium sebes 992; dan un a korelasi lin absorbansi) Kadar Kaliu uran sampel lu dikondis an terhadap ehingga aga aka sampel
gresi Y =
ata dan perh
man 54, Lam
ukuran terse
ihat pada Ga
a Kalibrasi L
librasi dari konsentrasi sar 0,9995; ntuk magne nier yang m ) (Ermer, 20 um, Kalsiu
l yang dilak sikan alat p sampel. K
ar diperoleh harus dien
0,4726X –
hitungan pe
mpiran 13, ha
ebut dipero ambar 4.4. Larutan Bak i keempat dengan ab untuk kals esium sebe menyatakan 005). um, Natrium kukan secar dengan bai Karena samp
h nilai abso ncerkan. Pe
– 0,0010 d
rsamaan ga alaman 56).
oleh kurva
ku Magnesi
mineral d sorbansi, d sium sebesa esar 0,9996. adanya hub
m, dan Ma
ra spektrofo ik dan ben pel memilik orbansi yan engenceran dengan koe aris regresi . kalibrasi la ium diatas dipe dengan koe
ar 0,9985; u . Nilai r ≥ bungan ant
agnesium d
fotometri se nar. Setelah
yaitu sebesar 125 kali (25/0,2) untuk kalium; 10 kali (25/2,5) untuk kalsium; 50 kali (25/0,5) untuk natrium dan 125 kali (25/0,2) untuk magnesium. Konsentrasi kalium, kalsium, natrium, dan magnesium dalam sampel ditentukan berdasarkan persamaan garis regresi kurva kalibrasi larutan baku kalium, kalsium, natrium, dan magnesium. (Data dan contoh perhitungan dapat dilihat pada Lampiran 14, halaman 57 dan Lampiran 15, halaman 59).
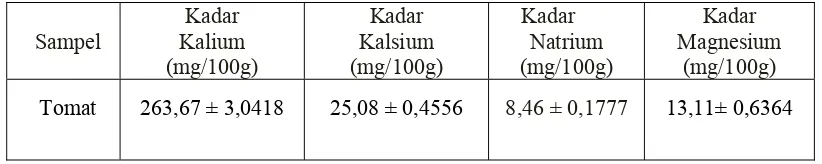
[image:50.595.110.521.353.435.2]Analisis dilanjutkan dengan perhitungan statistik (Perhitungan dapat dilihat pada Lampiran 16, halaman 61). Hasil analisis kuantitatif kalium, kalsium, natrium, dan magnesium pada sampel dapat dilihat pada Tabel 4.2.
Tabel 4.2. Kadar Kalium, Kalsium, Natrium, dan Magnesium Pada Tomat
Sampel
Kadar Kalium (mg/100g)
Kadar Kalsium (mg/100g)
Kadar Natrium (mg/100g)
Kadar Magnesium
(mg/100g)
Tomat 263,67 ± 3,0418 25,08 ± 0,4556 8,46 ± 0,1777 13,11± 0,6364
4.3 Validasi Metode Analisis
4.3.1 Uji Perolehan Kembali (Recovery)
Hasil uji perolehan kembali (recovery) kadar kalium, kalsium, natrium, dan magnesium setelah penambahan masing-masing larutan baku dapat dilihat pada Lampiran 19, halaman 73. Contoh perhitungannya pada Lampiran 20, halaman 75.
[image:51.595.114.512.346.434.2]Persen perolehan kembali (recovery) kadar mineral kalium, kalsium, natrium, dan magnesium dalam sampel dapat dilihat pada Tabel 4.3.
Tabel 4.3. Persen Uji Perolehan Kembali (recovery) Kalium, Kalsium, Natrium, dan Magnesium pada Tomat
No. Mineral Persen perolehan kembali (%)
Syarat rentang persen recovery (%)
1 Kalium 109,39
80 - 120
2 Kalsium 110,21
3 Natrium 90,43
4 Magnesium 101,17
4.3.2 Simpangan Baku Relatif
Dari perhitungan yang dilakukan terhadap data hasil pengukuran kadar mineral kalium, kalsium, natrium, dan magnesium pada tomat plum diperoleh nilai Simpangan Baku (SD) sebesar 9,0535 untuk kalium; 5,1618 untuk kalsium; 3,0965 untuk natrium; 2,8634 untuk magnesium dan nilai Simpangan Baku Relatif (RSD) sebesar 8,27% untuk kalium; 4,68% untuk kalsium; 3,42% untuk natrium; 2,83% untuk magnesium.
Menurut Harmita (2004), nilai Simpangan Baku Relatif (RSD) untuk analit dengan kadar part per million (ppm) adalah ≤ 16%. Dari hasil yang diperoleh menunjukkan bahwa metode yang dilakukan memiliki presisi yang baik. Data perhitungan Simpangan Baku Relatif (RSD) kadar mineral kalium, kalsium, natrium, dan magnesium dapat dilihat pada Lampiran 17, halaman 65.
4.3.3 Batas Deteksi dan Batas Kuantitasi
Berdasarkan data kurva kalibrasi kalium, kalsium, natrium, dan
magnesium diperoleh batas deteksi dan batas kuantitas untuk keempat mineral
tersebut. Dari hasil perhitungan diperoleh batas deteksi untuk mineral kalium,
kalsium, natrium, dan magnesium masing-masing sebesar 0,0208 mcg/ml; 0,2834 mcg/ml; 0,0247 mcg/ml dan 0,0138 mcg/ml Sedangkan batas kuantitasi untuk mineral kalium, natrium, dan magnesium masing-masing sebesar 0,0694 mcg/ml;
0,9447 mcg/ml; 0,0823 mcg/ml dan 0,0461 mcg/ml.
Dari hasil perhitungan dapat di lihat bahwa semua hasil yang diperoleh
pada pengukuran sampel berada diatas batas deteksi dan batas kuantitasi.
Perhitungan batas deteksi dan batas kuantitasi mineral kalium, kalsium, natrium,
BAB V
KESIMPULAN DAN SARAN
5.1 Kesimpulan
Berdasarkan hasil pemeriksaan kualitatif kandungan mineral kalium, kalsium, natrium, dan magnesium pada tomat plum yang diuji dengan reaksi kualitatif menunjukkan hasil yang positif bahwa tomat plum mengandung mineral kalium, kalsium, natrium, dan magnesium.
Hasil pemeriksaan secara kuantitatif kandungan mineral kalium, kalsium, natrium, dan magnesium pada tomat plum dengan menggunakan spektrofotometer serapan atom menunjukkan bahwa tomat plum mengandung mineral dengan kadar (263,67 ± 3,0418) mg/100 g untuk kalium; (25,0842 ± 0,4556) mg/100 g untuk kalsium; (8,4679 ± 0,1777) mg/100 g untuk natrium dan (13,1182 ± 0,6364) mg/100 g untuk magnesium. . Kadar mineral yang didapat berbeda dari literatur disebabkan besar kecilnya kadar mineral kalium, kalsium, natrium, dan magnesium dapat dipengaruhi oleh berbagai faktor diantaranya adalah dipengaruhi oleh keadaan tanah, letak geografis, tempat tumbuh dan keadaan musim.
5.2 Saran
DAFTAR PUSTAKA
Anonim¹ .(2012). Jenis-jenis tomat. Diakses tanggal 30 Agustus 2013. http://info buah tomat.blogspot.com/jenis-jenis tomat.html
Anonim² .(2012). Tomat si bulat kaya manfaat. Diakses tanggal 07 Maret 2012. http://id. Shvoong.com/medicine and health/alternative medicine/tomat si bulat kaya manfaat.
Achadi, L.E. (2007). Gizi dan Kesehatan Masyarakat. Edisi I. Departemen Gizi dan Kesehatan Masyarakat Fakultas Kesehatan Masyarakat, Universitas Indonesia. Jakarta: PT. Raja Grafindo Persada. Hal. 94.
Almatsier, S. (2004). Prinsip Dasar Ilmu Gizi. Jakarta: PT. Gramedia Pustaka Utama. Hal. 228-229, 233-237, 242-247.
Astawan, M. (2008). Sehat dengan Buah. Jakarta: PT. Dian Rakyat. Hal. 19. Barasi, M. (2007). Nutrition at a Glance. Penerjemah: Hermin. (2009). At a
Glance: Ilmu Gizi. Jakarta: Penerbit Erlangga. Hal. 62.
Bender, G.T. (1987). Principal of Chemical Instrumentation. Philadelphia: W.B. Sounders Company. Hal. 98.
Budiyanto, M.A.K. (2001). Dasar-dasar Ilmu Gizi. Edisi Kedua. Cetakan I. Malang: UMM-Press. Hal. 59.
Ditjen POM. (1979). Farmakope Indonesia. Edisi Ketiga. Jakarta: Departemen Kesehatan RI. Hal. 744.
Ermer, J. (2005). Method Validation in Pharmaceutical Analysis. Weinheim: Wiley-Vch Verlag GmbH & Co. KGaA. Hal. 171.
Fitriani, E. (2012). Untung Berlipat Budidaya Tomat Di Berbagai Media Tanam. Yogyakarta: Pustaka Baru Press. Hal. 16-19, 25.
Gandjar, I.G., dan Rohman, A. (2007). Kimia Farmasi Analisis. Cetakan I. Yogyakarta: Pustaka Pelajar. Hal. 298-312.
Harmita. (2004). Petunjuk Pelaksanaan Validasi Metode dan Cara Perhitungannya. Majalah Ilmu Kefarmasian. 1(3): 117-119, 122-123, 127-130.
Khopkar, S.M. (1985). Basic Concepts of Analytical Chemistry. Penerjemah: A. Saptorahardjo. (2003). Konsep Dasar Kimia Analitik. Jakarta: UI-Press. Hal. 283.
Lestari, A. (2012). Pengaruh Pemberian Jus Tomat (Lycopersicum commune) Terhadap Tekanan Darah Pada Wanita Postmenopause Hipertensif. Semarang: Fakultas Kedokteran
Sudjana. (2005). Metode Statistika. Edisi Keenam. Bandung: Tarsito. Hal. 68, 93, 239, 250.
Tan, H.T., dan Rahardja, K. (2007). Obat-Obat Penting. Edisi Keenam. Jakarta: PT Elex Media Komputindo. Hal.867-868.
Vogel, A.I. (1979). Textbook of Macro and Semimicro Qualitative Inorganic Analysis. Penerjemah: Setiono dan Hadyana Pudjaaatmaka. (1990). Vogel: Buku Teks Analisis Anorganik Kualitatif Makro dan Semimikro. Bagian I. Jakarta: Kalman Media Pustaka. Hal. 262, 263, 301, 307.
Wijayani, A., dan Wahyu, W. (2005). Usaha Meningkatkan Beberapa Varietas Tomat Dengan Sistem Budidaya Hidroponik. Yogyakarta: Fakultas Pertanian UPN. Hal 77- 83
Winarno, F.G. (1995). Kimia Pangan dan Gizi. Jakarta: PT Gramedia Pustaka Utama. Hal. 154-155.
Lampirann 2. Sampe
Gam
el yang digu
mbar 1. Tom unakan
Lampiran
Gam
Ga
n 3. Hasil A Magne
mbar 2. Ha pad
ambar 3. H pa
Analisis Ku esium Pada
sil analisis k datomat
Hasil analisis adatomat
ualitatif Kali Tomat
kualitatif ka
s kualitatif k
ium, Kalsiu
alium denga
kalsium den
um, Natrium
an asam pik
ngan asam s K m, dan
krat 1% b/v
sulfat 1 N Kristal Kalium
Kristal Kals sulfat
Gam
G
mbar 4. Has pad
Gambar 5.
T
sil analisis k datomat
Hasil reaks Titan 0,1% b Akuabides + Kuning T
kualitatif na
si kualitatif b/v padatom s + NaOH Titan 0,1%
S K
atrium deng
magnesium mat
Sampel + NaOH Kuning Titan 0,1%
gan asam pik
m dengan lar +
%
krat 1% b/v
rutan kuning Kristal Natrium
Pikrat
v
Lampiran 4. Bagan Alir Proses Destruksi Kering Buah Tomat
Ditimbang 10 gram di atas krus porselen Diarangkan di atas hot plate
Diabukan dalam tanur dengan temperatur awal 100oC dan perlahan – lahan temperatur dinaikkan hingga suhu 500oC dengan interval 25oC setiap 5 menit
Dibasahi dengan 10 tetes akuabides Ditambahkan 5 ml HNO3(1:1)
Diuapkan pada hot platesampai kering
Hasil
Dilakukan selama 24 jam dan dibiarkan hingga dingin pada desikator
Abu
Dilakukan selama 1 jam dan dibiarkan hingga dingin pada desikator
Dibersihkan dari pengotoran
Dimasukkan kembali ke dalam tanur dengan temperatur awal 100oC dan perlahan – lahan temperatur dinaikkan hingga suhu 500oC dengan interval 25oC setiap 5 menit.
Dicuci bersih
Lampiran 5. Bagan Alir Proses Pembuatan Larutan Sampel Sampel yang telah
didestruksi
Dilarutkan dengan 5 ml HNO3 (1:1) dalam krus Dituangkan ke dalam labu tentukur 50 ml Diencerkan dengan akuabides hingga garis tanda
Dimasukkan ke dalam botol Larutan sampel
Disaring dengan kertas saring Whatman No.42
Filtratt
Dibuang 5 ml untuk menjenuhkan kertas saring
Dilakukan analisis kualitatif
Dilakukan analisis kuantitatif dengan Spektrofotometer Serapan atom pada 766,5 nm untuk logam kalium, 422,7 nm untuk logam kalsium, 589,00 nm untuk logam natrium dan 285,2 nm untuk logam magnesium
Lampirann 6. Data K Serapa
Kalibrasi Ka an Atom
Lampiran 7. Data Kalibrasi Kalium dengan Spektrofotometer Serapan Atom, Perhitungan Persamaan Garis Regresi dan Koefisien Korelasi
No. Konsentrasi (mg/l) (X) Absorbansi (Y)
1. 0,0000 -0,0002
2. 0,5000 0,0181
3. 1,0000 0,0362
4. 2,0000 0,0725
5. 3,0000 0,1069
6. 4,0000 0,1375
No. X Y XY X2 Y2 x10-4
1. 0,0000 -0,0002 0,0000 0,0000 0,0004
2. 0,5000 0,0181 0,0091 0,2500 3,2761
3. 1,0000 0,0362 0,0362 1,0000 13,1044
4. 2,0000 0,0725 0,1450 4,0000 52,5625
5. 3,0000 0,1069 0,3207 9,0000 114,2761
6. 4,0000 0,1375 0,5512 16,0000 189,8884
10,500
X =1,7500
0,3713
Y = 0,0619
1,0622 30,2500 373,1079
a =
X
nX n Y X XY / / 2 2
=
10,5000
/6 2500 , 30 6 / ) 3713 , 0 ( 5000 , 10 0622 , 1 2 = 0,0347
Y = a X + b b = Y aX
= 0,0619 – (0,0347)( 1,7500) = 0,0012
Maka persamaan garis regresinya adalah: Y = 0,0347X + 0,0012
=
Lampirann 8. Data Spektr
Kalibrasi rofotometer
Kalsium Serapan At
m Pada tom
Lampiran 9. Data Kalibrasi Kalsium dengan Spektrofotometer Serapan Atom, Perhitungan Persamaan Garis Regresi dan Koefisien Korelasi (r) No. Konsentrasi (mg/l) (X) Absorbansi (Y)
1. 0,0000 0,0002
2. 0,5000 0,0166
3. 1,0000 0,0357
4. 2,0000 0,0671
5. 3,0000 0,0954
6. 4,0000 0,1222
No. X Y XY X2 Y2 x10-4
1. 0,0000 0,0002 0,0000 0,0000 0,0004
2. 0,5000 0,0166 0,0083 0,2500 2,7556
3. 1,0000 0,0357 0,0357 1,0000 12,7449
4. 2,0000 0,0671 0,1342 4,0000 45,0241
5. 3,0000 0,0954 0,2862 9,0000 91,0116
6. 4,0000 0,1222 0,4888 16,0000 149,3284
10,5000
X = 1,7500
0,3372
Y = 0,0562
0,9532 30,2500 300,865
a =
X
nX n Y X XY / / 2 2
=
10,5000
/6 2500 , 30 6 / 3372 , 0 5000 , 10 9532 , 0 2 = 0,0306
Y = a X + b b = Y aX
= 0,0562 – (0,0306)(1,7500) = 0,0027
Maka persamaan garis regresinya adalah: Y = 0,0306X + 0,0027
=
Lampirann 10. Data Spek
Kalibras ktrofotomete
si Natrium er Serapan A
m Pada Atom
Lampiran 11. Data Kalibrasi Natrium dengan Spektrofotometer Serapan Atom, Perhitungan Persamaan Garis Regresi dan Koefisien Korelasi.
No. Konsentrasi (mg/l) (X) Absorbansi (Y)
1. 0,0000 -0,0001
2. 0,1500 0,0511
3. 0,2000 0,0690
4. 0,3000 0,1046
5. 0,4000 0,1410
6. 0,5000 0,1839
No. X Y XY X2 Y2 x10-4
1. 0,0000 -0,0001 0,0000 0,0000 0,0001
2. 0,1500 0,0511 0,0076 0,0225 26,1121
3. 0,2000 0,0690 0,0138 0,04 47,6100
4. 0,3000 0,1046 0,0313 0,09 109,4116
5. 0,4000 0,1410 0,0564 0,16 198,8100
6. 0,5000 0,1839 0,0919 0,25 338,1921
1,5500
X = 0,2583
0,5495
Y = 0,0915
0,2011 0,5625 720,1359
a =
X
nX n Y X XY / / 2 2
=
1,55 /6 5625 , 0 6 / ) 5495 , 0 ( 5500 , 1 2011 , 0 2 = 0,3655
Y = a X + b b = Y aX
= 0,0915 – (0,3655)( 0,2583) = -0,0029
Maka persamaan garis regresinya adalah: Y = 0,3655X – 0,0029
=
Lampirann 12. Data Spek
Kalibrasi ktrofotomete
i Magnes er Serapan A
sium Pada Atom
Lampiran 13. Data Kalibrasi Magnesium dengan Spektrofotometer Serapan Atom, Perhitungan Persamaan Garis Regresi dan Koefisien Korelasi.
No. Konsentrasi (mg/l) (X) Absorbansi (Y)
1. 0,0000 -0,0004
2. 0,0500 0,0201
3. 0,1000 0,0464
4. 0,2000 0,0967
5. 0,3000 0,1411
6. 0,4000 0,1866
No. X Y XY X2 Y2 x10-4
1. 0,0000 -0,0004 0,0000 0,0000 0,0016
2. 0,0500 0,0201 0,0011 0,0025 4,0401
3. 0,1000 0,0464 0,0046 0,01 21,5296 4. 0,2000 0,0967 0,0193 0,04 93,5089
5. 0,3000 0,1411 0,0423 0,09 199,0921
6. 0,4000 0,1866 0,0746 0,16 348,1956
1,0500
X = 0,1750
0,4905
Y = 0,0818
0,1419 0,3025 666,3679
a =
X
nX n Y X XY / / 2 2
=