KARAKTERISASI SIMPLISIA DAN ISOLASI SERTA
ANALISIS KOMPONEN MINYAK ATSIRI DAUN SIRIH
HUTAN (Piper crocatum Ruiz & Pav) YANG SEGAR DAN
SIMPLISIA SECARA GAS CROMATOGRAPHY-MASS
SPECTROPHOTOMETRY
SKRIPSI
Diajukan untuk mUniv
ersitas Sumatera Uta
OLEH:
TRI NOVA LOVENA
NIM 111524070
PROGRAM EKSTENSI SARJANA FARMASI
FAKULTAS FARMASI
UNIVERSITAS SUMATERA UTARA
MEDAN
KARAKTERISASI SIMPLISIA DAN ISOLASI SERTA
ANALISIS KOMPONEN MINYAK ATSIRI DAUN SIRIH
HUTAN (Piper crocatum Ruiz & Pav) YANG SEGAR DAN
SIMPLISIA SECARA GAS CROMATOGRAPHY-MASS
SPECTROPHOTOMETRY
SKRIPSI
Diajukan sebagai salah satu syarat untuk memperoleh Gelar Sarjana Farmasi pada Fakultas Farmasi
Universitas Sumatera Utara
Diajukan uUniv
tera Uta
OLEH:
TRI NOVA LOVENA
NIM 111524070
PROGRAM EKSTENSI SARJANA FARMASI
FAKULTAS FARMASI
UNIVERSITAS SUMATERA UTARA
MEDAN
KATA PENGANTAR
Puji dan syukur panjatkan kehadirat Allah SWT, atas segala Rahmat dan
KaruniaNya sehingga penulis dapat menyelesaikan skripsi ini dengan judul
“Karakterisasi Simplisia Dan Isolasi Serta Analisis Komponen Minyak Atsiri
Daun Sirih Hutan (Piper crocatum Ruiz & Pav) Yang Segar Dan Simplisia Secara
Gas Chromatography-Mass Spectrometry”. Skripsi ini diajukan sebagai salah satu
syarat untuk memperoleh gelar sarjana farmasi pada Fakultas Farmasi Universitas
Sumatera Utara
Pada kesempatan ini penulis menyampaikan ucapan terima kasih kepada Bapak
Prof. Dr. Sumadio Hadisahputra, Apt, selaku Dekan Fakultas Farmasi dan terima
kasih kepada Ibu Prof. Dr. Julia Reveny, M.Si., Apt., selaku wakil Dekan I
Fakultas Farmasi Universitas Sumatera Utara yang telah memberikan fasilitas
selama masa pendidikan. Bapak Dr. M. Pandapotan Nasution, M.P.S., Apt.,
selaku pembimbing I yang telah memberikan waktu, bimbingan dan nasehat
selama penelitian hingga selesainya penyusunan skripsi ini. Ibu Dra. Herawaty
Ginting, M.Si., Apt., selaku pembimbing II yang telah memberikan waktu,
bimbingan dan nasehat selama penelitian hingga selesainya penyusunan skripsi
ini. Bapak dan Ibu staf pengajar Fakultas Farmasi Universitas Sumatera Utara
yang telah mendidik selama perkuliahan. Bapak dan Ibu kepala Laboratorium
Penelitian dan Farmakognosi yang telah memberikan fasilitas, petunjuk dan
membantu selama penelitian. Bapak Prof. Dr. Ginda Haro, M.Sc., Apt., Bapak
dosen penguji yang memberikan masukan, kritikan, arahan dan saran dalam
penyusunan skripsi ini.
Penulis juga ingin mempersembahkan rasa terima kasih yang tak terhingga
kepada Ayahanda Ramli dan Ibunda Nurhayati, S.Pd., atas doa dan
pengorbanannya dengan tulus dan ikhlas, untuk kakak tersayang Rini Hariani
Ratih, SST., M.Kes., Sefri Elvianur, SST., M.Biomed.
Penulis menyadari bahwa skripsi ini masih terdapat kekurangan, untuk itu kritik
dan saran yang mendukung sangat penulis harapkan. Akhirnya penulis
menyerahkan semua kepada Allah SWT untuk memohon Ridho-Nya, semoga
skripsi penelitian ini dapat bermanfaat bagi dunia pendidikan dan kesehatan.
Medan, Juli 2015 Penulis,
Karakterisasi Simplisia Dan Isolasi Serta Analisis Komponen
Minyak Atsiri Daun Sirih Hutan (
Piper crocatum
Ruiz & Pav)
Yang Segar Dan Simplisia Secara Gas Chromatography-Mass
Spectrometry
ABSTRAKMinyak atsiri yang disebut juga minyak menguap mempunyai komposisi kandungan kimia yang berbeda-beda sesuai dengan sumber penghasilnya. Sirih hutan (Piper crocatum Ruiz & Pav) famili Piperaceae adalah salah satu tumbuhan yang mengandung minyak atsiri dan banyak dimanfaatkan oleh masyarakat. Tujuan penelitian ini adalah untuk mengetahui kadar minyak atsiri dan perbedaan komponen minyak atsiri dari daun sirih hutan segar dan simplisia.
Penelitian yang dilakukan ini meliputi karakterisasi simplisia, isolasi minyak atsiri dengan cara destilasi air dan analisis komponen minyak atsiri daun sirih hutan (Piper crocatum Ruiz & Pav) yang segar dan simplisia secara Gas Chromatography-Mass Spectrometry (GC-MS). Penelitian ini bertujuan untuk mengetahui karakteristik simplisia serta perbedaan komposisi minyak atsiri antara daun sirih hutan yang segar dan simplisia dengan GC-MS.
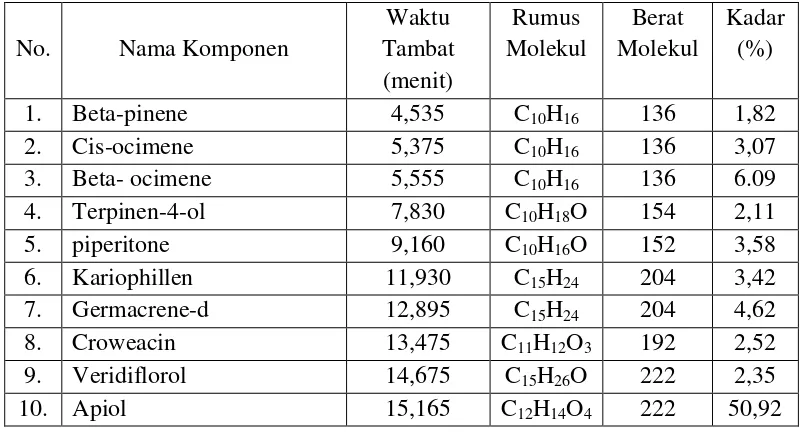
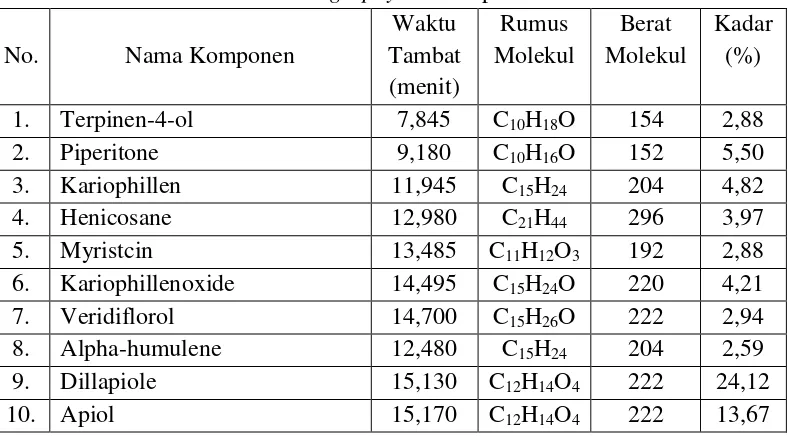
Hasil karakterisasi simplisia daun sirih hutan adalah kadar air 8,98% v/b, kadar sari yang larut dalam air 12,16 % b/b, kadar sari yang larut dalam etanol 3,15% b/b, kadar abu total 9,4% b/b dan kadar abu yang tidak larut dalam asam 5,5% b/b, penetapan kadar minyak atsiri dengan alat Stahldari daun sirih hutan segar diperoleh kadar minyak atsiri sebesar 1,09%v/b dan kadar minyak atsiri simplisia daun sirih hutan sebesar 1,23%v/b. Hasil penetapan indeks bias untuk minyak atsiri daun sirih hutan segar dan simplisia sebesar 1,51797. Bobot jenis minyak atsiri daun sirih hutan segar sebesar 1,0867 dan bobot jenis minyak atsiri daun sirih hutan simplisia sebesar 1,0869.Hasil analisis GC-MS minyak atsiri dari daun sirih hutan segar diperoleh 35 komponen dengan sepuluh komponen utama yaitu beta-pinene 1,82%, cis-Ocimene 3,07%, beta-ocimene 6,09%, terpinen-4-ol 2,11%, piperitone 3,58%, caryophyllene 3,42%, d-germacrene 4,62%, croweacin 2,52%, veridiflorol 2,35%, apiol 50,92%. Hasil analisis GC-MS minyak atsiri dari simplisia daun sirih hutan diperoleh 38 komponen dengan sepuluh 4-terpineol 2,88%, piperitone 5,50%, caryophyllene 4,82%, heneicosane 3,97%, myristcin 2,88%, caryophyllene oxide 4,21%, veridiflorol 2,94%, alpha-humulene 2,59%, dillapiole 24,12%, apiol 13,67%.
Simplex Characterization, Isolation and Analysis Of Essential Oil
Components Of Fresh and Simplex Of Forest Betel Leaves
(
Piper crocatum
Ruiz & Pav ) By Gas Chromatography-Mass
Spectrometry
ABSTRACTVolatile oils contain different chemical compositions depending on the producing sources. The forest betel (Piper crocatum Ruiz & Pav) of the family Piperaceae is one species that contains volatile oil that is widely used by local inhabitant. The objective of this study is to determine the content of volatile oil from fresh and simplex of forest betel leaves and analysis of their components.
This research includes simplex characteritation, isolation of volatile oil by water distillation and analysis of volatile oil components of fresh and simplex of forest betel leaves (Piper crocatum Ruiz & Pav) byGas Chromatography-Mass Spectrometry (GC-MS). The aim of research is to obtain information of simplex characteristics and essential oil composition of fresh forest betel leaf and simplex by GC-MS.
The result of simplex characterization of forest betel leaves simplex gave water value 8.98 % v/w, water soluble extract value 12.16% w/w, ethanol soluble extract value 3.15% w/w, total ash value 9.4% w/w, acid insoluble ash value 5.5% w/w, determination of oil content by Stahl apparatus of fresh forest betel leaves gave oil content 1.09% v/w and oil content of forest betel leaves simplex 1.23%. The result of the determination of the refractive index for betel leaves essential oil for fresh leaves 1.51797. Specific gravity of fresh betel leaves essential oil 1.0867 and simplex 1.0869. The result of the GC-MS analysis of volatile oil of fresh forest betel leaves gave 35 components with 10 main components, i.e. beta-pinene 1.82%, cis-ocimene 3.07%, beta-ocimene 6.09%, terpinen-4-ol 2.11%, piperitone 3.58%, caryophyllene 3.42%, d-germacrene 4.62%, croweacin 2.52%, veridiflorol 2.35%, apiol 50.92%. The result of GC-MS analysis of volatile oil from simplex of forest betel leaf gave 38 components with 10 main components, 4-terpineol 2.88%, piperitone 5.50%, caryophyllene 4.82%, heneicosane 3.97%, myristcin 2.88%, caryophyllene oxide 4.21%, veridiflorol 2.94%, alpha-humulene 2.59%, dillapiole 24.12%, apiol 13.67%.
DAFTAR ISI
Halaman
JUDUL ... i
HALAMAN JUDUL ... ii
HALAMAN PENGESAHAN SKRIPSI ... iii
KATA PENGANTAR ... iv
ABSTRAK ... vi
ABSTRACT ... vii
DAFTAR ISI ... viii
DAFTAR GAMBAR ... xii
DAFTAR TABEL ... xiv
DAFTAR LAMPIRAN ... xv
BAB I PENDAHULUAN ... 1
1.1 Latar Belakang ... 1
1.2 Perumusan Masalah ... 3
1.3 Hipotesis ... 4
1.4 Tujuan Penelitian ... 4
1.5 Manfaat Penelitian ... 4
BAB II TINJAUAN PUSTAKA ... 5
2.1 Uraian Sirih Hutan ... 5
2.1.1 Morfologi sirih hutan ... 5
2.1.2 Sistematika sirih hutan ... 6
2.1.3 Uraian kandungan kimia sirih hutan ... 6
2.2.1 Keberadaan minyak atsiri pada tumbuhan ... 7
2.2.2 Komposisi kimia minyak atsiri ... 7
2.2.3 Sifat fisika kimia minyak atsiri ... 8
2.2.3.1 Sifat fisika minyak atsiri ... 8
2.2.3.2 Sifat kimia minyak atsiri ... 10
2.3 Cara Isolasi Minyak Atsiri ... 11
2.3.1 Metode penyulingan ... 11
2.3.2 Metode pengepresan... 12
2.3.3 Ekstraksi dengan pelarut menguap... 12
2.3.4 Ekstraksi dengan lemak padat ... 12
2.3.5 Ecuelle ... 13
2.4 Kromatografi Gas ... 13
2.4.1 Gas pembawa ... 14
2.4.2 Sistem injeksi ... 15
2.4.3 Kolom ... 15
2.4.4 Fase diam ... 16
2.4.5 Suhu ... 16
2.4.6 Detektor ... 17
2.5 Spektrometri Massa (MS) ... 18
BAB III METODE PENELITIAN... 20
3.1 Alat Dan Bahan ... 20
3.1.1 Alat ... 20
3.1.2 Bahan ... 20
3.2.1 Pengambilan bahan tumbuhan ... 21
3.2.2 Indentifikasi tumbuhan ... 21
3.2.3 Pengolahan bahan tumbuhan... 21
3.3 Pemeriksaan Karakteristik Simplisia ... 21
3.3.1 Pemeriksaan makroskopik simplisia ... 21
3.3.2 Pemeriksaan mikroskopik serbuk simplisia ... 21
3.3.3 Penetapan kadar air ... 22
3.3.4 Penetapan kadar sari larut air ... 22
3.3.5 Penetapan kadar sari larut etanol... 23
3.3.6 Penetapan kadar abu total... 23
3.3.7 Penetapan kadar abu tidak larut dalam asam ... 23
3.3.8 Penetapan kadar minyak atsiri ... 24
3.4 Isolasi Minyak Atsiri ... 24
3.5 Karakterisasi Minyak Atsiri ... 25
3.5.1 Penentuan indeks bias ... 25
3.5.2 Penentuan bobot jenis ... 25
3.5.3 Analisis komponen minyak atsiri ... 26
BAB IV HASIL DAN PEMBAHASAN ... 27
4.1 Identifikasi Tumbuhan ... 27
4.2 Hasil Pemeriksaan Makroskopik Simplisia dan Mikroskopik Serbuk Simplisia Daun Sirih hutan ... 27
4.2.1 Hasil pemeriksaan makroskopik simplisia ... 27
4.2.2 Hasil pemeriksaan mikroskopik serbuk simplisia ... 27
4.3 Karakterisasi Minyak Atsiri ... 30
4.4 Penentuan Indeks Bias Dan Bobot Jenis Minyak Atsiri hasil Isolasi ... 30
4.5 Analisis Dengan GC-MS ... 31
4.5.1 Analisis komponen minyak atsiri dari daun sirih hutan segar ... 31
4.5.2 Analisis komponen minyak atsiri dari simplisia daun sirih hutan ... 32
4.5.3 Fragmentasi dan analisis hasil spektrometri massa minyak atsiri daun sirih hutan segar ... 36
4.5.4 Fragmentasi dan analisis hasil spektrometri massa minyak atsiri simplisia daun sirih hutan ... 46
BAB V KESIMPULAN DAN SARAN ... 56
5.1 Kesimpulan ... 56
5.2 Saran ... 57
DAFTAR PUSTAKA ... 58
DAFTAR GAMBAR
Gambar Halaman
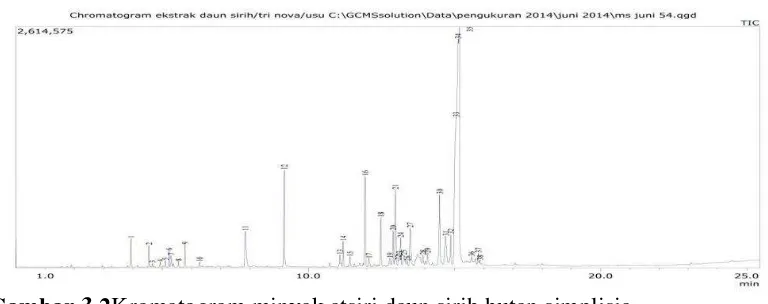
3.1 Kromatografi minyak atsiri daun sirih hutan segar ... 32
3.2 Kromatografi minyak atsiri daun sirih hutan simplisia ... 32
3.3 Rumus bangun dari senyawa beta-pinene ... 38
3.4 Rumus bangun dari senyawa cis-ocimene ... 39
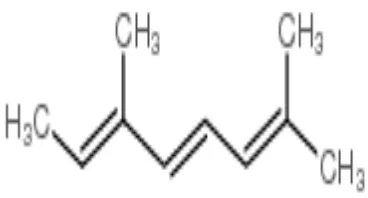
3.5 Rumus bangun dari senyawa beta-ocimene ... 40
3.6 Rumus bangun dari senyawa terpinen-4-ol ... 40
3.7 Rumus bangun dari senyawa pipertone... 41
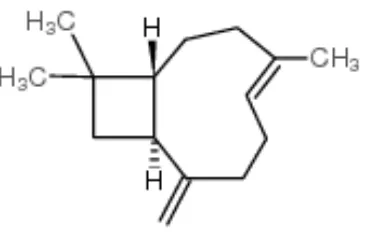
3.8 Rumus bangun dari senyawa kariophillen ... 42
3.9 Rumus bangun dari senyawa germacrene-d ... 43
3.10 Rumus bangun dari senyawa croweacin ... 44
3.11 Rumus bangun dari senyawa veridiflorol ... 44
3.12 Rumus bangun dari senyawa apiol ... 45
3.13 Rumus bangun dari senyawa terpinen-4-ol ... 48
3.14 Rumus bangun dari senyawa pipertone... 48
3.15 Rumus bangun dari senyawa kariophillen ... 49
3.16 Rumus bangun dari senyawa henicosan ... 50
3.18 Rumus bangun dari senyawa kariophillenoxide ... 52
3.19 Rumus bangun dari senyawa veridiflorol ... 53
3.20 Rumus bangun dari senyawa alpha-humulene ... 53
3.21 Rumus bangun dari senyawa dillapiole... 54
DAFTAR TABEL
Tabel Halaman
3.1 Hasil karakterisasi simplisia daun sirih hutan ... 28
3.2 Hasil penetapan kadar minyak atsiri dari daun segar dan simplisia .. 30
3.3 Hasil penentuan indeks bias dan bobot jenis minyak atsiri hasil
isolasi ... 30
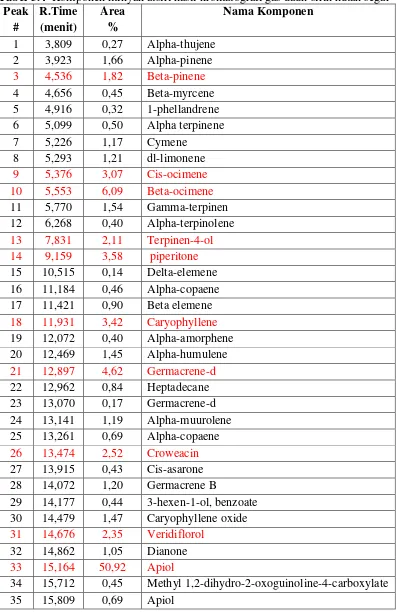
3.4 Komponen minyak atsiri hasil kromatografi gas daun sirih hutan segar ... 33
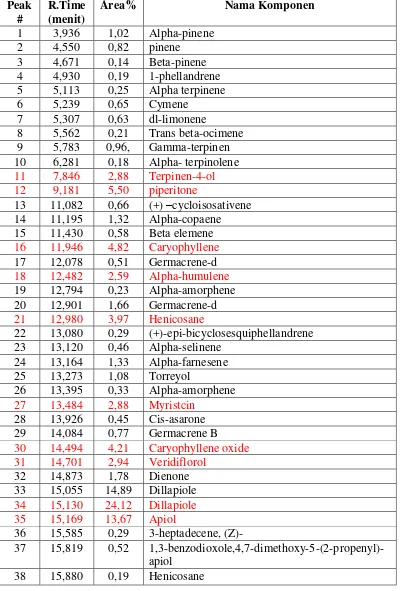
3.5 Komponen minyak atsiri hasil kromatografi gas daun sirih hutan
simplisia ... 34
3.6 Waktu tambat dan kadar komponen minyak atsiri hasil analisis GC-MS
daun sirih hutan segar ... 35
3.7 Waktu tambat dan kadar komponen minyak atsiri hasil analisis GC-MS
DAFTAR LAMPIRAN
Lampiran Halaman
1 Hasil identifikasi tumbuhan daun sirih hutan (Piper crocatum
Ruiz & Pav) ... 60
2 Gambar tumbuhan sirih Hutan (Piper crocatum Ruiz & Pav) .. 61
3 Gambar simplisia daun sirih hutan serta serbuk simplisia daun sirih hutan ... 62
4 Hasil pemeriksaan mikroskopik simplisia daun sirih ... 63
5 Gambar alat-alat yang digunakan ... 64
6 Perhitungan penetapan kadar air simplisia daun sirih hutan ... 67
7 Perhitungan penetapan kadar sari larut dalam air simplisia daun sirih hutan ... . . 68
8 Perhitungan penetapan kadar sari larut dalam etanol ... 69
9 Perhitungan penetapan kadar abu total simplisia daun sirih hutan ... 70
10 Perhitungan penetapan kadar abu tidak larut asam simplisia daun sirih hutan ... 71
11 Penetapan kadar minyak atsiri daun sirih hutan ... 72
12 Penetapan indeks bias minyak atsiri daun sirih hutan ... 75
13 Kromatogram GC minyak atsiri daun sirih hutan segar... 76
14 Spektrum massa dari puncak dengan waktu tambat 4,535 menit ... 77
16 Spektrum massa dari puncak dengan waktu tambat 5,555
menit ... 78
17 Spektrum massa dari puncak dengan waktu tambat 7,830
menit ... 78
18 Spektrum massa dari puncak dengan waktu tambat 9,160
menit ... 79
19 Spektrum massa dari puncak dengan waktu tambat 11,930
menit ... 79
20 Spektrum massa dari puncak dengan waktu tambat 12,895
menit ... 80
21 Spektrum massa dari puncak dengan waktu tambat 13,475
menit ... 80
22 Spektrum massa dari puncak dengan waktu tambat 14,675
menit ... 81
23 Spektrum massa dari puncak dengan waktu tambat 15,165
menit ... 81
24 Kromatogram GC minyak atsiri simplisia daun sirih hutan ... 82
25 Spektrum massa dari puncak dengan waktu tambat 7,845
menit ... 83
26 Spektrum massa dari puncak dengan waktu tambat 9,180
menit ... 83
27 Spektrum massa dari puncak dengan waktu tambat 11,945
menit ... 84
28 Spektrum massa dari puncak dengan waktu tambat 12,980
menit ... 84
29 Spektrum massa dari puncak dengan waktu tambat 13,485
menit ... 85
30 Spektrum massa dari puncak dengan waktu tambat 14,495
31 Spektrum massa dari puncak dengan waktu tambat 14,700
menit ... 86
32 Spektrum massa dari puncak dengan waktu tambat 15,055
menit ... 86
33 Spektrum massa dari puncak dengan waktu tambat 15,130
menit ... 87
34 Spektrum massa dari puncak dengan waktu tambat 15,170
Karakterisasi Simplisia Dan Isolasi Serta Analisis Komponen
Minyak Atsiri Daun Sirih Hutan (
Piper crocatum
Ruiz & Pav)
Yang Segar Dan Simplisia Secara Gas Chromatography-Mass
Spectrometry
ABSTRAKMinyak atsiri yang disebut juga minyak menguap mempunyai komposisi kandungan kimia yang berbeda-beda sesuai dengan sumber penghasilnya. Sirih hutan (Piper crocatum Ruiz & Pav) famili Piperaceae adalah salah satu tumbuhan yang mengandung minyak atsiri dan banyak dimanfaatkan oleh masyarakat. Tujuan penelitian ini adalah untuk mengetahui kadar minyak atsiri dan perbedaan komponen minyak atsiri dari daun sirih hutan segar dan simplisia.
Penelitian yang dilakukan ini meliputi karakterisasi simplisia, isolasi minyak atsiri dengan cara destilasi air dan analisis komponen minyak atsiri daun sirih hutan (Piper crocatum Ruiz & Pav) yang segar dan simplisia secara Gas Chromatography-Mass Spectrometry (GC-MS). Penelitian ini bertujuan untuk mengetahui karakteristik simplisia serta perbedaan komposisi minyak atsiri antara daun sirih hutan yang segar dan simplisia dengan GC-MS.
Hasil karakterisasi simplisia daun sirih hutan adalah kadar air 8,98% v/b, kadar sari yang larut dalam air 12,16 % b/b, kadar sari yang larut dalam etanol 3,15% b/b, kadar abu total 9,4% b/b dan kadar abu yang tidak larut dalam asam 5,5% b/b, penetapan kadar minyak atsiri dengan alat Stahldari daun sirih hutan segar diperoleh kadar minyak atsiri sebesar 1,09%v/b dan kadar minyak atsiri simplisia daun sirih hutan sebesar 1,23%v/b. Hasil penetapan indeks bias untuk minyak atsiri daun sirih hutan segar dan simplisia sebesar 1,51797. Bobot jenis minyak atsiri daun sirih hutan segar sebesar 1,0867 dan bobot jenis minyak atsiri daun sirih hutan simplisia sebesar 1,0869.Hasil analisis GC-MS minyak atsiri dari daun sirih hutan segar diperoleh 35 komponen dengan sepuluh komponen utama yaitu beta-pinene 1,82%, cis-Ocimene 3,07%, beta-ocimene 6,09%, terpinen-4-ol 2,11%, piperitone 3,58%, caryophyllene 3,42%, d-germacrene 4,62%, croweacin 2,52%, veridiflorol 2,35%, apiol 50,92%. Hasil analisis GC-MS minyak atsiri dari simplisia daun sirih hutan diperoleh 38 komponen dengan sepuluh 4-terpineol 2,88%, piperitone 5,50%, caryophyllene 4,82%, heneicosane 3,97%, myristcin 2,88%, caryophyllene oxide 4,21%, veridiflorol 2,94%, alpha-humulene 2,59%, dillapiole 24,12%, apiol 13,67%.
Simplex Characterization, Isolation and Analysis Of Essential Oil
Components Of Fresh and Simplex Of Forest Betel Leaves
(
Piper crocatum
Ruiz & Pav ) By Gas Chromatography-Mass
Spectrometry
ABSTRACTVolatile oils contain different chemical compositions depending on the producing sources. The forest betel (Piper crocatum Ruiz & Pav) of the family Piperaceae is one species that contains volatile oil that is widely used by local inhabitant. The objective of this study is to determine the content of volatile oil from fresh and simplex of forest betel leaves and analysis of their components.
This research includes simplex characteritation, isolation of volatile oil by water distillation and analysis of volatile oil components of fresh and simplex of forest betel leaves (Piper crocatum Ruiz & Pav) byGas Chromatography-Mass Spectrometry (GC-MS). The aim of research is to obtain information of simplex characteristics and essential oil composition of fresh forest betel leaf and simplex by GC-MS.
The result of simplex characterization of forest betel leaves simplex gave water value 8.98 % v/w, water soluble extract value 12.16% w/w, ethanol soluble extract value 3.15% w/w, total ash value 9.4% w/w, acid insoluble ash value 5.5% w/w, determination of oil content by Stahl apparatus of fresh forest betel leaves gave oil content 1.09% v/w and oil content of forest betel leaves simplex 1.23%. The result of the determination of the refractive index for betel leaves essential oil for fresh leaves 1.51797. Specific gravity of fresh betel leaves essential oil 1.0867 and simplex 1.0869. The result of the GC-MS analysis of volatile oil of fresh forest betel leaves gave 35 components with 10 main components, i.e. beta-pinene 1.82%, cis-ocimene 3.07%, beta-ocimene 6.09%, terpinen-4-ol 2.11%, piperitone 3.58%, caryophyllene 3.42%, d-germacrene 4.62%, croweacin 2.52%, veridiflorol 2.35%, apiol 50.92%. The result of GC-MS analysis of volatile oil from simplex of forest betel leaf gave 38 components with 10 main components, 4-terpineol 2.88%, piperitone 5.50%, caryophyllene 4.82%, heneicosane 3.97%, myristcin 2.88%, caryophyllene oxide 4.21%, veridiflorol 2.94%, alpha-humulene 2.59%, dillapiole 24.12%, apiol 13.67%.
BAB I
PENDAHULUAN
1.1Latar Belakang
Minyak atsiri merupakan zat yang memberikan aroma pada tumbuhan.
Minyak atsiri memiliki komponen yang berbeda-beda pada tiap tumbuhan dengan
karakteristik tertentu. Minyak atsiri banyak digunakan sebagai bahan pembuatan
parfum, kosmetik, serta bahan tambahan makanan dan obat (Buchbauer, 2000).
Minyak atsiri juga dikenal dengan nama minyak menguap atau minyak
terbang. Minyak atsiri merupakan senyawa yang berwujud cair, diperoleh dari
bagian tanaman seperti akar, kulit batang, buah, daun, biji, bunga atau bagian
lainnya dengan cara penyulingan, atau cara lain seperti dengan cara ekstraksi
menggunakan pelarut organik maupun dengan cara dipres atau dikempa serta
secara enzimatik (Sastrohamidjojo, 2004).
Minyak atsiri digunakan antara lain sebagai bahan wangi-wangian dan
sebagai minyak gosok untuk pengobatan. Hasil sulingan atau destilasi minyak
atsiri disebut juga bibit minyak wangi (Anonim, 2010). Minyak atsiri merupakan
minyak yang memberikan aroma pada tumbuhan, dimana minyak atsiri memiliki
komponen yang mudah menguap dan mempunyai rasa getir, berbau wangi sesuai
dengan aroma tanaman yang menghasilkannya (Muchtaridi, 2005).
Salah satu tumbuhan penghasil minyak atsiri adalah daun dari tumbuhan
sirih (Piper betle L) suku Piperaceae. Tumbuhan ini sejak lama sudah dikenal
oleh nenek moyang kita sebagai daun multi khasiat. Daun sirih banyak dipakai
kapur, gambir dan kapulaga untuk dikunyah. Kebiasaan nyirih ini ternyata bisa
memperkuat gigi dan menjauhkan mulut dari berbagai macam penyakit mulut
seperti sariawan, gusi pecah, sakit radang tenggorokan, karies gigi dan juga
digunakan sebagai obat keputihan. Umumnya daun sirih memiliki khasiat sebagai
antibakteri dan antiseptik. Aktivitas antibakteri dan antiseptik dari daun sirih
tersebut disebabkan adanya kandungan minyak atsiri yakni fenol betel, kavikol
dan eugenol (Anonim, 2008).Tumbuhan sirih memiliki beberapa varietas yang
dapat dibedakan dari segi bentuk, warna dan rasa, tergantung dari lingkungan dan
keadaan tanah tempat tumbuhnya. Faktor yang menentukan kualitas daun sirih
adalah jenis sirih, umur, cahaya matahari serta keadaan daunnya.Menurut
Sastroamidjojo (1997), Indonesia memiliki jenis tanaman obat yang banyak
ragamnya. Jenis tanaman yang termasuk dalam kelompok tanaman obat mencapai
lebih dari 1000 spesies, salah satunya yaitu sirih (Piper betle L.). Daun sirih dapat
digunakan sebagai antibakteri karena mengandung hidroksi kavikol, kavibetol,
estragol, eugenol, metileugenol, karvakrol, terpinen, seskuiterpen, fenilpropan
dan tanin. Sulianti dan Chairul (2002), menyatakan bahwa kandungan minyak
atsirisirih (Piper betle L) berkisar antara 0,9-1,2 %.
Analisis komponen kimia penyusun minyak atsiri Piper betle telah
dilakukan juga oleh beberapa peneliti dan diketahui sebagai komponen utama
penyusun minyak atsirinya antara lain kariofilena (30%), isoeugenol (22%) dan α
-kubebena (9%) (Agusta, 2000; Sulianti dan Chairul, 2002; Hertiani dan
Purwantini, 2002).
Tumbuhan sirih hutan (Piper crocatum Ruiz & Pav) termasuk suku
minyak atsiri.Hal ini di sebabkan karena kesukaran produksi minyak atsiri dari
tumbuhan ini adalah sulitnya mencari bahan baku karena belum dibudidayakan.
Padahal daun sirih hutan diperkirakan mempunyai potensi sebagai penghasil
minyak atsiri.
Berdasarkan hal tersebut di atas, peneliti tertarik untuk melakukan
penelitian yang meliputi karakterisasi simplisia, isolasi minyak atsiri dengan
metode destilasi air serta analisis komponen minyak atsiri secara Gas
Chromatography-Mass Spectrometry (GC-MS) dari daun sirih hutan yang segar
dan simplisia dengan tujuan untuk manfaatkan daun sirih hutan. Dengan
demikian, daun sirih hutan dapat dijadikan sebagai sumber minyak atsiri.
1.2 Perumusan Masalah
Berdasarkan uraian diatas maka perumusan masalah pada penelitian ini
adalah:
a. Apakah karakterisasi simplisia daun sirih hutan (Piper crocatum Ruiz & Pav)
dapat dilakukan sesuai dengan metode yang tertera pada buku Materia
Medika Indonesia?
b. Apakah ada perbedaan kadar dan komposisi minyak atsiri daun sirih hutan
(Piper crocatum Ruiz & Pav) simplisia dan segar yang dianalisis secara
1.3Hipotesis
Berdasarkan perumusan masalah diatas, maka hipotesis pada penelitian ini
adalah:
a. Karakterisasi simplisia daun sirih hutan (Piper crocatum Ruiz & Pav) dapat
dilakukan dengan metode yang tertera dalam Buku Materia Medika Indonesia
(MMI).
b. Terdapat perbedaan kadar dan komposisi minyak atsiri daun sirih hutan segar
dengan simplisia daun sirih hutan.
1.4 Tujuan Penelitian
Tujuan penelitian ini adalah:
a. Untuk mengetahui karakteristik simplisia daun sirih hutan (Piper crocatum
Ruiz & Pav) sesuai dengan cara karakterisasi yang terdapat dalam buku
Materia Medika Indonesia (MMI).
b. Untuk mengetahui kadar dan komposisi minyak atsiri yang diperoleh dari
daun sirih hutan (Piper crocatum Ruiz & Pav) segar dan simplisia yang
dianalisis secara GC-MS.
1.5 Manfaat Penelitian
Hasil penelitian ini diharapkan dapat memberikan informasi tentang
karakteristik simplisia, kadar dan komposisi minyak atsiri dari daun sirih hutan
segar dan simplisia serta manfaatkan daun sirih hutan sebagai obat atau sebagai
BAB II
TINJAUAN PUSTAKA
2.1 Uraian Sirih
Uraian tumbuhan sirih meliputi morfologi tumbuhan, sistematika
tumbuhan, kandungan kimia dan efek farmakologi daun sirih hutan.Daun sirih
banyak digemari dan digunakan oleh masyarakat karena rasanya yang enak.
Varietas sirih adalah sirih biasa (sirih melayu), sirih hutan, sirih udang, sirih
hitam, sirih merah, sirih silver dan sirih bulu. Sirih hutan jarang digunakan oleh
masyarakat karena selain daunnya yang keras, rasanya juga tidak enak. Sirih hutan
ini tumbuh di pohon yang terdapat di hutan tropis. (Anonim, 2008).
2.1.1Morfologi sirih hutan
Sirih hutan merupakan tanaman terna, tumbuh merambat atau menjalar.
Helaian daun berbentuk bundar telur sampai lonjong,panjang 5 cm sampai 18 cm,
lebar 2,5 cm sampai 10,5 cm pada bagian pangkal helai daun berbentuk jantung
(cordatus) atau agak bundar, tulang daun bagian bawah gundul atau berambut
sangat pendek, tebal, berwarna putih. Bunga berbentuk bulir untai (amentum),
berdiri sendiri di ujung cabang atau berhadapan dengan daun. Bulir jantan,
panjang gagang 1,5 cm sampai 3 cm, benang sari sangat pendek. Bulir betina,
panjang gagang 2,5 cm sampai 6 cm. Kepala putik 3 sampai 5. Buah buni, bulat,
gundul. Bulir masak berambut kelabu, rapat, tebal 1 cm sampai 1,5 cm (Ditjen
2.1.2Sistematika sirih (Heyne, 1987)
Sistematika sirih adalah sebagai berikut:
Divisio : Spermatophyta
Sub-divisio : Angiospermae
Kelas : Dicotyledoneae
Ordo : Piperales
Famili : Piperaceae
Genus : Piper
Spesies : Piper crocatum Ruiz & Pav
2.1.3 Uraian kandungankimiasirih hutan
Daun sirih mengandung senyawa organik yaitu minyak atsiri, alkaloida,
flavonoida, tannin, triterpenoid/steroida, dan saponin (Anonim, 2008).
2.2Minyak Atsiri
Minyak atsiri dihasilkan oleh tumbuhan, mudah menguap pada suhu
kamar tanpa mengalami dekomposisi, mempunyai rasa getir, berbau wangi sesuai
dengan bau tumbuhan penghasilnya, umumnya larut dalam pelarut organik dan
tidak larut dalam air (Ketaren, 1985).
Minyak atsiri adalah zat berbau yang terkandung dalam tumbuhan. Minyak
ini disebut juga minyak menguap (volatile oil), minyak eteris (ethereal oil), atau
minyak esensial (essensial oil). Minyak atsiri dalam keadaan segar dan murni
umumnya tidak berwarna, tetapi pada penyimpanan lama warnanya berubah
terlindung dari pengaruh cahaya, diisi penuh, ditutup rapat serta disimpan di
tempat yang kering dan gelap (Gunawan dan Mulyani, 2004).
Minyak atsiri yang terdapat pada daun sirih mengandung betel phenol,
saskuiterpen, eugenol dan kavicol yang memiliki daya mematikan kuman,
antioksidasi, antifungi, dan mampu menghilangkan bau badan, bersifat menahan
perdarahan, menyembuhkan luka pada kulit dan gangguan saluran pencernaan
(Damayanti, 1995).
2.2.1Keberadaan minyak atsiri pada tumbuhan
Minyak atsiri terdapat pada berbagai jaringan tumbuhan, seperti di dalam
rambut kelenjar (pada suku Labiatae), di dalam sel-sel parenkim (pada suku
Zingiberaceae dan Piperaceae), di dalam saluran minyak (pada suku
Umbelliferae), di dalam rongga-rongga skizogen dan lisigen(pada suku
Myrtaceae, Pinaceae dan Rutaceae), terkandung dalam semua jaringan (pada suku
Coniferae) (Tyler V.E., 1976).
2.2.2 Komposisi kimia minyak atsiri
Komposisi minyak atsiri pada umumnya berbeda pada setiap tumbuhan.
Hal ini disebabkan adanya perbedaan jenis tanaman penghasil, kondisi iklim,
tanah tempat tumbuh, umur panen, metode ekstraksi yang digunakan dan cara
penyimpanan minyak (Kataren, 1985).
Minyak atsiri biasanya terdiri dari berbagai campuran persenyawaan kimia
yang terbentuk dari unsur Karbon (C), Hidrogen (H), dan Oksigen (O), serta
beberapa persenyawaan kimia yang mengandung unsur Nitrogen (N) dan
Belerang (S). Pada umumnya komponen kimia minyak atsiri dibagi menjadi dua
a. Golongan hidrokarbon (terpen)
Senyawa yang termasuk golongan ini terbentuk dari unsur Karbon (C) dan
Hidrogen (H). Jenis hidrokarbon yang terdapat dalam minyak atsiri sebagian besar
terdiri dari monoterpen (2 unit isopren) dan sesquiterpen (3 unit isopren).
b. Golongan hidrokarbon teroksigenasi (terpenoid)
Komponen kimia dari golongan persenyawaan ini terbentuk dari unsur
Karbon (C), Hidrogen (H) dan Oksigen (O). Persenyawaan yang termasuk dalam
golongan ini adalah persenyawaan alkohol, aldehid, keton, ester, eter dan
peroksid. Ikatan karbon yang terdapat dalam molekulnya dapat terdiri dari ikatan
tunggal, ikatan rangkap dua dan ikatan rangkap tiga. Golongan hidrokarbon
teroksigenasi mempunyai aroma yang lebih wangi.Pembagian hidrokarbon
teroksigenasi berdasarkan biosintesis ada 2, yaitu:
1. Senyawa yang berasal dari asam asetat dibiosintesis melalui jalur asam
mevalonat, yaitu monoterpen dan sesquiterpen.
2. Senyawa fenilpropana yang dibiosintesis melalui jalur asam sikimat,
contoh: eugenol (Ketaren, 1985).
2.2.3 Sifat fisika kimia minyak atsiri
Analisis sifat fisikokimia dilakukan untuk mendeteksi pemalsuan,
mengevaluasi mutu dan kemurnian minyak serta mengidentifikasi jenis dan
kegunaan minyak atsiri.
2.2.3.1 Sifat fisika minyak atsiri
Masing-masing minyak atsiri mempunyai konstituen kimia yang berbeda,
tetapi dari segi fisikanya banyak persamaan. Minyak atsiri yang baru diekstraksi
Sifat-sifat fisika minyak atsiri, yaitu 1) berupa cairan 2) bau yang karakteristik, 3)
mempunyai indeks bias yang tinggi, 4) bersifat optis aktif dan 5) mempunyai
sudut putar optik (optical rotation) yang spesifik 5) titik didih. Parameter yang
dapat digunakan untuk tetapan fisika minyak atsiri antara lain :
a. Bobot jenis
Bobot jenis adalah perbandingan bobot zat di udara pada suhu 25°C
dengan volume,bobot jenis sama dengan berat di bagi volume. Penentuan bobot
jenis menggunakan alat piknometer. Bobot jenis merupakan salah satu kriterium
penting dalam menentukan mutu dan kemurnian minyak atsiri (Guenther, 1987).
b. Indeks bias
Indeks bias suatu zat adalah perbandingan kecepatan cahaya dalam udara
dan kecepatan cahaya dalam zat tersebut. Jika cahaya melewati media kurang
padat ke media lebih padat, maka sinar akan membelok atau “ membias” menjauhi
garis normal demikian pula sebaliknya. Penentuan indeks bias menggunakan alat
refraktometer. Indeks bias berguna untuk identifikasi suatu zat dan deteksi
ketidakmurnian (Guenther, 1987).
c. Putaran optik
Setiap jenis minyak atsiri mempunyai kemampuan memutar bidang
polarisasi cahaya ke arah kiri atau kanan. Karena bersifat optis aktif. Besarnya
pemutaran bidang polarisasi ditentukan oleh jenis minyak atsiri, suhu dan panjang
gelombang cahaya yang digunakan. Penentuan putaran optik menggunakan alat
2.2.3.2 Sifat kimia minyak atsiri
Minyak atsiri mempunyai sifat kimia yang khas, dimana perubahan sifat
kimia minyak atsiri merupakan ciri dari kerusakan minyak yang mengakibatkan
perubahan sifat kimia minyak, misalnya oleh proses oksidasi, hidrolisis dan
polimerisasi (resinifikasi).
a. Oksidasi
Proses oksidasi disebabkan oleh oksigen dari udara, menyebabkan minyak
atsiri menjadi rusak, warna minyak menjadi gelap, bau minyak berubah dari bau
alamiah, serta minyak menjadi lebih kental. Reaksi oksidasi pada minyak atsiri
terutama terjadi pada ikatan rangkap dalam terpen. Peroksida yang bersifat labil
akan berisomerisasi dengan adanya air, sehingga membentuk senyawa aldehid,
asam organik dan keton yang menyebabkan perubahan bau yang tidak
dikehendaki (Ketaren, 1985).
b. Hidrolisis
Proses hidrolisis terjadi dalam minyak atsiri mengandung ester. Proses
hidrolisis ester merupakan proses pemisahan gugus OR dalam molekul ester
sehingga terbentuk asam bebas dan alkohol. Ester akan terhidrolisis secara
sempurna dengan adanya air dan asam sebagai katalisator (Ketaren, 1985).
c. Resinifikasi (polimerisasi)
Beberapa fraksi dalam minyak atsiri dapat membentuk resin,yang
merupakan senyawa polimer. Resin ini dapat terbentuk selama proses pengolahan
(ekstraksi) minyak yang mempergunakan tekanan dan suhu tinggi serta selama
penyimpanan. Resinifikasi menyebabkan minyak atsiri memadat dan berwarna
campuran minyak dan resin, warnanya yang gelap dan berupa setengah padat.
(Ketaren, 1985).
2.3Cara isolasi minyak atsiri
Isolasi minyak atsiri dapat dilakukan dengan beberapa cara yaitu : 1)
penyulingan (distillation), 2) pengepresan (pressing), 3) ekstraksi dengan pelarut
menguap (solvent extraction), 4) ekstraksi dengan lemak padat, 5) ecuelle.
2.3.1Metode penyulingan
a. Penyulingan dengan air (water distillation)
Pada metode ini, bahan tumbuhan direbus dalam air mendidih dalam satu
wadah. Minyak atsiri akan dibawa oleh uap air yang kemudian didinginkan
dengan mengalirkannya melalui pendingin. Hasil sulingan adalah minyak atsiri
yang belum murni karena bercampur air dan zat lain. Perlakuan ini sesuai untuk
minyak atsiri yang tidak rusak oleh pemanasan (Guenther, 1987).
b. Penyulingan dengan air dan uap (water and steam distillation)
Bahan tumbuhan yang akan disuling dengan metode penyulingan air dan
uap ditempatkan dalam suatu tempat yang bagian bawah berlobang-lobang yang
ditopang diatas dasar alat penyulingan. Ketel diisi dengan air sampai permukaan
air berada tidak jauh di bawah saringan, uap akan naik bersama minyak atsiri
kemudian dialirkan melalui pendingin. Hasil sulingannya adalah minyak atsiri
yang belum murni (Guenther, 1987).
c. Penyulingan dengan uap (steam distillation)
Pada metode ini bahan tumbuhan dialiri uap panas dengan tekanan tinggi.
atsiri yang belum murni. Cara ini baik digunakan untuk bahan tumbuhan yang
mempunyai titik didih yang tinggi (Guenther, 1987).
2.3.2Metode pengepresan
Ekstraksi minyak atsiri dengan cara pengepresan umumnya dilakukan
terhadap bahan berupa biji, buah, atau kulit buah yang memilki kandungan
minyak atsiri yang cukup tinggi. Akibat tekanan pengepresan, maka sel-sel yang
mengandung minyak atsiri akan pecah dan minyak atsiri akan mengalir ke
permukaan bahan (Ketaren, 1985).
2.3.3Ekstraksi dengan pelarut menguap
Prinsipnya adalah melarutkan minyak atsiri dalam pelarut organik yang
mudah menguap. Ekstraksi dengan pelarut organik pada umumnya digunakan
mengekstraksi minyak atsiri yang mudah rusak oleh pemanasan uap dan air,
terutama untuk mengekstraksi minyak atsiri yang berasal dari bunga misalnya
bunga cempaka, melati, mawar dan kenanga. Pelarut yang umum digunakan
adalah petroleum eter, karbon tetra klorida dan sebagainya (Ketaren, 1985).
2.3.4Ekstraksi dengan lemak padat
Proses ini umumnya digunakan untuk mengekstraksi bunga-bungaan,
untuk mendapatkan mutu dan rendeman minyak atsiri yang tinggi. Metode
ekstraksi dapat dilakukan dengan dua cara yaitu enfleurasi dan maserasi
a. Enfleurasi (enfleurage)
Pada proses ini, absorbsi minyak atsiri oleh lemak dilakukan pada suhu
rendah (keadaan dingin) sehingga minyak terhindar dari kerusakan yang
minyak bunga yang masih melanjutkan kegiatan fisiologisnya dan memproduksi
minyak setelah bunga dipetik. Hasilnya disebut ekstrait (Ketaren, 1985).
b. Maserasi (maceration)
Pada cara ini absorbsi minyak atsiri oleh lemak dilakukan dalam keadaan
panas pada suhu 80ºC selama 1,5 jam. Cara ini dilakukan terhadap bahan
tumbuhan yang bila dilakukan penyulingan atau enfleurasi akan menghasilkan
minyak atsiri dengan rendeman yang rendah. Setelah selesai pemanasan,
campuran disaring panas-panas, jika perlu kelebihan lemak pada ampas disiram
dengan air panas. Kemudian dilakukan penyulingan untuk memperoleh minyak
atsiri (Ketaren, 1985).
2.3.5Ecuelle
Metode ini digunakan untuk mengisolasi minyak atsiri yang terdapat pada
buah-buahan seperti jeruk dengan cara menembus lapisan epidermis sampai ke
dalam jaringan yang mengandung minyak atsiri. Buah-buahan digelindingkan di
atas papan yang permukaannya bergerigi runcing untuk melukai kulit buah.
Kemudian tetesan minyak yang keluar dikumpulkan dalam suatu wadah (Tyler.,
1976).
2.4Kromatografi Gas
Kromatografi gas digunakan untuk memisahkan komponen campuran
kimia dalam suatu bahan, berdasarkan perbedaan polaritas campuran
komponen-komponen sampel. Fase gerak akan membawa campuran sampel menuju kolom
fasa diam. Campuran komponen-komponen dalam fase gerak akan berinteraksi
dengan kecepatan dan intensitas yang berbeda dimana interaksi komponen sampel
dengan fase diam dengan waktu yang paling singkat akan keluar pertama dari
kolom dan yang paling lama akan keluar paling akhir (Eaton, 1989).
Waktu yang menunjukkan berapa lama suatu senyawa tertahan di kolom
disebut waktu tambat (waktu retensi, retention time, Rt) yang diukur mulai saat
penyuntikan sampel sampai saat elusi terjadi (dihasilkan puncak atau peak)
(Gritter, et al, 1991).
Menurut Eaton (1989), hal yang mempengaruhi waktu retensi (Rt) yaitu :
1. Sifat senyawa sampel, semakin sama kepolaran molekul sampel dengan fasa
diam (adsorben) dan makin kurang keatsiriannya maka akan tertahan lebih lama di
kolom dan sebaliknya.
2. Temperatur kolom, semakin rendah temperatur maka kompenen sampel
semakin lama tertahan dalam kolom sehingga harga Rt semakin besar dan
sebaliknya.
3. Aliran gas pembawa, semakin lemah aliran gas maka komponen sampel
semakin lama tertahan dalam kolom dan sebaliknya.
4. Panjang kolom, semakin panjang kolom akan menahan komponen sampel
lebih lama dan sebaliknya.
Bagian utama dari kromatografi gas adalah gas pembawa, sistem injeksi,
kolom, fase diam, suhu, dan detektor.
2.4.1Gas pembawa
Gas pembawa harus memenuhi persyaratan antara lain harus inert, murni,
dan mudah diperoleh. Pemilihan gas pembawa tergantung pada detektor yang di
dan kering yang dapat dikemas dalam tangki bertekanan tinggi. Gas pemabawa
yang sering dipakai adalah Helium (He), Argon (Ar), Nitrogen (N2), Hidrogen
(H2), dan Karbon dioksida (CO2) (Agusta, 2000).
2.4.2Sistem injeksi
Sampel dimasukkan ke dalam ruang suntik melalui gerbang suntik (injection
port), biasanya berupa lubang yang ditutupi dengan septum atau pemisah karet
(rubber septum).Ruang suntik harus dipanaskan tersendiri, terpisah dari kolom,
dan biasanya pada suhu 10-15°C lebih tinggi dari suhu kolom.Jadi seluruh sampel
diuapkan segera setelah disuntikkan dan dibawa ke kolom (Gritter, et al, 1991).
2.4.3Kolom
Kolom dapat dibuat dari tembaga, baja nirkarat (stainless steel),
aluminium, dan kaca yang berbentuk lurus, lengkung, atau melingkar. Ada dua
macam kolom, yaitu kolom kemas dan kolom kapiler (McNair dan Bonelli, 1988).
Kolom kemas adalah pipa yang terbuat dari logam, kaca atau plastik yang
berisi penyangga padat (support material) yang inert. Fase diam, baik berwujud
padat maupun cair, diserap atau terikat secara kimia pada permukaan penyangga
padat tersebut. Kolom kemas (packed column) mempunyai diameter 0,5 cm dan
panjang 5-10 m (Agusta, 2000).
Kolom kapiler kini lebih banyak digunakan untuk menganalisis komponen
minyak atsiri. Hal ini disebabkan oleh keunggulankolom tersebut yang
memberikan hasil analisis dengan daya pisah yang tinggi dan sekaligus memilki
sensitivitas yang tinggi. Bahan kolom biasanya dari gelas, baja tahan karat atau
silika. Fase diam bersifat sebagai cairan berupa lapisan film dilapiskan pada
yang dibutuhkan sedikit dan pemisahan lebih sempurna. Kolom kapiler biasanya
mempunyai diameter 0,1 mm dan panjang mencapai 30 m (Agusta, 2000).
2.4.4Fase diam
Fase diam dibedakan berdasarkan kepolarannya, yaitu nonpolar, sedikit
polar, semi polar, polar dan sangat polar. Berdasarkan kepolaran minyak atsiri
yang non polar sampai semi polar, maka untuk keperluan analisis sebaiknya
digunakan kolom fase diam yang bersifat semi polar, misalnya SE-52, SE-54 atau
DB-5 (Agusta, 2000).
2.4.5Suhu
Tekanan uap sangat tergantung pada suhu, maka suhu merupakan faktor
utama dalam GC. Pada GC-MS terdapat tiga suhu yang berbeda, yaitu: suhu
injektor, suhu kolom, dan suhu detektor.
a. Suhu injektor
Suhu pada injektor harus cukup panas untuk menguapkan cuplikan
sedemikian cepat. Tapi sebaliknya, suhu harus cukup rendah untuk mencegah
peruraian atau penataan ulang kimiawi (rearrangement) akibat panas (McNair dan
Bonelli, 1988).
b. Suhu kolom
Pemisahan dapat dilakukan pada suhu tetap (isotermal), atau pada suhu yang
berubah secara terkendali (suhu diprogram, temperature programming). GC
isotermal paling baik dilakukan pada analisis rutin atau jika kita mengetahui agak
banyak mengenai sifat sampel yang akan dipisahkan. Pilihan awal yang baik
adalah suhu beberapa derajat di bawah titik didih komponen utama sampel. Pada
tinggi tertentu yang lain dengan laju kenaikan suhu yang diketahui dan terkendali
dalam waktu tertentu. Kenaikan suhu dapat secara linear dengan laju yang di
tentukan, bertahap, isotermal yang diikuti dengan peningkatan secara linear, linear
diikuti dengan isotermal, atau multilinear (laju berbeda saat berlainan)
(Gritter,etal, 1991).
c. Suhu detektor
Detektor harus cukup panas sehingga cuplikan dan air atau hasil samping
yang terbentuk pada proses pengionan tidak mengembun (McNair dan Bonelli,
1988).
2.4.6Detektor
Menurut McNair dan Bonelli (1988) ada dua detektor yang populer yaitu
detektor hantar-termal (thermal conductivity detector) dan detektor pengion nyala
(flame ionization detector).
a. Detektor hantar-termal (thermal conductivity detector)
Detektor ini menggunakan kawat pijar wolfram yang dipanaskan dengan
dialiri arus listrik yang tetap. Gas pembawa mengalir terus menerus melewati
kawat pijar yang panas tersebut dan suhu dibuat dengan laju tetap. Bila molekul
cuplikan yang bercampur dengan gas pembawa melewati kawat pijar meningkat.
Perubahan tahanan ini mudah diukur dengan jembatan Wheatstone dan sinyalnya
ditangkap oleh perekam dan tampak sebagai suatu puncak. Prinsip kerjanya
didasarkan pada kenyataan bahwa kemampuan suatu gas menghantar panas dari
b. Detektor pengion nyala (flame ionization detector)
Hidrogen dan udara digunakan untuk menghasilkan nyala. Suatu elektroda
pengumpul yang bertegangan arus searah ditempatkan diatas nyala dan mengukur
hantaran nyala. Dengan hidrogen murni, hantaran sangat rendah, tetapi ketika
senyawa organik dibakar, hantaran naik dan arus yang mengalir dapat diperkuat
(amplified) dalam bentuk signal atau puncak (peak) ke perekam (recorder).
Jenis detektor lain adalah Flame Photometric Detector (FPD) yang
digunakan untuk indikasi selektif dari fosfor dan sulfur. Nitrogen Phosphorous
Detector (NPD) yang digunakan untuk senyawa-senyawa yang mengandung
nitrogen dan fosfor. Electron Capture Detector (ECD) yang digunakan untuk
senyawa-senyawa organik kelompok elektro negatif, seperti halogen, peroksida
dan nitro. Mass Spectrometric Detector (MSD) yaitu spektrometer massa yang
disambungkan langsung dengan suatu kolom dalam kromatografi gas kapiler.
2.5Spektrometri Massa (MS)
Pada spektrometri massa MS molekul senyawa organik (sampel) ditembak
dengan berkas elektron berenergi tinggi dan menghasilkan ion bermuatan positif
(M+) yang disebut ion molekul yang mempunyai energi yang tinggi karena
lepasnya elektron dari molekul yang dapat pecah menjadi ion positif yang lebih
kecil (ion fragmen). Spektrum massa merupakan grafik antara limpahan relatif
ion-ion lawan perbandingan massa/muatan (m/e.,m/z) (Sastrohamidjojo, 1985).
Keuntungan utama spektrometri massa sebagai metode analisis yaitu
metode ini lebih sensitif dan spesifik untuk identifikasi senyawa yang tidak
adanya pola fragmentasi yang khas dari tiap senyawa sehingga dapat memberikan
informasi mengenai bobot molekul dan rumus molekul. Puncak ion molekul
penting dikenali karena memberikan informasi tentangbobot molekul senyawa
yang diperiksa. Puncak paling kuat (tertinggi) pada spektrum, disebut puncak
dasar (base peak), dinyatakan dengan kelimpahan 100% dan tinggi puncak lain,
termasuk puncak ion molekulnya dinyatakan sebagai persentase puncak dasar
tersebut (Silverstein, et al, 1986).
Spektrum massa hasil analisis spektroskopi massa merupakan gambaran
mengenai jumlah fragmen molekul yang terbentuk dari suatu komponen kimia
(masing-masing puncak pada kromatogram). Setiap fragmen yang terbentuk dari
pemecahan suatu komponen kimia memiliki massa yang berbeda dan ditampilkan
dalam bentuk diagram dua dimensi, m/z (m/e, massa/muatan) pada sumbu X dan
intensitas pada sumbu Y yang disebut dengan spektrum massa. Pola pemecahan
(fragmentasi) molekul untuk setiap komponen kimia sangat spesifik sehingga
dapat dijadikan sebagai patokan untuk menentukan struktur molekul suatu
komponen kimia. Selanjutnya, spektrum massa komponen kimia yang diperoleh
dari hasil analisis diidentifikasi dengan cara dibandingkan dengan spektrum massa
BAB III
METODE PENELITIAN
Metode penelitian ini dilakukan secara eksploratif yang meliputi penyiapan
sampel, karakterisasi simplisia, isolasi minyak atsiri dan analisis komponen
minyak atsiri dari daun sirih hutan (Piper crocatum Ruiz & Pav)secara GC-MS.
3.1 Alat Dan Bahan
3.1.1 Alat
Alat-alat yang digunakan pada penelitian ini adalah alat-alat gelas
laboratorium, neraca kasar (Ohaus), neraca listrik (Mettler Toledo), seperangkat
alat Stahl, seperangkat alat destilasi air (water distillation), piknometer, oven,
mikroskop, Gas Chromatograph-Mass Spectrometer (GC-MS) Shimadzu QP
2010 S, Refraktometer Abbe dan lemari pengering.
3.1.2 Bahan
Bahan yang digunakan pada percobaan ini adalah daun sirih hutan segar
dan simplisia serta bahan-bahan kimia, antara lain akuades, etanol 95%,
kloroform(E.Merck), natrium sulfat anhidrat (E.Merck), larutan kloralhidrat
jenuh,dan toluen (E.Merck).
3.2 Penyiapan Bahan Tumbuhan
Penyiapan sampel meliputi pengambilan bahan, identifikasi bahan dan
3.2.1 Pengambilan bahan tumbuhan
Metode pengambilan sampel dilakukan secara purposif, tanpa
membandingkan dengan tumbuhan yang sama dari daerah lain. Sampel diperoleh
dari hutan PLTA Koto Panjang, Desa Rantau Berangin Kecamatan Bangkinang
Barat, Kabupaten Kampar Provinsi Riau.
3.2.2 Identifikasi tumbuhan
Identifikasi tumbuhan dilakukan di “Herbarium Bogoriense” Pusat
Penelitian Biologi-LIPI Bogor.
3.2.3 Pengolahan bahan tumbuhan
Daun sirih hutan dibersihkan dari kotoran yang melekat, lalu dicuci
dengan air sampai bersih, ditiriskan, lalu ditimbang 7 kg. Sebagian daun sirih
hutan digunakan untuk isolasi minyak atsiri sampel segar sedangkan sebagian lagi
dikeringkan menjadi simplisia. Untuk dijadikan simplisia, sampel dikeringkan di
dalam lemari pengering pada suhu tidak lebih dari 40ºC sampai daun rapuh bisa
dipatahkan kemudian ditimbang 3 kg.
3.3 Pemeriksaan Karakteristik Simplisia
3.3.1 Pemeriksaan makroskopik simplisia
Pemeriksaan makroskopik dilakukan dengan mengamati bentuk/rupa,
warna, ukuran, bau dari simplisia daun sirih hutan.
3.3.2 Pemeriksaan mikroskopik serbuk simplisia
Pemeriksaan mikroskopik terhadap serbuk simplisia daun sirih hutan,
denganlarutan kloralhidrat jenuh dan ditutup dengan kaca penutup, kemudian
diamati dibawah mikroskop untuk melihat fragmen-fragmen spesifik.
3.3.3 Penetapan kadar air
Penetapan kadar air dilakukan dengan metode azeotropi sebagai berikut:
A. Penjenuhan toluen
Sebanyak 200 ml toluen dimasukkan ke dalam labu alas bulat, lalu
ditambahkan 2 ml air suling kemudian alat dipasang, dan didestilasi selama 2 jam.
Destilasi dihentikan dan dibiarkan dingin selama ± 30 menit, kemudian volume
air dalam tabung penerima dibaca dengan ketelitian 0,05 ml.
B. Penetapan kadar air simplisia
Labu berisi toluen tersebut dimasukkan 5 gram serbuk simplisia yang telah
ditimbang seksama, labu dipanaskan hati-hati selama 15 menit,setelah toluen
mendidih, kecepatan toluen diatur 2 tetes per detik sampai sebagian besar air
terdestilasi, kemudian kecepatan destilasi dinaikkan sampai 4 tetes per detik.
Setelah semua air terdestilasi, bagian dalam pendingin dibilas dengan toluen.
Destilasi dilanjutkan sampai 5 menit, tabung penerima dibiarkan mendingin pada
suhu kamar. Setelah air dan toluen memisah sempurna, volume air dibaca dengan
ketelitian 0,05 ml. Selisih kedua volume air yang dibaca sesuai dengan kadar air
yang terdapat dalam bahan yang diperiksa, kadar air dihitung dalam persen
(WHO, 1998).
3.3.4 Penetapan kadar sari larut air
Sebanyak 5 gram serbuk simplisia, dimaserasi selama 24 jam dalam 100
ml air-kloroform (2,5 ml kloroform dalam air suling sampai 1 liter) dalam labu
selama 18 jam, kemudian disaring. Sejumlah 20 ml filtrat pertama diuapkan
sampai kering dalam cawan penguap yang berdasar rata yang telah dipanaskan
dan ditara. Sisa dipanaskan pada suhu 105oC, kadar dalam persen sari yang larut
dalam air dihitung terhadap bahan yang telah dikeringkan (Depkes RI, 2008).
3.3.5 Penetapan kadar sari larut etanol
Sebanyak 5 gram serbuk simplisia yang telah dikeringkan di udara,
dimaserasi selama 24 jam dalam 100 ml etanol 95% dalam labu bersumbat sambil
dikocok sesekali selama 6 jam pertama, kemudian dibiarkan selama 18 jam.
Disaring cepat untuk menghindari penguapan etanol. Sejumlah 20 ml filtrat
diuapkan sampai kering dalam cawan penguap yang berdasar rata yang
telah dipanaskan dan ditara. Sisa dipanaskan pada suhu 105oC sampai bobot tetap.
Kadar dalam persen sari yang larut dalam etanol 95% dihitung terhadap bahan
yang telah dikeringkan di udara (Depkes RI, 1980).
3.3.6 Penetapan kadar abu total
Sebanyak 2 gram serbuk simplisia yang telah digerus dan ditimbang
seksama dimasukkan ke dalam krus porselin yang telah dipijar dan ditara,
kemudian diratakan. Krus porselin dipijar perlahan–lahan sampai arang habis,
pemijaran dilakukan pada suhu 500-600ºC selama 3 jam kemudian didinginkan
dan ditimbang sampai diperoleh bobot tetap. Kadar abu dihitung terhadap bahan
yang telah dikeringkan (Depkes RI, 1980).
3.3.7 Penetapan kadar abu tidak larut dalam asam
Abu yang telah diperoleh dalam penetapan kadar abu, dididihkan dalam 25
ml asam klorida encer selama 5 menit, bagian yang tidak larut asam dikumpulkan,
didinginkan dan ditimbang. Kadar abu yang tidak larut dalam asam dihitung
terhadap bahan yang dikeringkan (Depkes RI, 1980).
3.3.8 Penetapan kadar minyak atsiri
Penetapan kadar minyak atsiri dilakukan dengan menggunakan alat Stahl.
Caranya : sebanyak 15 gram daun sirih hutan dimasukkan dalam labu alas bulat
berleher pendek, ditambahkan air suling sebanyak 300 ml, labu diletakkan di atas
pemanas air. Hubungkan labu dengan pendingin dan alat penampung berskala,
buret diisi air sampai penuh, ditambahkan 0,2ml xilena sehingga membentuk
lapisan terpisah dengan air, selanjutnya dilakukan destilasi. Setelah penyulingan
selesai, biarkan tidak kurang dari 15 menit, catat volume minyak atsiri pada buret.
Hitung kadar minyak atsiri dalam % v/b (Depkes RI, 1995).
3.4 Isolasi Minyak Atsiri
Isolasi minyak atsiri dilakukan dengan metode penyulingan air (water
distillation).
Caranya : sebanyak 100 gramsimplisia dimasukkan kedalam labu alas bulat
berleher panjang 2 L ditambahkan air suling sampai sampel terendam,kemudian
dirangkai alat destilasi air. Destilasi dilakukan selama 4-5 jam. Minyak atsiri yang
diperoleh ditampung dalam corong pisah, setelah itu dipisahkan antara minyak
dan air,kemudian minyak atsiri yang diperoleh ditambahkan natrium sulfat
anhidrat, dikocok dan didiamkan selama 1 hari. Minyak atsiri dipipet dan
disimpan dalam botol berwarna gelap. Minyak yang diperoleh kemudian
3.5 Karakterisasi Minyak Atsiri
3.5.1 Penentuan indeks bias
Penentuan indeks bias dilakukan dengan menggunakan alat Refraktometer
Abbe.
Caranya : alat Refraktometer Abbe dihidupkan. Prisma atas dan prisma bawah
dipisahkan dengan membuka klem dan dibersihkan dengan mengoleskan kapas
yang telah dibasahi dengan alkohol dan dikeringkan. Cuplikan minyak diteteskan
ke prisma bawah lalu ditutup. Melalui teleskop dapat dilihat adanya bidang terang
dan bidang gelap lalu skrup pemutar prisma diputar sedemikian rupa, sehingga
bidang terang dan gelap terbagi atas dua bagian yang sama secara vertikal.
Dengan melihat skala dapat dibaca indeks biasnya.
3.5.2 Penentuan bobot jenis
Penentuan bobot jenis ditentukan dengan alat piknometer.
Caranya : piknometer kosong ditimbang dengan seksama. Piknometer kosong
diisi dengan air suling lalu ditimbang dengan seksama,kemudian piknometer
dikosongkan dan dibilas beberapa kali dengan alkohol kemudian dikeringkan
dengan bantuan hair dryer. Piknometer diisi minyak selanjutnya dilakukan seperti
pengerjaan pada air suling. Hasil bobot minyak atsiri yang diperoleh dengan
mengurangkan bobot piknometer yang diisi minyak atsiri dengan bobot
piknometer kosong. Bobot jenis minyak atsiri adalah hasil yang diperoleh dengan
membagi bobot minyak atsiri dengan bobot air suling dalam piknometer, kecuali
dinyatakan lain dalam monografi keduanya ditetapkan pada suhu 25ºC (Depkes
3.5.3 Analisis komponen minyak atsiri
Penentuan komponen minyak atsiri daun sirih hutan yang segar dan
simplisia dilakukan di Laboratorium Penelitian Fakultas Farmasi USU dengan
menggunakan seperangkat alat Gas Chromatography-Mass Spectrometer
(GC-MS) model Shimadzu QP 2010S.
Kondisi analisis GC adalah jenis kolom kapiler Rtx-1 MS, panjang kolom
30 m, diameter kolom dalam 0,25 mm, suhu injektor 270ºC, gas pembawa He
dengan laju alir 0,5 ml/menit. Suhu kolom terprogram (temperature programmed)
dengan suhu awal 60ºC selama 5 menit, lalu dinaikkan perlahan-lahan dengan laju
kenaikan 5,0ºC/menit sampai suhu akhir 280ºC yang dipertahankan selama 10
menit.
Cara identifikasi komponen minyak atsiri adalah dengan membandingkan
spektrum massa dari komponen minyak atsiri yang diperoleh (unknown) dengan
spektrum massa dalam data library yang memiliki tingkat kemiripan (similarity
BAB IV
HASIL DAN PEMBAHASAN
4.1 Identifikasi Tumbuhan
Hasil identifikasi tumbuhan yang dilakukan di “Herbarium Bogoriense”
Pusat Penelitian Biologi-LIPI Bogor terhadap daun sirih hutan yang diteliti adalah
jenis Piper caducibracteum C.DC dari suku Piperaceae.
4.2 Hasil Pemeriksaan Makroskopik Simplisia dan Mikroskopik Serbuk SimplisiaDaun Sirih Hutan.
4.2.1 Hasil pemeriksaan makroskopik simplisia
Pemeriksaan makroskopik simplisia daun sirih hutanmenunjukkan
simplisia berupa daun berbentuk bulat telur sampai lonjong, berwarna coklat
kehijauan, ujung runcing, ukuran panjang 15 cm dan lebar 3 cm. Gambar hasil
pemeriksaan makroskopik simplisia dapat dilihat pada Lampiran 3 halaman 62.
4.2.2 Hasil pemeriksaan mikroskopik serbuk simplisia
Hasil pemeriksaan mikroskopik serbuk simplisia adalah terdapatnya
fragmen-fragmen denganstomata anomositik, kelenjar minyak atsiri, rambut
penutup tipe multiseluler, sel-sel minyak dan berkas pembuluh xylem dengan
penebalan dinding bentuk spiral. Gambar hasil pemeriksaan mikroskopik serbuk
simplisia dapat dilihat pada Lampiran 4 halaman 63.
4.2.3 Hasil karakterisasi simplisia
Hasil karakterisasi simplisia daun sirih hutan yang diperoleh dapat dilihat
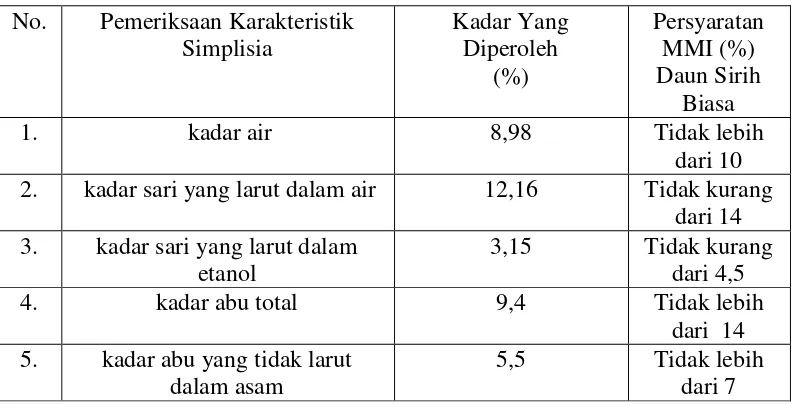
Tabel 3.1 Hasil karakterisasi simplisia daun sirih hutan
No. Pemeriksaan Karakteristik Simplisia Kadar Yang Diperoleh (%) Persyaratan MMI (%) Daun Sirih Biasa 1. kadar air 8,98 Tidak lebih
dari 10 2. kadar sari yang larut dalam air 12,16 Tidak kurang
dari 14 3. kadar sari yang larut dalam
etanol
3,15 Tidak kurang dari 4,5 4. kadar abu total 9,4 Tidak lebih
dari 14 5. kadar abu yang tidak larut
dalam asam
5,5 Tidak lebih dari 7
Hasil perhitungan kadar air simplisia daun sirih hutan selengkapnya dapat
dilihat pada Lampiran 6 halaman 67.Hasil pemeriksaan karakteristik simplisia
daun sirih hutan yaitu, kadar air sirih hutan 8,98%, (sirih biasa tidak lebih dari
10%), kadar abu total sirih hutan 9,4%, (sirih biasa tidak lebih dari 14%), kadar
abu tidak larut asam sirih hutan 5,5%, (sirih biasa tidak lebih dari 7%), kadar sari
larut dalam air sirih hutan 12,16%, (sirih biasa tidak kurang dari 14%), kadar sari
larut dalam etanol sirih hutan 3,15%, (sirih biasa tidak kurang dari 4,5%), kadar
minyak atsiri sirih hutan (simplisia) 1,23%, kadar minyak atsiri sirih hutan (daun
segar) 1,09%, (sirih biasa berkisar 0,9-1,2%).Kadar yang diperoleh dari hasil
karakterisasi simplisia dari daun sirih hutan tersebut memenuhi syarat sesuai
dengan standar Materia Medika Indonesia (MMI) edisi IV sehingga simplisia
dapat digunakan sebagai bahan penelitian.Hasil penelitian diperoleh kadar air
simplisia daun sirih hutan adalah 8,98%, hasil penelitian ini telah memenuhi
persyaratan MMI, dengan kadar air tidak lebih dari 10%, (Depkes RI,
simplisia yang digunakan, dari hasil penelitian diperoleh kadar air simplisia daun
sirih hutan 8,98%. Kadar air simplisia berhubungan denganupaya agar mutu
simplisia terjaga baik tidak ditumbuhi jamur. Apabila simplisia yang diinginkan
tidak cukup kering maka kemungkinan akan terjadi pertumbuhan jamur dan jasad
renik lainnya (BPOM RI, 2005).
Penetapan kadar sari dilakukan 2 pengujian yaitu kadar sari larut dalam
etanol dan air. Penetapan kadar sari simplisia menyatakan jumlah zat yang tersari
dalam air dan dalam etanol. Kadar sari yang larut dalam air dari simplisia daun
sirih hutan di peroleh lebih besar yaitu 12,16% dari pada kadar sari yang larut
dalam etanol 3,15%, hal ini berarti senyawa kimia yang tersari dalam air lebih
besar daripada yang tersari dalam etanol. Penetapan kadar sari yang larut dalam
air dan dalam etanol dilakukan untuk mengetahui jumlah senyawa yang dapat
tersari dalam air dan etanol dari suatu simplisia. Senyawa yang bersifat polar atau
larut dalam air akan tersari oleh air sedangkan senyawa-senyawa yang larut dalam
etanol akan tersari oleh etanol.
Penetapan kadar abu dimaksudkan untuk mengetahui kandungan mineral
internal yang terdapat didalam simplisia yang diteliti serta senyawa organik yang
tersisa selama pembakaran. Abu terbagi dua, yang pertama abu fisiologis adalah
abu yang berasal dari jaringan tumbuhan itu sendiri dan abu non fisiologis adalah
sisa setelah pembakaran yang berasal dari bahan-bahan dari luar (seperti pasir dan
tanah) yang terdapat pada permukaan simplisia (Depkes RI,1980).
Penetapan kadar minyak atsiri dengan menggunakan alat Stahl diketahui
bahwa minyak atsiri sirih hutan (simplisia) 1,23 %, minyak atsiri sirih hutan (daun
ini diketahui bahwa minyak atsiri lebih banyak terdapat pada daun sirih hutan
dibandingkan daun sirih biasa. Hal ini terjadi karena faktor lingkungan dimana
daun sirih hutan diperoleh dari hutan, sehingga faktor tersebut mempengaruhi
hasil metabolit yang diperoleh salah satunya adalah kadar minyak atsiri.
4.3 KarakterisasiMinyak Atsiri
Hasil karakterisasi minyak atsiri yang diperoleh dapat dilihat pada Tabel
[image:49.595.111.514.334.397.2]3.2 dibawah ini.
Tabel 3.2 Hasil penetapan kadar minyak atsiri dari daun segar dan simplisia
No. Sampel Kadar Minyak Atsiri (%v/b)
1. Daun Segar 1,09
2. Simplisia 1,23
Minyak atsiri yang di peroleh dengan menggunakan alat Stahl pada daun
sirih hutan simplisia 1,23% v/b, dan daun sirih hutan yang segar 1,09% v/b, dari
hasil diketahui bahwa minyak atsiri lebih banyak terdapat pada simplisia daripada
daun segar, disebabkan karena daun segar masih mengandung air sehingga
mempengaruhi hasil perhitungan kadar (persentase) minyak atsiri.
4.4 Penentuan Indeks Bias Dan Bobot Jenis Minyak Atsiri Hasil Isolasi
Hasil penentuan indeks bias dan bobot jenis minyak atsiri dapat dilihat
pada Tabel 3.3 dibawah ini. Hasil penentuan angka indeks bias minyak atsiri dari
daun sirih hutan segar dan simplisia yaitu 1,51797. Indeks bias merupakan
perbandingan antara kecepatan cahaya di udara dengan kecepatan cahaya di dalam
Tabel 3.3 Hasil penentuan indeks bias dan bobot jenis minyak atsiri hasil isolasi.
No. Sampel Indeks Bias Bobot Jenis
1. Simplisia 1,51797 1,0869
2. Daun Segar 1,51797 1,0867
Menurut Gunther, nilai indeks bias dapat dipengaruhi salah satunya oleh
adanya air dalam kandungan minyak atsiri, semakin banyak kandungan air, maka
semakin kecil nilai indeks biasnya. Ini karena sifat dari air yang mudah untuk
membiaskan cahaya yang datang (Armando, 2009).
Bobot jenis merupakan perbandingan dari suatu volume minyak atsiri
dengan berat air pada volume dan suhu yang sama. Dari data yang diperoleh
diketahui nilai bobot jenis minyak atsiri daun segar dan simplisia hampir tidak ada
bedanya disebabkan komponen kimia yang terkandung dalam minyak tersebut.
Bobot jenis adalah salah satu kriteria penting dalam menentukan mutu dan
kemurnian minyak atsiri. Nilai bobot jenis minyak berkisar 0,696-1,188 dan
umumnya lebih kecil dari 1,000 (Guenther, 1987).
4.5 Analisis Dengan GC-MS
4.5.1 Analisis komponen minyak atsiri dari daun sirih hutan segar
Hasil analisis komponen minyak atsiri hasil destilasi air dari daun sirih
huta