ISOLASI MINYAK ATSIRI DARI KULIT BUAH JERUK
KASTURI (Citrus microcarpa Bunge) SEGAR DAN
KERING SERTA ANALISIS KOMPONENNYA
SECARA GC-MS
SKRIPSI
Diajukan untuk melengkapi salah satu syarat untuk memperoleh
gelar Sarjana Farmasi pada Fakultas Farmasi
Universitas Sumatera Utara
OLEH:
TIOMANGSI M. SIHOTANG
NIM 091501074
PROGRAM STUDI SARJANA FARMASI
FAKULTAS FARMASI
UNIVERSITAS SUMATERA UTARA
MEDAN
ISOLASI MINYAK ATSIRI DARI KULIT BUAH JERUK
KASTURI (Citrus microcarpa Bunge) SEGAR DAN
KERING SERTA ANALISIS KOMPONENNYA
SECARA GC-MS
SKRIPSI
Diajukan untuk melengkapi salah satu syarat untuk memperoleh
Diajukan untuk melengkapi salah satu syarat untuk memperoleh
gelar Sarjana Farmasi pada Fakultas Farmasi
Universitas Sumatera Utara
rsitas Sumatera Utara
OLEH:
TIOMANGSI M. SIHOTANG
NIM 091501074
PROGRAM STUDI SARJANA FARMASI
FAKULTAS FARMASI
UNIVERSITAS SUMATERA UTARA
MEDAN
Prof. Dr. rer. nat. Effendy De Lux Putra, S.U., Apt.
NIP 195306191983031001
Dr. Marline Nainggolan, M.S., Apt. NIP 195709091985112001 Drs. Panal Sitorus, M.Si., Apt.
NIP 195310301980031002
PENGESAHAN SKRIPSI
ISOLASI MINYAK ATSIRI DARI KULIT BUAH JERUK
KASTURI (Citrus microcarpa Bunge) SEGAR DAN
KERING SERTA ANALISIS KOMPONENNYA
SECARA GC-MS
OLEH:
TIOMANGSI M. SIHOTANG
NIM 091501074
Dipertahankan dihadapan Panitia Penguji Skripsi Fakultas Farmasi Universitas Sumatera Utara Pada Tanggal: 31 Mei 2013
Pembimbing I,
Dr. Ginda Haro, M.Sc., Apt. NIP 195108161980031002
Drs. Panal Sitorus, M.Si., Apt. NIP 195310301980031002
Dra. Saleha Salbi, M.Si., Apt. NIP 194909061980032001
Prof. Dr. Sumadio Hadisahputra, Apt. NIP 195311281983031002
Panitia Penguji,
Pembimbing II,
Medan, Juli 2013 Fakultas Farmasi
KATA PENGANTAR
Puji dan syukur kehadirat Tuhan Yang Maha Esa, karena limpahan rahmat
kasih dan karuniaNya, sehingga penulis dapat menyelesaikan skripsi ini yang
berjudul ”Isolasi Minyak Atsiri dari Kulit Buah Jeruk Kasturi (Citrus microcarpa
Bunge) Segar dan Kering serta Analisis Komponennya Secara GC-MS”. Skripsi
ini diajukan sebagai salah satu syarat untuk memperoleh gelar sarjana farmasi
pada Fakultas Farmasi Universitas Sumatera Utara.
Pada kesempatan ini penulis menyampaikan ucapan terimakasih kepada
Bapak Prof. Dr. Sumadio Hadisahputra, Apt., selaku Dekan Fakultas Farmasi
Universitas Sumatera Utara yang telah memberikan fasilitas selama masa
pendidikan. Bapak Drs. Panal Sitorus, M.Si., Apt., selaku pembimbing yang telah
memberikan waktu, bimbingan dan nasehat selama penelitian hingga selesainya
penyusunan skripsi ini. Bapak Prof. Dr. rer. nat. Effendy De Lux Putra S.U., Apt.,
selaku penasehat akademis yang memberikan bimbingan kepada penulis dan juga
selaku pembimbing yang telah memberikan waktu, bimbingan dan nasehat selama
penelitian hingga selesainya penyusunan skripsi ini. Bapak dan Ibu staf pengajar
Fakultas Farmasi Universitas Sumatera Utara yang telah mendidik selama
perkuliahan. Bapak dan Ibu Kepala Laboratorium Penelitian dan Farmakognosi
yang telah memberikan fasilitas, petunjuk dan membantu selama penelitian.
Bapak Dr. Ginda Haro, M.Sc., Apt., Ibu Dr. Marline Nainggolan, M.S., Apt., dan
Dra. Saleha Salbi, M.Si., Apt., selaku dosen penguji yang memberikan masukan,
kritik, arahan dan saran dalam penyusunan skripsi ini.
Penulis juga ingin mempersembahkan rasa terima kasih yang tak terhingga
atas doa dan pengorbanannya dengan tulus dan ikhlas, untuk kakak dan abang
tersayang Nani Mariana Sihotang, Agustinus Sihotang, Parningotan Fidelis
Sihotang serta teman-teman STF 2009 yang selalu setia memberi doa, dorongan
juga semangat.
Penulis menyadari bahwa skripsi ini masih banyak kekurangannya, oleh
karena itu sangat diharapkan kritik dan saran yang bersifat membangun dari
semua pihak guna perbaikan skripsi ini. Akhir kata penulis berharap semoga
skripsi ini bermanfaat bagi ilmu pengetahuan khususnya bidang farmasi.
Medan, Juli 2013
Penulis,
ISOLASI MINYAK ATSIRI DARI KULIT BUAH JERUK KASTURI
(Citrus microcarpa Bunge) SEGAR DAN KERING SERTA ANALISIS
KOMPONENNYA SECARA GC-MS
ABSTRAK
Minyak atsiri merupakan minyak yang mudah menguap dengan komposisi yang berbeda-beda sesuai sumber penghasilnya dan terdiri dari campuran zat yang memiliki sifat fisika kimia berbeda-beda. Tumbuhan jeruk dari suku Rutaceae adalah salah satu tanaman yang mengandung minyak atsiri dan banyak dimanfaatkan masyarakat sebagai bumbu penyedap masakan dan pembuatan minuman. Salah satu dari tumbuhan jeruk yang dapat digunakan adalah jeruk kasturi (Citrus microcarpa Bunge). Penelitian yang dilakukan meliputi karakterisasi simplisia, isolasi minyak atsiri dengan cara destilasi air dan analisis komponen minyak atsiri secara Gas Chromatography-Mass Spectrometry (GC-MS) dari kulit buah jeruk kasturi segar dan kering.
Hasil pemeriksaan karakteristik simplisia kulit buah jeruk kasturi diperoleh kadar air 7,99%; kadar sari yang larut dalam air 21,76%; kadar sari yang larut dalam etanol 12,82%; kadar abu total 5,51%; kadar abu yang tidak larut dalam asam 0,35%; hasil penetapan kadar minyak atsiri dengan alat Stahl diperoleh kadar minyak atsiri kulit buah jeruk kasturi segar dan kering berturut-turut sebesar 0,93% v/b dan 1,27% v/b. Hasil penetapan indeks bias minyak atsiri kulit buah jeruk kasturi segar dan kering sama, yakni sebesar 1,4240. Bobot jenis minyak atsiri kulit buah jeruk kasturi segar dan kering berturut-turut sebesar 0,8526 dan 0,8522.
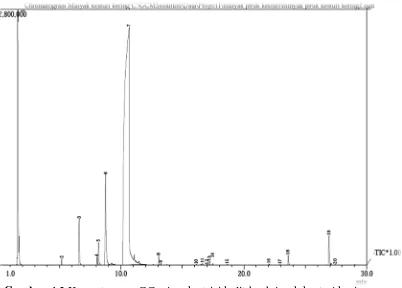
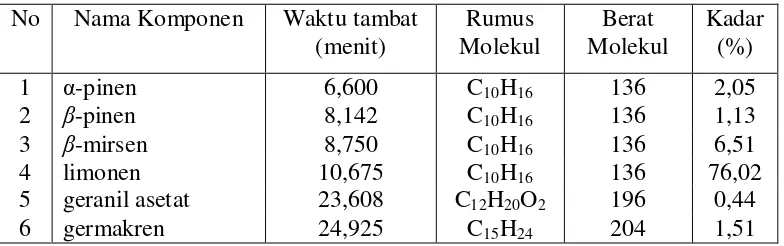
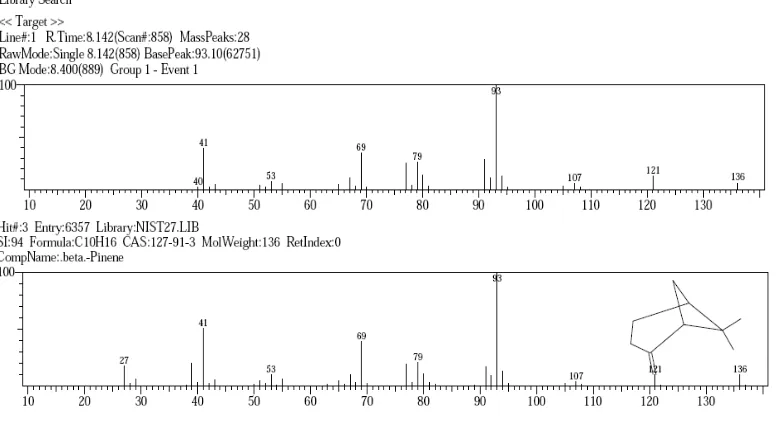
Hasil analisis GC-MS minyak atsiri yang diperoleh dari kulit buah jeruk kasturi (Citrus microcarpa Bunge) segar menunjukkan 23 komponen dengan 6 komponen utama yaitu: α-pinen (1,65%), β-pinen (1,15%), β-mirsen (6,26%), Limonen (77,03%), geranil asetat (0,56%) dan germakren (1,99%), sedangkan hasil analisis GC-MS minyak atsiri yang diperoleh dari kulit buah jeruk kasturi (Citrus microcarpa Bunge) kering menunjukkan 20 komponen dengan 6 komponen utama yaitu: α-pinen (2,05%), β-pinen (1,13%), β-mirsen (6,51%), limonen (76,02%), geranil asetat (0,44%) dan germakren (1,51%).
ISOLATION OF VOLATILE OIL FROM FRESH AND DRIED
Citrus microcarpa Bunge PEEL AND ANALYSIS OF THE COMPONENTS
BY GC-MS
ABSTRACT
Essential oil is volatile oil with different composition in accordance with the source and consists of a mixture with different physicochemical properties. Oranges are kind of plants containing essential oil and widely used as food flavoring or juice. One of them is Citrus microcarpa Bunge. This research was conducted on the characterization of botanicals, isolation of essential oil by water distillation and analysis of essential oil components by Gas Chromatography-Mass Spectrometry (GC-MS) of the fresh and dried peel of Citrus microcarpa
Bunge.
Test results of simplichia characterisation from Citrus microcarpa Bunge peel were level of water content 7.99%, level of water-soluble extract 21.76%, level of ethanol-soluble extract 12.82%, level of total ash 5.51%, level of acid- insoluble ash 0.35%, volatile oil content of fresh and dried Citrus microcarpa
Bunge peel consecutively 0.93% v/w and 1.27% v/w. The volatile oil of fresh and dried Citrus microcarpa Bunge peel had the same refractive index,m1.4240. Specific gravity of fresh and dried Citrus microcarpa Bunge peel consecutively were 0.8526 and specific gravity of dried Citrus microcarpa Bunge peel was 0.8522.
Gas Chromatography-Mass Spectrometry (GC-MS) analysis result of volatile oil from fresh Citrus microcarpa Bunge peel revealed 23 components with the presence of six main components, such as α-pinene (1.65%), β-pinene (1.15%), β-mirsene (6.26%), limonene (77.03%), geranyl acetate (0.56%), and germacrene (1.99%). Meanwhile GC-MS analysis result of volatile oil from dried
Citrus microcarpa Bunge peel revealed 20 components with the presence of six main components, such as α-pinene (2.05%), β-pinene (1.13%), β-mirsene (6.51%), limonene (76.02%), geranyl acetate (0.44%), and germacrene (1.51%).
DAFTAR ISI
Halaman
JUDUL ... i
HALAMAN JUDUL ... ii
LEMBAR PENGESAHAN ... iii
KATA PENGANTAR ... iv
ABSTRAK ... vi
ABSTRACT ... vii
DAFTAR ISI ... viii
DAFTAR TABEL ... xii
DAFTAR GAMBAR ... xiii
DAFTAR LAMPIRAN ... xv
BAB I PENDAHULUAN ... 1
1.1 Latar Belakang ... 1
1.2 Perumusan Masalah ... 3
1.3 Hipotesis ... 4
1.4 Tujuan Penelitian ... 4
1.5 Manfaat Penelitian ... 4
BAB II TINJAUAN PUSTAKA ... 5
2.1 Uraian Tumbuhan ... 5
2.1.1 Jeruk secara umum ... 5
2.1.2 Morfologi tumbuhan ... 5
2.1.3 Sistematika tumbuhan ... 6
2.1.5 Nama asing ... 6
2.1.6 Kandungan kimia ... 6
2.2 Minyak Atsiri ... 7
2.2.1 Aktivitas biologi dan kegunaan minyak atsiri ... 7
2.2.2 Komposisi minyak atsiri ... 8
2.3 Sifat Fisikokimia Minyak Atsiri ... 9
2.3.1 Sifat fisika minyak atsiri ... 9
2.3.2. Sifat kimia minyak atsiri ... 10
2.4 Isolasi Minyak Atsiri ... 11
2.4.1 Metode penyulingan ... 11
2.4.2 Metode pengepresan ... 12
2.4.3 Ekstraksi menggunakan pelarut mudah menguap ... 12
2.4.4 Ekstraksi dengan lemak padat ... 13
2.4.5 Ecuelle ... 13
2.5 Analisis Komponen Minyak Atsiri dengan GC-MS ... 14
2.5.1 Kromatografi gas ... 14
2.5.1.1 Gas pembawa ... 15
2.5.1.2 Sistem injeksi ... 15
2.5.1.3 Kolom ... 16
2.5.1.4 Fase diam ... 17
2.5.1.5 Suhu ... 17
2.5.1.6 Detektor ... 18
2.5.2 Spektrofotometri Massa ... 19
BAB III METODE PENELITIAN ... 21
3.2 Bahan ... 21
3.3 Penyiapan sampel ... 21
3.3.1 Pengambilan bahan ... 21
3.3.2 Identifikasi bahan ... 22
3.3.3 Pengolahan bahan ... 22
3.4 Pemeriksaan Makroskopik dan Mikroskopik Kulit Buah Jeruk Kasturi Segar ... 22
3.4.1 Pemeriksaan makroskopik ... 22
3.4.2 Pemeriksaan mikroskopik ... 23
3.5 Pemeriksaan Karakteristik Simplisia ... 23
3.5.1 Pemeriksaan makroskopik ... 23
3.5.2 Pemeriksaan mikroskopik ... 23
3.5.3 Penetapan kadar air ... 24
3.5.4 Penetapan kadar sari larut dalam air ... 24
3.5.5 Penetapan kadar sari larut dalam etanol ... 25
3.5.6 Penetapan kadar abu total ... 25
3.5.7 Penetapan kadar abu yang tidak larut dalam asam ... 25
3.6 Penetapan kadar minyak atsiri ... 26
3.7 Isolasi Minyak Atsiri ... 26
3.7.1 Isolasi minyak atsiri dari kulit buah jeruk kasturi segar ... 26
3.7.2 Isolasi minyak atsiri dari kulit buah jeruk kasturi kering ... 26
3.8 Identifikasi Minyak Atsiri ... 27
3.8.1 Penentuan indeks bias ... 27
3.8.2 Penentuan bobot jenis ... 27
BAB IV HASIL DAN PEMBAHASAN ... 29
4.1 Hasil identifikasi Tumbuhan ... 29
4.2 Hasil Pemeriksaan Makroskopik dan Mikroskopik Kulit Buah Jeruk Kasturi Segar ... 29
4.2.1 Hasil pemeriksaan makroskopik ... 29
4.2.2 Hasil pemeriksaan mikroskopik ... 29
4.3 Hasil Pemeriksaan Karakteristik Simplisia ... 30
4.3.1 Hasil pemeriksaan makroskopik ... 30
4.3.2 Hasil pemeriksaan mikroskopik ... 30
4.3.3 Hasil pemeriksaan karakterisasi simplisia ... 30
4.4 Hasil Penetapan Kadar Minyak Atsiri ... 32
4.5 Hasil Identifikasi Minyak Atsiri ... 32
4.6 Analisis dengan GC-MS ... 34
4.6.1 Analisis komponen minyak atsiri kulit buah jeruk kasturi segar ... 34
4.6.2 Analisis komponen minyak atsiri kulit buah jeruk kasturi kering ... 35
4.6.3 Analisis dan fragmentasi hasil spektrometri massa komponen minyak atsiri kulit buah jeruk kasturi segar . 37 4.6.4 Analisis dan fragmentasi hasil spektrometri massa komponen minyak atsiri kulit buah jeruk kasturi kering ... 44
BAB V KESIMPULAN DAN SARAN ... 52
5.1 Kesimpulan ... 52
5.2 Saran ... 53
DAFTAR PUSTAKA ... 54
DAFTAR TABEL
Halaman
Tabel 4.1 Hasil karakterisasi simplisia kulit buah jeruk kasturi ... 30
Tabel 4.2 Hasil penetapan kadar minyak atsiri ... 32
Tabel 4.3 Hasil penentuan indeks bias dan bobot jenis minyak atsiri hasil isolasi ... 32
Tabel 4.4 Waktu tambat dan konsentrasi komponen minyak atsiri hasil
analisis GC dari kulit buah jeruk kasturi segar ... 35
Tabel 4.5 Waktu tambat dan konsentrasi komponen minyak atsiri hasil
DAFTAR GAMBAR
Halaman
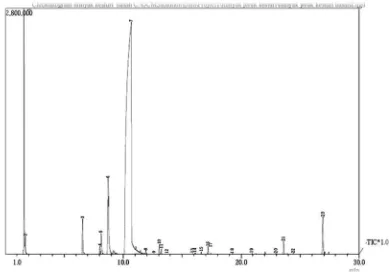
Gambar 4.1 Kromatogram minyak atsiri kulit buah jeruk
kasturi segar ... 34
Gambar 4.2 Kromatogram minyak atsiri kulit buah jeruk kasturi kering ... 35
Gambar 4.3 Spektrum massa puncak dengan Rt 6,567 menit ... 38
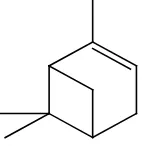
Gambar 4.4 Rumus bangun senyawa α-pinen ... 38
Gambar 4.5. Spektrum massa puncak dengan Rt8,142 menit ... 39
Gambar 4.6 Rumus bangun senyawa β-pinen ... 39
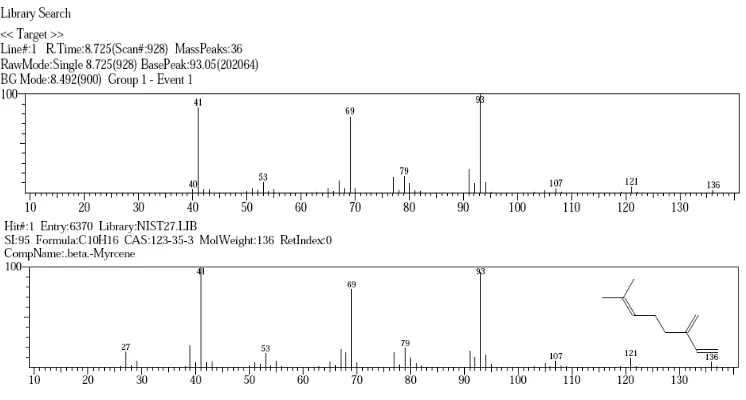
Gambar 4.7 Spektrum massa puncak dengan Rt 8,725 menit ... 40
Gambar 4.8 Rumus bangun senyawa β-mirsen ... 40
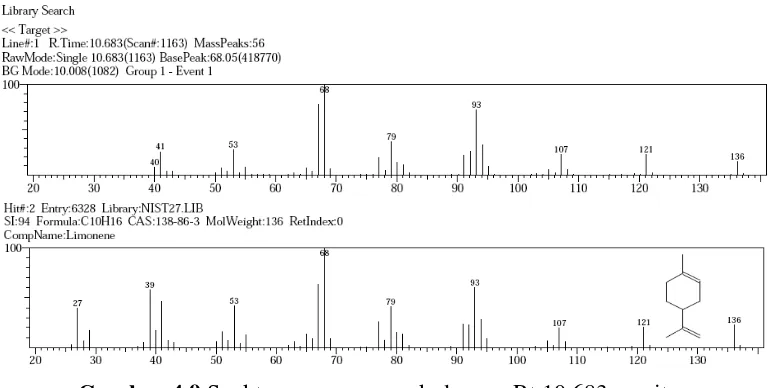
Gambar 4.9 Spektrum massa puncak dengan Rt 10,683 menit ... 41
Gambar 4.10 Rumus bangun senyawa limonen ... 41
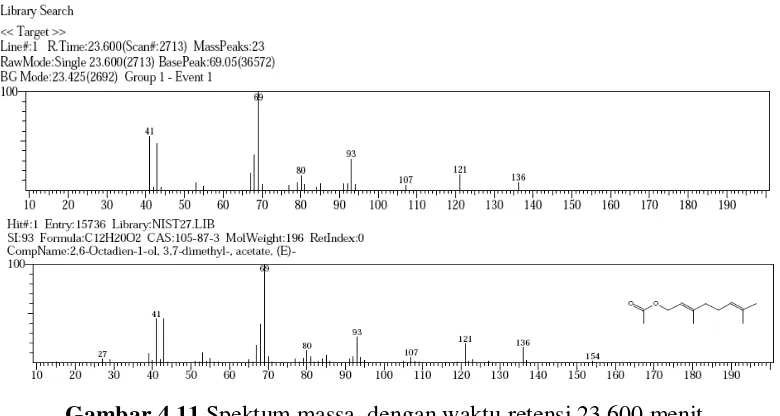
Gambar 4.11 Spektrum massa puncak dengan Rt 23,600 menit ... 42
Gambar 4.12 Rumus bangun senyawa geranil asetat ... 42
Gambar 4.13 Spektrum massa puncak dengan 26,917 menit ... 43
Gambar 4.14 Rumus bangun senyawa germakren ... 44
Gambar 4.15 Spektrum massa puncak dengan Rt 6,600 menit ... 45
Gambar 4.16 Rumus bangun senyawa α-pinen ... 45
Gambar 4.17 Spektrum massa puncak dengan Rt 8,142 menit ... 46
Gambar 4.18 Rumus bangun senyawa β-pinen ... 46
Gambar 4.19 Spektrum massa puncak dengan Rt 8,750 menit ... 47
Gambar 4.20 Rumus bangun senyawa β-mirsen ... 47
Gambar 4.22 Rumus bangun senyawa limonen ... 48
Gambar 4.23 Spektrum massa puncak dengan Rt 23,608 menit ... 49
Gambar 4.24 Rumus bangun senyawa geranil asetat ... 50
Gambar 4.25 Spektrum massa puncak dengan Rt 26,925 menit ... 50
DAFTAR LAMPIRAN
Halaman
Lampiran 1. Hasil identifikasi tumbuhan ... 57
Lampiran 2. Gambar tumbuhan jeruk kasturi dan buah jeruk kasturi ... 58
Lampiran 3. Gambar kulit buah jeruk kasturi segar dan kering dan serbuk simplisia kulit buah jeruk kasturi ... 59
Lampiran 4. Hasil pemeriksaan mikroskopik penampang melintang kulit buah jeruk kasturi segar ... 60
Lampiran 5. Hasil pemeriksaan mikroskopik serbuk simplisia kulit buah jeruk kasturi ... 61
Lampiran 6. Alat– alat yang digunakan ... 62
Lampiran 7. Perhitungan penetapan kadar air dari simplisia kulit buah
jeruk kasturi ... 65
Lampiran 8. Perhitungan penetapan kadar sari larut air dari simplisia kulit buah jeruk kasturi ... 66
Lampiran 9. Perhitungan penetapan kadar sari larut etanol dari
simplisia kulit buah jeruk kasturi ... 67
Lampiran 10. Perhitungan penetapan kadar abu total dari simplisia
kulit buah jeruk kasturi ... 68
Lampiran 11. Perhitungan penetapan kadar abu tidak larut asam dari
simplisia kulit buah jeruk kasturi ... 69
Lampiran 12. Penetapan kadar minyak atsiri kulit buah jeruk kasturi
segar ... 70
Lampiran 13. Penetapan kadar minyak atsiri kulit buah jeruk kasturi
kering ... 71
Lampiran 14. Penetapan indeks bias minyak atsiri kulit buah jeruk kasturi segar ... 72
Lampiran 15. Penetapan indeks bias minyak atsiri kulit buah jeruk kasturi kering ... 73
Lampiran 17. Penetapan bobot jenis minyak atsiri kulit buah jeruk kasturi kering ... 75
Lampiran 18. Flowsheet isolasi minyak atsiri kulit buah jeruk kasturi
(Citrus microcarpa Bunge) ... 76
Lampiran 19. Kromatogram GC minyak atsiri kulit buah jeruk kasturi
segar ... 77
Lampiran 20. Pola fragmentasi komponen minyak atsiri kulit buah
jeruk kasturi segar ... 79
Lampiran 21. Kromatogram GC minyak atsiri kulit buah jeruk kasturi
kering ... 82
Lampiran 22. Pola fragmentasi komponen minyak atsiri kulit buah
ISOLASI MINYAK ATSIRI DARI KULIT BUAH JERUK KASTURI
(Citrus microcarpa Bunge) SEGAR DAN KERING SERTA ANALISIS
KOMPONENNYA SECARA GC-MS
ABSTRAK
Minyak atsiri merupakan minyak yang mudah menguap dengan komposisi yang berbeda-beda sesuai sumber penghasilnya dan terdiri dari campuran zat yang memiliki sifat fisika kimia berbeda-beda. Tumbuhan jeruk dari suku Rutaceae adalah salah satu tanaman yang mengandung minyak atsiri dan banyak dimanfaatkan masyarakat sebagai bumbu penyedap masakan dan pembuatan minuman. Salah satu dari tumbuhan jeruk yang dapat digunakan adalah jeruk kasturi (Citrus microcarpa Bunge). Penelitian yang dilakukan meliputi karakterisasi simplisia, isolasi minyak atsiri dengan cara destilasi air dan analisis komponen minyak atsiri secara Gas Chromatography-Mass Spectrometry (GC-MS) dari kulit buah jeruk kasturi segar dan kering.
Hasil pemeriksaan karakteristik simplisia kulit buah jeruk kasturi diperoleh kadar air 7,99%; kadar sari yang larut dalam air 21,76%; kadar sari yang larut dalam etanol 12,82%; kadar abu total 5,51%; kadar abu yang tidak larut dalam asam 0,35%; hasil penetapan kadar minyak atsiri dengan alat Stahl diperoleh kadar minyak atsiri kulit buah jeruk kasturi segar dan kering berturut-turut sebesar 0,93% v/b dan 1,27% v/b. Hasil penetapan indeks bias minyak atsiri kulit buah jeruk kasturi segar dan kering sama, yakni sebesar 1,4240. Bobot jenis minyak atsiri kulit buah jeruk kasturi segar dan kering berturut-turut sebesar 0,8526 dan 0,8522.
Hasil analisis GC-MS minyak atsiri yang diperoleh dari kulit buah jeruk kasturi (Citrus microcarpa Bunge) segar menunjukkan 23 komponen dengan 6 komponen utama yaitu: α-pinen (1,65%), β-pinen (1,15%), β-mirsen (6,26%), Limonen (77,03%), geranil asetat (0,56%) dan germakren (1,99%), sedangkan hasil analisis GC-MS minyak atsiri yang diperoleh dari kulit buah jeruk kasturi (Citrus microcarpa Bunge) kering menunjukkan 20 komponen dengan 6 komponen utama yaitu: α-pinen (2,05%), β-pinen (1,13%), β-mirsen (6,51%), limonen (76,02%), geranil asetat (0,44%) dan germakren (1,51%).
ISOLATION OF VOLATILE OIL FROM FRESH AND DRIED
Citrus microcarpa Bunge PEEL AND ANALYSIS OF THE COMPONENTS
BY GC-MS
ABSTRACT
Essential oil is volatile oil with different composition in accordance with the source and consists of a mixture with different physicochemical properties. Oranges are kind of plants containing essential oil and widely used as food flavoring or juice. One of them is Citrus microcarpa Bunge. This research was conducted on the characterization of botanicals, isolation of essential oil by water distillation and analysis of essential oil components by Gas Chromatography-Mass Spectrometry (GC-MS) of the fresh and dried peel of Citrus microcarpa
Bunge.
Test results of simplichia characterisation from Citrus microcarpa Bunge peel were level of water content 7.99%, level of water-soluble extract 21.76%, level of ethanol-soluble extract 12.82%, level of total ash 5.51%, level of acid- insoluble ash 0.35%, volatile oil content of fresh and dried Citrus microcarpa
Bunge peel consecutively 0.93% v/w and 1.27% v/w. The volatile oil of fresh and dried Citrus microcarpa Bunge peel had the same refractive index,m1.4240. Specific gravity of fresh and dried Citrus microcarpa Bunge peel consecutively were 0.8526 and specific gravity of dried Citrus microcarpa Bunge peel was 0.8522.
Gas Chromatography-Mass Spectrometry (GC-MS) analysis result of volatile oil from fresh Citrus microcarpa Bunge peel revealed 23 components with the presence of six main components, such as α-pinene (1.65%), β-pinene (1.15%), β-mirsene (6.26%), limonene (77.03%), geranyl acetate (0.56%), and germacrene (1.99%). Meanwhile GC-MS analysis result of volatile oil from dried
Citrus microcarpa Bunge peel revealed 20 components with the presence of six main components, such as α-pinene (2.05%), β-pinene (1.13%), β-mirsene (6.51%), limonene (76.02%), geranyl acetate (0.44%), and germacrene (1.51%).
BAB I PENDAHULUAN
1.1Latar Belakang
Tumbuhan penghasil minyak atsiri yang saat ini tumbuh di wilayah
Indonesia hampir seluruhnya sudah dikenal oleh sebagian masyarakat, bahkan
beberapa jenis tumbuhan penghasil minyak atsiri menjadi bahan yang sangat
penting dalam kehidupan sehari-hari. Minyak atsiri dihasilkan dari bagian
tumbuhan tertentu seperti akar, batang, kulit, daun, bunga atau biji (Lutony dan
Rahmayati, 1994).
Minyak atsiri adalah zat berbau yang terkandung dalam tanaman, disebut
juga minyak menguap, minyak eteris atau minyak esensial karena mudah
menguap pada suhu kamar. Istilah esensial dipakai karena minyak atsiri mewakili
bau tanaman asalnya (Gunawan dan Mulyani, 2004).
Kegunaan minyak atsiri sangat luas dan spesifik, khususnya dalam
berbagai bidang industri, antara lain industri kosmetik, seperti industri parfum,
digunakan sebagai pewangi dalam berbagai produk minyak wangi, industri
makanan digunakan sebagai bahan penyedap atau penambah cita rasa, industri
farmasi atau obat-obatan (Lutony dan Rahmayati, 1994).
Minyak atsiri dari bagian kulit buah jeruk banyak digunakan sebagai
flavoring agent untuk berbagai makanan dan minuman, seperti: minuman beralkohol dan non alkohol, roti panggang, kembang gula, puding, gelatin desert, permen karet, dan bahan obat-obatan sebagai antinyeri, antiinfeksi, pembunuh
bakteri, dalam industri bahan pengawet, bahkan digunakan pula sebagai
Kulit jeruk merupakan limbah yang dapat diolah untuk menghasilkan produk bernilai tinggi, yaitu minyak atsiri. Produk ini disukai oleh konsumen untuk keperluan kesehatan dan bahan pengharum (Anonim, 2008).
Jeruk kasturi berasal dari Filipina yang dikenal dengan nama kalamansi
dan telah dibudidayakan secara luas. Jeruk ini tumbuh mencapai ketinggian 3-4
meter dengan buah yang relatif sangat kecil dibandingkan jeruk-jeruk jenis lain,
berbau khas dan sering dipakai sebagai bumbu masak. Di Indonesia jenis ini biasa
dikenal dengan nama jeruk limau dan umumnya digunakan sebagai penyedap
masakan dan dimanfaatkan sebagai obat batuk, gatal- gatal ataupun penghilang bau badan (Jamal, dkk., 2000).
Sejumlah penelitian telah dilakukan terhadap tumbuhan jeruk kasturi ini. Cheong, dkk., (2011) telah mengisolasi minyak atsiri dari kulit buah jeruk kasturi dan diperoleh komponen utama antara lain limonen, β-mirsen, β-pinen, α-pinen,
β-feladren dan sabinen. Jamal, dkk., (2000) menguji aktivitas minyak atsiri dari
kulit buah dan daun jeruk kasturi terhadap bakteri E. Coli, Salmonella entridis,
Staphylococcus epidermidis dan Staphylococcus aureus, dimana pada konsentrasi 25% telah dihasilkan diameter daerah hambat (DDH) yang setara dengan DDH
yang dihasilkan oleh kloramfenikol 50 ppm. Komponen utama minyak atsiri yang dihasilkan antara lain 4-metil-1-(1-metiletil)-3-sikloheksen-1-ol, β-linalool, α -terpineol, α-farnesena, β-sitral, L-isopulegol dan cis-linalil oksida.
melakukan karakterisasi sesuai dengan cara karakterisasi yang terdapat dalam
Materia Medika Indonesia untuk memperoleh karakteristik dari simplisia kulit
buah jeruk kasturi.
Berdasarkan pertimbangan uraian di atas, penulis tertarik memanfaatkan
kulit buah jeruk kasturi sebagai bahan penelitian. Bagian yang digunakan adalah
kulit buah yang masih segar dan yang sudah dikeringkan. Isolasi minyak atsiri
dilakukan dengan penyulingan air (Water distillation), karena metode ini mudah dilakukan dan hingga kini masih banyak digunakan oleh para perajin minyak atsiri
di berbagai negara, khususnya negara yang sedang berkembang termasuk
Indonesia (Lutony dan Rahmayati, 1994). Pelaksanaan penelitian meliput i
karakterisasi simplisia, isolasi serta analisis komponen minyak atsiri secara Gas
Chromatography-Mass Spectrometer (GC-MS) dari kulit buah jeruk kasturi segar dan kering.
1.2 Perumusan Masalah
Berdasarkan latar belakang di atas dapat diambil perumusan masalah,
yaitu:
1. Apakah karakteristik dari simplisia kulit buah jeruk kasturi dapat diperoleh
dengan menggunakan metode karakterisasi yang tertera pada Materia
Medika Indonesia?
2. Apakah terdapat perbedaan kadar minyak atsiri dari kulit buah jeruk
kasturi segar dan kering?
3. Apakah terdapat perbedaan komponen minyak atsiri dari kulit buah jeruk
1.3 Hipotesis
Berdasarkan perumusan masalah di atas maka dibuat hipotesis, yaitu:
1. Karakteristik dari simplisia kulit buah jeruk kasturi dapat diperoleh dengan
menggunakan metode karakterisasi yang tertera pada Materia Medika
Indonesia.
2. Terdapat perbedaan kadar minyak atsiri dari kulit buah jeruk kasturi segar
dan kering.
3. Terdapat perbedaan komponen minyak atsiri dari kulit buah jeruk kasturi
segar dan kering.
1.4 Tujuan Penelitian
1. Untuk mengetahui karakteristik dari simplisia kulit buah jeruk kasturi
diperoleh dengan menggunakan metode karakterisasi yang tertera pada
Materia Medika Indonesia.
2. Untuk mengetahui perbedaan kadar minyak atsiri dari kulit buah jeruk
kasturi segar dan kering.
3. Untuk mengetahui perbedaan komponen minyak atsiri dari kulit buah
jeruk kasturi segar dan kering.
1.5 Manfaat Penelitian
Hasil dari penelitian ini diharapkan memberikan informasi tentang kandungan
minyak atsiri dari kulit buah jeruk kasturi serta sebagai informasi
pemanfaatan limbah kulit buah jeruk kasturi sehingga memiliki nilai
BAB II
TINJAUAN PUSTAKA
2.1 Uraian Tumbuhan 2.1.1 Jeruk secara umum
Tanaman jeruk-jerukan, suku Rutaceae, banyak dibudidayakan orang dan
beranggotakan tidak kurang dari 1300 jenis tanaman. Suku Rutaceae dibagi dalam
tujuh sub famili (anak suku) dan 130 genus (marga), dimana yang menjadi induk
tanaman jeruk adalah sub famili Aurantioideae yang beranggotakan 33 genus.
Beberapa contoh spesies Citrus antara lain jeruk keprok (Citrus nobilis),
jeruk manis (Citrus aurantium), jeruk lemon (Citrus medica), jeruk besar (Citrus
maxima), jeruk grafefruit (Citrus paradise), jeruk kasturi (Citrus microcarpa), jeruk sambal (Citrus amblycarpa), jeruk purut (Citrus histrix), jeruk nipis (Citrus
aurantifolia) dan lain- lain (Sarwono, 1995).
2.1.2 Morfologi tumbuhan
Jeruk kasturi merupakan jenis tanaman jeruk dengan tinggi pohon 2-4
meter dan tajuk yang agak bulat, daun tersebar, berdaun majemuk beranak satu,
agak kecil, berwarna hijau tua bertangkai pendek, pada tepi daun terdapat bintil-
bintil kelenjar berbau sedap. Bunga majemuk, terletak diketiak daun atau pada
ujung cabang, berbau harum, waktu masih kuncup berbentuk bulat telur panjang,
daun pelindung kecil, kelopak berbentuk cawan terdiri dari 5 helai. Bakal buah
berbentuk bola, pada pangkal dan ujung datar, berwarna hijau kuning. Buah
berbentuk kecil, bertangkai pendek, berwarna kuning saat matang, hampir
berbentuk seperti bola, diameternya 3-5 cm dengan kulit buah yang tipis
2.1.3 Sistematika tumbuhan
Menurut Sarwono (1995) dan LIPI (2012), sistematika tumbuhan jeruk
kasturi adalah sebagai berikut:
Divisi : Spermatophyta
Subdivisi : Angiospermae
Kelas : Dicotyledonae
Bangsa : Rutales
Suku : Rutaceae
Marga : Citrus
Jenis : Citrus microcarpa (Bunge) Wijnands
2.1.4 Nama lain
Nama lain dari jeruk kasturi adalah jeruk peras dan jeruk potong (Anonim,
2010).
2.1.5 Nama asing
Nama asing dari jeruk kasturi adalah kalamansi (Filipina), calamondin,
chinese orange, golden lime (Inggris), limau chuit (Malaysia) (Anonim, 2010; Jamal, dkk., 2000).
2.1.6 Kandungan kimia
Kulit buah jeruk kasturi mengandung 1,2% minyak atsiri. Komponen
utama minyak atsiri tersebut adalah β-sitronelol (18%), β-pinen (15,31%) dan
D-limonen (14%). Selain itu, komponen lain yang terkandung dalam minyak atsiri
kulit buah jeruk kasturi adalah 4-metil-1-(1-metiletil)-3-sikloheksen-1-ol, β -linalool, α-terpineol, α-farnesena, β-sitral, L-isopulegol dan cis-linalil oksida
2.2 Minyak Atsiri
Minyak atsiri adalah zat berbau yang terkandung dalam tanaman. Minyak
ini disebut juga minyak menguap (volatile oil), minyak eteris (ethereal oil), atau
minyak esensial (essential oil). Minyak atsiri umumnya tidak berwarna pada keadaan segar dan murni, namun pada penyimpanan lama warnanya dapat
berubah menjadi lebih gelap. Pencegahannya, minyak atsiri harus terlindung dari
pengaruh cahaya, diisi penuh, ditutup rapat serta disimpan di tempat yang kering
dan gelap (Gunawan dan Mulyani, 2004; Ketaren, 1985).
Minyak atsiri terdapat dalam berbagai organ tumbuhan, seperti didalam
rambut kelenjar (famili Labiatae), didalam sel-sel parenkim (suku Zingiberaceae
dan Piperaceae), didalam saluran minyak yang disebut vittae (suku Umbelliferae),
didalam rongga-rongga skizogen dan lisigen (suku Myrtaceae, Pinaceae dan
Rutaceae), terkandung didalam semua jaringan (suku Conifera). Minyak atsiri
dapat terbentuk secara langsung oleh protoplasma akibat adanya peruraian lapisan
resin pada dinding sel atau oleh hidrolisis dari glikosida tertentu (Tyler et al,
1977).
2.2.1 Akivitas biologi dan kegunaan minyak atsiri
Minyak atsiri pada tumbuhan mempunyai dua fungsi yaitu: membantu
proses penyerbukan dengan menarik perhatian beberapa jenis serangga atau
hewan (atraktan) dan mencegah kerusakan tanaman oleh serangga atau hewan
(repellent). Minyak atsiri pada tumbuhan juga dapat digunakan sebagai sumber energi, antimikroba, penutup bagian kayu yang terluka dan mencegah penguapan
Minyak atsiri digunakan sebagai bahan baku dalam berbagai industri,
misalnya industri parfum, kosmetik, farmasi, bahan penyedap dalam industri
makanan dan minuman (Guenther, 1987).
Beberapa jenis bahan tumbuhan digunakan dalam pengobatan karena
kandungan minyak atsirinya. Pada beberapa kasus, minyak atsiri digunakan
sebagai obat setelah diekstraksi atau disuling dari sumbernya, misalnya minyak
kayu putih. Dalam bentuk murni, kebanyakan minyak atsiri dapat digunakan
untuk terapi beberapa jenis penyakit seperti radang selaput sendi, radang
tenggorokan, sakit kepala, radang usus besar, jantung berdebar dan lain
sebagainya (Agusta, 2000; Rusli, 2010).
2.2.2 Komposisi minyak atsiri
Minyak atsiri terdiri dari berbagai campuran persenyawaan kimia dengan
sifat fisika dan kimia yang juga berbeda. Pada umumnya perbedaan komposisi
minyak atsiri disebabkan perbedaan kondisi iklim, tanah tempat tumbuh, umur
panen, metode ekstraksi yang digunakan, cara penyiapan minyak atsiri dan jenis
tanaman penghasil.
Minyak atsiri biasanya terdiri dari berbagai campuran persenyawaan kimia
yang terbentuk dari unsur Karbon (C), Hidrogen (H), dan Oksigen (O).
Pada umumnya komponen kimia minyak atsiri dibagi menjadi dua golongan
yaitu:
a. Golongan Hidrokarbon
Persenyawaan yang termasuk golongan ini terbentuk dari unsur Karbon (C)
dan Hidrogen (H). Jenis hidrokarbon yang terdapat dalam minyak atsiri
isopren) yang titik didihnya berbeda, titik didih monoterpen sebesar 140o
C-180oC dan sesquiterpen > 200oC (Harborne, 1987; Ketaren 1985).
b. Golongan Hidrokarbon Teroksigenasi
Komponen kimia dari golongan persenyawaan ini terbentuk dari unsur Karbon
(C), Hidrogen (H) dan Oksigen (O). Persenyawaan yang termasuk dalam
golongan ini adalah persenyawaan alkohol, aldehid, keton, ester, eter dan
peroksid. Ikatan karbon yang terdapat dalam molekulnya dapat terdiri dari
ikatan tunggal, ikatan rangkap dua dan ikatan rangkap tiga. Golongan
hidrokarbon teroksigenasi merupakan senyawa yang penting dalam minyak
atsiri karena umumnya mempunyai aroma yang lebih wangi (Ketaren, 1985).
2.3 Sifat Fisikokimia Minyak Atsiri 2.3.1 Sifat fisika minyak atsiri
Parameter yang dapat digunakan untuk tetapan fisika minyak atsiri antara
lain:
a. Bau yang khas
Minyak atsiri adalah zat berbau, biasa dikenal dengan nama minyak eteris atau
minyak terbang (essential oil, volatile oil) yang dihasilkan oleh tanaman.
Minyak tersebut berbau wangi sesuai dengan bau tanaman penghasilnya
(Ketaren, 1985).
b. Indeks bias
Indeks bias suatu zat adalah perbandingan kecepatan cahaya dalam udara dan
kecepatan cahaya dalam zat tersebut. Jika cahaya melewati media kurang padat
ke media lebih padat maka sinar akan membelok atau membias dari garis
ketidakmurnian, penentuannya menggunakan alat refraktometer (Guenther,
1987).
c. Berat jenis
Nilai berat jenis (densitas) minyak atsiri merupakan perbandingan antara berat
minyak dengan berat air pada volume air yang samadengan volume minyak.
Berat jenis sering dihubuungkan dengan berat komponen yang terkandung
didalamnya. Semakin besar fraksi berat yang terkandung dalam minyak,
semakin besar pula nilai densitasnya. Berat jenis merupakan salah satu kriteria
penting dalam menentukan mutu dan kemurnian minyak atsiri (Armando,
2009).
d. Putaran optik
Setiap jenis minyak atsiri mempunyai kemampuan memutar bidang polarisasi
cahaya ke arah kiri atau kanan. Besarnya pemutaran bidang polarisasi
ditentukan oleh jenis minyak atsiri, suhu dan panjang gelombang cahaya yang
digunakan. Penentuan putaran optik menggunakan alat polarimeter dan
nilainya dinyatakan dengan derajat disosiasi (Armando, 2009; Ketaren, 1985).
2.3.2 Sifat kimia minyak atsiri
Perubahan sifat kimia minyak atsiri merupakan ciri dari adanya suatu
kerusakan minyak dan ini dapat terjadi pada beberapa jenis minyak atsiri.
Kerusakan minyak atsiri yang mengakibatkan perubahan antara lain dapat terjadi
selama penyimpanan dan biasanya disebabkan oleh terjadinya oksidasi,
polimerisasi serta hidrolisis, karena peristiwa tersebut maka minyak atsiri akan
berubah warna dan menjadi lebih kental. Proses-proses tersebut diaktifkan oleh
panas, oksigen udara, lembab, sinar matahari dan molekul logam berat. Minyak
setidaknya dapat diperlambat. Oleh karena itu, minyak atsiri sebaiknya disimpan
dalam wadah yang benar-benar kering dan harus bebas dari logam berat, serta
bebas dari cahaya yang masuk (Koensoemardiyah, 2010).
2.4 Isolasi Minyak Atsiri
Isolasi minyak atsiri dapat dilakukan dengan beberapa cara yaitu: 1)
penyulingan (distillation), 2) pengepresan (pressing), 3) ekstraksi dengan pelarut menguap (solvent extraction), 4) ekstraksi dengan lemak padat, 5) ecuelle.
2.4.1 Metode penyulingan
Penyulingan adalah salah satu metode untuk memisahkan komponen-
komponen suatu campuran dari dua jenis campuran atau lebih berdasarkan
perbedaan tekanan uap dari masing- masing zat tersebut. Metode penyulingan
minyak atsiri yang sering dilakukan antara lain:
a. Penyulingan dengan air (water distillation)
Pada metode ini, bahan tumbuhan dimasukkan dalam wadah yang berisi air,
selanjutnya direbus sampai uap air dan minyaknya mengalir dan didinginkan
melalui pipa dalam kondensor. Air dan minyak yang keluar dari kondensor
ditampung dalam labu pemisah (Yuliani dan Satuhu, 2012).
b. Penyulingan dengan air dan uap (water and steam distillation)
Bahan tumbuhan yang akan disuling dengan metode penyulingan air dan uap
ditempatkan dalam suatu tempat yang bagian bawah dan tengah
berlobang-lobang yang ditopang di atas dasar alat penyulingan. Ketel diisi dengan air
sampai permukaan air berada tidak jauh di bawah saringan, uap air akan naik
bersama minyak atsiri kemudian dialirkan melalui pendingin. Hasil
c. Penyulingan dengan uap (Steam distillation)
Pada metode ini, wadah dan tangki air sebagai sumber uap panas (boiler) diletakkan terpisah, di dalam boiler terdapat pipa yang berhubungan dengan
wadah. Air dari boiler akan mendidih, lalu uapnya mengalir ke wadah yang berisi bahan tumbuhan. Uap akan menembus sel-sel tumbuhan dan membawa
uap minyak atsiri yang selanjutnya akan mengalir melalui kondensor. Uap
minyak atsiri akan mengembun menjadi cairan dan ditampung pada labu
pemisah (Guenther, 1987; Yuliani dan Satuhu, 2012).
2.4.2 Metode pengepresan
Ekstraksi minyak atsiri dengan cara pengepresan umumnya dilakukan
terhadap bahan berupa biji, buah, atau kulit buah yang memiliki kandungan
minyak atsiri yang cukup tinggi. Akibat tekanan pengepresan, maka sel-sel yang
mengandung minyak atsiri akan pecah dan minyak atsiri akan mengalir ke
permukaan bahan (Ketaren, 1985).
2.4.3 Ekstraksi menggunakan pelarut mudah menguap
Metode ini digunakan untuk mengambil minyak bunga yang kurang stabil
dan dapat rusak oleh panas uap air. Dengan menggunakan pelarut yang mudah
menguap seperti kloroform, eter, aseton, alkohol dan petroleum eter. Pada
ekstraksi ini, bahan pelarut dialirkan secara berkesinambungan melalui
serangkaian penampan yang diisi bahan tumbuhan, sampai ekstraksi selesai.
Cairan ekstrak yang mengandung bahan pelarut dan unsur-unsur tumbuhan itu
disalurkan ke tabung hampa udara yang dipanaskan pada suhu sekedar untuk
menguapkan pelarut. Uap pelarut dialirkan ke kondensor untuk dicairkan kembali,
sedangkan unsur-unsur tumbuhan tertinggal dalam tabung hampa tersebut
2.4.4 Ekstraksi dengan lemak padat
Proses ini umumnya digunakan untuk mengekstraksi bunga-bungaan,
untuk mendapatkan mutu dan rendeman minyak atsiri yang tinggi. Metode
ekstraksi dapat dilakukan dengan dua cara, yaitu:
a. Ekstraksi dengan lemak tanpa pemanasan (Enfleurage)
Cara ini menggunakan media lemak padat. Metode ini digunakan karena
diketahui beberapa jenis bunga yang telah dipetik, enzimnya masih
menunjukkan kegiatan dalam menghasilkan minyak atsiri sampai beberapa
hari/minggu, seperti bunga melati, sehingga perlu perlakuan yang tidak
merusak enzim tersebut secara langsung. Caranya dengan menaburkan bunga
diatas media lilin dan dieramkan sampai beberapa hari/minggu, selanjutnya
lemak padat dikerok (dikenal dengan pomade) dan diekstraksi menggunakan
etanol (Gunawan dan Mulyani, 2004).
b. Ekstraksi dengan lemak panas
Pada cara ini absorbsi minyak atsiri oleh lemak dalam keadaan panas pada
suhu 80oC selama 1,5 jam. Cara ini dilakukan terhadap bahan tumbuhan yang
bila dilakukan penyulingan atau enfleurasi akan menghasilkan minyak atsiri
dengan rendeman yang rendah. Setelah selesai pemanasan, campuran disaring
panas-panas, jika perlu kelebihan lemak pada ampas disiram dengan air panas,
kemudian dilakukan penyulingan untuk memperoleh minyak atsiri (Ketaren,
1985).
2.4.5 Ecuelle
Metode mengeluarkan minyak jeruk dengan menusuk kelenjar minyak dan
Tonjolan tersebut cukup panjang untuk menembus epidermis. Tetes minyak yang
jatuh pada wadah kemudian dikumpulkan (Tyler et al., 1977).
2.5Analisis Komponen Minyak Atsiri dengan GC-MS
Analisis dan karakterisasi komponen minyak atsiri merupakan masalah
yang cukup rumit, ditambah dengan sifatnya yang mudah menguap pada suhu
kamar sehingga perlu diseleksi metode yang akan diterapkan untuk menganalisis
minyak atsiri. Sejak ditemukannya kromatografi gas (GC), kendala dalam analisis
komponen minyak atsiri ini mulai dapat diatasi walaupun terbatas hanya pada
analisis kualitatif dan penentuan kuantitatif komponen penyusun minyak atsiri
saja. Pada penggunaan GC, efek penguapan dapat dihindari bahkan dihilangkan
sama sekali. Perkembangan teknologi instrumentasi yang sangat pesat akhirnya
dapat melahirkan suatu alat yag merupakan gabungan dua sistem dengan prinsip
dasar yang berbeda satu sama lain tetapi dapat saling menguntungkan dan saling
melengkapi, yaitu gabungan antara kromatografi gas dan spektrometri massa
(GC-MS). Pada alat GC-MS, kedua alat dihubungkan dengan suatu interfase.
Kromatografi gas disini berfungsi sebagai alat pemisah berbagai komponen
campuran dalam sampel sedangkan spektrometer massa berfungsi untuk
mendeteksi masing-masing molekul komponen yang telah dipisahkan pada
kromatografi gas (Agusta, 2000).
2.5.1 Kromatografi gas
Kromatografi gas merupakan teknik pemisahan yang mana solut- solut
yang mudah menguap (dan stabil terhadap panas) bermigrasi melalui kolom yang
mengandung fase diam dengan suatu kecepatan yang tergantung pada rasio
titik didihnya, kecuali jika ada interaksi khusus antara solut dengan fase diam.
Pemisahan pada kromatografi gas didasarkan pada titik didih suatu senyawa
dikurangi dengan semua interaksi yang mungkin terjadi antara solut dengan fase
diam. Fase gerak yang berupa gas akan mengelusi solut dari ujung kolom lalu
menghantarkannya ke detektor. Penggunaan suhu yang meningkat (biasanya
kisaran 50oC- 350oC) bertujuan untuk menjamin bahwa solut akan menguap dan
karenanya akan cepat terelusi (Gandjar dan Rohman, 2008).
Komponen campuran dapat diidentifikasi dengan menggunakan waktu
tambat (waktu retensi) yang khas pada kondisi yang tepat. Waktu tambat ialah
waktu yang menunjukkan beberapa lama suatu senyawa tertahan dalam kolom
yang diukur mulai saat penyuntikan sampel sampai saat elusi terjadi (dihasilkan
puncak) (Gritter, dkk., 1991). Bagian utama dari kromatografi gas adalah gas
pembawa, sistem injeksi, kolom, fase diam, suhu dan detektor.
2.5.1.1 Gas pembawa
Gas pembawa harus memenuhi sejumlah persyaratan, antara lain harus
inert (tidak bereaksi dengan sampel, pelarut sampel, material dalam kolom), murni
dan mudah diperoleh. Gas pembawa yang paling sering dipakai adalah helium
(He), argon (Ar), nitrogen (N2), hidrogen (H2) dan karbondioksida (CO2).
Keuntungannya adalah karena semua gas ini tidak reaktif dan dapat dibeli dalam
keadaan murni dan kering yang dikemas dalam tangki bertekanan tinggi.
Pemiliihan gas pembawa tergantung pada detektor yang dipakai (Agusta, 2000).
2.5.1.2 Sistem injeksi
Sistem injeksi pada GC-MS dilakukan dengan menyuntikkan cuplikan ke
suntik harus dipanaskan tersendiri, terpisah dari kolom dan biasanya pada suhu
10-15oC lebih tinggi dari suhu kolom. Seluruh cuplikan diuapkan segera setelah
disuntikkan dan dibawa ke kolom (Gritter, dkk., 1991).
2.5.1.3 Kolom
Kolom merupakan tempat terjadinya proses pemisahan karena di
dalamnya terdapat fase diam (Gandjar dan Rohman, 2008). Kolom dapat terbuat
dari tembaga, baja tahan karat, aluminium atau gelas. Kolom dapat berbentuk
lurus, melengkung, ataupun gulungan spiral sehingga lebih menghemat ruang.
Ada dua macam kolom, yaitu kolom kemas dan kolom kapiler (Agusta, 2000;
McNair dan Bonelli, 1988).
Kolom kemas terdiri dari fase cair (sekurang- kurangnya pada suhu
kromatografi) yang tersebar pada permukaan penyangga yang lembam (inert)
yang terdapat dalam tabung yang relatif besar (diameter dalam 1-3 mm). Jenis
kolom ini terbuat dari gelas atau logam yang tahan karat atau dari tembaga dan
aluminium. Efisiensi kolom akan meningkat dengan semakin bertambah halusnya
partikel fase diam ini. Semakin kecil diameter partikel fase diam, maka
efisiensinya akan meningkat. Ukuran partikel fase diam biasanya berkisar antara
60- 80 mesh (Gandjar dan Rohman, 2008).
Kolom kapiler berbeda dengan kolom kemas, dalam hal adanya rongga
pada bagian dalam kolom yang menyerupai pipa (tube) dengan ukuran 0,02-0,2
mm. Kolom kapiler kini lebih banyak digunakan untuk menganalisis komponen
minyak atsiri. Hal ini disebabkan oleh kelebihan kolom tersebut yang memberikan
hasil analisis dengan daya pisah yang tinggi dan sekaligus memiliki sensitivitas yang
tinggi. Keuntungan kolom kapiler adalah jumlah sampel yang dibutuhkan sedikit dan
2.5.1.4 Fase diam
Fase diam dibedakan berdasarkan kepolarannya, yaitu nonpolar, semi polar,
dan polar. Berdasarkan minyak atsiri yang non polar sampai sedikit polar, maka untuk
keperluan analisis sebaiknya digunakan kolom fase diam yang bersifat non polar,
misalnya SE-52 dan SE-54. Jika dalam analisis minyak atsiri digunakan kolom yang
lebih polar, sejumlah puncak yang dihasilkan menjadi lebar (tidak tajam) dan
sebagian puncak tersebut juga membentuk ekor. Begitu juga dengan garis dasarnya
tidak rata dan terlihat bergelombang. Bahkan kemungkinan besar komponen yang
bersifat nonpolar tidak akan terdeteksi sama sekali (Agusta, 2000).
2.5.1.5Suhu
a. Suhu injektor
Suhu pada injektor harus cukup panas untuk menguapkam cuplikan sedemikian
cepat, tetapi sebaliknya suhu harus cukup rendah untuk mencegah peruraian
atau penataan ulang akibat panas (Gandjar dan Rohman, 2008).
b. Suhu kolom
Kromatografi gas didasarkan pada 2 sifat senyawa yang dipisahkan yakni,
kelarutan senyawa dalam cairan tertentu dan tekanan uapnya atau keatsiriannya
(titik didih senyawa). Oleh karena tekanan uap berbanding langsung dengan
suhu, maka suhu merupakan faktor yang utama pada kromatografi gas
(Gandjar dan Rohman, 2008). Pemisahan dapat dilakukan pada suhu tetap
(isotermal) atau pada suhu yang berubah secara terkendali (suhu diprogram,
temperature programming). GC isotermal paling banyak dilakukan pada analisis rutin atau jika kita mengetahui agak banyak mengenai sifat sampel
Pilihan awal yang baik adalah suhu beberapa derajat dibawah titik didih
komponen utama sampel. Pada GC suhu diprogram, suhu dinaikkan mulai dari
suhu tertentu sampai suhu tertentu lainnya dengan laju yang diketahui dan
terkendali pada waktu tertentu (Gritter, dkk., 1991).
c. Suhu detektor
Detektor harus cukup panas sehingga cuplikan/fase diam tidak mengembun
dan juga untuk mencegah pengembunan air atau hasil samping yang terbentuk
pada proses pengionan (McNair dan Bonelli, 1988).
2.5.1.6 Detektor
Detektor merupakan perangkat yang diletakkan pada ujung kolom tempat
keluar fase gerak (gas pembawa) yang membawa komponen hasil pemisahan.
Detektor pada kromatografi adalah suatu sensor elektronik yang berfungsi
mengubah sinyal gas pembawa dan komponen-komponen didalamnya menjadi
sinyal elektronik. Sinyal elektronik detektor akan sangat berguna untuk analisa
kuanlitatif maupun kuantitatif terhadap komponen-komponen yang terpisah
diantara fase diam dan fase gerak (Gandjar dan Rohman, 2008).
Beberapa jenis detektor adalah Flame Photometric Detector (FPD) yang digunakan untuk indikasi selektif dari fosfor dan sulfur. Nitrogen Phosphorous
Detector (NPD) yang digunakan untuk senyawa-senyawa yang mengandung nitrogen dan fosfor. Electron Capture Detector (ECD) yang digunakan untuk
senyawa-senyawa organik kelompok elektrofilik (elektro negatif), seperti halogen,
peroksida dan nitro. Mass Spectrometric Detector (MSD) yaitu merupakan sambungan langsung dari suatu spektrometer massa dengan suatu kolom dalam
2.5.2 Spektrometri Massa
Suatu spektrometer massa bekerja dengan membangkitkan molekul-
molekul bermuatan atau fragmen- fragmen molekul baik dalam keadaan sangat
hampa atau segera sebelum sampel memasuki ruang sangat hampa (Watson,
2010). Molekul senyawa organik pada spektrometer massa, ditembak dengan
berkas elektron dan menghasilkan ion bermuatan positif yang mempunyai energi
yang tinggi karena lepasnya elektron dari molekul yang dapat pecah menjadi ion
yang lebih kecil (Sastrohamidjojo, 2004).
Spektrum massa hasil analisis sistem spektroskopi massa merupakan
gambaran mengenai jenis dan jumlah fragmen molekul yang terbentuk dari suatu
komponen kimia (masing-masing puncak pada kromatogram). Setiap fragmen
yang terbentuk dari pemecahan suatu komponen kimia memiliki berat molekul
yang berbeda dan ditampilkan dalam bentuk diagram dua dimensi, m/z (m/e,
massa/muatan) pada sumbu X dan intensitas pada sumbu Y yang disebut dengan
spektrum massa. Pola pemecahan (fragmentasi) molekul yang terbentuk untuk
setiap komponen kimia sangat spesifik sehingga dapat dijadikan sebagai patokan
untuk menentukan struktur molekul suatu komponen kimia. Selanjutnya,
spektrum massa komponen kimia yang diperoleh dari hasil analisis diidentifikasi
dengan cara dibandingkan dengan spektrum massa yang terdapat dalam suatu
bank data (Agusta, 2000).
Spektrometer massa terdiri dari sistem pemasukan cuplikan, ruang
pengion dan percepatan, tabung analisis, pengumpul ion dan penguat dan
pencatat. Keuntungan utama spektrometri massa sebagai metode analisis yaitu
metode ini lebih sensitif dan spesifik untuk identifikasi senyawa yang tidak
Hal ini disebabkan adanya pola fragmentasi yang khas sehingga dapat
memberikan informasi mengenai bobot molekul dan rumus molekul. Puncak ion
molekul penting dikenali karena memberikan bobot molekul senyawa yang
diperiksa. Puncak paling kuat pada spektrum, disebut puncak dasar (base peak), dinyatakan dengan nilai 100% dan kekuatan puncak lain, termasuk puncak ion
molekulnya dinyatakan sebagai persentase puncak dasar tersebut (Silverstein,
BAB III
METODE PENELITIAN
Metode penelitian ini meliputi penyiapan sampel, pemeriksaan
karakteristik simplisia, isolasi minyak atsiri kulit buah jeruk kasturi (Citrus
microcarpa Bunge) segar dan kering serta analisis komponen-komponen minyak atsirinya secara GC-MS.
3.1 Alat
Alat-alat yang digunakan dalam penelitian adalah alat-alat gelas
laboratorium, mikroskop, refraktometer Abbe, piknometer, oven, neraca listrik (Mettler Toledo), neraca kasar (Ohaus), alat Stahl, alat destilasi air (Water
Distillation), Gas Chromatograph-Mass Spectrometer (GC-MS) model Shimadzu
QP 2010 Plus.
3.2 Bahan
Bahan-bahan yang digunakan dalam penelitian ini adalah kulit buah jeruk
kasturi segar dan kering, natrium sulfat anhidrat p.a (E. Merck), kloralhidrat p.a
(E. Merck), kloroform p.a (E. Merck), etanol 96%, toluen p.a, HCl p.a, dan air suling.
3.3 Penyiapan Sampel 3.3.1 Pengambilan bahan
Metode pengambilan bahan dilakukan dengan cara purposif yaitu diambil
daerah lain. Bahan diperoleh dari Pasar Tradisional Padangbulan, Kelurahan Titi
Rante, Kecamatan Medan Baru, Medan tanpa membandingkan dengan bahan
yang sama dari daerah lain. Sampel yang digunakan adalah kulit buah jeruk
kasturi (Citrus microcarpa Bunge) segar dan kering.
3.3.2 Identifikasi bahan
Identifikasi bahan dilakukan di Herbarium Bogoriense, Bidang Botani Pusat, Pusat Penelitian Biologi, Lembaga Ilmu Pengetahuan Indonesia (LIPI)
Bogor. Hasil determinasi dapat dilihat pada Lampiran 1, halaman 57.
3.3.3 Pengolahan bahan
Pengolahan bahan dilakukan terhadap buah jeruk kasturi. Buah kasturi
yang digunakan adalah buah yang berwarna hijau kekuningan dengan diameter
4-6 cm. Buah dibersihkan dari kotoran yang melekat, disortasi lalu dicuci dengan air
sampai bersih, ditiriskan lalu buah dikupas, bagian flavedo dan albedonya
dipisahkan kemudian dibagi dua. Sebagian ditimbang sebagai sampel kulit buah
jeruk kasturi segar.
Sebagian kulit buah jeruk kasturi segar dikeringkan di lemari pengering
pada suhu 50-60oC (sekitar 1 minggu) sampai menjadi simplisia kemudian
ditimbang.
3.4 Pemeriksaan Makroskopik dan Mikroskopik Kulit Buah Jeruk Kasturi Segar
3.4.1 Pemeriksaan makroskopik
Pemeriksaan makroskopik dilakukan dengan memperhatikan bentuk,
3.4.2 Pemeriksaan mikroskopik
Pemeriksaan mikroskopik dilakukan terhadap penampang melintang dari
kulit buah jeruk kasturi segar.
Caranya: 2-3 tetes larutan kloralhidrat diteteskan di atas kaca objek lalu sayatan
kulit buah segar diletakkan diatasnya, kemudian ditutup dengan kaca penutup,
dipanaskan, lalu diamati di bawah mikroskop.
3.5 Pemeriksaan Karakteristik Simplisia
Pemeriksaan karakteristik simplisia meliputi pemeriksaan makroskopik,
pemeriksaan mikroskopik, penetapan kadar air, penetapan kadar sari larut dalam
air, penetapan kadar sari larut dalam etanol, penetapan kadar abu total, penetapan
kadar abu tidak larut dalam asam.
3.5.1 Pemeriksaan makroskopik
Pemeriksaan makroskopik dilakukan dengan mengamati bentuk luar,
ukuran serta warna dari kulit buah jeruk kasturi kering.
3.5.2 Pemeriksaan mikroskopik
Pemeriksaan mikroskopik dilakukan terhadap serbuk simplisia kulit buah
jeruk kasturi.
Caranya: serbuk simplisia ditaburkan diatas kaca objek yang telah ditetesi dengan
larutan kloralhidrat dan tutup dengan kaca penutup, kemudian diamati di bawah
3.5.3 Penetapan kadar air a. Penjenuhan toluen
Sebanyak 200 ml toluen dan 2 ml air suling dimasukkan ke dalam labu
alas bulat, dipasang alat penampung dan pendingin, kemudian didestilasi selama 2
jam. Destilasi dihentikan dan dibiarkan dingin selama 30 menit, kemudian volume
air dalam tabung penerima dibaca dengan ketelitian 0,05 ml.
b. Penetapan kadar air simplisia
Sebanyak 5 gram serbuk simplisia yang telah ditimbang seksama
dimasukkan ke dalam labu lalu dipanaskan hati-hati selama 15 menit. Setelah
toluen mendidih, kecepatan tetesan diatur 2 tetes untuk tiap detik sampai sebagian
besar air terdestilasi, kemudian kecepatan tetesan diatur 2 tetes untuk tiap detik
sampai sebagian besar air terdestilasi, kemudian kecepatan destilasi dinaikkan
sampai 4 tetes tiap detik. Setelah semua air terdestilasi, bagian dalam pendingin
dibilas dengan toluen. Destilasi dilanjutkan selama 5 menit, kemudian tabung
penerima dibiarkan mendingin pada suhu kamar. Setelah air dan toluen memisah
sempurna, volume air dibaca dengan ketelitian 0,05 ml. Selisih kedua volume air
yang dibaca sesuai dengan kandungan air yang terdapat dalam bahan yang
diperiksa. Kadar air dihitung dalam persen (WHO, 1998).
3.5.4 Penetapan kadar sari larut dalam air
Sebanyak 5 gram serbuk simplisia yang telah dikeringkan, dimaserasi
selama 24 jam dalam 100 ml air-kloroform (2,5 ml kloroform dalam air suling
sampai 1 liter) dalam labu bersumbat sambil dikocok sesekali selama 6 jam
pertama, dibiarkan selama 18 jam, kemudian disaring. Sejumlah 20 ml filtrat
pertama diuapkan sampai kering dalam cawan penguap yang berdasar rata yang
Kadar dalam persen sari yang larut dalam air dihitung terhadap bahan yang telah
dikeringkan (Depkes, 1995).
3.5.5 Penetapan kadar sari larut dalam etanol
Sebanyak 5 gram serbuk simplisia yang telah dikeringkan, dimaserasi
selama 24 jam dalam 100 ml etanol 95% dalam labu bersumbat sambil dikocok
sesekali selama 6 jam pertama, kemudian dibiarkan selama 18 jam. Kemudian
disaring cepat untuk menghindari penguapan etanol. Sejumlah 20 ml filtrat
diuapkan sampai kering dalam cawan penguap yang berdasar rata yang telah
dipanaskan dan ditara. Sisa dipanaskan pada suhu 105oC sampai bobot tetap.
Kadar dalam persen sari yang larut dalam etanol 95% dihitung terhadap bahan
yang telah dikeringkan (Depkes, 1995).
3.5.6 Penetapan kadar abu total
Sebanyak 2 gram serbuk simplisia yang telah digerus dan ditimbang
seksama dimasukkan dalam krus porselin yang telah dipijar dan ditara, kemudian
diratakan. Krus dipijar perlahan-lahan sampai arang habis, pijaran dilakukan pada
suhu 500-600oC selama 3 jam kemudian didinginkan dan ditimbang sampai
diperoleh bobot tetap. Kadar abu dihitung terhadap bahan yang telah dikeringkan
(WHO, 1998).
3.5.7 Penetapan kadar abu tidak larut dalam asam
Abu yang diperoleh dalam penetapan kadar abu dididihkan dalam 25 ml
asam klorida encer selama 5 menit, bagian yang tidak larut dalam asam
dikumpulkan, disaring melalui kertas saring dipijarkan sampai bobot tetap,
kemudian didinginkan dan ditimbang. Kadar abu yang tidak larut dalam asam
3.6 Penetapan kadar minyak atsiri
Penetapan kadar minyak atsiri dilakukan dengan menggunakan alat Stahl. Caranya: sebanyak 15 g kulit buah jeruk kasturi yang telah dirajang dimasukkan
dalam labu alas bulat berleher pendek, ditambahkan air suling sebanyak 300 ml,
labu diletakkan di atas pemanas listrik. Hubungkan labu dengan pendingin dan
alat penampung berskala, buret diisi air sampai penuh, selanjutnya dilakukan
destilasi. Setelah penyulingan selesai, biarkan tidak kurang dari 15 menit, catat
volume minyak atsiri pada buret. Hitung kadar minyak atsiri dalam % v/b (Ditjen
POM, 1979).
3.7 Isolasi Minyak Atsiri
Isolasi minyak atsiri dilakukan dengan metode penyulingan air (water
distillation).
3.7.1 Isolasi minyak atsiri kulit buah jeruk kasturi segar
Sebanyak 200 gram sampel yang telah dirajang dimasukkan dalam labu
alas datar berleher panjang 2 L ditambahkan air suling sampai sampel terendam.
Kemudian dirangkai alat destilasi air. Destilasi dilakukan selama 4-5 jam. Minyak
atsiri yang diperoleh ditampung dalam corong pisah setelah itu dipisahkan antara
minyak dan air, kemudian minyak atsiri yang diperoleh ditambahkan natrium
sulfat anhidrat, dikocok dan didiamkan selama 1 hari. Minyak atsiri dipipet dan
disimpan dalam botol berwarna gelap (Guenther, 1987; Yuliani dan Satuhu,
2012).
3.7.2. Isolasi minyak atsiri kulit buah jeruk kasturi kering
Sebanyak 100 gram sampel yang telah dirajang dimasukkan dalam labu
Kemudian dirangkai alat destilasi air. Destilasi dilakukan selama 4-5 jam. Minyak
atsiri yang diperoleh ditampung dalam corong pisah setelah itu dipisahkan antara
minyak dan air, kemudian minyak atsiri yang diperoleh ditambahkan natrium
sulfat anhidrat, dikocok dan didiamkan selama 1 hari. Minyak atsiri dipipet dan
disimpan dalam botol berwarna gelap (Guenther, 1987; Yuliani dan Satuhu,
2012).
3.8 Identifikasi Minyak Atsiri 3.8.1 Penentuan indeks bias
Penentua indeks bias dilakukan dengan alat refraktometer Abbe.
Caranya: Alat refraktometer Abbe dihidupkan. Prisma atas dan prisma bawah dipisahkan dengan membuka klem dan dibersihkan dengan mengoleskan kapas
yang telah dibasahi dengan alkohol. Cuplikan minyak diteteskan ke prisma bawah
lalu ditutup. Melalui teleskop dapat dilihat adanya bidang terang dan bidang gelap
lalu skrup pemutar prisma diputar sedemikian rupa, sehingga bidang terang dan
gelap terbagi atas dua bagian yang sama secara vertikal. Dengan melihat skala
dapat dibaca indeks biasnya.
3.8.2. Penentuan bobot jenis
Penentuan bobot jenis dilakukan dengan alat piknometer.
Caranya: piknometer kosong ditimbang dengan seksama. Piknometer kosong diisi
dengan air suling lalu ditimbang dengan seksama. Piknometer dikosongkan dan
dibilas beberapa kali dengan alkohol kemudian dikeringkan dengan bantuan
hairdryer. Piknometer diisi minyak selanjutnya dilakukan seperti pengerjaan pada air suling. Hasil bobot minyak atsiri yang diperoleh dengan mengurangkan bobot
minyak atsiri adalah hasil yang diperoleh dengan membagi bobot minyak atsiri
dengan bobot air suling dalam piknometer, kecuali dinyatakan lain dalam
monograf keduanya ditetapkan pada suhu 25oC (Ditjen POM, 1995).
3.9 Analisis Komponen Minyak Atsiri
Penentuan komponen minyak atsiri dilakukan di Laboratorium Penelitian
Fakultas Farmasi USU dengan menggunakan seperangkat alat GC-MS model
Shimadzu QP-2010 Plus dan Auto Injecto AOC-20i.
Kondisi analisis adalah jenis kolom kapiler Rtx-5 MS, panjang kolom 3 m,
diameter dalam kolom 0,25 mm, suhu injektor 270oC, gas pembawa He dengan
laju alir 1,16 ml/menit. Suhu kolom terprogram (temperature programming) dengan suhu awal 60oC selama 5 menit, lalu dinaikkan perlahan-lahan dengan laju
kenaikan 5,0oC/menit sampai suhu akhir 280oC yang dipertahankan.
Cara identifikasi komponen minyak atsiri adalah dengan membandingkan
spektrum massa dan komponen minyak atsiri yang diperoleh (unknown) dengan
BAB IV
HASIL DAN PEMBAHASAN
4.1 Hasil Identifikasi Tumbuhan
Hasil identifikasi yang dilakukan di Herbarium Bogoriense, Bidang
Botani, Pusat Penelitian Biologi, Lembaga Ilmu Pengetahuan Indonesia (LIPI)
Bogor terhadap tumbuhan jeruk kasturi menunjukkan bahwa jeruk kasturi adalah
jeruk Citrus microcarpa Bunge dari suku Rutaceae. Hasil identifikasi dapat
dilihat pada Lampiran 1, halaman 57.
4.2 Hasil Pemeriksaan Makroskopik dan Mikroskopik Kulit Buah Jeruk Kasturi Segar
4.2.1 Hasil pemeriksaan makroskopik
Hasil pemeriksaan makroskopik kulit buah jeruk kasturi segar dicirikan
dengan kulit buah berwarna hijau, bagian dalam berwarna putih, kulit tipis, berupa
potongan-potongan kecil kulit buah, panjang kira-kira 3-4 cm, lebar 1-2 cm dan
berbau khas. Gambar dapat dilihat pada Lampiran 3, halaman 59.
4.2.2 Hasil pemeriksaan mikroskopik
Hasil pemeriksaan mikroskopik pada penampang melintang kulit buah
jeruk kasturi segar tampak kutikula, bagian sel epidermis, kristal kalsium oksalat
berbentuk prisma, rongga lisigen, kelenjar minyak, bagian sel parenkim dan
4.3 Hasil Pemeriksaan Karakteristik Simplisia 4.3.1 Hasil pemeriksaan makroskopik
Hasil pemeriksaan makroskopik simplisia kulit buah jeruk kasturi kering
dicirikan dengan kulit buah berwarna hijau kecoklatan, bagian dalam berwarna
putih kecoklatan, menggulung ke dalam, berupa potongan-potongan kecil kulit
buah yang telah dikeringkan dan berbau khas. Serbuk simplisia kulit buah jeruk
kasturi dicirikan dengan serbuk berwarna hijau kecoklatan dan berbau khas.
Gambar dapat dilihat pada Lampiran 3, halaman 59.
4.3.2 Hasil pemeriksaan mikroskopik
Hasil pemeriksaan mikroskopik serbuk simplisia kulit buah jeruk kasturi
tampak parenkim, fragmen rongga lisigen, kristal kalsium oksalat bentuk prisma
dan berkas pembuluh. Gambar dapat dilihat pada Lampiran 5, halaman 61.
4.3.3 Hasil pemeriksaan karakterisasi simplisia
Karakteristik simplisia dari kulit buah jeruk kasturi dapat dilihat pada
Tabel 4.1 (data selengkapnya dapat dilihat pada Lampiran 7-11, halaman 65-69).
Berdasarkan tabel diatas dapat dilihat bahwa kadar air yang diperoleh dari
simplisia kulit buah jeruk kasturi adalah sama yakni sebesar 7,99%, namun
terdapat perbedaan untuk karakteristik yang lain. Hal ini kemungkinan disebabkan
No Karakteristik Hasil pemeriksaan
(%) Hasil pemeriksaan (%) literatur* 1. 2. 3. 4. 5. Kadar air
Kadar sari larut air Kadar sari larut etanol Kadar abu total
Kadar abu tidak larut asam
[image:48.595.108.500.520.668.2]7,99 21,76 18,82 5,51 0,35 7,99 27,15 10,68 7,81 0,90
Tabel 4.1 Hasil karakterisasi simplisia kulit buah jeruk kasturi
oleh perbedaan tempat pengambilan sampel (sumber sampel) dimana karakteristik
simplisia dipengaruhi oleh lingkungan tempat tumbuh seperti kondisi tanah,
cuaca, kondisi udara, umur tumbuhan dan sebagainya (BPOM, 2005).
Pengeringan simplisia dilakukan untuk mendapatkan simplisia yang tidak
mudah rusak sehingga dapat disimpan dalam waktu yang lebih lama. Penurunan
mutu atau kerusakan simplisia dapat dicegah dengan mengurangi kadar air dan
penghentian reaksi enzimatik. Kadar air simplisia kulit buah jeruk kasturi yang
diperoleh yaitu 7,99% dan memenuhi peryaratan literatur untuk kadar air simplisia
yaitu kurang dari 10% (BPOM, 2005; Trease dan Evans, 1983).
Penetapan kadar sari larut dalam air dan dalam etanol dilakukan untuk
mengetahui jumlah senyawa yang dapat tersari dalam air dan dalam etanol dari
suatu simplisia. Senyawa yang bersifat polar dan larut dalam air pada simplisia
kulit buah jeruk kasturi seperti glikosida, protein, polisakarida dan zat warna akan
tersari oleh air dengan hasil 27,15% sedangkan senyawa-senyawa yang tidak larut
dalam air dan larut dalam etanol seperti flavonoid, steroid serta antrakinon akan
tersari oleh etanol dengan hasil 10,68% (Depkes, 1986; Ginting, 2012).
Penetapan kadar abu dimaksudkan untuk mengetahui kandungan mineral
internal yang terdapat di dalam simplisia serta senyawa organik yang tersisa
selama pemijaran.
Abu total terbagi dua yang pertama abu fisiologis adalah abu yang berasal
dari jaringan tumbuhan itu sendiri dan abu non fisiologis adalah sisa setelah
pembakaran yang berasal dari bahan-bahan dari luar yang terdapat pada
permukaan simplisia. Kadar abu tidak larut asam untuk menentukan jumlah silika,
khususnya pasir yang ada pada simplisia dengan cara melarutkan abu total dalam
Tabel 4.3 Hasil penentuan indeks bias dan bobot jenis minyak atsiri hasil isolasi
4.4 Hasil Penetapan Kadar Minyak Atsiri
Penetapan kadar minyak atsiri dengan menggunakan alat Stahl diketahui bahwa kadar minyak atsiri kulit buah jeruk kasturi segar adalah 0,93% v/b,
sementara pada kulit buah jeruk kasturi kering adalah 1,27% v/b, dari hasil ini
diketahui bahwa minyak atsiri lebih banyak terdapat pada kulit buah jeruk kasturi
kering. Hal ini disebabkan oleh kadar air pada kulit buah jeruk kasturi kering lebih
sedikit dibandingkan kadar air pada kulit buah jeruk kasturi segar sehingga
berpengaruh pada bobot sampel. Hasil penetapan kadar minyak atsiri dari kulit
buah jeruk kasturi segar dan kering dapat dilihat pada Tabel 4.2 (data
selengkapnya dapat dilihat pada Lampiran 12-13, halaman 70-71).
4.5 Hasil Identifikasi Minyak Atsiri
Hasil penentuan indeks bias dan bobot jenis minyak atsiri hasil isolasi dari
kulit buah jeruk kasturi dapat dilihat pada Tabel 4.3 (data selengkapnya dapat
dilihat pada Lampiran 14-17, halaman 72-75).
Hasil pengukuran indeks bias minyak atsiri dari kulit buah jeruk kasturi
segar dan kering adalah sama yaitu 1,4240. Hal ini menunjukkan bahwa
perubahan kecil pada komposisi komponen minyak atsiri tidak mempengaruhi
harga indeks bias.
No. Sampel Kadar yang
diperoleh (% v/b)
1. Kulit buah jeruk kasturi segar 0,93
2. Kulit buah jeruk kasturi kering 1,27
No. Sampel Indeks bias Bobot jenis
1 Kulit buah jeruk kasturi segar 1,4240 0,8526
[image:50.595.113.417.381.442.2]2 Kulit buah jeruk kasturi kering 1,4240 0,8522
Indeks bias merupakan perbandingan antara kecepatan cahaya di dalam
udara dengan kecepatan cahaya di dalam zat pada suhu tertentu. Indeks bias
berguna untuk identifikasi kemurnian dan berhubungan erat dengan
komponen-komponen yang tersusun dalam minyak atsiri yang dihasilkan (Armando, 2009).
Bobot jenis minyak atsiri merupakan perbandingan antara bobot minyak
dengan bobot air pada volume air yang sama dengan volume minyak. Bobot jenis
merupakan salah satu kriteria paling penting dalam menentukan mutu dan
kemurnian minyak atsiri (Armando, 2009).
Hasil penelitian menunjukkan terdapat perbedaan nilai bobot jenis dari
minyak atsiri yang berasal dari kulit buah jeruk kasturi segar dan yang kering.
Bobot jenis minyak atsiri dari kulit buah jeruk kasturi segar adalah sebesar 0,8526
dan minyak atsiri dari kulit buah jeruk kasturi kering adalah sebesar 0,8522. Hal
ini disebabkan pada identifikasi minyak atsiri dengan GC-MS diperoleh
komponen senyawa kimia dari minyak atsiri kulit buah jeruk kasturi segar lebih
banyak dibandingkan dengan minyak atsiri kulit buah jeruk kasturi kering.
Menurut Armando, bobot jenis merupakan salah satu kriteria paling penting dalam
menentukan mutu dan kemurnian minyak atsiri. Bobot jenis sering dihubungkan
dengan berat komponen yang terkandung di dalamnya. Semakin besar fraksi berat
Gambar 4.1 Kromatogram GC mi