KARAKTERISASI SIMPLISIA DAN ISOLASI MINYAK
ATSIRI DARI DAUN SALAM KOJA (Murraya koenigii L.
Spreng) SEGAR DAN KERING SERTA ANALISIS
KOMPONENNYA SECARA GC-MS
SKRIPSI
OLEH:
ARTA MARIA HUTAGAOL NIM 101501133
PROGRAM STUDI SARJANA FARMASI
FAKULTAS FARMASI
UNIVERSITAS SUMATERA UTARA
MEDAN
KARAKTERISASI SIMPLISIA DAN ISOLASI MINYAK
ATSIRI DARI DAUN SALAM KOJA (Murraya koenigii L.
Spreng) SEGAR DAN KERING SERTA ANALISIS
KOMPONENNYA SECARA GC-MS
SKRIPSI
Diajukan untuk Melengkapi Salah Satu Syarat untuk Memperoleh Gelar Sarjana Farmasi pada Fakultas Farmasi
Universitas Sumatera Utara
OLEH:
ARTA MARIA HUTAGAOL NIM 101501133
PROGRAM STUDI SARJANA FARMASI
FAKULTAS FARMASI
UNIVERSITAS SUMATERA UTARA
MEDAN
PENGESAHAN SKRIPSI
KARAKTERISASI SIMPLISIA DAN ISOLASI MINYAK
ATSIRI DARI DAUN SALAM KOJA (Murraya koenigii L.
Spreng) SEGAR DAN KERING SERTA ANALISIS
KOMPONENNYA SECARA GC-MS
OLEH:
ARTA MARIA HUTAGAOL NIM 101501133
Dipertahankan dihadapan Panitia Penguji Skripsi Fakultas Farmasi Universitas Sumatera Utara
Pada Tanggal: 6 Juni 2014
Pembimbing I, Panitia Penguji,
Drs. Panal Sitorus, M.Si., Apt. Dr. M. Pandapotan Nasution, MPS., Apt. NIP 195310301980031002 NIP 194908111976031001
Drs. Panal Sitorus, M.Si., Apt.
Pembimbing II, NIP 195310301980031002
Prof. Dr. rer. nat. Effendy De Lux Putra, S.U., Apt. Dr. Marline Nainggolan, M.S., Apt. NIP 195306191983031001 NIP 195709091985112001
Dra. Herawaty Ginting, M.Si., Apt.
NIP 195112231980032002
Medan,
Fakultas Farmasi
Universitas Sumatera Utara Dekan,
KATA PENGANTAR
Puji dan syukur kehadirat Tuhan Yang Maha Esa, karena limpahan rahmat
kasih dan karuniaNya, sehingga penulis dapat menyelesaikan skripsi ini yang
berjudul “Karakterisasi Simplisia dan Isolasi Minyak Atsiri dari Daun Salam Koja
(Murraya koenigii L. Spreng) Segar dan Kering serta Analisis Komponennya
Secara GC-MS”. Skripsi ini diajukan sebagai salah satu syarat untuk memperoleh
gelar sarjana farmasi pada Fakultas Farmasi Universitas Sumatera Utara.
Pada kesempatan ini penulis menyampaikan ucapan terimakasih kepada
Bapak Prof. Dr. Sumadio Hadisahputra, Apt., selaku Dekan Fakultas Farmasi
USU Medan yang telah memberikan fasilitas selama masa pendidikan. Bapak Drs.
Panal Sitorus, M.Si, Apt., dan Prof. Dr. rer. nat. Effendy De Lux Putra, S.U., Apt.,
selaku pembimbing yang telah memberikan waktu, bimbingan, dan nasehat
selama penelitian hingga selesainya penyusunan skripsi ini. Ibu Dra. Djendakita
Purba, M.Si., Apt., selaku penasehat akademik yang telah memberikan bimbingan
kepada penulis selama masa perkuliahan. Bapak dan Ibu staf pengajar Fakultas
Farmasi Universitas Sumatera Utara yang telah mendidik selama masa
perkuliahan. Bapak dan Ibu Kepala Laboratorium Penelitian dan Farmakognosi
yang telah memberikan fasilitas, petunjuk dan membantu selama penelitian.
Bapak Dr. M. Pandapotan Nasution, MPS., Apt., Ibu Dr. Marline Nainggolan,
M.S., Apt., dan Ibu Dra. Herawaty Ginting, M.Si., Apt., selaku dosen penguji
yang telah memberikan kritik, saran, dan arahan kepada penulis dalam
Penulis juga ingin mempersembahkan rasa terima kasih yang tak terhingga
kepada Ayahanda (alm) T. Hutagaol dan Ibunda L. Pasaribu atas doa dan
pengorbanannya dengan tulus dan ikhlas bagi kesuksesan penulis, juga untuk
abang dan kakak tersayang Herbet Hutagaol, Jimmy Hutagaol, Marihot Hutagaol,
Junita Hutagaol, David Hutagaol serta teman-teman STF 2010 yang selalu setia
memberi doa, dorongan dan semangat.
Penulis menyadari bahwa penulisan skripsi ini masih banyak kekurangan,
oleh karena itu penulis mengharapkan kritik dan saran yang membangun untuk
penyempurnaannya. Semoga skripsi ini dapat bermanfaat bagi ilmu pengetahuan
dan ilmu kefarmasian khususnya.
Medan, Mei 2014
Penulis
KARAKTERISASI SIMPLISIA DAN ISOLASI MINYAK ATSIRI DARI DAUN SALAM KOJA (Murraya koenigii L. Spreng) SEGAR DAN KERING
SERTA ANALISIS KOMPONENNYA SECARA GC-MS
ABSTRAK
Minyak atsiri merupakan minyak yang mudah menguap dengan komposisi yang berbeda–beda sesuai sumber penghasilnya dan terdiri dari campuran zat yang memiliki sifat fisika kimia berbeda–beda. Salam koja (Murraya koenigii L. Spreng) dari family Rutaceae adalah salah satu tumbuhan yang mengandung minyak atsiri dan digunakan pada pengobatan tradisional untuk penyembuhan luka, sebagai analgesik, antiinflamasi dan dimanfaatkan masyarakat sebagai bumbu masak.
Penelitian ini bertujuan untuk mengetahui karakteristik simplisia dan mengetahui perbedaan kadar minyak atsiri serta komponen minyak atsiri daun salam koja segar dan kering.
Penelitian yang dilakukan meliputi karakterisasi simplisia, isolasi minyak atsiri dengan cara destilasi air dan analisis komponen minyak atsiri dengan Gas
Cromatography-Mass Spectrometry (GC-MS).
Hasil karakterisasi simplisia daun salam koja diperoleh kadar air 4,65%; kadar sari yang larut dalam air 28,42%; kadar sari yang larut dalam etanol 115,08%; kadar abu total 8,84%; kadar abu yang tidak larut dalam asam 1,13%. Hasil penetapan kadar minyak atsiri dengan alat Stahl diperoleh kadar minyak atsiri daun salam koja segar dan kering berturut-turut sebesar 0,17% v/b dan 0,66% v/b. Hasil penetapan indeks bias minyak atsiri daun salam koja segar dan kering sama, yakni sebesar 1,4465; bobot jenis minyak atsiri daun salam koja segar dan kering berturut-turut sebesar 0,8901 dan 0,8902. Hasil analisis GC-MS minyak atsiri yang diperoleh dari daun salam koja segar sebanyak 61 komponen dengan enam komponen utama yaitu: kariofillen (14,92%), α-pinen (8,43%), β -felandren (7,28%), α-humulen (5,68%), β-selinen (4,67%) dan 2-β-pinen (2,32%), sedangkan hasil analisis GC-MS minyak atsiri yang diperoleh dari daun salam koja kering sebanyak 57 komponen dengan enam komponen utama yaitu kariofillen (15,59%), α-pinen (12,96%), β-felandren (8,22%), α-humulen (5,87%), β-selinen (4,52%) dan 2-β-pinen (2,93%).
SIMPLEX CHARACTERIZATION AND ISOLATION OF VOLATILE OIL FROM FRESH AND DRIED LEAVES OF Murraya koenigii L. Spreng
AND ANALYSIS OF THE COMPONENTS BY GC-MS
ABSTRACT
Essential oils contain different chemical composition in accordance with the source and consist of a mixture of ingredients of different physicochemical properties. Murraya koenigii (L.) Spreng of the family Rutaceae is one of plants containing essential oil and used in traditional medicine as a wound healer, analgesic, anti-inflammatory and widely used as food flavoring.
The objective of this research was to determine the characteristics of simplex and determine the difference in essential oil content and essential oil components of fresh and dried Murraya koenigii (L.) Spreng leaves.
This research consist of simplex characterization, isolation of essential oil by water distillation and analysis of essential oil components by Gas Chromatography-Mass Spectrometry (GC-MS)
The result of simplex characterization of the leaves of Murraya koenigii (L.) Spreng exhibited water content 4.65%; water-soluable extract 28.42%; ethanol-soluble extract 15.08%; total ash 8.84%; acid insoluble ash 1.13%. The volatile oil content of fresh and dried Murraya koenigii L. Spreng leaves consecutively were 0.17% v/w and 0.66% v/w. The volatile oil of fresh and dried
Murraya koenigii L. Spreng leaves had the same refractive index 1.4465 and
specific gravity of fresh and dried Murraya koenigii (L.) Spreng leaves consecutively were 0.8901 and 0.8902. Gas Chromatography-Mass Spectrometry (GC-MS) analysis result of volatile oil from fresh Murraya koenigii L. Spreng leaf reaveled the presence of 61 compounds with six main components, such as caryophyllene (14.92%), α-pinene (8.43%), β-phellandrene (7.28%), α-humulene (5.68%), β-selinene (4.67%) dan 2-β-pinene (2.32%). Meanwhile GC-MS analysis result of volatile oil from dried Murraya koenigii (L.) Spreng leaves reaveled the presence of 57 compounds with six main components, such as caryophyllene (15.59%), α-pinene (12.96%), β-phellandrene (8.22%), α -humulene (5.87%), β-selinene (4.52%) dan 2-β-pinene (2.93%).
DAFTAR ISI
Halaman
JUDUL ... i
HALAMAN JUDUL ... ii
LEMBAR PENGESAHAN ... iii
KATA PENGANTAR ... iv
ABSTRAK ... vi
ABSTRACT ... vii
DAFTAR ISI ... viii
DAFTAR TABEL ... xii
DAFTAR GAMBAR ... xiii
DAFTAR LAMPIRAN ... xv
BAB I PENDAHULUAN ... 1
1.1 Latar Belakang ... 1
1.2 Perumusan Masalah ... 3
1.3 Hipotesis ... 3
1.4 Tujuan Penelitian ... 3
1.5 Manfaat Penelitian ... 4
BAB II TINJAUAN PUSTAKA ... 5
2.1 Uraian Tumbuhan ... 5
2.1.1 Morfologi tumbuhan ... 5
2.1.2 Sistematika tumbuhan ... 5
2.1.4 Nama asing ... 6
2.1.5 Kandungan kimia ... 6
2.2 Minyak Atsiri ... 6
2.2.1 Keberadaan minyak atsiri pada tumbuhan ... 7
2.2.2 Komposisi kimia minyak atsiri ... 7
2.3 Sifat Fisikokimia Minyak Atsiri ... 9
2.3.1 Sifat fisika minyak atsiri ... 9
2.3.2 Sifat kimia minyak atsiri ... 10
2.4 Isolasi Minyak Atsiri ... 10
2.4.1 Metode penyulingan ... 10
2.4.2 Metode pengepresan ... 11
2.4.3 Ekstraksi dengan pelarut menguap ... 12
2.4.4 Ekstraksi dengan lemak padat ... 12
2.4.5 Ecuelle ... 13
2.5 Analisis Komponen Minyak Atsiri dengan GC-MS ... 13
2.5.1 Kromatografi gas ... 14
2.5.1.1 Gas pembawa ... 15
2.5.1.2 Sistem injeksi ... 15
2.5.1.3 Kolom ... 15
2.5.1.4 Fase diam ... 16
2.5.1.5 Suhu ... 17
2.5.1.6 Detektor ... 17
BAB III METODE PENELITIAN ... 20
3.1 Alat-alat ... 20
3.2 Bahan-bahan ... 20
3.3 Penyiapan Sampel ... 20
3.3.1 Pengambilan bahan ... 21
3.3.2 Identifikasi bahan ... 21
3.3.3 Pengolahan bahan ... 21
3.4 Pemeriksaan Makroskopik dan Mikroskopik Daun Salam Koja Segar ... 21
3.4.1 Pemeriksaan makroskopik ... 21
3.4.2 Pemeriksaan mikroskopik ... 21
3.5 Pemeriksaan Karakteristik Simplisia ... 22
3.5.1 Pemeriksaan makroskopik simplisia ... 22
3.5.2 Pemeriksaan mikroskopik serbuk simplisia ... 22
3.5.3 Penetapan kadar air ... 22
3.5.4 Penetapan kadar sari larut dalam air ... 23
3.5.5 Penetapan kadar sari larut dalam etanol ... 23
3.5.6 Penetapan kadar abu total ... 24
3.5.7 Penetapan kadar abu yang tidak larut dalam asam .. 24
3.5.8 Penetapan kadar minyak atsiri ... 24
3.6 Isolasi Minyak Atsiri ... 25
3.7 Identifikasi Minyak Atsiri ... 25
3.7.1 Penetapan parameter fisika ... 25
3.7.1.2 Penentuan bobot jenis ... 26
3.7.2 Analisis komponen minyak atsiri ... 26
BAB IV HASIL DAN PEMBAHASAN ... 28
4.1 Identifikasi Tumbuhan ... 28
4.2 Hasil Pemeriksaan Makroskopik dan Mikroskopik Daun Salam Koja Segar ... 28
4.2.1 Hasil pemeriksaan makroskopik ... 28
4.2.2 Hasil pemeriksaan mikroskopik ... 28
4.3 Hasil Pemeriksaan Karakteristik Simplisia ... 29
4.3.1 Hasil pemeriksaan makroskopik simplisia ... 29
4.3.2 Hasil pemeriksaan mikroskopik serbuk simplisia .. 29
4.3.3 Hasil Pemeriksaan karakterisasi simplisia ... 29
4.4 Hasil Penetapan Kadar Minyak Atsiri ... 31
4.5 Penentuan Indeks Bias dan Bobot Jenis Minyak Atsiri Hasil Isolasi ... 31
4.6 Analisis dengan GC-MS ... 32
4.6.1 Fragmentasi hasil spektrofotometri massa minyak atsiri daun salam koja segar ... 43
4.6.2 Fragmentasi hasil spektrofotometri maassa minyak atsiri daun salam koja kering ... 52
BAB V KESIMPULAN DAN SARAN ... 61
5.1 Kesimpulan ... 61
5.2 Saran ... 62
DAFTAR PUSTAKA ... 63
DAFTAR TABEL
Halaman
Tabel 4.1 Hasil karakterisasi simplisia daun salam koja ... 29
Tabel 4.2 Hasil penetapan kadar minyak atsiri ... 31
Tabel 4.3 Hasil penentuan indeks bias dan bobot jenis minyak
atsiri ... 31
Tabel 4.4 Komponen minyak atsiri daun salam koja segar ... 33
Tabel 4.5 Komponen minyak atsiri daun salam koja kering ... 37
Tabel 4.6 Waktu tambat dan kadar komponen minyak atsiri hasil
analisis GC-MS daun salam koja segar ... 41
Tabel 4.7 Waktu tambat dan kadar komponen minyak atsiri hasil
DAFTAR GAMBAR
Halaman
Gambar 4.1 Kromatogram minyak atsiri daun salam koja segar ……. 33
Gambar 4.2 Kromatogram minyak atsiri daun salam koja kering …... 37
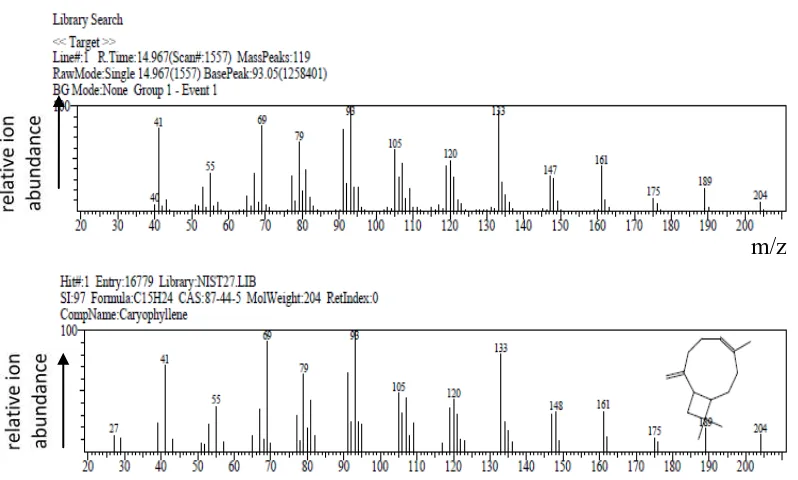
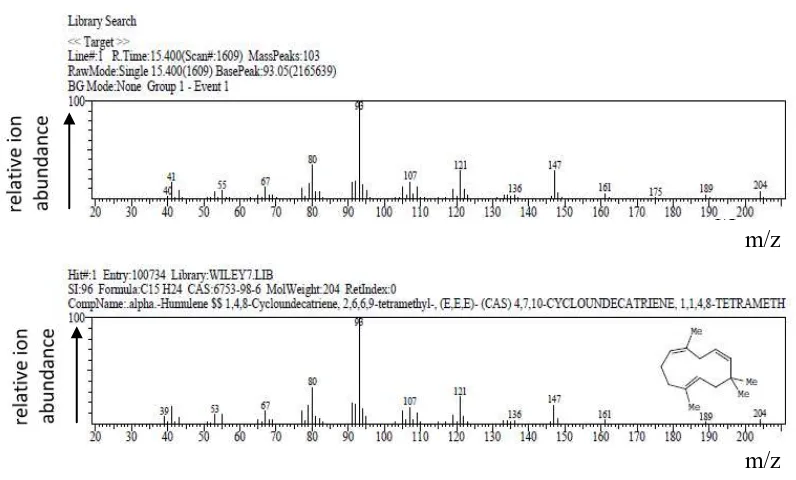
Gambar 4.3 Spektrum massa puncak dengan Rt 14,967 menit ... 43
Gambar 4.4 Rumus bangun dari senyawa kariofillen ... 44
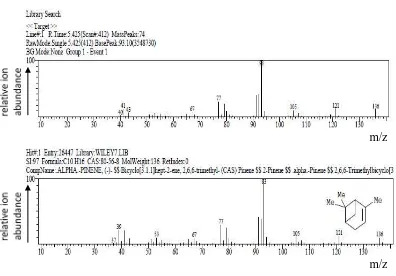
Gambar 4.5 Spektrum massa puncak dengan Rt 5,425 menit ... 45
Gambar 4.6 Rumus bangun dari senyawa α-pinen ... 45
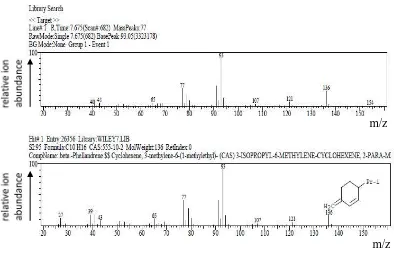
Gambar 4.7 Spektrum massa puncak dengan Rt 7,675 menit ... 46
Gambar 4.8 Rumus bangun dari senyawa β-felandren ... 47
Gambar 4.9 Spektrum massa puncak dengan Rt 15,400 menit ... 47
Gambar 4.10 Rumus bangun dari senyawa α-humulen ... 48
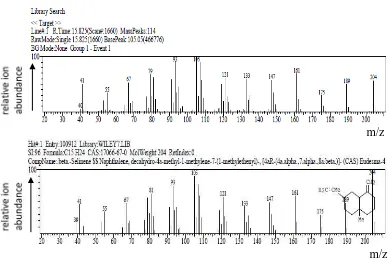
Gambar 4.11 Spektrum massa puncak dengan Rt 15,825 menit ... 49
Gambar 4.12 Rumus bangun dari senyawa β-selinen ... 49
Gambar 4.13 Spektrum massa puncak dengan Rt 6,425 menit ... 50
Gambar 4.14 Rumus bangun dari senyawa 2-β-pinen ... 51
Gambar 4.15 Spektrum massa puncak dengan Rt 14,950 menit ... 52
Gambar 4.16 Rumus bangun dari senyawa kariofillen ... 52
Gambar 4.17 Spektrum massa puncak dengan Rt 5,433 menit ... 53
Gambar 4.18 Rumus bangun dari senyawa α-pinen ... 54
Gambar 4.19 Spektrum massa puncak dengan Rt 7,642 menit ... 54
Gambar 4.20 Rumus bangun dari senyawa β-felandren ... 55
Gambar 4.22 Rumus bangun dari senyawa α-humulen ... 56
Gambar 4.23 Spektrum massa puncak dengan Rt 15,817 menit ... 57
Gambar 4.24 Rumus bangun dari senyawa β-selinen ... 58
Gambar 4.25 Spektrum massa puncak dengan Rt 6,408 menit ... 59
DAFTAR LAMPIRAN
Halaman
Lampiran 1 Hasil identifikasi tumbuhan ... 66
Lampiran 2 Gambar tumbuhan salam koja dan daun salam koja ... 67
Lampiran 3 Gambar daun salam koja segar dan kering serta serbuk
simplisia daun salam koja ... 68
Lampiran 4 Gambar mikroskopik daun salam koja segar dan serbuk
simplisia daun salam koja ... 69
Lampiran 5 Gambar alat yang digunakan ... 71
Lampiran 6 Perhitungan penetapan kadar air dari simplisia daun
salam koja ... 74
Lampiran 7 Perhitungan penetapan kadar sari larut air simplisia
daun salam koja ... 75
Lampiran 8 Perhitungan penetapan kadar sari larut etanol simplisia
daun salam koja ... 76
Lampiran 9 Perhitungan penetapan kadar abu total simplisia daun
salam koja ... 77
Lampiran 10 Perhitungan penetapan kadar abu tidak larut asam
simplisia daun salam koja ... 78
Lampiran 11 Perhitungan penetapan kadar minyak atsiri daun salam
koja ... 79
Lampiran 12 Perhitungan penetapan kadar indeks bias minyak atsiri
daun salam koja ... 81
Lampiran 13 Perhitungan penetapan bobot jenis minyak atsiri daun
salam koja ... 82
KARAKTERISASI SIMPLISIA DAN ISOLASI MINYAK ATSIRI DARI DAUN SALAM KOJA (Murraya koenigii L. Spreng) SEGAR DAN KERING
SERTA ANALISIS KOMPONENNYA SECARA GC-MS
ABSTRAK
Minyak atsiri merupakan minyak yang mudah menguap dengan komposisi yang berbeda–beda sesuai sumber penghasilnya dan terdiri dari campuran zat yang memiliki sifat fisika kimia berbeda–beda. Salam koja (Murraya koenigii L. Spreng) dari family Rutaceae adalah salah satu tumbuhan yang mengandung minyak atsiri dan digunakan pada pengobatan tradisional untuk penyembuhan luka, sebagai analgesik, antiinflamasi dan dimanfaatkan masyarakat sebagai bumbu masak.
Penelitian ini bertujuan untuk mengetahui karakteristik simplisia dan mengetahui perbedaan kadar minyak atsiri serta komponen minyak atsiri daun salam koja segar dan kering.
Penelitian yang dilakukan meliputi karakterisasi simplisia, isolasi minyak atsiri dengan cara destilasi air dan analisis komponen minyak atsiri dengan Gas
Cromatography-Mass Spectrometry (GC-MS).
Hasil karakterisasi simplisia daun salam koja diperoleh kadar air 4,65%; kadar sari yang larut dalam air 28,42%; kadar sari yang larut dalam etanol 115,08%; kadar abu total 8,84%; kadar abu yang tidak larut dalam asam 1,13%. Hasil penetapan kadar minyak atsiri dengan alat Stahl diperoleh kadar minyak atsiri daun salam koja segar dan kering berturut-turut sebesar 0,17% v/b dan 0,66% v/b. Hasil penetapan indeks bias minyak atsiri daun salam koja segar dan kering sama, yakni sebesar 1,4465; bobot jenis minyak atsiri daun salam koja segar dan kering berturut-turut sebesar 0,8901 dan 0,8902. Hasil analisis GC-MS minyak atsiri yang diperoleh dari daun salam koja segar sebanyak 61 komponen dengan enam komponen utama yaitu: kariofillen (14,92%), α-pinen (8,43%), β -felandren (7,28%), α-humulen (5,68%), β-selinen (4,67%) dan 2-β-pinen (2,32%), sedangkan hasil analisis GC-MS minyak atsiri yang diperoleh dari daun salam koja kering sebanyak 57 komponen dengan enam komponen utama yaitu kariofillen (15,59%), α-pinen (12,96%), β-felandren (8,22%), α-humulen (5,87%), β-selinen (4,52%) dan 2-β-pinen (2,93%).
SIMPLEX CHARACTERIZATION AND ISOLATION OF VOLATILE OIL FROM FRESH AND DRIED LEAVES OF Murraya koenigii L. Spreng
AND ANALYSIS OF THE COMPONENTS BY GC-MS
ABSTRACT
Essential oils contain different chemical composition in accordance with the source and consist of a mixture of ingredients of different physicochemical properties. Murraya koenigii (L.) Spreng of the family Rutaceae is one of plants containing essential oil and used in traditional medicine as a wound healer, analgesic, anti-inflammatory and widely used as food flavoring.
The objective of this research was to determine the characteristics of simplex and determine the difference in essential oil content and essential oil components of fresh and dried Murraya koenigii (L.) Spreng leaves.
This research consist of simplex characterization, isolation of essential oil by water distillation and analysis of essential oil components by Gas Chromatography-Mass Spectrometry (GC-MS)
The result of simplex characterization of the leaves of Murraya koenigii (L.) Spreng exhibited water content 4.65%; water-soluable extract 28.42%; ethanol-soluble extract 15.08%; total ash 8.84%; acid insoluble ash 1.13%. The volatile oil content of fresh and dried Murraya koenigii L. Spreng leaves consecutively were 0.17% v/w and 0.66% v/w. The volatile oil of fresh and dried
Murraya koenigii L. Spreng leaves had the same refractive index 1.4465 and
specific gravity of fresh and dried Murraya koenigii (L.) Spreng leaves consecutively were 0.8901 and 0.8902. Gas Chromatography-Mass Spectrometry (GC-MS) analysis result of volatile oil from fresh Murraya koenigii L. Spreng leaf reaveled the presence of 61 compounds with six main components, such as caryophyllene (14.92%), α-pinene (8.43%), β-phellandrene (7.28%), α-humulene (5.68%), β-selinene (4.67%) dan 2-β-pinene (2.32%). Meanwhile GC-MS analysis result of volatile oil from dried Murraya koenigii (L.) Spreng leaves reaveled the presence of 57 compounds with six main components, such as caryophyllene (15.59%), α-pinene (12.96%), β-phellandrene (8.22%), α -humulene (5.87%), β-selinene (4.52%) dan 2-β-pinene (2.93%).
BAB I PENDAHULUAN
1.1Latar Belakang
Tumbuhan penghasil minyak atsiri yang saat ini tumbuh di wilayah
Indonesia hampir seluruhnya sudah dikenl masyarakat, bahkan beberapa jenis
tumbuhan penghasil minyak atsiri menjadi bahan yang sangat penting dalam
kehidupan sehari-hari. Minyak atsiri dihasilkan dari bagian tumbuhan tertentu
seperti akar, batang, kulit, daun, bunga atau biji (Lutony dan Rahmayati, 1994).
Minyak atsiri adalah suatu substansi yang terkandung dalam tanaman yang
memiliki aroma yang sangat spesifik. Minyak ini disebut juga minyak menguap,
minyak eteris, minyak esensial karena minyak ini sangat mudah menguap pada
suhu kamar (Gunawan dan Mulyani, 2004).
Kegunaan minyak atsiri sangat luas dan spesifik, khususnya dalam
berbagai bidang industri, antara lain industri kosmetik, seperti industri parfum,
digunakan sebagai pewangi dalam berbagai produk minyak wangi, industri
makanan digunakan sebagai penyedap atau penambah cita rasa dan industri
farmasi atau obat-obatan. Meningkatnya ragam kegunaan dari minyak atsiri maka
permintaan minyak atsiri akan tetap prospektif dimasa yang akan datang. Selain
itu, sadarnya masyarakat untuk menggunakan minyak atsiri alami yang resikonya
lebih aman dibandingkan minyak tiruan yang diproduksi secara sintesis sehingga
banyak perusahaan yang memilih istilah back to nature untuk menggunakan
Daun salam koja merupakan salah satu sumber penghasil minyak atsiri
yang berasal dari suku rutaceae. Pohonnya (Murraya koenigii L. Spreng) belum
banyak dikenal di Indonesia, hanya beberapa daerah saja seperti Aceh dan
Sumatera Barat yang sudah mengenal pohon ini dengan baik sebab daun salam
koja digunakan sebagai rempah penyedap masakan khas daerah ini (Anonima,
2013). Beberapa penelitian telah dilakukan terhadap minyak atsiri daun salam
koja ini. Berdasarkan penelitian sebelumnya yang dilakukan di Malaysia, daun
salam koja segar mengandung 0,12% minyak atsiri dimana hasil analisis GC-MS
meghasilkan dua komponen utama yaitu caryophyllen dan α-humulen yang
merupakan golongan hidrokarbon sesquiterpen (Dikui, 2009). Menurut
Chowdhurry, et al., (2008), komponen utama minyak atsiri dari daun salam koja
yang cenderung memberikan rasa dan bau adalah pinen, sabinen, caryophyllen,
cadinol dan cadinen. Nagappan, et al., (2012) menguji aktivitas minyak atsiri dari
daun salam koja terhadap kemampuan menutup luka pada marmut, dimana
minyak atsiri mempunyai kemampuan menutup luka karena mempunyai aktivitas
antiinflamasi, antibakteri dan antioksidan.
Berdasarkan hal tersebut di atas, penulis tertarik memanfaatkan daun
salam koja sebagai bahan penelitian yang diambil dari daerah Tapak Tuan, Aceh
Selatan dengan membandingkan hasil randemen dan perbedaan komponen antara
daun yang masih segar dan yang sudah dikeringkan, karena perbedaan lingkungan
(iklim, kondisi tanah, suhu) tempat tumbuh sampel dapat mempengaruhi
komponen penyusun minyak atsiri suatu tumbuhan (Ketaren, 1985). Isolasi
minyak atsiri dilakukan dengan penyulingan air (Water distillation), karena
pengrajin minyak atsiri di berbagai Negara, khususnya negara yag sedang
berkembang termasuk Indonesia (Lutony dan Rahmayati, 1994). Pelaksanaan
penelitian meliputi karakterisasi simplisia, isolasi dengan metode destilasi air
serta analisis komponen minyak atsirinya secara Gas Chromatography-Mass
Spectrometry (GC-MS).
1.2 Perumusan Masalah
Berdasarkan latar belakang di atas, maka perumusan masalah pada
penelitian ini adalah:
a. bagaimana karakteristik simplisia daun salam koja?
b. apakah ada perbedaan kadar minyak atsiri dan komponen minyak atsiri
dari daun salam koja segar dan kering yang dianalisis secara GC-MS?
1.3 Hipotesis
Berdasarkan perumusan masalah di atas maka hipotesisnya adalah:
a. karakteristik simplisia daun salam koja dapat ditentukan sesuai dengan
karakterisasi yang terdapat pada Materia Medika Indonesia (MMI).
b. terdapat perbedaan kadar minyak atsiri dan komponen minyak atsiri dari
daun salam koja segar dan kering yang dianalisis secara GC-MS.
1.4 Tujuan Penelitian
Tujuan penelitian ini adalah:
a.
untuk mengetahui karakteristik simplisia daun salam koja sesuai denganb. untuk mengetahui perbedaan kadar minyak atsiri dan komponen minyak
atsiri yang diperoleh dari daun salam koja segar dan kering yang dianalisis
secara GC-MS.
1.5 Manfaat Penelitian
Hasil penelitian diharapkan memberikan informasi tentang karakteristik
simplisia, isolasi minyak atsiri dan analisis komponennya secara GC-MS dari
daun salam koja segar dan kering serta bermanfaat bagi pengembangan ilmu
pengetahuan tentang bahan alam penghasil minyak atsiri yang terdapat di
BAB II
TINJAUAN PUSTAKA
2.1 Uraian Tumbuhan
Salam koja (Murraya koenigii) merupakan tanaman yang berasal dari
keluarga jeruk jerukan (Rutaceae), daunnya sering digunakan sebagai rempah
-rempah masakan khas India dan Srilanka. Di Indonesia daun salam koja dikenal
sebagai rempah masakan khas Sumatera terutama Aceh (Anonima, 2013;
Anonimb, 2013).
Salam koja ditemukan pertama kali di wilayah Uttar Pradesh, India dan
sekarang tersebar luas disemua bagian India. Tanaman ini kemudian juga
dibudidayakan di Srilanka, China, Australia, benua Pasifik dan juga
didistribusikan ke negara-negara Asia Selatan (Dikui, 2009).
2.1.1 Morfologi tumbuhan
Salam koja merupakan tumbuhan perdu atau pohon kecil dengan tinggi
+ 0,8 - 4 meter dan diameter batang maksimal + 40 cm. Daunnya berbentuk
menyirip, berukuran lebih kecil dan berwarna hijau tua mengkilap. Bunganya
putih kecil, berkelompok dan memiliki bau yang harum dengan buah berbentuk
bulir berwarna ungu atau kehitaman (Anonimb, 2013; Anonimc, 1995).
2.1.2 Sistematika tumbuhan
Menurut Sihotang (2013) dan LIPI (2013) sistematika tumbuhan salam
koja adalah sebagai berikut:
Kingdom : Plantae
Subdivisi : Angiospermae
Kelas : Dicotyledoneae
Ordo : Rutales
Familia : Rutaceae
Genus : Murraya
Spesies : Murraya koenigii (L.) Spreng
2.1.3 Nama lain
Kari, temuru, garupillai (Anonima, 2013; Anonimc,1995).
2.1.4 Nama asing
Curry (English) (Anonimb, 2013).
2.1.5 Kandungan kimia
Daun salam koja mengandung 0,12% minyak atsiri. Kandungan minyak
atsiri yang utama pada daun kari yaitu caryophyllen dan α-humulen. Selain itu,
komponen lain yang terkandung dalam minyak atsiri daun salam koja adalah
linalool, β-selinen, β-elemen, cubenol, phytol, α-selinen, β-terpineol, α-kopaen,
aromadendrene, naphthalene, δ-cadinen, dan sphatulenol (Nagappan, et al., 2012).
2.2 Minyak Atsiri
Minyak atsiri adalah zat berbau yang terkandung dalam tanaman. Minyak
ini disebut juga minyak menguap (volatile oil), minyak eteris (ethereal oil), dan
minyak esensial (essential oil) karena pada suhu biasa (suhu kamar) mudah
menguap di udara terbuka. Istilah esensial dipakai karena minyak atsiri mewakili
bau dari tanaman asalnya. Minyak atsiri dalam keadaan segar dan murni
menjadi lebih gelap karena oksidasi. Untuk mencegahnya, minyak atsiri harus
terlindung dari pengaruh cahaya, diisi penuh, ditutup rapat serta disimpan di
tempat yang kering dan gelap (Gunawan dan Mulyani, 2004).
Kegunaan minyak atsiri sangat luas dan spesifik, khususnya dalam
berbagai bidang industri. Contohnya, dalam industri kosmetik (sabun, pasta gigi,
sampo); dalam industri makanan digunakan sebagai bahan penyedap dan
penambah cita rasa; dalam industri parfum sebagai pewangi; dalam industri
farmasi atau obat-obatan (antinyeri, antiinfeksi, pembunuh bakteri, dan
antikanker) (Lutony dan Rahmayati, 1994).
2.2.1 Keberadaan minyak atsiri pada tumbuhan
Minyak atsiri dalam tumbuhan terdapat dalam berbagai jaringan, seperti di
dalam rambut kelenjar (pada suku Labiatae), di dalam sel - sel parenkim (pada
suku Zingiberaceae dan Piperaceae), di dalam rongga - rongga skizogen dan
lisigen (pada suku Myrtaceae, Pinaceae dan Rutaceae), di dalam saluran minyak
(pada suku Umbelliferae) dan terkandung di dalam semua jaringan (pada suku
Coniferae) (Gunawan dan Mulyani, 2004).
2.2.2 Komposisi kimia minyak atsiri
Pada umumnya, perbedaan komposisi minyak atsiri disebabkan perbedaan
jenis tanaman penghasil, kondisi iklim, tanah tempat tumbuh, umur panen, metode
ekstraksi yang digunakan dan cara penyimpanan minyak (Ketaren, 1985).
Minyak atsiri sebagian besar terdiri dari senyawa terpena, yaitu senyawa
yang strukturnya terdiri dari satuan - satuan isoprene. Satuan isoprene ini saling
bergabung membentuk rantai yang lebih panjang dengan cara menggandeng
Minyak atsiri biasanya terdiri dari berbagai campuran persenyawaan kimia
yang terbentuk dari unsur Karbon (C), Hidrogen (H) dan Oksigen (O). Komponen
kimia minyak atsiri pada umumnya dibagi menjadi dua golongan yaitu:
a. Golongan Hidrokarbon (Terpen)
Persenyawaan yang termasuk golongan ini terbentuk dari unsur Karbon
(C) dan Hidrogen (H). Jenis hidrokarbon yang terdapat dalam minyak atsiri
sebagian besar terdiri dari monoterpen (2 unit isopren) dan sesquiterpen (3 unit
isopren) yang titik didihnya berbeda, titik didih monoterpen sebesar 140oC - 180oC
dan sesquiterpen > 200oC (Harborne, 1987; Ketaren, 1985).
b. Golongan Hidrokarbon Teroksigenasi (Terpenoid)
Komponen kimia dari golongan persenyawaan ini terbentuk dari unsur
Karbon(C), Hidrogen (H) dan Oksigen (O). Persenyawaan yang termasuk dalam
golongan ini adalah persenyawaan alkohol, aldehid, keton, ester, eter dan
peroksid. Ikatan karbon yang terdapat dalam molekulnya dapat terdiri dari ikatan
tunggal, ikatan rangkap dua dan ikatan rangkap tiga. Golongan hidrokarbon
teroksigenasi merupakan senyawa yang penting dalam minyak atsiri karena
umumnya mempunyai aroma yang lebih wangi (Ketaren, 1985).
Berdasarkan biosintesis, maka komponen-komponen minyak atsiri dapat
dibagi sebagai berikut :
1. Turunan terpenoid yang terbentuk melalui jalur asam asetat mevalonat
2. Turunan fenil propanoid yang merupakan senyawaa aromatik, terbentuk
2.3 Sifat Fisikokimia Minyak Atsiri 2.3.1 Sifat fisika minyak atsiri
Minyak atsiri mempunyai konstituen kimia yang berbeda, tetapi dari segi
fisikanya banyak yang sama. Minyak atsiri yang baru diektraksi umumnya tidak
berwarna atau berwarna kekuningan. Sifat - sifat fisika minyak atsiri, yaitu: 1)
mempunyai indeks bias yang tinggi, 2) bersifat optis aktif dan 3) mempunyai
sudut putar optik (optical rotation) yang spesifik. Parameter yang dapat
digunakan untuk tetapan fisika minyak atsitri antara lain:
a. Berat jenis
Nilai berat jenis (densitas) minyak atsiri merupakan perbandingan antara
berat minyak dengan berat air pada volume air yang sama dengan volume minyak.
Berat jenis sering dihubungkan dengan berat komponen yang terkandung
didalamnya. Semakin besar berat komponen terkandung dalam minyak, semakin
besar pula nilai densitasnya. Berat jenis merupakan salah satu kriteria penting
dalam menentukan mutu dan kemurnian minyak atsiri (Armando, 2009).
b. Indeks bias
Indeks bias suatu zat adalah perbandingan kecepatan cahaya dalam udara
dan kecepatan cahaya dalam zat tersebut. Refraktometer adalah alat yang cepat
dan tepat untuk menetapkan nilai indeks bias. Refraktometer Abbe dengan
kisaran 1,3 - 1,7 digunakan untuk analisis minyak atsiri dan ketepatan alat ini
cukup untuk keperluan praktis. Pembacaan dapat dilakukan tanpa menggunakan
table konversi, minyak yang digunakan 1 - 2 tetes. Indeks bias berguna untuk
c. Putaran optik
Setiap jenis minyak atsiri mempunyai kemampuan memutar bidang
polarisasi cahaya ke arah kiri atau kanan. Besarnya pemutaran bidang polarisasi
ditentukan oleh jenis minyak atsiri, suhu dan panjang gelombang cahaya yang
digunakan. Sifat optis aktif suatu minyak ditentukan dengan polarimeter, dan
nilainya dinyatakan dalam derajat rotasi (Guenther, 1947).
2.3.2 Sifat kimia minyak atsiri
Perubahan sifat kimia minyak atsiri merupakan ciri dari adanya kerusakan
minyak. Perubahan dapat terjadi selama penyimpanan dan biasanya disebabkan oleh
terjadinya oksidasi, hidrolisis dan resinifikasi, karena peristiwa tersebut maka minyak
atsiri akan berubah warna menjadi lebih gelap dan lebih kental. Proses - proses
tersebut diaktifkan oleh panas, oksigen, lembab, dan sinar matahari. Oleh karena itu
minyak atsiri sebaiknya disimpan dalam wadah yang benar - benar kering dan bebas
dari cahaya agar proses – proses tersebut dapat diperlambat (Koensoemardiyah, 2010).
2.4 Isolasi Minyak Atsiri
Isolasi minyak atsiri dapat dilakukan dengan beberapa cara yaitu: 1)
penyulingan (distillation), 2) pengepresan (pressing), 3) ekstraksi dengan pelarut
menguap (solvent extraction), 4) ekstraksi dengan lemak padat dan 5) ecuelle.
2.4.1 Metode penyulingan
Penyulingan adalah salah satu metode untuk memisahkan komponen
-komponen suatu campuran dari dua jenis campuran atau lebih berdasarkan
perbedaan tekanan uap dari masing-masing zat tersebut. Metode penyulingan
a. Penyulingan dengan air (water distillation)
Pada metode ini, bahan tumbuhan dimasukkan dalam wadah yang berisi air,
selanjutnya direbus sampai uap air dan minyaknya mengalir dan didinginkan
melalui pipa dalam kondensor. Air dan minyak yang keluar dari kondensor
ditampung dalam labu pemisah (Yuliani dan Satuhu, 2012).
b. Penyulingan dengan air dan uap (water and steam distillation)
Bahan tumbuhan yang akan disuling dengan metode penyulingan air dan
uap ditempatkan dalam suatu tempat yang bagian bawah dan tengah berlubang-
lubang yang ditopang diatas dasar alat penyulingan. Ketel diisi dengan air
sampai permukaan air berada tidak jauh di bawah saringan, uap air akan naik
bersama minyak atsiri kemudian dialirkan melalui pendingin. Hasil
sulingannya adalah minyak atsiri yang belum murni (Guenther, 1947).
c. Penyulingan dengan uap (steam distillation)
Pada metode ini, wadah dan tangki air sebagai sumber uap panas (boiler)
diletakkan terpisah, didalam boiler terdapat pipa yang berhubungan dengan
wadah. Air dari boiler akan mendidih, lalu uapnya mengalir ke wadah yang
berisi bahan tumbuhan. Uap akan menembus sel - sel tumbuhan dan membawa
uap minyak atsiri yang selanjutnya akan mengalir melalui kondensor. Uap
minyak atsiri akan mengembun menjadi cairan dan ditampung pada labu
pemisah (Guenther, 1947; Yuliani dan Satuhu, 2012).
2.4.2 Metode pengepresan
Ekstraksi minyak atsiri dengan cara pengepresan umumnya dilakukan
terhadap bahan berupa biji, buah, atau kulit buah yang memiliki kandungan
mengandung minyak atsiri akan pecah dan minyak atsiri akan mengalir ke
permukaan bahan (Ketaren, 1985).
2.4.3 Ekstraksi dengan pelarut menguap
Prinsipnya adalah melarutkan minyak atsiri dalam pelarut organik yang
mudah menguap. Metode ini digunakan untuk mengambil minyak bunga yang
kurang stabil dan dapat dirusak oleh panas uap air. Dengan menggunakan pelarut
yang mudah menguap seperti kloroform, eter, aseton, alkohol, petroleum eter.
Pada ekstraksi ini, bahan pelarut dialirkan secara berkesinambungan melalui
serangkaian penampan yang diisi bahan tumbuhan, sampai ekstraksi selesai.
Cairan ekstrak yang mengandung bahan pelarut dan unsur - unsur tumbuhan itu
disalurkan ke tabung hampa udara yang dipanaskan pada suhu sekedar untuk
menguapkan pelarut. Uap pelarut dialirkan ke kondensor untuk dicairkan kembali,
sedangkan unsur - unsur tumbuhan tertinggal dalam tabung hampa tersebut
(Guenther, 1947).
2.4.4 Ekstraksi dengan lemak padat
Proses ini umumnya digunakan untuk mengekstraksi bunga - bungaan, untuk
mendapatkan mutu dan rendeman minyak atsiri yang tinggi. Metode ekstraksi
dapat dilakukan dengan dua cara, yaitu:
a. Ekstraksi dengan lemak tanpa pemanasan (Enfleurage)
Cara ini menggunakan media lemak padat. Metode ini digunakan karena
diketahui beberapa jenis bunga yang telah dipetik, enzimnya masih
menunjukkan kegiatan dalam menghasilkan minyak atsiri sampai beberapa
hari/minggu, seperti bunga melati, sehingga perlu perlakuan yang tidak
diatas media lilin dan dieramkan sampai beberapa hari/minggu, selanjutnya
lemak padat dikerok (dikenal dengan pomade) dan diekstraksi menggunakan
etanol (Gunawan dan Mulyani, 2004).
b. Ekstraksi dengan lemak panas (Maceration)
Cara ini dilakukan terhadap bahan tumbuhan yang bila dilakukan
penyulingan atau enfleurasi akan menghasilkan minyak atsiri dengan rendeman
yang rendah. Pada cara ini absorbsi minyak atsiri oleh lemak dalam keadaan
panas pada suhu 80oC selama 1,5 jam. Selesai pemanasan, campuran disaring
panas-panas, jika perlu kelebihan lemak pada ampas disiram dengan air panas.
Kemudian dilakukan penyulingan untuk memperoleh minyak atsiri
(Ketaren, 1985).
2.4.5. Ecuelle
Metode ini digunakan untuk mengisolasi minyak atsiri yang terdapat pada
buah - buahan seperti jeruk dengan cara menembus lapisan epidermis sampai ke
dalam jaringan yang mengandung minyak atsiri. Metode mengeluarkan minyak
jeruk dengan menusuk kelenjar minyak dan menggelindingkan buah pada wadah
yang memiliki tonjolan tajam yang berjejer. Tonjolan tersebut cukup panjang untuk
menembus epidermis. Tetes minyak yang jatuh pada wadah kemudian dikumpulkan
(Tyler et al., 1977).
2.5 Analisis Komponen Minyak Atsiri dengan GC-MS
Analisis dan karakterisasi komponen minyak atsiri merupakan masalah
yang cukup rumit, ditambah dengan sifatnya yang mudah menguap pada suhu
minyak atsiri. Sejak ditemukannya kromatografi gas (GC), kendala dalam analisis
komponen minyak atsiri ini mulai dapat diatasi walaupun terbatas hanya pada
analisis kualitatif dan penentuan kuantitatif komponen penyusun minyak atsiri
saja. Pada penggunaan GC, efek penguapan dapat dihindari bahkan dihilangkan
sama sekali. Perkembangan teknologi instrumentasi yang sangat pesat akhirnya
dapat melahirkan suatu alat yang merupakan gabungan dua sistem dengan prinsip
dasar yang berbeda satu sama lain tetapi dapat saling menguntungkan dan saling
melengkapi, yaitu gabungan antara kromatografi gas dan spektrometri massa
(GC-MS). Pada alat GC-MS, kedua alat dihubungkan dengan suatu interfase.
Kromatografi gas disini berfungsi sebagai alat pemisah berbagai komponen
campuran dalam sampel sedangkan spektrometer massa berfungsi untuk
mendeteksi masing-masing molekul komponen yang telah dipisahkan pada
kromatografi gas (Agusta, 2000).
2.5.1 Kromatografi gas
Kromatografi gas merupakan teknik pemisahan yang mana solut - solut
yang mudah menguap dan stabil terhadap panas bermigrasi melalui kolom yang
mengandung fase diam dengan suatu kecepatan yang tergantung pada rasio
distribusinya. Pada umumnya solut akan terelusi berdasarkan pada peningkatan
titik didihnya, kecuali jika ada interaksi khusus antara solut dan fase diam. Fase
gerak yang berupa gas akan mengelusi solut dari ujung kolom lalu
menghantarkannya ke detektor. Penggunaan suhu yang meningkat (biasanya
kisaran 50ºC - 350ºC) bertujuan untuk menjamin bahwa solute akan menguap dan
Komponen campuran dapat diidentifikasi dengan menggunakan waktu
tambat (waktu retensi) yang khas pada kondisi yang tepat. Waktu tambat ialah
waktu yang menunjukkan berapa lama suatu senyawa tertahan dalam kolom yang
diukur mulai saat penyuntikan sampel sampai saat elusi terjadi (dihasilkan
puncak) (Gritter, dkk., 1985). Bagian utama dari kromatografi gas adalah gas
pembawa, sistem injeksi, kolom, fase diam, suhu dan detektor.
2.5.1.1 Gas pembawa
Pemilihan gas pembawa tergantung pada detektor yang dipakai. Syarat gas
pembawa antara lain inert, murni dan dapat disimpan dalam tangki tekanan tinggi.
Gas pembawa yang sering dipakai adalah Helium (He), Argon (Ar), Nitrogen
(N2), Hidrogen (H2) dan Karbon dioksida (CO2). Helium merupakan tipe gas
pembawa yang sering digunakan karena memberikan efisiensi kromatografi yang
lebih baik (mengurangi pelebaran pita) (Gandjar dan Rohman, 2007).
2.5.1.2 Sistem injeksi
Cuplikan dimasukkan ke dalam ruang suntik melalui gerbang suntik
(injection port), biasanya berupa lubang yang ditutupi dengan septum atau karet
pemisah (rubber septum). Ruang suntik harus dipanaskan tersendiri, terpisah dari
kolom dan biasanya pada suhu 10 - 15ºC lebih tinggi dari suhu kolom. Jadi
seluruh cuplikan diuapkan segera setelah disuntikkan dan dibawa ke kolom
(Gritter, dkk., 1985).
2.5.1.3 Kolom
Kolom merupakan tempat terjadinya proses pemisahan karena didalamnya
terdapat fase diam (Gandjar dan Rohman, 2007). Kolom dapat dibuat dari
lurus, lengkung, melingkar. Ada dua macam kolom, yaitu kolom kemas dan
kolom kapiler (Agusta, 2000; McNair dan Bonelli, 1988).
Kolom kemas terdiri dari fase cair (sekurang-kurangnya pada suhu
kromatografi) yang tersebar pada permukaan penyangga yang lembab (inert) yang
terdapat dalam tabung yang relatif besar (diameter dalam 1 - 3 mm). Jenis kolom
ini terbuat dari gelas atau logam yang tahan karat atau dari tembaga dan
aluminium. Efisiensi kolom akan meningkat dengan semakin bertambah halusnya
partikel fase diam. Semakin kecil diameter partikel fase diam, maka efisiensinya
akan meningkat. Ukuran partikel fase diam biasanya berkisar antara 60-80 mesh
(Gandjar dan Rohman, 2007).
Kolom kapiler berbeda dengan kolom kemas, dalam hal adanya rongga
pada bagian dalam kolom yang menyerupai pipa (tube) dengan ukuran 0,02 - 0,2
mm. Kolom kapiler kini lebih banyak digunakan untuk menganalisis komponen
minyak atsiri. Hal ini disebabkan oleh keunggulan kolom tersebut yang
memberikan hasil analisis dengan daya pisah yang tinggi dan sekaligus memiliki
sensitivitas yang tinggi. Keuntungan kolom kapiler adalah jumlah sampel yang
dibutuhkan sedikit dan pemisahan lebih sempurna (Agusta, 2000; Gandjar dan
Rohman, 2007).
2.5.1.4 Fase diam
Fase diam dibedakan berdasarkan kepolarannya, yaitu nonpolar, sedikit
polar, semipolar, polar dan sangat polar. Berdasarkan kepolaran minyak atsiri yang
nonpolar sampai sedikit polar, maka untuk keperluan analisis sebaiknya digunakan
kolom fase diam yang bersifat sedikit polar, misalnya SE-52 dan SE-54 (Agusta,
2.5.1.5 Suhu
a. Suhu injektor
Suhu pada injektor harus cukup panas untuk menguapkan cuplikan
sedemikian cepat, tetapi sebaliknya suhu harus cukup rendah untuk mencegah
peruraian atau penataan ulang akibat panas (Gandjar dan Rohman, 2007).
b. Suhu kolom
Pemisahan dapat dilakukan pada suhu tetap (isotermal) atau pada suhu
yang berubah secara terkendali (suhu diprogram, temperature programming).
GC isotermal paling banyak dilakukan pada analisis rutin atau jika kita
mengetahui agak banyak mengenai sifat sampel yang akan dipisahkan. Pilihan
awal yang baik adalah suhu beberapa derajat dibawah titik didih komponen
utama sampel. Pada GC suhu diprogram, suhu dinaikkan mulai dari suhu
tertentu sampai suhu tertentu lainnya dengan laju yang diketahui dan terkendali
pada waktu tertentu (Gritter, dkk., 1985).
c. Suhu detektor
Detektor harus cukup panas sehingga cuplikan/fase diam tidak
mengembun dan juga untuk mencegah pengembunan air atau hasil samping
yang terbentuk pada proses pengionan (McNair dan Bonelli, 1988).
2.5.1.6 Detektor
Detektor yang populer yaitu detektor hantar-termal (thermal conductivity
detector) dan detektor pengion nyala (flame ionization detector) (McNair dan
Bonelli,1988).
a. Detektor hantar-termal (Thermal Conductivity Detector, TCD)
dialiri arus listrik yang tetap. Gas pembawa mengalir terus menerus melewati
kawat pijar yang panas itu dan suhu dibuat dengan laju tetap. Bila molekul
cuplikan yang bercampur dengan gas pembawa melewati kawat pijar meningkat,
terjadi perubahan tahanan yang diukur dengan jembatan Wheatstone dan sinyalnya
ditangkap oleh perekam dan tampak sebagai suatu puncak. Prinsip kerjanya
didasarkan pada kemampuan suatu gas menghantar panas dari kawat pijar dan
merupakan fungsi bobot molekul gas tersebut (McNair dan Bonelli,1988).
b. Detektor pengion nyala (Flame Ionization Detector, FID)
Hidrogen dan udara digunakan untuk menghasilkan nyala. Suatu elektroda
pengumpul yang bertegangan arus searah ditempatkan diatas nyala dan mengukur
hantaran nyala. Dengan hidrogen murni, hantaran sangat rendah, tetapi ketika
senyawa organik dibakar, hantaran naik dan arus yang mengalir dapat diperkuat
ke perekam (McNair dan Bonelli,1988).
2.5.2 Spektrometri massa (MS)
Spektrometri massa (MS) ialah molekul senyawa organik (sampel)
ditembak dengan elektron berenergi tinggi dan salah satu elektron valensinya akan
lepas. Hasilnya adalah suatu radikal ion (suatu spesi dengan satu elektron tak
berpasangan) dan ion bermuatan +1. Spektrum massa merupakan grafik antara
limpahan relatif ion lawan perbandingan massa dan muatan (m/z, m/e). Suatu
spektrometer massa bekerja dengan membangkitkan molekul-molekul bermuatan
atau fragmen-fragmen molekul baik dalam keadaan sangat hampa atau segera
sebelum sampel memasuki ruang sangat hampa (Watson, 2005; Supratman,
2010). Molekul senyawa organik pada spektrometer massa, ditembak dengan
yang tinggi karena lepasnya elektron dari molekul yang dapat pecah menjadi ion
yang lebih kecil (Sastrohamidjojo, 2004).
Spektrum massa hasil analisis sistem spektroskopi massa merupakan
gambaran mengenai jenis dan jumlah fragmen molekul yang terbentuk dari suatu
komponen kimia (masing - masing puncak pada kromatogram). Setiap fragmen
yang terbentuk dari pemecahan suatu komponen kimia memiliki berat molekul
yang berbeda dan ditampilkan dalam bentuk diagram dua dimensi, m/z (m/e,
massa/muatan) pada sumbu X dan intensitas pada sumbu Y yang disebut
spektrum massa. Pola pemecahan (fragmentasi) molekul yang terbentuk untuk
setiap komponen kimia sangat spesifik sehingga dapat dijadikan sebagai patokan
untuk menentukan struktur molekul suatu komponen kimia. Selanjutnya,
spektrum massa komponen kimia yang diperoleh dari hasil analisis diidentifikasi
dengan cara dibandingkan dengan spektrum massa yang terdapat dalam suatu
bank data (Agusta, 2000).
Keuntungan utama spektrometri massa sebagai metode analisis yaitu
metode ini lebih sensitif dan spesifik untuk identifikasi senyawa yang tidak
diketahui atau untuk menetapkan keberadaan senyawa tertentu. Hal ini
disebabkan adanya pola fragmentasi yang khas sehingga dapat memberikan
informasi mengenai bobot molekul dan rumus molekul. Puncak ion molekul
penting dikenali karena memberikan bobot molekul senyawa yang diperiksa.
Puncak paling kuat (tertinggi) pada spektrum, disebut puncak dasar (base peak),
dinyatakan dengan nilai 100% dan kekuatan puncak lain, termasuk puncak ion
molekulnya dinyatakan sebagai persentase puncak dasar tersebut (Silverstein,
BAB III
METODE PENELITIAN
Metode penelitian ini dilakukan secara eksplorasi yang meliputi penyiapan
sampel, karakterisasi simplisia, isolasi minyak atsiri dan analisis komponen dari
daun salam koja (Murraya koenigii) segar dan kering secara GC-MS.
3.1 Alat - alat
Alat - alat yang digunakan pada penelitian adalah neraca kasar (Ohaus),
lemari pengering, mikroskop, neraca listrik (Mettler Toledo), alat-alat gelas
laboratorium, oven, seperangkat alat Stahl, seperangkat alat destilasi air (Water
Distillation), piknometer, Refraktometer Abbe, Gas Chromatograph-Mass
Spectrometer (GC-MS) model Shimadzu QP 2010 S.
3.2 Bahan - bahan
Bahan - bahan yang digunakan dalam penelitian adalah daun salam koja
segar dan kering, bahan-bahan kimia kecuali dinyatakan lain adalah pro analisis
antara lain akuades (teknis), etanol 96%, kloralhidrat (E. Merck ), kloroform (E.
Merck ), natrium sulfat anhidrat (E. Merck ) dan toluen (E. Merck).
3.3 Penyiapan Sampel
Penyiapan sampel meliputi pengambilan bahan, identifikasi bahan dan
3.3.1 Pengambilan bahan
Metode pengambilan bahan dilakukan secara purposif. Bahan diambil dari
Daerah Tapak Tuan, Aceh Selatan tanpa membandingkan dengan bahan yang
sama dari daerah lain. Bahan yang digunakan adalah daun salam koja segar dan
kering.
3.3.2 Identifikasi bahan
Identifikasi bahan dilakukan di “Herbarium Bogoriense” Bidang Botani
Pusat Penelitian Biologi LIPI Bogor.
3.3.3 Pengolahan bahan
Pengolahan bahan dilakukan terhadap daun salam koja yaitu daun
dibersihkan dari kotoran yang melekat, disortasi basah lalu dicuci dengan air
sampai bersih, ditiriskan, kemudian ditimbang (6 kg), sebagian daun salam koja
digunakan untuk isolasi minyak atsiri sampel segar sedangkan sebagian lagi
dikeringkan.
Sebanyak 3,5 kg daun salam koja dikeringkan di lemari pengering pada suhu tidak
lebih dari 40 - 50˚C sampai menjadi simplisia kemudian ditimbang (1,065 kg).
3.4 Pemeriksaan Makroskopik dan Mikroskopik Daun Salam Koja Segar
3.4.1 Pemeriksaan makroskopik
Pemeriksaan makroskopik dilakukan dengan mengamati bentuk luar dari
daun salam koja segar.
3.4.2 Pemeriksaan mikroskopik
Pemeriksaan mikroskopik dilakukan terhadap penampang melintang dari
Caranya: sayatan melintang daun salam koja diletakkan diatas kaca objek yang
telah ditetesi dengan larutan kloralhidrat jenuh, dipanaskan, ditutup dengan kaca
penutup, lalu diamati di bawah mikroskop.
3.5 Pemeriksaan Karakteristik Simplisia
Pemeriksaan karakteristik simplisia meliputi pemeriksaan makroskopik,
pemeriksaan mikroskopik, penetapan kadar air, penetapan kadar sari larut dalam
air, penetapan kadar sari larut dalam etanol, penetapan kadar abu total, penetapan
kadar abu tidak larut dalam asam.
3.5.1 Pemeriksaan makroskopik simplisia
Pemeriksaan makroskopik dilakukan dengan mengamati bentuk luar,
ukuran serta warna dari daun salam koja kering.
3.5.2 Pemeriksaan mikroskopik serbuk simplisia
Pemeriksaan mikroskopik dilakukan terhadap serbuk simplisia daun salam
koja kering.
Caranya: serbuk simplisia ditaburkan diatas kaca objek yang telah ditetesi dengan
larutan kloralhidrat jenuh dan ditutup dengan kaca penutup, kemudian diamati di
bawah mikroskop.
3.5.3 Penetapan kadar air
a. Penjenuhan toluen
Toluen sebanyak 200 ml dimasukkan ke dalam labu alas bulat, lalu
ditambahkan 2 ml air suling, kemudian alat dipasang dan dilakukan destilasi
selama 2 jam. Destilasi dihentikan dan dibiarkan dingin selama ± 30 menit,
b. Penetapan kadar air simplisia
Labu berisi toluen tersebut dimasukkan 5 g serbuk simplisia yang telah
ditimbang seksama, dipanaskan hati-hati selama 15 menit. Setelah toluen
mendidih, kecepatan toluen diatur 2 tetes per detik sampai sebagian besar air
terdestilasi, kemudian kecepatan destilasi dinaikkan sampai 4 tetes per detik.
Setelah semua air terdestilasi, bagian dalam pendingin dibilas dengan toluen.
Destilasi dilanjutkan selama 5 menit, tabung penerima dibiarkan mendingin pada
suhu kamar. Setelah air dan toluen memisah sempurna, volume air dibaca dengan
ketelitian 0,05 ml. Selisih kedua volume air yang dibaca sesuai dengan kadar air
yang terdapat dalam bahan yang diperiksa. Kadar air dihitung dalam persen
(WHO, 2011).
3.5.4 Penetapan kadar sari larut air
Sebanyak 5 g serbuk yang telah dikeringkan, dimaserasi selama 24 jam
dalam 100 ml air - kloroform (2,5 ml kloroform dilarutkan di dalam 1 L akuades)
dalam labu tersumbat sambil sesekali dikocok selama 6 jam pertama, kemudian
dibiarkan selama 18 jam, lalu disaring. Sejumlah 20 ml filtrat pertama diuapkan
sampai kering dalam cawan penguap berdasar rata yang telah dipanaskan dan
ditara. Sisa dipanaskan pada suhu 105˚C sampai bobot tetap. Kadar dalam
persensari yang larut dalam air dihitung terhadap bahan yang telah dikeringkan
(Depkes, 1995).
3.5.5 Penetapan kadar sari larut etanol
Sebanyak 5 g serbuk yang telah dikeringkan, dimaserasi selama 24 jam
dalam 100 ml etanol 95% dalam labu tersumbat sambil sesekali dikocok selama 6
menghindari penguapan etanol. Sejumlah 20 ml filtrat pertama diuapkan sampai
kering dalam cawan penguap berdasar rata yang telah dipanaskan dan ditara. Sisa
dipanaskan pada suhu 105˚C sampai bobot tetap. Kadar dalam persen sari yang
larut dalam etanol 95% dihitung terhadap bahan yang telah dikeringkan (Depkes,
1995).
3.5.6 Penetapan kadar abu total
Sebanyak 2 g serbuk yang telah digerus dan ditimbang seksama
dimasukkan ke dalam krus porselin yang telah dipijar dan ditara, kemudian
diratakan. Krus porselin dipijar perlahan-lahan sampai arang habis, pemijaran
dilakukan pada suhu 500 - 600˚C selama 3 jam kemudian didinginkan dan
ditimbang sampai diperoleh bobot tetap. Kadar abu dihitung terhadap bahan yang
telah dikeringkan (WHO, 2011).
3.5.7 Penetapan kadar abu tidak larut dalam asam
Abu yang telah diperoleh dalam penetapan kadar abu dididihkan dalam 25
ml asam klorida encer selama 5 menit, bagian yang tidak larut asam dikumpulkan,
disaring melalui kertas saring dan dipijar sampai bobot tetap, kemudian
didinginkan dan ditimbang. Kadar abu yang tidak larut dalam asam dihitung
terhadap bahan yang dikeringkan (WHO, 2011).
3.5.8 Penetapan kadar minyak atsiri
Penetapan kadar minyak atsiri dilakukan dengan menggunakan alat Stahl.
Caranya: sebanyak 15 g daun salam koja yang telah diremukkan dimasukkan
dalam labu alas bulat berleher pendek, ditambahkan air suling sebanyak 300 ml,
pasang alat, diisi buret dengan air hingga penuh, dipanaskan dengan tangas udara,
penyulingan selesai, biarkan tidak kurang dari 15 menit, catat volume minyak
atsiri pada buret. Hitung kadar minyak atsiri dalam % v/b (Ditjen POM, 1979).
3.6 Isolasi Minyak Atsiri
Isolasi minyak atsiri dilakukan dengan metode penyulingan air (water
distillation).
Caranya: sebanyak 100 g serbuk simplisia dimasukkan dalam labu alas datar
berleher panjang 2 L ditambahkan akuades sampai sampel terendam. Kemudian
dirangkai alat destilasi air. Destilasi dilakukan selama 4 - 5 jam. Minyak atsiri
yang diperoleh ditampung dalam corong pisah, setelah itu dipisahkan antara
minyak dan air. Kemudian minyak atsiri yang diperoleh ditambahkan natrium
sulfat anhidrat dan didiamkan selama 1 hari. Minyak atsiri dipipet dan disimpan
dalam botol berwarna gelap.
3.7 Identifikasi Minyak Atsiri
3.7.1 Penetapan parameter fisika
3.7.1.1 Penentuan indeks bias
Penentuan indeks bias dilakukan dengan menggunakan alat Refraktometer
Abbe.
Caranya: alat Refraktometer Abbe dihidupkan. Prisma atas dan prisma bawah
dipisahkan dengan membuka klem dan dibersihkan dengan mengoleskan kapas
yang telah dibasahi dengan alkohol dan dikeringkan. Cuplikan minyak diteteskan
ke prisma bawah lalu ditutup. Melalui teleskop dapat dilihat adanya bidang terang
bidang terang dan gelap terbagi atas dua bagian yang sama secara vertikal.
Dengan melihat skala dapat dibaca indeks biasnya.
3.7.1.2 Penentuan bobot jenis
Penentuan bobot jenis ditentukan dengan alat piknometer.
Caranya: Piknometer kosong ditimbang dengan seksama. Piknometer kosong diisi
dengan air suling lalu ditimbang dengan seksama. Kemudian piknometer
dikosongkan dan dibilas beberapa kali dengan alkohol kemudian dikeringkan
dengan bantuan hair dryer. Piknometer diisi minyak atsiri yang akan ditentukan
berat jenisnya selanjutnya dilakukan seperti pengerjaan pada air suling. Hasil
bobot minyak atsiri yang diperoleh dengan mengurangkan bobot piknometer yang
diisi minyak atsiri dengan bobot piknometer kosong. Bobot jenis minyak atsiri
adalah hasil perbandingan bobot minyak atsiri terhadap bobot air suling dalam
piknometer dengan volume dan suhu yang sama, kecuali dinyatakan lain dalam
monograf keduanya ditetapkan pada suhu 25˚C (Ditjen POM, 1995).
3.7.2 Analisis komponen minyak atsiri
Penentuan komponen minyak atsiri dilakukan di Laboratorium Penelitian
Fakultas Farmasi USU dengan menggunakan seperangkat alat Gas
Chromatograph-Mass Spectrometer (GC-MS).
Kondisi analisis adalah jenis kolom kapiler Rtx-5 MS, panjang kolom 3 m,
diameter kolom dalam 0,25 mm, suhu injektor 270˚C, gas pembawa He dengan
laju alir 1,16 ml/menit. Suhu kolom terprogram (temperature programing) dengan
suhu awal 60˚C selama 5 menit, lalu dinaikkan perlahan -lahan dengan laju
kenaikan 5,0˚C/menit sampai suhu akhir 280˚C yang dipertahankan selama 30
Cara identifikasi komponen minyak atsiri adalah dengan membandingkan
spektrum massa dari komponen minyak atsiri yang diperoleh (unknown) dengan
spektrum massa dalam data library yang memiliki tingkat kemiripan (similary
BAB IV
HASIL DAN PEMBAHASAN
4.1 Identifikasi Tumbuhan
Hasil identifikasi yang dilakukan di “Herbarium Bogoriense” Pusat
Penelitian Biologi-LIPI Bogor terhadap salam koja yang diteliti adalah Murraya
Koenigii (L.) Spreng , dari suku Rutaceae. Hasil identifikasi dapat dilihat pada
Lampiran 1, halaman 66.
4.2 Hasil Makroskopik dan Mikroskopik Daun Salam Koja Segar 4.2.1 Hasil pemeriksaan makroskopik
Hasil pemeriksaan makroskopik daun salam koja segar dicirikan dengan
warna permukaan luar hijau, permukaan daun berbentuk jorong sampai bundar
panjang, panjang 4 - 5 cm, lebar 2 cm, ujung daun meruncing, pinggir daun rata
atau agak beringgit, permukaan daun licin. Gambar selengkapnya dapat dilihat
pada Lampiran 3, halaman 68.
4.2.2 Hasil pemeriksaan mikroskopik
Hasil pemeriksaan mikroskopik daun salam koja segar adalah terdapat
rambut penutup, kutikula, lapisan epidermis, jaringan palisade, kristal kalsium
oksalat, adanya fragmen rongga minyak lisigen, jaringan parenkim, tulang daun,
dan berkas pembuluh. Gambar selengkapnya dapat dilihat pada Lampiran 4,
4.3 Hasil Pemeriksaan Karakteristik Simplisia 4.3.1 Hasil pemeriksaan makroskopik simplisia
Hasil pemeriksaan makroskopik simplisia daun salam koja adalah, warna
daun hijau kecoklatan, bagian luar berwarna putih kecoklatan, menggulung
kedalam. Serbuk simplisia daun salam koja dicirikan dengan serbuk berwarna
hijau kecoklatan dan berbau khas. Gambar selengkapnya dapat dilihat pada
Lampiran 3, halaman 68.
4.3.2 Hasil pemeriksaan mikroskopik serbuk simplisia
Hasil pemeriksaan mikroskopik serbuk simplisia daun salam koja adalah
terdapat jaringan parenkim, fragmen rongga minyak lisigen, kristal kalsium
oksalat, rambut penutup, stomata tipe anomositik dan berkas pengangkut. Gambar
selengkapnya dapat dilihat pada Lampiran 4, halaman 70.
4.3.3 Hasil pemeriksaan karakterisasi simplisia
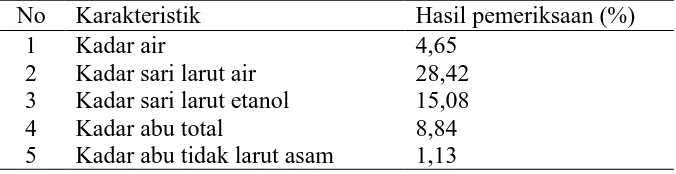
Hasil karakterisasi terhadap simplisia daun salam koja dapat dilihat pada
Tabel 4.1 berikut ini dan data hasil perhitungan dapat dilihat pada Lampiran 6-10,
[image:46.595.115.453.568.655.2]halaman 74-78.
Tabel 4.1 Hasil karakterisasi simplisia daun salam koja
No Karakteristik Hasil pemeriksaan (%)
1 Kadar air 4,65
28,42 2 Kadar sari larut air
3 Kadar sari larut etanol 15,08
4 Kadar abu total 8,84
1,13 5 Kadar abu tidak larut asam
Kadar air simplisia menunjukkan jumlah air yang terkandung dalam
simplisia, dari hasil penelitian diperoleh kadar air simplisia 4,65% dan memenuhi
simplisia dilakukan untuk mendapatkan simplisia yang tidak mudah rusak oleh
mikroba seperti jamur sehingga dapat disimpan dalam waktu yang lebih lama..
Kadar air simplisia berpengaruh dengan proses enzimatik dan media pertumbuhan
kapang dan jasad renik. Selain itu kadar air juga berpengaruh pada hasil minyak
atsiri yang diperoleh. Semakin tinggi kadar air maka hasil minyak atsiri yang
diperoleh akan semakin kecil karena perbandingan antara bahan tumbuhan dengan
air yang terkandung dalam tumbuhan akan semakin kecil sedangkan minyak atsiri
hanya terdapat di dalam bahan tumbuhan (BPOM RI, 2005; Trease dan Evans,
1983).
Penetapan kadar sari dilakukan terhadap 2 pengujian yaitu kadar sari larut
dalam etanol dan dalam air. Penetapan kadar sari yang larut dalam air dan dalam
etanol dilakukan untuk mengetahui jumlah senyawa yang dapat tersari dalam air
dan etanol dari simplisia. Senyawa yang bersifat polar atau larut dalam air pada
simplisia daun salam koja seperti glikosida, protein, polisakarida dan zat warna
akan tersari oleh air dengan hasil 28,42% sedangkan senyawa-senyawa yang tidak
larut dalam air atau larut dalam etanol seperti flavonoid, alkaloid akan tersari oleh
etanol dengan hasil 15,08% (Dikui, 2009).
Penetapan kadar abu dimaksudkan untuk mengetahui kandungan mineral
internal yang terdapat di dalam simplisia serta senyawa organik setelah
pembakaran. Abu total terbagi dua, yang pertama abu fisiologis adalah abu yang
berasal dari jaringan tumbuhan itu sendiri dan abu non fisiologis adalah sisa yang
berasal dari benda asing yang terdapat pada permukaan simplisia. Kadar abu tidak
larut asam untuk menentukan jumlah silika, khususnya pasir yang ada pada
4.4 Hasil Penetapan Kadar Minyak Atsiri
Penetapan kadar minyak atsiri dengan menggunakan alat Stahl diketahui
bahwa kadar minyak atsiri daun salam koja segar sebesar 0,17% v/b, sementara
kadar minyak atsiri daun salam koja kering sebesar 0,66% v/b.
Hasil penetapan kadar minyak atsiri menunjukkan bahwa kadar minyak
atsiri pada sampel kering lebih tinggi dari kadar minyak atsiri pada sampel segar,
hal ini disebabkan oleh kadar air pada daun salam koja segar sehingga
berpengaruh pada bobot sampel. Hasil penetapan kadar minyak atsiri dari daun
salam koja segar dan kering dapat dilihat pada tabel 4.2 berikut ini dan data hasil
[image:48.595.115.440.404.450.2]perhitungan dapat dilihat pada Lampiran 11, halaman 79.
Tabel 4.2 Hasil penetapan kadar minyak atsiri
4.5 Penentuan Indeks Bias dan Bobot Jenis Minyak Atsiri Hasil Isolasi
Hasil penentuan indeks bias dan bobot jenis minyak atsiri dapat dilihat
pada Tabel 4.3 berikut ini dan data hasil perhitungan dapat dilihat pada Lampiran
12-13, halaman 81-82
Tabel 4.3 Hasil penentuan indeks bias dan bobot jenis minyak atsiri
No Sampel Indeks Bias Bobot Jenis
1 Daun salam koja segar 1,4465 0,8901
2 Daun salam koja kering 1,4465 0,8902
Penetapan indeks bias minyak atsiri daun salam koja segar dan kering
hasilnya sama yaitu sebesar 1,4465 dan bobot jenis daun salam koja segar dan
kering tidak berbeda jauh yaitu masing-masing sebesar 0,8901 dan 0,8902.
No Sampel Kadar yang diperoleh (% b/v)
1 2
Daun salam koja segar Daun salam koja kering
[image:48.595.115.478.609.659.2]Komponen minyak atsiri daun salam koja segar dengan daun salam koja kering
yang diperoleh tidak mempengaruhi harga indeks bias.
Indeks bias merupakan perbandingan antara kecepatan cahaya di dalam
udara dengan kecepatan cahaya di dalam zat pada suhu tertentu. Indeks bias
berguna untuk identifikasi kemurnian dan berhubungan erat dengan
komponen-komponen yang tersusun dalam minyak atsiri yang dihasilkan (Armando, 2009).
Penetapan bobot jenis minyak atsiri daun salam koja segar dan kering
memenuhi syarat bobot jenis minyak atsiri di literatur. Nilai bobot jenis minyak
atsiri berkisar antara 0,696-1,188 dan pada umumnya nilai tersebut lebih kecil dari
1,000 (Guenther, 1947).
Bobot jenis merupakan salah satu kriteria penting dalam menentukan mutu
dan kemurnian minyak atsiri dimana bobot jenis sering dihubungkan dengan berat
komponen yang terkandung di dalamnya. Semakin besar fraksi berat yang
terkandung dalam minyak, semakin besar pula nilai bobot jenisnya (Armando,
2009).
4.6 Analisis dengan GC-MS
Hasil analisis komponen minyak atsiri hasil destilasi air dari daun salam
koja segar dengan Gas Chromatograph (GC) diperoleh 61 puncak dan diambil
enam komponen utama berdasarkan konsentrasi tertinggi sedangkan hasil analisis
komponen minyak atsiri daun salam koja kering diperoleh 57 puncak dan diambil
enam komponen utama berdasarkan konsentrasi tertinggi. Hasil selengkapnya
Gambar 4.1 Kromatogram GC minyak atsiri daun salam koja segar
Berdasarkan hasil analisis GC minyak atsiri daun salam koja segar
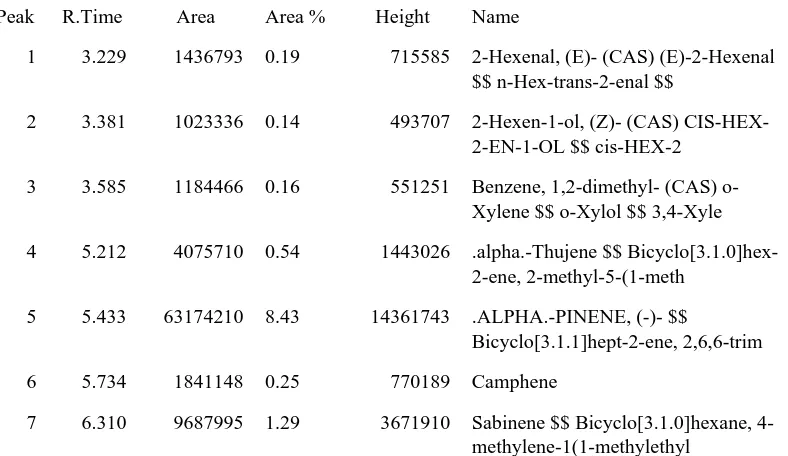
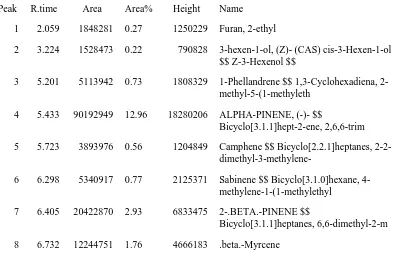
diperoleh 61 komponen dengan data pada Tabel 4.4 di bawah ini.
Tabel 4.4 Komponen minyak atsiri daun salam koja segar Peak R.Time Area Area % Height Name
1 3.229 1436793 0.19 715585 2-Hexenal, (E)- (CAS) (E)-2-Hexenal $$ n-Hex-trans-2-enal $$
2 3.381 1023336 0.14 493707 2-Hexen-1-ol, (Z)- (CAS) CIS-HEX-2-EN-1-OL $$ cis-HEX-2
3 3.585 1184466 0.16 551251 Benzene, 1,2-dimethyl- (CAS) o-Xylene $$ o-Xylol $$ 3,4-Xyle
4 5.212 4075710 0.54 1443026 .alpha.-Thujene $$ Bicyclo[3.1.0]hex-2-ene, 2-methyl-5-(1-meth
5 5.433 63174210 8.43 14361743 .ALPHA.-PINENE, (-)- $$
Bicyclo[3.1.1]hept-2-ene, 2,6,6-trim
6 5.734 1841148 0.25 770189 Camphene
[image:50.595.117.511.501.729.2]8 6.418 17374925 2.32 5702865 2-.BETA.-PINENE $$
Bicyclo[3.1.1]heptane, 6,6-dimethyl-2
9 6.744 10103090 1.35 3783539 .beta.-Myrcene $$ 1,6-octadiene, 7-methyl-3-methylene- (CAS)
10 7.076 7593894 1.01 2498270 1-PHELLANDRENE $$
11 7.384 2590777 0.35 1117487 .ALPHA.. TERPINENE $$ PARA-MENTHA-1,3-DIENE $$
12 7.451 13400699 1.79 4538680 Benzene, 1-methyl-4-(1-methylethyl)- (CAS) p-Cymene $$
13 7.674 54574855 7.28 11503083 .beta.-Phellandrene $$ Cyclohexene, 3-methylene-6-(1-methylet
14 7.836 4025901 0.54 1413414 cis-Ocimene $$ 1,Octatriene, 3,7-dimethyl-, (E)- (CAS)
15 8.101 19027748 2.54 6505698 1,3,6-Octatriene, 3,7-dimethyl, (E)- (CAS) .BETA. OCIMENE
16 8.338 5037245 0.67 2065501 .gamma.-Terpinene $$
1,4-Cyclohexadiene, 1-methyl-4-(1-meth
17 9.001 1886194 0.25 831777 .ALPHA.-TERPINOLENE $$ Cyclohexene, 1-methyl-4-(1-meth
18 9.120 3193929 0.43 1268999 Linalool $$ 1,6-Octadien-3-ol, 3,7-dimethyl- (CAS) Linalool $$
19 9.574 2278597 0.30 891210 p-menth-2-en-1-ol $$
20 9.907 1701491 0.23 671001 Bicyclo[3.1.1]hept-3-en-2-ol, 4,6,6-trimethyl-, [1S-(1.alpha.,
21 10.461 1915454 0.26 792239 4-Hexen-1-ol, 5-methyl-2-(1-methylethenyl)-
22 10.533 2251791 0.30 716732 Cryptone $$
4-Isopropyl-2-cyclohexen-1-one $$ 2-Cyclohexen-1
23 10.675 10950789 1.46 3391894 2-Cyclohexen-1-ol, 3-methyl-6-(1-methylethyl)-, cis-
24 10.873 2489822 0.33 1019446 Verbenol $$ 4,6,6-Trimethylbicyclo-[3.1.1]-hept-3-en-2-ol $$
25 12.641 7840602 1.05 1887696 2,6-Octadien-1-ol, 3-methyl-, acetate $$ Geraniol acetate $$
26 12.886 1117574 0.15 371253 Isopulegol acetate $$ 2-Isopropenyl-5-methylcyklohexyl acetate
27 13.657 2550502 0.34 809053 Bicykloelemene $$
28 13.878 2269978 0.30 736156 .alpha.-Cubebene
Gambar

Dokumen terkait
Penelitian yang dilakukan meliputi karakterisasi simplisia, isolasi minyak atsiri dengan cara destilasi air dan analisis komponen minyak atsiri secara Gas
ISOLASI MINYAK ATSIRI DARI SIMPLISIA KULIT KAYU SINTOK ( Cinnamomum sintoc Blume) DENGAN METODE.. DESTILASI UAP DAN AIR SERTA ANALISIS KOMPONENNYA
KARAKTERISASI SIMPLISIA, ISOLASI, DAN ANALISIS KOMPONEN MINYAK ATSIRI DARI RIMPANG DAN DAUN KUNYIT (Curcuma.. domestica Val.) KERING
Hasil penelitian diharapkan memberikan informasi tentang karakterisasi simplisia, isolasi minyak atsiri dan analisis komponennya secara GC-MS dari kulit buah jeruk jingga (Citrus
Analisis Farmasi: Buku Ajar untuk Mahasiswa Farmasi dan Praktisi Kimia Farmasi. Jakarta:
Penelitian yang dilakukan meliputi karakterisasi simplisia, isolasi minyak atsiri dengan cara destilasi air dan analisis komponen minyak atsiri secara Gas
The Effect of Water Extract of Salam Koja Leaf (Murraya koenigii (L.) spreng) Against Root-Knot Nematode (Meloidogyne spp.) in Tomato Plants.. Toto Sunarto 1 and Brigitta
Karunia-Nya lah sehingga tesis dengan judul : ANALISIS SENYAWA KIMIA MINYAK ATSIRI DAUN KARI ( Murraya koenigii L. ) DENGAN GC – MS DAN UJI AKTIVITAS