PENGESAHAN SKRIPSI
ISOLASI MINYAK ATSIRI DARI SEREH MERAH
(
Andropogon citratus
DC. ) SEGAR DAN KERING
SERTA ANALISIS KOMPONEN
SECARA GC-MS
OLEH:
BETTY MEILYA SITUMORANG NIM 111524002
Dipertahankan di Hadapan Panitia Penguji Skripsi Fakultas Farmasi Universitas Sumatera Utara
Pada Tanggal: September 2013
Pembimbing I, Panitia Penguji,
Drs. Panal Sitorus, M.Si., Apt. Dr. Marline Nainggolan, M.S., Apt. NIP 195310301980031002 NIP 195709091985112001
Drs. Panal Sitorus, M.Si., Apt.
Pembimbing II, NIP 194909101980031002
Prof.Dr.rer.nat.Effendy De Lux Putra, SU., Apt. Dra. Aswita Hafni Lubis, M.Si., Apt. NIP 195306191983031001 NIP 195304031983032001
Drs. Fathur Rahman Harun, M.Si., Apt. NIP 19520104198003002
Medan
Fakultas Farmasi
Universitas Sumatera utara Dekan,
KATA PENGANTAR
Puji syukur penulis ucapkan kepada Tuhan Yang Maha Esa atas segala rahmat dan karunia-Nya, sehingga penulis dapat menyelesaikan penelitian dan penyusunan skripsi ini. Skripsi ini disusun untuk melengkapi salah satu syarat
untuk memperoleh gelar Sarjana Farmasi pada Fakultas Farmasi Universitas Sumatera Utara, dengan judul Isolasi Minyak Atsiri dari Sereh Merah
(Andropogon citratus DC.) Segar dan Kering Serta Analisis Komponen Secara GC-MS.
Pada kesempatan ini dengan kerendahan hati dan hormat, penulis
mengucapkan terimakasih kepada Bapak Drs. Panal Sitorus, M.Si., Apt., dan Bapak Prof. Dr. rer. nat. Effendy De Lux Putra, S.U., Apt., yang telah
membimbing, memberikan petunjuk, saran-saran dan motivasi selama penelitian hingga selesainya skripsi ini. Ibu Dr. Marline Nainggolan, M.S., Apt., Bapak Drs. Fathur Rahman Harun, M.Si., Apt., dan Ibu Dra. Aswita
Hafni Lubis, M.Si., Apt., selaku dosen penguji yang telah memberikan kritik, saran dan arahan kepada penulis dalam menyelesaikan skripsi ini. Bapak Prof.
Dr. Sumadio Hadisahputra, Apt., selaku Dekan Fakultas Farmasi USU Medan, yang telah memberikan bimbingan dan penyediaan fasilitas sehingga penulis dapat menyelesaikan pendidikan. Bapak dan Ibu staf pengajar Fakultas Farmasi
Penulis juga mengucapkan terima kasih dan penghargaan yang tiada terhingga kepada Ayahanda P. Situmorang dan alm. Ibunda K. Pasaribu yang
telah memberikan cinta dan kasih sayang yang tidak ternilai dengan apapun, pengorbanan baik materi maupun motivasi beserta doa yang tulus yang tidak
pernah berhenti, untuk kakak-kakakku tersayang Lastry, dan Irma Suryani, S.Kom., dan adik-adikku tersayang Rudy, Margareth, dan Dedy Wijaya, dan sahabat-sahabat saya (”pemuda-pemudi gereja”, Nedy, Bettika, Febrin, Nova,
Ruth) yang selalu setia memberikan doa, dorongan dan semangat.
Penulis menyadari sepenuhnya bahwa dalam penulisan skripsi ini masih
jauh dari kesempurnaan, oleh karena itu dengan segala kerendahan hati, penulis menerima kritik dan saran demi kesempurnaan skripsi ini. Akhirnya, penulis berharap semoga skripsi ini dapat memberi manfaat bagi kita semua.
Medan, Oktober 2013 Penulis,
ISOLASI MINYAK ATSIRI DARI SEREH MERAH (Andropogon citratusDC.) SEGAR DAN KERING SERTA
ANALISIS KOMPONEN SECARA GC-MS
ABSTRAK
Minyak atsiri adalah istilah yang digunakan untuk minyak mudah menguap yang diperoleh dari bagian tanaman seperti daun, bunga, buah, kulit batang dan akar. Minyak sereh merupakan komoditi ekspor utama diantara berbagai jenis minyak atsiri, kandungan utama minyak sereh adalah sitronellal dan geraniol, kadar minyak atsiri dari tumbuhan sereh 0,5-1,2%. Sereh merah (Andropogon citratus DC.) dari family Poaceae adalah salah satu tumbuhan yang mengandung minyak atsiri dan dimanfaatkan masyarakat sebagai obat gosok. Tujuan penelitian ini adalah untuk mengetahui komponen dan kadar komponen minyak atsiri dari sereh merah segar dan kering.
Penelitian meliputi pengambilan dan pengolahan sampel, karakterisasi simplisia, penetapan kadar minyak atsiri dengan menggunakan alat Stahl, isolasi minyak atsiri sereh merah segar dan kering dengan menggunakan metode penyulingan air (water distillation), identifikasi minyak atsiri meliputi penetapan parameter fisika dan analisis komponen dengan menggunakan alat GC-MS.
Hasil pemeriksaan karakterisasi sereh merah kering diperoleh kadar air 5,983%; kadar sari yang larut dalam air 10,737%; kadar sari yang larut dalam etanol 9,809%; kadar abu total 4,27% dan kadar abu yang tidak larut dalam asam 0.39%. Kadar minyak atsiri dari sereh merah segar sebesar 0,42% v/b dan sereh merah kering sebesar 0,623%v/b. Indeks bias sereh merah segar dan kering sebesar 1,456. Bobot jenis sereh merah segar sebesar 0,8549 dan sereh merah kering sebesar 0,8544.
Hasil analisis minyak atsiri dari tumbuhan sereh merah segar, diperoleh enam komponen utama yaitu citronella (11,56%), β-citronellol (7,64%), geraniol (2,80%), eugenol (0,44%),citronellyl acetate (4,15%), elemol (10,76%). Hasil analisis GC-MS minyak atsiri dari sereh merah kering menunjukkan enam komponen utama yaitu, citronella (12,45%), β-citronellol (7,11%), geraniol (3,60%), eugenol (0,64%), δ-cadine (4,56%), elemol (17,35%).
ISOLATION OF VOLATILE OIL FROM FRESH AND DRIED RED LEMONGRASS (Andropogon citratusDC.) AND ANALYSIS OF
COMPONENTS BY GC-MS
ABSTRACT
Essential oil is a term used for volatile oil and obtained from part of plant such as leaves, flowers, fruit, bark and roots. Lemongrass oil is a major export commodities among the various types of essential oil. The main content of lemongrass oil are sitronellal and geraniol, and content oil of lemongrass is 0.5 to 1.2%. Andropogon citratus DC. of the family Poaceae is one of plant that contains essential oil and is widely used as a liniment. The objective of this research is to determine the component and content oil of fresh and dried red lemongrass.
The research includes sample collecting and processing, characterization of simplex, determination of essential oil content using Stahl, isolation of essential oil from fresh and dried red lemongrass using water distillation, the identification of essential oils include the determination of physical parameters and component analysis by Gas Chromatography-Mass Spectrometry (GC-MS) The results of simplex characterization of lemongrass red peel gave water value 5.983%; content of water-soluble extract 10.737%; content of ethanol-soluble extract 9.809%, total ash content 4.27% and acid insoluble ash 0.39%. Results of the assay of lemongrass red with Stahl tool obtained lemongrass essential oil content of fresh red by 0.42% v/w and botanicals lemongrass red at 0.623% v/w. The refractive index of both fresh and dried red lemongrass peel were 1.456. The specific gravity of fresh and dried red lemongrass peel were 0.8549 and 0.8544 respectively.
The result of GC-MS analysis of volatile oil from fresh lemongrass red essential oil peel contained 27 compounds with six main components they are citronella 11.56%, β-citronellol 7.64%, geraniol 2.80%, eugenol 0.44%, citronellyl acetate 4.15%, elemol 10.76%. Mean while the results of GC-MS analysis of volatile oil of dried lemongrass essential oil peel contained 25 compounds with six main components they are citronella 12.45%, β-citronellol 7.11%, geraniol 3.60%, eugenol 0.64%, δ-cadine 4.56%, elemol 17.35%.
DAFTAR ISI
Halaman
JUDUL ... i
HALAMAN JUDUL ... ii
LEMBAR PENGESAHAN ... iii
KATA PENGANTAR ... iv
ABSTRAK ... vi
ABSTRACT ... vii
DAFTAR ISI ... viii
DAFTAR TABEL ... xii
DAFTAR GAMBAR ... xiii
DAFTAR LAMPIRAN ... xiv
BAB I PENDAHULUAN ... 1
1.1 Latar Belakang ... 1
1.2 Perumusan Masalah ... 3
1.3 Hipotesis ... 4
1.4 Tujuan Penelitian ... 4
1.5 Manfaat Penelitian ... 4
BAB II TINJAUAN PUSTAKA... 5
2.1 Uraian Tumbuhan... 5
2.1.3 Nama asing... 6
2.1.4 Morfologi tumbuhan ... 6
2.1.5 Sistematika tumbuhan ... 6
2.1.6 Penggunaan tumbuhan ... 7
2.1.7 Kandungan kimia ... 7
2.2 Minyak Atsiri ... 7
2.2.1 Keberadaan minyak atsiri dalam tanaman ... 7
2.2.2 Komposisi kimia minyak atsiri ... 8
2.3 Sifat Fisikokimia Minyak Atsiri ... 9
2.3.1 Sifat fisik minyak atsiri ... 9
2.3.2 Cara isolasi minyak atsiri ... 10
2.4 Analisis Komponen Minyak Atsiri dengan GC-MS ... 13
2.4.1 Kromatografi gas ... 14
2.4.1.1 Gas pembawa ... 15
2.4.1.2 Sistem injeksi ... 15
2.4.1.3 Kolom ... 15
2.4.1.4 Fase diam ... 16
2.4.1.5 Suhu ... 16
2.4.1.6 Detektor ... 16
2.5 Spektrofotometri Massa ... 16
BAB III METODE PENELITIAN ... 18
3.1 Alat dan Bahan ... 18
3.1.2 Bahan ... 18
3.2 Penyiapan Sampel ... 19
3.2.1 Pengambilan sampel ... 19
3.2.2 Identifikasi tumbuhan ... 19
3.2.3 Pengolahan sampel ... 19
3.3 Pemeriksaan Karakteristik Simplisia ... 19
3.3.1 Pemeriksaan makroskopik ... 19
3.3.2 Pemeriksaan mikroskopik... 20
3.3.3 Penetapan kadar air ... 20
3.3.4 Penetapan kadar sari larut air... 21
3.3.5 Penetapan kadar sari larut etanol ... 21
3.3.6 Penetapan kadar abu total ... 22
3.3.7 Penetapan kadar abu tidak larut dalam asam ... 22
3.3.8 Penetapan kadar minyak atsiri ... 22
3.4 Isolasi Minyak Atsiri ... 23
3.5 Identifikasi Minyak Atsiri ... 23
3.5.1 Penentuan indeks bias ... 23
3.5.2 Penentuan bobot jenis ... 24
3.5.3 Analisis komponen minyak atsiri ... 24
BAB IV HASIL DAN PEMBAHASAN ... 26
4.1 Identifikasi Tumbuhan ... 26
4.2.2 Hasil pemeriksaan mikroskopik ... 26
4.2.3 Hasil pemeriksaan karakterisasi simplisia ... 26
4.3 Identifikasi Minyak Atsiri ... 29
4.4 Penentuan Indeks Bias dan Bobot Jenis Minyak Atsiri Hasil Isolasi ... 29
4.5 Analisis dengan GC-MS ... 31
4.5.1 Fragmentasi dan analisis hasil spektrofotometri massa minyak atsiri sereh merah segar ... 35
4.5.2 Fragmentasi dan analisis hasil spektrofotometri massa minyak atsiri sereh merah kering ... 40
BAB V KESIMPULAN DAN SARAN ... 46
5.1 Kesimpulan ... 46
5.2 Saran ... 47
DAFTAR PUSTAKA ... 48
DAFTAR TABEL
Halaman Tabel 4.1 Hasil karakterisasi simplisia sereh merah ... 27
Tabel 4.2 Hasil penetapan kadar minyak atsiri ... 29 Tabel 4.3 Hasil penentuan indeks bias dan bobot jenis minyak atsiri
hasil isolasi ... 29 Tabel 4.4 Komponen sereh merah segar ... 32 Tabel 4.5 Komponen sereh merah kering ... 33
Tabel 4.6 Waktu tambat dan kadar komponen minyak atsiri hasil
analisis GC-MS sereh merah segar ... 34 Tabel 4.7 Waktu tambat dan kadar komponen minyak atsiri hasil
DAFTAR GAMBAR
Halaman
Gambar 4.1 Kromatogram minyak atsiri sereh merah segar ... . 31
Gambar 4.2 Kromatogram minyak atsiri sereh merah kering ... . 32
Gambar 4.3 Rumus bangun dari senyawa sitronella ... . 36
Gambar 4.4 Rumus bangun dari senyawa β-citronellol ... . 37
Gambar 4.5 Rumus bangun dari senyawa geraniol ... . 37
Gambar 4.6 Rumus bangun dari senyawa eugenol ... . 38
Gambar 4.7 Rumus bangun dari senyawa citronellyl acetate ... . 39
Gambar 4.8 Rumus bangun dari senyawa elemol ... . 39
Gambar 4.9 Rumus bangun dari senyawa sitronella ... . 41
Gambar 4.10 Rumus bangun dari senyawa β-citronellol ... . 42
Gambar 4.11 Rumus bangun dari senyawa geraniol ... . 42
Gambar 4.12 Rumus bangun dari senyawa eugenol ... . 43
Gambar 4.13 Rumus bangun dari senyawa δ-cadinene ... . 44
DAFTAR LAMPIRAN
Halaman Lampiran 1 Hasil identifikasi tumbuhan sereh merah (Andropogon
citratusDC.) ... 51
Lampiran 2 Gambar tumbuhan sereh merah (Andropogon citratusDC.) ... 52
Lampiran 3 Batang sereh merah segar dan kering serta serbuk simplisia sereh merah ... 53
Lampiran 4 Hasil pemeriksaan mikroskopik simplisia sereh merah pada perbesaran 10x40 ... 54
Lampiran 5 Alat-alat yang digunakan ... 56
Lampiran 6 Perhitungan penetapan kadar air simplisia sereh merah ... 59
Lampiran 7 Perhitungan penetapan kadar sari larut dalam air simplisia sereh merah ... 60
Lampiran 8 Perhitungan penetapan kadar sari larut etanol ... 61
Lampiran 9 Perhitungan penetapan kadar abu total simplisia sereh merah ... 62
Lampiran 10 Perhitungan penetapan kadar abu tidak larut asam simplisia sereh merah ... 63
Lampiran 11 Penetapan kadar minyak atsiri sereh merah ... 64
Lampiran 12 Penetapan indeks bias minyak atsiri sereh merah ... 66
Lampiran 13 Kromatogram GC minyak atsiri sereh merah segar ... 67
Lampiran 14 Spektrum massa dari puncak dengan waktu tambat 12,617 menit ... 68
15,633 menit ... 69 Lampiran 17 Spektrum massa dari puncak dengan waktu tambat
18,317 menit ... 69 Lampiran 18 Spektrum massa dari puncak dengan waktu tambat
18,517 menit ... 70
Lampiran 19 Spektrum massa dari puncak dengan waktu tambat
23,892 menit ... 70
Lampiran 20 Kromatogram GC minyak atsiri sereh merah kering ... 71 Lampiran 21 Spektrum massa dari puncak dengan waktu tambat
12,892 menit ... 72 Lampiran 22 Spektrum massa dari puncak dengan waktu tambat
14,917 menit ... 72 Lampiran 23 Spektrum massa dari puncak dengan waktu tambat
15,633 menit ... 73 Lampiran 24 Spektrum massa dari puncak dengan waktu tambat
18,317 menit ... 73 Lampiran 25 Spektrum massa dari puncak dengan waktu tambat
23,358 menit ... 74
Lampiran 26 Spektrum massa dari puncak dengan waktu tambat
23,908 menit ... 74
Lampiran 27 Gambar pola fragmentasi komponen minyak atsiri
ISOLASI MINYAK ATSIRI DARI SEREH MERAH (Andropogon citratusDC.) SEGAR DAN KERING SERTA
ANALISIS KOMPONEN SECARA GC-MS
ABSTRAK
Minyak atsiri adalah istilah yang digunakan untuk minyak mudah menguap yang diperoleh dari bagian tanaman seperti daun, bunga, buah, kulit batang dan akar. Minyak sereh merupakan komoditi ekspor utama diantara berbagai jenis minyak atsiri, kandungan utama minyak sereh adalah sitronellal dan geraniol, kadar minyak atsiri dari tumbuhan sereh 0,5-1,2%. Sereh merah (Andropogon citratus DC.) dari family Poaceae adalah salah satu tumbuhan yang mengandung minyak atsiri dan dimanfaatkan masyarakat sebagai obat gosok. Tujuan penelitian ini adalah untuk mengetahui komponen dan kadar komponen minyak atsiri dari sereh merah segar dan kering.
Penelitian meliputi pengambilan dan pengolahan sampel, karakterisasi simplisia, penetapan kadar minyak atsiri dengan menggunakan alat Stahl, isolasi minyak atsiri sereh merah segar dan kering dengan menggunakan metode penyulingan air (water distillation), identifikasi minyak atsiri meliputi penetapan parameter fisika dan analisis komponen dengan menggunakan alat GC-MS.
Hasil pemeriksaan karakterisasi sereh merah kering diperoleh kadar air 5,983%; kadar sari yang larut dalam air 10,737%; kadar sari yang larut dalam etanol 9,809%; kadar abu total 4,27% dan kadar abu yang tidak larut dalam asam 0.39%. Kadar minyak atsiri dari sereh merah segar sebesar 0,42% v/b dan sereh merah kering sebesar 0,623%v/b. Indeks bias sereh merah segar dan kering sebesar 1,456. Bobot jenis sereh merah segar sebesar 0,8549 dan sereh merah kering sebesar 0,8544.
Hasil analisis minyak atsiri dari tumbuhan sereh merah segar, diperoleh enam komponen utama yaitu citronella (11,56%), β-citronellol (7,64%), geraniol (2,80%), eugenol (0,44%),citronellyl acetate (4,15%), elemol (10,76%). Hasil analisis GC-MS minyak atsiri dari sereh merah kering menunjukkan enam komponen utama yaitu, citronella (12,45%), β-citronellol (7,11%), geraniol (3,60%), eugenol (0,64%), δ-cadine (4,56%), elemol (17,35%).
ISOLATION OF VOLATILE OIL FROM FRESH AND DRIED RED LEMONGRASS (Andropogon citratusDC.) AND ANALYSIS OF
COMPONENTS BY GC-MS
ABSTRACT
Essential oil is a term used for volatile oil and obtained from part of plant such as leaves, flowers, fruit, bark and roots. Lemongrass oil is a major export commodities among the various types of essential oil. The main content of lemongrass oil are sitronellal and geraniol, and content oil of lemongrass is 0.5 to 1.2%. Andropogon citratus DC. of the family Poaceae is one of plant that contains essential oil and is widely used as a liniment. The objective of this research is to determine the component and content oil of fresh and dried red lemongrass.
The research includes sample collecting and processing, characterization of simplex, determination of essential oil content using Stahl, isolation of essential oil from fresh and dried red lemongrass using water distillation, the identification of essential oils include the determination of physical parameters and component analysis by Gas Chromatography-Mass Spectrometry (GC-MS) The results of simplex characterization of lemongrass red peel gave water value 5.983%; content of water-soluble extract 10.737%; content of ethanol-soluble extract 9.809%, total ash content 4.27% and acid insoluble ash 0.39%. Results of the assay of lemongrass red with Stahl tool obtained lemongrass essential oil content of fresh red by 0.42% v/w and botanicals lemongrass red at 0.623% v/w. The refractive index of both fresh and dried red lemongrass peel were 1.456. The specific gravity of fresh and dried red lemongrass peel were 0.8549 and 0.8544 respectively.
The result of GC-MS analysis of volatile oil from fresh lemongrass red essential oil peel contained 27 compounds with six main components they are citronella 11.56%, β-citronellol 7.64%, geraniol 2.80%, eugenol 0.44%, citronellyl acetate 4.15%, elemol 10.76%. Mean while the results of GC-MS analysis of volatile oil of dried lemongrass essential oil peel contained 25 compounds with six main components they are citronella 12.45%, β-citronellol 7.11%, geraniol 3.60%, eugenol 0.64%, δ-cadine 4.56%, elemol 17.35%.
BAB I PENDAHULUAN
1.1 Latar Belakang
Minyak atsiri atau disebut juga volatil oil atau essential oil adalah istilah yang digunakan untuk minyak mudah menguap yang diperoleh dari bagian tanaman seperti daun, bunga, buah, kulit batang dan akar
(Arswendiyumna, dkk., 2010). Minyak atsiri dalam keadaan segar dan murni umumnya tidak berwarna namun pada penyimpanan lama, minyak atsiri dapat
teroksidasi dan membentuk resin serta warnanya berubah menjadi lebih tua (gelap). Pencegahannya, minyak atsiri harus disimpan dalam bejana gelas yang berwarna gelap dan disimpan di tempat yang kering dan sejuk (Gunawan dan
Mulyani, 2010).
Sifat minyak atsiri yang menonjol antara lain mudah menguap pada
suhu kamar, mempunyai rasa getir, berbau wangi sesuai dengan aroma tanaman yang menghasilkannya, umumnya larut dalam pelarut organik (Lutony dan Rahmayanti, 2000). Minyak sereh merupakan komoditi ekspor
utama diantara berbagai jenis minyak atsiri, kandungan utama minyak sereh adalah sitronellal dan geraniol (Agustian, dkk., 2004).
komponen kimia tersebut adalah hal yang paling mendasar dalam menentukan aroma maupun kegunaan (sebagai bahan pengharum, kosmetik, obat, dll) jadi
penentuan komponen penyusun dan komposisi masing-masing komponen tersebut di dalam minyak atsiri merupakan hal yang sangat penting dalam
menentukan kegunaan, kualitas, ataupun mutu dari suatu minyak atsiri (Harborne, 1984).
Tanaman sereh sudah sejak lama dibudidayakan di Indonesia, memiliki
nama daerah yang berbeda-beda diantaranya serai (Jawa, Madura, Gayo), sarai (Minang), sorai (Lampung), see (Bali), kedoung witu (Sumba), di
mancanegara, tanaman sereh dikenal dengan citronella gross. Negara lain yang terus membudidayakan tanaman sereh antara lain Srilanka, Taiwan, Guatemala, dan yang terbesar adalah Republik Rakyat Cina (RRC) (Susetyo
dan Haryati, 2004).
Minyak sereh merupakan salah satu jenis minyak atsiri terpenting,
dalam jumlah besar dapat digunakan untuk menghasilkan sitral, yang merupakan komponen utama dari minyak tersebut. Minyak sereh tersebut berkadar sitral tinggi (75-85%) sehingga memiliki bau lemon yang kuat dan
dinamakanlemongrass(Guenther,1987).
Tumbuhan sereh merupakan jenis rumput-rumputan yang sudah sejak
2005). Secara empiris penggunaan sereh merah ini banyak digunakan untuk obat gosok, obat gatal-gatal (kudisan), dan untuk masuk angin.
Kebutuhan minyak atsiri meningkat terus seiring dengan kegunaan yang makin beragam dari minyak atsiri, hal ini merupakan upaya untuk menambah
produksi zat pewangi yang dapat dipakai oleh masyarakat (Gunawan dan Mulyani, 2010). Kebutuhan industri pada saat ini, bahan baku yang disediakan ada yang bersifat segar dan kering, dimana nantinya akan berpengaruh pada
hasil yang didapat dalam proses penyulingan (Nambiar dan Matela, 2013). Berdasarkan hal tersebut di atas, peneliti tertarik untuk melakukan
pemeriksaan yang meliputi karakterisasi simplisia, isolasi dengan metode destilasi air serta analisis komponen minyak atsiri secara gas chromatography-mass spectrometer (GC-MS) dari pelepah daun sereh merah segar dan kering
dengan alasan memanfaatkan pelepah daun sereh merah, dengan demikian pelepah daun sereh merah dapat dijadikan sebagai sumber minyak atsiri.
1.2 Perumusan Masalah
Berdasarkan uraian diatas maka perumusan masalah pada penelitian ini
adalah:
a. apakah karakterisasi tumbuhan sereh merah dapat ditentukan sesuai
dengan metode yang tertera pada Materia Medika Indonesia?
1.3 Hipotesis
Berdasarkan perumusan masalah diatas, maka hipotesis pada penelitian
ini adalah:
a. karakterisasi tumbuhan sereh merah dapat ditentukan sesuai dengan
metode yang tertera pada Materia Medika Indonesia (MMI).
b. terdapat perbedaan komponen dan kadar komponen minyak atsiri sereh merah kering dengan sereh merah segar.
1.4 Tujuan Penelitian
Tujuan penelitian ini adalah:
a. untuk mengkarakterisasi tumbuhan sereh merah sesuai dengan cara karakterisasi yang terdapat dalam Materia Medika Indonesia (MMI).
b. untuk mengetahui perbedaan komponen dan kadar komponen minyak atsiri yang diperoleh dari tumbuhan sereh merah segar dan kering yang
dianalisis secara GC-MS.
1.5 Manfaat Penelitian
Hasil penelitian ini diharapkan dapat memberikan informasi tentang karakterisasi simplisia, isolasi minyak atsiri dan analisis secara GC-MS dari
BAB II
TINJAUAN PUSTAKA
2.1 Uraian Tumbuhan
Tumbuhan sereh tumbuh liar di berbagai daerah tropis dan subtropis di benua Asia, Afrika, dan Amerika. Di Indonesia, tumbuhan ini dapat tumbuh hampir di seluruh wilayah nusantara (Susetyo dan Haryati, 2004).
Tanaman sereh yang menghasilkan minyak atsiri dalam perdagangan dikenal 2 jenis, yaitu minyak India Barat (cymbopogon citrates) dan minyak
India Timur (cymbopogon flexuosus) (Sonawane, et al., 2008). Cymbopogon adalah genus yang asli di daerah tropis dan semi tropis Asia dan dibudidayakan di Amerika Selatan, Amerika Tengah, dan Afrika (Shah, et al., 2011).
Cymbopogon merupakan tanaman yang sangat besar dengan keluarga yang terdiri dari 500 genus dan 8000 spesies herbal. Cymbopogon citratus dan
cymbopogon flexuosus mengandung minyak atsiri dimana kadar sitralnya tinggi (70-80%) (Negrelle dan Gomes, 2007). Tanaman ini pada pertumbuhannya membutuhkan cahaya matahari dan curah hujan yang cukup,
iklim tropis dan udara lembab. Rumpun ini tumbuh paling subur di atas tanah berpasir atau pasir bercampur kapur. Tanaman muda dapat dipanen untuk
pertama kalinya pada saat berumur empat sampai delapan bulan tergantung pada iklim dan kondisi tanah (Guenther, 1987).
2.1.2 Nama daerah
Nama daerah: Sereue (Aceh), Sere (Gayo, Jawa Tengah, Madura,
Bugis), Sangge-sangge (Batak Toba), Sarae Arun (Minangkabau), Sorae (Lampung), Sereh (Sunda), See (Melayu), Patahampori (Bima), Kedoung witu
(Sumba), Sare (Makasar), Garamakusu (Manado dan Ternate), Serai (Ambon) (Susetyo dan Haryati, 2004).
2.1.3 Nama asing
Nama asing: Lemongrass
2.1.4 Morfologi tumbuhan
Tumbuhan ini merupakan semak, tahunan dengan tinggi 50-100 cm. Batang tidak berkayu, beruas-ruas pendek dengan warna putih kotor. Daun tunggal, berpelepah dengan pangkal pelepah memeluk batang, ujung runcing,
tepi rata dengan panjang 25-75 cm, lebar 0,5-1,5 cm, pertulangan sejajar, warna hijau, akar serabut (Depkes, 2000).
2.1.5 Sistematika tumbuhan
Menurut Depkes (2000), sistematika tumbuhan sereh (Andropogon
citratusDC.) adalah sebagai berikut. Divisi : Spermatophyta Sub divisi : Angiospermae Kelas : Monocotyledoneae Bangsa : Poales
Suku : Gramineae
Marga :Andropogon
2.1.6 Penggunaan tumbuhan
Daun Andropogon citratus berkhasiat sebagai obat demam, obat
gatal-gatal, obat gosok, obat masuk angin (Depkes, 2000).
2.1.7 Kandungan kimia
Daun Andropogon citratus mengandung alkaloida, saponin, flavonoida, polifenol dan minyak atsiri (Depkes, 2000).
2.2 Minyak Atsiri
Minyak atsiri adalah zat beraroma yang terkandung dalam tanaman.
Minyak ini disebut minyak menguap, minyak eteris atau minyak esensial (essential oil, volatile oil) karena pada suhu kamar mudah menguap di udara terbuka, mempunyai rasa getir (pungent taste). Istilah essensial dipakai karena
minyak atsiri mewakili bau dari tanaman asalnya. Minyak ini umumnya larut dalam pelarut organik, tidak larut dalam air dan minyak atsiri dalam keadaan
segar dan murni umumnya tidak berwarna (Gunawan dan Mulyani, 2010).
2.2.1 Keberadaan minyak atsiri dalam tanaman
Minyak atsiri dalam tumbuhan terdapat dalam berbagai jaringan, seperti
didalam rambut kelenjar (pada suku Labiatae), di dalam sel-sel parenkim (pada suku Zingiberaceae dan Piperaceae), di dalam rongga-rongga skizogen dan
Minyak atsiri dalam tumbuhan berperan sebagai pengusir serangga pemakan daun dan sebaliknya minyak ini dapat juga berfungsi sebagai penarik
serangga guna membantu proses penyerbukan dan sebagai cadangan makanan (Gunawan dan Mulyani, 2010). Minyak atsiri terdapat pada bagian tanaman
seperti daun, bunga, biji, batang atau kulit dan akar atau rimpang (Agusta, 2000).
2.2.2. Komposisi kimia minyak atsiri
Minyak astiri umumnya terdiri dari unsur karbon (C), hidrogen (H) dan oksigen (O) dan kadang-kadang mengandung unsur nitrogen (N) dan belerang
(S). Variasi komposisi minyak atsiri disebabkan oleh perbedaan jenis tanaman penghasil, kondisi iklim, tanah tempat tumbuh, metode ekstaksi yang dipergunakan dan cara penyimpanan minyak (Gunawan dan Mulyani, 2010).
Pada umumnya komponen kimia minyak astiri dibagi menjadi dua golongan:
a. Golongan hidrokarbon
Persenyawaan yang termasuk hidrokarbon terbentuk dari unsur hidrogen (H) dan karbon (C). Jenis hidrokarbon yang terdapat dalam alam dan minyak
astiri sebagian besar terdiri dari monoterpen (2 unit isoprene), sesquiterpen (3 unit isoprene), diterpene (4 unit isoprene) dan politerpen (Gunawan dan
Mulyani, 2010).
b. Golongan hidrokarbon teroksigenasi
Persenyawaan yang termasuk hidrokarbon terdiri dari unsur hidrogen
golongan ini adalah persenyawaan alkohol, aldehida, keton, ester dan eter. Ikatan karbon yang terdapat dalam molekulnya dapat terdiri dari ikatan
tunggal, ikatan rangkap dua dan ikatan rangkap tiga. Terpen mengandung ikatan tunggal dan ikatan rangkap dua.
Secara kimia, terpena minyak atsiri dapat dipilih menjadi dua golongan, yaitu monoterpena (C10) dan seskuiterpena (C15) yang titik didihnya berbeda,
dimana titik didih monoterpena 140-180°C dan titik didih seskuiterpena
>200°C (Harborne, 1984).
2.3. Sifat Fisikokimia Minyak Astiri
Analisis fisikokimia dilakukan untuk mendeteksi pemalsuan, mengevaluasi mutu dan kemurnian minyak serta mengidentifikasi jenis dan
kegunaannya (Gunawan dan Mulyani, 2010).
2.3.1 Sifat fisik minyak atsiri
Menurut Koensoemardiyah (2010), minyak atsiri mempunyai konstituen kimia yang berbeda, tetapi dari segi fisikanya banyak yang sama. Minyak atsiri yang baru diekstraksi (masih segar) umumnya tidak berwarna
atau berwarna kekuning-kuningan. Sifat-sifat fisika minyak atsiri, yaitu: - analisis berat jenis
- mempunyai indeks bias yang tinggi - rotasi optik
a) Berat jenis
Penentuan bobot jenis menggunakan alat piknometer, Bobot jenis
minyak atsiri merupakan perbandingan antara bobot minyak dengan bobot air pada volume air yang sama dengan volume minyak. Bobot jenis merupakan
salah satu kriteria paling penting dalam menentukan mutu dan kemurnian minyak atsiri (Guenther, 1987).
b) Indeks bias
Penentuan indeks bias menggunakan alat refraktometer. Indeks bias merupakan perbandingan antara kecepatan cahaya di dalam udara dengan
kecepatan cahaya di dalam zat tersebut pada suhu tertentu. Indeks bias berguna untuk identifikasi kemurnian (Armando, 2009). Nilai indeks bias suatu jenis minyak dipengaruhi oleh suhu, yaitu pada suhu yang lebih tinggi indeks bias
semakin kecil (Ketaren, 1986).
c) Putaran optik
Penentuan putaran optik menggunakan alat polarimeter. Setiap jenis minyak atsiri mempunyai kemampuan memutar bidang polarisasi cahaya ke arah kanan atau kiri. Besarnya perputaran bidang polarisasi ditentukan oleh
jenis minyak atsiri, suhu, panjang kolom yang berisi minyak atsiri dan panjang gelombang cahaya yang digunakan (Guenther, 1987).
2.3.2 Cara isolasi minyak atsiri
1. Penyarian dengan lemak dingin (enfleurage)
Metode enfleurage disebut dengan penyarian secara “maserasi dingin
dengan lemak padat”. Suatu pelat kaca diberi bingkai kemudian ditutup dengan
lemak hewan yang telah dimurnikan sehingga tidak berbau, setelah itu,
mahkota bunga yang akan diambil minyak atsirinya ditebarkan di atasnya dengan sedikit ditekan. Bunga-bunga tersebut dalam keadaan segar atau baru dipetik, mahkota bunga itu dibiarkan di atas lempengan lemak tersebut selama
beberapa hari supaya minyak merembes dari bunga ke dalam lemak. Mahkota bunga yang ditekan di atas lempengan tersebut diambil dan diganti dengan
mahkota bunga yang baru. Hal ini dilakukan berulang kali sampai lempengan lemak jenuh oleh minyak atsiri, setelah itu lemak yang jenuh dengan minyak atsiri dicuci dengan alkohol, lalu alkohol tersebut diuapkan sehingga diperoleh
minyak atsiri yang diinginkan.
2. Penyarian dengan pelarut yang mudah menguap
Metode ini kurang umum dilakukan karena pelarut yang memenuhi syarat agak terlalu mahal untuk digunakan, yang dapat mengakibatkan harga minyak atsiri menjadi mahal. Cara ini dilakukan untuk memisahkan minyak
atsiri yang berharga mahal, misalnya minyak melati.
3. Penyarian dengan lemak panas
4. Penyulingan
Penyulingan dapat dibagi menjadi 3 bagian, antara lain:
a. Penyulingan air (water distillation)
Metode penyulingan air merupakan metode yang paling sederhana
diantara proses penyulingan lainnya. Metode ini lebih mirip dengan merebus, yaitu bahan yang akan disuling dimasukkan ke dalam ketel suling berisi air mendidih hingga terendam seluruhnya ke dalam air. Uap yang keluar dialirkan
melalui pipa menuju kondensor sehingga didapatkan air dan minyak, lalu dipisahkan minyak dengan air (Susetyo dan Haryati, 2004).
b. Penyulingan air dan uap (water and steam distillation)
Metode penyulingan ini disebut juga dengan sistem kukus. Prinsipnya, metode ini menggunakan uap bertekanan rendah, dibandingkan dengan
penyulingan air perbedaannya terletak pada pemisahan bahan dan air. Penempatan keduanya masih dalam satu ketel suling dimana air dimasukkan ke
dalam dasar ketel hingga 1/3 bagian ketel dan selanjutnya bahan dimasukkan kedalam ketel suling dan ketel ditutup rapat.
Saat air direbus dan mendidih, uap yang terbentuk akan melalui
sarangan lewat lubang-lubang kecil dan melewati celah-celah bahan. Minyak atsiri dalam bahan pun akan ikut bersama uap panas melalui pipa menuju
c. Penyulingan uap (steam distillation)
Metode penyulingan ini, air sebagai sumber uap panas terdapat dalam
“boiler’ yang letaknya terpisah dari ketel penyulingan. Uap yang dihasilkan
mempunyai tekanan lebih tinggi dari tekanan udara luar. Proses penyulingan
dengan uap ini baik jika digunakan untuk menyuling bahan baku minyak atsiri berupa kayu, kulit batang, maupun biji-bijian yang keras. Penyulingan dengan uap sebaiknya dimulai dengan tekanan uap yang rendah (kurang lebih 1 atm),
kemudian perlahan-lahan tekanan uap dinaikkan menjadi kurang lebih 3 atm (Armando, 2009).
2.4 Analisis Komponen Minyak Atsiri dengan GC-MS
Analisis komponen minyak atsiri merupakan masalah yang cukup rumit
karena minyak atsiri mengandung campuran senyawa dan sifatnya yang mudah menguap pada suhu kamar. Kendala dalam analisis komponen minyak atsiri
mulai dapat diatasi setelah ditemukannya kromatografi gas (GC). Efek penguapan dapat dihindari bahkan dapat dihilangkan sama sekali pada penggunaan GC. Perkembangan teknologi instrumentasi yang pesat akhirnya
dapat menghasilkan suatu alat yang merupakan dua sistem dengan prinsip dasar yang berbeda satu sama lain tetapi saling melengkapi, yaitu gabungan
2.4.1 Kromatografi gas
Kromatografi gas digunakan untuk memisahkan komponen campuran
kimia dalam suatu bahan berdasarkan perbedaan polaritas campuran. Fase gerak akan membawa campuran sampel menuju kolom. Campuran dalam fase
gerak akan berinteraksi dengan fase diam. Setiap komponen yang terdapat dalam campuran berinteraksi dengan kecepatan yang berbeda dimana interaksi komponen dengan fase diam dengan waktu yang paling cepat akan keluar
pertama dari kolom dan yang paling lambat akan keluar paling akhir (Eaton, 1989). Waktu yang menunjukkan berapa lama suatu senyawa dapat tertahan di
kolom disebut waktu tambat (waktu retensi) yang diukur mulai saat penyuntikan sampai saat elusi terjadi (Gritter, dkk., 1991).
Menurut Eaton (1989) hal yang mempengaruhi harga waktu retensi
yaitu:
1. Sifat senyawa, semakin sama tingkat kepolaran dengan kolom dan makin
kurang keatsiriannya maka akan tertahan lebih lama di kolom dan sebaliknya.
2. Sifat adsorben, semakin sama kepolaran dengan senyawa maka senyawa
akan semakin lama tertahan dan sebaliknya.
3. Konsentrasi adsorben, semakin banyak adsorben maka senyawa semakin
lama tertahan dan sebaliknya.
5. Aliran gas pembawa, semakin kecil aliran gas pembawa maka senyawa semakin lama tertahan dan sebaliknya.
6. Panjang kolom, semakin panjang kolom maka senyawa akan semakin lama tertahan dan sebaliknya.
Komponen kromatografi gas adalah gas pembawa, sistem injeksi, kolom, fase diam, suhu, detektor.
2.4.1.1 Gas pembawa
Gas pembawa harus memenuhi persyaratan antara lain: harus inert, murni dan mudah diperoleh, pemilihan gas pembawa tergantung pada detektor
yang dipakai. Gas pembawa yang sering dipakai adalah helium (He), argon (Ar), nitrogen (N2), hidrogen (H2)dan karbon dioksida (CO2)(Agusta, 2000).
Gas pembawa bervariasi untuk packed column dalam rentang antara 25 dan
150 ml/menit, sedangkan untuk kolom kapiler antara 1 dan 25 ml/menit (De Lux Putra, 2012).
2.4.1.2 Sistem injeksi
Cuplikan dimasukkan kedalam ruang suntik melalui gerbang suntik, biasanya berupa lubang yang ditutupi dengan septum atau pemisah karet.
Ruang suntik harus dipanaskan tersendiri, terpisah dari kolom dan biasanya pada suhu 10-15ºC lebih tinggi dari suhu kolom maksimum, jadi seluruh
cuplikan diuapkan segera setelah disuntikkan dan dibawa ke kolom (Gritter, dkk., 1991).
kemas terbuat dari gelas atau logam yang tahan karat atau dari tembaga dan aluminium. Panjang kolom kemas 1-5 m dengan diameter dalam 1-4 mm,
sedangkan kolom kapiler terbuat dari silika dengan kandungan logam <1ppm. Diameter dalam kolom kapiler 0,02-0,2 mm (Gandjar dan Rohman, 2008).
2.4.1.4 Fase diam
Cairan yang digunakan sebagai fase diam dalam kromatografi gas harus stabil terhadap panas dan kimia (De Lux Putra, 2012). Berdasarkan kepolaran
minyak atsiri yang nonpolar sampai sedikit polar, maka untuk keperluan analisis sebaiknya digunakan kolom fase diam yang bersifat sedikit polar,
misalnya SE-52 dan SE-54 (Agusta, 2000).
2.4.1.5 Suhu
Tekanan uap sangat tergantung pada suhu, maka suhu merupakan faktor
utama dalam GC. Pada GC-MS terdapat tiga pengendali suhu yang berbeda, yaitu: suhu injektor, suhu kolom dan suhu detektor (Agusta, 2000).
2.4.1.6 Detektor
Detektor yang populer yaitu detektor hantar-termal(thermalconductivity
detector) dan detektor pengion nyala (flameionization detector) (Mc Nair dan Bonelli, 1988).
2.5 Spektrometri Massa
Prinsip spektrometri massa (MS) ialah molekul senyawa organik (sampel) ditembak dengan berkas elektron dan menghasilkan ion bermuatan
molekul yang dapat pecah menjadi ion positif yang lebih kecil (ion fragmen). Spektrum massa merupakan grafik antara limpahan relatif lawan perbandingan
massa/muatan (m/z) (Sastrohamidjojo, 2004).
Keuntungan utama spektrometri massa sebagai metode analisis yaitu
metode ini lebih sensitif dan spesifik, untuk identifikasi senyawa yang tidak diketahui atau untuk menetapkan keberadaan senyawa tertentu, hal ini disebabkan adanya pola fragmentasi yang khas sehingga dapat memberikan
informasi mengenai bobot molekul dan rumus molekul. Puncak ion molekul penting dikenali karena memberikan bobot molekul senyawa yang diperiksa.
BAB III
METODE PENELITIAN
Metode penelitian ini dilakukan secara eksperimental yang meliputi
penyiapan sampel, karakterisasi simplisia, isolasi minyak atsiri dan analisis komponen minyak atsiri dari tumbuhan sereh merah (Andropogon citratus DC.) secara GC-MS.
3.1 Alat dan Bahan 3.1.1 Alat
Alat-alat yang digunakan dalam percobaan ini adalah alat-alat gelas laboratorium, neraca kasar (O’haus), neraca listrik (Mettler Toledo),
seperangkat alat Stahl, seperangkat alat destilasi air (water distillation), piknometer, oven, mikroskop, Gas Chromatography-Mass Spectrometer
(GC-MS) Shimadzu QP 2010 S,Refraktometer Abbedan lemari pengering.
3.1.2 Bahan
Bahan yang digunakan dalam percobaan ini adalah sereh merah segar
dan kering serta bahan-bahan kimia. Bahan kimia yang digunakan dalam penelitian antara lain akuades, etanol 96%, kloroform (E. Merck), natrium
3.2 Penyiapan Sampel
Penyiapan sampel meliputi pengambilan bahan, identifikasi bahan dan
pengolahan bahan menjadi sampel.
3.2.1 Pengambilan sampel
Metode pengambilan sampel dilakukan secara purposif, tanpa membandingkan tumbuhan yang sama dari daerah lain. Sampel diperoleh dari Desa Siraituruk Porsea, Provinsi Sumatera Utara.
3.2.2 Identifikasi tumbuhan
Identifikasi tumbuhan dilakukan di “Herbarium Bogoriense” bidang
botani Pusat Penelitian Biologi LIPI Bogor.
3.2.3 Pengolahan sampel
Pengolahan sampel dilakukan terhadap pelepah daun sereh merah,
pelepah daun dibersihkan dari kotoran yang melekat, lalu dicuci dengan air sampai bersih, ditiriskan lalu pelepah daun sereh merah dikupas dan dirajang
lalu ditimbang. Sebagian pelepah daun sereh merah digunakan untuk isolasi minyak atsiri sampel segar sedangkan sebagian lagi dikeringkan. Sampel dikeringkan di lemari pengering pada suhu tidak lebih dari 40ºC sampai
simplisia rapuh kemudian ditimbang.
3.3 Pemeriksaan Karakteristik Simplisia 3.3.1 Pemeriksaan makroskopik simplisia
3.3.2 Pemeriksaan mikroskopik
Pemeriksaan mikroskopik dilakukan terhadap serbuk simplisia sereh
merah. Serbuk simplisia ditaburkan diatas kaca objek yang telah ditetesi dengan larutan kloralhidrat jenuh dan ditutup dengan kaca penutup, kemudian
diamati dibawah mikroskop.
Pemeriksaan mikroskopik dilakukan terhadap sereh merah segar. Sampel diiris tipis melintang lalu diletakkan diatas kaca objek kemudian
ditetesi dengan larutan fluorogusinol HCL dan ditutup dengan kaca penutup, kemudian diamati dibawah mikroskop.
3.3.3 Penetapan kadar air
Penetapan kadar air dilakukan dengan cara sebagai berikut:
A. Penjenuhan toluen
Sebanyak 200 ml toluen dimasukkan ke dalam labu alas bulat, lalu ditambahkan 2 ml air suling kemudian alat dipasang, dan didestilasi selama 2
jam. Destilasi dihentikan dan dibiarkan dingin selama ± 30 menit, kemudian volume air dalam tabung penerima dibaca dengan ketelitian 0,05 ml.
B. Penetapan kadar air simplisia
Labu berisi toluen tersebut dimasukkan 5 g serbuk simplisia yang telah ditimbang seksama, labu dipanaskan hati-hati selama 15 menit. Setelah toluen
mendidih, kecepatan toluen diatur 2 tetes per detik sampai sebagian besar air terdestilasi, kemudian kecepatan destilasi dinaikkan sampai 4 tetes per detik. Setelah semua air terdestilasi, bagian dalam pendingin dibilas dengan toluen.
pada suhu kamar. Setelah air dan toluen memisah sempurna, volume air dibaca dengan ketelitian 0,05 ml. Selisih kedua volume air yang dibaca sesuai dengan
kadar air yang terdapat dalam bahan yang diperiksa. Kadar air dihitung dalam persen (WHO, 1998).
3.3.4 Penetapan kadar sari larut air
Sebanyak 5 g serbuk simplisia yang telah dikeringkan, dimaserasi selama 24 jam dalam 100 ml air-kloroform (2,5 ml kloroform dalam air suling
sampai 1 liter) dalam labu bersumbat sambil dikocok sesekali selama 6 jam pertama, kemudian dibiarkan selama 18 jam, kemudian disaring. Sejumlah 20
ml filtrat pertama diuapkan sampai kering dalam cawan penguap yang berdasar rata yang telah dipanaskan dan ditara. Sisa dipanaskan pada suhu 105oC, kadar dalam persen sari yang larut dalam air dihitung terhadap bahan yang telah
dikeringkan (Depkes RI, 2008).
3.3.5 Penetapan kadar sari larut etanol
Sebanyak 5 g serbuk simplisia yang telah dikeringkan di udara, dimaserasi selama 24 jam dalam 100 ml etanol 95% dalam labu bersumbat sambil dikocok sesekali selama 6 jam pertama, kemudian dibiarkan selama 18
jam. Disaring cepat untuk menghindari penguapan etanol. Sejumlah 20 ml filtrat diuapkan sampai kering dalam cawan penguap yang berdasar rata yang
3.3.6 Penetapan kadar abu total
Sebanyak 2 g serbuk yang telah digerus dan ditimbang seksama
dimasukkan ke dalam krus porselin yang telah dipijar dan ditara, kemudian diratakan. Krus porselin dipijar perlahan–lahan sampai arang habis, pemijaran
dilakukan pada suhu 500-600oC selama 3 jam kemudian didinginkan dan ditimbang sampai diperoleh bobot tetap. Kadar abu dihitung terhadap bahan yang telah dikeringkan (Depkes RI, 1980).
3.3.7 Penetapan kadar abu tidak larut dalam asam
Abu yang telah diperoleh dalam penetapan kadar abu, dididihkan dalam
25 ml asam klorida encer selama 5 menit, bagian yang tidak larut asam dikumpulkan, disaring melalui kertas saring dan dipijar sampai bobot tetap, kemudian didinginkan dan ditimbang. Kadar abu yang tidak larut dalam asam
dihitung terhadap bahan yang dikeringkan (Depkes RI, 1980).
3.3.8 Penetapan kadar minyak atsiri
Penetapan kadar minyak atsiri dilakukan dengan menggunakan alat
Stahl. Caranya : sebanyak 15 g pelepah daun sereh merah yang telah dirajang dimasukkan dalam labu alas bulat berleher pendek, ditambahkan air suling
sebanyak 300ml, labu diletakkan di atas pemanas listrik. Hubungkan labu dengan pendingin dan alat penampung berskala, buret diisi air sampai penuh,
3.4 Isolasi Minyak Atsiri
Isolasi minyak atsiri dilakukan dengan metode penyulingan air (water
distillation).
Caranya : sebanyak 100 g rajangan simplisia dimasukkan kedalam labu alas
bulat berleher panjang 2 L ditambahkan air suling sampai sampel terendam. Kemudian dirangkai alat destilasi air. Destilasi dilakukan selama 4-5 jam. Minyak atsiri yang diperoleh ditampung dalam corong pisah, setelah itu
dipisahkan antara minyak dan air. Kemudian minyak atsiri yang diperoleh ditambahkan natrium sulfat anhidrat, dikocok dan didiamkan selama 1 hari.
Minyak atsiri dipipet dan disimpan dalam botol berwarna gelap. Minyak yang diperoleh kemudian dianalisis dengan GC-MS.
3.5 Identifikasi Minyak Atsiri 3.5.1 Penentuan indeks bias
Penentuan indeks bias dilakukan dengan menggunakan alat
Refraktometer Abbe.
Caranya : alat Refraktometer Abbe dihidupkan. Prisma atas dan prisma bawah
dipisahkan dengan membuka klem dan dibersihkan dengan mengoleskan kapas yang telah dibasahi dengan alkohol. Cuplikan minyak diteteskan ke prisma
3.5.2 Penentuan bobot jenis
Penentuan bobot jenis ditentukan dengan alat piknometer.
Caranya : piknometer kosong ditimbang dengan seksama. Piknometer kosong diisi dengan air suling lalu ditimbang dengan seksama. Piknometer
dikosongkan dan dibilas beberapa kali dengan alkohol kemudian dikeringkan dengan bantuan hair dryer. Piknometer diisi minyak selanjutnya dilakukan seperti pengerjaan pada air suling. Hasil bobot minyak atsiri yang diperoleh
dengan mengurangkan bobot piknometer yang diisi minyak atsiri dengan bobot piknometer kosong. Bobot jenis minyak atsiri adalah hasil yang diperoleh
dengan membagi bobot minyak atsiri dengan bobot air suling dalam piknometer, kecuali dinyatakan lain dalam monografi keduanya ditetapkan pada suhu 25oC (Depkes RI, 1995).
3.5.3 Analisis komponen minyak atsiri
Penentuan komponen minyak atsiri dilakukan di Laboratorium
Penelitian Fakultas Farmasi USU dengan menggunakan seperangkat alat Gas
Chromatography-Mass Spectrometer(GC-MS).
Kondisi analisis GC adalah jenis kolom dalam kapiler Rtx-1 MS,
panjang kolom 30 m, diameter kolom dalam 0,25 mm, suhu injektor 270oC, gas pembawa He dengan laju alir 0,5 ml/menit. Suhu kolom terprogram
Cara identifikasi komponen minyak atsiri adalah dengan membandingkan spektrum massa dari komponen minyak atsiri yang diperoleh
BAB IV
HASIL DAN PEMBAHASAN
4.1 Identifikasi Tumbuhan
Hasil identifikasi tumbuhan yang dilakukandi “Herbarium Bogoriense” Pusat Penelitian Biologi-LIPI Bogor terhadap sereh merah yang diteliti adalah jenis Andropogon citratus DC. dari suku Poaceae. Data selengkapnya dapat
dilihat pada Lampiran 1, halaman 51.
4.2 Hasil Pemeriksaan Makroskopik dan Mikroskopik Batang Sereh Merah (Andropogon citratusDC.)
4.2.1 Hasil pemeriksaan makroskopik
Pemeriksaan makroskopik sereh merah (Andropogon citratus DC.) menunjukkan daun berbentuk lanset, tunggal, berpelepah, pangkal pelepah
memeluk batang, kasar, ujung runcing, tepi rata, panjang 25-27 cm, lebar 0,5-1,5 cm, pertulangan sejajar (Depkes RI, 2000).
4.2.2 Hasil pemeriksaan mikroskopik
Hasil pemeriksaan mikroskopik serbuk simplisia sereh merah tampak stomata pada epidermis tipe halter, sel-sel parenkim ada yang berisi tetes-tetes
minyak. Gambar selengkapnya dapat dilihat pada Lampiran 4, halaman 54.
4.2.3 Hasil pemeriksaan karakterisasi simplisia
daun sereh merah selengkapnya dapat dilihat pada Lampiran 6-10, halaman 59-63.
Tabel 4.1Hasil karakterisasi simplisia sereh merah
No Pemeriksaan Karakteristik Simplisia Kadar Penelitian (%)
1. Kadar air 5,98
2. Kadar sari yang larut dalam air 10,74 3. Kadar sari yang larut dalam etanol 9,81
4. Kadar abu total 4,27
5. Kadar abu yang tidak larut dalam asam 0,39
Berdasarkan hasil penelitian terhadap karakterisasi simplisia pelepah daun sereh merah telah memenuhi persyaratan MMI (Depkes RI, 1989).
Pengeringan simplisia dilakukan untuk mendapatkan simplisia yang tidak mudah rusak sehingga dapat disimpan dalam waktu yang lebih lama.
Penurunan mutu atau perusakan simplisia dapat dicegah dengan mengurangi kadar air dan penghentian reaksi enzimatik. Reaksi enzimatik tidak berlangsung lagi bila kadar air dalam simplisia kurang dari 10% (BPOM RI,
2005).
Hasil penelitian diperoleh kadar air simplisia pelepah daun sereh merah
adalah 5,98%. Kadar air simplisia berhubungan dengan proses pengeringan simplisia. Pengeringan merupakan suatu usaha untuk menurunkan kadar air bahan sampai tingkat yang diinginkan. Kadar air yang cukup aman, maka
simplisia tidak mudah rusak dan dapat disimpan dalam jangka waktu yang cukup lama. Apabila simplisia yang dihasilkan tidak cukup kering maka
Simplisia dinilai cukup aman bila mempunyai kadar air kurang dari 10% (Depkes RI, 1980).
Penetapan kadar sari dilakukan terhadap 2 pengujian yaitu kadar sari larut dalam etanol dan air. Penetapan kadar sari simplisia menyatakan jumlah
zat yang tersari dalam air dan dalam etanol. Simplisia pelepah daun sereh merah kadar sari yang larut dalam air diperoleh lebih besar 10,74% dari kadar sari yang larut dalam etanol 9,81%. Penetapan kadar sari yang larut dalam air
dan dalam etanol dilakukan untuk mengetahui jumlah senyawa yang dapat tersari dalam air dan etanol dari suatu simplisia. Senyawa yang bersifat polar
dan larut dalam air akan tersari oleh air sedangkan senyawa-senyawa yang tidak larut dalam air dan larut dalam etanol akan tersari oleh etanol.
Penetapan kadar abu dimaksudkan untuk mengetahui kandungan
mineral internal yang terdapat didalam simplisia yang diteliti serta senyawa organik yang tersisa selama pembakaran. Abu total terbagi dua, yang pertama
abu fisiologis adalah abu yang berasal dari jaringan tumbuhan itu sendiri dan abu non fisiologis adalah sisa setelah pembakaran yang berasal dari bahan-bahan dari luar yang terdapat pada permukaan simplisia. Kadar abu tidak larut
asam untuk menentukan jumlah silika, khususnya pasir yang ada pada simplisia dengan cara melarutkan abu total dalam asam klorida (Depkes RI,
4.3 Identifikasi Minyak Atisiri
Hasil data identifikasi minyak atsiri yang diperoleh dapat dilihat pada
Tabel 4.2 di bawah ini.
Tabel 4.2Hasil penetapan kadar minyak atsiri
No Sampel Kadar minyak atsiri (% v/b)
Hasil penelitian Hasil berdasarkan literature 1.
2.
Segar Kering
0,42 0,62
0,8-1,2 0,8-1,2
Penetapan kadar minyak atsiri dengan menggunakan alat Stahl diketahui bahwa minyak atsiri sereh merah kering 0,62% v/b sementara pada
sereh merah yang segar 0,42% v/b dari hasil ini diketahui bahwa minyak atsiri lebih banyak terdapat pada sereh merah kering.
4.4 Penentuan Indeks Bias dan Bobot Jenis Minyak Atsiri Hasil Isolasi Hasil penentuan indeks bias dan bobot jenis minyak atsiri dapat dilihat
pada Tabel 4.3 di bawah ini.
Tabel 4.3 Hasil penentuan indeks bias dan bobot jenis minyak atsiri hasil isolasi
No. Sampel Indeks Bias Bobot Jenis
1 Sereh merah kering 1,456 0,8544
2 Sereh merah segar 1,456 0,8549
kering yang tidak signifikan tidak menghasilkan perbedaan nilai indeks bias. Nilai indeks bias sampel memenuhi syarat dalam literatur, indeks bias berguna
untuk identifikasi suatu zat dan deteksi ketidakmurnian. Nilai indeks bias sekitar 1,56-1,75 dengan menggunakan alat refraktometer (Susetyo dan
Haryati, 2004).
Indeks bias merupakan perbandingan antara kecepatan cahaya di dalam udara dengan kecepatan cahaya di dalam zat tersebut pada suhu tertentu.
Indeks bias berguna untuk identifikasi kemurnian dan indeks bias minyak atsiri juga berhubungan erat dengan komponen-komponen yang tersusun dalam
minyak atsiri yang dihasilkan (Armando, 2009). Semakin panjang rantai karbon dan semakin banyak ikatan rangkap, indeks bias bertambah besar. Nilai indeks bias suatu jenis minyak dipengaruhi oleh suhu, yaitu pada suhu yang
lebih tinggi indeks bias semakin kecil (Ketaren, 1986).
Bobot jenis minyak atsiri merupakan perbandingan antara bobot
minyak dengan bobot air pada volume air yang sama dengan volume minyak. Bobot jenis merupakan salah satu kriteria paling penting dalam menentukan mutu dan kemurnian minyak atsiri. Nilai bobot jenis minyak atsiri sereh antara
0,850-0,892 pada suhu 25°C (Susetyo dan Haryati, 2004).
Hasil penelitian ini didapatkan bahwa perbedaan metode penyulingan
Peak R.Time Area% Nama Komponen
1 2.443 13.29 Pentane, 3-methyl-(CAS) 3-Methylpentane 2 2.473 5.31 Hexane (CAS) n-Hexane
3 2.668 0.88 Cyclopentane, methyl-$$Methylcyclopentane $$ 4 2.810 0.81 Cyclohexane
5 9.270 1.27 1-Limonene $$ Cyclohexene, 1-methyl-4-(1-methylethenyl) 6 11.113 0.50 LINALOOL
7 12.617 11.56 CITRONELLA $$ 6-Octenal, 3,7-dimethyl-(CAS) Citronellal$$ 8 12.888 0.45 Cyclohexanol, 5-methyl-2-(1-methylethenyl)
9 14.940 7.64 beta-Citronellol $$ 6-octenol, 3,7-dimethyl- (CAS) Citronnel 10 15.629 2.80 GERANIOL $$
11 15.862 0.61 E-Citral $$ 2,6-Octadienal, 3,7-dimethyl- (E)- (CAS) Geranial $ 12 18.315 0.44 Eugenol
13 18.521 4.15 Citronellyl acetate $$ 6-Octen-1-ol, 3,7-dimethyl-, acetate (CAS) 14 19.247 4.16 Neryl acetate $$ 6-Octen-1-o1, 3,7-dimethyl-, acetate, (CAS) 15 20.016 2.75 BETA ELEMENE $$
16 22.365 3.34 GERMACRENE $$
17 22.804 0.90 alpha-Muurolene$$Naphthalene, 1,2,4a,5,6,8a-hexahydro 18 23.154 0.91 BICYCLO, 2-methylen-4,8,8-trimethyl
19 23.362 3.82 Delta-Cadinene$$Naphthalene, 1,2,3,5,6,8a-hexahydro 20 23.895 10.76 Elemol$$ Cyclohexanemethanol, 4-ethenyl-alpha
21 24.614 1.35 Naphthalene, 1,2,3,4,4a,5,6,8a-octahydro-7-methyl-4-methylene 22 25.390 1.25 FARNESOL $$
23 25.683 0.97 1h-Cyclopropa(A)Naphthalene, decahydro
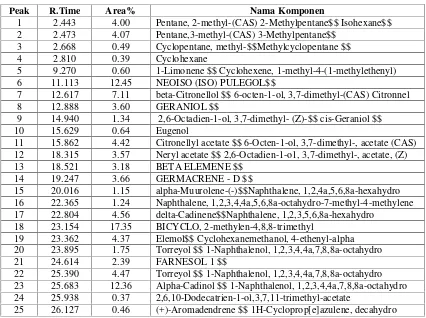
Berdasarkan hasil kromatogram minyak atsiri sereh merah kering diperoleh 25 komponen dengan data pada tabel 4.5 di bawah ini.
Tabel 4.5 Komponen sereh merah kering
Peak R.Time Area% Nama Komponen
1 2.443 4.00 Pentane, 2-methyl-(CAS) 2-Methylpentane$$ Isohexane$$ 2 2.473 4.07 Pentane,3-methyl-(CAS) 3-Methylpentane$$
3 2.668 0.49 Cyclopentane, methyl-$$Methylcyclopentane $$ 4 2.810 0.39 Cyclohexane
5 9.270 0.60 1-Limonene $$ Cyclohexene, 1-methyl-4-(1-methylethenyl) 6 11.113 12.45 NEOISO (ISO) PULEGOL$$
7 12.617 7.11 beta-Citronellol $$ 6-octen-1-ol, 3,7-dimethyl-(CAS) Citronnel 8 12.888 3.60 GERANIOL $$
9 14.940 1.34 2,6-Octadien-1-ol, 3,7-dimethyl- (Z)-$$ cis-Geraniol $$ 10 15.629 0.64 Eugenol
11 15.862 4.42 Citronellyl acetate $$ 6-Octen-1-ol, 3,7-dimethyl-, acetate (CAS) 12 18.315 3.57 Neryl acetate $$ 2,6-Octadien-1-o1, 3,7-dimethyl-, acetate, (Z) 13 18.521 3.18 BETA ELEMENE $$
14 19.247 3.66 GERMACRENE - D $$
15 20.016 1.15 alpha-Muurolene-(-)$$Naphthalene, 1,2,4a,5,6,8a-hexahydro 16 22.365 1.24 Naphthalene, 1,2,3,4,4a,5,6,8a-octahydro-7-methyl-4-methylene 17 22.804 4.56 delta-Cadinene$$Naphthalene, 1,2,3,5,6,8a-hexahydro
18 23.154 17.35 BICYCLO, 2-methylen-4,8,8-trimethyl
19 23.362 4.37 Elemol$$ Cyclohexanemethanol, 4-ethenyl-alpha 20 23.895 1.75 Torreyol $$ 1-Naphthalenol, 1,2,3,4,4a,7,8,8a-octahydro 21 24.614 2.39 FARNESOL 1 $$
22 25.390 4.47 Torreyol $$ 1-Naphthalenol, 1,2,3,4,4a,7,8,8a-octahydro 23 25.683 12.36 Alpha-Cadinol $$ 1-Naphthalenol, 1,2,3,4,4a,7,8,8a-octahydro 24 25.938 0.37 2,6,10-Dodecatrien-1-ol,3,7,11-trimethyl-acetate
25 26.127 0.46 (+)-Aromadendrene $$ 1H-Cycloprop[e]azulene, decahydro
Berdasarkan hasil yang diperoleh dari sereh merah segar dan kering diperoleh komponen utama yang sebagian besar sama, akan tetapi dengan
kadar yang berbeda-beda. Hal ini dapat disebabkan karena adanya proses pengeringan pada sereh merah kering dapat mempengaruhi kadar minyak atsiri yang terdapat didalamnya jika dibandingkan dengan sereh merah segar yang
Waktu tambat dan kadar keenam komponen minyak atsiri dari sereh merah segar hasil analisis GC dapat dilihat pada Tabel 4.6 di bawah ini.
Tabel 4.6 Waktu tambat dan kadar komponen minyak atsiri hasil analisis GC sereh merah segar
No. Nama Komponen Waktu tambat (menit)
1. Sitronella 12,617 C10H18O 154 11,56
2. β-sitronellol 14,942 C10H20O 156 7,64
3. Geraniol 15,633 C10H18O 154 2,80
4. Eugenol 18,317 C10H12O2 164 0,44
5. Sitronellyl acetate 18,517 C12H22O2 198 4,15
6. Elemol 23,892 C15H26O 222 10,76
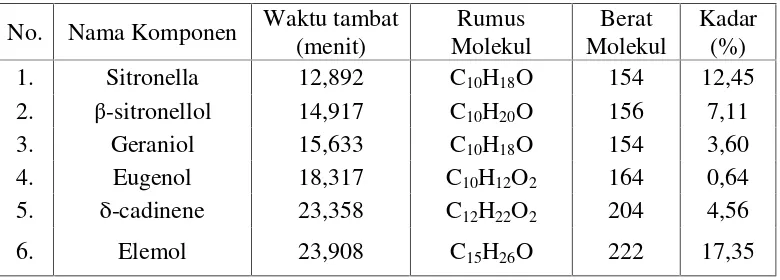
Waktu tambat dan kadar keenam komponen minyak atsiri dari sereh merah kering hasil analisis GC dapat dilihat pada Tabel 4.7 di bawah ini.
Tabel 4.7 Waktu tambat dan kadar komponen minyak atsiri hasil analisis GC dari sereh merah kering
No. Nama Komponen Waktu tambat (menit)
1. Sitronella 12,892 C10H18O 154 12,45
2. β-sitronellol 14,917 C10H20O 156 7,11
3. Geraniol 15,633 C10H18O 154 3,60
4. Eugenol 18,317 C10H12O2 164 0,64
5. δ-cadinene 23,358 C12H22O2 204 4,56
6. Elemol 23,908 C15H26O 222 17,35
Menurut literatur, komponen utama minyak atsiri dari sereh adalah sitronella, sitronelol, dan geraniol. Sedangkan komponen lainnya terdapat
4.5.1 Fragmentasi dan analisis hasil spektrofotometri massa minyak atsiri sereh merah segar
Fragmentasi hasil spektrofotometri massa komponen minyak atsiri sereh merah segar dengan metode destilasi air adalah sebagai berikut:
1. Puncak dengan waktu tambat 12,617 menit mempunyai M+ 154 diikuti fragmen m/z 139, 121, 95, 69, 55, 41. Gambar spektrum massa dapat dilihat
pada lampiran 14, halaman 70.
2. Puncak dengan waktu tambat 14,942 menit mempunyai M+ 156 diikuti fragmen m/z 138, 123, 109, 95, 81, 55, 41. Gambar spektrum masa dapat
dilihat pada Lampiran 15, halaman 70.
3. Puncak dengan waktu tambat 15,633 menit mempunyai M+ 154 diikuti
fragmen m/z 136, 121, 93, 55, 41. Gambar spektrum massa dapat dilihat pada Lampiran 16, halaman 71.
4. Puncak dengan waktu tambat 18,317 menit mempunyai M+ 164 diikuti
fragmen m/z 149, 131, 103, 77, 51. Gambar spektrum massa dapat dilihat pada Lampiran 17, halaman 71.
5. Puncak dengan waktu tambat 18,517 menit mempunyai M+ 198 diikuti fragmen m/z 138, 123, 109, 95, 81, 41. Gambar spektrum massa dapat dilihat pada Lampiran 18, halaman 72.
6. Puncak dengan waktu tambat 23,892 menit mempunyai M+ 222 diikuti fragmen m/z 204, 189, 161, 135, 121, 107, 93, 41. Gambar spektrum massa
dapat dilihat pada Lampiran 19, halaman 72.
1. Spektrum massa puncak dengan waktu tambat 12,617 menit
Dengan membandingkan spektrum massaunknown dengan datalibrary
yang memiliki tingkat similarity index tertinggi (97%) maka senyawa tersebut adalah Sitronella (C10H18O) dengan rumus bangun seperti Gambar 4.3 berikut
ini.
Gambar 4.3Rumus bangun dari senyawa Sitronella
Spektrum massa unknown memberikan puncak ion molekul M+ 154
yang merupakan berat molekul dari C10H18O. Pelepasan CH3 menghasilkan
fragmen [C9H15O]+ dengan m/z 139 dari puncak molekul C10H18O. Pelepasan
H2O menghasilkan fragmen [C9H13] dengan m/z 121. Pelepasan C2H2
menghasilkan fragmen [C7H11]+ dengan m/z 95. Pelepasan C2H2menghasilkan
fragmen [C5H9]+ dengan m/z 69. Pelepasan CH2 menghasilkan fragmen
[C4H7]+dengan m/z 55. Pelepasan CH2menghasilkan fragmen [C3H5]+dengan
m/z 41.
2. Spektrum massa puncak dengan waktu tambat 14,942 menit
Dengan membandingkan spektrum massa unknowndengan datalibrary yang memiliki tingkat similarity idex tertinggi (97%) maka senyawa tersebut
dapat disimpulkan sebagai β-sitronellol (C10H20O) dengan rumus bangun
seperti Gambar 4.4 berikut ini.
Spektrum massa unknown memberikan puncak ion molekul M+ 156 yang merupakan berat molekul dari C10H20O. Pelepasan H2O menghasilkan
fragmen [C10H18] dengan m/z 138 dari puncak molekul C10H20O. Pelepasan
CH3 menghasilkan fragmen [C9H15]+ dengan m/z 123. Pelepasan CH2
menghasilkan fragmen [C8H13]+dengan m/z 109. Pelepasan CH2menghasilkan
fragmen [C7H11]+ dengan m/z 95. Pelepasan CH2 menghasilkan fragmen
[C6H9]+ dengan m/z 81. Pelepasan C2H2 menghasilkan fragmen [C4H7]+
dengan m/z 55. Pelepasan CH2menghasilkan fragmen [C3H5]+dengan m/z 41.
3. Spektrum massa puncak dengan waktu tambat 15,633 menit
Dengan membandingkan spektrum massa unknown dengan datalibrary yang memiliki tingkat similarity indextertinggi (94%), maka senyawa tersebut dapat disimpulkan sebagai Geraniol (C10H18O) dengan rumus bangun seperti
pada Gambar 4.5 berikut ini.
Gambar 4.5Rumus bangun dari senyawa Geraniol
Spektrum massa unknown memberikan puncak ion molekul M+ 154 yang merupakan berat molekul dari C10H18O. Pelepasan H2O menghasilkan
fragmen [C10H16] dengan m/z 136 dari puncak molekul C10H18O. Pelepasan
CH3 menghasilkan fragmen [C9H13]+ dengan m/z 121. Pelepasan C2H4
menghasilkan fragmen [C7H9]+ dengan m/z 93. Pelepasan C3H2 menghasilkan
fragmen [C4H7]+ dengan m/z 55. Pelepasan CH2 menghasilkan fragmen
4. Spektrum massa puncak dengan waktu tambat 18,317 menit
Dengan membandingkan spektrum massa unknowndengan datalibrary
yang memiliki tingkat similarity index tertinggi (93%) maka senyawa ini disimpulkan sebagai Eugenol (C10H12O2) dengan rumus bangun seperti
Gambar 4.6 berikut ini.
Gambar 4.6Rumus bangun dari senyawa Eugenol
Spektrum massa unknown memberikan puncak ion molekul M+ 164
yang merupakan berat dari C10H12O2. Pelepasan CH3 menghasilkan fragmen
[C9H9O2]+ dengan m/z 149 dari puncak molekul C10H12O2. Pelepasan H2O
menghasilkan fragmen [C9H7O] dengan m/z 131. Pelepasan CO menghasilkan
fragmen [C8H7]+ dengan m/z 103. Pelepasan C2H2 menghasilkan fragmen
[C6H5]+ dengan m/z 77. Pelepasan C2H2 menghasilkan fragmen [C4H3]+
dengan m/z 51.
5. Spektrum massa puncak dengan waktu tambat 18,517 menit
Dengan membandingkan spektrum massa unknowndengan datalibrary
yang memiliki tingkatsimiliarity indextertinggi (95%) maka senyawa tersebut dapat disimpulkan sebagai Sitronellyl acetate (C12H22O2) dengan rumus bangun
seperti Gambar 4.7 berikut ini.
Spektrum massa unknown memberikan puncak ion molekul M+ 198 yang merupakan berat dari C12H22O2. Pelepasan C2H4O2 menghasilkan
fragmen [C10H18]+ dari puncak molekul C12H22O2. Pelepasan CH3
menghasilkan fragmen [C9H15]+dengan m/z 123. Pelepasan CH2menghasilkan
fragmen [C8H13]+ dengan m/z 109. Pelepasan CH2 menghasilkan fragmen
[C7H11]+ dengan m/z 95. Pelepasan CH2 menghasilkan fragmen [C6H9]+
dengan m/z 81. Pelepasan C3H4menghasilkan fragmen [C3H5]+dengan m/z 41.
6. Spektrum massa puncak dengan waktu tambat 23,892 menit
Dengan membandingkan spektrum massa unknowndengan datalibrary
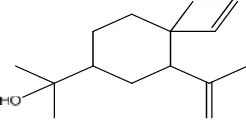
yang memiliki tingkatsimiliarity indextertinggi (91%) maka senyawa tersebut dapat disimpulkan sebagai Elemol (C15H26O) dengan rumus bangun seperti
Gambar 4.8 berikut ini.
Gambar 4.8Rumus bangun dari senyawa Elemol
Spektrum massa unknown memberikan puncak ion molekul M+ 204 yang merupakan berat dari C15H26O. Pelepasan CH3 menghasilkan fragmen
[C14H23O] dengan m/z 189 dari puncak molekul [C15H26O]. Pelepasan H2O
menghasilkan fragmen [C14H21] dengan m/z 161. Pelepasan C2H2
menghasilkan fragmen [C12H19]+ dengan m/z 135. Pelepasan CH2
menghasilkan fragmen [C11H17]+ dengan m/z 121. Pelepasan CH2
fragmen [C5H9]+ dengan m/z 41. Pelepasan CH2 menghasilkan fragmen
[C4H7]+dengan m/z 27.
4.5.2 Fragmentasi dan analisis hasil spektrofotometri massa minyak atsiri sereh merah kering
Fragmentasi hasil spektrofotometri massa komponen minyak atsiri sereh merah kering sebagai berikut:
1. Spektrum massa puncak dengan waktu tambat 12,892 menit mempunyai M+ 154 diikuti fragmen m/z 136, 121, 95, 81, 55, 41. Gambar spektrum massa dapat dilihat pada Lampiran 21, halaman 74.
2. Spektrum massa puncak dengan waktu tambat 14,917 menit mempunyai M+ 156 diikuti fragmen m/z 138, 123, 109, 95, 81, 55, 41. Gambar spektrum
massa dapat dilihat pada Lampiran 22, halaman 74.
3. Spektrum massa puncak dengan waktu tambat 15,633 menit mempunyai M+ 154 diikuti fragmen m/z 136, 121, 93, 53, 41. Gambar spektrum massa
dapat dilihat pada Lampiran 23, halaman 75.
4. Spektrum massa puncak dengan waktu tambat 18,317 menit mempunyai M+
164 diikuti fragmen m/z 149, 131, 65, 51. Gambar spektrum massa dapat dilihat pada Lampiran 24, halaman 75.
5. Spektrum massa puncak dengan waktu tambat 23,358 menit mempunyai M+
204 diikuti fragmen m/z 189, 161, 119, 105, 91, 41. Gambar spektrum massa dapat dilihat pada lampiran 25, halaman 76.
Analisis hasil spektofotometri massa komponen minyak atsiri sereh merah kering adalah sebagai berikut:
1. Puncak dengan waktu tambat 12,892 menit
Dengan membandingkan spektrum massaunknown dengan datalibrary
yang memiliki tingkat similarity index tertinggi (91%) maka senyawa tersebut dapat disimpulkan sebagai Sitronella (C10H18O) dengan rumus bangun seperti
Gambar 4.9 di bawah ini.
Gambar 4.9 Rumus bangun dari senyawa Sitronella
Spektrum massa unknown memberikan puncak ion molekul M+ 154 yang merupakan berat molekul dari C10H18O. Pelepasan H2O menghasilkan
fragmen [C10H16] dengan m/z 136 dari puncak molekul C10H18O. Pelepasan
CH3 menghasilkan fragmen [C9H13]+ dengan m/z 121. Pelepasan C2H2
menghasilkan fragmen [C7H11]+ dengan m/z 95. Pelepasan CH2menghasilkan
fragmen [C6H9]+ dengan m/z 81. Pelepasan C2H2 menghasilkan fragmen
[C4H7]+dengan m/z 55. Pelepasan CH2menghasilkan fragmen [C3H5]+dengan
m/z 41.
2. Puncak dengan waktu tambat 14,917 menit
Dengan membandingkan spektrum massa unknowndengan datalibrary yang memiliki tingkat similarity idex tertinggi (97%) maka senyawa tersebut dapat disimpulkan sebagai β-sitronellol (C10H20O) dengan rumus bangun