PENYERAPAN LOGAM ZINKUM (Zn) DALAM AIR LIMBAH
PABRIK BENANG KARET MENGGUNAKAN BATUBARA
YANG DIAKTIFASI DAN ANALISISNYA DENGAN
METODE SPEKTROFOTOMETRI
SERAPAN ATOM
TESIS
Oleh
SUSILAWATI 117006009/KIM
FAKULTAS MATEMATIKA DAN ILMU PENGETAHUAN ALAM
UNIVERSITAS SUMATERA UTARA
PENYERAPAN LOGAM ZINKUM (Zn) DALAM AIR LIMBAH
PABRIK BENANG KARET MENGGUNAKAN BATUBARA
YANG DIAKTIFASI DAN ANALISISNYA DENGAN
METODE SPEKTROFOTOMETRI
SERAPAN ATOM
TESIS
Diajukan sebagai salah satu syarat untuk memperoleh gelar Magister Sains Dalam Program Studi Ilmu Kimia pada Fakultas Matematika dan Ilmu Pengetahuan Alam
Universitas Sumatera Utara
Oleh
SUSILAWATI 117006009/KIM
FAKULTAS MATEMATIKA DAN ILMU PENGETAHUAN ALAM
UNIVERSITAS SUMATERA UTARA
Judul Tesis : PENYERAPAN LOGAM ZINKUM (Zn) DALAM AIR LIMBAH PABRIK BENANG KARET
MENGGUNAKAN BATUBARA YANG DIAKTIFASI DAN ANALISISNYA DENGAN METODE
SPEKTROFOTOMETRI SERAPAN ATOM Nama Mahasiswa : Susilawati
Nomor Pokok : 117006009 Program Studi : Ilmu Kimia
Menyetujui, Komisi Pembimbing
Prof.Dr. Zul Alfian, MSc
Ketua Anggota
Prof.Dr. Harry Agusnar, MSc,M.Phil
Ketua Program Studi, Dekan
Telah diuji pada
Hari / Tanggal : Sabtu / 27 April 2013
PANITIA PENGUJI TESIS
Ketua : Prof.Dr. Zul Alfian, MSc
Anggota : 1. Prof.Dr. Harry Agusnar, MSc, M.Phil 2. Prof.Dr. Harlem Marpaung
3. Prof.Dr. Yunazar Manjang
PENYERAPAN LOGAM ZINKUM (Zn) DALAM AIR LIMBAH
PABRIK BENANG KARET MENGGUNAKAN BATUBARA
YANG DIAKTIFASI DAN ANALISISNYA DENGAN
METODE SPEKTROFOTOMETRI
SERAPAN ATOM
ABSTRAK
Di dalam industri produksi benang karet, logam zinkum digunakan sebagai bahan pengisi untuk meningkatkan elastisitas benang karet yang tinggi sebelum terjadi proses penggumpalan. Telah dilakukan penelitian tentang penyerapan logam zinkum (Zn) dalam air limbah pabrik benang karet menggunakan batu bara aktif yang diaktifasi dan analisisnya dengan metode spektrofotometri serapan atom.Adsorben yang digunakan berasal dari bongkahan batubara. Dilakukan proses adsorpsi terhadap variasi dari larutan aktifasi dengan menggunakan HCl dengan konsentrasi 0,3 N; 0,5N dan 0,7 N. Sedangkan variasi waktu penyerapan selama 24 jam, 36 jam dan 48 jam. Proses adsorpsi terlebih dahulu dilakukan terhadap larutan standar Zn 5 mg/L. Dari hasil penelitian didapati konsentrasi yang terbaik untuk aktifasi pada 0,5 N dan lama waktu penyerapan 36 jam. Hasil penelitian menunjukkan kadar logam Zn pada air limbah sebesar 62,2168 mg/L.Setelah dilakukan proses penyerapan terhadap air limbah tersebut dengan menggunakan arang aktif batubara komersil dan waktu penyerapan 36 jam diperoleh penurunan konsentrasi logam Zn menjadi 8,2204 ± 0,0040 mg/L dengan persentase sebesar 86.78 %. Sedangkan dengan menggunakan arang aktif batu bara aktifasi HCl0,5 N waktu penyerapan selama 36 jam diperoleh penurunan konsentrasi menjadi 4,2910 ± 0,0057 mg/L dengan persentase 92,78 %. Sehingga penggunaan arang aktif batu bara untuk penurunan konsentrasi logam Zn sangat baik digunakan pada pengolahan air limbah pabrik benang karet sesuai dengan KEP – 51/MENLH/10/1995 sebesar 5 -10 mg/L.
ABSORPTION OF ZINKUM (ZN) USING ACTIVATED COAL IN
WASTEWATER THE RUBBER THREAD MANUFACTORY
AND ANALYSIS BY ATOMICABSORPTION
SPECTROPHOTOMETRIC METHOD
ABSTRACT
In the industrial production ofrubber thread, zinkum use das filler material to improve the highelasticityof rubber thread before the clotting process.A study of metal absorption zinkum (Zn) using actived coal in the waste water plant the rubber thread manufactory and analysis by atomic absorption spectrophotometry method. Adsorbent were taken from lumps of coal. Do adsorption process of the variation of the activation solution using HCl with a concentration of 0.3 N, 0.5 N and 0.7 N. While the variation of time soaking for 24 hours, 36 hours and 48 hours. Adsorption process conducted prior to the standard solution of Zn 5 mg / L. From theresults ofthe research foundthatthe best concentration for activation at 0.5N and long 36 hour absorption time. The results showed Zn metal content in wastewater by 62.2168 mg / L. After immersion of the waste water using activated charcoal and coal commercially obtained 36 hours soaking time decreased metal concentrations of Zn being 8.2204 ± 0.0040 mg / L with a percentage of 86.78%. While using activated charcoal coal activation 0.3 N HCl for 36 hours soaking time obtained a decrease in the concentration of 4.2910 ± 0.0057 mg / L with a percentage of 92.78%. So the use of activated charcoal to coal decreased concentrations of Zn metal is best used at the waste water treatment in accordance rubber thread manufactory with the license KEP - 51/MENLH/10/1995 for 5 -10 mg / L.
DA FTAR RIWAYAT HIDUP
DATA PRIBADI
Nama : Susilawati
Tempat dan Tanggal Lahir : Gunung Para, 8 Mei 1965
Alamat Rumah : JalanKramad Gang Katu No. 148B LubukPakam
Handphone : 085276816467
E – mail : susi_suwito@yahoo.com
InstansiTempatBekerja : SMA Negeri 2 LubukPakam
Alamat Kantor : Jalan Hamparan Perak LubukPakam
Telepon : 061-7954302
DATA PENDIDIKAN
SD Negeri 02126 Gudung Para 1972 – 1979
KATA PENGANTAR
Puji dan syukur penulis panjatkan kehadirat Allah SWT yang memberi limpahan rahmat dan hidayah-Nya sehingga penulis dapat menyelesaikan tesis dengan judul “Penyerapan Logam Zinkum (Zn) Dalam Air Limbah Pabrik Benang Karet Menggunakan Batubara Yang Diaktifasi Dan Analisisnya Dengan Metode Spektrofotometri Serapan Atom”.
Dengan selesainya tesis ini, penulis mengucapkan terima kasih yang sebesar-besarnya kepada : Rektor Universitas Sumatera Utara, Bapak Prof. Dr. dr. Syahril Pasaribu, DMTH, M.Sc,CTM, SpA(K), atas kesempatan dan fasilitas yang diberikan kepada penulis untuk menyelesaikan Program Magister, Dekan FMIPA Dr.Sutarman, M.Sc. Ketua Program Studi Kimia, Bapak Prof. Basuki Wirjosentono, MS,Ph.D dan Sekretaris Program Studi Kimia, Bapak Dr. Hamonangan Nainggolan, M.Sc. Atas kesempatan yang telah diberikan kepada penulis untuk menjadi mahasiswa Program Mangister pada Sekolah Pascasarjana Universitas Sumatera Utara.
Terimakasih yang sebesar-besarnya dan penghargaan yang setinggi-tingginya kepada :
1. Bapak Prof. Dr.ZulAlfian, M.Sc, selaku Dosen Pembimbing Utama dan Bapak Prof.Dr.HarryAgusnar,M.Sc,M.Phil, selaku Anggota Komisi Pembimbing yang setiap saat dengan penuh perhatian dan selalu menyediakan waktu untuk memberikan bimbingan, saran dan motivasi sehingga tesis ini dapat penulis selesaikan.
2. Bapak Prof.Dr. Harlem Marpaung, BapakDr.Darwin Yunus,M.S., beserta Bapak Prof. Dr.Yunazar Manjang selaku dosen pembanding yang banyak memberikan saran dan masukan dalam penulisan tesis ini.
4. Suami tercinta Ahmad Jaelani, ananda tersayang Lusiana Bima Mindo Manurung, S.Pd, Ahmed Bima Agam Manurung, Trys Bima Septiani Manurung dan Rizky Bima Nugraha Manurung yang memberikan semangat dan dukungan yang sangat luar biasa untuk terselesainya studi penulis.
5. Rasa terimakasih penulis sampaikan kepada kakanda Paini, Sukmaniati, abangda Suwarno serta adinda Syamsuriani, Sri Hartati dan Nurwanti Agustina, SE yang merupakan semangat dan motivator bagi penulis selama mengikuti program Magister Ilmu Kimia Fakultas Matematika dan Ilmu Pengetahuan Alam.
6. Bapak dan Ibu Dosen serta pegawai Sekolah pascasarjana Program Studi Ilmu Kimia yang telah memberikan ilmu dan motivasi bagi penulis.
7. Pemerintahan Provinsi Sumatera Utara yang memberikan kesempatan kepada penulis untuk mengikuti Program Beasiswa Pascasarjana tahun 2011
8. Kepala Dinas Pendidikan Pemuda dan Olahraga Kabupaten Deli serdang Ibu Hj. Sa’adah Lubis, S.Pd, M.AP yang memberikan rekomendasi agar penulis mengikuti Program Beasiswa Pasca Sarjana
9. Bapak Kepala Sekolah, Drs. H. Ramlan, M.Pd.,Wakil Kepala Sekolah Dra. Fauziah, M.Pd serta Guru – guru dan tata usaha diSMA Negeri 2 Lubuk Pakam, atas izin dan bantuannya saya ucapkan terimakasih.
10. Teman-teman mahasiswa angkatan 2011, ZulMakmur T, M. Saleh, Taufik, Puji P., Zuhairiah, Poppy, Zamaliyah, Fitri I., Silvya, Herlina H., dan teman – teman seperjuangan lainnya di Program Studi Magiter Ilmu yang telah banyak memberikan bantuan moril dan dorongan kepada penulis.
Penulis menyadari bahwa tesis ini masih banyak kekurangan dan masih jauh dari sempurna, oleh karena itu penulis sangat mengharapkan kritik dan saran yang sifatnya membangun dari pihak pembaca untuk kesempurnaan bagi penelitian dan kemajuan ilmu. Amin.
Medan, 27 April 2013
DAFTAR ISI
DAFTAR TABEL viii
DAFTAR GAMBAR ix
BAB 1 PENDAHULUAN 1
1.1 Latar Belakang 3
1.2 Permasalahan 3
1.3 Pembatasan Masalah 3
1.4 Tujuan Penelitian 3
1.5 Manfaat Penelitian 4
1.6 Lokasi Penelitian 4
1.7 Metodologi Penelitian 4
BAB 2 TINJAUAN PUSTAKA 5
2.1 Batubara 5
2.1.1 Klasifikasi batubara 7
2.1.2 Pemanfaatan batubara 10
2.1.3 Arang Aktif Batubara 10
2.2. Industri Benang Karet 12
2.2.1 Proses Pembuatan Benang Karet 13
2.2.2 Tahap – tahap Pengolahan Lateks Bekas Menjadi Sarung
Tangan Karet 14
2.2.3 Sifat Kimia Air Limbah 15
2.2.4 Limbah Industri Karet 16
2.3. Zinkum (Zn) 17
2.3.2 Logam Zinkum dalam kehidupan manusia 17
2.4 Spektrofotometri Serapan Atom (SSA) 17
2.4.1 Instrumentasi Spektrofotometri Serapan Atom 18
BAB 3 METODE DAN BAHAN PENELITIAN 20
3.1 Alat – alat dan Bahan 20
3.2.5 Penyerapan logam zinkum pada larutan standar Zinkum 5 mg/L Dengan menggunakan Arangaktif Batubara yang komersil
dan variasi waktu 22
3.2.6 Penyerapan logam zinkum pada larutan standar Zinkum 5 mg/L Dengan menggunakan Arang aktif Batubara yang diaktifasi
dan variasi waktu 22
3.2.7 Penyerapan logam zinkum dari air buangan limbah dengan menggunakan Arang aktif Batubara yang komersil dan yang telah
diaktifasi 22
3.3 Pembuatan larutan standar zinkum (SNI 06 – 6989.7 – 2009) 23 3.3.1 Pembuatan larutan standar zinkum 1000 mg/L 23 3.3.2 Pembuatan larutan standar zinkum 100 mg/L 23 3.3.3 Pembuatan larutan standar zinkum 10 mg/L 23 3.3.4 Pembuatan larutan seri standar zinkum 0; 0,1; 0,5; 1;
1,5; 2mg/L 23
3.3.5 Pembuatan kurva standar zinkum dan penentuan
3.4 Bagan Penelitian 24
3.4.1 Pembuatan pereaksi HCl 24
3.4.1.1 Pembuatan HCL 0,3 N 24
3.4.1.2 Pembuatan HCL 0,5 N 24
3.4.1.3 Pembuatan HCL 0,5 N 24
3.4.2 Aktifasi Arang aktif batubara dengan HCl 25
3.4.3 Preparasi Terhadap Sampel 26
3.4.4 Penyerapan logam zinkum pada larutan standar Zinkum 5 mg/L Dengan menggunakan Arang aktif Batubara yang komersil
dan variasi waktu 26
3.4.5. Penyerapan logam zinkum pada larutan standar Zinkum 5 mg/L Dengan menggunakan Arang aktif Batubara yang diaktifasi dan
variasi waktu 27
3.4.6 Penyerapan logam zinkum dari air buangan limbah dengan menggunakan Arang aktif Batubara yang komersil dan yang
telah diaktifasi 27
3.4.7 Penyerapan logam zinkum dari air buangan limbah dengan menggunakan Arang aktif Batubara yang telah diaktifasi 28 3.4.8 Pembuatan Kurva Kalibrasi Zinkum (Zn) menggunakan SSA
Nyala (SNI 06 – 6989.7 – 2009) 29
BAB 4 HASIL PENELITIAN 30
4.1 Hasil Penelitian 30
4.1.1 Pengukuran Kandungan Zinkum (Zn) 30
4.1.2 Penurunan garis regresi dengan Metode Least Square 31 4.1.2.1 Perhitungan Koefisien Korelasi 32 4.1.2.2 Penentuan kadar logam Zinkum (Zn) pada penyerapan
larutan standar Zn 5 mg/L dengan menggunakan arang aktif batubara yang komersil dan variasi waktu 33 4.1.2.3 Penentuan kadar logam Zinkum (Zn) pada penyerapan
4.1.2.4 Penentuan kadar logam Zinkum (Zn) pada air buangan limbah dengan menggunakan arang aktif batubara yang komersil dan yang telah diaktifasi 37 4.1.2.5 Persentase penurunan konsentrasi logam Zinkum (Zn)
terhadap larutan standar Zn 5 mg/L dan sampel air
buangan limbah 39
4.2. Pembahasan 40
BAB 5 KESIMPULAN DAN SARAN 43
5.1 Kesimpulan 43
5.2 Saran 43
DAFTAR TABEL
Nomor Judul Halaman
Tabel 2.1. Komposisi elemen dari berbagai tipe batubara 8 Tabel 2.2. Volume Penggunaan Air oleh Industri Sarung Tangan Karet 16
Tabel 2.3. Kandungan unsur Kimia yang terdapat pada limbah benang karet
16
Tabel 4.1. Kondisi alat SSA Merek Shimadzu tipe AA-6300 pada pengukuran konsentrasi logam Zinkum (Zn)
30
Tabel 4.2. Data absorbansi larutan seri standar logam Zinkum (Zn) 30 Tabel 4.3. Penurunan persamaan garis regresi dengan metode Least
Square untuk logam Zinkum (Zn)
31
Tabel 4.4. Hasil pengukuran absorbansi pada sampel larutan standar 5 mg/L
33
Tabel 4.5. Hasil pengukuran kadar logam Zinkum (Zn) 34 Tabel 4.6. Hasil pengukuran absorbansi pada sampel larutan standar
5 mg/L
35
Tabel 4.7. Hasil pengukuran konsentrasi logam Zinkum (Zn) 36 Tabel 4.8. Hasil pengukuran absorbansi pada sampel air buangan
limbah
37
Tabel 4.9. Hasil pengukuran kadar logam Zinkum (Zn) 38 Tabel 4.10. Data persentase (%) penurunan konsentrasi logam Zinkum
dalam larutan standar setelah penambahan arang aktif batubara komersil dengan variasi waktu penyerapan
39
Tabel 4.11. Data persentase (%) penurunan konsentrasi logam Zinkum dalam larutan standar setelah penambahan arang aktif batubara yang diaktifasi dengan variasi waktu penyerapan
40
Tabel 4.12. Data persentase (%) penurunan konsentrasi logam Zinkum dalam sampel air buangan limbah setelah penambahan arang aktif batubara dengan variasi waktu penyerapan
DAFTAR GAMBAR
Nomor Judul Halaman
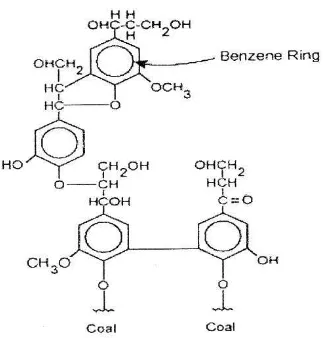
Gambar 2.1. Rumus bangun batubara 5
Gambar 2.2. Antrasit 8
Gambar 2.3. Bitumen danSubbitumin 9
Gambar 2.4. Lignit 9
DAFTAR LAMPIRAN
Nomor Judul Halaman
Gambar 2.1. Rumus bangun batubara 5
Gambar 2.2. Antrasit 8
Gambar 2.3. Bitumen danSubbitumin 9
Gambar 2.4. Lignit 9
PENYERAPAN LOGAM ZINKUM (Zn) DALAM AIR LIMBAH
PABRIK BENANG KARET MENGGUNAKAN BATUBARA
YANG DIAKTIFASI DAN ANALISISNYA DENGAN
METODE SPEKTROFOTOMETRI
SERAPAN ATOM
ABSTRAK
Di dalam industri produksi benang karet, logam zinkum digunakan sebagai bahan pengisi untuk meningkatkan elastisitas benang karet yang tinggi sebelum terjadi proses penggumpalan. Telah dilakukan penelitian tentang penyerapan logam zinkum (Zn) dalam air limbah pabrik benang karet menggunakan batu bara aktif yang diaktifasi dan analisisnya dengan metode spektrofotometri serapan atom.Adsorben yang digunakan berasal dari bongkahan batubara. Dilakukan proses adsorpsi terhadap variasi dari larutan aktifasi dengan menggunakan HCl dengan konsentrasi 0,3 N; 0,5N dan 0,7 N. Sedangkan variasi waktu penyerapan selama 24 jam, 36 jam dan 48 jam. Proses adsorpsi terlebih dahulu dilakukan terhadap larutan standar Zn 5 mg/L. Dari hasil penelitian didapati konsentrasi yang terbaik untuk aktifasi pada 0,5 N dan lama waktu penyerapan 36 jam. Hasil penelitian menunjukkan kadar logam Zn pada air limbah sebesar 62,2168 mg/L.Setelah dilakukan proses penyerapan terhadap air limbah tersebut dengan menggunakan arang aktif batubara komersil dan waktu penyerapan 36 jam diperoleh penurunan konsentrasi logam Zn menjadi 8,2204 ± 0,0040 mg/L dengan persentase sebesar 86.78 %. Sedangkan dengan menggunakan arang aktif batu bara aktifasi HCl0,5 N waktu penyerapan selama 36 jam diperoleh penurunan konsentrasi menjadi 4,2910 ± 0,0057 mg/L dengan persentase 92,78 %. Sehingga penggunaan arang aktif batu bara untuk penurunan konsentrasi logam Zn sangat baik digunakan pada pengolahan air limbah pabrik benang karet sesuai dengan KEP – 51/MENLH/10/1995 sebesar 5 -10 mg/L.
ABSORPTION OF ZINKUM (ZN) USING ACTIVATED COAL IN
WASTEWATER THE RUBBER THREAD MANUFACTORY
AND ANALYSIS BY ATOMICABSORPTION
SPECTROPHOTOMETRIC METHOD
ABSTRACT
In the industrial production ofrubber thread, zinkum use das filler material to improve the highelasticityof rubber thread before the clotting process.A study of metal absorption zinkum (Zn) using actived coal in the waste water plant the rubber thread manufactory and analysis by atomic absorption spectrophotometry method. Adsorbent were taken from lumps of coal. Do adsorption process of the variation of the activation solution using HCl with a concentration of 0.3 N, 0.5 N and 0.7 N. While the variation of time soaking for 24 hours, 36 hours and 48 hours. Adsorption process conducted prior to the standard solution of Zn 5 mg / L. From theresults ofthe research foundthatthe best concentration for activation at 0.5N and long 36 hour absorption time. The results showed Zn metal content in wastewater by 62.2168 mg / L. After immersion of the waste water using activated charcoal and coal commercially obtained 36 hours soaking time decreased metal concentrations of Zn being 8.2204 ± 0.0040 mg / L with a percentage of 86.78%. While using activated charcoal coal activation 0.3 N HCl for 36 hours soaking time obtained a decrease in the concentration of 4.2910 ± 0.0057 mg / L with a percentage of 92.78%. So the use of activated charcoal to coal decreased concentrations of Zn metal is best used at the waste water treatment in accordance rubber thread manufactory with the license KEP - 51/MENLH/10/1995 for 5 -10 mg / L.
BAB 1
PENDAHULUAN
1.1.Latar Belakang
Penyerapan (Adsorpsi) secara umum adalah suatu proses pemisahan bahan dari campuran gas atau cair, bahan yang harus dipisahkan ditarik oleh permukaan sorben padat dan diikat oleh gaya-gaya yang berkerja pada permukaan tersebut. Absorben adalah bahan padat dengan luas permukaan dalam yang sangat besar. Permukaan yang luas ini terbentuk karena banyaknya pori yang halus pada ikatan tersebut. Biasanya luasnya berada dalam orde 200 – 1000 m2/g adsorben, dengan diameter pori sebesar 0,0003 – 0,02 μm. Adsorben yang sering dikenal ialah karbon aktif, silika gel, zeolit alam, tapis molekuler (moleculer sieve), tanah kelantang (bleaching earth), aluminium oksida dan lain-lain (Bernasconi, G., 1995).
Salah satu adsorben yang banyak digunakan adalah karbon aktif.Karbon aktif yang digunakan berasal dari hasil pembakaran dengan suhu tertentu untuk menghasilkan karbon dengan ukuran partikel tertentu.Batubara merupakan salah satu komoditi yang penggunaanya dilakukan hanya sebatas untuk bahan bakar. Tingkat karbon yang dihasilkan dari batu bara mencapai 90% (Laksana, A.B.,2011). Indonesia merupakan negara yang memiliki kelimpahan batubara yang dikelola PT. Bukit Asam.Dengan nilai kandungan karbon yang tinggi maka batubara dapat digunakan sebagai salah satu adsorben untuk menyerap logam-logam berat.
Dan beberapa penelitian yang telah dilakukan tentang penggunaan adsorben sebagai penyerap logam-logam berat. Davidson R.J. (2009), dengan penelitian mekanisme dari penyerapan logam emas menggunakan batubara aktif. Pada penelitian tersebut beberapa perbandingan meliputi pengaruh dari kekuatan ion mengadsorpsi logam emas, pengaruh pH pada adsoprsi logam emas, dan pengaruh temperatur.Hasil yang diperoleh bahwa ion yang baik untuk menyerap adalah kation Kalsium dan anion Hidroksil.Sedangkan pH yang semakin tinggi mengakibatkan penurunan penyerapan logam emas.
Souundarrajan (2012), dengan penelitian penyerapan logam Kromium (VI) dari larutan standar dan pembelajaran kinetiknya. Hasil yang diperoleh menunjukkan Penyerapan terhadap Cr (VI) dengan kitosan menghasilkan peningkatan penyerapan pada pH 5 dalam menyerap logam tersebut, sedangkan waktu kontak terbaik selama 300 menit (5 jam) .
Logam berat ialah unsur logam dengan berat molekul yang tinggi. Dalam kadar rendah logam berat pada umumnya sudah beracun bagi tumbuhan dan hewan, termasuk manusia. Logam berat yang sering mencemari lingkungan perairan adalah : Hg, Zn, Cd, As, dan Pb (Notohadiprawiro, T. 1993).
Perawatan pencemaran air mempunyai nilai (biaya) yang cukup tinggi sehingga mempengaruhi harga produk. Upaya pemulihan kondisi air cemar, bagaimanapun akan memerlukan biaya yang mungkin lebih besar tetapi bila dibandingkan dengan nilai efek yang ditimbulkan pada kesehatan semua makhluk hidup jauh lebih besar (Ridwan, 2008).
Hal ini yang mendorong penulis untuk melakukan penelitian tentang penyerapan logam zinkum (Zn) dalam air limbah pabrik benang karet menggunakan batubara aktif yang diaktifasi dan analisisnya dengan metode Spektrofotometri Serapan Atom (SSA).
1.2.Permasalahan
1. Bagaimana pengaruh konsentrasi aktifator larutan HCl terhadap kemampuan adsorben dalam menyerap logam Zinkum (Zn) pada air buangan limbah pabrik benang karet.
2. Apakah kadar logamzinkum(Zn) pada air buangan limbah pabrik benang karetsetelah diadsorpsi dengan menggunakan arang aktif batu bara melebihi nilai ambang batas sesuai KEP – 51/MENLH/10/1995.
1.3.Pembatasan masalah
Dalam penelitian ini dibatasi pada :
1. Absorben yang digunakan adalah arang aktif batubara komersil dari bongkahan batubara.
2. Ukuran partikel arang aktif adalah ≤ 100 mesh
3. Aktifator yang digunakan untuk arang aktif bongkahan batubara adalah HCl 0,3 N, HCl 0,5 N dan HCl 0,7 N.
4. Variasi waktu penyerapan adalah 24 jam, 36 jam dan 48 jam.
5. Pengujian terhadap penyerapan digunakan larutan standar Zinkum (Zn) sebesar 5 mg/L
6. Analisis yang digunakan untuk menganalisis logam Zn menggunakan Spektrofotometer Serapan Atom (SSA).
1.4. Tujuan Penelitian
Adapun tujuan dari penelitian ini adalah :
2. Untuk menentukan persentase penurunan kadar logam Zinkum (Zn) dari air buangan limbah dengan menggunakan arang aktif sebagai adsorben.
1.5.Manfaat Penelitian
Dari hasil penelitian ini diharapkan dapat memberikan informasi bahwa konsentrasi aktifator dan penggunaan perbandingan massa adsorben dapat menurunkan kadar logam yang terdapat di dalam air buangan limbah pabrik sehingga air yang dibuang ke badan sungai sesuai dengan peraturan KEP – 51/MENLH/10/1995.
1.6. LokasiPenelitian
1. Laboratorium Kimia Analitik FMIPA Universitas Sumatera Utara 2. Laboratorium Ilmu Dasar UPT PP LIDA Universitas Sumatera Utara.
1.7. Metodologi Penelitian
1. Penelitian ini merupakan analisis yang dilakukan di laboratorium
2. Sampel yang digunakan adalah larutan standar Zinkum (Zn) 5 mg/L dan air limbah pertama pabrik benang karet.
3. Aktifator yang digunakan arang aktif batubara adalah HCl.
4. Metode pengaktifan yang digunakan adalah pemanasan, pengasaman dan penyerapan.
BAB 2
TINJAUAN PUSTAKA
2.1. Batubara
Komposisi kimia batubara hampir sama dengan komposisi kimia jaringan tumbuhan, keduanya mengandung unsur utama yang terdiri dari unsur C. H. O, N, S, P. hal ini mudah dimengerti, karena batubara terbentuk dari jaringan tumbuhan yang telah mengalami proses pembatubaraan (coalification).
Batubara terbentuk dari sisa-sisa tumbuhan yang sudah mati, dengan komposisi utama terdiri dari sellulosa. Proses pembentukan batubara dikenal sebagai proses pembatubaraan atau coalification. Faktor fisika dan kimia yang ada di alam akan mengubah sellulosa menjadi lignit, subbitumina, bitumina, atau antrasit. Reaksi pembentukan batubara dapat diperlihatkan sebagai berikut :
Gambar 2.1. Rumus bangun batubara
5(C6H10O5) C20H22O4 + 3CH4 + 8H2O + 6CO2 + CO Sellulosa lignit gas metan
gelap, dan dapat dibakar.Apabila batubara tersebut mudah dibakar dan menghasilkan kalori tinggi, disebut batubara, tetapi apabila batubara tersebut tidak mudah dibakar dan menghasilkan kalori rendah disebut sebagai batubara muda. (Sukandarrumidi, 2006)
Batubara adalah bahan bakar padat yang paling penting. Konsumsi dunia mencapai sekitar 4x109 t/tahun, 7x108 t/tahun di antaranya dikonsumsi di Amerika Serikat. Cadangan yang diketahui ada di AS diperkirakan cukup untuk pemakaian 200 tahun dengan laju konsumsi saat ini, tetapi sebagian besar adalah batubara berkadar belerang tinggi yang dapat menimbulkan pencemaran udara yang serius. (Austin, G. 1996)
Indonesia menjadi salah satu negara penghasil sumber daya alam tebesar di dunia.Salah satu potensi kekayaan alam yang dihasilkan Indonesia adalah batubara.Potensi sumber daya batubara Indonesia cukup besar yaitu 61,366 miliar ton yang tersebar di 19 daerah provinsi termasuk provinsi Sumatera Selatan. Dari potensi tersebut jumlah yang paling banyak adalah batubara jenis kalori sedang sebesar 37,69467 milyar ton, batubara jenis kalori rendah sebesar 14,94962 milyar ton dan selebihnya batubara dengan nilai kalori tinggi dan sangat tinggi (Indonesia Energy, 2006). Oleh karena itu Indonesia sebagai salah satu negara pengekspor batubara terbesar, memilikipotensi dalam pengembangan batubara (Chrisman, A. 2008).
Kegiatan pertambangan batubara di Indonesia saat ini menunjukkan peningkatan yang sangat pesat. PT Tambang Batubara Bukit Asam sebagai satu-satunya BUMN di bidang batubara telah tumbuh menjadi perusahaan berskala besar dengan produksi 7 juta ton pertahun berdasarkan Peraturan Pemerintah No. 23 tahun 1968 yang dikenal sebagai Unit II.
Demikian juga Kerja Sama Operasional (KSO) yang sebagian besar dari produksi Penanaman Modal Asing (PMA) telah menunjukkan keberhasilan produksinya sampai pada tingkat dua kali lebih besar daripada PT Bukit Asam.(Sukandarrumidi, 1995).
2.1.1 Klasifikasi batubara
Batubara diklasifikasikan menurut sifat pembakarannya, menjadi antrasit, bitumen, subbitumin, dan lignit.Setiap jenis mempunyai subbagian lagi.Antrasit merupakan bahan bakar rumah tangga yang sangat berguna, karena pembakarannya besar, tetapi cadangannya sudah mulai habis.Batubara bitumen terutama digunakan dalam pembakaran yang menghasilkan energi atau karbonisasi untuk pembuatan kokas, ter, bahan kimia batubara, dan gas pabrik kokas (Austin, 1996).
Tabel 2.1. Komposisi elemen dari berbagai tipe batubara Komposisi Elemen dari Beberapa Tipe Batubara
Jenis Batubara Persentase Massa
% C % H % O % H2O % Volatile Matter
Lignit 60-70 5-6 20-30 50-70 45-55 Subbituminous 75-80 5-6 15-20 25-30 40-45
Bituminous 80-90 4-5 10-15 5-10 20-40
Antrasit 90-95 2-3 2-3 2-5 5-7
a. Sifat batubara jenis antrasit :
─ Warna hitam sangat mengkilat, kompak
─ Nilai kalor sangat tinggi, kandungan karbon sangat tinggi ─ Kandungan air sangat sedikit
─ Kandungan abu sangat sedikit ─ Kandungan sulfur sangat sedikit
Gambar 2.2. Antrasit b. Sifat batubara jenis bitumen/subbitumin :
─ Warna hitam mengkilat, kurang kompak
─ Nilai kalor tinggi, kandungan karbn relatif tinggi ─ Kandungan air sedikit
Gambar 2.3. Bitumen dan Subbitumin
c. Sifat batubara jenis lignit : ─ Warna hitam, sangat rapuhvx
─ Nilai kalor rendah kandungan karbon sedikit ─ Kandungan air tinggi
─ Kandungan abu dan sulfur banyak
2.1.2 Pemanfaatan Batubara
Pemakaian batubara di Indonesia terutama ditujukan untuk Pembangkit Listrik dan Pabrik Semen. Batubara dapat pula dipergunakan tidak sebagai bahan bakar, tetapi dipergunakan sebagai reduktor pada proses peleburan timah, industri fero-nikel, industri besi dan baja, sebagai bahan pemurnian pada industri kimia (dalam bentuk karbon aktif), sebagai bahan pembuatan kalsium karbida (dalam bentuk kokas atau semikokas). (Sukandarrumidi, 2006).
Batubara merupakan batuan sedimentasi berwarna hitam atau hitam kecoklat-coklatan yang mudah terbakar dan terbentuk dari batuan endapan organik yang terdiri dari karbon hidrogen, oksigen, dan unsur-unsur lain. Oleh karena itu batubara digunakan sebagai bahan dasar pembuatan karbon aktif.Disamping karena memiliki unsur karbon yang cukup besar, pembuatan karbon aktif dari bahan dasar batubara juga dapat meningkatkan nilai ekonomi dari batubara tersebut (Chrisman, 2008).
2.1.3 Arang Aktif Batubara
Arang aktif merupakan senyawa karbon amorf, yang dapat dihasilkan dari bahan-bahan yang mengandung karbon atau dari arang yang diperlakukan dengan cara khusus untuk mendapatkan permukaan yang lebih luas. Luas permukaan arang aktif berkisar antara 300-3500 m2/gram dan ini berhubugan dengan struktur pori internal yang menyebabkan arang aktif mempunyai sifat sebagai adsorben. Arang aktif dapat mengadsorpsi gas dan senyawa-senyawa kimia tertentu atau sifat adsorpsinya selektif, tergantung pada besar atau volume pori-pori dan luas permukaan.Daya serap arang aktif sangat besar, yaitu 25-100% terhadap berat arang aktif.
Bahan baku yang berasal dari hewan, tumbuh-tumbuhan, limbah ataupun mineral yang mengandung karbon dapat dibuat menjadi arang aktif, antara lain tulang, kayu lunak, sekam, tongkol jagung, tempurung kelapa, ampas pembuatan kertas, serbuk gergaji, kayu keras, dan batubara ( Tryana, 2003).
hidrokarbon yang melapisi permukaan arang. Penelitian selanjutnya, pada kedua proses tersebut terjadi tahap-tahap sebagai berikut :
1. Dehidrasi yaitu proses menghilangkan air
2. Karbonisasi yaitu proses penguraian selulosa organic menjadi unsur karbon, serta mengeluarkan senyawa-senyawa non karbon
3. Aktifasi yaitu proses pembentukan dan peyusunan karbon sehingga pori-pori menjadi lebih besar.
Pada prinsipnya arang aktif dapat dibuat dengan dua cara, yaitu cara kimia dan cara fisika. Pada pembuatan arang aktif, mutu yang dihasilkan sangat tergantung dari bahan baku yang digunakan, bahan pengaktif, suhu dan cara pengaktifannya.
1. Pembuatan Arang Aktif secara Kimia
Prinsipnya yaitu penyerapan arang dengan senyawa kimia sebelum dipanaskan. Pada proses pengaktifan secara kimia, arang direndam dalam larutan pengaktifasi selama 24 jam lalu ditiriskan dan dipanaskan pada suhu 600-900°C selama 1-2 jam. Pada suhu tinggi ini bahan pengaktif akan masuk diantara sela-sela lapisan heksagonal dan selanjutnya membuka permukaan yang tertutup. Dari hasil penelitian yang membuat arang aktif dari batubara, lalu mengekstrak arang aktif tersebut dengan HCl 0,5 M menghasilkan arang aktif struktur mikroporinya lebih besar.
2. Pembuatan Arang Aktif secara Fisika
Prinsipnya adalah pemberian uap air atau gas CO2 kepada arang yang telah dipanaskan.Arang aktif yang telah dihaluskan dimasukkan ke dalam tungku aktivasi lalu dipanaskan pada suhu 800-1000°C.
Dalam proses penjernihan air, arang aktif selain mengadsorpsi logam-logam seperti besi, tembaga, nikel, juga dapat menghilangkan bau warna, dan rasa yang terdapat dalam larutan atau buangan air. Karena arang aktif lebih bersifat nonpolar, maka komponen non polar dengan berat molekul tinggi ( 4 sampai 20 atom karbon) yang terdapat dalam buangan air pabrik dan diadsorpsi oleh arang aktif.
Penggunaan karbon aktif terutama adalah untuk pemurnian larutan, ,misalnya pembersihan larutan gula tebu, gula bit dan gula jagung, dan untuk menghilangkan rasa dan bau air minuman, minyak nabati dan gemuk hewani, minuman alkohol, bahan kimia, dan bahan obat-obatan (Austin, 1996).
2.2. Industri Benang Karet
Pabrik benang karetmerupakan industri yang mengelola bahan baku karet (lateks) menjadi produk jadi. Pabrik ini mempunyai 3 (tiga) pabrik pengolahan, yaitu :
Rubber Article Factory (RAF) Dipping Process Factory (DPF) Rubber Thread Factory (RTF)
Pabrik – pabrik ini mempunyai sistem pengolahan yang berbeda. Bahan baku yang digunakan DPF dan RTF adalah bahan baku lateks, sedangkan RAF menggunakan bahan baku padat (karet yang telah dikeringkan).
Produk – produk yang dihasilkan ketiga pabrik tersebut adalah :
1. RAF menghasilkan artikel karet, pita karet, rubber cownmats, dock fender dan conveyer belt.
2. DPF menghasilkan sarung tangan karet 3. RTF menghasilkan benang karet
Bahan baku untuk pembuatan benang karet adalah lateks DRC 60% (lateks pekat hasil pemusingan) yang berasal dari pusat Pengolahan Karet (PPK).
Rubber Thread Factory (RTF) adalah medium amoniak yang kadarnya 0,40 – 0,54%, sebagai bahan pemantap ditambah larutan ammonium laurat 20% dosis 4 – 5 mL/L. Lateks pekat inilah yang dipakai sebagai bahan baku dalam pembuatan benang karet.
Proses pembuatan karet menjadi benang karet dengan cara lateks pekat yang masuk diperiksa di laboratorium kimia dan diuji kemudian lateksnya di simpan ditempat penyimpanan lateks yang tersedia. Disamping itu bahan-bahan kimia yang akan digunakan diperiksa dan diuji di laboratorium kimia, lalu disimpan di tempat tersedia lalu ditimbang. Bahan kimia tersebut diproses menjadi pengemulsi kemudian dimasukkan ke dalam tangki storage masing-masing, setelah itu ditimbang sesuai dengan formulasi yang ditentukan. Kedua bahan tersebut dicampur ditangki inactive
membentuk compound, lalu ditambahkan zat activator yaitu ZDBC dan ZnO untuk membentuk active compound. Active compound tersebut dimaturasi untuk proses pematangan lalu dihomogenkan dengan mixer. Setelah homogen, compound diperiksa dan didinginkan ke dalam cooling storage tank pada temperatur 13oC. Setelah pendinginan active compound diperiksa kemudian dilewatkan ke dalam feeding sistem yang berfungsi sebagai penyimpanan sementara agar buih dan kotoran yang ada dapat hilang. Compound active tersebut dialirkan ke dalam header dan diteruskan melalui
capillary dalam acid bath yang berfungsi untuk menggumpalkan agar berbentuk benang. Kemudian dibilas dengan menggunakan air panas pada suhu 60 – 70oC pada water bath kemudian dikeringkan dalam drying oven pada suhu 105 – 110oC, lalu dilewatkan melalui talcum box agar tidak lengket. Air bilasan benang karet tersebut dikeluarkan melalui pipa langsung dibuang ke kolam pengolahan limbah. Benang karet tersebut dilewatkan melalui ribboning agar berbentuk pita-pita benang, lalu diperiksa di laboratorium Fisika. Kemudian pita tersebut dikeringkan dengan proses vulkanisasi dan didinginkan. Dan hasil akhirnya terbentuk pita benang karet yang akan di ekspor.
2.2.1. Proses Pembuatan Benang Karet
16 – 2623 – 1992, meliputi tegangan putus 270,1 N/ mm2, perpanjangan putus 801 %, modulus 1,2 N/ mm2, dan ketahanan sobek 680 N/ mm2 .
Adapun yang menjadi bahan – bahan dalam pengolahan lateks pekat menjadi sarung tangan karet adalah lateks pekat dengan kadar karet kering 60% , dan sebagai bahan anti koagulan adalah NH4OH, Belerang, Texapon 10%, KOH 10%, dan sebagai zat akseerator adalah ZnO, ZDEC, dan bahan pengisi adalah Titan Oksida, Silikon, dan Tanin.
2.2.2. Tahap – Tahap Pengolahan Lateks Pekat menjadi Sarung Tangan Karet
A. Pembuatan dispersi
1. Bahan – bahan akselerator tersebut dimasukkan dalam sebuah drum yang didalamnya dilengkapi peluru – peluru, kemudian drum ditutup rapat dan diletakkan dalam wadah yang berputar ( gilingan dispersi ) , Dan dibiarkan berputar selama 24 jam.
2. Hasil dispersi dicampurkan kedalam lateks pekat, diaduk sampai merata dan campuran disimpan selama 3 – 5 hari untuk diperam ( maturing ). Pemeraman bertujuan agar campuran lebih homogen dan terjadi pemvulkanisasian.
3. Untuk mengetahui tahap vulkanisasi periksa campuran dengan memipet 10 ml campuran dan tambahkan Chlorofom sambil diaduk 5 menit, dan gumpalan diperiksa.
B. Persiapan Cetakan
1. Pencelupan dengan asam, untuk membersihkan cetakan ( acid washing dip ) 2. Pembilasan cetakan ( Formers drying)
2.2.3. Sifat Kimia Air Limbah
Limbah adalah buangan yang dihasilkan dari suatu proses produksi baik industri maupun domestik (rumah tangga), yang kehadirannya pada suatu saat dan tempat tertentu tidak dikehendaki lingkungan karena tidak memiliki nilai ekonomis. Bila ditinjau secara kimiawi, limbah ini terdiri dari bahan kimia organik dan anorganik. Dengan konsentrasi dan kuantitas tertentu, kehadiran limbah dapat berdampak negatif terhadap lingkungan terutama bagi kesehatan manusia, sehingga perlu dilakukan penanganan terhadap limbah. Tingkat bahaya keracunan yang ditimbulkan oleh limbah tergantung pada jenis dan karakteristik limbah.
Kandungan Bahan kimia yang ada dalam limbah cair dapat merugikan lingkungan melalui berbagai cara. Bahan organik terlarut dapat menghabiskan oksigen dalam limbah serta akan menimbulkan rasa dan bau yang tidak sedap pada penyediaan air bersih. Hal yang lebih berbahaya adalah jika bahan organik yang terlarut bersifat toksik.
Tabel 2.2. Volume Penggunaan Air oleh Industri Sarung Tangan Karet
No Volume Air Debit Air (m3 / Hari)
1 Volume air baku produksi 300
2 Volume limbah awal/inlet 16,5
3 Volume limbah akhir/outlet 8,5
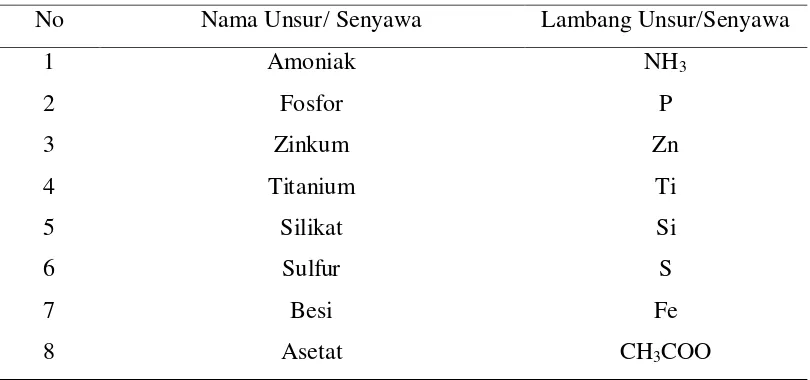
Tabel 2.3. Kandungan unsur Kimia yang terdapat pada limbah benang karet
No Nama Unsur/ Senyawa Lambang Unsur/Senyawa
1 Amoniak NH3
2 Fosfor P
3 Zinkum Zn
4 Titanium Ti
5 Silikat Si
6 Sulfur S
7 Besi Fe
8 Asetat CH3COO
2.2.4. Limbah Industri Karet
Pada proses pengolahan karet, dihasilkan air limbah yang mengandung berbagai jenis bahan organik dan anorganik serta mikroba sehingga diperkirakan dapat mengganggu ekosistem perairan. Kualitas dan kuantitas air limbah dari industri karet ini sangat bergantung pada jenis aktivitas dan besar kecilnya industri. Pada umumnya air limbah industri ini berasal dari :
1. Air hasil proses produksi
2. Air hasil pencucian alat-alat, mesin, wadah, dan lain – lain 3. Air hasil proses pemanasan dan pendinginan
Limbah industri yang dibuang tanpa diolah terlebih dahulu akan menimbulkan pencemaran dan gangguan terhadap kesehatan manusia, keseimbangan lingkungan / ekologi dan keindahan lingkungan.(Sugiharto,1987)
2.3. Zinkum (Zn)
2.3.1. Sifat- sifat logam zinkum
Zinkum dengan nomor atom 30 dan massa atom 65,38 dalam sistem periodik unsur terletak pada periode 4 dan golongan IIB. Zinkum adalah logam yang putih kebiruan, logam yang mudah ditempa dan liat pada suhu antara 110 – 150 oC. Zinkum melebur pada suhu 410 oC dan mendidih pada 906 oC. Logamnya yang murni, melarut lambat sekali dalam asam dan dalam alkali.( Vogel, 1979). Zinkum masuk ketatanan lingkungan perairan melalui limbah industri, pengelasaan logam dan patri. Zinkum merupakan unsur penting dalam banyak metaloenzim, obat luka. (Manahan, 1994).
2.3.2. Logam zinkum dalam kehidupan manusia
Tubuh yang normal membutuhkan 12 – 15 miligram zinkum setiap hari. Kebanyakan orang mendapatkan zat tersebut secara alami melalui makanan atau minuman yang dikonsumsi. Namun jika zat zinkum yang masuk ke dalam tubuh berlebihan, maka dapat mengakibatkan keracunan Zinkum. Usus tertekan, muntah, keram perut, diare dan mual berkepanjangan. Gejala tersebut jika tidak segera ditangani dapat menyebabkan sakit kuning, kejang, demam dan tekanan darah rendah, bahkan kematian.
Sedangkan (Eamens dkk, 1984 dan Darmono, 1995) menyatakan keracunan zinkum dengan gejala – gejala : osteomalasea, kalkulirenalis, dan proteinuria. Keracunan zinkum sering dijumpai bersamaan dengan keracunan kadmium secara kronis.
2.4.Spektrofotometri Serapan Atom (SSA)
memanfaatkan fenomena interaksi materi dengan gelombang elektromagnetik seperti sinar-X, ultraviolet, cahaya tanpak dan inframerah. Fenomena interaksi bersifat spesifik baik absorbsi maupun emisi. Interaksi tersebut menghasilkan signal-signal yang disadap sebagai analisa kualitatif dan kuantitatif.
SSA adalah metoda analisis yang berdasarkan pada pengukuran radiasi cahaya yang diserap atom bebas. Analisis menggunakan alat SSAini memiliki keuntungan dari hasil analisisnya yang sangat peka, teliti dan cepat, pengerjaannya relatip sederhana serta tidak perlu dilakukan pemisahan unsur logam dalam pelaksanaannya. (Walsh, A, 1995)
Analisis SSA yang didasarkan pada penyerapan energi radiasi dari sumber nyala atom-atom yang berada pada tingkat energi dasar. Komponen-komponen utama yang menyusun SSA adalah sumber cahaya, atomizer, monokromator, detector, dan penampilan data (Anderson,1987). Penggunaan SSA dalam menganalisa kandungan logam-logam, dikarenakan dengan metode SSA unsur-unsur dengan energi eksitasi rendah.
2.4.1 Instrumentasi Spektrofotometri Serapan Atom
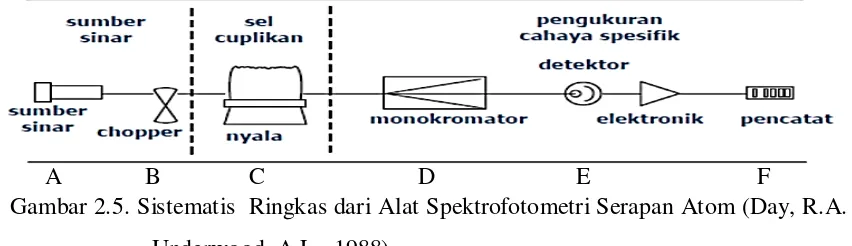
Gambar 2.5. Sistematis Ringkas dari Alat Spektrofotometri Serapan Atom (Day, R.A. Underwood, A.L., 1988)
Keterangan :
A. Sumber sinar lampu katoda berongga
Lampukatodaberonggamerupakansumber sinar yang memancarkan spektrum dari unsur logam yang akandianalisa (setiap logammemiliki lampu khususuntuklogam tersebut)
B. Chopper
Mengatur sinar yang dipancarkan C. Tungku
Tempat pembakaran(untuk memecahkan larutan sampel pada tetesan halus dan meleburkannya kedalam nyala untuk diatomkan).
D. Monokromator
Mendispersi sinar yang ditransmisikan oleh atom. E. Detektor
Mengukur sinar yang ditranmisikan dan memberikan signal sebagai respon terhadap sinar yang diterima.
F. Pencatat bacaan nilai absorbansi
BAB 3
METODE DAN BAHAN PENELITIAN
3.1. Alat-alat dan bahan
3.1.1. Alat-alat yang digunakan
- Spektrofotometri Serapan Atom AA-6300 Shimadzu
- Lampu hallow katoda
- Erlemeyer 250 ml
- Alat – alat gelas yang biasa digunakan di laboratorium Pyrex
- PH meter WlkLAB
- Kertas saring Whatman No. 40
- Hotplate magnetik strirer Cimarec
- Neraca analitik AND
- Alu dan lumpang
3.1.2. Bahan-bahan yang digunakan
- Akuades
3.2.1. Cara pengambilan sampel
Sampel arang aktif batubara diambil dari daerah Kotamadya Kisaran yang
berasal dari PT. Bukit Asam Tbk. Sedangkan sampel limbah diambil dari salah satu
pabrik pengolahan benang karet di daerah tanjung Morawa, Deli Serdang, Sumatera
Teknik pengambilan sampel dilakukan secara berkala.Sampel diambil dari air
buangan pertama pada minggu pertama, minggu kedua dan minggu ketiga.Dianggap
mampu mewakili sampel lainnya.
3.2.2. Pembuatan pereaksi HCl
3.2.2.1. Pembuatan HCl 0,3 N
Sebanyak 2,5 mL HCl(p) dimasukkan ke dalam labu takar 100 mL secara perlahan-lahan. Ditambahkan akuades secara perlahan-lahan sampai garis tanda. Di tunggu sampai larutan benar-benar dingin. Setelah dingin, kemudian dihomogenkan.
3.2.2.2. Pembuatan HCl 0,5 N
Sebanyak 4 mL HCl(p) dimasukkan ke dalam labu takar 100 mL secara perlahan-lahan. Ditambahkan akuades secara perlahan-lahan sampai garis tanda. Di tunggu sampai larutan benar-benar dingin. Setelah dingin, kemudian dihomogenkan.
3.2.2.3. Pembuatan HCl 0,7 N
Sebanyak 5,8 mL HCl(p) dimasukkan ke dalam labu takar 100 mL secara perlahan-lahan. Ditambahkan akuades secara perlahan-lahan sampai garis tanda. Di tunggu sampai larutan benar-benar dingin. Setelah dingin, kemudian dihomogenkan.
3.2.3. Aktifasi arang aktif dengan HCl
Sebanyak 25 gram arang aktif batubara 100 mesh dimasukkan ke dalam gelas beaker yang
berisi 100 mL HCl0,3N. Di aduk dengan menggunakan magnetik strirer selama 2 jam
dengan kecepatan 80 rpm sambil dipanaskan pada suhu 100 oC. Di saring dengan menggunakan akuades sampai pH netral. Dipanaskan di dalam oven pada suhu 105 oC. Kemudian dihaluskan kembali. Hal yang sama dilakukan untuk aktifasi arang aktif dengan
3.2.4. Preparasi Terhadap Sampel(SNI 06 – 6989 .7 – 2004)
Sebanyak 10 mL sampel dimasukkan ke dalam beaker glass. Kemudian ditambahkan sebanyak 5 mL HNO3 pekat lalu diaduk sampai homogen. Campuran yang diperoleh dipanaskan diatas pemanas listrik sampai hampir kering. Setelah hampir kering lalu didinginkan. Setelah dingin, ditambahkan 50 ml aquadest, kemudian dimasukkan kedalam labu ukur 100 ml melalui kertas saring dan ditepatkan 100 ml dengan aquadest.
3.2.5. Penyerapan logam Zinkum pada larutan standar Zinkum 5 mg/Ldengan menggunakan arang aktif batubara yang komersil dan variasi waktu
Sebanyak 25 ml sampel dimasukkan kedalam gelas beaker 250 ml. Ditambahkan 5 gram arang aktif batubara yang komersil. Diaduk dengan menggunakan magnetik bar selama 24 jam.Disaring, dan filtrat yang mengandung ion logam Zinkum diukur absorbansinya dengan Spektrofotometer SerapanAtom pada λspesifik 213,9nm. Dilakukan hal yang sama dilakukan untuk variasi waktu 36 jam dan 48 jam.
3.2.6. Penyerapan logam Zinkum pada larutan standar Zinkum 5 mg/Ldengan menggunakan arang aktif batubara yang diaktifasi dan variasi waktu
Sebanyak 25 ml sampel dimasukkan kedalam gelas beaker 250 ml. Ditambahkan 5 gram arang aktif batubara yang diaktifasi dengan HCl 0,3 N. Diaduk dengan menggunakan magnetik bar selama 24 jam. Disaring, dan filtrat yang mengandung ion logam Zinkum diukur absorbansinya dengan Spektrofotometer SerapanAtom pada λspesifik 213,9nm. Dilakukan hal yang sama dilakukan untuk aktifasi arang aktif dengan menggunakan HCl 0,5 N dan HCl 0,7 N serta variasi waktu 36 jam dan 48 jam.
3.2.7. Penyerapan logam Zinkum dari air buangan limbah dengan menggunakan arang aktif batubara komersil dan yang telah diaktifasi
filtrat yang mengandung ion logam Zinkum diukur absorbansinya dengan Spektrofotometer SerapanAtom pada λspesifik 213,9nm. Dilakukan hal yang sama dilakukan untuk arang aktif komersil dan aktifasi arang aktif dengan menggunakan HCl 0,5 N dan HCl 0,7 N.
3.2.5. Pembuatan larutan standar Zinkum (SNI 06 – 6989.7 – 2009)
3.2.5.1. Pembuatan larutan standar zinkum 1000 mg/L
Sebanyak 4,3990 g ZnSO4. 7H2O dimasukkan ke dalam beaker 250 ml lalu
ditambahkan akuades sambil diaduk hingga larut.Dimasukkan ke dalam labu ukur
1.000 mL kemudian ditambahkan akuades sampai garis tanda lalu dihomogenkan.
3.2.5.1 Pembuatan larutan standar zinkum100 mg/L
Sebanyak5ml larutan induk zinkum1000 mg/L dimasukkan kedalam labu takar 50ml
lalu diencerkan dengan akuades sampai garis tanda dan dihomogenkan.
3.2.5.2 Pembuatan larutan standar zinkum 10 mg/L
Sebanyak 5 ml larutan standar zinkum 100 mg/L dimasukkan kedalam labu takar 50
ml lalu diencerkan dengan aquades sampai garis tanda dan dihomogenkan.
3.2.5.3. Pembuatan larutan Seri Standar zinkum0; 0,1;0,5; 1; 1,5; 2 mg/L
Sebanyak0 ml;0,5 ml;2,5 ml;5 ml; 7,5ml dan 10 ml larutanzinkum10mg/Ldimasukkan
masing-masing kedalam labu takar 50 ml lalu diencerkan dengan akuades sampai
garis tanda dan dihomogenkan.
3.2.5.4. Pembuatan Kurva Standar zinkum dan Penentuan Kadar zinkumpada sampel
Larutan blanko diukur absorbansinya dengan menggunakan Spektrofotometer Serapan Atom pada λspesifik 213,9nm. Perlakuan dilakukan sebanyak 3kali. Dilakukan hal
yang sama untuk larutan seri standar zinkum0; 0,1; 0,5; 1; 1,5; 2 mg/L dan larutan
2,5 ml HCl(p)
Dimasukkan ke dalam labu takar 100 mL
Ditambahkan akuades perlahan-lahan melalui dinding tabung sampai garis batas
Diaduk sampai homogen HCl 0,3 N
4 ml HCl(p)
Dimasukkan ke dalam labu takar 100 mL
Ditambahkan akuades perlahan-lahan melalui dinding tabung sampai garis batas
Diaduk sampai homogen HCl 0,5 N
5,8 ml HCl(p)
Dimasukkan ke dalam labu takar 100 mL
Ditambahkan akuades perlahan-lahan melalui dinding tabung sampai garis batas
Diaduk sampai homogen HCl 0,7 N
3.4. Bagan Penelitian
3.4.1 Pembuatan pereaksi HCl
3.4.1.1 Pembuatan HCl 0,3 N
3.4.1.2 Pembuatan HCl 0,5 N
Batubara
Serbuk
Arang aktif Bebas Air
Arang aktif Berwarna Kehijauan
Endapan Filtrat
Arang aktifteraktifasi
3.4.2 Aktifasi Arang Aktif Batubara dengan HCl (Austin, 1996)
Dihaluskan
Diayak menggunakan saringan ukuran partikel ≤ 100 mesh
Ditimbang sebanyak 25 gram Dimasukkan kedalam beaker glass
Dipanaskan didalam tanur pada suhu 300 oC
Dibiarkan hingga suhunya turun Ditambahkan 100 mL HCl0,3N
Dipanaskan diatas hotplate pada suhu 100 oC sambil diaduk dengan magnetik stirer selama 2 jam
Disaring
Dibilas sampai mencapai pH 7
Dipanaskan dalam oven pada suhu 100 oC sampai benar-benar kering
10 ml Sampel
Dimasukkan ke dalam beaker glass Ditambahkan 5 mL HNO3 (p) Diaduk sampai homogen
Hasil
Dipanaskan sampai hampir kering lalu dikeringkan Ditambahkan 50 mL akuades
Dimasukkah kedalam labu ukur 100 mL melalui kertas saring
Ditambahkan akuades sampai garis tanda
25 mL larutan standar Zinkum 5 mg/L
Filtrat
Endapan
Hasil
3.4.3 Preparasi terhadap sampel(SNI 06 – 6989 .7 – 2004)
3.4.4 Penyerapan logam Zinkum padalarutan standar Zinkum 5 mg/L dengan menggunakan arang aktif batubara yang komersil dan variasi waktu
Dimasukkan kedalam gelas Beaker Ditambahkan 5 gram arang aktif komersil
Diaduk dengan menggunakan magnetik stirer selama 24 jam Disaring dengan menggunakan kertas saring Whatman No 40
Diukur absorbansinya dengan menggunakan Spektrofotometer Serapan Atom dengan λspesifik213,9 nm
25 mL sampel
25 mL larutan standar Zinkum 5 mg/L
3.4.5 Penyerapan logam Zinkum padalarutan standar Zinkum 5 mg/L dengan menggunakan arang aktif batubara yang diaktifasi dan variasi waktu
Dimasukkan kedalam gelas Beaker
Ditambahkan 5 gram arang aktif yang diaktifasi HCl 0,3 N Diaduk dengan menggunakan magnetik stirer selama 24 jam Disaring dengan menggunakan kertas saring Whatman No 40
Diukur absorbansinya dengan menggunakan Spektrofotometer Serapan Atom dengan λspesifik213,9 nm
Dilakukan hal yang sama dilakukan untuk aktifasi arang aktif dengan menggunakan HCl 0,5 N dan HCl 0,7 N serta variasi waktu 36 jam dan 48 jam
3.4.6 Penyerapan logam Zinkum pada air buangan limbah dengan menggunakan arang aktif batubara komersil
Dimasukkan kedalam gelas Beaker Ditambahkan 5 gram arang aktif komersil
Diaduk dengan menggunakan magnetik stirer sesuai waktu terbaik
Disaring dengan menggunakan kertas saring Whatman No 40
25 mL sampel
Filtrat
Endapan
Hasil
3.4.7 Penyerapan logam Zinkum pada air buangan limbah dengan menggunakan arang aktif batubara yang telah diaktifasi
Dimasukkan kedalam gelas Beaker
Ditambahkan 5 gram arang aktif yang telah diaktifasi
Diaduk dengan menggunakan magnetik stirer sesuai waktu terbaik
Disaring dengan menggunakan kertas saring Whatman No 40
3.4.8. Pembuatan Kurva Kalibrasi Zinkum (Zn) menggunakan SSA Nyala (SNI06 – 6989.7 – 2009)
Ditambah akuades tepat tanda batas
Ditambah akuades tepat tanda batas
Diatur keasamaan pH 3 Dioptimalkan alat SSA
Mengukur larutan standar Zinkum (Zn)
dengan Nyala pada λ213,9 nm Buat kurva kalibrasi
Pengukuran absorbansi sampel
Larutan standar logam Zinkum (Zn) 1000 mg/L
Larutan standar logamZinkum(Zn) 100 mg/L
Larutan standar Zn konsentrasi 0; 0,1; 0,5; 1; 1,5; 2 mg/L
Hasil
Sebanyak 5 ml dimasukkan Kedalam labu ukur 50 ml
Sebanyak 5 ml masukkan Kedalam labu ukur 50 ml
Larutan standar logam Zinkum (Zn) 10 mg/L
0 ml; 0,5 ml; 2,5 ml; 5 ml; 7,5ml; 10 ml Masing-masing kedalam labu ukur 50 ml 4,3990 g ZnSO4. 7H2O dilarutkan di dalam beaker glass
BAB 4
HASIL PENELITIAN
4.1. Hasil Penelitian
4.1.1. Pengukuran Kandungan Zinkum(Zn)
Kondisi alat Spektrofotometer Serapan Atom (SSA) pada pengukuran
konsentrasi zinkum dapat dilihat pada tabel 4.1.
Tabel 4.1. Kondisi alat SSA Merek Shimadzu tipe AA-6300 pada pengukurankonsentrasi logam Zinkum (Zn)
No Parameter Spesifikasi
1.
Tabel 4.2. Data absorbansi larutan seri standar logam Zinkum (Zn)
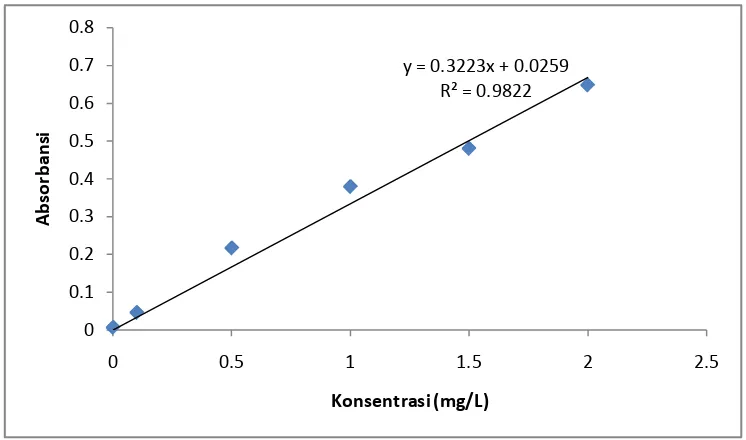
Gambar 4.1. Kurva kalibrasi larutan seri standar Zinkum (Zn)
4.1.2.Penurunan garis regresi dengan Metode Least Square
Hasil pengukuran absorbansi seri larutan standar Zn pada tabel 4.2 diplotkan
terhadap konsentrasi larutan standar sehingga diperoleh suatu kurva kalibrasi berupa
garis linier. Persamaan garis regresi untuk kurva kalibrasi ini dapat diturunkan dengan
metode Least Square dengan data pada tabel 4.2.
Tabel 4.3. Penurunan persamaan garis regresi dengan metode Least Square
Keterangan : xi = Konsentrasi
Persamaan garis regresi untuk kurva kalibrasi dapat diturunkan dari persamaan garis :
y = ax + b
dimana a = slope
b = intersept
Selanjutnya harga slope dapat ditentukan dengan menggunakan metode Least Square
sebagai berikut :
� = ∑(��− �̅)(��− ��) ∑(��− �̅)2 �= �� − ��̅
Dengan mensubtitusikan harga-harga yang tercantum pada tabel 4.9 di atas
makadiperoleh persamaan :
a = 1.0094
3.1750 = 0.3223
b = 0.0259
maka persamaan garis yang diperoleh y = 0.3223x+ 0.0259
4.1.2.1 Perhitungan Koefisien Korelasi
Koefisien korelasi (r) dapat ditentukan sebagai berikut ;
r = ∑(��−�̅)(��−��)
�∑(��−�̅)2∑(��−��)2
= 1.0094
�(3.1750)(0.3244)
4.1.2.2. Penentuan kadar logam Zinkum (Zn)pada penyerapan larutan standar Zn 5 mg/Ldengan menggunakan arang aktif batubara yang komersil dan variasi waktu
Kadar Zn dapat ditentukan dengan menggunakan metode kurva kalibrasi dengan
mensubtitusikan nilai y (absorbansi) yang diperoleh dari hasil pengukuran terhadap
garis regresi dan kurva kalibrasi y = 0.3223x + 0.0259 sehingga diperoleh konsentrasi
Zn.
Untuk penyerapan logam zinkum dengan menggunakan arang aktif batubara yang
komersil selama 24 jam,36 jamdan 48 jam
Tabel 4.4.Hasil pengukuran absorbansi pada sampel larutan standar 5 mg/L
No WaktuPengadukan Absorbansi
(x3-�̅)2= (0.6148 - 0.6106) 2 = 0.0001
Daridatahasilpengukurankadarlogam zinkum (Zn) pada proses penyerapan logam
zinkum pada larutan standar zinkum 5 mg/L dengan menggunakan arang aktif
batubara yang komersil dengan variasi waktu 24 jam ialah sebesar :0.6106 ± 0,0015
mg/L.Perhitungan yang sama dilakukan terhadap penentuan kadar logam Znpada
proses penyerapan logam zinkum pada larutan standar zinkum 5 mg/L dengan
menggunakan arang aktif batubara yang komersil dengan variasi waktu 36 jam dan 48
jam. Data selengkapnya pada tabel 4.5.
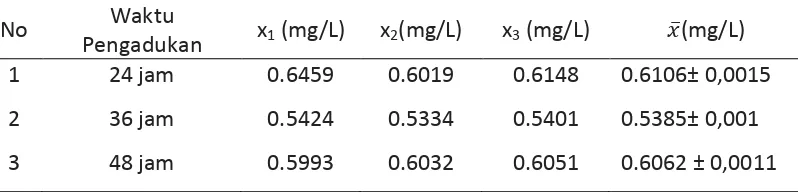
Tabel 4.5. Hasilpengukuran kadar logamZinkum (Zn)
No Waktu
Pengadukan x1 (mg/L) x2(mg/L) x3 (mg/L) �̅(mg/L)
1 24 jam 0.6459 0.6019 0.6148 0.6106± 0,0015
2 36 jam 0.5424 0.5334 0.5401 0.5385± 0,001
3 48 jam 0.5993 0.6032 0.6051 0.6062 ± 0,0011
4.1.2.3 Penentuan kadar logam Zinkum (Zn)pada penyerapan larutan standar Zn 5 mg/L dengan menggunakan arang aktif batubara yang diaktifasi dan variasi waktu
Kadar Zn dapat ditentukan dengan menggunakan metode kurva kalibrasi dengan
garis regresi dan kurva kalibrasi y = 0.3223x + 0.0259 sehingga diperoleh konsentrasi
Zn.
Untuk penyerapan logam zinkum menggunakan arang aktif batubara yang diaktifasi
menggunakan HCl 0,3 N dengan proses pengadukan selama 24 jam
Tabel 4.6.Hasil pengukuran absorbansi pada sampel larutan standar 5 mg/L
�̅=0.1288 mg/L
Daridatahasilpengukurankadar logam zinkum (Zn) pada proses penyerapan logam
zinkum pada larutan standar zinkum 5 mg/L dengan menggunakan arang aktif
batubara yang diaktifasi menggunakan HCl 0.3 N dengan proses pengadukan selama
24 jam ialah sebesar : 0.1288 ± 0,0040 mg/L.Perhitungan yang sama dilakukan
terhadap penentuan kadar logam Znpada proses penyerapan logam zinkum pada
larutan standar zinkum 5 mg/L dengan menggunakan arang aktif batubara yang
diaktifasi menggunakan HCl 0.5 N dan HCl 0.7 N dengan proses pengadukan selama
36 jam dan 48 jam. Data selengkapnya pada tabel 4.7.
Tabel 4.7. Hasilpengukuran konsentrasi logamZinkum (Zn)
Penga-II 36 jam 0.0004 0.0008 0.0009 0.0006 ± 0,0001
III 48 jam 0.0725 0.0745 0.0748 0.0738 ± 0,0012
4.1.2.4. Penentuan kadarlogam Zinkum (Zn)pada air buangan limbah dengan menggunakan arang aktif batubara yang komersil dan yang telah diaktifasi
Kadar Zn dapat ditentukan dengan menggunakan metode kurva kalibrasi dengan
mensubtitusikan nilai y (absorbansi) yang diperoleh dari hasil pengukuran terhadap
garis regresi dan kurva kalibrasi y = 0.3223x + 0.0259 sehingga diperoleh konsentrasi
Zn.
Untuk penyerapan logam zinkum dengan menggunakan arang aktif batubara yang
komersil selama 36 jam
Tabel 4.8. Hasil pengukuran absorbansi pada sampel air buangan limbah
x2 = 0.4297 mg/L
Daridatahasilpengukurankadar logam zinkum (Zn) pada proses penyerapan logam
zinkum pada air buangan limbah dengan menggunakan arang aktif batubara yang
komersil dengan waktu 36 jam ialah sebesar :0.4291 ± 0.0057 mg/L.Perhitungan yang
sama dilakukan terhadap penentuan kadar logam Znpada proses penyerapan logam
zinkum pada air buangan limbah dengan menggunakan arang aktif batubara yang
diaktifasi dengan HCl 0.5 N dengan waktu 36 jam. Data selengkapnya pada tabel 4.9.
Tabel 4.9. Hasilpengukuran kadar logamZinkum (Zn)
3 0.5 N 36 jam 0.4275 0.4297 0.4304 10 4.2910 ±
0,0057
4.1.2.5. Persentase penurunan konsentrasi logam Zinkum (Zn) terhadap larutan standar Zn 5 mg/L dan sampel air buangan limbah
Dari data diatas dapat ditentukan persentase (%) penurunan konsentrasi logam Zinkum
(Zn) dengan menggunakan rumus :
������ (%)����������= ( ��������������� − �������������ℎ��)
��������������� � 100%
Maka persentase (%) penurunan konsentrasi logam Zinkum (Zn) dalam larutan standar
setelah penambahan arang aktif batubara yang komersil dan variasi waktu adalah :
Untuk arang aktif batubara yang komersil dengan waktu penyerapan 24 jam
������ (%)����������� = ( 5−0.6106)��/�
5 ��/� � 100%
= 87.78 %
Dengan cara yang sama dapat dihitung persentase (%) penurunan konsentrasi logam
Zinkum (Zn) dalam larutan standar setelah penambahan arang aktif batubara yang
diaktifasi. Data selengkapnya pada tabel 4.10 ; 4.11 dan 4.12.
Tabel 4.10. Data persentase (%) penurunan konsentrasi logam Zinkum dalam larutan standar setelah penambahan arang aktif batubara komersil dengan variasi waktu penyerapan.
Tabel 4.11. Data persentase (%) penurunan konsentrasi logam Zinkum dalam larutan standar setelah penambahan arang aktif batubara yang diaktifasi dengan variasi waktu penyerapan.
No
Penga-Tabel 4.12. Data persentase (%) penurunan konsentrasi logam Zinkum dalam sampel air buangan limbah setelah penambahan arang aktif batubara dengan variasi waktu penyerapan.
No Konsentrasi
HCl
Waktu Penyerapan
Konsentrasi (mg/L) Persentase (%)
4.2. Pembahasan
Penentuan konsentrasi logam Zinkum (Zn) dalam larutan standar dan air buangan limbah pabrik benang karet sebelum dan setelah penambahan arang aktif batubara komersil dan yang diaktifasi dengan variasi tertentu serta variasi waktu penyerapan dilakukan dengan mengukur nilai absorbansi dan konsentrasi dari larutan sampel tersebut menggunakan alat Spektrofotometer Serapan Atom pada panjang gelombang tertentu. Konsentrasi larutan standar sebelum penambahan arang aktif batubara komersil yang dapat dibandingkan dengan arang aktif batubara yang telah diaktifasi menggunakan konsentrasi HCl tertentu.Kemudian ditentukan persentase (%) penurunan konsentrasi tersebut. Dari hasil yang terbaik penurunannya akan digunakan terhadap air buangan limbah pabrik benang karet baik arang aktif yang komersil maupun yang telah diaktifasi.
Pada hasil penelitian ini diperoleh pada penyerapan larutan standar Zn 5 mg/L dengan menggunakan adsorben arang aktif yang berasal dari batubara komersil dengan variasi waktu penyerapanterhadap larutan standar selama 24 jam, 36 jam dan 48 jam yaitu untuk waktu 24 jam sebesar 0.6106 ± 0.0015 mg/L dengan persentase sebesar
87.78 %. Dengan waktu 36 jam sebesar 0.5385± 0.001 mg/L dengan persentase
sebesar 89.23 %. Dengan waktu 48 jam sebesar 0.6062 ± 0.0011 mg/L dengan
persentase sebesar 87.87 %(Tabel 4.10).
Sedangkan dengan menggunakan adsorben arang aktif berasal dari batubara
yang diaktifasi larutan HCl variasi konsentrasi 0.3 N, 0.5 N dan 0.7 N dengan variasi waktu penyerapan terhadap larutan standar selama 24 jam, 36 jam dan 48 jam yaitu untuk aktifasi menggunakan 0.3 N dengan waktu 24 jam sebesar 0.1288 ± 0.0040 mg/L dengan persentase sebesar 97.42%. Dengan waktu 36 jamsebesar 0.1436 ±
0.0009 mg/L dengan persentase sebesar 97.12 %. Dengan waktu 48 jam sebesar
0.0400 ± 0.0013 mg/L dengan persentase sebesar 92 %. Untuk aktifasi menggunakan
0.5 N dengan waktu 24 jam sebesar 0.3486 ± 0.0014 mg/L dengan persentase sebesar 93.02%. Dengan waktu 36 jam sebesar 0.0063 ± 0.0002 mg/L dengan persentase
persentase sebesar 98.85 %. Untuk aktifasi menggunakan 0.7 N dengan waktu 24 jam sebesar 0.0825± 0.0002 mg/L dengan persentase sebesar 98.35%. Dengan waktu 36 jam sebesar 0.0006 ± 0.0001 mg/L dengan persentase sebesar 99,80 %. Dengan waktu
48 jam sebesar 0.0738 ± 0.0012 mg/L dengan persentase sebesar 98.52 % (Tabel
4.11).
Dari hasil yang diperoleh maka yang paling baik digunakan adalah arang aktif batubara yang diaktifasi dengan menggunakan HCl 0.5 N dengan waktu penyerapan selama 36 jam. Maka arang aktif tersebut akan digunakan untuk menyerap logam Zn yang terdapat pada air buangan limbah pabrik sarung tangan.
Kadar logam Zinkum (Zn) yang terdapat pada sampel air buangan limbah adalah sekitar 62.2168 ± 0.0001 mg/L. Setelah dilakukan proses penyerapan terhadap air limbah tersebut dengan menggunakan arang aktif batubara komersil dan waktu penyerapan 36 jam diperoleh penurunan konsentrasi logam Zn menjadi 8.2204 ± 0.0040 mg/L dengan persentase sebesar 86.78 %. Sedangkan dengan menggunakan arang aktif batubara aktifasi HCl 0.5 N waktu penyerapan selama 36 jam diperoleh penurunan konsentrasi menjadi 4.2910 ± 0.0057 mg/L dengan persentase 92.78 % (Tabel 4.12).
BAB 5
KESIMPULAN DAN SARAN
5.1. Kesimpulan
Dari data yang diperoleh pada penelitian ini, maka dapat disimpulkan bahwa :
1. Pada arang aktif batubara komersil diperoleh hasil yang terbaik dengan waktu
penyerapan selama 36 jam diperoleh penurunan konsentrasi sebesar 86.23 %
terhadap larutan standar Zinkum (Zn). Sedangkan larutan HCl 0.5 N paling
baik digunakan sebagai aktifator arang aktif batubara dengan waktu
penyerapan selama 36 jam, yang mampu menyerap logam Zinkum (Zn) sebesar
99,87 % terhadap larutan standar Zinkum (Zn).
2. Pada air limbah buangan pabrik industri benang karet diperoleh konsentrasi
awal logam zinkum (Zn) sebesar 62.2168 ± 0.0001 mg/L. Setelah dilakukan
proses penyerapan terhadap air limbah tersebut dengan menggunakan arang
aktif batubara komersil dan waktu penyerapan 36 jam diperoleh penurunan
konsentrasi logam Zn menjadi 8.2204 ± 0.0040 mg/L dengan persentase
sebesar 86.78 %. Sedangkan dengan menggunakan arang aktif batubara aktifasi
HCl 0.5 N waktu penyerapan selama 36 jam diperoleh penurunan konsentrasi
menjadi 4.2910 ± 0.0057 mg/L dengan persentase 92.78 %. Dari data yang
diperoleh bahwa penggunaan arang aktif batubara baik yang komersil maupun yang diaktifasi sangat baik menurunkan kadar logam Zinkum (Zn) pada air buangan limbah pabrik benang karet sebelum dibuang ke sungai tidak melebihi ambang batas sesuai dengan KEP-51/MENLH/10/1995 sebesar 5 – 10 mg/L.
5.2.Saran
Perlu dilakukan penelitian lebih lanjut terhadap batubara sebagai adsorben
masih dapat dilakukan pemurnian kembali atau digunakan untuk penyerapan logam
DAFTAR PUSTAKA
Anderson, R 1987, Sample Preatreatment&Seperation, John Wily & SonsNewYork. Austin, G. T. 1996. Industri Proses Kimia.Jilid 1.Edisi 5. Jakarta: Erlangga.
Basset, J, Denny. RC,Jeffery, B. H dan MenhaniJ., 1994,Buku ajar Vogel Kimia Analitik Kuantitatif Anorganik, Edisi ke empat. TerjemahanPudjaatmaka Jakarta: EGC
Bernasconi, G.1995. Teknologi Kimia. Jakarta: PT Pradnya Pramita
Badan Standarisasi Nasional,2009, SNI 06-6989.7-2009: Cara Uji Kadar Zinkum (Zn) dengan Spektrofotometri Serapan Atom (SSA), hal 1-13.
Chrisman, A. 2008.Preparasi Karbon Aktif.Tesis.Universitas Indonesia.
Darmono. 1995. Logam dalam Sistem Biologi Makhluk Hidup. Jakarta: UI Press. Davidson, R.J., 1974, The Mechanism of Gold Adsorption on Activated Charcoal,
Journal of the South African Institute of Mining And Metallurgy, South African.
Day, R.A. Jr, Underwood, A.L., 1988, Analisa Kimia Kuantitatif, Erlangga, Jakarta. Haris.DC.AndDaniel, 1978, Quantitative Chemical Analysis, W. H. Freeman.
Andcompany. New. York
Khopkar, SM, 2002, Konsep Ilmu Dasar Kimia. UI Pres Jakarta.
Krauss.E.H., 1959. Mineralogy an Introduction to the Study of Minerals and Cristal.The Maple Press Company, New York.
Kurniawan, A.R., 2012, Efisiensi Adsorpsi Untuk Air Limbah Pewarnaan Jeans Menggunakan Batubara Dengan Pilot Plant Kolom Vertikal, Institut Teknologi Sepuluh Nopember, Surabaya.
Laksana, A.B., 2011. Tingkatan Batubara. Jilid I, Trimedya Citra, Jakarta.
Manahan, S. E., 1994, Environmental Chemistry, Sixth Edition, LewisPublishers, United State of America.
Mulja.M, 1995,Analisis Instrumental, Surabaya ; Airlangga University
Notohadiprawiro, T. 1993. Logam Beratdalam Pertanian Diakses tanggal 20 Desember 2010
Putri, M., 2008.Abu Terbang Batubara Sebagai Adsorben. Majari Magazine, Jakarta. Ridwan, M. Hrp., 2008. Penurunan Kadar Logam Seng Pada Air Limbah PT. Industri
Karet Nusantara Dengan Metode Elektrokoagulasi, USU Library, Medan. Sounndarrajan, M., et all., 2012. Adsorptive Removal of Chromium (IV) From Aqueous
Srihapsari,2006.Penggunaan Zeolit Alam yang Telah Diaktivasi Dengan Larutan HCl untuk Menjerap Logam-Logam Penyebab Kesadahan Air.Univesitas Negeri Semarang
Sugiharto. 1997. Dasar-Dasar Pengolahan Air Limbah. Cetakan Pertama. Jakarta: UI Press
Sukandarrumidi. 2006. Batubara dan Pemanfaatannya. Yogyakarta: Gajah Mada Universit Press.
Tryana, M. 2003. Arang Aktif (Pengenalan dan Proses Pembuatannya). USU Digital Library. Medan
Walsh,A,1995. Application of Atomic Absorption Spectra to Chemical Analysis,
LAMPIRAN
Gambar 2. Serbuk Batubara komersil
Gambar 3. Serbuk Batubara 100 mesh
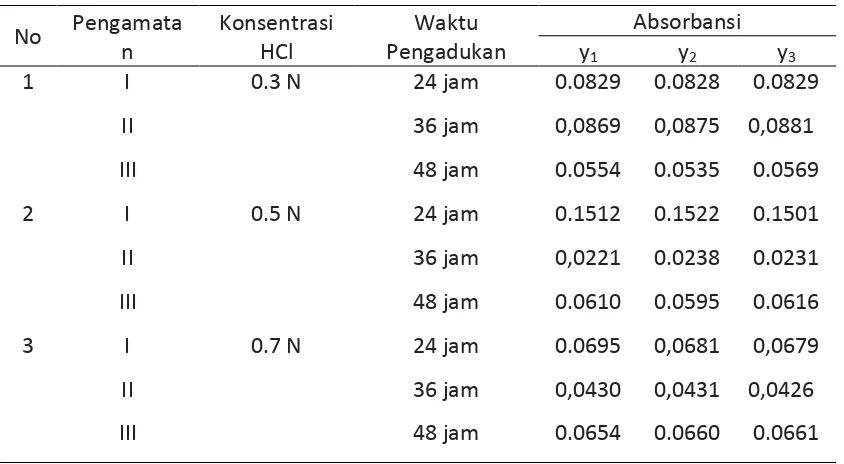
Tabel 2. Hasil pengukuran absorbansi pada sampel air buangan limbah
Tabel 3. Hasilpengukuran kadar logamZinkum (Zn)Minggu I
No Konsentrasi
Tabel 4. Hasil pengukuran absorbansi pada sampel air buangan limbah