viii
UJI TOKSISITAS SUBKRONIS INFUSA DAUN SIRSAK (Annonae
muricatae folium) TERHADAP ORGAN HATI DAN KADAR SGPT TIKUS
PUTIH JANTAN DAN BETINA Meita Eryanti
Fakultas Farmasi Universitas Sanata Dharma Yogyakarta
Intisari
Daun sirsak banyak dimanfaatkan untuk mengatasi berbagai penyakit oleh masyarakat dari berbagai negara. Sayangnya, penelitian untuk mengungkapkan keamanan penggunaan infusa daun sirsak masih kurang. Penelitian ini bertujuan untuk mengetahui wujud efek toksik subkronis pada hati dan kadar SGPT akibat konsumsi infusa daun sirsak.
Lima puluh ekor tikus jantan dan betina dibagi secara acak menjadi 5 kelompok, 1 kelompok kontrol, dan 4 kelompok perlakuan dengan dosis 108; 180; 301; dan 503 mg/kgBB selama 30 hari. Pengambilan darah untuk menentukan kadar SGPT dilakukan sebelum diberi perlakuan dan pada hari ke 31. Pada hari ke 31 separuh dari total tikus dikorbankan untuk dibuat preparat histologinya. Lalu dilakukan uji reversibilitas selama 14 hari. Data berupa kadar SGPT dan bobot hati yang didapat kemudian dianalisis dengan one way Annova dan deskripsi histologi hati.
Hasilnya, terjadi perbedaan yang tidak bermakna antara kadar SGPT sebelum dan sesudah perlakuan dan kadar SGPT kontrol dengan kelompok perlakuan. Hasil pemeriksaan histologinya, 2 hewan mengalami degenerasi hidropik dari 50 hewan uji.
Kesimpulannya, tidak terjadi efek toksik pada pemberian infusa daun sirsak selama 30 hari pada hati tikus jantan dan betina galur Sprague dawley
sehingga perlu dilakukan uji toksisitas kronik untuk mengungkap efek toksik yang tidak nampak pada penelitian ini.
Kata kunci: Sirsak, toksisitas, subkronis, SGPT, hati
Abstract
Graviola leaves being used to address in variety of diseases by people from various countries. Unfortunately, studies to reveal the safety of graviola leaves infusion used is still lacking. The study aims to determine the form of subchronic toxicity effects on the liver and SGPT’s levels due to consumption of graviola leaves infusion.
As a result, there was no significant difference between the levels of SGPT before and after treatment and levels of SGPT between the control and the treatment group. The histology examination results, two animals had hydropic degeneration of the 50 animals.
The conclusion is there were no toxic effects on the provision infusion of graviola leaves for 30 days in the liver of male and female rats of Sprague Dawley strain that chronic toxicity tests need to be done to uncover the toxic effects that are not performed in this study.
UJI TOKSISITAS SUBKRONIS INFUSA DAUN SIRSAK (Annonae
muricatae folium) TERHADAP ORGAN HATI DAN KADAR SGPT TIKUS
PUTIH JANTAN DAN BETINA
SKRIPSI
Diajukan untuk Memenuhi Salah Satu Syarat Memperoleh Gelar Sarjana Farmasi (S. Farm)
Program Studi Farmasi
Oleh: Meita Eryanti NIM: 098114026
FAKULTAS FARMASI
UNIVERSITAS SANATA DHARMA YOGYAKARTA
ii
UJI TOKSISITAS SUBKRONIS INFUSA DAUN SIRSAK (Annonae
muricatae folium) TERHADAP ORGAN HATI DAN KADAR SGPT TIKUS
PUTIH JANTAN DAN BETINA
SKRIPSI
Diajukan untuk Memenuhi Salah Satu Syarat Memperoleh Gelar Sarjana Farmasi (S. Farm)
Program Studi Farmasi
Oleh: Meita Eryanti NIM: 098114026
FAKULTAS FARMASI
UNIVERSITAS SANATA DHARMA YOGYAKARTA
iii
Persetujuan Pembimbing
UJI TOKSISITAS SUBKRONIS INFUSA DAUN SIRSAK (ANNONA
MURICATA FOLIUM) TERHADAP ORGAN HATI DAN KADAR SGPT
TIKUS PUTIH JANTAN DAN BETINA
skripsi yang diajukan oleh:
Meita Eryanti NIM: 098114026
telah disetujui oleh
Pembimbing Utama
iv
Pengesahan Skripsi Berjudul
UJI TOKSISITAS SUBKRONIS INFUSA DAUN SIRSAK (ANNONA
MURICATA FOLIUM) TERHADAP ORGAN HATI DAN KADAR SGPT
TIKUS PUTIH JANTAN DAN BETINA
Oleh: Meita Eryanti NIM: 098114026
Dipertahankan dihadapan Panitia Penguji Skripsi Fakultas Farmasi
Universitas Sanata Dharma Pada tanggal: 10 Januari 2013
Mengetahui Fakultas Farmasi Universitas Sanata Dharma Dekan
Ipang Djunarko, M.Sc, Apt. Pembimbing:
Phebe Hendra, M.Si, PhD, Apt. Tim Penguji:
1. Phebe Hendra M.Si, PhD, Apt. ……….
2. Ipang Djunarko, M.Sc, Apt ……….
v
That is what alchemists do. They show that, when we strive to become
better than we are, everything around us becomes better, too.
vi
PERNYATAAN KEASLIAN KARYA
Saya menyatakan dengan sesungguhnya bahwa skripsi yang saya tulis ini tidak memuat karya atau bagian karya orang lain, kecuali yang disebutkan dalam kutipan dan daftar pustaka, sebagaimana layaknya karya ilmiah.
Apabila di kemudian hari ditemukan indikasi plagiarism dalam naskah ini, maka saya bersedia menanggung segala sanksi sesuai peraturan perundang-undangan yang berlaku
.
Yogyakarta, 10 Januari 2013 Penulis,
viii
UJI TOKSISITAS SUBKRONIS INFUSA DAUN SIRSAK (Annonae
muricatae folium) TERHADAP ORGAN HATI DAN KADAR SGPT TIKUS
PUTIH JANTAN DAN BETINA Meita Eryanti
Fakultas Farmasi Universitas Sanata Dharma Yogyakarta
Intisari
Daun sirsak banyak dimanfaatkan untuk mengatasi berbagai penyakit oleh masyarakat dari berbagai negara. Sayangnya, penelitian untuk mengungkapkan keamanan penggunaan infusa daun sirsak masih kurang. Penelitian ini bertujuan untuk mengetahui wujud efek toksik subkronis pada hati dan kadar SGPT akibat konsumsi infusa daun sirsak.
Lima puluh ekor tikus jantan dan betina dibagi secara acak menjadi 5 kelompok, 1 kelompok kontrol, dan 4 kelompok perlakuan dengan dosis 108; 180; 301; dan 503 mg/kgBB selama 30 hari. Pengambilan darah untuk menentukan kadar SGPT dilakukan sebelum diberi perlakuan dan pada hari ke 31. Pada hari ke 31 separuh dari total tikus dikorbankan untuk dibuat preparat histologinya. Lalu dilakukan uji reversibilitas selama 14 hari. Data berupa kadar SGPT dan bobot hati yang didapat kemudian dianalisis dengan one way Annova dan deskripsi histologi hati.
Hasilnya, terjadi perbedaan yang tidak bermakna antara kadar SGPT sebelum dan sesudah perlakuan dan kadar SGPT kontrol dengan kelompok perlakuan. Hasil pemeriksaan histologinya, 2 hewan mengalami degenerasi hidropik dari 50 hewan uji.
Kesimpulannya, tidak terjadi efek toksik pada pemberian infusa daun sirsak selama 30 hari pada hati tikus jantan dan betina galur Sprague dawley
sehingga perlu dilakukan uji toksisitas kronik untuk mengungkap efek toksik yang tidak nampak pada penelitian ini.
Kata kunci: Sirsak, toksisitas, subkronis, SGPT, hati
Abstract
Graviola leaves being used to address in variety of diseases by people from various countries. Unfortunately, studies to reveal the safety of graviola leaves infusion used is still lacking. The study aims to determine the form of subchronic toxicity effects on the liver and SGPT’s levels due to consumption of graviola leaves infusion.
As a result, there was no significant difference between the levels of SGPT before and after treatment and levels of SGPT between the control and the treatment group. The histology examination results, two animals had hydropic degeneration of the 50 animals.
The conclusion is there were no toxic effects on the provision infusion of graviola leaves for 30 days in the liver of male and female rats of Sprague Dawley strain that chronic toxicity tests need to be done to uncover the toxic effects that are not performed in this study.
ix
ditemukannya senyawa acetogenin dalam daun sirsak oleh Mc Laughin pada tahun 1995 (Mc Laughin, Liau, and Alali, 1999) yang dapat berfungsi membunuh sel kanker, daun sirsak kemudian booming digunakan dalam terapi antikanker baik sebagai penyembuh maupun sebagai pencegah bahkan banyak dokter yang mulai menyarankan pengkonsumsiannya setiap hari untuk menjaga kesehatan (Duryatmo, 2011).
x
pembuatannya maka penelitian ini menggunakan infusa yang memiliki patokan baku pembuatannya dan serupa dengan rebusan. Pengujian dilakukan pada organ hati karena organ hati merupakan organ utama metabolisme zat zat yang masuk dalam tubuh.
Berdasarkan latar belakang tersebut, permasalahan yang akan diteliti adalah a. Seperti apa wujud biokimia efek toksik pada SGPT dan wujud struktural
efek toksik infusa daun sirsak pada histologi organ hati pada uji toksisitas subkronis?
b. Apakah spektrum efek toksik senyawa uji tersebut berkaitan dengan
takaran dosis?
c. Adakah keterbalikan spektrum efek toksik yang terjadi?
Bahan, Alat, dan Cara Penelitian
1. Subjek uji yang digunakan adalah tikus putih galur Sprague Dawley jantan dan betina, berusia 2 – 2,5 bulan, berat badan 170 – 280 gram, yang diperoleh dari laboratorium Hayati Imono Fakultas Farmasi Universitas Sanata Dharma. 2. Bahan uji yang digunakan adalah daun sirsak dalam kondisi dewasa dan segar
berwarna hijau tua, dan diperoleh dari kebun milik H.Sunarto di dusun Jetis Baran, Sardonoharjo, Ngaglik, Sleman, Provinsi Daerah Istimewa Yogyakarta pada bulan Mei - Juni 2012.
xi
oleh Laboratorium Patologi Fakultas Kedokteran Hewan Universitas Gadjah Mada.
4. Bahan yang digunakan sebagai kontrol adalah aquadest yang diperoleh dari Laboratorium Farmakognosi Fitokimia, Fakultas Farmasi, Universitas Sanata Dharma, Yogyakarta.
Alat penelitian yang digunakan adalah jarum suntik peroral, spuit injeksi, seperangkat alat bedah, alat alat gelas (Pyrex), timbangan (analytical balance), blender, ayakan, mikroskop, kamera digital, metabolic cage, panci infusa yang didapat di laboratorium Farmakognosi Fitokimia dan laboratorium Farmakologi Toksikologi Fakultas Farmasi Universitas Sanata Dharma.
Cara Penelitian dalam penelitian ini adalah sebagai berikut:
a. Pembuatan serbuk daun sirsak
Sejumlah daun sirsak dicuci dan dikeringkan dalam oven selama 3 hari pada suhu ± 470C. Kemudian daun diblender hingga menjadi serbuk halus. Setelah itu serbuk diayak dengan ayakan no.40.
b. Penetapan kadar air daun sirsak kering
xii
toluene. Toluena juga dituang dalam tabung penerima melalui alat pendingin. Selanjutnya labu dipanaskan selama 15 menit.
Ketika toluene mulai mendidih, penyulingan dilakukan dengan kecepatan 2 tetes perdetik hingga sebagian besar air tersuling, lalu kecepatan penyulingan dinaikkan hingga 4 tetes per detik. Setelah semua air tersuling, bagian dalam pendingin dicuci dengan toluene sambil dibersihkan. Setelah air dan toluene memisah sempurna, volume air dibaca dan ditetapkan kadarnya dalam persen.
c. Penetapan dosis daun sirsak
Penentuan kisaran dosis untuk uji pendahuluan ini didasarkan pada pengobatan yang digunakan dalam masyarakat yaitu 2 gram serbuk yang kemudian dicampur 100 ml dan direbus kemudian diminum air rebusannya. 2 gram serbuk daun sirsak untuk manusia 70 kg.
Selanjutnya dilakukan orientasi konsentrasi tertinggi infusa daun sirsak yang dapat dibuat. Hasilnya, konsentrasi tertinggi yang dapat dibuat adalah 6 gram/ 100 ml (6% b/v). Sehingga peringkat dosisnya adalah Dosis I = 108 mg/kg BB; Dosis II = 180 mg/kg BB; Dosis III = 301 mg/kg BB dan Dosis IV = 503 mg/kg BB.
d. Pembuatan infusa daun sirsak
xiii
aquadest panas yang dilewatkan pada ampas serbuk hingga volumenya kembali menjadi 150 ml. Sembilan gram serbuk daun sirsak dalam 150 ml air setara dengan 6g serbuk daun sirsak dalam 100 ml aquadest (6% b/v) yang merupakan konsentrasi tertinggi yang dapat dibuat berdasarkan hasil orientasi. e. Pengelompokan dan perlakuan hewan uji
Lima puluh ekor tikus yang terdiri dari tikus jantan dan betina masing-masing 25 ekor, dibagi secara acak menjadi 5 kelompok perlakuan (masing-masing 10 tikus: 5 jantan dan 5 betina). Kelompok I adalah kelompok kontrol negatif dengan perlakuan aquadest, kelompok II – V adalah kelompok perlakuan dengan peringkat dosis berturut turut 108, 180, 301, dan 504 mg/kg BB secara peroral dengan kekerapan sekali sehari selama 30 hari.
Semua tikus pada kelompok I – V pada hari ke nol diambil darahnya melalui sinus orbitalis mata. Masing-masing cuplikan darah diambil serumnya dan ditetapkan kadar SGPT (Serum Glutamic Pyruvic Transaminase) nya secara spektrofotometri. Pada hari ke 31 semua tikus dilakukan pengambilan darah untuk penentuan kadar SGPT dan separuh dari total tikus dikorbankan untuk dibuat preparat histopatologisnya untuk organ hati. Pada hari ke 31 sampai dengan hari ke 44 tikus diberi pakan dan minuman (tanpa perlakuan sediaan uji), lalu pada hari ke 45, sisa tikus dikorbankan dan kemudian dibuat preparat histopatologisnya untuk organ hati sebagai uji reversibilitas. Parameter lainnya yang diamati berupa gejala klinis, berat badan, konsumsi pakan, dan konsumsi minum yang diamati setiap hari.
xiv
Data histologi organ dideskripsikan secara kualitatif. Untuk data berat badan, asupan makanan, asupan minuman, dan hasil pemeriksaan SGPT dilakukan analisis dengan Kolmogorov- Smirnov (K-S) untuk melihat data terdistribusi normal atau tidak. Hasil K-S menunjukkan bahwa data
terdistribusi normal jika nilai signifikansi (α) > 0,05. Selanjutnya dilakukan uji
homogenitas untuk mengetahui homogenitas varian. Data dikatakan homogen
jika α > 0,01. Jika varian homogen, maka dilakukan uji Dunnet untuk
mengetahui perbedaan antara kelompok kontrol dengan kelompok perlakuan. Terdapat perbedaan jika nilai F < 0,05. Untuk membandingkan data sebelum dan sesudah perlakuan digunakan metode analisis Paired samples T-test.
Jika data tidak terdistribusi normal, maka dilakukan analisis nonparametrik
Kruskal Wallis (K-W). Data dikatakan berbeda bermakna jika signifikansi kurang dari 0,05. Untuk mengetahui perbedaan antar kelompok, dilakukan analisis dengan Mann-Whitney U. Jika signifikansi kurang dari 0,05 maka dikatakan terdapat perbedaan bermakna antar kelompok uji. Pengujian statistik uji Kolmogorov- Smirnov, uji homogenitas, uji Dunnet, uji Kruskal Wallis, dan uji Mann-Whitney U menggunakan program Assistat 7.6 Beta. Sedangkan uji paired samples T-test menggunakan Microsoft Excel 2007.
Hasil dan Pembahasan
1. Pembuatan Sediaan Uji
xv
Sehingga, didapat rendemen sebesar 22,5%. Serbuk tersebut kemudian ditetapkan kadar airnya dengan destilasi toluene hasilnya didapat kadar 9,7%. Kadar tersebut masih dibawah dari kadar air dalam simplisia yang ditetapkan oleh Departemen Kesehatan dalam Materia Medika Indonesia (1995) yaitu 10%.
2. Perkembangan Berat Badan Tikus
Rata-rata berat badan tikus jantan dan betina terlihat pada gambar 1 dan gambar 2.
Gambar1. Grafik perkembangan berat badan tikus jantan perhari akibat perlakuan infusa daun sirsak secara subkronis
Keterangan gambar: kontrol=aquadest dosis 503 mg/kg BB; dosis I=108 mg/kg BB; dosis II=180 mg/kg BB; dosis III=301 mg/kg BB, dosis IV=503 mg/kg BB
xvi
Keterangan gambar: kontrol=aquadest dosis 503 mg/kg BB; dosis I=108 mg/kg BB; dosis II=180 mg/kg BB; dosis III=301 mg/kg BB, dosis IV=503 mg/kg BB
Rata-rata perubahan berat badan tikus jantan kemudian diuji normalitasnya dengan uji kolmogorov-smirnov hasilnya, data tidak normal sehingga dilanjutkan dengan uji non-parametrik. Rata-rata tersebut kemudian diuji perbedaannya dengan kelompok kontrol dengan kruskal wallis test. Hasilnya, ke 4 dosis tidak memiliki perbedaan yang bermakna dengan kelompok kontrol.
Tabel I. Rata-rata perubahan berat badan tikus jantan perhari akibat perlakuan infusa daun sirsak secara subkronis
Keterangan: data direpresentasikan dalam mean ± SD
Rata-rata perubahan berat badan tikus betina kemudian diuji normalitasnya dengan uji kolmogorov-smirnov hasilnya, data tidak normal sehingga dilanjutkan dengan uji non-parametrik. Rata-rata tersebut kemudian diuji perbedaannya dengan kelompok kontrol dengan kruskal wallis test. Hasilnya, ke 4 dosis tidak memiliki perbedaan yang bermakna dengan kelompok kontrol.
xvii
Keterangan: data direpresentasikan dalam mean ± SD
3. Asupan Makanan Perhari
Rata-rata asupan makanan diuji normalitasnya dengan uji Kolmogorov-Smirnov hasilnya, data tersebut terdistribusi secara normal. Rata-rata tersebut kemudian diuji perbedaannya dengan kelompok kontrol dengan Dunnet test. Hasilnya, ada perbedaan yang bermakna dari keempat dosis terhadap kontrol.
Tabel III. Tabel rata-rata asupan makanan tikus jantan selama 30 hari pemberian infusa daun sirsak
Keterangan: data direpresentasikan dalam mean ± SD
Rata-rata pola makan tikus betina perharinya diuji normalitasnya dengan uji kolmogorov-Smirnov dan hasilnya data terdistribusi secara normal. Kemudian diuji homogenitasnya hasilnya data tersebut homogen. Lalu diuji perbedaannya dengan kelompok kontrol dengan dunnet test. Hasilnya, terdapat perbedaan yang tidak bermakna dengan kelompok kontrol.
Tabel IV. Tabel rata-rata asupan makanan tikus betina tiap hari selama 30 hari pemberian infusa daun sirsak
Dosis Rata-rata asupan makanan selama 30 hari (g)
xviii
Keterangan: data direpresentasikan dalam mean ± SD
4. Asupan minuman perhari
Rata-rata asupan minuman tikus jantan diuji normalitasnya dengan uji Kolmogorov-Smirnov hasilnya, data tersebut terdistribusi tidak normal maka untuk mengetahui perbedaannya digunakan uji kruskal Wallis hasilnya antara dosis dan kontrol berbeda tidak bermakna.
Tabel V. rata-rata asupan minuman tikus jantan selama 30 hari pemberian infusa daun sirsak
Keterangan: data direpresentasikan dalam mean ± SD
Rata-rata asupan minuman tikus betina juga diuji normalitasnya dengan uji kolmogorov-Smirnov hasilnya data terdistribusi secara normal. Data lalu diuji homogenitasnya dan hasilnya data tersebut homogen. Data kelompok kontrol kemudian diuji perbedaannya dengan kelompok perlakuan dengan dunnet test.
xix
Tabel VI. Rata-rata asupan minuman tikus betina selama 30 hari pemberian infusa daun sirsak (mean ±SD)
Untuk menginterpretasi adanya kerusakan sel hati, pada penelitian ini dilakukan pengukuran kadar SGPT dalam serum. Kenaikan jumlah SGPT biasanya menunjukkan adanya kerusakan hati seperti nekrosis, sirosis, dan neoplasma.
Tabel VII. Hasil pemeriksaan SGPT hewan uji jantan sebelum dan sesudah 30 hari perlakuan infusa daun sirsak Hasil uji T: tb = tidak bermakna (blia hasil uji> 0,05)
b = bermakna
perubahan - = terjadi penurunan kadar + = terjadi peningkatan kadar
xx Infusa daun sirsak dosis
301 mg/kg BB
53,5 ± 11,8 66,2 ± 5,1 12,7 0.057(tb)
Infusa daun sirsak dosis 503 mg/kg BB
47,8 ± 3,4 56,2 ± 10,3 8,9 0.049(b)
Keterangan: data direpresentasikan dalam mean ± SD Hasil uji T: tb = tidak bermakna (blia hasil uji> 0,05)
b = bermakna
Sebelum perlakuan, tikus diambil darahnya untuk diperiksa SGPT . Nilai SGPT normal untuk tikus adalah 10 – 50 IU/L (Derelanko and Holinger, 1995). Data hasil kemudian diuji normalitasnya dan homogenitasnya. Hasilnya, data tersebut normal dan homogen. Angka angka tersebut berbeda secara tidak signifikan secara statistika melalui tukey test sehingga dapat dikatakan bahwa semua tikus memiliki awal yang sama sebelum dilakukan perlakuan.
Setelah 30 hari perlakuan, tikus kembali diambil darahnya untuk kembali dilakukan pemeriksaan SGPT. Selanjutnya dilakukan Paired-samples T Test
untuk mengetahui ada tidaknya perbedaan bermakna antara sebelum dan sesudah perlakuan selama 30 hari. Hasil uji pada tikus jantan dan betina selama perlakuan dapat dilihat pada tabel VII dan VIII.
xxi
Data dari tikus jantan kemudian diuji normalitas secara statistika. Hasilnya, datanya tidak terdistribusi dengan normal sehingga kemudian diuji secara non parametrik dengan Kruskal Wallis test, hasilnya rata-rata dari kelima kelompok perlakuan berbeda tidak bermakna. Maka dapat disimpulkan bahwa variabel dosis tidak merubah nilai dari SGPT tikus jantan. Data untuk tikus betina kemudian diuji normalitas dan homogenitasnya. Hasil dari kedua uji menyatakan bahwa data terdistribusi normal dan homogen. Kemudian dilakukan dunnet test
untuk mengetahui perbedaan antara kontrol dengan kelompok perlakuan hasilnya rata-ratanya berbeda secara tidak signifikan.
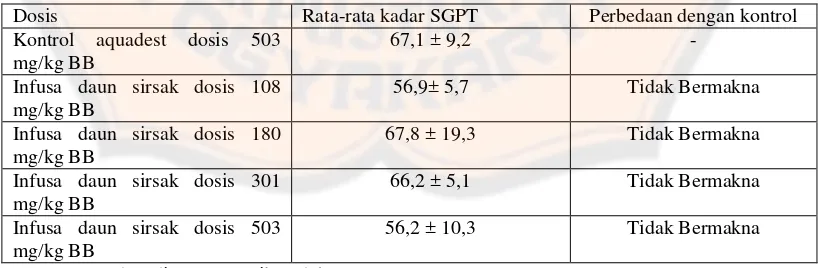
Tabel IX. Rata-rata kadar SGPT tikus jantan setelah 30 hari pemberian infusa daun sirsak
Dosis Rata-rata kadar SGPT Perbedaan dengan kontrol Kontrol aquadest dosis 503
Keterangan: data direpresentasikan dalam mean ± SD
Tabel X. Rata-rata kadar SGPT tikus betina setelah 30 hari pemberian infusa daun sirsak
Dosis Rata-rata kadar SGPT Perbedaan dengan kontrol Kontrol aquadest dosis 503
xxii
Dengan demikian, maka dapat disimpulkan jika kadar SGPT tidak mengalami peningkatan setelah diberi perlakuan infusa daun sirsak selama 30 hari dan ada perbedaan yang tidak bermakna antara kelompok kontrol dan perlakuan setelah pemberian infusa daun sirsak.
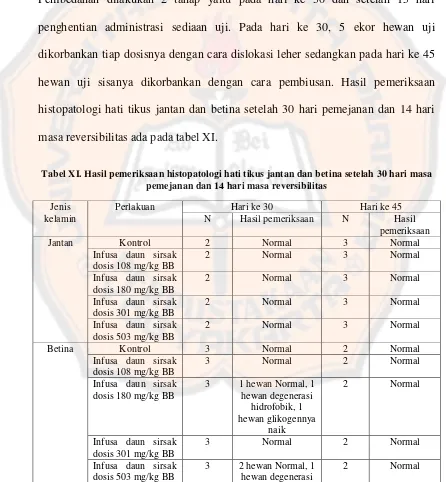
Pada penelitian ini dilakukan pengamatan histologi pada organ hati. Pembedahan dilakukan 2 tahap yaitu pada hari ke 30 dan setelah 15 hari penghentian administrasi sediaan uji. Pada hari ke 30, 5 ekor hewan uji dikorbankan tiap dosisnya dengan cara dislokasi leher sedangkan pada hari ke 45 hewan uji sisanya dikorbankan dengan cara pembiusan. Hasil pemeriksaan histopatologi hati tikus jantan dan betina setelah 30 hari pemejanan dan 14 hari masa reversibilitas ada pada tabel XI.
xxiii
hidrofobik
Keterangan: Normal = vena sentralis berbentuk lingkaran (agak lonjong) dikelilingi oleh hepatosit yang tersusun radier dengan inti berwarna biru tua. Sinusoid diantara hepatosit dengan sel endotel yang pipih dan gelap.
Pada kontrol, semua hewan uji jantan baik dari kelompok perlakuan maupun kelompok reversibel kondisi histologi hatinya dinyatakan normal. Gambaran hati normalnya tampak seperti pada gambar 3. Pada gambar a nampak lobus berbentuk poligonal, dan pada lobus terdapat vena sentralis. Tampak pula pada gambar b, hepatosit dengan inti sel yang nampak normal begitu juga dengan sinusoid yang juga normal.
a.
b
.
Gambar3. penampakan hati normal. a. perbesaran 100x. b. perbesaran 400x pada kontrol jantan
Keterangan gambar:a. vena centralis b. hepatosit c. sinusoid d. nucleus hepatosit
xxiv
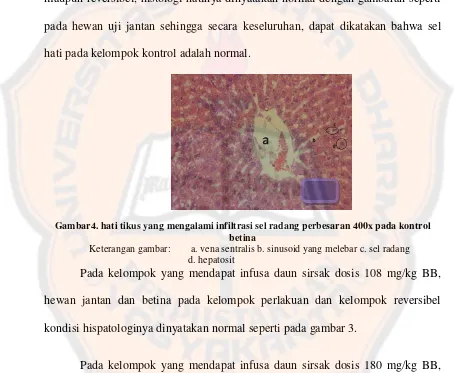
dilakukan dengan dislokasi leher. Pada gambar 4 (perbesaran 400) terlihat jaringan mengalami infiltrasi sel radang disekitar sel retikuloendotelial pada sinusoid dan terlihat sinusoid disekitar vena sentralis melebar akan tetapi hal itu masih dianggap normal karena infasinya tidak melebihi batas normal.
Gambar pada hewan uji yang lain dari kelompok kontrol perlakuan maupun reversibel, histologi hatinya dinyatakan normal dengan gambaran seperti pada hewan uji jantan sehingga secara keseluruhan, dapat dikatakan bahwa sel hati pada kelompok kontrol adalah normal.
Gambar4. hati tikus yang mengalami infiltrasi sel radang perbesaran 400x pada kontrol betina
Keterangan gambar: a. vena sentralis b. sinusoid yang melebar c. sel radang d. hepatosit
Pada kelompok yang mendapat infusa daun sirsak dosis 108 mg/kg BB, hewan jantan dan betina pada kelompok perlakuan dan kelompok reversibel kondisi hispatologinya dinyatakan normal seperti pada gambar 3.
Pada kelompok yang mendapat infusa daun sirsak dosis 180 mg/kg BB, semua hewan uji jantan baik dari kelompok perlakuan maupun kelompok reversibel kondisi histologi hatinya dinyatakan normal (gambar 3 a dan b).
xxv
karena adanya gangguan metabolisme seperti hipoksia dan keracunan bahan kimia yang mempengaruhi sodium channel. Perubahan ini bersifat reversibel. Tampak pembengkakan sel hati sehingga terlihat sitoplasma lebih terang (karena sel mengalami lisis) jika dibandingkan dengan sitoplasma hati normal dan juga batas sel tidak jelas (gambar 5).
Gambar5. hati yang mengalami degenerasi hidropik perbesaran 400x pada dosis 180 mg/kg BB
Keterangan gambar: a. vena sentralis b. nucleus hepatosit c. batas antar sel yang tidak jelas d. hepatosit yang mengalami degenerasi hidrofobik
xxvi
Gambar6. sel mengalami penumpukan jumlah glikogen perbesaran 400x pada dosis 180 mg/kg BB
Keterangan gambar: a. duktus b. hepatosit yang mengalami penumpukan glikogen c. glikogen d. nucleus e. batas antar sel yang tidak jelas
Pada kelompok yang mendapat infusa daun sirsak dosis 301 mg/kg BB, semua hewan uji jantan dan betina baik dari kelompok perlakuan maupun kelompok reversibel gambaran histologi hatinya menunjukkan gambaran normal (gambar 3 a dan b). Pada kelompok yang memperoleh infusa daun sirsak dosis 503 mg/kg BB, semua hewan uji jantan baik dari kelompok perlakuan maupun kelompok reversible kondisi histologi hatinya dinyatakan normal (gambar 3 a dan b). Sedangkan hewan uji betina, terdapat hewan yang mengalami degenerasi hidropik. Tampak pembengkakan sel hati sehingga terlihat sitoplasma lebih terang (karena sel mengalami lisis) jika dibandingkan dengan sitoplasma hati normal dan juga batas sel tidak jelas (gambar 5).
Kesimpulan
xxvii
mg/kg BB. Terjadi keterbalikan efek toksik dari infusa daun sirsak karena pada dosis 180 mg/kg BB dan 503 mg/kg BB kelompok uji reversibilitas semua hewan dinyatakan normal.
Daftar Pustaka
Anonim, 2004, Monograph of Graviola, Raintree nutrition Inc., Carson City. Arthur, F. K. N., Woode, E., Terlabi, E.O., and Larbie, C., 2011, Evaluation of Acute and Subchronic Toxicity of Annona Muricata (Linn.) Aqueous Extract in Animals, Euro. J. Exp. Bio., 1 (4), 115 – 124.
Backer dan Bakhuizen van den Brink, 1963, Flora of Java, vol I, Noordhoflbroningen, Nederlands.
Champy, P., Hoglinger, G.U., Feger, J., Gleye, C., Hocquemiller, R., Laurens, A., et al., 2004, Annonacin, a Lipophilic Inhibitor of Mitochondrial Complex I, Induces Nigral and Striatal Neurodegeneration in Rats: Possible Relevance for Atypical Parkinsonism in Guadeloupe, Journal of Neurochemistry, 88, 63
– 69.
Depkes, 1989, Materia Medika Indonesia, jilid V, Departemen Kesehatan Republik Indonesia, Jakarta, 41.
Depkes, 1995, Materia Medika Indonesia, jilid VI, Departemen Kesehatan Republik Indonesia, Jakarta, 323-324.
Derelanko, M. J., and Holinger, M. A., 1995, Handbook of Toxicology, 2nd edition, CRCpress, USA, 87.
Donatus, I.A., 2001, Toksisitas Dasar, Laboratorium Farmakologi-Toksikologi, Fakultas Farmasi, Universitas Gadjah Mada, 178.
Duryatmo, S., 2011, Dokter Bicara Daun Sirsak, Trubus, 469, 12 – 17. Kaplowitz, N., 2004, Drug-Induced Liver Injury, CID, 38 (2), S44 – S48. Lu, F. C., 1995, Toksikologi Dasar : Asas, Organ Sasaran, dan Penilaian Risiko, Penerbit Universitas Indonesia, Jakarta, 206 – 214.
Timbrell, J. A., 2009, Principles of Biochemical Toxicology, fourth edition, Informa Healthcare, USA, 194 – 200.
Walker, Hall, and Hurst, 1990, Clinical Methods: The History, Physical, and Laboratory Examinations, third edition, Boston, diakses dari
xxviii PRAKATA
Puji syukur penulis panjatkan kepada Tuhan Yang Maha Esa atas anugrah
yang diberikan sehingga penulis dapat menyelesaikan skripsi dengan judul ” Uji Toksisitas Subkronis Infusa Daun Sirsak (Annonae muricatae folium) Terhadap Organ Hati Dan Kadar Sgpt Tikus Putih Jantan Dan Betina“.
Karya tulis ini disusun untuk memenuhi salah satu syarat memperoleh gelar Sarjana Farmasi dan penulis berharap skripsi ini dapat bermanfaat untuk menambah pengetahuan dalam dunia kefarmasian pada umumnya.
Pada kesempatan ini, penulis menyampaikan terima kasih atas segala bantuan yang penulis terima baik secara langsung maupun tidak langsung sehingga penulis dapat menyelesaikan karya tulis ini. Adapun ucapan terimakasih yang tulus hendak penulis ucapkan kepada :
1. Dekan Fakultas Farmasi Universitas Sanata Dharma Yogyakarta.
2. Ibu Phebe Hendra, M.Si., PhD, Apt. selaku dosen pembimbing yang telah memberikan segala waktu dan kesabarannya dalam mendampingi penulis dalam penulisan karya tulis ini.
5. Semua pihak yang tidak dapat disebutkan satu-persatu yang telah mendukung untuk terwujudnya karya tulis ini.
Semoga Tuhan yang Maha Kasih membalas segala budi baik yang telah mendukung penulis sehingga karya tulis ini dapat terselesaikan.
Segala kesempurnaan adalah milik Tuhan. Penulis menyadari bahwa karya tulis ini masih belum sempurna. Oleh karena itu, penulis mengharapkan kritik dan saran yang membangun agar karya ini menjadi lebih baik dan bermanfaat. Penulis juga menyampaikan maaf setulus-tulusnya apabila ada kesalahan dan kata-kata yang kurang berkenan di hati pembaca. Akhir kata, semoga karya tulis ini berguna bagi perkembangan dunia kesehatan pada umumnya dan dunia kefarmasian pada khususnya.
Yogyakarta, 10 Januari 2013
xxix DAFTAR ISI
PERSETUJUAN PEMBIMBING ... III PENGESAHAN SKRIPSI BERJUDUL ... IV PERNYATAAN KEASLIAN KARYA ... VI PRAKATA ... VII DAFTAR ISI ... XXIX DAFTAR TABEL ... XXXIII DAFTAR GAMBAR ... XXXV DAFTAR LAMPIRAN ... XXXVII INTISARI ... XL
ABSTRACT ... XLI BAB I PENGANTAR ... 1
A. Latar Belakang ... 1
1. Permasalahan ... 3
2. Keaslian penelitian ... 3
3. Manfaat penelitian ... 4
B. Tujuan Penelitian ... 4
1. Tujuan umum ... 4
2. Tujuan khusus ... 5
BAB II PENELAAHAN PUSTAKA ... 6
A. Daun Sirsak ... 6
1. Klasifikasi tanaman ... 6
xxx
3. Morfologi daun sirsak ... 7
4. Kandungan kimia daun sirsak ... 7
5. Kegunaan daun sirsak ... 8
6. Toksisitas daun sirsak ... 9
B. Uji Toksisitas Subkronis ... 9
C. Toksisitas Hati ... 11
1. Anatomi dan fisiologi hati ... 13
2. Fungsi hati ... 15
3. Patogenesis kerusakan hati akibat induksi senyawa toksik ... 16
4. Tipe kerusakan hati yang diakibatkan induksi senyawa toksik ... 19
a. Perubahan bobot hati ... 19
b. Perlemakan hati (Steatosis) ... 19
c. Nekrosis hati ... 20
d. Sirosis ... 21
e. Hepatitis kronis aktif ... 21
f. Karsinogenesis ... 22
D. Serum Glutamat Piruvat Transaminase (SGPT) ... 22
E. Keterangan Empiris ... 23
BAB III METODE PENELITIAN ... 24
A. Jenis dan Rancangan Penelitian ... 24
B. Variabel dan Definisi Operasional ... 24
1. Variabel utama ... 24
xxxi
C. Bahan Penelitian ... 25
D. Alat Penelitian ... 26
E. Tata Cara Penelitian ... 27
1. Penyiapan hewan uji ... 27
2. Percobaan pendahuluan ... 27
a. Determinasi tanaman sirsak ... 27
b. Pembuatan serbuk daun sirsak ... 27
c. Penetapan kadar air daun sirsak kering ... 27
d. Penetapan dosis daun sirsak ... 28
3. Pembuatan infusa daun sirsak ... 29
4. Pengelompokan dan perlakuan hewan uji ... 30
5. Penetapan kadar SGPT ... 31
6. Pembuatan dan pemerikasaan preparat histologi ... 31
F. Analisis Hasil ... 32
BAB IV HASIL DAN PEMBAHASAN ... 35
A. Pembuatan Sediaan Uji ... 36
B. Pengamatan Umum ... 36
1. Perkembangan Berat Badan Tikus ... 37
2. Asupan Makanan Perhari ... 40
3. Asupan minuman perhari ... 42
C. Pemeriksaan SGPT ... 45
D. Pemeriksaan Histologi Hati ... 50
xxxii
A. Kesimpulan ... 59
B. Saran ... 59
xxxiii
DAFTAR TABEL
xxxiv
xxxv
DAFTAR GAMBAR
xxxvi
xxxvii
DAFTAR LAMPIRAN
xxxviii
xxxix
xl Intisari
Daun sirsak banyak dimanfaatkan untuk mengatasi berbagai penyakit oleh masyarakat dari berbagai negara. Sayangnya, penelitian untuk mengungkapkan keamanan penggunaan infusa daun sirsak masih kurang. Penelitian ini bertujuan untuk mengetahui wujud efek toksik subkronis pada hati dan kadar SGPT akibat konsumsi infusa daun sirsak.
Lima puluh ekor tikus jantan dan betina dibagi secara acak menjadi 5 kelompok, 1 kelompok kontrol, dan 4 kelompok perlakuan dengan dosis 108; 180; 301; dan 503 mg/kgBB selama 30 hari. Pengambilan darah untuk menentukan kadar SGPT dilakukan sebelum diberi perlakuan dan pada hari ke 31. Pada hari ke 31 separuh dari total tikus dikorbankan untuk dibuat preparat histologinya. Lalu dilakukan uji reversibilitas selama 14 hari. Data berupa kadar SGPT dan bobot hati yang didapat kemudian dianalisis dengan one way Annova dan deskripsi histologi hati.
Hasilnya, terjadi perbedaan yang tidak bermakna antara kadar SGPT sebelum dan sesudah perlakuan dan kadar SGPT kontrol dengan kelompok perlakuan. Hasil pemeriksaan histologinya, 2 hewan mengalami degenerasi hidropik dari 50 hewan uji.
Kesimpulannya, tidak terjadi efek toksik pada pemberian infusa daun sirsak selama 30 hari pada hati tikus jantan dan betina galur Sprague dawley
sehingga perlu dilakukan uji toksisitas kronik untuk mengungkap efek toksik yang tidak nampak pada penelitian ini.
xli
Abstract
Graviola leaves being used to address in variety of diseases by people from various countries. Unfortunately, studies to reveal the safety of graviola leaves infusion used is still lacking. The study aims to determine the form of subchronic toxicity effects on the liver and SGPT’s levels due to consumption of graviola leaves infusion.
Fifty male and female rats were divided randomly into 5 groups, 1 control group and 4 treated groups dosed of 108; 180; 301, and 503 mg/kg BB for 30 days. Blood sampling to determine levels of SGPT were performed before treatment and at 31st day. On 31st day half of the mice were sacrificed to make preparations of histology. Then recovery test was done for 14 days. Data in the form of SGPT levels and liver weights were obtained and analyzed with one-way Annova and liver histologies were described.
As a result, there was no significant difference between the levels of SGPT before and after treatment and levels of SGPT between the control and the treatment group. The histology examination results, two animals had hydropic degeneration of the 50 animals.
The conclusion is there were no toxic effects on the provision infusion of graviola leaves for 30 days in the liver of male and female rats of Sprague Dawley strain that chronic toxicity tests need to be done to uncover the toxic effects that are not performed in this study.
1 BAB I PENGANTAR
A. Latar Belakang
Sebelum pengobatan modern masuk Indonesia, masyarakat Indonesia banyak menggunakan bahan alam sebagai media pengobatan. Mereka menggunakan bagian tanaman, hewan, dan mineral yang kemudian diracik untuk menyembuhkan penyakit. Berdasarkan peraturan menteri kesehatan nomor 246/Menkes/Per/V/1990 pasal 1 menyebutkan bahwa obat tradisional adalah bahan atau ramuan bahan yang berupa bahan tumbuhan, hewan, dan mineral, sediaan galenik atau campuran bahan bahan tersebut, yang secara tradisional telah digunakan untuk pengobatan berdasarkan pengalaman (Depkes, 1990). Sehingga penggunaan bahan tanaman, hewan, dan mineral yang diracik tersebut untuk melakukan pengobatan disebut pengobatan tradisional.
menjaga kesehatan (Duryatmo, 2011). Sejak itu pula, mulai banyak penelitian mengenai efek farmakologis dari daun sirsak misalnya antilipidemia dan antidiabetes (Adewole, and Ojewole, 2009) serta sebagai antinociceptive dan antiinflamasi (Sousa, Vieira, Pinho, Yamamoto, and Alves, 2010).
Kini, disaat berkembangnya obat modern, pengobatan tradisional masih menjadi idola untuk sebagian orang karena pengobatan tradisional dianggap lebih aman daripada obat modern. Daun sirsak kini menjadi idola sebagian orang untuk dikonsumsi rutin sebagai pencegah penyakit. Namun, ada kejadian atipikal Parkinson di French West Indies dihubungkan dengan kebiasaan masyarakatnya yang suka mengkonsumsi daun sirsak dalam bentuk sediaan teh (Caparros-Lefebvre and Elbaz, 1999). Oleh karena itu, perlu adanya pengujian yang mendalam mengenai efek buruk pengkonsumsian daun sirsak secara berulang dalam jangka waktu yang lama.
infusa karena masyarakat biasa mengkonsumsinya dalam bentuk rebusan. Sediaan rebusan sangat sulit distandarisasi karena tidak ada patokan yang baku untuk pembuatannya maka penelitian ini menggunakan infusa yang memiliki patokan baku pembuatannya dan serupa dengan rebusan. Pengujian dilakukan pada organ hati karena organ hati merupakan organ utama metabolisme zat zat yang masuk dalam tubuh. Sehingga bila ada zat yang berbahaya yang masuk dalam tubuh, organ hati yang berpotensi besar untuk terjadi kerusakan. Kerusakan organ hati dapat terlihat dalam hispatologi hati tersebut, apakah terjadi ketidaknormalan dalam hispatologinya atau tidak. Indikator lain dari adanya kerusakan fungsi hati adalah kadar SGPT. Kadar SGPT nilainya akan berubah bila terjadi kelainan fungsi hati.
1. Permasalahan
Berdasarkan latar belakang tersebut, permasalahan yang akan diteliti adalah d. Seperti apa wujud biokimia efek toksik pada SGPT dan wujud struktural
efek toksik infusa daun sirsak pada histologi organ hati pada uji toksisitas subkronis?
e. Apakah spektrum efek toksik senyawa uji tersebut berkaitan dengan takaran dosis?
f. Adakah keterbalikan spektrum efek toksik yang terjadi?
2. Keaslian penelitian
daun sirsak hasilnya adalah LD50 ekstrak air daun sirsak adalah lebih dari 200
mg/kg secara i.p (Adewole et al., 2009). Ekstrak daun sirsak dinyatakan aman karena LD50nya lebih dari 5 g/kg BB secara per oral dan untuk dosis tinggi
daun sirsak menyebabkan kerusakan ginjal bila dikonsumsi dalam jangka waktu 14 hari pada tikus walaupun secara umum pengkonsumsian ekstrak air daun sirsak tidak menimbulkan efek buruk (Arthur et al, 2011). Ekstrak air daun sirsak juga memiliki efek hepatoprotektif terhadap hati tikus yang terinduksi CCl4 dan asetaminofen pada dosis 400 mg/kg BB (Arthur, Woode,
Terlabi, and Larbie, 2012).
Sejauh pengetahuan peneliti, penelitian uji toksisitas subkronik infusa daun sirsak dalam waktu 30 hari pada tikus putih belum pernah dilakukan.
3. Manfaat penelitian a. Manfaat teoritis
Penelitian ini diharapkan dapat bermanfaat untuk pengembangan ilmu pengetahuan farmasi terutama pada penggunaan obat tradisional.
b. Manfaat praktis
Penelitian ini diharapkan dapat memberikan informasi mengenai efek toksik subkronis pada hati akibat pemberian infusa daun sirsak.
B. Tujuan Penelitian
1. Tujuan umum
2. Tujuan khusus
Penelitian ini dilakukan untuk:
a. Mengungkapkan wujud biokimia efek toksik infusa daun sirsak pada kadar SGPT dan wujud struktural efek toksik infusa daun sirsak pada hati tikus betina dan jantan pada pemejanan subkronis.
b. Mengungkapkan apakah efek toksik senyawa uji berkaitan dengan
takaran dosis atau tidak.
6 BAB II
PENELAAHAN PUSTAKA
A. Daun Sirsak
1. Klasifikasi tanaman
Kingdom : Plantae (Tumbuhan)
Subkingdom : Tracheobionta (Tumbuhan berpembuluh)
Super Divisi : Spermatophyta (Menghasilkan biji)
Divisi : Magnoliophyta (Tumbuhan berbunga)
Kelas : Magnoliopsida (berkeping dua / dikotil)
Sub Kelas : Magnoliidae
Ordo : Magnoliales
Famili : Annonaceae
Genus : Annona
Spesies : Annona muricata L. (Anonim, 2008).
2. Deskripsi tanaman sirsak
diameternya 15 – 23 cm, luarnya berwarna kuning kehijauan dan dalamnya berwarna putih (Anonim, 2004).
3. Morfologi daun sirsak
Daun sirsak atau Annona muricata folium adalah daun dari tanaman
Annona muricata L., suku Annonaceae. Daun ini berbau agak keras dan rasanya agak kelat. Daun sirsak adalah daun tunggal, berwarna kehijauan sampai hijau kecoklatan, helaian daunnya seperti kulit. Bentuk dari daun sirsak adalah bundar panjang, lanset, atau bundar telur terbalik. Panjang tiap helainya adalah 6 cm sampai 18 cm dan lebarnya antara 2 cm hingga 6 cm. Ujung daun sirsak meruncing pendek, begitu juga dengan pangkalnya. Tepi daun sirsak adalah rata. Panjang tangkai daun sirsak sekitar 0.7 cm. Permukaan daun sirsak licin agak mengkilat. Tulang daun daun sirsak menyirip dan ibu tulangnya menonjol pada permukaan bawah (Depkes, 1989).
4. Kandungan kimia daun sirsak
Secangkir infusa atau dekokta daun sirsak mengandung 140 µg kelompok senyawa acetogenin (Lannuzel, Hoglinger, Champy, Michel, Hircsh, and Ruberg, 2006). Acetogenin yang ada dalam daun sirsak adalah
annocatalin, annohexocin, annonomicin, annomontacin, annomuricatin A dan
B, annomuricin A hingga E, annomutacin, annonacin, annonacinone, annopentocin A hingga C, cis-annonacin, cis-corossolone, cohibin A hingga
D, gigantetrocin A dan B, gigantetrocinone, gigantetronenin, goniothalamicin, iso-annonacin, javoricin, montanacin, montecristin, muracin A hingga G,
dan B, muricatin D, muricatocin A hingga G, muricin H, muricin I, muricoreacin, murihexocin 3, murihexocin A hingga C, murihexol, murisolin, robustocin, rolliniastatin 1 dan 2, saba-delin, solamin, uvariamicin I dan IV, dan xylomicin (Anonim, 2004). Selain itu, ekstrak air daun sirsak mengandung saponin, tannin terkondensasi, glikosida, dan flavonoid (Arthur et al., 2011). Daun sirsak juga mengandung senyawa alkaloid, Annonamine (Matsushige, Kotake, Matsunami, Otsuka, Ohta, and Takeda, 2012).
5. Kegunaan daun sirsak
Daun sirsak banyak digunakan sebagai obat tradisional untuk pengobatan penyakit abses, arthritis, asthenia, asma, bronchitis, selesma, batuk, diabetes, disentri, demam, edema, batu empedu, hipertensi, kelainan pencernaan, infeksi, kecacingan, sakit liver, malaria, neuralgia, palpitasi, rematik, dan tumor. Juga dapat sebagai astringen dan diuretik (Anonim, 2004). Penelitian invivo membuktikan manfaat daun sirsak antara lain: Ekstrak air daun sirsak menghambat lipid peroksida dan meningkatkan produksi insulin dan antioksidan endogen sehingga ekstrak air daun sirsak dapat melindungi
dan memelihara sel β pancreas (Adewole and Caxton-Martins, 2006) dan sel
hati pada tikus(Adewole and Ajowole, 2009). Ekstrak air daun sirsak juga memiliki efek hepatoprotektif terhadap hati tikus yang terinduksi CCl4 dan
6. Toksisitas daun sirsak
Caparros-Lefebvre dan Elbaz (1999) mengemukakan bahwa ada hubungan antara pengkonsumsian herbal teh daun sirsak dalam jangka panjang dapat menyebabkan terjadinya Progressive Supranuclear Palsy dan Parkinson karena herbal teh daun sirsak mengandung senyawa benzyltetrahydroisoquinolines yang bersifat toksik terhadap sel sel otak. Konsumsi daun sirsak dalam jangka waktu yang panjang dapat menginduksi toksik yang terkumulasi yang dapat menyebabkan atypical parkinsonism syndrome (Champy, Hoglinger, Feger, Gleye, Hocquemiller, Laurens, et al.,
2004). Infusa daun sirsak juga mengandung annonacin yang dapat menembus
blood brain barrier dan menginduksi neurodegenerasi pada basal ganglia seperti yang terjadi pada atypical parkinsonism (Lannuzel et al., 2006).
B. Uji Toksisitas Subkronis
Sebuah uji toksisitas dirancang untuk menghasilkan data tentang efek buruk dari suatu zat pada manusia, hewan, atau lingkungan. Kebanyakan uji toksisitas menguji efek tertentu yang bersifat khas, yang disebut end point, seperti kanker (karsinogenik) atau iritasi mata (ketoksikan ocular). Walau begitu, uji toksisitas juga ada yang bersifat umum seperti uji toksisitas pemaparan tunggal (uji toksisitas akut) dan uji toksisitas pemaparan berulang (uji toksisitas repeat dose), dimana hewan coba diberikan zat dengan dosis harian untuk menghitung NOAELs (No Observable Adverse Effect Level) dan menentukan kerusakan organ atau sistem akibat pemejanan zat selama 1 bulan, 3 bulan, atau 2 tahun. Uji toksisitas dimaksudkan untuk menentukan kebahayaan suatu zat pada manusia yang biasa diungkap dengan keamanan dan pada lingkungan yang disebut ekotoksisitas (Anonim, 2009).
Uji toksisitas subkronis adalah uji yang digunakan untuk menentukan toksisitas yang timbul dari paparan berulang beberapa minggu sampai beberapa bulan, biasanya digunakan pengujian secara oral, dermal, dan inhal. Pada uji ini dilakukan pengamatan klinis yang rinci dan pemeriksaan patologi (Monnosson, 2007).
mikroskopik, untuk dosis rendah dan menengah dilakukan pengamatan bila memang diperlukan (A.R) (Derelanko and Holinger, 1995).
Tabel I. Eksperimental desain - uji toksisitas subkronis pada hewan pengerat
selama 4 minggu
Keterangan A.S = all survivors A.R = as required (Derelanko and Holinger, 1995).
C. Toksisitas Hati
Senyawa toksik dapat sangat berbahaya pada organ organ tertentu meskipun banyak organ dan jaringan yang lain dapat menjadi target senyawa toksik. Organ organ tertentu dapat menjadi target senyawa toksik dengan alasan:
1. Organ tersebut merupakan penyuplai darah
3. Organ tersebut berada di posisi tertentu dan memiliki fungsi tertentu 4. Rentan terhadap gangguan
5. Memiliki kemampuan memperbaiki kerusakan 6. Adanya sistem uptake tertentu
7. Memiliki kemampuan memetabolisme senyawa dan memiliki kesetimbangan sistem toksikasi dan detoksikasi
8. Berikatan dengan makromolekul tertentu (Timbrell, 2009).
Jika senyawa induk bersifat toksik, faktor seperti enzim penginduksi dan penginhibisi, yang merubah metabolisme atau merubah distribusi atau ekskresi, akan memiliki kecenderungan merubah ketoksikan senyawa tersebut. Sistem uptake yang spesifik akan mempengaruhi distribusi, dan rute ekskresi tertentu akan menjadi jenuh. Metabolisme bisa menyebabkan penampakan dari tipe toksisitas yang berbeda. Jika metabolitnya toksik, kemudian faktor yang meningkatkan metabolisme dapat meningkatkan toksisitas, sehingga bila jalur detoksifikasinya juga tidak meningkat, tidak terjadi keseimbangan. Metabolit toksik atau metabolit yang hampir toksik bisa dihasilkan di sebuah organ seperti hati dan ditransportasikan ke organ lain. Interaksi antara toksin atau metabolit yang reaktif dengan reseptor terjadi di jaringan yang spesifik (Timbrell, 2009).
1. Hati mampu memetabolisme senyawa asing yang masuk dalam tubuh tapi hasil metabolism tidak selalu berupa detoksifikasi. Bisa saja hasil metabolism berupa racun sehingga meracuni hati.
2. Hati memiliki peran penting sebagai perantara metabolisme dan sintesis,
sebagai konsekuensinya, interfensi dengan jalur metabolisme endogen dapat memicu ketoksikan.
3. Sekresi bile oleh hati. Hal ini merujuk pada ekskresi biliary senyawa asing
yang menjadikan konsentrasinya tinggi.
4. Suplai darah menentukan bahwa hati terpapar senyawa toksik dengan
konsentrasi yang tinggi yang diserapnya dari gastrointestinal (Timbrell, 2009).
1. Anatomi dan fisiologi hati
Hati adalah sebuah organ yang terletak di abdomen atas dan terbagi menjadi 2 lobes mayor dan 2 lobes minor (Stine and brown, 1996). Senyawa yang memasuki tubuh melalui gastrointestinal diserap dalam sistem peredaran darah hepatic-portal dan masuk ke hati melalui portal vein (Timbrell, 2009). Walaupun sebenarnya darah memasuki hati dengan 2 cara, yaitu melalui
hepatic artery dan portal vein. Darah keluar dari hati melalui hepatic vein, dan
bile dikeluarkan melalui hepatic duct lalu melalui common bile duct menuju usus halus atau melalui cystic duct menuju ke gall bladder untuk disimpan (Stine and Brown 1996).
vein ke inferior vena cava (Timbrell, 2009). Sel dalam hati disusun secara khusus dengan pola hexagonal yang disebut lobules. Sel epitel yang disebut hepatosit terlihat seperti menyebar keluar dari central vein. Kolom hepatosit memiliki kanal yang disebut sinusoid yang tersusun dari sel endothelial yang sangat permeabel dan mengandung sel fagosit yang disebut sel kupffer. Tiga vessel lainnya ditemukan pada tiap ujung heksagon, yaitu cabang dari portal vein, cabang dari hepatic artery, dan bile duct. Darah mengalir masuk melalui cabang hepatic artery dan portal vein, melalui sinusoid, dan mengalir keluar melalui central vein. Bile dihasilkan di hepatosit dan mengalir keluar melalui
bile canaliculi ke bile duct (Stine and Brown, 1996).
Tiap hepatic artery/ portal vein tidak hanya mensuplai darah ke satu
Banyak hepatosit yang mengandung enzim yang dapat mengubah senyawa toksik secara kimia. Senyawa toksik tersebut bisa jadi lebih toksik, atau menjadi kurang toksik. Ada 2 tipe biotransformasi yaitu reaksi fase 1 dan reaksi fase 2 (Stine and Brown, 1996).
Reaksi fase 1 adalah oksidasi dan hidrolisis senyawa, yang dilakukan oleh sistem enzim yang disebut system sitokrom P450. Sistem ini terdiri dari beberapa jenis enzim berbeda, termasuk beberapa bentuk dari sitokrom P450 itu sendiri. Mereka memetabolisme steroid, senyawa endogen, dan xenobiotik (Stine and Brown, 1996).
Sitokrom P450 monooksigenase terdiri dari haemoprotein yang disebut sitokrom P450 (CYP) dan flavoprotein yang disebut NADPH-sitokrom P450 reduktase. CYP adalah sebuah senyawa dan merupakan sebuah tempat pengikatan oksigen dalam sistem enzim tersebut dan reduktase-nya adalah
donor electron. CYP3A4 adalah enzim CYP yang paling penting di dalam hati diikuti CYP1A2, CYP2C9, CYP2D6, CYP2E1, dan CYP2C19. Hidroksilasi beberapa obat dimediasi oleh CYP2D6 dan demetilasinya didominasi oleh CYP1A2, CYP2C, dan CYP3A4 (Greaves, 2000).
Reaksi fase 2 meliputi konjugasi senyawa toksik (metabolit hasil dari reaksi fase 1) dengan molekul lainnya. Biasanya, aksi ini meningkatkan ukuran dan kelarutan pada air senyawa tersebut, dan membuatnya mudah untuk diekskresikan (Stine and Brown, 1996).
Hati adalah organ yang memiliki peran penting dalam proses metabolisme. Darah yang mengandung nutrien dari saluran pencernaan singgah ke hati (melalui vena portal), dimana nutrien seperti karbohidrat, lipid, dan vitamin diambil dari darah dan disimpan hingga suatu waktu dibutuhkan. Sel hati juga bisa memetabolisme karbohidrat, lipid, dan protein (Stine and Brown, 1996). Hati juga mensintesis dan mensekresi bile, yang mengandung air, ion, lipid, dan pigmen bile. Bile disimpan di gall bladder dan disekresikan ke usus halus (Stine and Brown, 1996). Hati juga tempat terjadinya metabolisme xenobiotik. Artinya, hepatosit memiliki resiko terpapar toksik yang teraktifkan yang merupakan hasil dari metabolisme senyawa toksik (Stine and Brown, 1996).
3. Patogenesis kerusakan hati akibat induksi senyawa toksik
Kerusakan hati yang diakibatkan oleh senyawa toksik ada yang bisa diprediksi dan ada yang tidak bisa diprediksi. Senyawa yang menyebabkan kerusakan hati yang bisa diprediksi biasanya menampakkan gejalanya dalam beberapa hari dan biasanya menimbulkan toksisitas hati secara langsung yang disebabkan oleh senyawa induk maupun metabolitnya. Sedangkan yang tidak bisa diprediksi gejalanya tampak setelah beberapa minggu sampai satu tahun. Kebanyakan kejadian kerusakan hati akibat induksi senyawa toksik adalah tidak bisa diprediksi dan merupakan hipersensitif yang dimediasi oleh imun atau idiosyncratic (Kaplowitz, 2004).
berefek secara langsung pada biokimia sel. Metabolit senyawa kimia bisa berupa senyawa elektrofilik atau radikal bebas yang memiliki kemampuan untuk beinteraksi dengan makromolekul selular seperti protein, lipid, dan asam nukleat, yang menyebabkan disfungsi protein, peroksidasi lipid,kerusakan DNA, dan stress oksidatif (Kashaw, Nema, and Agarwal, 2011). Konsekuensi dari reaksi kimia tersebut bisa berefek langsung pada organel tapi bisa juga mempengaruhi organel secara tidak langsung melalui aktivasi dan inhibisi sinyal kinase, faktor transkripsi, dan ekspresi gen. Kerusakan intraselular mengakibatkan kematian sel yang disebabkan oleh penyusutan sel dan pembongkaran nukleus (apoptosis) atau pembengkakan dan lisis (nekrosis). Kematian hepatosit adalah penyebab utama kerusakan hati meskipun sel sinusoidal endothelial dan epithelium bile duct juga bisa menjadi target kerusakan (Kaplowitz, 2004).
sistem imun sehingga menyebabkan serangan autoimun pada hepatosit yang normal (Kaplowitz, 2004).
Selain itu, metabolit reaktif juga menyebabkan gangguan gradient ion dan cadangan kalsium intraseluler, yang mengakibatkan gangguan mitokondrial dan hilangnya produksi energi. Kerusakan tersebut menghasilkan sejumlah besar oksidan yang merusak sel hepatik. Aktifasi beberapa enzim dari sistem sitokrom P-450 seperti CYP2E1 juga menyebabkan stress oksidatif. Kerusakan hepatosit dan sel bile duct menyebabkan akumulasi bile acid di hati. Hal ini yang menyebabkan kerusakan hati lebih lanjut. Kerusakan fungsi sel bisa memuncak pada sel mati dan menyebabkan gagal hati. Kerusakan dan kematian sel hati juga dapat memicu timbulnya reaksi imun, baik imun aktif maupun pasif. Stres dan kerusakan hepatosit menghasilkan sinyal yang menstimulasi aktivasi sel lainnya, terutama sistem imun pasif, seperti sel Kupfer, NK sel, dan NKT cells. Sel sel tersebut berkontribusi pada kelangsungan kerusakan sel dengan memproduksi mediator proinflamatori dan mengeluarkan kemokin yang menyebabkan datangnya sel inflamasi yang lebih banyak. Hal ini menunjukkan bahwa berbagai sitokin inflamasi, seperti
TNF-α, IFN-ϒ, dan IL-1β, dihasilkan selama pengrusakan sel hepatik yang
sistem imun pasif yang ditentukan oleh kerentanan dan adaptasi individu terhadap kerusakan sel hepatik (Kashaw et al, 2011).
4. Tipe kerusakan hati yang diakibatkan induksi senyawa toksik
Kerusakan yang terjadi pada hati akibat induksi dari senyawa toksik dapat berupa:
a. Perubahan bobot hati
Penyebab perubahan bobot hati berbeda-beda. Bobot hati bisa meningkat karena akumulasi lipid, glikogen atau senyawa lain atau karena kerusakan sel, kongesti sel, hipertrofi atau hiperplasia dari hepatoselular yang disertai dengan proliferasi RE halus atau peroksisom. Pengaruh hipertrofi centrilobular dengan kenaikan massa hati pada rodent biasanya dihubungkan dengan proliferasi RE halus dan induksi enzim adaptif (Greaves, 2000).
b. Perlemakan hati (Steatosis)
Perlemakan hati adalah hati yang mengandung berat lipid lebih dari 5%. Adanya kelebihan lemak dalam hati dapat dibuktikan secara histokimia. Lesi dapat bersifat akut, seperti yang disebabkan oleh etionin, fosfor, atau tetrasiklin. Mekanisme perlemakan hati yang paling umum adalah rusaknya pelepasan trigliserida hati ke plasma. Penimbunan lipid hati dapat terjadi lewat beberapa mekanisme:
c. Hilangnya kalium dari hepatosit, mengakibatkan gangguan transfer VLDL melalui membrane sel
d. Penghambatan sintesis fosfolipid (Lu, 1995).
Penampakan mikroskopik dari steatosis ada 2 macam yaitu mikrovesikular, lipid-containing cytoplasmic vacuoles, dan makrovesikular, ada satu vakuola tiap sel. Makrovesikular dikarakteristikkan dengan adanya satu vakuola berlemak yang besar yang menggeser posisi nukleus ke periphery. Senyawa penyebab makrovesikular mengganggu proses pengeluaran lipid dari sel (Greaves, 2000).
Mikrovesikular steatosis merupakan pertanda dari kerusakan hati yang serius atau terjadi keracunan dalam organ hati. Sitoplasma sel hati terisi oleh sejumlah kecil lipid yang sering memberikan tampilan berbusa dan inti sel tetap tinggal ditengah sel. Pada manusia, mikrovesikular streatosis dihubungkan dengan penyakit hati seperti fatty liver akut pada kehamilan dan Reye’s syndrome (Greaves, 2000).
c. Nekrosis hati
Nekrosis adalah kematian hepatosit dan biasanya merupakan kerusakan akut. Nekrosis hati merupakan manifestasi toksik yang berbahaya tetapi tidak selalu kritis karena hati memiliki kapasitas pertumbuhan kembali yang cepat (Lu, 1995).
Perubahan morfologi awal antara lain berupa edema sitoplasma, dilatasi Retikulum endoplasma, dan disagregasi polisom. Perubahan yang terdahulu merupakan pembengkakan mitokondria progresif dengan kerusakan krista, pembengkakan sitoplasma, penghancuran organel dan hati, dan pecahnya membran plasma (Lu, 1995).
d. Sirosis
Sirosis didefinisikan sebagai proses difusi yang dikarakteristikkan oleh fibrosis dan konversi hati normal menjadi nodules yang strukturnya abnormal oleh WHO (Greaves, 2000). Sirosis ditandai dengan adanya septa kolagen yang tersebar di sebagian besar hati. Sirosis berasal dari nekrosis sel tunggal karena kurangnya perbaikan. Kemudian keadaan ini menyebabkan aktivitas fibroblastik dan pembentukan jaringan parut (Lu, 1995).
e. Hepatitis kronis aktif
Kondisi inflamasi kronik dikarakteristikkan dengan adanya senyawa penyebab inflamasi terutama limfosit dan sel plasma dengan bervariasi jumlah neutrofil dan eosunofil, yang meluas hingga area portal dan memanjang hingga lobule hati dan mengikis limiting plate (Greaves, 2000).
senyawa metabolitnya mungkin bertindak sebagai hapten dengan berkombinasi dengan makromolekul dalam hati dan mengubah antigenic
mereka dengan hasilnya adalah sensitisasi limfosit dan kerusakan hepatosit (Graves, 2000).
f. Karsinogenesis
Karsinoma hepatoseluler dan kolangiokarsinoma adalah jenis neoplasma yang paling umum pada hati (Lu, 1995). Pada manusia, karsinoma hati bergantung pada kuantitas dan karakter sitoplasma, ukuran dan derajat hiperkromatis inti sel, rasio nukleus dan sitoplasma, kohesifitas sel tumor, dan gambaran umum sel (Greaves, 2000).
D. Serum Glutamat Piruvat Transaminase (SGPT)
Transferase adalah gugus enzim yang mengkatalisis interkonvensi asam amino dan oxoacids dengan memindahkan gugus amino. SGPT (Serum Glutamat Piruvat Transaminase) atau sering disebut juga ALT (Alanine Aminotransferase) biasa digunakan untuk mendeteksi dan mendiagnosis adanya penyakit hati. Kerusakan sel hati dimanifestasikan dengan peningkatan aktivitas transaminase (Walker, Hall, and Hurst, 1990).
E. Keterangan Empiris
24 BAB III
METODE PENELITIAN
A. Jenis dan Rancangan Penelitian
Penelitian pengaruh pemberian berulang infusa daun sirsak terhadap hati dan kadar SGPT tikus putih jantan dan betina galus Sprague Dawley termasuk dalam penelitian eksperimental murni dengan menggunakan rancangan penelitian acak lengkap pola searah.
B. Variabel dan Definisi Operasional
1. Variabel utama
Variabel utama dalam penelitian ini terdiri dari variabel bebas dan variabel tergantung.
a. Variabel bebas: dosis air infusa daun sirsak. Dosis air infusa daun sirsak adalah sejumlah serbuk daun sirsak (mg) yang dibuat infusa dalam 100 ml aquadest tiap satuan berat badan (kg) hewan uji.
b. Variabel tergantung: kerusakan struktur anatomi hati yang dilihat dari gambaran histologi hati dan perubahan kadar SGPT dalam darah hewan uji.
2. Variabel pengacau
Variabel pengacau dalam penelitian ini terdiri dari variabel pengacau terkendali dan variabel pengacau tidak terkendali.
a) galur Sprague Dawley
b) jenis kelamin jantan dan betina c) umur 2 – 2,5 bulan
d) berat badan 170 – 280 gram
e) keadaan fisik yang berstatus sehat dan tikus betina sedang dalam keadaan tidak hamil
2) bahan uji berupa daun sirsak
a) Daun berwarna hijau tua berupa daun dewasa, utuh dan terlihat sehat (tidak terkena gigitan serangga maupun ada noda jamur). b) Daun diperoleh dari satu pohon yang sama, yang lokasinya
jauh dari jalan raya dan tidak terpapar pestisida. b. Variabel tidak dikendalikan:
2) keadaan patologis tikus: meskipun keadaan fisik tikus dinyatakan berstatus sehat, tapi itu tidak bisa menjamin keadaan hatinya berstatus sehat.
C. Bahan Penelitian
1. Subjek uji yang digunakan adalah tikus putih galur Sprague Dawley jantan
dan betina, berusia 2 – 2,5 bulan, berat badan 170 – 280 gram, yang diperoleh dari laboratorium Hayati Imono Fakultas Farmasi Universitas Sanata Dharma. 2. Bahan uji yang digunakan adalah daun sirsak dalam kondisi dewasa dan segar
3. Bahan untuk membuat preparat histopatologi hati adalah larutan formalin 37%, larutan formalin p.a 10%, larutan alkohol 80%, larutan alkohol 95%, larutan alkohol absolut, cairan xylol, cairan paraffin, paraffin blok, Mayers Egg Albumin, larutan hematoksilin, dan larutan eosin alkohol yang disediakan oleh Laboratorium Patologi Fakultas Kedokteran Hewan Universitas Gadjah Mada.
4. Bahan yang digunakan sebagai kontrol adalah aquadest yang diperoleh dari
Laboratorium Farmakognosi Fitokimia, Fakultas Farmasi, Universitas Sanata Dharma, Yogyakarta.
D. Alat Penelitian
1. jarum suntik peroral 2. spuit injeksi
3. seperangkat alat bedah 4. alat alat gelas (Pyrex)
5. timbangan (analytical balance) 6. blender
7. ayakan 8. mikroskop 9. kamera digital
10.metabolic cage
E. Tata Cara Penelitian
1. Penyiapan hewan uji
Hewan uji yang digunakan berjumlah 50 ekor (25 jantan dan 25 betina), ditempatkan dalam metabolic cage. Hewan uji yang digunakan adalah tikus putih jantan dan betina galur Sprague Dawley; umur 2 – 2,5 bulan; berat badan 170 – 280 g.
2. Percobaan pendahuluan a. Determinasi tanaman sirsak
Determinasi tanaman sirsak dilakukan dengan cara mencocokkan ciri ciri yang dipunyai tanaman sirsak dengan buku acuan (Backer and Bakhizen van den Brink, 1963).
b. Pembuatan serbuk daun sirsak
Sejumlah daun sirsak dicuci dan dikeringkan dalam oven selama 3 hari pada suhu ± 470C. Kemudian daun diblender hingga menjadi serbuk halus. Setelah itu serbuk diayak dengan ayakan no.40.
c. Penetapan kadar air daun sirsak kering
toluene. Toluena juga dituang dalam tabung penerima melalui alat pendingin. Selanjutnya labu dipanaskan selama 15 menit.
Ketika toluene mulai mendidih, penyulingan dilakukan dengan kecepatan 2 tetes perdetik hingga sebagian besar air tersuling, lalu kecepatan penyulingan dinaikkan hingga 4 tetes per detik. Setelah semua air tersuling, bagian dalam pendingin dicuci dengan toluene sambil dibersihkan. Setelah air dan toluene memisah sempurna, volume air dibaca dan ditetapkan kadarnya dalam persen.
d. Penetapan dosis daun sirsak
Penentuan kisaran dosis untuk uji pendahuluan ini didasarkan pada pengobatan yang digunakan dalam masyarakat yaitu 2 gram serbuk yang kemudian dicampur 100 ml dan direbus kemudian diminum air rebusannya. 2 gram serbuk daun sirsak untuk manusia 70 kg.
Konversi manusia ke tikus = 0,018
2 � × 0,018 = 0,036 � 200 � �
= 0,00018 gram per gram berat badan = 180 mg/ kg BB
Dosis 180 mg/kg BB digunakan sebagai peringkat kedua.
� = � ×1
2 � �
� �
= 6 �
100 ×2,5
300 � = 0,0005 g/ gBB
= 0,5 mg/ gBB tikus = 500 mg/ kg BB tikus.
Untuk menentukan dosis pertama dan ketiga, faktor perkalian dosis ditentukan terlebih dahulu dengan rumus:
faktor perkalian dosis = � � ���
� ℎ
−1
dengan
n = jumlah peringkat dosis dosis tertinggi = 500 mg/ kg BB dosis terendah = 180 mg/ kg BB
Hasilnya diperoleh 1,673; sehingga dosis pertama adalah 180 mg/ kg BB dibagi 1,673 dan dosis ketiga adalah 180 mg/ kg BB dikali dengan 1,673, sehingga peringkat dosisnya adalah
Dosis I = 108 mg/kg BB Dosis II = 180 mg/kg BB Dosis III = 301 mg/kg BB Dosis IV = 503 mg/kg BB 3. Pembuatan infusa daun sirsak