LAPORAN TUGAS AKHIR
Pengaruh Konsentrasi Substrat dan Enzim Terhadap Produk Gula
Reduksi Pada Pembuatan Gula Cair dari Tepung Sorgum Merah Secara Hidrolisis Enzimatis
The Effect of Substrat and and Enzyme Concentration to the Reducing Sugar Product on The Production of Sugar from Red Sorghum Flour through Enzymatis
Hydrolisis
Diajukan untuk memenuhi salah satu syarat menyelesaikan program studi D-IV Teknik Kimia Produksi Bersih di Jurusan Teknik Kimia
POLBAN
Disusun Oleh :
Dahliana Alami (141424008)
Mira Auliya Tsaqila (141424021)
PROGRAM STUDI DIV TEKNIK KIMIA PRODUKSI BERSIH
JURUSAN TEKNIK KIMIA
LEMBAR PENGESAHAN
Pengaruh Konsentrasi Substrat dan Enzim Terhadap Produk Gula Reduksi Pada Pembuatan Gula Cair dari Tepung Sorgum Merah Secara Hidrolisis
Enzimatis
Penulis :
1. Dahliana Alami NIM 141424008 2. Mira Auliya Tsaqila NIM 141424021
Penguji : 1. Dr.Ir. Ahmad Rifandi, M.Sc
2. Dr.Ir. Bintang Iwhan Moehady, M.Sc 3. Ir. Unung Leoanggareni, MT
Laporan Tugas Akhir ini telah disidangkan pada tanggal 17 Januari 2018 dan disahkan sesuai dengan ketentuan.
Menyetujui, Pembimbing
LEMBAR PERSEMBAHAN
Alhamdulillahirrabbil’alamiin, Penulis mengucapkan puji dan syukur kepada Allah SWT dan Nabi Muhammad SAW karena atas rahmat dan karunia-Nya, penulis dapat
menyelesaikan Tugas Akhir dengan judul “Pengaruh Konsentrasi Substrat dan Enzim
Terhadap Produk Gula Reduksi Pada Pembuatan Gula Cair dari Tepung Sorgum
Merah Secara Hidrolisis Enzimatis” tepat pada waktunya. Penulis mengucapkan
terimakasih yang sebesar-besarnya kepada:
1. Kedua orang tua kami, serta adik dan kakak kami yang telah membantu baik
dalam bentuk moril dan materil.
2. Ibu Ayu Ratna Permanasari S.T.,M.T. selaku dosen pembimbing. Telah
banyak meluangkan waktunya untuk membimbing kami terimakasih atas
kesabarannya dan pengertiannya kepada kami.
3. Seluruh teman kelas 4A-TKPB yang telah membantu dan mendukung penulis
untuk menyelesaikan Tugas Akhir ini.
4. Teknisi Bu Yanti, Pak Acep dan Pak Cep Dedi yang telah membantu dan
menyiapkan bahan di laboratorium dan juga memberikan saransaran dalam Tugas
Akhir ini.
5. Iqbal Fathurachman yang telah meluangkan waktunya untuk mengajari dalam
hal format penulisan pada laporan ini.
6. Teman-teman tim laboratorium bioproses yang bersama-sama berjuang di lab,
yaitu Asri Nurdiana, Intan, Weni, Melani terimakasih telah menemani,
cerita-cerita, makan bareng dan membantu kami.
7. Teman seperjuangan kami bersama yaitu Alviera, Elis, Ghina, Desi, Dini,
Hasna, Lili, Rizka yang selalu memberi semangat kepada kami agar penulis dapat
menyelesaikan Tugas Akhir ini dengan baik dan tepat waktu.
8. Serta seluruh pihak yang tidak bisa kami sebutkan satu persatu.
Bandung, Januari 2018
PERNYATAAN TERTULIS
“Kami yang bertanda tangan di bawah ini menyatakan bahwa laporan Tugas Akhir ini adalah murni hasil pekerjaan kami sendiri. Tidak ada pekerjaan orang lain yang digunakan tanpa menyebutkan sumbernya.
Materi dalam laporan ini tidak/belum pernah disajikan/digunakan sebagai bahan untuk makalah/Tugas Akhir orang lain kecuali kami mengatakan dengan jelas bahwa kami menggunakannya.
Kami memahami bahwa laporan Tugas Akhir yang diserahkan ini dapat diperbanyak dan atau dikomunikasikan untuk tujuan mendeteksi adanya plagiatisme.”
Judul Tugas Akhir:
Pengaruh Konsentrasi Substrat dan Enzim Terhadap Produk Gula Reduksi Pada
Pembuatan Gula Cair dari Tepung Sorgum Merah Secara Hidrolisis Enzimatis
Bandung , Januari 2018
Yang Menyatakan,
Dahliana Alami Mira Auliya Tsaqila 141424008 141424021
Mengetahui, Pembimbing
KATA PENGANTAR
Puji dan syukur penulis panjatkan kehadirat Allah SWT, karena atas berkat dan limpahan karunia-Nya penulis dapat menyelesaikan laporan tugas akhir yang berjudul “Pengaruh Konsentrasi Substrat dan Enzim Terhadap Produk Gula Reduksi Pada Pembuatan Gula Cair dari Tepung Sorgum Merah Secara Hidrolisis Enzimatis”. Penulisan laporan tugas akhir merupakan bagian dari kurikulum pendidikan di program studi Teknik Kimia Produksi Bersih, Politeknik Negeri Bandung.
Dalam penyusunan laporan ini penulis mendapatan dukungan, bantuan, kerjasama,
saran, dan do’a dari berbagai pihak. Pada kesempatan ini penulis ingin mengucapkan
terimakasih kepada:
1. Ibu Ayu Ratna Permanasari S.T.,M.T. selaku dosen pembimbing pelaksanaan
Tugas Akhir.
2. Dr.Ir. Ahmad Rifandi, M.Sc, Dr.Ir. Bintang Iwhan Moehady, M.Sc dan Ir. Unung
Leoanggareni, MT selaku penguji sidang tugas akhir
3. Ibu Dr, Ir.Endang Sri Rahayu, MT. Selaku Koordinator Mata Kuliah Tugas Akhir
Program Studi D-IV Teknik Kimia Produksi Bersih Politeknik Negeri Bandung
4. Bapak Dr.Ir.Bintang Iwhan Moehady, M.Sc selaku Ketua Jurusan Teknik Kimia
Politeknik Negeri Bandung
5. Bapak Ir. Mukhtar Ghozali, M.Sc selaku Ketua Program Studi D-IV Teknik Kimia
Produksi Bersih Politeknik Negeri Bandung
6. Seluruh dosen Jurusan Teknik Kimia Politeknik Negeri Bandung atas bantuan dan
masukkanya dalam penyusunan laporan Tugas Akhir
7. Teknisi laboratorium yang senantiasa membantu dalam pengerjaan penelitian.
Penulis menyadari masih banyak kekurangan dalam penulisan laporan tugas
akhir ini. Maka dari itu, penulis mengharapkan saran dan kritik yang membangun dari
semua pihak demi tercapainya laporan tugas akhir yang lebih baik. Akhir kata penulis
berharap semoga laporan tugas akhir ini bermanfaat bagi pembaca.
Bandung, Januari 2018
ABSTRAK
Tepung sorgum merah belum banyak dimanfaatkan sebagai bahan pangan
seperti beras, singkong dan jagung, sehingga perlu dicari alternatif untuk lebih
mengoptimalkan manfaatannya, salah satu cara yaitu dengan mengolahnya menjadi
gula cair. Penelitian ini bertujuan untuk menentukan kondisi optimum pembuatan
gula cair dari tepung sorgum merah dengan proses hidrolisis enzimatis. Dalam
percobaan ini ukuran partikel tepung adalah 125μm. Enzim yang digunakan yaitu α
-amilase untuk proses likuifikasi dan gluko-amilase untuk proses sakarifikasi. Variasi
enzim yang digunakan adalah 0,033 ppm, 0,067 ppm, dan 0,1 ppm. Konsentrasi
substrat divariasikan yaitu 10%, 20%, 30%, dan 40% (b / v) dalam 300 ml suspensi.
Proses likuifikasi dilakukan pada suhu 90°C selama 60 menit, sedangkan proses
sakarifikasi dilakukan pada suhu 60°C selama 120 menit dengan pH 6 konstan setiap
proses. Konsentrasi gula reduksi yang paling tinggi diperoleh pada konsentrasi
substrat 40% dengan volume enzim 0,067 ppm sebesar 115,7384 g/l.
ABSTRACT
Red sorghum flour has not been widely used as food such as rice, cassava and corn, so it needs to find an alternative to further optimize utilization, one way is to process it into liquid sugar. This study aims to determine the optimum conditions of making liquid sugar from red sorghum flour with enzymatic hydrolysis process. In this experiment the size of the starch particles is 125μm. The enzyme used is α-amylase for the process of liquification and glucoamylase for the saccharification process. The enzyme variations used were 0.033 ppm, 0.067 ppm, and 0.1 ppm. Substrate concentrations varied 10%, 20%, 30%, and 40% (w/v) in 300 ml of suspension. The liqufication process is carried out at 90 ° C. for 60 minutes, while the saccharification process is carried out at 60 ° C. for 120 minutes with constant pH 6 of each process. The highest concentration of reducing sugar was obtained at a substrate concentration of 40% with an enzyme volume of 0.067 ppm of 115.7384 g/l.
Keywords: Red Sorghum Flour¸ Liquid Sugar, Hydrolysis, α-Amylase,
DAFTAR ISI
1.4 Ruang Lingkup Penelitian ... 3
BAB II TINJAUAN PUSTAKA ... 4
2.1 Hidrolisis Pati ... 4
2.4 Analisis Produk ... 12
2.4.1 Analisis Kadar Gula Total menggunakan Portable Brix ... 13
2.4.2 Analisis Kadar Glukosa menggunakan Asam Dinitrosalisilat ... 13
BAB III METODOLOGI PENELITIAN ... 15
3.1 Alat dan Bahan yang digunakan... 15
3.2 Tahapan Kegiatan Penelitian ... 16
3.2.2 Tahap kedua ( Pelaksanaan) ... 17
3.3 Metode Penelitian ... 19
3.3.1 Metode Pengambilan Data ... 19
3.3.2 Metode Analisis... 20
3.4 Kondisi Operasi ... 20
3.4.1 Kondisi Operasi Tetap ... 20
3.4.2 Variasi Konsentrasi Substrat dan Enzim ... 20
3.5 Pengolahan Data ... 21
BAB IV HASIL DAN PEMBAHASAN ... 22
4.1 Proses Hidrolisis Enzimatis ... 22
4.2.Analisis Gula Reduksi menggunakan Uji DNS (Asam Dinitrosalisilat)... 26
4.3 Kandungan Gula Reduksi Pada Hasil Akhir ... 29
4.4 Analisis Karakteristik Produk ... 31
BAB V KESIMPULAN DAN SARAN ... 32
5.1 Kesimpulan... 32
5.2 Saran ... 32
DAFTAR TABEL
Tabel 2. 1 Sifat Amilograf tepung sorgum... 12
Tabel 2. 2 Perbandingan Kandungan Nutrisi Tepung Sorgum dan Terigu. ... 12
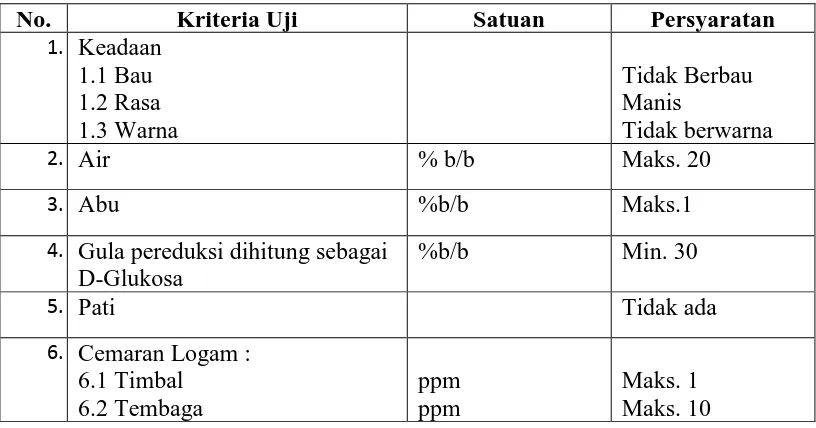
Tabel 2. 3 Standar mutu gula cair menurut SNI 01-2978-1992 ... 12
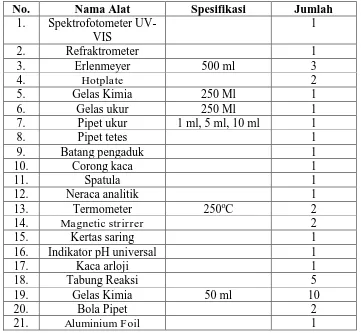
Tabel 3. 1 Peralatan yang akan digunakan ... 15
Tabel 3. 2 Bahan yang digunakan ... 15
Tabel 3. 3 Kandungan Tepung Sorghum Merah ... 16
Tabel 3. 4 Karakteristik enzim yang digunakan... 17
Tabel 3. 5 Variasi Konsentrasi Substrat dan Enzim ... 20
Tabel 3. 6 Data kinerja enzim ... 21
DAFTAR GAMBAR
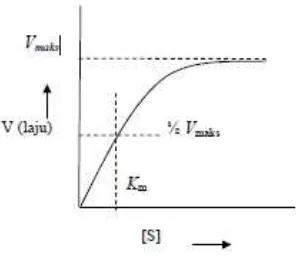
Gambar 2. 1 Hubungan antara konsentrasi substrat dengan laju reaksi enzim ... 7
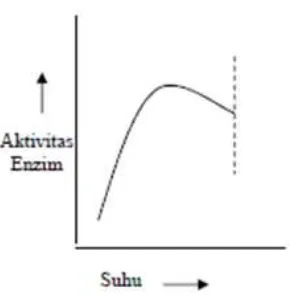
Gambar 2. 2 Hubungan suhu dengan aktivitas enzim (Shahib, 2005) ... 8
Gambar 2. 3 Mekanisme kerja α-amilase... 10
Gambar 2. 4 Tanaman Sorgum merah. ... 11
Gambar 3. 1 Penelitian pembentukan gula reduksi dari tepung sorgum merah .... 19
Gambar 3. 2 Kurva Standar Glukosa ... 21
Gambar 4.1 Konsentrasi gula total pada likuifikasi konsentrasi substrat 10% ... 22
Gambar 4.2 Konsentrasi gula total pada likuifikasi konsentrasi substrat 20% ... 23
Gambar 4.3 Konsentrasi gula total pada likuifikasi konsentrasi substrat 30% ... 23
Gambar 4.4 Konsentrasi gula total pada likuifikasi konsentrasi substrat 40%. .... 24
Gambar 4.5 Konsentrasi gula total pada sakarafikasi konsentrasi substrat 10% .. 25
Gambar 4.6 Konsentrasi gula total pada sakarafikasi konsentrasi substrat 20% .. 25
Gambar 4.7 Konsentrasi gula total pada sakarafikasi konsentrasi substrat 30% .. 26
Gambar 4.8 Konsentrasi gula total pada sakarafikasi konsentrasi substrat 40% .. 26
Gambar 4.9 Konsentrasi gula reduksi dengan variasi konsentrasi substrat 10% .. 27
DAFTAR LAMPIRAN
LAMPIRAN A DAFTAR RIWAYAT HIDUP
LAMPIRAN B PROSEDUR PENELITIAN
LAMPIRAN C HASIL PENELITIAN DAN PENGOLAHAN DATA
LAMPIRAN D DOKUMENTASI
LAMPIRAN E FORMULIR BIMBINGAN KAMPUS
BAB I PENDAHULUAN
1.1 Latar Belakang
Industri makanan dan minuman mulai banyak menggunakan gula cair
karena memiliki beberapa kelebihan antara lain gula cair tidak mengkristal, lebih
mudah diproses karena lebih mudah larut, lebih praktis, dan memiliki tampilan
yang lebih menarik jika dibandingkan dengan gula pasir pada umumnya.
Daerah penghasil sorgum dengan pola pengusahaan tradisional adalah
Jawa Tengah (Purwodadi, Pati, Demak, Wonogiri), Daerah Istimewa Yogyakarta
(Gunung Kidul, Kulon Progo), Jawa Timur (Lamongan, Bojonegoro, Tuban,
karakteristiknya pada penelitian sebelumnya. Kandungan pati tepung sorgum
tidak terlalu tinggi jika dibandingan dengan kandungan pati bahan lainnya, dan
juga tepung sorgum tidak mengandung gluten seperti pada terigu. Oleh karena itu
tepung sorgum tidak dapat digunakan sebagai pengganti tepung terigu pada
industri bakery (roti dan sebagainya) (Suarni, 2012), selain itu tepung sorgum belum banyak dimanfaatkan sebagai bahan pangan seperti beras, singkong dan
jagung, sehingga perlu dicari alternatif untuk lebih mengoptimalkan
manfaatannya, yaitu dengan cara diolah menjadi gula cair.
Untuk menjadi gula cair, tepung sorgum merah perlu di hidrolisis terlebih
dahulu, hidrolisis dapat dilakuan dengan katalis asam dan enzimatis. Tetapi,
hidrolisis dengan katalis asam mempunyai kelemahan, antara lain memerlukan
peralatan yang tahan korosi dan terbentuknya senyawa inhibitor seperti furfural,
5-hydroxymethylfurfural (HMF) selama proses hidrolisis asam (Millati dkk,
2002). Hidrolisis enzimatis lebih efektif dilakukan karena katalis enzim bekerja
secara spesifik sehingga hasil hidrolisis dapat dikendalikan, mencegah adanya
menghidrolisis serat adalah enzim selulase dan enzim yang menghidrolisis pati adalah enzim α–amylase dan glukoamilase (Selviana, 2014)
Menurut Risnoyatiningsih (2011) Pati ubi jalar kuning dapat dibuat
sebagai bahan baku pembuatan sirup glukosa dengan proses hidrolisis enzim.
Semakin lama waktu inkubasi dan semakin besar penambahan enzim
glukoamilase, maka glukosa yang didapatkan semakin besar. Untuk membuat
glukosa dari pati ubi jalar kuning dan untuk mendapatkan hasil tertinggi 5,64%
kadar glukosa, konversi 66,08%, diperlukan kondisi proses pada suhu 60°, pH 4,5
dengan penambahan enzim glukoamilase 0,07 ml dengan waktu hidrolisis 5 hari.
Menurut Permanasari dan Yulistiani (2015) Gula cair dapat dihasilkan
dari hidrolisis pati dengan bantuan α-amilase dan glukoamilase pada
perbandingan 1:1.Kecepatan hidrolisis yang optimum diperoleh pada penambahan
volume enzim sebanyak 0,3 ml dengan substrat 33,3% yaitu sebesar 32% Brix,
dengan total waktu liquifikasi dan sakarifikasi 40 menit.
Melihat dari penelitian sebelumnya, maka pada penelitian ini akan dibuat
gula cair dari pati sorgum merah dengan cara hidrolisis enzimatis menggunakan α-amilase dan glukoamilase. Hal tersebut yang menjadikan topik ini diangkat sebagai tugas akhir sebagai salah satu syarat untuk menyelesaikan program studi
D4 – Teknik Kimia Produksi Bersih.
1.2Rumusan Masalah
a. Bagaimana pengaruh konsentrasi substrat dan enzim pada pembuatan gula cair
dari tepung sorgum merah secara hidrolisis enzimatis.
b. Mencari kondisi optimum proses pembuatan gula cair dari tepung sorgum
merah ditinjau dari laju hidrolisis dan konsentrasi gula reduksi yang dihasilkan.
1.3 Tujuan Penelitian
Tujuan dari penelitian ini adalah:
a. Mempelajari pengaruh konsentrasi substrat dan enzim pada pembuatan gula
-amilase dan gluko-amilase yang ditinjau dari konsentrasi gula reduksi yang
dihasilkan.
b. Menentukan kondisi optimum dari pembuatan gula cair dari tepung sorgum
merah untuk menghasilkan gula reduksi maksimum.
1.4 Ruang Lingkup Penelitian
Ruang lingkup penelitian ini dilakukan dalam batas lingkup sebagai berikut.
a. Menggunakan bahan baku yaitu tepung sorghum merah dengan ukuran
partikel 125 µm.
b. Menggunakan katalisator yaitu enzim α-amilase dan glukoamilase.
c. Menggunakan variasi jumlah enzim 0,033 ppm , 0,067 ppm dan 0,1 ppm
serta konsentrasi substrat 10%, 20%, 30%, dan 40% (b/v). (Permanasari,
2017)
d. Karakteristik enzim yang digunakan yaitu α-amilase 148,39 kNu/g dan
glukoamilase 293 AGU/g. (Permanasari, 2017)
e. Proses gelatinasi, likuifikasi dan sakarifikasi (semua proses) diatur pada pH 6
f. Temperatur yang digunakan pada proses hidrolisis enzimatis adalah
Gelatinasi 50 oC (Tepung sorgum pada 50 oC sudah menggumpal) ,
Likuifikasi 90 oC, dan Sakarifikasi 60 oC. Pemurnian 80 oC (Proses
Pemucatan larutan). (Permanasari, 2017)
g. Waktu yang digunakan adalah Likuifikasi 1 jam, Sakarifikasi 2 jam,
Pemurnian 15 menit
h. Analisis yang akan dilakukan yaitu :
• Analisis kadar air pada tepung sorghum merah
• Analisis gula total dengan menggunakan Refraktometer
• Analisis gula reduksi dengan Uji DNS
BAB II
dalam Herawati (2011). Pati merupakan homopolimer glukosa dengan ikatan α- glikosidik. Berbagai macam pati tidak sama sifatnya, tergantung dari panjang
rantai C-nya serta lurus atau bercabang rantai molekulnya. Pati terdiri dari 2 fraksi
yang dapat dipisahkan dengan air panas. Fraksi terlarut disebut amilosa dan fraksi
yang tidak larut disebut amilopektin (Risnoyatiningsih, 2011).
Amilosa merupakan suatu polimer rantai tunggal tidak bercabang, terbentuk
dari 500-20.000 monomer α-D-glukosa yang dihubungkan oleh ikatan α-1,4
glikosidik. Sedangkan amilopektin adalah suatu polimer rantai bercabang terbentuk dari 100.000 monomer glukosa yang dihubungkan oleh ikatan α-1,4 glikosidik pada rantai utama dan α-1,6 glikosidik pada percabangannya
(Kunamneni, 2005). Kandungan amilosa pada tepung sorgum termasuk dalam
kategori sedang dan sesuai untuk pangan yaitu mendekati terigu (20-25%). Rasio
amilosa dan amilopektin sangat menentukan produk akhir dari suatu bahan
makanan (Suarni, 2012).
Sebagian besar karbohidrat, terutama golongan monosakarida dan
beberapa golongan disakarida, mempunyai sifat mereduksi terutama dalam
suasana basa. Golongan tersebut biasa dikenal dengan gula pereduksi, contoh dari
gula pereduksi diantaranya yaitu: glukosa, fruktosa, galaktosa, laktosa dan
maltosa.(Kinanti, 2017)
2.1 Hidrolisis Pati
Hidrolisis adalah proses dekomposisi kimia dengan menggunakan bantuan air
untuk memisahkan ikatan kimia dari substansinya. Sedangkan Hidrolisis pati
amilum yang lebih sederhana seperti dekstrin, isomaltosa, dan glukosa (Terahara,
2004).
Produk hasil hidrolisis pati umumnya dikarakterisasi berdasarkan tingkat
derajat hidrolisisnya dan dinyatakan dengan nilai DE (Dekstrosa Equivalen) yang
menunjukkan prosentase dekstrosa murni dalam total padatan substrat yang
dihirolisis. Hidrolisis pati menjadi sirup glukosa melalui tiga tahapan, yaitu
gelatinisasi, likuifikasi, dan sakarifikasi (Rahmawati, 2015)
Faktor-faktor yang dapat mempengaruhi proses hidrolisis pati antara lain yaitu
konsentrasi substrat, konsentrasi enzim, suhu, pH dan lama proses hidrolisis.
Enzim mempunyai spesifitas yang tinggi, sehingga kinerja enzim akan optimal
jika substrat yang digunakan cocok dan dalam konsentrasi yang tepat. Selain itu
konsentrasi enzim juga berpengaruh terhadap likuifikasi sebab efektivas kerja
enzim berbanding lurus dengan konsentrasi enzim, sehingga semakin optimal
kerja enzim, maka proses hidrolisis juga akan semakin cepat (Jariyah, 2002).
2.1.1 Gelatinasi
Gelatinisasi merupakan proses awalan sebelum likuifikasi. Gelatinisasi
adalah proses pembengkakan granula pati akibat pemanasan yang memutus ikatan
hidrogen pada ikatan glikosida pati. Pembengkakan granula tersebut bersifat
irreversible atau tidak bisa kembali lagi ke bentuk semula. Likuifikasi yang dilakukan tanpa gelatinisasi terlebih dahulu akan membutuhkan waktu yang lebih
lama dibandingkan dengan substrat yang telah mengalami gelatinisasi (Mitsuki,
2005)
Proses Likuifikasi diawali dengan gelatinisasi pati atau pemanasan granula
pati dengan air hingga mengembang dan rusak, suhu pada gelatinasi diatur pada
kisaran 66 C, sehingga pati dapat terlarut yang ditandai dengan menurunnya viskositas larutan. (Ruiz, 2011)
2.1.2 Likuifikasi
Likuifikasi merupakan proses hidrolisis pati menjadi molekul-molekul
mencapai 15-20% atau sampai larutan berwarna merah bata jika direaksikan
dengan larutan iodin. (Misset, 2003)
Likuifikasi merupakan proses pencairan gel pati untuk memperoleh
viskositas yang lebih rendah dengan cara menghidrolisis pati menjadi
molekul-molekul yang lebih sederhana dari oligosakarida atau dekstrin melalui bantuan enzim α-amilase.
Aktivitas enzim α-amilase menentukan cepat lambatnya proses likuifikasi.
Enzim ini akan bekerja lebih cepat jika menggunakan substrat yang berbentuk gel
atau yang sebelumnya telah digelatinisasi. Likuifikasi dapat dilakukan pada suhu
105°C, pH 6 selama 5 menit atau pada suhu 95-97°C, pH 6 selama 1-3 jam
dengan menggunakan α-amilase termostabil. Enzim α-amilase ini memecah ikatan α -(1,4) glikosidik secara acak pada bagian dalam substrat dan menghasilkan gula reduksi dan dekstrin dengan rantai glukosa jumlah kecil. (Norman, 2001)
α-amilase
Pada tahap sakarifikasi dekstrin hasil likuifikasi akan dihidrolisis lebih
lanjut oleh enzim tunggal (glukoamilase) maupun enzim campuran (glukoamilase
dan pullulanase) yang biasa disebut dextrozyme untuk dikonversi menjadi
glukosa. (Whitehurts, 2002) Sakarifikasi dapat dilakukan pada suhu antara
55-60°C dengan pH 4.5 yang mana proses tersebut membutuhkan waktu antara 24-72
jam. (Goodfrey, 1996)
glukoamilase
(C6H12O5)10 + 10 H2O 10(C6H12O6)
Dekstrin Air Glukosa
2.2 Enzim
Enzim adalah suatu protein yang bertindak sebagai katalisator reaksi
biologis atau lebih sering disebut sebagai biokatalisator (Mahartantri, 2005).
Menurut Winarno dan Fardianz (1984), dengan adanya katalisator enzim suatu
reaksi dapat dipercepat kira-kira 1012 sampai 1020 kali jika dibandingkan dengan
reaksi tanpa katalisator. Berdasarkan hukum Michaelis-Menten kecepatan reaksi
akan meningkat seiring dengan meningkatnya konsentrasi substrat. Kecepatan
reaksi akan terus meningkat dengan nilai yang semakin kecil hingga mencapai
titik batas dimana enzim jenuh dengan substrat. Faktor-faktor yang mempengaruhi
kerja enzim adalah :
a. Konsentrasi enzim
Konsentrasi enzim secara langsung mempengaruhi kecepatan laju reaksi
enzimatik. Pada suatu konsentrasi substrat tertentu, laju reaksi bertambah
dengan bertambahnyakonsentrasi enzim (Poedjiadi, 1994).
b. Konsentrasi substrat
Laju reaksi enzimatik akan meningkat dengan bertambahnya konsentrasi
substrat rendah,bagian aktif enzim hanya menampung substrat sedikit. Bila
konsentrasi substrat diperbesar, makin banyak substrat yang berhubungan
dengan enzim pada bagian aktif, sehingga konsentrasi enzim-substrat makin
besar dan menyebabkan besarnya laju reaksi.Namun pada batas konsentrasi
substrat tertentu, semua bagian aktif telah dipenuhi substrat. Dalam kondisi
ini, bertambahnya konsentrasi enzim–substrat, sehingga jumlah hasil
reaksinya pun tidak bertambah (Poedjiadi, 1994). Hubungan antara
konsentrasi substrat dengan laju reaksi enzim ditunjukkan dalam Gambar 1
c. Suhu
Suhu dapat meningkatkan laju reaksi enzimatik sampai batas tertentu. Suhu
yang terlalu tinggi (jauh dari suhu optimum suatu enzim) akan
menyebabkan enzim terdenaturasi. Bila enzim terdenaturasi, maka bagian
aktifnya akan terganggu dan dengan demikian konsentrasi efektif enzim
menjadi berkurang. Hal ini menyebabkan laju reaksi enzimatik menurun
(Poedjiadi, 1994).
Gambar 2. 2 Hubungan suhu dengan aktivitas enzim (Shahib, 2005)
d. pH
Enzim Struktur ion enzim bergantung pada pH lingkungan. Enzim dapat
berbentuk ion positif dan ion negatif (zwitter ion). Dengan demikian perubahan pH akan mempengaruhi efektivitas bagian aktif enzim dalam
membentuk kompleks enzim–substrat. Selain itu, pH yang tinggi dapat
menyebabkan terjadinya proses denaturasi dan ini akan menghakibatkan
menurunnya aktivitas enzim. Enzim menunjukkan aktivitas maksimum pada
kisaran pH antara 4,5–8,0 (Winarno, 1986)
2.2.1 Enzim α-amilase
golongan yaitu termostabil (tahan panas) dan termolabil (tidak tahan panas). α
-amilase yang termostabil dapat diperoleh dari Bacillus lichenoformis, Bacillus subtilis, Bacillus stearothermop Hilus dan Bacillus amyloliquefaciens, sedangkan yang termasuk termolabil dihasilkan dari jamur seperti Aspergilus oryzae dan Aspergilus niger. α-amilase termodifikasi dapat bekerja pada suhu hingga 105-110ºC dengan kisaran pH 5.1-5.6 selama 60-180 menit. (Sivaramakrishnan, 2006)
Aktivitas enzim α-amilase dipengaruhi oleh beberapa faktor yang diantaranya adalah pH dan suhu. Enzim α-amilase mempunyai kondisi optimum
pada suhu 90-105°C dengan pH 5.6-6.0. Suhu yang terlampau tinggi dari kondisi
optimum akan menganggu dan merusak enzim, sedangkan pemberian suhu yang
terlampau rendah dari kondisi optimum akan menyebabkan gelatinisasi pati tidak
sempurna. (Richardson, 2002).
Aktivitas α-amilase ditentukan dengan mengukur hasil degradai pati, biasanya dari penurunan kadar pati yang larut atau dari kadar amilosa bereaksi dengan iodium akan berwarna coklat. Selain itu keaktivan α-amilase dapat dinyatakan dengan cara pengukuran viskositas dan jumlah pereduksi yang
terbentuk. (Winarno, 1995).
Cara kerja α-amilase pada molekul amilosa terjadi 2 tahap pertama,
degradasi amilosa menjadi maltosa dan maltotriosa yang terjadi secara acak.
Degradasi ini terjadi sangat cepat dan diikuti dengan menurunnya viskositas
dengan cepat. Yang kedua, relatif sangat lambat yaitu pembentukan glukosa dan maltosa sebagai hasil akhir yang terjadi secara tidak acak. Sedangkan cara kerja α -amilase pada molekul amilopektin akan menghasilkan glukosa, maltosa, dan α -limit dextrin. Jenis α- limit dextrin yaitu oligosakarida yang terdiri dari 4 atau lebih residu gula yang mengandung ikatan α-1,6. (Winarno, 1995)
Gambar 2. 3 Mekanisme kerja α-amilase.
(Rahmawati, A.Y., 2015)
2.2.2 Glukoamilase
Glukoamilase yang dikenal juga dengan amiloglukosidase (AMG) atau α
-(1,4)-D- glukan glukohidrolase. Glukoamilase dapat dihasilkan dari jamur:
Aspergillus spp, Rhizopus oryzae, Rhizopus niveus, dari yeast: Saccharomycopsis fibuligera, Saccharomyces diasticus, dan dari bakteri : Clostridium acetobutylicum. Glukoamilase yang dihasilkan dari aspergillus awanori dan Aspergillus niger tergolong thermostabil dan mempunyai kisaran pH yang lebih optimal. Kedua mikroba tersebut sekarang secara universal digunakan untuk
sakarifikasi pati. Glukoamilase murni banyak digunakan untuk pembuatan sirup glukosa dari maltodekstrin yang diproduksi oleh α-amilase dari pemurnian pati.
Enzim glukoamilase bersifat eksoamilase, yaitu dapat memotong ikatan α -1,4 pada pati. Disamping itu glukoamilase juga dapat memotong ikatan α-1,6, sehingga molekul-molekul pati dapat dikonversikan menjadi molekul-molekul
glukosa bebas. Enzim glukoamilase (amiloglukosidase) mempunyai suhu
optimum 500C – 600C dan pH optimum 4,0 – 5,0 (Winarno, 1995).
Faktor-faktor yang mempengaruhi aktivitas dan stabilitas enzim
glukoamilase diantaranya adalah:
- Suhu, kondisi suhu optimum untuk enzim ini adalah 40-60°C.
- Nilai pH optimum untuk aktivitas enzim ini adalah 4,5.
- Waktu reaksi yang diperlukan untuk hidrolisis pati sekitar 48-96 jam
2.3 Sorgum
Sorgum merupakan tanaman asli dari wilayah-wilayah tropis dan subtropis di
bagian Pasifik Tenggara dan Australia, wilayah yang terdiri dari Australia,
Selandia Baru dan Papua. Sorgum merupakan tanaman dari keluarga Poaceae dan marga Sorghum. Sorgum sendiri memiliki 32 spesies. Diantara spesies-spesies tersebut, yang paling banyak dibudidayakan adalah spesies Sorghum bicolor. Tanaman ini sekeluarga dengan tanaman serealia lainnya seperti padi, jagung dan
gandum serta tanaman lain seperti bambu dan tebu (Daru, 2003).
Sorgum (Sorghum bicolor L. Moench) merupakan tanaman pangan penting kelima setelah padi, gandum, jagung, dan barley, dan menjadi makanan utama
lebih dari 750 juta orang di daerah tropis setengah kering di Afrika, Asia, dan
Amerika Latin. Di Indonesia sorgum merupakan tanaman sereal pangan ketiga
setelah padi dan jagung. Sorgum merupakan bahan pangan pendamping beras
yang mempunyai keunggulan komparatif terhadap serealia lain seperti jagung,
gandum, dan beras. Komoditas ini mempunyai kandungan nutrisi dasar yang tidak
kalah penting dibandingkan dengan serealia lainnya, dan mengandung unsur
pangan fungsional. Biji sorgum mengandung karbohidrat 73%, lemak 3,5%, dan
protein 10%, bergantung pada varietas dan lahan pertanaman.
Gambar 2. 4 Tanaman Sorgum merah.
Kandungan amilosa tepung varietas sorgum termasuk sedang dan sesuai
untuk pangan, mendekati terigu (20-25%). Rasio amilosa dan amilopektin sangat
menentukan produk akhir dari suatu bahan makanan. Sifat amilograf bahan
pangan memberikan petunjuk dalam pemilihan varietas yang sesuai dengan
antara 29,0-29,5 menit. Sementara suhu awal gelatinisasi berkisar antara
72,5-76,5°C. Berikut adalah sifat amilograf dari beberapa varietas tepung sorgum.
Tabel 2. 1 Sifat Amilograf tepung sorgum
.
Varietas
Awal gelatinase Granul pati pecah Viskositas
Waktu
Sumber: Suarni dan Firmansyah (2005)
Tabel 2. 2 Perbandingan Kandungan Nutrisi Tepung Sorgum dan Terigu.
Kandungan Nutrisi
Tepung Terigu Tepung Sorgum
UPCA-SI Isiap Dorado
Standar mutu gula cair dapat di lihat di bawah ini :
Tabel 2. 3 Standar mutu gula cair menurut SNI 01-2978-1992
No. Kriteria Uji Satuan Persyaratan
1. Keadaan
6.3 Seng ppm Maks. 25
analisis sebagai berikut :
2.4.1 Analisis Kadar Gula Total menggunakan Portable Brix
Portable Brix Meter merupakan alat yang dapat digunakan untuk
mengukur besarnya konsentrasi larutan yang terkandung di dalam suatu larutan.
Satuan skala pembacaan Portable Brix Meter adalah %Brix. Brix adalah zat
padat kering yang terlarut dalam suatu larutan yang dihitung sebagai
sukrosa. Brix juga dapat didefinisikan sebagai prosentase massa sukrosa yang
terkandung di dalam massa larutan sukrosa. Sedangkan massa larutan sukrosa
adalah massa sukrosa yang ditambah dengan massa pelarutnya. (Eko, 2010)
Menurut Rohman dan Soemantri (2007) ,kadar gula total merupakan
kandungan gula keseluruhan dalam suatu bahan pangan yang terdiri dari gula
pereduksi dan gula non-pereduksi. Sehingga yang terhitung pada kadar gula total
yaitu gula reduksi dan non-reduksi, yang terdiri dari golongan monosakarida,
disakarida, oligosakarida dan polisakarida. Gula pereduksi diantaranya yaitu
glukosa, fruktosa, galatoksa, laktosa dan maltosa.
2.4.2 Analisis Kadar Glukosa menggunakan Asam Dinitrosalisilat
Analisa residu glukosa sebagai gula reduksi dilakukan menggunakan reagen
asam dinitrosalisilat (DNS). Dalam analisa ini terlebih dahulu dibuat kurva
standar glukosa. Metode DNS adalah metode penentuan kadar gula reduksi
dengan menggunakan pereaksi asam 3,5 – dinitrosalisilat. Menurut Miller (1959)
metode ini digunakan untuk menguji keberadaan gugus karbonil bebas atau yang
biasa disebut dengan gula reduksi. Gugus karbonil didapatkan dari reaksi oksidasi
gugus aldehid dalam glukosa atau gugus keton dalam fruktosa. Selain reaksi
dinitrosalisilat (DNS) menjadi 3 – amino, 5 – asam nitrosalisilat. Reaksi yang
terjadi adalah sebagai berikut :
✓ Gugus aldehid
oksida si
gugus karbonil
✓ Asam 3,5 – dinitrosalisilat
reduksi
3 – amino, 5 – asam nitrosalisilat
Reaksi di atas menunjukkan bahwa 1 mol gula (gugus aldehid) akan
bereaksi dengan 1 mol asam 3,5 – dinitrosalisilat. Reaksi oksidasi glukosa dapat
dipengaruhi oleh oksigen terlarut, karena itu ditambahkan sulfit ke dalam larutan
pereaksi DNS untuk menyerap oksigen terlarut tersebut. Selain itu juga
BAB III
METODOLOGI PENELITIAN
3.1 Alat dan Bahan yang digunakan
Alat dan bahan yang dipergunakan dalam pelaksanaan penelitian ini ditunjukkan
dalam Tabel 3.1 dan Tabel 3.2 sebagai berikut.
Tabel 3. 1 Peralatan yang akan digunakan
No. Nama Alat Spesifikasi Jumlah
1. Spektrofotometer
UV-Tabel 3. 2 Bahan yang digunakan
No. Nama Bahan Spesifikasi Jumlah Sumber
1. Tepung sorgum
4. Aquades 20 Liter Toko Kimia (Brathachem)
5. Karbon aktif serbuk Teknis Toko Kimia
6. Kapur tohor (CaO) Teknis Toko Kimia
Dinitrosalisilat
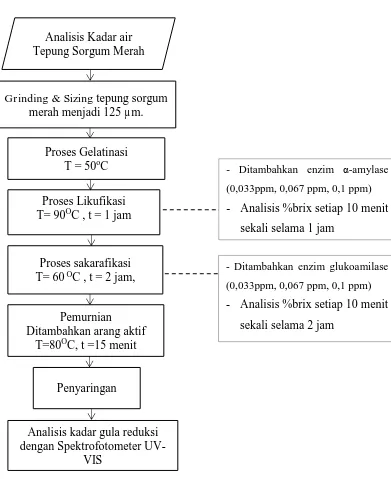
Kegiatan Penelitian “Pengaruh Konsentrasi Substrat dan Enzim Terhadap Produk Gula Reduksi Pada Pembuatan Gula Cair dari Tepung Sorgum Merah
Secara Hidrolisis Enzimatis” dengan bahan tepung sorgum merah yang
mempunyai ukuran 125 µm akan dilaksanakan dengan metode eksperimen secara
hidrolisis enzimatis. Proses pembuatan gula cair ada 2 tahapan utama yaitu proses
hidrolisis pati dan pemurnian gula cair. Hidrolisis pati yang meliputi proses
gelatinasi, likuifikasi, sakarifikasi, sedangkan pemurnian gula cair, meliputi
pemucatan, serta penyaringan.
3.2.1 Tahap Pertama (Persiapan Awal)
Tepung Sorgum Merah dianalisis terlebih dahulu kandungan kadar airnya.
Setelah itu, dilakukan pengubahan ukuran tepung sorgum merah dengan
menggunakan alat grinding & sizing dengan ukuran 125 µm. Tepung sorghum merah ditimbang sesuai dengan konsentrasi susbtrat 10%, 20%, 30%, dan 40%.
Berikut dibawah ini adalah kandungan tepung sorghum merah dan karakteristik
enzim α-amilase dan glukoamilase.
Tabel 3. 3 Kandungan Tepung Sorghum Merah
Tabel 3. 4 Karakteristik enzim yang digunakan
No Karakteristik Enzim Enzim
α-amilase Glukoamilase
1 Bentuk Cair Cair
2 Aktivitas Enzim 148,39(KNU/g) 293(AGU/g)
3 Densitas (g/ml) 1,244 g 1,155
4 Total viable count (/g) < 100 < 200 5 Bakteri Koliform (/g) < 4 < 4
3.2.2 Tahap kedua ( Pelaksanaan)
a) Proses Gelatinasi
Membuat suspensi pati sebagai substrat sebanyak 300 ml dengan variasi
konsentrasi 10% , 20%, 30% dan 40 (b/v) yang dipanaskan hingga suhu 50oC
sebagai proses gelatinasi hingga larutan mengental.
b) Proses Likuifikasi
Setelah proses gelatinisasi dilanjutkan dengan Likuifikasi suhu operasi diatur
90oC. Ditambahkan enzim α-amylase dengan variasi volume enzim 0,033 ppm ,
0,067 ppm dan 0,1 ppm , diaduk menggunakan magnetic stirer lalu pH diatur 6-6,4 dengan menambahkan kapur CaO jika diperlukan. Substrat menjadi
benar-benar cair dan berwarna coklat bening selama 1 jam dan disampling setiap 10
menit untuk dilakukan analisis kadar gula total menggunakan alat Refraktometer.
Sedangkan pada menit 30 dan 60 dilakukan analisis gula reduksi dengan uji DNS
menggunakan spektrofotometer Lalu setelah itu, suhu larutan kemudian
diturunkan hingga 60 C.
c) Proses Sakarifikasi
diaduk mengunakan magnetic stirer . Lalu dilakukan analisis kadar gula total menggunakan Refraktometer setiap 10 menit selama 2 jam. Disetiap 30 menit
sekali dan produk dilakukan analisis gula reduksi menggunakan spektrofotometer.
d) Pemurnian
Proses pemurnian gula reduksi dilakukan dengan proses pemucatan larutan.
Larutan hidrolisis dicampurkan dengan sedikit arang aktif dan dipanaskan hingga
suhu 80C selama 15 menit.
e) Penyaringan
Setelah proses pemucatan lalu dilakukan penyaringan. Campuran substrat dan
arang aktif selanjutnya disaring hingga diperoleh filtrat berwarna kuning muda.
Kadar gula reduksi dianalisis menggunakan metode spektrofotometri UV-VIS
Gambar 3. 1 Penelitian pembentukan gula reduksi dari tepung sorgum merah
3.3 Metode Penelitian
3.3.1 Metode Pengambilan Data
Pada proses likuifikasi, data sampel gula diambil setiap 10 menit sekali dalam
kurun waktu 1 jam dan 2 jam pada saat proses sakarafikasi untuk menganalisis
kadar gula total. Data pada setiap 30 menit sekali dari keseluruhan proses,
dianalisis untuk mengetahui kadar gula reduksi. Untuk produk, dilakukan Analisis Kadar air
Grinding & Sizing tepung sorgum merah menjadi 125 µm.
- Analisis %brix setiap 10 menit
sekali selama 1 jam
- - Ditambahkan enzim glukoamilase (0,033ppm, 0,067 ppm, 0,1 ppm)
- Analisis %brix setiap 10 menit
pengambilan sample untuk mengetahui karakteristik produk maka dianalisis
densitas dan pH nya.
3.3.2 Metode Analisis
Analisis yang dilakukan adalah analisis kandungan gula total menggunakan
metode refraktometer untuk mengetahui nilai %brix, analisis gula reduksi
menggunakan metode Uji DNS dengan alat Spektrofotometer UV-VIS dengan
ukuran gelombang 540 nm, analisis karakterstik produk yaitu dengan metode
piknometer untuk mengetahui massa jenis dan metode pH meter untuk
mengetahui nilai pH.
3.4 Kondisi Operasi
3.4.1 Kondisi Operasi Tetap
a) pH 6 untuk proses gelatinasi, likuifikasi dan sakarifikasi (semua proses)
b) Temperatur
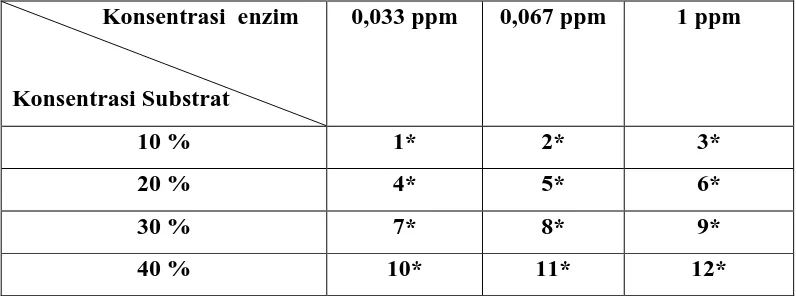
3.4.2 Variasi Konsentrasi Substrat dan Enzim
Tabel 3. 5 Variasi Konsentrasi Substrat dan Enzim
3.5 Pengolahan Data
Data yang diolah meliputi perhitungan konsentrasi gula reduksi, perhitungan
standar glukosa, perhitungan kecepatan kerja enzim, memebuat grafik nilai %Brix
terhadap waktu, membuat kurva standar glukosa, membuat kurva konsentrasi gula
reduksi terhadap waktu, membuat kurva konsentrasi gula reduksi terhadap
konsentrasi substrat.
Berdasarkan pada Gambar 3.3 didapatkan garis lurus (intercept) sebesar y = 0,5559x digunakan untuk menentukan konsentrasi gula reduksi
Gambar 3. 2 Kurva Standar Glukosa
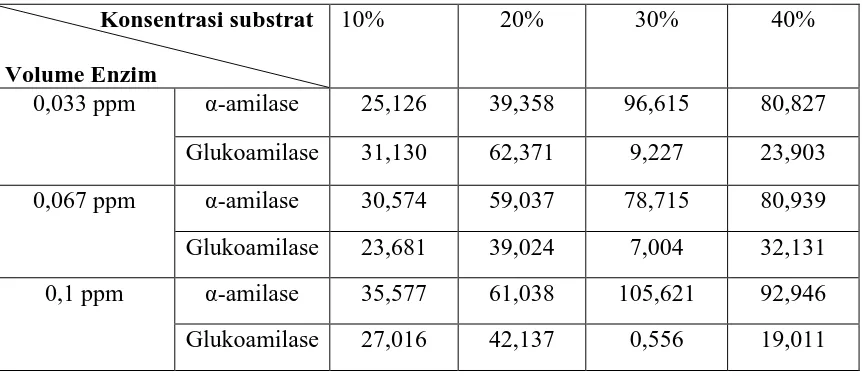
Tabel 3. 6 Data kinerja enzim
Konsentrasi substrat
Glukoamilase 23,681 39,024 7,004 32,131
BAB IV
HASIL DAN PEMBAHASAN 4.1 Proses Hidrolisis Enzimatis
Pada proses hidrolisis pati terjadi menjadi glukosa melalui tiga tahapan,
yaitu gelatinisasi, likuifikasi, dan sakarifikasi. Proses gelatinasi terjadi pada saat
konsentrasi substrat yang dilarutkan dalam aquadest dipanaskan pada temperatur
50oC hingga mengental. Gelatinasi untuk merenggangkan ikatan-ikatan yang ada
pada amilosa dan amilopektin sehingga lebih memudahkan enzim bekerja..
Pemecahan amilosa dan amilopektin yang terdapat pada tepung sorghum
merah menjadi gula reduksi (glukosa) terjadi melalui proses likufisasi dan
sakarafikasi yang terjadi selama tiga jam dengan variasi konsentrasi substrat dan
volume enzim. Sebagai batasan untuk proses hidrolisis (likufikasi dan
sakarafikasi) adalah waktu hidrolisis selama tiga jam.
Gula total dapat diukur menggunakan refraktometer untuk mengetahui
nilai %brixnya. Nilai brix diukur setiap 10 menit selama proses berlangsung.
Kenaikan konsentrasi gula total sebanding dengan pembentukan gula reduksi dari
proses hidrolisis tepung sorghum merah.
Pada proses likuifikasi dengan enzim α-amilase yang divariasikan volumenya
terjadi selama satu jam dengan temperatur 90oC. Hasil dari proses likufisasi dapat
ditinjau dari gambar dibawah ini.
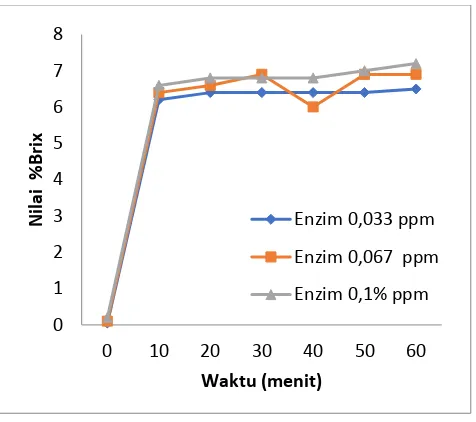
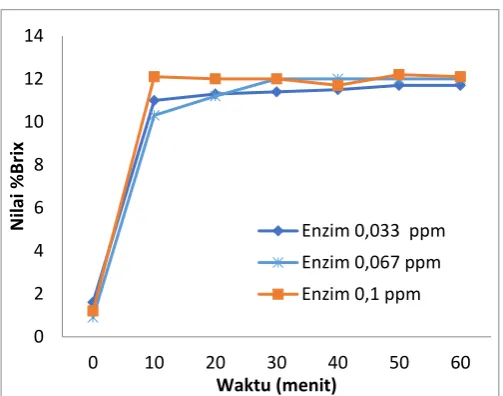
Gambar 4. 1 Kurva Peningkatan Konsentrasi Gula Total pada proses likuifikasi dengan variasi konsentrasi substrat 10% dengan masing masing variasi konsentrasi Enzim
Gambar 4. 2 Kurva Peningkatan Konsentrasi Gula Total pada proses likuifikasi dengan variasi konsentrasi substrat 20% dengan masing masing variasi konsentrasi Enzim
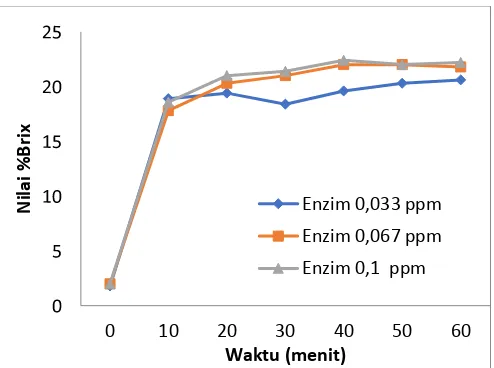
Gambar 4. 3 Kurva Peningkatan Konsentrasi Gula Total pada proses likuifikasi dengan variasi konsentrasi substrat 30% dengan masing masing variasi konsentrasi Enzim
Gambar 4. 4 Kurva peningkatan konsentrasi gula total pada proses likuifikasi dengan variasi konsentrasi substrat 40% dengan masing-masing variasi konsentrasi enzim.
Berdasarkan gambar diatas, dapat dilihat bahwa untuk semua variasi enzim
diberbagai konsentrasi pada menit 10 nilai brix mulai meningkat. Peningkatan
nilai brix terjadi secara perlahan ini menunjukkan bahwa α-amilase dapat
mengubah pati sorgum merah dengan cepat karena aktivitas enzim yang tinggi.
Peningkatan konsentrasi gula total yang ditunjukkan dengan% brix sama dengan
kenaikan konsentrasi gula pereduksi (Permanasari, 2017).
Pada gambar 4.1 (a) nilai brix konstan pada 6-7%, (b) konstan pada 12%, (c)
konstan pada 16-17%, (d) nilai brix konstan pada 22%. Hal ini menunjukan
bahwa setiap konsentrasi substrat menghasilkan gula total cukup tinggi pada
proses lukifisasi dalam 10 menit pertama, dan akan meningkat hingga konstan
karena substrat (amilosa dan amilopektin) hampir habis pada larutan susbtrat
tersebut. Sedangkan untuk konsentrasi substrat terendah (a) total gula maksimum
terbentuk sampai brix 7% karena 10% merupakan konsentrasi substrat terendah
sehingga kandungan amilosa dan amilopektin yang menjdai glukosa juga paling
rendah. Selain itu konsentrasi enzim juga berpengaruh terhadap likuifikasi sebab
efektivas kerja enzim berbanding lurus dengan konsentrasi enzim, sehingga
semakin optimal kerja enzim, maka proses hidrolisis juga akan semakin cepat
(Jariyah, 2002).
Proses sakarafikasi terjadi pada saat proses likufisasi berakhir yaitu pada
yang bekerja yaitu menggunakan enzim glukoamilase. Pada proses sakarafikasi
tidak terjadi peningkatan yang signifikan dari total konsentrasi gula total. Hasil
menunjukkan bahwa kurva meningkat secara fluktuatif, tetapi masih dalam nilai
konstan, hal ini dapat disebabkan karena pengaruh suhu yang tidak seragam.
Meskipun praktikan telah mengatur suhu pada yang sama pada hotplate saat proses hidrolisis, tetapi pengaruh suhu dari lingkungan juga mempengaruhi.
Gambar 4. 5 Kurva peningkatan konsentrasi gula total pada proses sakarafikasi dengan variasi konsentrasi substrat 10% dengan masing-masing variasi konsentrasi enzim
Gambar 4. 6 Kurva peningkatan konsentrasi gula total pada proses sakarafikasi dengan variasi konsentrasi substrat 20% dengan masing-masing variasi konsentrasi enzim
Gambar 4. 7 Kurva peningkatan konsentrasi gula total pada proses sakarafikasi dengan variasi konsentrasi substrat 30% dengan masing-masing variasi konsentrasi enzim
Gambar 4. 8 Kurva peningkatan konsentrasi gula total pada proses sakarafikasi dengan variasi konsentrasi substrat 40% dengan masing-masing variasi konsentrasi enzim
4.2. Analisis Gula Reduksi menggunakan Uji DNS (Asam Dinitrosalisilat) Analisis gula reduksi dengan menggunakan spektrofotometer lebih akurat
dibandingkan dengan analisis menggunakan refraktometer, karena menggunakan
reagen. Reagen yang digunakan adalah DNA (Asam Dinitrosalisilat) atau biasa
disebut dengan uji DNS, metode ini digunakan untuk menguji keberadaan gugus
karbonil bebas atau yang biasa disebut dengan gula reduksi.(Miller,1959)
sehingga dapat diketahui konsentrasi glukosa yang didapatkan.
Hasil dari analisis gula reduksi menggunakan spektrofotometer dapat dilihat pada
dibawah ini.
Gambar 4. 9 Kurva Peningkatan Konsentrasi gula reduksi dengan variasi konsentrasi substrat 10 % dan variasi volume enzim
Gambar 4. 10 Kurva Peningkatan Konsentrasi gula reduksi dengan variasi konsentrasi substrat 20 % dan variasi volume enzim
Gambar 4. 11 Kurva Peningkatan Konsentrasi gula reduksi dengan variasi konsentrasi substrat 30 % dan variasi volume enzim
Gambar 4. 12 Kurva Peningkatan Konsentrasi gula reduksi dengan variasi konsentrasi substrat 40% dan variasi volume enzim
Berdasarkan gambar diatas terjadi peningkatan gula reduksi secara
signifikan di setiap konsentrasi. Kinerja enzim bekerja dengan konsentrasi
substrat dengan mendegradasi amilosa dan amilopektin menjadi glukosa.
Peningkatan gula reduksi pada menit 60 (likuifikasi) hingga 90 (sakarafikasi)
terjadi peningkatan yang cukup tinggi yaitu pada saat proses sakarafikasi. Hal ini
terajadi karena pada proses sakarafikasi dengan menggunanakan enzim
glukoamilase dapat memotong ikatan α-1,4 dan α-1,6 pada amilosa dan
amilokpetin menjadi molekul-molekul glukosa bebas.
Proses lukifikasi menggunakan bantuan enzim α-amilase, dimana enzim
ini bekerja dengan memecahkan ikatan α-(1,4)-glikosida dari bagian dalam secara
acak pada amilosa maupun amilopektin. Sedangkan pada proses sakarafikasi
dengan bantuan enzim glukoamilase dapat memotong ikatan α-1,4 pada pati. Disamping itu glukoamilase juga dapat memotong ikatan α-1,6, sehingga molekul-molekul pati dapat dikonversikan menjadi molekul-molekul glukosa
bebas.(Winarno, 1995)
4.3 Kandungan Gula Reduksi Pada Hasil Akhir
Gambar 4. 13 Grafik Peningkatan Gula Reduksi Pada Hasil Akhir
Berdasarkan Gambar 4.13 Konsentrasi gula reduksi tertinggi dihasilkan
oleh konsentrasi substrat 40% dan terendah 10%. Semakin tinggi konsentrasi
substrat semakin tinggi produk yang dihasilkan, produk yang paling tinggi adalah
amilokleptin lebih sedikit dan larutan sangat encer karena banyak mengandung
air.
Dapat dilihat perbedaan nilai konsentrasi gula yang dihasilkan dari tabel
diatas pada konsentrasi substrat 10% konsentrasi gula reduksi rata rata 81 g/l
untuk konsentrasi substrat 20% rata rata konsentrasi gula reduksi 135 g/l kenaikan
konsentrasi gula yang dihasilkan sekitar 45%. Tetapi untuk selanjutnya pada
konsentrasi 30% dan 40% konsentrasi gula rata rata yang dihasilkan adalah 138
g/l dan 144 g/l. Kenaikan konsentrasi gula reduksi pada konsentrasi substrat 20%,
30% dan 40% tidak terlalu signifikan. Sehingga, dengan konsentrasi substrat 20%
dapat menghasilkan produk yang tinggi karena ditinjau dari segi ekonomis
perbedaanya dengan konsentrasi substrat 40% tidak terlalu tinggi. Bertambahnya
konsentrasi substrat tidak menyebabkan bertambahya konsentrasi kompleks enzim
substrat, sehingga produk reaksi tidak bertambah besar (Poedjadi, 1994). Dapat
dikatakan bahwa semakin banyak volume enzim tidak menentukan menghasilkan
produk paling besar karena produk yang dihasilkan lebih berpengaruh pada
konsentrasi substrat.
Kemampuan enzim paling baik adalah 0,067 ppm karena produk paling
tinggi pada konsentrasi enzim 0,067 ppm. Tetapi untuk kecepatan hidrolisis yang
paling baik adalah 0,1 ppm. Semakin banyak enzim laju hidrolisis semakin cepat,
tetapi tidak selalu menghasilkan produk yang paling tinggi. Pada proses hidrolisis
aktivias enzim berpengaruh pada produksi gula reduski. Semakin tinggi
konsentrasi enzim maka kecepatan reaksi akan meningkat hingga batas
konsentrasi tertentu. Namun, hasil hidrolisis substrat akan konstan dengan
naiknya konsentrasi enzim. Hal ini disebabkan penambahan enzim sudah tidak
efektif lagi (Reed, 1975).
Laju aktivitas enzim akan meningkat dengan meningkatnya kadar substrat
sampai suatu titik. Sekali enzim jenuh dengan substrat, penambahan kadar
4.4 Analisis Karakteristik Produk
Tabel 4. 1 Analisis data karakteristik produk
Konsentrasi Volume enzim
pemucatan dan penyaringan, pH tidak dilakukan pengukuran kembali. pada proses
pemucatan ditambahkan dengan karbon aktif, setelah ditambahkan karbon aktif
yang dapat menurunkan nilai pH, sehingga pH akhir yang yaitu pada rentang
4,6-5,2.
Dari tabel diatas dapat dilihat bahwa dengan bertambahnya konsentrasi
substrat dan enzim, bertambah juga densitasnya. Densitas yang terbesar adalah
1,104 g/cm3dengan konstrasi substrat yaitu 40% dan volume enzim 0,1 ppm.
Densitas yang paling besar ini menunjukan terbentuknya gula cair yang lebih
besar karena semakin tinggi massa jenis suatu benda, maka semakin besar pula
massa setiap volumenya Dibandingkan dengan konsentrasi substrat dan volume
BAB V
KESIMPULAN DAN SARAN
5.1 Kesimpulan
Dari penelitian ini dapat disimpulkan :
1. Dari range konsentrasi substrat 10%-40%, konsentrasi gula reduksi
tertinggi diperoleh pada konsentrasi substrat 40% dengan volume enzim
0,067 ppm sebesar 115,7384 g/l.
2. Kerja enzim yang paling baik adalah pada volume 0,067 pada proses
likuifikasi ppm tidak pada 0,1 ppm
5.2 Saran
Saran yang dapat diberikan untuk memperbaiki penelitian ini untuk penelitian
selanjutnya adalah:
1. Untuk mengetahui gula reduksi tidak perlu mengukur nilai brix
menggunakan refraktometer, tetapi langsung di ukur nilai gula reduksi
dengan menggunakan spektrofotometer dengan reagen DNS.
2. Pada saat proses pemucatan, sebaiknya pH di ukur sehingga produk gula
cair tetap terjaga pada rentang 6-6,4. Untuk hasil yang dapat lebih
terpantau sebaiknya pengukuran pH juga dilakukaan sebelum proses
likuifikasi.
3. Penelitian selanjutnya disarankan dengan range konsentrasi substrat
DAFTAR PUSTAKA
Goodfrey, T and S. West. 1996. Industrial Enzymology Second Edition. Macmillan Press Ltd. London.
Herawati, Heny. 2011. Potensi Pengembangan Produk Pati Tahan Cerna sebagai
Pangan Fungsional. Jurnal Litbang Pertanian, 30(1), 2011. Balai
Pengkajian Teknologi Pertanian, Jawa Tengah
Hidayanto, Eko., Rofiq, Abdul., Sugito, Heri., 2010. Aplikasi Portable Brix Meter
untuk Pengukuran Indeks Bias. Vol. 13, No. 4, hal 113 – 118. Undip.
Semarang.
Imaningsih, Nelis. 2012. Profil Gelatinisasi Beberapa Formulasi
Tepung-tepungan. Untuk Pendugaan Sifat Pemasakan. Penel Gizi Makan 2012,
35(1): 13-22.
Jariyah. 2002. Analisis Komponen Gula Pada Sirup Maltosa Hasil Hidrolisis Pati
Garut Secara Enzimatis. Tesis. UB. Malang.
Kinanti, Langen. 2017.Praktikum Analisis Kadar Gula Reduksi, Kadar Gula Total
dan Kadar Pati.Jurnal Fakultas Teknologi Industri Pertanian Universitas
Padjajaran
Kunamneni, A., Permaul, K., dan Singh, S. 2005. Amylase production in solid state fermentation by the thermophilic fungus Thermomyces lanuginosus, Journal of Bioscience and Bioengineering. Vol. 100 (2): 168-171.
Lehninger, A. L., 1982, Dasar-dasar Biokimia, Jlilid 1, Alih bahasa, Maggi
Thenawijaya, Erlangga, Jakarta.
Mahartantri, L., 2005. Pembuatan Glukosa Kasar dari Pati Beberapa
Varietas/Klon Ubi Jalar (Ipomea batatas l.) Secara Hidrolisis Enzimatis.
Skripsi. Jurusan Teknologi Hasil Pertanian. Unibraw.
Miller, G.L., 1958. Use of Dinitrosalicylic Acid Reagent for Determination of Reducing Sugar. Analytical Chemistry - ANAL CHEM , vol. 31, no. 3, pp. 426-428.
Misset, O. 2003. Xylose (Glucose) Isomerase. In J.R. Whitaker., A.G.J. Voragen., and D.W.S. Wong (ed). Handbook of Food Enzymology. Marcell
Dekker, Inc. New York.
Mitsuiki S, Mukaea K, Sakai M, Goto M, Hayashida S, Furukawa K. 2005. Comparative Characterization of Raw Starch Hydrolizing α Amylase from Various Bacillus Strains. J. Enzmic Tech 37, 410-416.
Norman H, and Vang. 2001. Enzymatic Preparation of Glucose Syrup from Starch. United State Patent. 6.267.826.
Permanasari, Ayu R., Yulistiani, Fitria. 2015. “Pembuatan Gula Cair Dari Pati Singkong Dengan Menggunakan Hidrolisis Enzimatis” Jurnal Fluida Teknik Kimia Polban.
Permanasari A R, Yulistiani F, Djenar N S. 2017. Liquid Sugar Production From Red Sorghum Starch As Raw Material To Produce High Fructose Syrup (HFS). Advanced Science Letters Volume 23 Number 6 June 2017 American Scientific Publishers pp: 5775-5779.
Permanasari, Ayu R., Yulistiani, Fitria.,2017.Production of High Fructose Syrup by Enzymatic Hydrolysis in Various Enzyme and Substrate Concentration of Red Sorghum Starch.
Permanasari A R, Yulistiani F, Purnama R W, Widjaja T, Gunawan S. 2017. The Effect of Enzyme and Substrate Concentration on the Fructose Syrup Production by Enzymatice Hydrolysis. Unpublished.
Poedjiadi, A. 1994. Dasar-dasar Biokimia (Edisi Revisi). UI Press. Jakarta. 476
hlm.
Rahmawati, A.Y., Sutrisno, A. 2015 Hidrolisis Tepung Ubi Jalar Ungu (Ipomea Batatas L.) Secara Enzimatis Menjadi Sirup Glukosa Fungsional: Kajian Pustaka. Jurnal Pangan dan Agroindustri Vol. 3 No 3 p.1152-1159.
Reed, G. 1975. Enzymes in Food Processing. Academic Press. New York. 212. Richardson, T.H, Tan, X., Frey, G., Callen, W., Cabell, M., Lam, D. Macomber,
Risnoyatiningsih, Sri., 2011, “Hidrolisis Pati Ubi Jalar Kuning Menjadi Glukosa Secara Enzimatis”, UPN Veteran Jawa Timur: Jurnal Teknik Kimia Vol.5, N0.2.
Robi’a, Sutrisno, Aji., 2015, “Karakteristik Sirup Glukosa Dari Tepung Ubi Ungu (Kajian Suhu Likuifikasi Dan Konsentrasi Α-Amilase)”, Kajian Pustaka. Jurnal Pangan dan Agroindustri Vol. 3 No 4 p.1531-1537.
Rohman, A., Soemantri. 2007. Analisis Makanan. Universitas Gadjah Mada, Jawa
Tengah.
Ruiz, Monica I., Shancez, Clara I., Torres, Rodrigo G., Molina, Daniel R., 2011, “Enzymatic Hydrolysis of Cassava Starch for Production of Bioethanol with a Colombian Wild Yeast Strain”, Brazil: J. Braz. Chem. Soc., Vol. 22, No. 12, 2337-2343.
Selviana. 2014. Pengaruh Konsentrasi Enzim Selulase, Α–Amilase Dan Glukoamilase Terhadap Kadar Gula Reduksi Dari Onggok. Bandar
Lampung : Universitas Lampung.
Sirappa, M.P. 2003.Prospek pengembangan sorgum di Indonesia sebagai
komoditas alternatif untuk pangan, pakan, dan industri.Jurnal Litbang
Pertanian 22(4):133-140.
Shahib, N. 2005. Biologi Molekular Medik I. Unpad Press. Bandung
Sivaramakrishnan S, Gangadaran D, Nampoothiri K.M, Soccol C.R, Pandey A.
2006. α-Amylase From Microbial Sources An Overview on Recent Developments. Journal of Food Technology and Biotechnology 44 : 2, 173–184.
Standar Nasional Indonesia. 1992. SNI 01-2978-1992 - Sirup Glukosa. Pusat Standardisasi Industri Departemen Perindustrian.
Suarni dan I.U. Firmansyah. 2005, “Potensi sorgum varietas unggul sebagai bahan pangan untuk menunjang agroindustry”, Prosiding Lokakarya Nasional BPTP Lampung, Universitas Lampung. p.541-546.
Suarni, 2012, “Potensi Sorgum sebagai Bahan Pangan Fungsional”, IPTEK TANAMAN PANGAN VOL. 7 NO. 1 (58-66).
Storage Root of Purple-Fleshed Sweet Potato, Ipomoea batatas L.” Journal of Biomedicine and Biotechnology.2004:5. 279–286.
Triyono, Agus., 2008, Karakteristik Gula Glukosa Dari Hasil Hidrolisis Pati Ubi
Jalar (Ipomoea Batatas, L.) Dalam Upaya Pemanfaatan Pati Umbi –
Umbian, Prosiding Seminar Nasional Teknoin 2008 Bidang Teknik
Kimia dan Tekstil (B7-B1).
Volk WA and MF Wheeler. 1988. Mikrobiologi Dasar. Jilid 1. S Adisoemarto (Ed.). Erlangga, Jakarta. Terjemahan dari Basic Microbiology 5* Ed. Whitehurts, R.J. and B.A. Law. 2002. Enzymes in Food Technology. Sheffield
Academic Press. Canada.
Winarno, F.G dan Fardianz, S. 1984. Biofermentasi dan Biosintesa Protein.
Penerbit Angkasa. Bandung.
Winarno, 1995, “Enzim Pangan”, Penerbit PT Gramedia Utama, Jakarta
LAMPIRAN A
DAFTAR RIWAYAT HIDUP
BIODATA MAHASISWA
Nama : Mira Auliya Tsaqila
NIM : 141424021
Kelas : 4A D4-Teknik Kimia Produksi Bersih
Alamat : kp. Kepuh kelapa 2. RT01/RW17. Karangpawitan.
Karawang 41315
No. Hp : 085846683557
Email : miratsaqila@gmail.com
Judul Tugas Akhir : Pengaruh Konsentrasi Substrat dan Enzim Terhadap Produk
Gula Reduksi Pada Pembuatan Gula Cair dari Tepung
Sorgum Merah Secara Hidrolisis Enzimatis
Dosen Pembimbing : Ayu Ratna Permanasari, ST., MT.
Mahasiswa yang melaksanakan TA
BIODATA MAHASISWA
Nama : Dahliana Alami
NIM : 141424008
Kelas : 4A D4-Teknik Kimia Produksi Bersih
Alamat : Desa Mekarsari RT 02/01 Kecamatan Jatisari, Kabupaten
Karawang 41374
No. Hp : 089649877440
Email : dahlianalami@gmail.com
Judul Tugas Akhir : Pengaruh Konsentrasi Substrat dan Enzim Terhadap Produk
Gula Reduksi Pada Pembuatan Gula Cair dari Tepung
Sorgum Merah Secara Hidrolisis Enzimatis
Dosen Pembimbing : Ayu Ratna Permanasari, ST., MT.
Mahasiswa yang melaksanakan TA
LAMPIRAN B
Prosedur Penelitian
1. Analisis Kadar Glukosa menggunakan DNS
Langkah-langkah yang dilakukan untuk analisa kadar gula reduksi :
A. Prosedur Pembuatan Larutan Standar Glukosa
1. Membuat larutan persediaan dengan cara mencampurkan 0,1 g glukosa dalam 100
mL aquadest.
2. Membuat larutan standar glukosa dengan mengencerkan larutan persediaan (1)
dengan pengenceran 0:5, 1:4, 2:3, 3:2, 4:1, 5:0
B. Prosedur Pembuatan Larutan DNS
1. Melarutkan 16 g NaOH dalam 200 mL aquades, kemudian ditambahkan 10 g
larutan DNS dan diaduk menggunakan stirrer sampai benar-benar larut.
2. Melarutkan 30 g NaK-tartrat dan 8 g Na-metabisulfit kedalam 500 ml aquadest.
3. Mencampurkan larutan (1) dengan (2) dan ditambahkan aquades sampai 1000 mL.
C. Prosedur Pembuatan Kurva Standar Glukosa
1. Mencampurkan 2 mL larutan persediaan yang mengandung glukosa dengan 3 mL
larutan DNS.
2. Memanaskan campuran dalam air mendidih selama 15 menit.
3. Mendinginkan campuran (2) menggunakan es atau air mengalir.
4. Mengulangi langkah (1) – (3) untuk konsentrasi larutan glukosa berbeda.
5. Mengukur dan mencatat absorbansi pada spektrophotometer UV-VIS dengan
panjang gelombang 540 nm.
6. Membuat grafik dengan memplot antara kadar glukosa sebagai gula reduksi dengan
absorbansi.
D. Prosedur Pembuatan Larutan Blanko
1. Mencampurkan 2 mL aquades dengan 3 mL larutan DNS.
2. Memanaskan campuran dalam air mendidih selama 5 menit.
3. Mendinginkan campuran (2) menggunakan es atau air mengalir.
E. Prosedur Analisis Sampel
1. Mencampurkan larutan sampel yang telah diencerkan 200 kali menggunakan
aquades dengan 3 mL larutan DNS.
3. Mendinginkan campuran (2) menggunakan es atau air mengalir.
4. Mengulangi langkah (1) – (3) untuk sampel yang berbeda.
5. Mengukur dan mencatat absorbansi pada spektrophotometer dengan panjang
gelombang 540 nm.
6. Mensubstitusi absorbansi yang diperoleh dengan persamaan dari kurva standar
glukosa.
Analisis Hasil
Analisis dilakukan terhadap gula reduksi, meliputi :
a. Analisis gula total dan gula reduksi hasil pada proses likuifikasi dan
sakarifikasi menggunakan alat Refraktometer.
b. Analisis kadar gula reduksi pada produk akhir gula cair menggunakan pereaksi
DNS dan diukur absorbansinya menggunakan spektrofotometer UV-VIS.
c. Analisis karakteristik produk akhir gula reduksi yaitu berat jenis menggunakan
LAMPIRAN C
HASIL PENELITIAN DAN
1. Penentuan Gula Total (%Brix) menggunakan Refraktometer
Tabel B.1 Data %Brix Konsentrasi Substrat 10%
%Brix
Tabel B.2 Data %Brix Konsentrasi Substrat 20%
140 12 12,1 13
150 12,2 12,3 12,4
160 12 12 12,8
170 11,6 11,8 12,8
180 12 12,2 12,8
Tabel B.3 Data %Brix Konsentrasi Substrat 30%
%Brix
Tabel B.4 Data %Brix Konsentrasi Substrat 40%
80 20,9 22,3 22,4
Tabel B.5 Data Standar Glukosa
No Glukosa Aquades Absorbansi Konsentrasi (g/L)
1 0 5 0,002 0
2 1 4 0,406 0,2
3 2 3 0,787 0,4
4 3 2 1,008 0,6
• Perhitungan Penentuan Standar Glukosa Gula = 0,1 gram
3. Penentuan Gula Reduksi Menggunakan Uji DNS
Tabel B.6 Analisis Glukosa Pada Konsentrasi Substrat 10%
Menit Absorbansi Konsentrasi glukosa (g/l)
0,033 ppm 0,067 ppm 0,1 ppm 0,033 ppm 0,067 ppm 0,1 ppm 30 0,236 0,264 0,287 26,23848 29,35152 31,90866 60 0,239 0,288 0,333 26,57202 32,01984 37,02294
120 0,458 0,71 0,471 50,92044 78,9378 52,36578 150 0,503 0,484 0,538 55,92354 53,81112 59,81484 180 0,519 0,501 0,576 57,70242 55,70118 64,03968
Hasil 0,57 0,575 0,582 63,3726 63,9285 64,70676
Tabel B.7 Analisis Glukosa Pada Konsentrasi Substrat 20%
Menit Absorbansi Konsentrasi gula (g/l)
Tabel B.8 Analisis Glukosa Pada Konsentrasi Substrat 30%
Menit Absorbansi Konsentrasi Gula (g/l)
0,033 ppm 0,067 ppm 0,1 ppm 0,033 ppm 0,067 ppm 0,1 ppm
Tabel B.9 Analisis Glukosa Pada Konsentrasi Substrat 40%
Menit Absorbansi Konsentrasi Gula (g/l)
• Perhitungan Menentukan Konsentrasi Gula (g/l)
Dari kurva standar glukosa didapatkan intersep sebesar y = 0,5559x
Contoh :
- Konsentrasi Substrat 40%
Pengenceran : 200x
Waktu : 30 menit
Volume Enzim : 0,033 ppm
Absorbansi : 0,537
Konsentrasi Gula y = 0,5559 (g/l) x 0,537
= 0,3807x 200
= 59,70366 g/l
Tabel B.10 Data Konsentrasi Gula (g/l) hasil
konsentrasi enzim
Konsentrasi Gula (g/l)
10% 20% 30% 40%
LAMPIRAN D
No. Gambar Keterangan
1. Tepung Sorghum
dihaluskan terlebih dahulu sebelum dimasukkan ke sieve shaker dan diambil ukuran partikel 125 µm.
2. Tepung sorgum
berukuran 125 µm ditimbang terlebih dahulu sebelum memasuki proses selanjutnya.
3. Proses likuifikasi,
4. Proses penyaringan
5. Uji DNS
LAMPIRAN E
LAMPIRAN F
LAMPIRAN G
Pengaruh Konsentrasi Substrat dan Enzim Terhadap Produk
Gula Reduksi Pada Pembuatan Gula Cair dari Tepung
Sorgum Merah Secara Hidrolisis Enzimatis
ORIGINALITY REPORT
19
%
14
%
4
%
10
%
SIMILARITY INDEX INTERNET SOURCES PUBLICATIONS STUDENT PAPERS
PRIMARY SOURCES
Submitted to Politeknik Negeri Bandung
1
Student Paper
5
%
Kwan, Alice M., Alexander G. Fung, Peter A.
2
Jansen, Michael Schivo, Nicholas J. Kenyon,
Jean-Pierre Delplanque, and Cristina E. Davis.
"Personal Lung Function Monitoring Devices for
Asthma Patients", IEEE Sensors Journal, 2015.
Publication3
%
repository.uinjkt.ac.id
3
repository.usu.ac.id
4
Internet Source
2
%
eprints.uns.ac.id
5
Internet Source
1
%
www.scribd.com
6
Internet Source
1
%
obvil.paris-sorbonne.fr
7 Internet Source
1
%
eprints.upnyk.ac.id
8
Internet Source
<
1
%
dokumen.tips
9
Internet Source
<
1
%
digilib.unimed.ac.id
10
Internet Source
<
1
%
repository.ipb.ac.id
11
perpustakaan.untirta.ac.id
12
Internet Source
<
1
%
digilib.polban.ac.id
13
Internet Source
<
1
%
eprints.ums.ac.id
14
Internet Source
<
1
%
rludifkunjani.wordpress.com 15
Internet Source
<
1
%
repository.its.ac.id
16
Internet Source
<
1
%
Submitted to Fakultas Ekonomi Universitas
17
Indonesia
Student Paper
<
1
%
library.polmed.ac.id
repository.unhas.ac.id
19 Internet Source
<
1
%
Exclude quotes Off Exclude matches Off