LAPORAN PRAKTIKUM BIOKIMIA LAPORAN PRAKTIKUM BIOKIMIA “
“ANALISIS KUANTITATIF KADAR PROTEIN TELUR PUYUHANALISIS KUANTITATIF KADAR PROTEIN TELUR PUYUH DENGAN METODE BIURET SECARA SPEKTROFOTOMETRI” DENGAN METODE BIURET SECARA SPEKTROFOTOMETRI”
DISUSUN OLEH DISUSUN OLEH DEVI AYU SEPTIANI DEVI AYU SEPTIANI
[E1M 015 020] [E1M 015 020]
PROGRAM STUDI PENDIDIKAN PROGRAM STUDI PENDIDIKAN
FAKULTAS KEGURUAN DAN ILMU PENGETAHUAN FAKULTAS KEGURUAN DAN ILMU PENGETAHUAN
UNIVERSITAS MATARAM UNIVERSITAS MATARAM
2017 2017
▸ Baca selengkapnya: biuret mengandung zat
(2)Analisis Kuantitatif Kadar Protein Telur
Analisis Kuantitatif Kadar Protein Telur Puyuh dengan Metode BiuretPuyuh dengan Metode Biuret secara Spektrofotometri
secara Spektrofotometri
A.
A. AbstrakAbstrak
Tujuan dari pratikum analisis kuantitatif kadar protein telur puyuh Tujuan dari pratikum analisis kuantitatif kadar protein telur puyuh dengan metode Biuret secara spektrofotometri ini adalah untuk menganalisis dengan metode Biuret secara spektrofotometri ini adalah untuk menganalisis kandungan protein pada telur puyuh dengan metode Biuret, dan memahami kandungan protein pada telur puyuh dengan metode Biuret, dan memahami penggunaaan
penggunaaan spektrofotometer spektrofotometer sebagai sebagai alat alat untuk untuk menganalisis menganalisis kadarkadar protein. Metode
protein. Metode biuret digunakan untuk biuret digunakan untuk menganalisis adanmenganalisis adanya ikatan peptidaya ikatan peptida dengan cara menambahkan reagen biuret ke dalam sampel yang kemudian dengan cara menambahkan reagen biuret ke dalam sampel yang kemudian diukur absorbansinya menggunakan spektrofotometer. Sampel yang diukur absorbansinya menggunakan spektrofotometer. Sampel yang digunakan pada praktikum ini adalah sampel putih telur puyuh. Protein digunakan pada praktikum ini adalah sampel putih telur puyuh. Protein merupakan senyawa organik kompleks yang memiliki berat molekul tinggi. merupakan senyawa organik kompleks yang memiliki berat molekul tinggi. Protein adalah salah satu bio-makromolekul yang penting peranannya bagi Protein adalah salah satu bio-makromolekul yang penting peranannya bagi semua organisme.
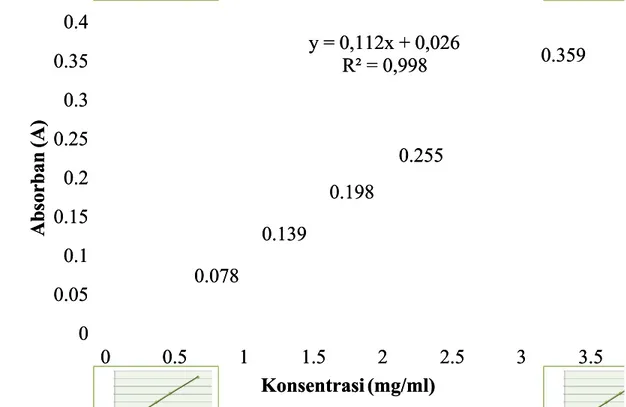
semua organisme. Berdasarkan hasil praktikum Berdasarkan hasil praktikum didapatkan persamaan didapatkan persamaan garisgaris liniear y = 0.112x + 0.026 sehingga konsentrasi
liniear y = 0.112x + 0.026 sehingga konsentrasi yang didapat sebesar 0.1383yang didapat sebesar 0.1383 gr/100ml, dari hasil yang didapat pada praktikum tidak berbeda jauh dengan gr/100ml, dari hasil yang didapat pada praktikum tidak berbeda jauh dengan literatur yaitu pada konsentrasi hasil penilitian pada literatur sebesar 0,1323 literatur yaitu pada konsentrasi hasil penilitian pada literatur sebesar 0,1323 gr/100ml. Kurva pada hasil pengamatan menunjukkan perbandingan antara gr/100ml. Kurva pada hasil pengamatan menunjukkan perbandingan antara absorbansi dengan konsentrasi kaseinnya dimana didapat kurva garis lurus absorbansi dengan konsentrasi kaseinnya dimana didapat kurva garis lurus (linear) yang artinya semakin tinggi nilai konsentrasi kaseinnya maka (linear) yang artinya semakin tinggi nilai konsentrasi kaseinnya maka semakin tinggi nilai absorbansinya.
semakin tinggi nilai absorbansinya.
Kata kunci : protein, putih telur puyuh, metode biuret Kata kunci : protein, putih telur puyuh, metode biuret
B.
B. PendahuluanPendahuluan
Telur merupakan salah satu sumber protein hewani yang banyak Telur merupakan salah satu sumber protein hewani yang banyak dikonsumsi dan memberikan sumbangan besar bagi tercapainya kecukupan dikonsumsi dan memberikan sumbangan besar bagi tercapainya kecukupan gizi masyarakat. Pada satu butir telur terkandung hampir semua zat gizi gizi masyarakat. Pada satu butir telur terkandung hampir semua zat gizi yang diperlukan oleh tubuh dan mudah dicerna, salah satunya mengandung yang diperlukan oleh tubuh dan mudah dicerna, salah satunya mengandung semua asam amino essensial yang dibutuhkan tubuh untuk hidup sehat. semua asam amino essensial yang dibutuhkan tubuh untuk hidup sehat. Fungsi dari kandungan protein yang terdapat pada telur antara lain sebagai Fungsi dari kandungan protein yang terdapat pada telur antara lain sebagai
▸ Baca selengkapnya: percobaan telur dan cuka
(3)zat pembagun tubuh, baik pembentuk sel-sel yang baru maupun mengganti zat pembagun tubuh, baik pembentuk sel-sel yang baru maupun mengganti sel-sel yang rusak. Kandungan zat gizi atau kadar protein pada telur didapat sel-sel yang rusak. Kandungan zat gizi atau kadar protein pada telur didapat pada
pada berbagai berbagai jenis jenis telur telur baik baik telur telur ayam ayam ras, ras, telur telur ayam ayam kampung, kampung, telurtelur bebek, telur puyuh, dan lain-lain,
bebek, telur puyuh, dan lain-lain, dimana kadar protein pada dimana kadar protein pada masing-masingmasing-masing jenis telur berbeda-beda (Hidayati dan Mardiono, 2009).
jenis telur berbeda-beda (Hidayati dan Mardiono, 2009).
Burung puyuh (coturnix coturnix japanica) merupakan salah satu Burung puyuh (coturnix coturnix japanica) merupakan salah satu unggas yang sedang dikembangkan dan ditingkatkan produksinya. Selain unggas yang sedang dikembangkan dan ditingkatkan produksinya. Selain menghasilkan daging, burung puyuh juga merupakan produsen telur dengan menghasilkan daging, burung puyuh juga merupakan produsen telur dengan produktivitas
produktivitas cukup cukup tinggi tinggi yaitu yaitu 200-300 200-300 butir/ekor/tahun. butir/ekor/tahun. dilihat dilihat dari dari nilainilai kandungan gizinya telur puyuh mengandung 13.6% protein dan 8.2% lemak kandungan gizinya telur puyuh mengandung 13.6% protein dan 8.2% lemak (Schaible, 1970).
(Schaible, 1970).
Protein merupakan senyawa organik kompleks yang memiliki berat Protein merupakan senyawa organik kompleks yang memiliki berat molekul tinggi. Protein adalah salah satu bio-makromolekul yang penting molekul tinggi. Protein adalah salah satu bio-makromolekul yang penting peranannya
peranannya bagi bagi semua semua organisme. organisme. Protein Protein juga juga berperan berperan penting penting dalamdalam struktur dan fungsi semua sel makhluk hidup dan virus. Molekul protein struktur dan fungsi semua sel makhluk hidup dan virus. Molekul protein mengandung karbon, hidrogen, oksigen, nitrogen dan kadang kala sulfur mengandung karbon, hidrogen, oksigen, nitrogen dan kadang kala sulfur serta fosfor. Keistimewaan lain dari protein ini adalah strukturnya yang serta fosfor. Keistimewaan lain dari protein ini adalah strukturnya yang mengandung N (15.30 - 18%), C (52.40%), H (6.90
mengandung N (15.30 - 18%), C (52.40%), H (6.90
–
–
7.30%), O (21 7.30%), O (21–
–
23.50%), S (0.8 - 2%), disamping C, H, O (Seperti juga karbohidrat dan 23.50%), S (0.8 - 2%), disamping C, H, O (Seperti juga karbohidrat dan lemak), dan S kadang-kadang P, Fe dan Cu (sebagai senyawa kompleks lemak), dan S kadang-kadang P, Fe dan Cu (sebagai senyawa kompleks dengan protein (Sudarmaji, 1989).dengan protein (Sudarmaji, 1989).
Analisis protein dapat dilakukan dengan dua metode, yaitu secara Analisis protein dapat dilakukan dengan dua metode, yaitu secara kualitatif dan secara kuantitatif. Analisis protein secara kualitatif terdiri atas kualitatif dan secara kuantitatif. Analisis protein secara kualitatif terdiri atas reaksi Xantoprotein, reaksi Hopkins-Cole, reaksi Milon, reaksi Nitroprusida reaksi Xantoprotein, reaksi Hopkins-Cole, reaksi Milon, reaksi Nitroprusida dan reaksi Sakaguchi. Sedangkan analisis protein secara kuantitatif terdiri dan reaksi Sakaguchi. Sedangkan analisis protein secara kuantitatif terdiri dari metode Kjeldahl, metode titrasi formol, metode Lowry, metode dari metode Kjeldahl, metode titrasi formol, metode Lowry, metode spektrofotometri visible (Biuret), dan metode spektrofotometri UV spektrofotometri visible (Biuret), dan metode spektrofotometri UV (Maligan, 2014).
(Maligan, 2014).
Metode biuret merupakan salah satu larutan yang digunakan untuk uji Metode biuret merupakan salah satu larutan yang digunakan untuk uji protein.
protein. Larutan Larutan ini ini merupakan merupakan campuran campuran antara antara ion ion kupri kupri sulfat sulfat yangyang dimasukkan dalam suasana basa, cntohnya CuSO4.5H2O yang dimasukkan dimasukkan dalam suasana basa, cntohnya CuSO4.5H2O yang dimasukkan
atau dicampur dengan NaOH. Uji ini menunjukkan adanya atau dicampur dengan NaOH. Uji ini menunjukkan adanya senyawa-senyawa yang mengandung gugus amida asam yang berada bersama gugus senyawa yang mengandung gugus amida asam yang berada bersama gugus amida yang lain. Larutan ini digunakan untuk mendeteksi protein dalam amida yang lain. Larutan ini digunakan untuk mendeteksi protein dalam jumlah
jumlah besar besar yang yang ditandai ditandai dengan dengan adanya adanya perubahan perubahan warna. warna. Jika Jika suatusuatu sampel diuji mengandung lebih dari 2 ikatan peptida maka akan muncul sampel diuji mengandung lebih dari 2 ikatan peptida maka akan muncul warna ungu yang berarti uji ini menghasilkan reaksi positif. Warna ini warna ungu yang berarti uji ini menghasilkan reaksi positif. Warna ini muncul karena terbentuknya ikatan koordinasi kompleks antara atom Cu muncul karena terbentuknya ikatan koordinasi kompleks antara atom Cu dengan 4 atom nitrogen yang berasal dari ikatan paeptida (Clark,1964). dengan 4 atom nitrogen yang berasal dari ikatan paeptida (Clark,1964).
Spektrofotometer UV-vis merupakan alat dengan teksnik Spektrofotometer UV-vis merupakan alat dengan teksnik spektrofotometer pada daerah ultra violet (UV) dan sinar tampak (visible). spektrofotometer pada daerah ultra violet (UV) dan sinar tampak (visible). Alat ini digunakan untuk mengukur serapan sinal ultra violet atau sinar Alat ini digunakan untuk mengukur serapan sinal ultra violet atau sinar tampak oleh suatu materi atau larutan. Konsentrasi larutan yang dianalisis tampak oleh suatu materi atau larutan. Konsentrasi larutan yang dianalisis sebanding dengan jumlah sinar yang diserap oleh zat yang terdapat dalam sebanding dengan jumlah sinar yang diserap oleh zat yang terdapat dalam larutan tersebut (Daintith, 2004).
larutan tersebut (Daintith, 2004).
C.
C. Alat dan Bahan PraktikumAlat dan Bahan Praktikum
1.
1. AlatAlat
Alat-alat yang digunakan pada praktikum analisa kuantitatif protein Alat-alat yang digunakan pada praktikum analisa kuantitatif protein dengan metode biuret secara spektrofotometri ini adalah sebagai berikut: dengan metode biuret secara spektrofotometri ini adalah sebagai berikut: a.
a. Tabung reaksiTabung reaksi b.
b. ErlenmeyerErlenmeyer c.
c. Pipet tetesPipet tetes d.
d. Labu takar 100 mlLabu takar 100 ml e.
e. Gelas ukur 25 mlGelas ukur 25 ml f.
f. Gelas kimia 100 mlGelas kimia 100 ml g. g. PengadukPengaduk h. h. SpatulaSpatula i. i. KuvetKuvet j.
j. Neraca analitik Neraca analitik k.
2.
2. BahanBahan
Bahan-bahan yang digunakan pada praktikum analisa kuantitatif Bahan-bahan yang digunakan pada praktikum analisa kuantitatif protein dengan metode
protein dengan metode biuret sbiuret secara spektrofotometri ecara spektrofotometri ini adalah ini adalah sebagaisebagai berikut:
berikut: a.
a. Putih telur puyuhPutih telur puyuh b.
b. Tembaga (II) sulfat (CuSOTembaga (II) sulfat (CuSO44..55HH22O)O)
c.
c. Kalium natrium tartrat (KNaCKalium natrium tartrat (KNaC44HH44OO44.4H.4H22O)O)
d.
d. Serum albumin murni atau kaseinSerum albumin murni atau kasein e. e. NaOH 3% NaOH 3% f. f. NaOH 10% NaOH 10% g. g. AquadesAquades D.
D. Prosedur KerjaProsedur Kerja
1.
1. Pembuatan Reagen BiuretPembuatan Reagen Biuret a.
a. Menyiapkan alat dan bahan yang digunakan.Menyiapkan alat dan bahan yang digunakan. b.
b. Menimbang 150 mg tembaga (II) sulfat (CuSOMenimbang 150 mg tembaga (II) sulfat (CuSO44..55HH22O) dan 150 mgO) dan 150 mg
Kalium natrium tartrat (KNaC
Kalium natrium tartrat (KNaC44HH44OO44.4H.4H22O) pada neraca analitik.O) pada neraca analitik.
c.
c. Melarutkan dengan aquades sebanyak 50 ml pada labu takar 100 ml,Melarutkan dengan aquades sebanyak 50 ml pada labu takar 100 ml, sedikit demi sedikit.
sedikit demi sedikit. d.
d. Menambahkan 30 ml NaOH 10% kedalam larutan sambil dikocok-Menambahkan 30 ml NaOH 10% kedalam larutan sambil dikocok-kocok.
kocok. e.
e. Mengencerkan larutan dengan aquades dalam labu takar 100 mlMengencerkan larutan dengan aquades dalam labu takar 100 ml samapi batas tera.
samapi batas tera.
(Bakhtra, 2016) (Bakhtra, 2016) .. 2.
2. Pembuatan Larutan Standar ProteinPembuatan Larutan Standar Protein a.
a. Menyiapkan alat dan bahan yang digunakan.Menyiapkan alat dan bahan yang digunakan. b.
b. Menimbang 300 mg serum albumin murni atau kasein pada neracaMenimbang 300 mg serum albumin murni atau kasein pada neraca analitik.
analitik. c.
c. Melarutkan dengan aquades sebanyak 100 ml sehingga konsentrasiMelarutkan dengan aquades sebanyak 100 ml sehingga konsentrasi larutannya 3 mg/ml.
d.
d. Menambahkan beberapa tetes NaOH 3% kedalam larutan sambilMenambahkan beberapa tetes NaOH 3% kedalam larutan sambil dikocok-kocok.
dikocok-kocok. e.
e. Mengukur absorbansi larutan dengan panjang gelombang 520 nmMengukur absorbansi larutan dengan panjang gelombang 520 nm menggunakan spektrofotometer.
menggunakan spektrofotometer.
3.
3. Pembuatan Kurva StandarPembuatan Kurva Standar a.
a. Menyiapkan alat dan bahan yang digunakan.Menyiapkan alat dan bahan yang digunakan. b.
b. Mengencerkan larutan standar pada masing-masing tabung reaksiMengencerkan larutan standar pada masing-masing tabung reaksi dengan konsentrasi yaitu 0.5 mg/ml, 1 mg/ml, 1.5 mg/ml, 2 mg/ml, dengan konsentrasi yaitu 0.5 mg/ml, 1 mg/ml, 1.5 mg/ml, 2 mg/ml, dan 3 mg/ml.
dan 3 mg/ml. c.
c. Memasukkan larutan standar pada 5 tabung reaksi, masing-masingMemasukkan larutan standar pada 5 tabung reaksi, masing-masing sebanyak 10 ml.
sebanyak 10 ml. d.
d. Melarutkan larutan standar yang digunakan dengan menambahkanMelarutkan larutan standar yang digunakan dengan menambahkan aquades dan reagen biuret, perbandingan volume aquades dan reagen aquades dan reagen biuret, perbandingan volume aquades dan reagen biuret yaitu 2 : 3.
biuret yaitu 2 : 3. e.
e. Menghitung masing-masing perbandingan volume aquades danMenghitung masing-masing perbandingan volume aquades dan reagen biuret untuk masing-masing konsentrasi yang diinginkan reagen biuret untuk masing-masing konsentrasi yang diinginkan dengan perbandingan 2 : 3.
dengan perbandingan 2 : 3. f.
f. Perbandingan volume aquades dan reagen biuret yang digunakanPerbandingan volume aquades dan reagen biuret yang digunakan untuk konsentrasi 0.5 mg/ml adalah 25ml : 36 ml, konsentrasi 1 untuk konsentrasi 0.5 mg/ml adalah 25ml : 36 ml, konsentrasi 1 mg/ml perbandingannya 12 ml : 18 ml, konsentrasi 1.5 mg/ml mg/ml perbandingannya 12 ml : 18 ml, konsentrasi 1.5 mg/ml perbandingannya 8 ml
perbandingannya 8 ml : : 12 ml, 12 ml, konsentrasi 2 konsentrasi 2 mg/ml perbandingan mg/ml perbandingan 66 ml : 9 ml, dan konsentrasi 3 mg/ml perbandingannya 4 ml : 6 ml. ml : 9 ml, dan konsentrasi 3 mg/ml perbandingannya 4 ml : 6 ml. g.
g. Menyimpan tabung pada suhu 37° C selama 10 menit ataMenyimpan tabung pada suhu 37° C selama 10 menit ata u pada suhuu pada suhu kamar selama 30 menit sampai terbentuk warna ungu sempurna. kamar selama 30 menit sampai terbentuk warna ungu sempurna. h.
h. Memasukkan masing-masing larutan standar yang sudah didiamkanMemasukkan masing-masing larutan standar yang sudah didiamkan pada kuvet.
pada kuvet. i.
i. Mengukur absorbansi dengan panjang 520 nm menggunakanMengukur absorbansi dengan panjang 520 nm menggunakan spektrofotometer.
4.
4. Preparasi SampelPreparasi Sampel a.
a. Menyiapkan alat dan bahan yang digunakan.Menyiapkan alat dan bahan yang digunakan. b.
b. Menimbang 1 gram putih telur puyuh dengan menggunakan neracaMenimbang 1 gram putih telur puyuh dengan menggunakan neraca analitik.
analitik. c.
c. Memasukkan putih telur puyuh kedalam erlenmeyer.Memasukkan putih telur puyuh kedalam erlenmeyer. d.
d. Melarutkan putih telur puyuh dengan menggunakan aquadesMelarutkan putih telur puyuh dengan menggunakan aquades sebanyak 100 ml.
sebanyak 100 ml. e.
e. Mengambil 1 ml larutan putih telur puyuh dan ditambahkan reagenMengambil 1 ml larutan putih telur puyuh dan ditambahkan reagen biuret pada tabung reaksi.
biuret pada tabung reaksi. f.
f. Menyimpan tabung pada suhu 37°C selama 10 menit atau pada suhuMenyimpan tabung pada suhu 37°C selama 10 menit atau pada suhu kamar selama 30 menit sampai terbentuk warna ungu sempurna. kamar selama 30 menit sampai terbentuk warna ungu sempurna. g.
g. Memasukkan larutan putih telur puyuh yang sudah didiamkan padaMemasukkan larutan putih telur puyuh yang sudah didiamkan pada kuvet.
kuvet. h.
h. Mengukur absorbansi dengan panjang 520 nm menggunakanMengukur absorbansi dengan panjang 520 nm menggunakan spektrofotometer.
spektrofotometer.
E.
E. Hasil dan Hasil dan PembahasPembahasanan
1.
1. Hasil PraktikumHasil Praktikum a.
a. Perhitungan Nilai Absorban HasilPerhitungan Nilai Absorban Hasil Nilai
Nilai absorban absorban hasil hasil dari dari setiap setiap larutan larutan dapat dapat dihitung dihitung sebagaisebagai berikut ;
berikut ;
Standar IStandar I A
Astandar Istandar I = A= A pengukuran pengukuran - A - A blanko blanko
= 0.203 = 0.203
–
–
0.125 0.125 = 0.078 = 0.078 Standar IIStandar II AAstandar Istandar I = A= A pengukuran pengukuran - A - A blanko blanko
= 0.264
= 0.264
–
–
0.125 0.125 = 0.139= 0.139
Standar IIIStandar III A
= 0.323 = 0.323
–
–
0.125 0.125 = 0.198 = 0.198 Standar IVStandar IV AAstandar Istandar I = A= A pengukuran pengukuran - A - A blanko blanko
= 0.38 = 0.38
–
–
0.125 0.125 = 0.255 = 0.255 Standar VStandar V AAstandar Istandar I = A= A pengukuran pengukuran - A - A blanko blanko
= 0.484
= 0.484
–
–
0.125 0.125 = 0.078= 0.078
Sampel Putih Telur PuyuhSampel Putih Telur Puyuh A
Astandar Istandar I = A= A pengukuran pengukuran - A - A blanko blanko
= 0.306
= 0.306
–
–
0.125 0.125 = 0.181= 0.181
b.
b. Tabel Hasil PengamatanTabel Hasil Pengamatan Hasil pengamatan
Hasil pengamatan dari pengukuran dari pengukuran absorbansi absorbansi disajikan dalam tabeldisajikan dalam tabel sebagai berikut :
sebagai berikut :
Tabel 1.b. Hasil pengukuran absorbansi dari praktikum Tabel 1.b. Hasil pengukuran absorbansi dari praktikum
No
No Larutan Larutan KonsentrasiKonsentrasi (mg/ml) (mg/ml) Absorbansi Panjang Absorbansi Panjang Gelombang Gelombang (nm) (nm) 1 1 Blanko Blanko 3 3 0,125 0,125 520520 2 2 Standar Standar I I 0.5 0.5 0.2030.203 3 3 Standar Standar II II 1 1 0.2640.264 4
4 Standar Standar III III 1.5 1.5 0.3230.323 5
5 Standar Standar IV IV 2 2 0.380.38 6
6 Standar Standar V V 3 3 0.4840.484 7
7 Sampel Sampel PutihPutih Telur Puyuh Telur Puyuh
X 0,306
Tabel 2.b. Hasil perhitungan absorbansi hasil dari larutan standar Tabel 2.b. Hasil perhitungan absorbansi hasil dari larutan standar
No
No Larutan Larutan KonsentrasiKonsentrasi (mg/ml) (mg/ml) Absorbansi Absorbansi Hasil Hasil 1 1 Standar Standar I I 0.5 0.5 0.0780.078 2 2 Standar Standar II II 1 1 0.1390.139 3
3 Standar Standar III III 1.5 1.5 0.1980.198 4
4 Standar Standar IV IV 2 2 0.2550.255 5
5 Standar Standar V V 3 3 0.3590.359
c.
c. Kurva hasil pengamatanKurva hasil pengamatan
Disajikan kurva standar nilai absorbansi dan kadar protein Disajikan kurva standar nilai absorbansi dan kadar protein berdasarkan dari data Tabel 2.b. sebagai berikut:
berdasarkan dari data Tabel 2.b. sebagai berikut:
Gambar 1. Kurva standar hubungan antara nilai absorbansi dan Gambar 1. Kurva standar hubungan antara nilai absorbansi dan
kadar protein kadar protein
d.
d. Penentuan besarnya konsentrasi sampelPenentuan besarnya konsentrasi sampel Diketahui
Diketahui : : A A blanko blanko = = 0.1250.125 A
A pengukuran pengukuran = = 0.3060.306 y
y = A= A pengukuran pengukuran- A- A blanko blanko 0.078 0.078 0.139 0.139 0.198 0.198 0.255 0.255 0.359 0.359 y = 0,112x + 0,026 y = 0,112x + 0,026 R² = 0,998 R² = 0,998 0 0 0.05 0.05 0.1 0.1 0.15 0.15 0.2 0.2 0.25 0.25 0.3 0.3 0.35 0.35 0.4 0.4 0 0 00..55 11 11..55 22 22..55 33 33..55 A A b b s s o o r r b b a a n n ( ( A A ) ) Konsentrasi (mg/ml) Konsentrasi (mg/ml)
= 0.306
= 0.306
–
–
0.125 0.125 = 0.181= 0.181 Ditanya
Ditanya : : x x (konsentrasi (konsentrasi sampel) sampel) = = ... ... ?? Penyelesaian :
Penyelesaian : Berdasarkan
Berdasarkan dari kurva dari kurva Gambar.1, didGambar.1, didapatkan persamaan garis apatkan persamaan garis luruslurus (liniear) untuk penentuan konsentrasi sampel dari protein putih telur (liniear) untuk penentuan konsentrasi sampel dari protein putih telur puyuh, yaitu : puyuh, yaitu : y y = = 0.112x 0.112x + + 0.0260.026 y = slope , x = intersept y = slope , x = intersept
kemudian disubstitusi nilai absorbansi sampel dari persamaan kemudian disubstitusi nilai absorbansi sampel dari persamaan tersebut tersebut 0.181 0.181 = = 0.112x 0.112x + + 0.0260.026 0.112x 0.112x = = 0.1810.181
–
–
0.026 0.026 0.112x 0.112x = = 0.1550.155 x x ==0.1550.155 0.112 0.112 x x = = 1.3831.383Jadi x (konsentrasi sampel) dalam 1 ml yang didapat sebesar 1.383 Jadi x (konsentrasi sampel) dalam 1 ml yang didapat sebesar 1.383 mg/ml. mg/ml. Konsentrasi dalam 100 ml = 1,383 mg/ml x 100 ml Konsentrasi dalam 100 ml = 1,383 mg/ml x 100 ml = 138,3 mg/100 ml = 138,3 mg/100 ml = 0.1383 gr/100 ml = 0.1383 gr/100 ml Konsentrasi dalam 100 g Konsentrasi dalam 100 gr r = 0.1383 = 0.1383 gr x 100 gr x 100 grgr = 13.83 dalam 100 gr /100 ml = 13.83 dalam 100 gr /100 ml Jadi konsentrasi telur puyuh dalam 100 gram sebesar 13.83 Jadi konsentrasi telur puyuh dalam 100 gram sebesar 13.83
2.
2. PembahasanPembahasan
Protein merupakan senyawa organik kompleks yang memiliki berat Protein merupakan senyawa organik kompleks yang memiliki berat molekul tinggi. Protein adalah salah satu bio-makromolekul yang molekul tinggi. Protein adalah salah satu bio-makromolekul yang penting
mengandung karbon, hidrogen, oksigen, nitrogen dan kadang kala sulfur mengandung karbon, hidrogen, oksigen, nitrogen dan kadang kala sulfur serta fosfor. Fungsi utama protein dalam tubuh adalah sebagai zat serta fosfor. Fungsi utama protein dalam tubuh adalah sebagai zat pembentuk jaringan
pembentuk jaringan baru dan baru dan mempertahankan jaringan mempertahankan jaringan yang sudah yang sudah adaada agar tidak mudah rusak. protein juga dapat digunakan sebagai bahan agar tidak mudah rusak. protein juga dapat digunakan sebagai bahan bakar
bakar apabila apabila keperluan keperluan energi energi tubuh tubuh tidak tidak dapat dapat terpenuhi terpenuhi oleholeh karbohidrat dan lemak. Protein juga berperan dalam mengatur proses karbohidrat dan lemak. Protein juga berperan dalam mengatur proses dalam tubuh. Dengan cara zat-zat pengatur proses dalam tubuh. Protein dalam tubuh. Dengan cara zat-zat pengatur proses dalam tubuh. Protein dapat mengatur kesetimbangan cairan dalam jaringan dan pembuluh dapat mengatur kesetimbangan cairan dalam jaringan dan pembuluh darah, yaitu dengan cara menimbulkan tekanan osmotik koloid. Selain darah, yaitu dengan cara menimbulkan tekanan osmotik koloid. Selain itu, sifat protein yaitu amfoter yang artinya dapat bereaksi dengan itu, sifat protein yaitu amfoter yang artinya dapat bereaksi dengan suasana asam atau basa, sehingga dapat mengatur keseimbangan asam suasana asam atau basa, sehingga dapat mengatur keseimbangan asam basa dalam tubuh.
basa dalam tubuh.
Praktikum analisis kuantitatif kadar protein telur puyuh ini Praktikum analisis kuantitatif kadar protein telur puyuh ini dilakukan denan teknik spektroskopi. Teknik spektroskopi merupakan dilakukan denan teknik spektroskopi. Teknik spektroskopi merupakan metode yang menggunakan alat spektrofotometer. Teknik ini dilakukan metode yang menggunakan alat spektrofotometer. Teknik ini dilakukan dengan menghitung kadar protein berdasarkan kemampuan protein dengan menghitung kadar protein berdasarkan kemampuan protein menyerap atau membaurkan cahaya disekitar daerah UV-Visible. menyerap atau membaurkan cahaya disekitar daerah UV-Visible. Penentuan protein berdasarkan absorbansi sinar UV termasuk teknik Penentuan protein berdasarkan absorbansi sinar UV termasuk teknik yang cepat, mudah dan tidak merusak bahan. Teknik spektroskopi yang cepat, mudah dan tidak merusak bahan. Teknik spektroskopi memiliki beberapa metode berdasarkan reagen yang digunakan, memiliki beberapa metode berdasarkan reagen yang digunakan, diantaranya adalah metode biuret, metode
diantaranya adalah metode biuret, metode Lowry Lowry, metode Brandford dan, metode Brandford dan metode pengikatan warna.
metode pengikatan warna.
Metode yang digunakan pada praktikum kali ini adalah metode Metode yang digunakan pada praktikum kali ini adalah metode Biuret dimana pengukuran absorbansi pada sampelnya menggunakan Biuret dimana pengukuran absorbansi pada sampelnya menggunakan alat spektrosfotometer yang digunakan panjang gelombangnya 520 nm. alat spektrosfotometer yang digunakan panjang gelombangnya 520 nm. Metode ini hanya dapat digunakan untuk protein terlarut. Pada Metode ini hanya dapat digunakan untuk protein terlarut. Pada penetapan kadar protein
penetapan kadar protein secara spektrofotometri secara spektrofotometri digunakan bovin serumdigunakan bovin serum albumin (BSA) serum albumin murni (kasein) sebagai pembanding albumin (BSA) serum albumin murni (kasein) sebagai pembanding karena memberikan tingkat keakuratan yang tinggi. Pengukuran kadar karena memberikan tingkat keakuratan yang tinggi. Pengukuran kadar protein
protein pada pada praktikum praktikum ini ini dilakukan dilakukan dengan dengan menggunakan menggunakan kurvakurva standar. Kurva standar dibuat dari hubungan antara konsentrasi larutan standar. Kurva standar dibuat dari hubungan antara konsentrasi larutan
dengan absorbansinya. Kurva standar dibuat dari larutan standar, dimana dengan absorbansinya. Kurva standar dibuat dari larutan standar, dimana larutan standar merupakan larutan yang sudah diketahui nilai larutan standar merupakan larutan yang sudah diketahui nilai konsentrasinya. Larutan standar ini diperlukan untuk menghitung nilai konsentrasinya. Larutan standar ini diperlukan untuk menghitung nilai konsentrasi sampel protein yang diukur menggunakan persamaan garis konsentrasi sampel protein yang diukur menggunakan persamaan garis dari larutan standar yang diperoleh. Larutan standar yang digunakan dari larutan standar yang diperoleh. Larutan standar yang digunakan adalah larutan serum albumin murni (kasein). Pengukuran nilai adalah larutan serum albumin murni (kasein). Pengukuran nilai absorbansi larutan standar dan larutan sampel menggunakan alat absorbansi larutan standar dan larutan sampel menggunakan alat spektrofotometer. Spektrofotometer merupakan alat yang digunakan spektrofotometer. Spektrofotometer merupakan alat yang digunakan untuk mengukur absorbansi dengan cara melewatkan cahaya dengan untuk mengukur absorbansi dengan cara melewatkan cahaya dengan panjang
panjang gelombang tertegelombang tertentu ntu pada pada suatu suatu obyek obyek kaca kaca yang disebut yang disebut kuvet.kuvet. Sebagian dari cahaya tersebut akan diserap dan sisanya akan dilewatkan, Sebagian dari cahaya tersebut akan diserap dan sisanya akan dilewatkan, dimana nilai absorbansi dari cahaya yang diserap sebanding dengan dimana nilai absorbansi dari cahaya yang diserap sebanding dengan konsentrasi larutan dalam kuvet.
konsentrasi larutan dalam kuvet.
Reaksi biuret merupakan reaksi warna yang umum untuk gugus Reaksi biuret merupakan reaksi warna yang umum untuk gugus peptida (-CO-NH-N)
peptida (-CO-NH-N) dan dan protein. Reaksi protein. Reaksi positif pada positif pada metode metode Biuret Biuret iniini ditandai dengan terbentuknya warna ungu karena terbentuk senyawa ditandai dengan terbentuknya warna ungu karena terbentuk senyawa kompleks antara Cu
kompleks antara Cu2+2+ dan N dari molekul peptida. Senyawa dengan dan N dari molekul peptida. Senyawa dengan dipeptida memberikan warna ungu, biru dan merah. Prinsip kerja dipeptida memberikan warna ungu, biru dan merah. Prinsip kerja penentuan
penentuan kadar kadar protein protein dengan dengan metode metode Biuret Biuret ini ini adalah adalah untukuntuk menganalisa adanya ikatan peptida dengan cara menambahkan reagen menganalisa adanya ikatan peptida dengan cara menambahkan reagen biuret
biuret ke ke dalam dalam sampel sampel yang yang kemudian kemudian diukur diukur absorbansinyaabsorbansinya menggunakan spektrofotometer.
menggunakan spektrofotometer.
Berdasarkan hasil perhitungan praktikum dengan menggunakan Berdasarkan hasil perhitungan praktikum dengan menggunakan persamaan
persamaan liniear liniear y y = = 0.112x 0.112x + + 0.026 0.026 kemudian kemudian konsentrasinyakonsentrasinya diaplikasikan ke dalam rumus dan didapatkan perhitungan konsentrasi diaplikasikan ke dalam rumus dan didapatkan perhitungan konsentrasi sampel putih telur puyuh sebesar 13.83 dalam 100 gr per 100 ml atau sampel putih telur puyuh sebesar 13.83 dalam 100 gr per 100 ml atau 0.1383 gr/100 ml. Apabila dibandingkan hasil praktikum dengan 0.1383 gr/100 ml. Apabila dibandingkan hasil praktikum dengan literatur
literatur didapatkan hasil didapatkan hasil yang yang tidak berbeda tidak berbeda jauh dari jauh dari literatur yaituliteratur yaitu sebesar 0.1323 gr/100ml. Selain itu, kurva pada hasil pengamatan sebesar 0.1323 gr/100ml. Selain itu, kurva pada hasil pengamatan menunjukkan perbandingan antara absorbansi dengan konsentrasi menunjukkan perbandingan antara absorbansi dengan konsentrasi
semakin tinggi nilai konsentrasi kaseinnya maka semakin tinggi nilai semakin tinggi nilai konsentrasi kaseinnya maka semakin tinggi nilai absorbansinya, hal itu sesuai dengan literatur yang ada. Pada praktikum absorbansinya, hal itu sesuai dengan literatur yang ada. Pada praktikum ini, adanya perbedaan nilai konsentrasi yang tidak berbeda jauh dari ini, adanya perbedaan nilai konsentrasi yang tidak berbeda jauh dari literatur merupakan kesalahan yang mungkin diakibatkan oleh literatur merupakan kesalahan yang mungkin diakibatkan oleh kelemahan dari metode Biuret yang digunakan seperti sifatnya yang kelemahan dari metode Biuret yang digunakan seperti sifatnya yang kurang sensitive dibandingkan dengan metode kuantitati lainnya (seperti kurang sensitive dibandingkan dengan metode kuantitati lainnya (seperti metode Lowry), serta NH
metode Lowry), serta NH44++ dalan konsentrasi tinggi dapat mengganggu dalan konsentrasi tinggi dapat mengganggu reaksi antar alarutan Biuret dengan sampel
reaksi antar alarutan Biuret dengan sampel
F.
F. SimpulanSimpulan
Pada percobaan tentang analisis kuantitatif kadar protein telur puyuh Pada percobaan tentang analisis kuantitatif kadar protein telur puyuh dengan metode Biuret secara spektrofotometri, terjadi pembentukan arna dengan metode Biuret secara spektrofotometri, terjadi pembentukan arna ungu dimana ini menujukkan adanya oembentukan senyawa kompleks ungu dimana ini menujukkan adanya oembentukan senyawa kompleks dengan Cu
dengan Cu2+2+. Penentuan kadar protein dengan metode Biuret ini didasarkan. Penentuan kadar protein dengan metode Biuret ini didasarkan pada pengukuran serapan cahaya oleh ikatan kompleks yang b
pada pengukuran serapan cahaya oleh ikatan kompleks yang berwarna ungu.erwarna ungu. Semakin tiggi konsentari larutan protein semakin banyak ikatan peptida Semakin tiggi konsentari larutan protein semakin banyak ikatan peptida dalam larutan maka pembentukan kompleks semakin banyak, ini dapat dalam larutan maka pembentukan kompleks semakin banyak, ini dapat dilihat dari warna ungu yang semakin pekat. Pengukuran nilai absorbansi dilihat dari warna ungu yang semakin pekat. Pengukuran nilai absorbansi larutan menggunakan spektrofotometer UV-Vis pada panjang gelombang larutan menggunakan spektrofotometer UV-Vis pada panjang gelombang 520 nm. Dan didapatkan persamaan garis liniear y = 0.112x + 0.026 520 nm. Dan didapatkan persamaan garis liniear y = 0.112x + 0.026 sehingga konsentrasi yang didapat sebesar 0.1383 gr/100ml, hasil yang sehingga konsentrasi yang didapat sebesar 0.1383 gr/100ml, hasil yang didapat pada praktikum tidak berbeda jauh dengan literatur yaitu didapat didapat pada praktikum tidak berbeda jauh dengan literatur yaitu didapat konsentrasi sebesar 0,1323 gr/100ml. Kurva pada hasil pengamatan konsentrasi sebesar 0,1323 gr/100ml. Kurva pada hasil pengamatan menunjukkan perbandingan antara absorbansi dengan konsentrasi kaseinnya menunjukkan perbandingan antara absorbansi dengan konsentrasi kaseinnya dimana didapat kurva garis lurus (linear) yang artinya semakin tinggi nilai dimana didapat kurva garis lurus (linear) yang artinya semakin tinggi nilai konsentrasi kaseinnya maka semakin tinggi nilai absorbansinya.
DAFTAR PUSTAKA DAFTAR PUSTAKA
Bakhtra, Dwi Dini Aulia dan Aisyah Mardiah. (2016). Penetapan Kadar Protein Bakhtra, Dwi Dini Aulia dan Aisyah Mardiah. (2016). Penetapan Kadar Protein dalam Telur Unggas Melalui Analisis Nitrogen Menggunakan Metode dalam Telur Unggas Melalui Analisis Nitrogen Menggunakan Metode Kjeldahl.
Kjeldahl. Farmasi Higea Farmasi Higea No.2 Vol. 8: 146). No.2 Vol. 8: 146). Clark, J. M. (1964). Experimental Biochemistr
Clark, J. M. (1964). Experimental Biochemistry. USA: W. H. Freeman Company.y. USA: W. H. Freeman Company. Daintith, John. (2004).
Daintith, John. (2004). Kamus Kimia Lengkap Kamus Kimia Lengkap. Jakarta: Erlangga.. Jakarta: Erlangga.
Hidayati Nur dan Mardiyono. (2009). Pengaruh Waktu Pengasinan Terhadap Hidayati Nur dan Mardiyono. (2009). Pengaruh Waktu Pengasinan Terhadap
Kadar Protein Putih Telur.
Kadar Protein Putih Telur. Biomedika Biomedika No.1 Vol.2 Hal 81-82. No.1 Vol.2 Hal 81-82. Maligan, Jaya Mahar. (2014).
Maligan, Jaya Mahar. (2014). Protein Analysis. Malang: Universitasi Brawijaya. Protein Analysis. Malang: Universitasi Brawijaya. Schaible. (1970). Didalam Nugroho dan Mayun.
Schaible. (1970). Didalam Nugroho dan Mayun. Beternak Beternak Burung Burung PuyuhPuyuh.. Semarang: Eka Offset.
Semarang: Eka Offset. Sudarmaji, S, dkk. (1989).
Sudarmaji, S, dkk. (1989). Analisa Analisa Bahan Bahan Makanan dan Makanan dan PertanianPertanian. Yogyakarta:. Yogyakarta: Penerbit Liberty.