Riska
Riska Ria Ria Lestari Lestari (06101410016) (06101410016) 11 LAPORAN TETAP
LAPORAN TETAP PRAKTIKUM BIOKIMIA PRAKTIKUM BIOKIMIA
I.
I. NOMOR NOMOR PERCOBAAN PERCOBAAN :: V (Lima)V (Lima) II.
II. NAMA NAMA PERCOBAAN PERCOBAAN :: PENENTUAN KADAR PROTEINPENENTUAN KADAR PROTEIN SECARA BIURET
SECARA BIURET III.
III. TUJUAN TUJUAN :: Menentukan Absorban Secara BiuretMenentukan Absorban Secara Biuret Dengan Menggunakan Spektometer Dengan Menggunakan Spektometer IV.
IV. DASAR TEORIDASAR TEORI
Teknik spektroskopi pada daerah ultra violet dan sinar tampak biasa disebut Teknik spektroskopi pada daerah ultra violet dan sinar tampak biasa disebut spektroskopi UV-Via, dari spektrum absorbsi dapat diketahui panjang gelombang spektroskopi UV-Via, dari spektrum absorbsi dapat diketahui panjang gelombang dengan absorbans maksimum dari suatu unsur atau senyawa. Konsentrsi suatu unsur dengan absorbans maksimum dari suatu unsur atau senyawa. Konsentrsi suatu unsur atau senyawa juga mudah dapat dihitung dari kurva standar yang diukur pada panjang atau senyawa juga mudah dapat dihitung dari kurva standar yang diukur pada panjang gelombang dengan absorbans maksimum.
gelombang dengan absorbans maksimum.
Spektrofotometer adalah alat pengukuran yang didasarkan pada interaksi Spektrofotometer adalah alat pengukuran yang didasarkan pada interaksi cahaya/ sinar monokromatis dengan materi, yaitu pada saat sejumlah cahaya/ sinar cahaya/ sinar monokromatis dengan materi, yaitu pada saat sejumlah cahaya/ sinar monokromatis dilewatkan pada sebuah larutan., ada seebagian sinar yang diserap, monokromatis dilewatkan pada sebuah larutan., ada seebagian sinar yang diserap, dihamburkan, dipantulkan dan sebagian lagi diteruskan. Namun karena jumlah sinar dihamburkan, dipantulkan dan sebagian lagi diteruskan. Namun karena jumlah sinar yang dihamburkan dan dipantulkan sangat kecil, maka dianggap tidak ada. Apabila yang dihamburkan dan dipantulkan sangat kecil, maka dianggap tidak ada. Apabila radiasi atau cahaya putih dilewatkan melalui larutan berwarna, maka radiasi dengan radiasi atau cahaya putih dilewatkan melalui larutan berwarna, maka radiasi dengan panjang gelombang
panjang gelombang tertentu akan tertentu akan diserap (absopsi) secara diserap (absopsi) secara selektif dan radiasi selektif dan radiasi lainnyalainnya akan diteruskan (transmisi). Absorpsi maksimum dari larutan berwarna terjadi pada akan diteruskan (transmisi). Absorpsi maksimum dari larutan berwarna terjadi pada daerah warna yang berlawanan, mislanya larutan warna merah akan menyerap rasiasi daerah warna yang berlawanan, mislanya larutan warna merah akan menyerap rasiasi maksimum pada daerah warna hijau. Dengan perkataan lain warna yang diserrap maksimum pada daerah warna hijau. Dengan perkataan lain warna yang diserrap adalah warna komplementer dari warna yang diamati.
adalah warna komplementer dari warna yang diamati.
Semua senyawa organik mampu mengabsorbsi cahaya, sebab senyawa Semua senyawa organik mampu mengabsorbsi cahaya, sebab senyawa organik mengandung elektron valensi yang dapat dieksitasi ke tingkat energi yang organik mengandung elektron valensi yang dapat dieksitasi ke tingkat energi yang lebih tinggi. Pengabsorbsian sinar ultra violet dan sinar tampak yang panjang lebih tinggi. Pengabsorbsian sinar ultra violet dan sinar tampak yang panjang gelombangnya lebih besar, terbatas pada sejumlah gugus fungsional (chromophore) gelombangnya lebih besar, terbatas pada sejumlah gugus fungsional (chromophore) yang mengandung elektron valensi dengan energi eksitasi rendah.
Riska Ria Lestari (06101410016) 2 Berdasarkan hukum Lambert-Beer, absorbansi dari suatu sampel akan sebanding dengan ketebala, konsentrasi sampel dan absorbtivitas molar. Bila ketebalan benda (b) atau konsentrasi materi (c) yang dilewati bertambah, maka cahaya akan lebih banyak diseerap. Jadi absorbansi berbansing lurus dengan ketebalan dan konsentrasi. Selain itu faktor yang berpengaruh terhadapa besar kecilnya absorbansi adalah absortivitas molar (Ɛ) dari larutan yang diukur itu sendiri. Sehingga persamaan di atas dapat dirumuskan sebagai berikut:
A = Ɛ b c
H uk um Dasar Spektr oskopi Adsorbsi
Jika suatu berkas sinar melewati suatu medium homogen, sebagian dari cahaya datang (Po) diadsorbsi sebanyak (Pa), sebagian dapat diabaikan dipantulkan (Pr), sedangkan sisanya ditransmisikan (Pt) dengan efek intensitas murni sebesar :
Po = Pa + Pt + Pr,
Dimana : Po = intensitas radiasi yang masuk, Pa = intensitas cahaya yang diadsorbsi
Pr = intensitas bagian cahaya yang dipantulkan Pt = intensitas cahaya yang ditransmisikan.
Dalam hal ini berlaku hubungan Hukum Beer-Lambert :
T = abc
Po
Pt
10b = jarak tempuh optik, c = konsentrasi log (T) = log abc
Po Pt
a = tetapan absortivitas, T = transmitansi
log abc A
Pt Po T log 1 A = adsorbansi - log (T ) i.e. A = abc
Riska Ria Lestari (06101410016) 3 1 1 T
T opasitas (tidak tembus cahaya)
A = abc
A = absorpsivitas (yakni tetap)
Hukum di atas dapat ditinjau sebagai berikut :
1. Jika suatu berkas radiasi monokromatik yang sejajar jatuh pada medium pengadsorbsi pada sudut tegak lurus setiap lapisan yang sangat kecilnya akan
menurunkan intensitas berkas.
2. Jika suatu cahaya monokromatis mengenai suatu medium yang transparan, laju pengurangan intensitas dengan ketebalan medium sebanding dengan intensitas cahaya.
3. Intensitas berkas sinar monokromatis berkurang secara eksponensial bila Konsentarsi zat pengadsorbsi bertambah.
Hal di atas, adalah persamaan yang mendasar untuk spektroskopi adsorbsi, dikenal dengan hukum Beer’s Lambert atau Hukum Beer Bougar.
Karena : A = abc, A c bila ab konstan
A b bila ac konstan
A bc bila a konstan.
Penyimpangan Dari H ukum Beer
Jika hukum Beer diikuti, maka kita akan menmperoleh garis lurus. Hal ini terjadi bila, digunakan sinar yang monokromatis. Bila menggunakan sinar yang polikromatis, maka akan menyebabkan melebarnya pita radiasi sehingga akan terjadi penyimpangan yang besar. Penyimpangan juga jelas teramati pada konsentrasi lebih besar pada kurva absorbansi terhadap konsentrasi. Kurva akan mulai melengkung pada konsentrasi yang tinggi. Bila kurva absorbsi yang diperoleh pada berbagai panjang gelombang yang digunakan bersifat datar, maka diharapkan Hukum Beer berlaku. Penyimpangan negatif dari hukum Beer menyebabkan kesalahan relatif yang
makin membesar dari konsentrasi sebenarnya.
Biuret adalah senyawa dengan dua ikatan eptida yang terbentuk pada pemanasan dua molekul urea. Ion Cu2+dari peraksi biuret dalam suasan basa akan
Riska Ria Lestari (06101410016) 4 bereaksi dengan polipeptida atau ikatan – ikatan peptida yang menyusun protein
membentuk senyawa kompleks berwarna ungu atau violet. Reaksi ini positif terhadap dua buah ikatan peptida atau lebih, tetapi negatif untuk asam amino bebas atau dipeptida. Semua asam amino, atau peptida yang mengandung asam-α amino bebas akan bereaksi dengan ninhidrin membentuk senyawa berwarna biru-ungu. Namun, prolin dan hidroksipilin menghasilkan senyawa berwarna kuning.
Protein merupakan molekul rumit dan penggolongannya kebanyakan berdasarkan pada kelarutan dalam berbagai pelarut. Akan tetapi, secara meningkat, setelah pengetahuan mengenai susunan dan struktur molekul bertambah, dipakai kriteria lain untuk penggolongan. Ini termasuk dalam sifat ultrasentrifugasi dan elektroforesis.
Protein dikelompokkan ke dalam golongan utama berikut : a. Protein sederhana
b. Protein konjugasi, dan c. Protein turunan.
Keterangan :
a. Protein Sederhana
Protein sederhana hanya menghasilkan asam amino saja jika dihidrolisis dan termasuk golongan berikut :
Albumin
Albumin larut dalam air netral yang tidak mengandung garam. Biasanya ada protein yang berbobot molekul nisbi rendah.
Contohnya, albumin telur, laktalbumin, dan albumin serum dalam protein air dadih susu, leukosin serealia, dan legumelin dalam biji polong.
Globulin
Globulin larut dalam larutan garam netral dan hampir tidak larut dalam air. Contohnya, globulin serum dan -laktoglobulin dalam susu, myosin dan aktin dalam daging, dan glisinin dalam kedelai.
Riska Ria Lestari (06101410016) 5 Glutelin
Glutelin larut dalam asam atau basa yang sangat encer dan tidak larut dalam pelarut yang netral. Protein ini terdapat dalam serealia, seperti glutenin dalam
gandum dan orizenin dalam beras. Prolamin
Prolamin larut dama alcohol 50 samapi 90 persen dan tidak larut dalam air. Protein ini mengandung sejumlah besar prolina dan asam glutamat dan terdapat dalam serealia.
Contohnya, zein dalam jagung, gliadin dalam gandum, dan hordein dalam barli.
Skleroprotein
Skleroprotein tidak larut dalam air dan pelarut netral dan tahan terhadap hidrolisis memakai enzim. Ini merupakan protein serat yang berperan pada struktur dan pengikatan. Kolagen dari jaringan otot dimasukkan dalam golongan ini, seperti gelatin, yang diperoleh dari kolagen.Contoh yang lain termasuk elastin, yaitu komponen tendon, dan keratin, komponen rambut dan kuku binatang.
Histon
Histon adalah protein yang bersifat basa, karena kandungan lisina dan arigininanya tinggi. Larut dalam air dan diendapkan oleh ammonia.
Protamin
Protamin adalah protein bersifat basa kuat, berbobot mlekul rendah (4000 sampau 8000). Protein ini kaya akan ariginina.
Riska Ria Lestari (06101410016) 6 b. Protein Konjugasi
Protein konyugasi mengandung bagian asam amino yang terikat pada bahan nonprotein seperti lipid, asam nukleat, atau karbohidrat. Beberapa protein konjugasi penting, yaitu :
Fosfoprotein
Fosfoprotein merupakan golongan yang penting yang mencakup protein makanan yang penting. Gugus fosfs\at terikat pada gugus hidroksil dari serina dan teronina. Golongan ini mencakup kasein susu dan fosfoprotein kuning telur.
Lipoprotein
Lipoprotei adalah gabungan lipid denanga protein dan mempunyai daya mengemulsi yang sangat baik. Lipoprotein terdapat dalam susu dan kuning telur.
Nukleoprotein
Nukleoprotein merupakan gabungan asal nukleat dengan protein. Senyawa ini terdapat dalam inti sel.
Glikoprotein
Glikoprotein adalah gabungan karbohidrat dengan protein. Biasanya jumlah karbohidrat kecil, tetapi beberapa glikoprotein mengandung karbohidart 8 sampai 20 persen. Satu contoh mukoprotein seperti itu ialah ovomusin putih telur.
Kromoprotein
Kromoprotein ialah yang gugus prostetiknya berwarna. Terdapat banyak senyawa jenis ini, termasuk di dalamnya hemoglobin dan myoglobin, klorofil, dan flavoprotein.
c. Protein Turunan
Protein turunan adalah senyawa yang diperoleh dengan metode kimia atau dengan metode enzimatik dan dipilah ke dalam turunan primer dan turunan sekunder, bergantung pada derajat perubahan yang terjadi. Turunan primer sedikit dimodifikasi
Riska Ria Lestari (06101410016) 7 dan tidak larut dalam air, kasein yang dikoagulasi dengan rennet (isi lambung sapi) meruapak contoh protein turunan primer.
Turunan sekunder mengalami perubahan yang lebih besar dan mencakup
protease, pepton, dan peptida. Perbedaan antara hasil urai ini terletak pada ukuran dan kelarutan. Semua larut dalam air dan dikoagulasi oleh bahang, tetapi protease dapat diendapkan dengan larutan ammonium sulfat jenuh. Peptida mengandung dua atau lebih sisa asam amino. Hasil urai ini terbentuk selama p emrosesan banyak makanan, misalnya selama pematangan keju.
V. ALAT DAN BAHAN 1. ALAT 1. Pipet tetes 2. Gelas ukur 3. Beker gelas 4. Spektometer 5. Tabung reaksi 6. Kuvet 2. BAHAN: 1. Larutan Biuret
2. Larutan standar protein 3. Aquades
3.SAMPEL
1. Larutan asam amino arginin
(1%,2%,3%,4%,5%,6%,7%,8%,9%,10%)
VI. PROSEDUR PERCOBAAN
Pipet ke dalam tabung reaksi 1 ml larutan protein yang mengandung 1 sampai 10 mg per ml. Tambahkan 4 ml reagen biuret. Kocok dan diamkan selama 30 menit pada suhu kamar. Baca serapannya pada 540 nm. Untuk blanko dipakai campuran 1 ml air dan 4ml reagen biuret yang juga diamkan selama 30 menit pada suhu kamar. Hukum Lambert – beer berlaku untuk larutan – larutan protein
antara 1 dan mg per ml.
VII. HASIL PENGAMATAN
Berikut ini merupakan hasil pengamatan pada percobaan menentukan kadar protein dengan biuret melalui spektometer :
No Larutan Konsentrasi Absorbansi
1 Blanko - 0,000 2 Arginin 1% 0,005 3 Arginin 2% 0,012 4 Arginin 3% 0,015 5 Arginin 4% 0,017 6 Arginin 5% 0,021 7 Arginin 6% 0,026 8 Arginin 7% 0,027 9 Arginin 8% 0,032 10 Arginin 9% 0,061 11 Arginin 10% 0,063 12 Sampel 1% 0,005
VIII. ANALISA DATA
Membuat Kurva Standar Konsentrasi Protein Vs Absorban Dengan : X = Konsentrasi protein (c)
Y = Absorbansi (A) No. X Y XY X2 1. 1 0,005 0,005 1 2. 2 0,012 0,024 4 3. 3 0,015 0,045 9 4. 4 0,017 0,068 16 5. 5 0,021 0,105 25 6. 6 0,026 0,156 36 0 0.01 0.02 0.03 0.04 0.05 0.06 0.07 1% 2% 3% 4% 5% 6% 7% 8% 9% 10% Series1
Kurva standar absorbansi Kurva standar absorbansi
7. 7 0,027 0,189 49 8. 8 0,032 0,256 64 9. 9 0,061 0,549 81 10. 10 0,063 0,63 100 ∑ 55 0,279 2,027 385 Slope (A) =
2 2 . . . X X n Y X XY n
=
2 55 385 10 279 , 0 55 027 , 2 10
= 0,00596 Intersept (B) =
2 2 2 . . . X X n X XY X Y
=
2 55 385 10 55 027 , 2 385 279 , 0
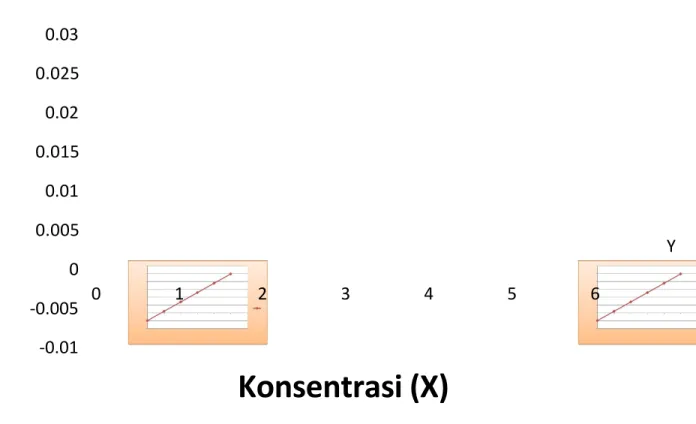
= -0,00493Persamaan Regresi Linier : Y = 0,00596X + (-0,00493) Kurva standar : Y = 0,00596X + (-0,00493)
X 0 1 2 3 4 5
Gambar 1. Grafik Kurva standar : Y = 0,00596X + (-0,00493)
Konsentrasi protein yang sebenarnya dalam Albumin :
Konsentrasi protein pada saat 1 mg/ml Y = 0,005
0,005 = 0,00596X + (-0,00493) X = 1,66 mg/ml
Konsentrasi protein pada saat 2 mg/ml Y = 0,012
0,012 = 0,00596X + (-0,00493) X = 2,84 mg/ml
Konsentrasi protein pada saat 3 mg/ml Y = 0,015
0,015 = 0,00596X + (-0,00493) X = 3,34 mg/ml
Konsentrasi protein pada saat 4 mg/ml Y = 0,017
0,017 = 0,00596X + (-0,00493) X = 3,67 mg/ml
Konsentrasi protein pada saat 5 mg/ml Y = 0,021 -0.01 -0.005 0 0.005 0.01 0.015 0.02 0.025 0.03 0 1 2 3 4 5 6
Konsentrasi (X)
Y0,021 = 0,00596X + (-0,00493) X = 4,35 mg/ml
Konsentrasi protein pada saat 6 mg/ml Y = 0,026
0,026 = 0,00596X + (-0,00493) X = 5,18 mg/ml
Konsentrasi protein pada saat 7 mg/ml Y = 0,027
0,027 = 0,00596X + (-0,00493) X = 5,35 mg/ml
Konsentrasi protein pada saat 8 mg/ml Y = 0,032
0,032 = 0,00596X + (-0,00493) X = 6,19 mg/ml
Konsentrasi protein pada saat 9 mg/ml Y = 0,061
0,061 = 0,00596X + (-0,00493) X = 11,06 mg/ml
Konsentrasi protein pada saat 10 mg/ml Y = 0,063
0,063 = 0,00596X + (-0,00493) X = 11,39 mg/ml
VIII. PEMBAHASAN
Pada percobaan kali ini, yakni percobaan mengenai penetapan kadar protein secara biuret ini bertujuan untuk mengetahui atau menetapkan kadar protein secara biuret dengan menggunakan alat spektometer yakni dengan cara
melihat kekuatan serapan atau absorban dari setiap sampel. Pada percobaan ini sampel protein yang digunakan adalah asam amino arginin, di mana aarginin bersifat basa yang dibuat dalam konsentrasi 1%,2%, sampai dengan 10%. Selain itu, dalam percobaan ini juga digunakan reagen Biuret yang dibuat dengan melarutkan tembaga (II) sulfat hidrat dan natrium kalium tartrat ke dalam air dan ditambahkan pula dengan basa kuat NaOH. Ion Cu2+ dari reagen biuret dalam suasana basa akan bereaksi dengan polipeptida atau iktan-ikatan peptida yang menyusun protein membentuk senyawa kompleks berwarna ungu.
Pada percobaan ini larutan sampel yang telah direaksikan dengan reagen biuret didiamkan selama 30 menit, dalam beberapa selang waktu maka akan
terjadi sedikit perubahan pada warna larutan yakni warna larutan sampel protein ini akan menjadi lebih pekat (ungu).
Setelah beberapa lama larutan sampel ini didiamkan, selanjutnya larutan sampel ditempatkan kedalam alat spektrofotometri ini dengan menggunakan dengan kuvet , larutan yang dimasukkan kedalam kuvet. Kuvet ini pun sangant sensitif, maka ketika memegang ataupun menaruhnya ke dalam spektroskopi harus sangat hati-hati, karena jika tersentuh dengan tangan hal inidapat mempengaruhi hasil pengukuran nilai absorbansi. Selain itu juga memrlukan Blanco. Blanko yang digunakan ialah air (aquadest) yang juga direaksikan dengan biuret terlebih dahulu, yakni digunakan sebagai pengkaliber spektroskopi.
Dari percobaan yang telah dilakukan didapatlah hasil pengamatan berupa nilai absorban yang berkisar antara 0,064 hingga 0,304 untuk kepekatan 1% hingga 10% larutan sampel protein arginin . Dari hasil data yang diperoleh setelah dilakukan analisis dengan kurva regresi ternyata didapatkan bahwa perbandingan konsentrasi secara praktik maupun teori tidak jauh berbeda.
Dalam percobaan ini juga dilakukan pengamatan terhadap sampel yang belum diketahui konsentrasinya, setelah diukur dengan spektroskopi
didapatkanlah harga absorban dari larutan ini yakni 1,107. Nilai yang kami peroleh tidak sesuai dengan teori yang seharusnya nilai yang didapatkan ini berkisar antara 0,2 hingga 0,3. Hal ini dapat disebabkan oleh beberapa hal antara lain adanya ketidaksempurnaan saat pengkaliberasian alat, dan juga karena cara ketika memegang kuvet kurang hati-hati sehingga mempengaruhi hasil yang diperoleh.
XI. Kesimpulan
1) Pada percobaan penentuan kadar protein secara biuret, terjadi pembentukan warna biru ungu, hal inin menunjukkan adanya pembentukan senyawa kompleks dengan Cu2+.
2) Penentuan kadar protein secara biuret didassarkan pada pengukuran serapan cahaya oleh ikatan kompleks yang berwarna ungu.
3) Semakin tinggi konsentrasi larutan protein maka semakin banyak ikatan peptida dalam larutan yang menyebabkan pembentukan kompleks semakin banyak, hal inin dpat dilihat dari warna ungu yang semakin pekat.
4) Addsorban suatu larutan bebrnbanding lurus dengan konsentrasinya, sehingga semakin besar konsentrasi yang digunaka, maka akan semakin besarr pula adsorban yang digunakan.
5) Ketelitian menggunakan alat dan mengkaliberasikan suatu alat akan sangat mempengaruhi hasil pengamatan yang didapatkan.
6) Larutan sampel jangan didiamkan terlalu lama karena dapat menyebabkan larutan berubah warna menjadi lebih pekat sehingga mempengaruhi hasil pengamatan.
7) Semakin tinggi konsentrasi maka nilai absorbannya semakin besar sedangkan nilai % T nya semakin kecil.
8) Adsorban suatu larutan berbanding lurus dengan konsentrasinya, sehingga semakin besar konsentrasi yang digunakan, maka semakin besar pula adsorban yang digunakan.
9) Semakin tinggi kepekatan maka akan semakin besar pula nilai absorban yang didapatkan, artinya akan semakin kecil transmitannya.
XII. DAFTAR PUSTAKA
Lehninger, Albert, 1992, Dasar-dasar Biokimia Jilid 1, Erlangga: Jakarta. Sukaryawan, Made. 2011. Petunjuk Praktikum Biokimia. Universitas
Sriwijaya:Fakultas Keguruan dan Ilmu Pendidikan.
Riska Ria Lestari (06101410016) 18 XIII. GAMBAR ALAT
1. pipet tetes 1. gelas ukur 2. beker gelas 3. spektofotometer 4. tabung reaksi 5. batang pengaduk 6. Kuvet
Riska Ria Lestari (06101410016) 19 XIV. Pertanyaan dan Jawaban
1. Buatlah standar kurva dan tetapkan kadar protein larutan protein yang diberikan?
Jawab : Kurva seperti yang terlampir
2. Berikan penjelasan tentang hukum Lambert-beer?
Jawab : Hukum lambert-beer menyatakan hubungan antara konsentrasi dengan adsorbansi yang semakin besar konsentrasi maka semakin besar pula absorbansinya.
3. Senyawa apakah yang dapat menganggu cara biuret seperti di atas?
Jawab : Senyawa yang memberikan endapan warna hitam atau merah. Jika hal tersebut terbentuk maka reagen biuret tidak terbentuk.
4. Mengapa reaksi tersebut juga disebut dengan reaksi biuret? Jawab : Karena menggunakan reagen biuret
5. Senyawa kompleks apa yang terjadi? Jawab : Senyawa kompleks bewarna ungu
6. Apakah peptida juga memberikan reaksi biuret, jika memberikan, berikan penjelasan dan bagaimana cara menentukan kadar protein yang bercampur di
dalam peptide? Jawab :
Ya, karena pada uji tersebut berfungsi untuk menunjukkan adanya ikatan peptida pada molekul protein dengan memberikan efek warna ungu. Cara
menentukannya yaitu dengan menambahkan reagen biuret pada larutan protein dengan pengukuran adsorbansi.