Laporan Praktikum Hari, Tanggal : Senin, 12 Mei 2014 Struktur Fungsi Subseluler Waktu : 08.00 — 11.00 WIB
PJP : Syaefudin, Ssi, Msi Asisten : Synta Haqqul F
Puji Rahmadani Syahrul Mustofa
PENENTUAN KADAR PROTEIN HATI TIKUS
(METODE BIURET)
Kelompok 15
Tubagus Iqbal Maulana G84120048
Ella Deffi Lestari G84120017 Muhammad Munasir G84120079
DEPARTEMEN BIOKIMIA
FAKULTAS MATEMATIA DAN ILMU PENGETAHUAN ALAM INSTITUT PERTANIAN BOGOR
PENDAHULUAN
Protein merupakan makromolekul yang penting bagi mahkluk hidup. Protein merupakan suatu polimer atau makromolekul. Satuan monomer pembentuk protein adalah asam amino. Terdapat dua puluh jenis asam amino yang merupakan penyusun protein pada mahkluk hidup (Campbell et al 2002). Banyak peran penting srotein dalam mahkluk hidup. Peranan protein dalam mahkluk hidup seperti dapat berperan sebagai biokatalisator (enzim), berperan dalam sistem pergerakan, berperan dalam sistem imun, dan sebagai penentu ekspresi gen (Yuono T 2007). selain itu protein juga merupakan komponen penyusun sel.
Analisis protein dapat dilakukan dengan dua cara, yaitu secara kualitatif dan secara kuantitatif. Analisis protein secara kualitatif terdiri atas reaksi Xantoprotein, reaksi Hopkins-Cole, reaksi Millon, reaksi Nitroprusida, dan reaksi Sakaguchi. Sedangkan analisis protein secara kuantitatif terdiri dari metode Kjeldahl, metode titrasi formol, metode Lowry, metode spektrofotometri visible (Biuret), dan metode spektrofotometri UV (Poedjiadi, 2007). Metode pengukuran kadar protein kali ini adalah metode Biuret. Metode ini berprinsip pada reaksi yang terjadi antara ion tembaga dengan ikatan peptide yang ada pada protein. Reaksi Biuret menggunakan tiga macam reagen, yaitu reagen A, B, dan C. Reagen A mengandung CuSO4 dalam akuades. CuSO4 berfungsi sebagai penyedia
ion Cu2+ untuk membentuk kompleks dengan protein. Reagen B mengandung KI
dalam akuades. KI berfungsi untuk mencegah terjadinya reduksi pada Cu2+
sehingga tidak mengendap. Reagen C mengandung Na-sitrat, Na2CO3, dan NaOH.
Na-sitrat dan Na2CO3 berfungsi sebagai buffer dan NaOH berfungsi untuk
menyediakan seasana basa (Martono et al. 2012).
Uji ini dapat mendeteksi kehadiran ikatan peptida. Uji Biuret didasarkan pada reaksi antara ion Cu2+ dan ikatan peptida dalam suasana basa. Warna
kompleks ungu menunjukkan adanya protein. Intensitas warna ynag dihasilkan merupakan ukuran jumlah ikatan peptida yang ada dalam protein. Ion Cu2+ dari
pembentukan warna ini dapat terjadi pada senyawa yang mengandung dua gugus karbonil yang berikatan dengan nitrogen atau atom karbon. Kelebihan metode pengukuran dengan menggunakan metode Biuret ialah mudah dilakukan dan menggunakan bahan yang murah. Namun, kekurangannya ialah metode ini memerlukan bahan yang cukup karena sensitivitasnya yang rendah (Pamungkas KR 2010).
Praktikum kali ini bertujuan menentukan konsentrasi atau kadar protein sel hati tikus. Kadar tersebut dilihat dari fraksi homogenat, fraksi inti, fraksi mitokondria, fraksi mikrosom, dan fraksi sitosol.
METODE PRAKTIKUM Waktu dan Tempat
Praktikum dilaksanakan pada pulkul 08.00—11.00 tanggal 12 Mei 2014 di Laboratorium Pendidikan Departemen Biokimia Fakultas Matematika dan Ilmu Pengetahuan Alam Institut Pertanian Bogor.
Alat dan Bahan
Alat-alat yang digunakan dalam percobaan ini adalah pipet Mohr, pipet tetes, tabung reaksi, vortex, dan spektrofotometer. Bahan-bahan yang digunakan pada praktikum ini antara lain larutan BSA (2 mg/mL), sampel masing-masing fraksi, akuades, SDS 5 %, dan reagen Biuret.
Prosedur Percobaan
Pembuatan Kurva Standar. menyiappkan yujuh buah tabung reaksi. Tabung reaksi 1 diisi 0,1 ml BSA(2 mg/ml) dan 1,2 ml H2O, tabung 2 diisi 0,2 ml
BSA(2mg/ml) dan 1,1 ml H2O, tabung 3 diisi 0,4 ml BSA ( 2 mg/ml) da
Pembuatan kirva standar dilakukan dengan mula-mula n 0,9 ml H2O, tabung 4
diisi 0,6 ml BSA (2 mg/ml) dan 0,7 ml H2O, tabung 5 diisi 0,8 ml (2 mg/ml) dan
0,5 ml H2O, tabung 6 diisi 1 ml BSA ( 2 mg/ml) dan 0,3 ml H2O, dan tabung 7
diisi 1,2 ml BSA ( 2 mg/ml) dan 0,1 ml H2O. Blanko dibuat dari 1,3 ml akuades.
Kemudian, setiap tabung ditambahkan 0,2 ml deoksikolat 5% dalam 0,01N KOH, 3 ml reagen biuret dan vortex lalu diinkubasi 37oC selama 15 menit. Setiap tabung
Penentuankonsentrasi protein sampel fraksi. Setiap tabung diukur absorbansinya menggunakan spektrofotometer dengan panjang gelombang 540 nm.
HASIL DAN PEMBAHASAN
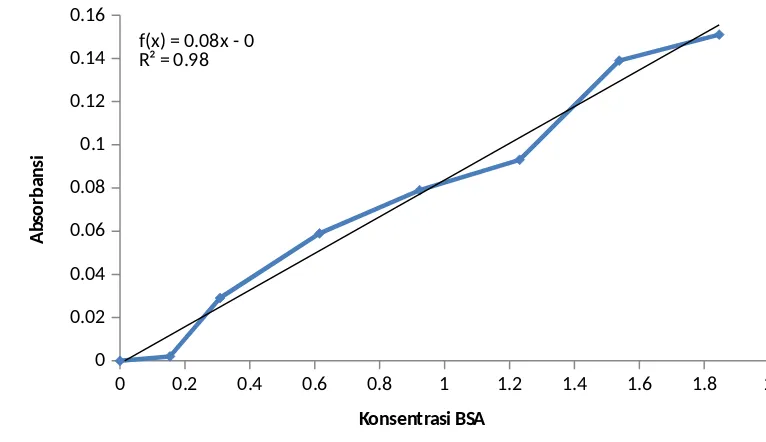
Hasil percobaan disajkan dalam bentuk tabel dan grafik. Tabel 1 dan gambar grafik menunjukkan data pembuatan kurva standar dan tabel 2 menunjukkan konsentrasi protein sel hati tikus dari berbagai fraksi.
Tabel 1 Analisis kuantitatif protein
T abung
Absorbansi terukur
Absorbansi terkoreksi
Konsentrasi BSA (mg/mL) B
lanko 0.053 0 0
1 0.055 0.002 0.154
2 0.082 0.029 0.308
3 0.112 0.059 0.615
4 0.132 0.079 0.923
5 0.146 0.093 1.231
6 0.192 0.139 1.538
7 0.204 0.151 1.846
Contoh perhitungan:
absorbansi terkoreksi tabung 2= absorbansi terukur – absorbansi blanko = 0.082 – 0.029
= 0.053 Tabung 1
[BSA]
V1 x M1 = V2 x M2
0.1 mL x 2 mg/mL = 1.3 mL x M2
0 0.2 0.4 0.6 0.8 1 1.2 1.4 1.6 1.8 2
Gambar 1 Hubungan konsentrasi BSA dengan nilai absorbansi
Tabel 2 Analisis kuantitatif protein
Fraksi ansi terukurAbsorb orbansi Abs terkoreksi
enat 0.243 1 0.18 26.000 6.333 5 Inti 0.164 2 0.10 26.000 1.880 3 Mitoko
ndria 0.136 4 0.07 26.000 3.214 2 Mikroso Sitosol 0.275 6 0.07 2.600 3.833 2
Contoh perhitungan: Homogenat
Absorbansi terkoreksi = absorbansi terukur – absorbansi blanko = 0.243 – 0.062
= 0.181 Faktor pengenceran ¿V akhir
V awal=
1.3mL 0.05mL=26 [Protein] : y = a + bx
0.181 = -0.001 + 0.084x [Protein] = 2.167 * 26
x = 2.167 [Protein] = 56.333
Pengujian kadar protein dengan menggunakan metode Biuret pada dasarnya adalah pengujuan dengan melihat reaksi yang terjadi antara ion Cu2+ dan
ikatan peptide protein dalam suasana basa. Keberadaan protein ditunjukkan dengan terbentuknya kompleks warna ungu. Kepekatan warana yang dihasikan sebanding dengan jumlah ikatan peptide yang ada dalam protein tersebut. Reaksi yang terjadi ini hanya positif untuk dua buah ikatan peptide atau lebih. Reaksi menunjukkan hasil yang negatif untuk asam amino atau ikatan peptida.
ribosom. (Campbell et al 2005). Fraksi mikrosom memiliki kandungan protein paling sedikit yang disebabkkan protein yang terlibat dalam setiap proses di fraksi tersebut lebih banyak yang telah dihasilkan dan terdapat dalam sitosol sel. Penyebablain dapat berasal dari kondisi tikus yang kekurangan antioksidan. Kadar tersebut dapat lebih tinggi lagi jika tikus diberikan perlakuan antioksidan seperti yang dilakukan Wijayanti DA et al (2003) dengan hasil kadar protein yang lebih tinggi dan terjaga pada tikus dengan perlakuan antioksidan.
SIMPULAN
Kadar protein terbanyak dalam fraksi penyusun homogenate terdapat pada fraksi inti. Kadar paling sedikit terdapat pada fraksi mikrosom. Tingginya kadar protein bergantung pada letak protein berperan.
DAFTAR PUSTAKA
Campbell NA Reece JB Mitchell G. 2005. Biologi Edisi Kelima jilid 1. Lestari R et al.Jakarta (ID): Erlangga. Terjemahan dari : Biology.
Machin A. 2012. Potensi hidrolisat tempe sebagai penyedap rasa melalui pemanfaatan ekstrak buah nanas. Biosantifika 4(2) : 70-77.
Martono Y, Hartini S, Gunawan IR. 2012. Analisis protein dan identifikasi asam amino pada tepung gaplek terfotifikasi protein tepung biji saga pohon (Adenanthera paranina LINN.). Dalam : Pemberdayaan manusia dan alam yang berkelanjutan melalui sains. Prosiding. Jakarta (ID): 109-116.
Pamungkas KR, Nafwa S. 2010. Kitosan sebagai matriks pendukung
ammobilisasi papain. Dalam : Prosiding tugas Akhir Semester Genap. Prosiding. Institut Teknologi Sepuluh Nopember.
Poedjiadi, Anna. 2007. Dasar Biokimia. Jakarta: UI Press
Wijayanti DA, Tato S, Mangkoewijojo S. 2003. Engaruh antioksidan flavonoid terhadap kadar protein mikrosomal hati tikus yang diinduksi dengan karbon tetraklorid. J. Sain. Vet. 11(2): 18-21.