APLIKASI DESAIN FAKTORIAL
SKRIPSI
Diajukan untuk Memenuhi Salah Satu Syarat Memperoleh Gelar Sarjana Farmasi (S. Farm.)
Program Studi Ilmu Farmasi
Oleh:
Felicia Satya Christania
NIM : 068114028
FAKULTAS FARMASI UNIVERSITAS SANATA DHARMA
ii
OPTIMASI FORMULA KRIM ANTI AGEING EKSTRAK ETIL ASETAT ISOFLAVON TEMPE dengan CETYL ALCOHOL dan HUMEKTAN GLISERIN :
APLIKASI DESAIN FAKTORIAL
SKRIPSI
Diajukan untuk Memenuhi Salah Satu Syarat Memperoleh Gelar Sarjana Farmasi (S. Farm.)
Program Studi Ilmu Farmasi
Oleh:
Felicia Satya Christania
NIM : 068114028
FAKULTAS FARMASI UNIVERSITAS SANATA DHARMA
v y an g un i k
Dan men y el amat kan di r i ki t a dar i si t uasi y an g t i dak men y en an gkan
-Aj ahn Br ahm-
vi PERNYATAAN KEASLIAN KARYA
Saya menyatakan dengan sesungguhnya bahwa skripsi yang saya tulis ini tidak
memuat karya atau bagian karya orang lain, kecuali yang telah disebutkan dalam
vii
Yang bertanda tangan di bawah ini, saya mahasiswa Universitas Sanata Dharma :
Nama : Felicia Satya Christania
Nomor Mahasiswa : 068114028
Demi pengembangan ilmu pengetahuan, saya memberikan kepada Perpustakaan Universitas Sanata Dharma karya ilmiah saya yang berjudul :
OPTIMASI FORMULA KRIM ANTI-AGEING EKSTRAK ETIL ASETAT ISOFLAVON TEMPE DENGAN CETYL ALCOHOL DAN HUMEKTAN GLISERIN APLIKASI : DESAIN FAKTORIAL
beserta perangkat yang diperlukan (bila ada). Dengan demikian saya memberikan kepada Perpustakaan Universitas Sanata Dharma hak untuk menyimpan, mengalihkan dalam bentuk media lain, mengelolanya dalam bentuk pangkalan data, mendistribusikan secara terbatas, dan mempublikasikannya di internet atau media lain untuk kepentingan akademis, tanpa perlu meminta izin dari saya maupun memberikan royalty kepada saya selama tetap mencantumkan nama saua sebagai penulis.
Demikian pernyataan ini yang saya buat dengan sebenarnya.
Dibuat di Yogyakarta
viii
PRAKATA
Puji syukur kepada Bapa atas berkat, rahmat, kasih dan penyertaanNya,
sehingga penulis dapat menyelesaikan skripis berjudul “Optimasi Formula Krim
Anti-Ageing Ekstrak Etil Asetat Isoflavon Tempe dengan Cetyl Alcohol dan
Humektan Gliserin : Aplikasi Desain Faktorial” sebagai salah satu syarat untuk
mencapai gelar Sarjana Farmasi (S. Farm) pada Fakultas Farmasi Universitas
Sanata Dharma Yogyakarta.
Penulis selama perkuliahan, penelitian, dan penyusunan skripsi ini telah
banyak mendapatkan bantuan dari berbagai pihak berupa bimbingan, nasihat,
pengarahan, dorongan, saran, dan kritikan. Pada kesempatan ini penulis ingin
menyampaikan penghargaan dan ucapan terima kasih kepada :
1. Rita Suhadi, M.Si., Apt selaku Dekan Fakultas Farmasi Sanat Dharma
Yogyakarta.
2. Rini Dwiastuti, M.Sc., Apt selaku dosen pembimbing atas segala kritik,
masukan, diskusi, dan keakraban yang boleh penulis rasakan bersama ibu
selama penelitian proyek payung dan penyusunan skripsi.
3. Dewi Setyaningsih, M.Sc., Apt selaku dosen penguji atas bimbingan,
saran, kritik, dan pengarahannya selama penyusunan skripsi ini.
4. Yustina Sri Hartini, M.Si., Apt selaku dosen penguji atas bimbingan,
saran, kritik, dan pengarahannya selama penyusunan skripsi ini.
5. Yohanes Dwiatmaka, M.Si., selaku kepala laboratorium atas kesediaan
ix
Mas Bimo, Mas Otok, Mas Agung, Pak Timbul, dan Pak Yuwono, atas
bantuan dan kerjasamanya selama penulis melakukan penelitian.
8. Mama, Papi, kalian orang tua terhebat untukku, terima kasih untuk cinta,
doa, kesabaran, teguran, dukungan, dan kesetiaan yang tidak pernah habis.
9. Adek Tika tercinta, yang selalu menemaniku setiap kali lembur, terima
kasih untuk teguran yang penuh kasih sayang, cinta, doa, perhatian, dan
dukungan.
10.Galih dan Jelly, sebagai bagian dari kebersamaan dengan adek tercinta,
terimakasih untuk dukungan yang selalu diberikan.
11.Sahabatku yang selalu membuatku percaya diri dan termotivasi, Yashinta
Widyaningtyas, dan sahabatku yang selalu memberi ketenangan dan
keheningan, Lulu Lunggati B.M. Terima kasih untuk perjuangan,
keceriaan dan kebodohan kita, aku bersyukur memiliki kalian.
12.Malaikat kecilku Luther-Helen, Chiroo-Bolivia, Adek, untuk cinta dan
kesetiaan yang boleh bunda dan tante rasakan.
13.Mama Wiwik yang selalu mengiringku dengan doa dan kasih sayang.
14.Om Ubay yang sangat setia memberikan saran, kritik, nilai, dukungan, dan
kesabaran untuk menemani kami ngelab selama penyusunan skripsi ini.
15.Dotie, Fani, Vica, Mary, Lil, Dissa, Adit, Reno, Boim, Robi, Pungky,
x
16.Dani, Rico, Intan, Iren, Rani, Cica, Wiwit,Grace, Zi, Cik Vita, Ardani, Lia,
Yosephine, Joice, Melia teman-teman seperjuangan dalam penelitian,
terima kasih untuk kebersamaan, sharing, dan diskusi selama ini.
17.Bos Fian, Ko David, terimakasih untuk dukungan dan masukan selama
penyusunan skripsi ini.
18.Sahabatku, Riyo, Mary, Tusi, Krisna, Erlina terimakasih untuk dukungan
yang selalu ada.
19.Teman-teman FST 2006 serta semua pihak yang telah memberi bantuan,
dukungan, doa, dan keceriaan yang tidak dapat disebutkan satu per satu.
Akhir kata, penulis menyadari bahwa penyusunan skripsi ini masih
banyak kekurangannya mengingat keterbatasan kemampuan dan pengalaman yang
dimiliki. Oleh sebab itu kritik dan saran yang membangun sangat diperlukan oleh
penulis demi kesempurnaan skripsi ini. Semoga skripsi ini dapat bermanfaat bagi
perkembangan ilmu pengetahuan.
xi
merupakan salah satu bahan makanan khas Indonesia yang mudah ditemui dan mengandung isoflavon yang mempunyai daya antioksidan lebih besar daripada kedelai, dengan demikian penelitian ini juga dapat menaikkan nilai guna tempe.
Penelitian ini menggunakan rancangan eksperimental murni. Optimasi formula yang dilakukan dengan menggunakan metode desain faktorial dan teknik analisis statistik Yate’s treatment dengan taraf kepercayaan 95%. Optimasi dilakukan pada komposisi cetyl alcohol dan humektan gliserin dengan parameter sifat fisik krim yang diuji meliputi : viskositas, daya sebar, serta stabilitas krim meliputi pergeseran viskositas setelah penyimpanan selama 30 hari. Selain itu juga dilakukan uji daya antioksidan dengan metode DPPH pada ekstrak etil asetat isoflavon tempe.
Dari penelitian ini diperoleh bahwa cetyl alcohol merupakan faktor yang berpengaruh dominan dan signifikan dalam menentukan sifat fisik viskositas krim, sedangkan gliserin dan interaksi cetyl alcohol-gliserin bukan merupakan faktor yang berpengaruh dominan dalam menentukan sifat fisik dan stabilitas krim.
xii
ABSTRAC
The aim of study of this researh is to optimization anti-ageing cream of etil asetat extract isoflavon tempe with cetyl alcohol and gliserin as humectant of cream. Tempe is one of the favourite food from Indonesia that have a big potetial antioxidant activity.
This research is use pure experimental device and formula optimation that was done by using factorial design method and statistical analysis of Yate’s Treatment. The optimization condusted at cetyl alcohol and humectant gliserin, with the physical properties of cream that was tested through spreadibility, viscosity, and stability of cream by using alteration of viscosity.
The result of this research was indicated that cetyl alcohol was the dominant factor in determining the viscosity. Gliserin and Interaction is not determining physical and stability properties.
xiii
HALAMAN JUDUL ...ii
HALAMAN PERSETUJUAN PEMBIMBING ...iii
HALAMAN PENGESAHAN ...iv
HALAMAN PERSEMBAHAN ...v
PERNYATAAN KEASLIAN KARYA ...vi
HALAMAN PERNYATAAN PERSETUJUAN PUBLIKASI...vii
PRAKATA ...viii
INTISARI ...xi
ABSTRAK. ... xii
DAFTAR ISI ...xiii
DAFTAR TABEL ...xvii
DAFTAR GAMBAR ...xviii
DAFTAR LAMPIRAN ...xix
BAB I PENDAHULUAN A. Latar Belakang ...1
1. Permasalahan ...3
2. Keaslian Penelitian ...3
3. Manfaat Penelitian ...3
B. Tujuan Penelitian ...4
xiv
2. Tujuan Khusus ...4
BAB II PENELAAHAN PUSTAKA A. Isoflavon dan Tempe ...5
B. Skin Ageing...5
C. Uji DPPH ...7
D. Krim ...8
E. Cetyl Alcohol ...9
F. Gliserin ...10
G. Desain Faktorial ...12
H. Landasan Teori ...13
I. Hipotesis ...15
BAB III METODE PENELITIAN A. Jenis dan Rancangan Penelitian ...16
B. Variabel dan Definisi Operasional ...16
1. Variabel bebas ...16
2. Varabel Tergantung ...16
3. Variabel Pengacau Terkendali ...16
4. Varabel Pengacau tak Terkendali ...16
C. Bahan Penelitian ...18
D. Alat Penelitian ...18
E. Tata Cara Penelitian ...19
1. Pengumpulan, Pengolahan, Isolasi Isoflavon Tempe ...19
xv
F. Analisis Hasil ...24
BAB IV HASIL dan PEMBAHASAN A. Isolasi dan Identifikasi Ekstrak Etil Asetat Isoflavon Tempe ...25
1. Isolasi Ekstrak Etil Asetat Isoflavon Tempe ...25
2. Identifikasi Ekstrak Etil Asetat Isoflavon Tempe ...29
B. Uji Antioksidan Isoflavon Tempe ...30
C. Pembuatan Krim ...32
D. Sifat dan Stabilitas Krim ...34
1. Pengujian Tipe Krim ...34
2. Karakteristik Ukuran Droplet ...35
3. Uji Sifat Fisik dan Stabilitas Krim ...38
a. Daya Sebar ...38
b. Viskositas ...41
c. Pergeseran viskositas ...43
E. Optimasi Formula ...46
a. Daya Sebar ...46
b. Viskositas ...47
c. Pergeseran Viskositas ...47
xvi BAB V KESIMPULAN dan SARAN
A. Kesimpulan ...50
B. Saran ...51
DAFTAR PUSTAKA ...52
Lampiran ...54
xvii
Tabel II. Komponen Isoflavon Glukosida ...6
Tabel III. Rancangan Percobaan Desain Faktorial ...12
Tabel IV. Rancangan Formula Desain Faktorial ...21
Tabel V. Perhitungan Rf Uji KLT Ekstrak Etil Asetat Isoflavon Tempe ...30
Tabel VI. Hasil Perhitungan % Scavenging Ekstrak Etil Asetat Isoflavon Tempe ...32
Tabel VII. Hasil Perhitungan Statistik Distribusi Ukuran Droplet ...36
Tabel VIII. Efek Faktor terhadap Respon Daya Sebar ...39
Tabel IX. Hasil Perhitungan Yate’s Treatment untuk Respon Daya Sebar ...39
Tabel X. Efek Faktor terhadap Respon Viskositas ...41
Tabel XI. Hasil Perhitungan Yate’s Treatment untuk Respon Viskositas ...41
Tabel XII. Efek Faktor terhadap Respon Pergeseran Viskositas ...43
xviii
DAFTAR GAMBAR
Gambar 1. Struktur Kimia Isoflavon Aglikon ...6
Gambar 2. Struktur Kimia Isoflavon Glukosida ...6
Gambar 3. Struktur Kimia Cetyl Alcohol...10
Gambar 4. Struktur kimia Gliserin ...10
Gambar 5. Skema Singkat Alur Penelitian ...18
Gambar 6. Skema Mekanisme isoflavon sebagai Anti-ageing ...29
Gambar 7. Hasil uji KLT ...30
Gambar 8. Skema Tahapan Reaksi Isoflavon sebagai Antioksidan ...31
Gambar 9. Hasil Pengujian Mikroskopik Tipe Krim...34
Gambar 10. Karakteristik Ukuran Droplet ...35
Gambar 11. Kurva Nilai Tengah Diameter Droplet vs % Frekuensi ...37
Gambar 12. Grafik Pengaruh Faktor terhadap Respon Daya Sebar ...40
Gambar 13. Grafik Pengaruh Faktor terhadap Respon Viskositas ...42
Gambar 14. Grafik Pengaruh Faktor terhadap Respon Pergeseran Viskositas ...45
Gambar 15. Grafik Contour Plot Daya Sebar Krim ...46
Gambar 16. Grafik Contour Plot Viskositas Krim ...47
Gambar 17. Grafik Contour Plot Pergeseran Viskositas ...48
xix
Lampiran 2. Perhitungan Uji Antioksidan Metode DPPH...55
Lampiran 3. Data Penimbangan, Notasi, dan Formula Desain Faktorial ...62
Lampiran 4. Data Sifat Fisik dan Stabilitas Krim ...63
Lampiran 5. Perhitungan Efek Sifat Fisik dan Stabilitas Krim ...70
Lampiran 6. Persamaan Desain Faktorial ...76
Lampiran 7. Yates’s Treatment...84
1
BAB I PENGANTAR
A. Latar Belakang
Tempe adalah salah satu bahan makanan asli Indonesia yang sangat
digemari karena harganya murah, mudah ditemui, dan rasanya enak. Di dalam
tempe ditemukan suatu zat antioksidan dalam bentuk isoflavon yaitu daidzein,
glistein, dan genistein seperti pada kedelai, selain itu ditemukan pula antioksidan
faktor II (6,7,4, trihidroksiflavon) yang merupakan agen antioksidan yang hanya
terdapat di dalam tempe sebagai hasil dari fermentasi kedelai (Anonim, 2008).
Faktor II mempunyai aktivitas antioksidan yang secara in-vitro lebih tinggi
dibandingkan dengan isoflavon dalam kedelai (Ariani, 2003).
Isoflavon mempunyai efek terhadap radiasi UV yaitu meningkatkan sistem
imun sama besar dengan energi UV yang menyebabkan kerusakan kulit, dikenal
dengan istilah photoageing (Zulli, F., Schmid, D., Muggli, R., Hanay, C., 2002).
Isoflavon dapat diaplikasikan dalam kosmetik dengan berbagai bentuk sediaan
misalnya gel, lotion, dan krim yang dapat diformulasikan secara mudah dalam
fase air (Schmid, 2004). Konsentrasi isoflavon yang biasa digunakan dalam
kosmetik adalah 1-500 mg/kg atau 20-100 mg/kg (Zulli et.al, 2002).
Dalam penelitian ini isoflavon diformulasikan dalam bentuk sediaan
krim. Hal ini terkait dengan kelebihan dari sediaan krim dibandingkan dengan
memberi rasa melembabkan di kulit, mudah dibersihkan dan dapat atau tidak
dapat dicuci dengan air (Mitsui, 1993).
Suatu sediaan, untuk dapat diterima oleh masyarakat harus memenuhi
parameter sifat fisik dan stabilitas. Sifat fisik dan stabilitas suatu sediaan krim
dapat ditentukan oleh basis dan humektan. Cetyl alcohol sebagai basis yang juga
bersifat sebagai thickening agent sehingga mampu menjaga stabilitas,
memperbaiki tekstur, dan meningkatkan konsistensi (Bennet, 1970). Sedangkan
humektan merupakan suatu bahan higroskopis yang ditambahkan bertujuan untuk
mempertahankan kelembapan sediaan sehingga dapat mempermudah aplikasi
krim dengan memberikan daya sebarnya yang cukup serta dapat mempertahan
konsistensi. Oleh karena cetyl alcohol dan gliserin memiliki sifat yang saling
berlawanan yaitu dapat meningkatkan viskositas dan meningkatkan daya sebar,
maka dalam penelitian ini dilakukan optimasi formula cetyl alcohol sebagai basis
dan gliserin sebagai humektan.
Optimasi formula dilakukan menggunakan aplikasi desain faktorial.
Metode ini mempunyai kelebihan yaitu selain dapat mengetahui efek dari tiap
bahan yang digunakan terhadap sifat-difat fisik sediaan juga dapat digunakan
untuk mengetahui efek yang tmbul dati interaksi bahan-bahan yang digunakan.
Dalam penelitian ini dilakukan pula uji aktivitas antioksidan isoflavon
secara in-vitro dengan metode DPPH (2,2-difenil-1-1pikrilhidrazil) yang
3
1. Permasalahan
a. Apakah ekstrak etil asetat isoflavon tempe mempunyai aktivitas
antioksidan melalui uji penangkapan radikal hidroksil dengan metode
DPPH yang dinyatakan dengan % scavenging ?
b. Efek mana yang lebih dominan dalam mempengaruhi sifat fisik dan
stabilitas krim di antara efek cetyl alcohol, efek gliserin, dan efek
interaksi ?
c. Apakah diperoleh area komposisi optimum dari campuran cetyl
alcohol-gliserin yang memenuhi parameter sifat fisika dan stabilitas krim ?
2. Keaslian Penelitian
Sejauh penelusuran pustaka yang dilakukan penulis, penelitian tentang
formulasi sediaan krim anti ageing isoflavon tempe dengan basis tidak larut
air cetyl alcohol dan basis larut air gliserin belum pernah dilakukan.
3. Manfaat Penelitian
a. Manfaat Teoritis. Menambah pengetahuan mengenai bentuk sediaan anti
ageing isoflavon dari tempe dan cara mengisolasi isoflavon dari tempe.
b. Manfaat Metodologi. Menambah informasi ilmu pengetahuan kefarmasian
mengenai upaya pengembangan dan aplikasi metode desain faktorial
dalam menemukan area komposisi optimum krim anti ageing isoflavon
dari tempe dengan komposisi cetyl alcohol dan gliserin.
c. Manfaat Praktis. Adanya sediaan krim anti ageing isoflavon dari tempe ini
masyarakat dapat menggunakan senyawa yang berasal dari bahan yang
B. Tujuan Penelitian a. Tujuan Umum
Membuat formula krim yang memiliki daya anti ageing dengan bahan
aktif isoflavon dari tempe.
b. Tujuan Khusus
1. Mengetahui apakah fraksi etil asetat isoflavon dari tempe mempunyai
aktivitas antioksidan melalui uji penangkapan radikal hidroksil dengan
metode DPPH yang dinyatakan dengan % scavenging.
2. Mengetahui efek mana yang lebih dominan dalam mempengaruhi sifat
fisik dan stabilitas krim di antara efek cetyl alcohol, efek gliserin, dan efek
interaksi.
3. Mengetahui area komposisi optimum dari campuran cetyl alcohol–gliserin
5
BAB II
PENELAAHAN PUSTAKA
A. Isoflavon dan Tempe
Tempe hasil fermentasi ditemukan adanya isoflavon genistein, daidzein,
dan faktor-II. Genistein dan Daidzein telah ada pada kedelai rendam sebagai
bahan baku tempe, tetapi faktor-II hanya dijumpai pada tempe. Faktor-II dapat
terbentuk karena selama proses perendaman fermentasi kedelai β-glukosidase
akan aktif dan mengubah glisitin, genistin, dan daidzin yang telah ada pada
kedelai menjadi daidzein, genistein, dan glisitein. Selanjutnya selama proses
fermentasi kedelai rendam terjadi biokonversi lebih lanjut daidzein dan glisiteni
menjadi faktor-II. Faktor-II mempunyai daya antioksidan yang secara in-vitro
jauh lebih tinggi bila dibandingkan antioksidan lain (Ariani, 2003).
Isoflavon terdiri atas komponen polar (terikat gula/glikon) dan komponen
nonpolar (tidak terikat gula/aglikon) (Tensiska, Marsetio, Yudiastuti, S.O.N.,
2007). Isoflavon glikosida tidak aktif secara biologi. Isoflavon aktif untuk
perawatan kulit harus dalam bentuk aglycone yang ini mempunyai sedikit
kelarutan dalam air dan minyak (Schmid, 2004). Isoflavon diaplikasikan dalam
kosmetik, harus diaktifkan terlebih dahulu misalnya dalam bentuk aglikon, sebab
di dalam kulit tidak terdapat enzim hidrolisis. Dalam bentuk glikosida maka
isoflavon tidak akan terpenetrasi sampai lapisan kulit yang lebih dalam, misalnya
senyawa yang dapat lewat adalah aglikon yang dapat larut air (Zulli et.al, 2002).
Struktur isoflavon adalah sbb:
Gambar 1. Struktur Kimia Isoflavon Aglikon
Tabel I. Komponen Isoflavon Aglikon
R1 R2 Komponen
H H Daidzein
OH H Genistein
H OCH3 Glisitein
H OH Faktor-II
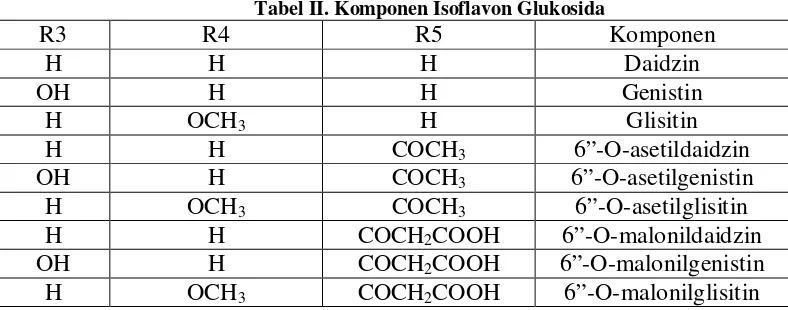
Gambar 2. Struktur Kimia Isoflavon Glukosida
Tabel II. Komponen Isoflavon Glukosida
R3 R4 R5 Komponen
H H H Daidzin
OH H H Genistin
H OCH3 H Glisitin
H H COCH3 6”-O-asetildaidzin
OH H COCH3 6”-O-asetilgenistin
H OCH3 COCH3 6”-O-asetilglisitin
H H COCH2COOH 6”-O-malonildaidzin
OH H COCH2COOH 6”-O-malonilgenistin
7
B. Kromatografi Lapis Tipis
Kromatografi lapis tipis (KLT) adalah metode kromatografi cair yang
paling sederhana dan mempunyai beberapa kelebihan. Kelebihan KLT adalah
sample yang digunakan sedikit, diperoleh pemisahan senyawa yang amat berbeda,
waktu yang dibutuhkan singkat, serta jumlah pelarut yang digunakan sangat
sedikit. KLT dapat digunakan untuk dua tujuan. Pertama, untuk hasil kuantitatif,
kualitatif, dan preparative. Kedua, digunakan untuk mengetahui sistem pelarut dan
sistem penyangga yang akan dipakai dalam kromatografi kolom atau kromatografi
cair kinerja tinggi (KCKT) (Gritter, R., Bobbit, J.M., Schwarting, A., 1991).
Kromatografi lapis tipis adalah metode pemisahan fisikokimia. Lapisan
yang memisahkan, yang terdiri atas fase diam, ditempatkan pada penyangga yang
berupa plat gelas, logam, atau lapisan yang cocok. Campuran yang akan
dipisahkan berupa larutan, ditotolkan pada fase diam. Setelah plat atau lapisan
ditaruh di dalam bejana terttup rapat yang berisi larutan pengembang yang cocok
(fase gerak), pemisahan terjadi selama perambatan kapiler (pengembangan).
Selanjutnya senyawa yang tidak berwarna harus dideteksi (Stahl, 1985).
Seyawa yang dihasilkan pada lempeng fase diam terkadang masih sulit
untuk dideteksi. Hal ini dapat diatasi dengan menambahkan pereaksi yang mampu
memperjelas bercak, sehingga mempermudah dalam melakukan deteksi.
Senyawa-senyawa yang sering digunakan untuk pereaksi pendeteksi KLT antara
lain ammonia, ALCL3, FeCL3, sitroborat, dan lain-lain (Mabry, T.J., Markham,
Deteksi paling sederhana adalah jika senyawa menunjukkan penyerapan
di daerah UV gelombang pendek (radiasi utama kira-kira 254 nm) atau jika
senyawa ini dapat dieksitasi ke fluoresensi radiasi UV gelombang pendek dan
atau gelombang panjang (365 nm). Jika dengan kedua cara ini senyawa tidak
dapat dideteksi maka harus dicoba dengan reaksi kimia. Pertama tanpa pemanasan
lalu bila perlu degan pemanasan. Jarak pengembangan pada senyawa pada
kromatogram biasanya dinyatakan dengan angka Rf atau hRf (Stahl, 1985).
tFaseGerak JarakRamba
tolan kDariPento PusatBerca
Jaraktitik Rf
C. Skin Ageing
Skin ageing adalah suatu proses yang dipengaruhi oleh waktu yang dapat
dipercepat oleh faktor eksternal misalnya radiasi UV. Mekanisme ini berlangsung
di dermis dan mengurangi kemampuan untuk pembentukan lapisan baru serta
mempercepat degradasi lapisan. Manifestasi dari fenomena skin ageing bisa
bermacam-macam, misalnya keriput, kulit kendor karena berkurangnya
kemampuan elastisitas dan kekencangan (Zulli et.al, 2002).
Skin ageing dapat disebabkan oleh berbagai macam faktor internal
maupun eksternal, salah satu faktor eksternal tersebut adalah paparan sinar
matahari yang sering disebut photoageing. Mekanisme penuaan yang dipicu oleh
faktor eksternal paparan sinar matahari adalah adanya penurunan jumlah ceramide
akibat reaksi dengan Reactive Oxygen Species (ROS) yang dapat dihambat dengan
adanya antioksidan sebagai salah satu mekanisme anti ageing. Sebab radikal
9
Anion superoksida yang mengurangi oksigen menginisiasi reaksi ageing, sebab
anion superoksida mempunyai peran penting dalam pembentukan ROS misalnya
hidrogen peroksida, radikal hidroksil, dan oksigen singlet yang dapat memicu
kerusakan akibat reaksi oksidatif pada lemak, protein, dan DNA (Lee, J., Renita,
M., Fioritto, R.J., 2004).
Isoflavon dapat mempunyai mekanisme anti-ageing sebagai antioksidan
maupun fitoestrogen :
a. Mekanisme sebagai fitoestrogen
Isoflavon sebagai fitoestrogen dapat mempunyai mekanisme sebagai
anti-ageing karena struktur isoflavon aglikon yang berbentuk
heterosiklik fenol. Struktur tersebut mempunyai bentuk yang sangat
mirip dengan estrogen steroid, sehingga reseptor estrogen akan
dengan mudah menangkap isoflavon dan akan menstimulasi kolagen
di dalam kulit (Schmid, 2004). Mekanisme fitoestrogen ini, biasa
diberikan dengan sistem penghantaran oral.
b. Mekanisme sebagai antioksidan
Paparan sinar UV dapat mengandung ROS (Reactive Oxygen
Species) yang dapat mengaktivasi transkripsi dari MMPs. Enzim
tersebut merupakan salah satu enzim proteolitik yang akan
mendegradasi kolagen, elastin, dan protein-protein lain yang
berfungsi untuk menjaga elastisitas kulit. Isoflavon yang mempunyai
fungsi sebagai antioksidan dapat menangkap ROS sehingga akan
kulit tetap terjaga dan photoaging dapat dihambat (Chiang et.al,
2004), seperti ditunjukkan dalam gambar 6. Isoflavon dapat berfungsi
sebagai antioksidan karena adanya gugus fenol yang mempunyai
atom hidrogen sehingga dapat menangkap elektron bebas dari ROS
menjadi elektron berpasangan yang lebih stabil. Selanjutnya,
isoflavon akan teroksidasi oleh radikal bebas sehingga protein-protein
penyusun elastisitas kulit seperti kolagen dan elastin tidak akan
terdegradasi. Oleh karena itu, kandungan faktor II yang hanya ada di
dalam isoflavon tempe merupakan antioksidan yang lebih baik
dibandingkan isoflavon dalam kedelai biasa yang hanya mengandung
genistein dan daizein. Hal ini disebabkan karena pada senyawa faktor
II sebagai hasil fermentasi kedelai mempunyai gugus fenol yang lebih
banyak.
Sinar UV ↓ ROS
↓
Adanya atom hidrogen isoflavon sebagai agen antioksidan yang mengikat elektron dari ROS
↓
Tidak terjadi aktivasi MMPs ↓
Tidak terjadi degradasi kolagen, elastin, dll ↓
Tidak terjadi reaksi photoaging
11
D. Uji DPPH (2,2-difenil-1-pikrilhidrazil)
Uji DPPH merupakan salah satu metode yang dapat digunakan untuk
mengukur daya antioksidan suatu sampel. DPPH berfungsi sebagai senyawa
radikal bebas stabil yang ditetapkan secara spektrofotometri melalui persen
peredaman absorbansi. Peredaman warna ungu merah pada panjang gelombang
517 nm dikaitkan dengan kemampuan minyak atsiri atau ekstrak sebagai
antiradikal bebas (Purwata, I.M.O.A., Rita, W.S., Yoga, R., 2009).
Besarnya aktivitas antioksidan ditandai dengan nilai IC50, yaitu
konsentrasi larutan sampel yang dibutuhkan untuk menghambat 50% radikal
bebas DPPH (Andayani, R., Yovita, L., Maimunah, 2008). Aktivitas antioksidan
kuat jika IC50 lebih kecil dari 200 µg/ml. Kapasitas antiradikal bebas metode
DPPH diukur dari peredaman warna ungu merah dari DPPH pada panjang
gelombang 517 nm ± 20 nm (Purwata dkk, 2009). Perhitungan aktivitas
penangkapan radikal DPPH (% scavenging) dihitung dengan rumus :
% 100 ) (
x blanko
Absorbansi
sampel Absorbansi
blanko
Absorbansi
(Sunarni, T., Pramono, S., Asmah, R., 2007).
Adanya aktivitas antioksidan dari sampel akan menyebabkan perubahan
warna pada larutan DPPH dalam metanol yang semula violet pekat jadi kuning
pucat. Sampel dinyatakan aktif sebagai antiradikal bebas jika % peredaman (%
E. Krim
Krim adalah bentuk sediaan setengah padat mengandung satu atau lebih
bahan obat terlarut atau terdispersi dalam bahan dasar yang sesuai. Emulsi minyak
dalam air atau dispersi mikrokristal asam-asam lemak atau alkohol berantai
panjang dalam air, yang dapat dicuci dengan air dan lebih ditujukan untuk
penggunaan kosmetika (Anonim, 1995). Sebuah vanishing cream merupakan
emulsi dari asam stearat, disebut vanishing cream karena tidak tampak mengkilap
(vanish) ketika digunakan. Fase eksternalnya adalah air. Dengan penambahan
gliserin (10%) sebagai bahan pembuat lunak dinilai krim akan berkilau mutiara
sediaan ini menjadi lebih cemerlang (Voigt, 1994). Emulsifying agent adalah
sabun atau campuran sabun dari sodium, potassium, dan ammonia biasanya dalam
bentuk emulsi minyak dalam air (Young, 1972).
Krim merupakan suatu sistem emulsi yang stabilitasnya ditentukan oleh
elastisitas emulgator dari lapisan tipis batas antar muka. Menurut aturan Bancroft,
fase dimana emulgator terlarut atau terakumulasi di dalamnya adalah bahan
pendispersi, contoh sabun yang dapat larut dalam air merupakan emulgator m/a.
Suatu sistem emulsi akan menunjukkan stabilitas dan tingkat dispersitas yang
optimal, jika lapisan tipis menyaluti batas antar permukaan secara total. Banyak
emulgator memberikan lapisan tipis yang sangat stabil dan dapat menyalut
droplet. Jika ada droplet bersentuhan, maka lapisan tipis semacam itu akan
memberi perlindungan untuk menghindari penggabungan (Voigt, 2004).
Salah satu emulgator m/a yang dapat digunakan pada sediaan obat yang
13
stabil adalah sabun amin. Sabun amin salah satu contohnya adalah
Trietanolaminstearat yang terbentuk dari hasil reaksi penyabunan antara asam
stearat dan TEA. Pada susunan rantai sabun trietanolaminstearat, hidrokarbon
yang simetris mewakili bagian tidak polar dari molekul. Sebaliknya karboksil
hidrofil menunjukkan tidak adanya keseimbangan muatan, oleh karena itu gugus
bersifat polar. Kesatuan molekul ini gugus polar dan tidak polar menyatu sehingga
membuatnya sebagai senyawa amfifil (Voigt, 2004). Struktur sabun trietanolamin
adalah sbb :
[OH-CH2-CH2-N(HCH2CH2OH)-CH2-CH2-OH]C17H35-COO
-F. Cetyl Alcohol
Cetyl alcohol mengandung tidak kurang dari 90% C16H34O, selebihnya
terdiri dari alkohol yang sejenis. Pemeriannya berupa serpihan putih licin, granul
atau kubus, berwarna putih, bau khas lemah, rasa lemah. Kelarutannya tidak larut
dalam air, larut dalam etanol dan dalam eter, kelarutan bertambah dengan naiknya
suhu (Anonim, 1995). Struktur cetyl alcohol adalah sbb:
Gambar 4. Struktur Kimia Cetyl Alcohol
Cetyl alcohol mampu menjaga stabilitas, memperbaiki tekstur dan
meningkatkan konsistensi serta dapat bersifat sebagai emollient, emulsifying
agent, dan mampu menyerap air. Di dalam emulsi minyak dalam air, cetyl alcohol
dalam air. Kombinasi dengan emulsifier ini akan menghasilkan suatu sistem yang
tertutup, barier monomolecular pada antar muka minyak-air yang membentuk
barier mekanik sehingga dapat mencegah terjadinya droplet yang coalesence
(Rowe, R., Sheskey, P.J., Quinn, M.E., 2009).
G. Gliserin
Gliserin dapat diperoleh dari minyak dan lemak yang diproduksi dalam
pembuatan sabun dan asam lemak. Gliserin merupakan cairan jernih seperti sirup,
tidak berwarna, rasa manis, hanya boleh berbau khas lemah (tajam atau tidak
enak), higroskopik, dan netral terhadap lakmus. Gliserin dapat bercampur dengan
air dan dengan etanol, tidak larut dalam kloroform, dalam minyak lemak, dalam
eter, dan dalam minyak menguap (Anonim, 1995). Struktur gliserin adalah sbb:
Gambar 5. Struktur Kimia Gliserin
Pada pemakaian topikal, seringkali gliserin digunakan untuk humectant
dan emollient, sehingga dapat digunakan untuk mempertahankan kelembapan
kulit dan meningkatkan daya sebar. Gliserin digunakan sebagai solvent atau
cosolvent di dalam krim dan emulsi. Gliserin biasa ditambahkan di dalam fase air
15
H. Metode Desain Faktorial
Metode desain faktorial dapat digunakan untuk mendesain suatu
percobaan untuk mengetahui faktor yang dominan berpengaruh secara signifikan
terhadap suatu respon dan memungkinkan kita mengetahui interaksi di antara
faktor-faktor tersebut (Voigt, 1994). Keuntungan dari metode desain faktorial ini
adalah memiliki efisiensi yang maksimum dalam mengetahui efek yang dominan
dalam menentukan respon, selain itu bahwa metode ini dapat digunakan untuk
mengidentifikasi efek masing-masing faktor maupun efek interaksi antar faktor
(Muth, 1999).
Metode desain faktorial merupakan aplikasi persamaan regresi yaitu
teknik untuk memberikan model hubungan antara variabel respon dengan satu
atau lebih variabel bebas. Model yang diperoleh dari analisis tersebut berupa
persamaan matematika. Desain faktorial dua level berarti ada dua faktor (misal A
dan B) yang masing-masing faktor diuji pada dua level yang berbeda, yaitu level
rendah dan level tinggi (Bolton, 1997). Rancangan percobaan yang diperlukan
dengan metode desain faktorial dua faktor dan dua level sbb:
Tabel III. Rancangan percobaan desain faktorial dengan 2 faktor dan 2 level
Formula Faktor A Faktor B
(1) - -
a + -
b - +
ab + +
Keterangan :
Optimasi campuran dua bahan (dua faktor) dengan desain faktorial
dianalisis berdasarkan rumus:
Y = b0 + b1(A) + b2(B) + b12 (A)(B)...(1)
Dengan:
Y = respon hasil atau sifat yang diamati
(A),(B) = level bagian A, level bagian B, yang nilainya -1 dan +1 b0, b1, b2, b12 = koefisien, dapat dihitung dari hasil percobaan
Dari persamaan di atas dan data yang diperoleh kemudian dibuat contour
plot suatu respon tertentu yang dapat digunakan untuk mengetahui komposisi
campuran yang optimum (Bolton, 1997).
Besarnya efek masing-masing faktor, maupun efek interaksinya dapat
diperoleh dengan menghitung selisih antara respon pada level tinggi dan rata-rata
respon pada level rendah, yaitu:
Efek faktor A =
2 ) 1
( ab b
a
Efek faktor B =
2 ) 1
( ab a
b
Efek faktor C =
2 ) 1
( a
b
ab
(Bolton, 1997).
I. Landasan Teori
Tempe diketahui mempunyai potensi sebagai bahan anti ageing dengan
adanya kandungan isoflavon yang mempunyai daya antioksidan yang lebih besar
dibandingkan dengan kedelai karena adanya senyawa faktor-II. Senyawa ini
hanya dijumpai pada tempe karena terbentuk selama proses perendaman
fermentasi kedelai (Ariani, 2003).
Radiasi sinar UV dapat menyebabkan photoaging akibat reaksi dengan
17
scavengers dapat mencegah peristiwa photoaging tersebut sehingga akan
mengurangi kerusakan collagen yang berperan sebagai protein pembentuk
elastisitas kulit. Oleh karena itu, isoflavon tempe mempunyai potensi sebagai
anti-ageing yang efektif mencegah photoaging (Chiang et.al, 2007).
Bentuk sediaan yang digemari untuk aplikasi kosmetik yaitu krim. Hal
ini disebabkan oleh sifat krim yang mudah dioleskan, mudah menyebar, daya
penetrasi tinggi, memberi rasa melembabkan di kulit, mudah dibersihkan dan
dapat atau tidak dapat dicuci dengan air (Mitsui, 1993).
Cetyl alcohol sebagai basis tidak larut air dalam formula krim ini
mempunyai kemampuan untuk menjaga stabilitas, memperbaiki tekstur, dan
meningkatkan konsistensi krim (Rowe et.al, 2009). Sedangkan gliserin sebagai
humektan bersifat dapat mempertahankan kelembapan kulit dan meningkatkan
daya sebar (Rowe et.al, 2009). Cetyl alcohol dan gliserin yang mempunyai sifat
berlawanan, yaitu cetyl alcohol meningkatkan viskositas dan gliserin
meningkatkan daya sebar maka dilakukan optimasi kedua bahan tersebut sehingga
dapat diperoleh komposisi optimum yang sesuai dengan sifat fisik dan stabilitas
krim.
Untuk mengetahui efek faktor dan interaksi yang paling dominan dari
masing-masing uji sifat fisis dan stabilitas krim, maka digunakan metode desain
J. Hipotesis
Hipotesis dari penelitian ini adalah :
a. Ekstrak etil asetat isoflavon tempe mempunyai daya antioksidan melalui uji
penangkapan radikal hidroksil dengan metode DPPH.
b. Terdapat pengaruh yang bermakna (signifikan) dari komposisi cetyl alcohol,
gliserin, dan interaksi cetyl alcohol-gliserin dalam formula krim anti-ageing
yang dominan dalam menentukan sifat fisik dan stabilitas krim anti ageing
19
BAB III
METODE PENELITIAN
A. Jenis dan Rancangan Penelitian
Penelitian dilakukan dengan metode eksperimental murni yang bersifat
eksploratif dengan menggunakan desain faktorial.
B. Variabel dan Definisi Operasional
Variabel yang digunakan dalam penelitian ini adalah sbb:
1. Variabel Bebas
Komposisi cetyl alcohol dan humektan gliserin.
2. Variabel Tergantung
Sifat fisis dan stabilitas krim anti ageing isoflavon tempe yang meliputi :
viskositas, daya sebar, tipe emulsi, dan pergeseran viskositas.
3. Variabel Pengacau Terkendali
Kondisi wadah tempat penyimpanan dan intensitas cahaya penyimpanan.
4. Variabel Pengacau Tak Terkendali
Suhu dan kelembaban ruangan penelitian.
Definisi operasional yang digunakan dalam penelitian ini adalah sbb :
a. Basis adalah bahan dasar krim yang menentukan sifat dasar krim dan
menentukan keberhasilan atau kegagalan terapi (Voigt, 2004).
b. Faktor adalah gliserin pada level rendah 5 gram dan level tinggi 10 gram;
c. Interaksi gliserin-cetyl alcohol yang mempengaruhi sifat fisik dan
stabilitas.
d. Respon adalah sifat atau hasil percobaan yang diamati yaitu sifat fisik
berupa daya sebar dan viskositas. Stabilitas fisik berupa pergeseran
viskositas.
e. Daya antioksidan adalah dinyatakan dengan % scavenging, dikatakan aktif
sebagai antioksidan jika % scavenging leih besar dari atau sama dengan
50% (Purwata, 2009) dan dikatakan antioksidan kuat jika nilai IC50
kurang dari 200 µg/ml ( Andayani dkk, 2008).
f. Daya sebar adalah kemampuan penyebaran krim pada kulit 5-7 cm dengan
aplikasi beban 125 gram selama 1 menit (Garg, A., Aggarwal, D., Garg,
S., Singla, A.K., 2002).
g. Viskositas adalah memiliki rentang viskositas yang dapat diterima adalah
145-175 d.Pa.s.
h. Pergeseran viskositas adalah dikatakan stabil jika setelah penyimpanan
selama 30 hari terjadi pergeseran viskositas kurang dari 11%.
i. Contour plot adalah grafik yang merupakan hasil dari respon sifat fisis dan
stabilitas krim.
j. Contour plot superimpossed adalah grafik area pertemuan yang memuat
semua arsiran dalam contour plot yang diprediksikan sebagai area
21
k. Area optimum adalah area kondisi yang menghasilkan krim dengan daya
sebar 5 sampai 7 cm, viskositas 145-175 d.Pa.s, persen pergeseran
viskositas adalah kurang dari 11%.
C. Bahan Penelitian
Tempe dibungkus daun pisang dan berbentuk persegi panjang (diperoleh
dari pasar STAN, Paingan, Sleman), aquadest, Metanol teknis, Petroleum eter
teknis, Etil asetat teknis (Brataco), MgSO4 teknis, plat silica GF254, Metanol p.a,
pereaksi DPPH, Asam stearat farmasetis, VCO, Cetyl Alcohol farmasetis,
Trietanolamin, Gliserin, BHT (Brataco), dan Metil paraben.
D. Alat Penelitian
Glasswares Lab. FTS USD (pyrex), vaccum rotary evaporator
(Janke-Kulken), seperangkat spectrophotometer UV/Vis (optima), neraca elektrik,
waterbath, mixer (Airlux), viscotester (Rion-Japan VT-04), tabung skala, alat uji
daya sebar, mikroskop BM-180 Boeco Germany, Spektrofotometer visibel, dan
E. Tata Cara Penelitian
Pengumpulan dan pengolahan tempe ↓
Isolasi Isoflavon tempe ↓
Identifikasi kualitatif isoflavon tempe dengan KLT ↓
Uji Antioksidan metode DPPH ↓
Formulasi Krim ↓
Uji Sifat Fisik dan Stabilitas Sediaan
Gambar 6. Alur Penelitian Singkat
1. Pengumpulan Tempe, Pengolahan Tempe, dan Isolasi Isoflavon Tempe
Tempe yang dibungkus dengan daun pisang berbentuk persegi panjang
sebanyak 1 kg, diperoleh dari pasar STAN paingan Sleman pada saat pagi hari.
Tempe tersebut kemudian dihaluskan dan ditimbang sebanyak enam ratus gram.
600 gram tempe ditambah 400 mL aquadest. Kemudian diblender selama 3x5
menit. Ditambahkan 1.200 mL metanol teknis, dimaserasi selama dua belas jam
pada kecepatan 120 rpm. Setelah dimaserasi dua belas jam kemudian disaring.
Ektrak yang diperoleh dipekatkan dengan vaccum rotary evaporator pada suhu
600C selama kurang lebih 1 jam untuk setiap 300 mL ekstrak metanol sampai
diperoleh ekstrak kental ±100 mL (Ariani, 2003).
Ekstrak kental diekstraksi dengan penggojogan selama satu menit,
menggunakan pelarut 5x150 mL petroleum eter, ambil fase bagian bawah
kemudian diekstraksi lagi dengan 5x150 mL etil asetat. Fase etil asetat di bagian
atas diambil dan dibebaskan dari air dengan MgSO4 anhidrat sebanyak ±15 gram
23
asetat dengan vaccum rotary evaporator pada suhu 400C selama kurang lebih 1
jam untuk setiap 300 mL ekstrak etil asetat sampai diperoleh ekstrak kental etil
asetat isoflavon (Ariani, 2003).
2. Identifikasi Isoflavon dengan Metode Kromatografi Lapis Tipis (KLT)
Sedikit isolat hasil isolasi isoflavon dilarutkan dalam metanol p.a dan
ditotolkan sebanyak sembilan kali totolan menggunakan pipa kapiler pada fase
diam silica gel GF 254. Ditunggu hingga kering kemudian eluen dikembangkan
dalam fase gerak kloroform : metanol = 3 : 1. Setelah eluen dikembangkan,
reaksikan dengan uap amonia selama sepuluh menit dan diamati dengan lampu
UV 254nm (Ariani, 2003).
3. Uji Antioksidan Isoflavon dari Tempe dengan Metode DPPH
a.Pembuatan Larutan Reagen DPPH 0,1 mM. Ditimbang 0, 00788 gram
DPPH. Dilarutkan dalam metanol p.a, tambahkan sampai 200 ml.
b.Pembuatan Larutan Stok Antioksidan Pembanding BHT. Ditimbang
0,0027 gram BHT. Dilarutkan dalam metanol p.a, ditambahkan sampai 25
ml. Sehingga akan didapat larutan stok BHT dengan konsentrasi 0,5 mM.
c.Pembuatan Seri Konsentrasi Antioksidan Pembanding BHT. Diambil
larutan stok BHT sebanyak 1 ml; 1,5 ml; 2 ml; 5 ml. Kemudian
masing-masing konsentrasi dilarutkan dan ditambahkan dengan metanol p.a
sampai 10 ml. Sehingga akan diperoleh seri konsentrasi BHT 0,05 mM;
0,075 mM; 0,1 mM; 0,25 mM.
d.Pengukuran Absorbansi BHT dengan Spektrofotometer Visibel. Diambil
sebanyak 0,5 ml. Ulangi perlakuan yang sama untuk setiap seri
konsentrasi. Didiamkan dalam ruangan gelap dengan suhu kamar selama
tiga puluh menit. Setelah tiga puluh menit, diukur absorbansi pada
panjang gelombang 517 nm.
e.Pembuatan Larutan Stok Ekstrak Etil Asetat Isoflavon. Ditimbang 12,5
gram ekstrak etil asetat isoflavon. Dilarutkan dalam metanol p.a,
ditambahkan sampai 25 ml. Sehingga akan diperoleh larutan stok ekstrak
etil asetat isoflavon dengan konsentrasi 50 % b/v.
f. Pembuatan Seri Konsentrasi Ekstrak Etil Asetat Isoflavon. Diambil larutan
stok ekstrak etil asetat isoflavon sebanyak 2 ml; 4 ml; 6 ml; 8 ml; 10 ml.
Kemudian masing-masing konsentrasi dilarutkan dan ditambahkan
dengan metanol p.a sampai 10 ml. Sehingga akan diperoleh seri
konsentrasi ekstrak etil asetat isoflavon 10 % b/v; 20 % b/v; 30 % b/v; 40
% b/v; 50 % b/v.
g.Pengukuran Absorbansi Sampel dengan Spektrofotometer Visible.
Diambil larutan reagen DPPH sebanyak 7,5 ml ditambahkan dengan
larutan sampel (ekstrak etil asetat isoflavon) sebanyak 0,5 ml. Perlakuan
diulang untuk setiap seri konsentrasi. Didiamkan dalam ruangan gelap
dengan suhu kamar selama tiga puluh menit. Setelah tiga puluh menit,
diukur absorbansi pada panjang gelombang 517 nm (Lee, J., Renita, M.,
25
4. Formulasi Sediaan Krim Anti-aging isoflavon dari Tempe
Formula vanishing cream yang digunakan dalam formulasi sediaan krim
ini adalah formula standar (Young, 1972) sbb :
a. Stearic acid 20,0
Cetyl alcohol 0,50
Triethanolamine 1,20
b. Sodium hydroxide one microspatula-full
Glycerine 8,0
Distilled water 69,94
Preservative (Nipagin) one microspatulla-full
c. Perfume three or four drops
Modifikasi formula yang digunakan dalam penelitian ini adalah sbb :
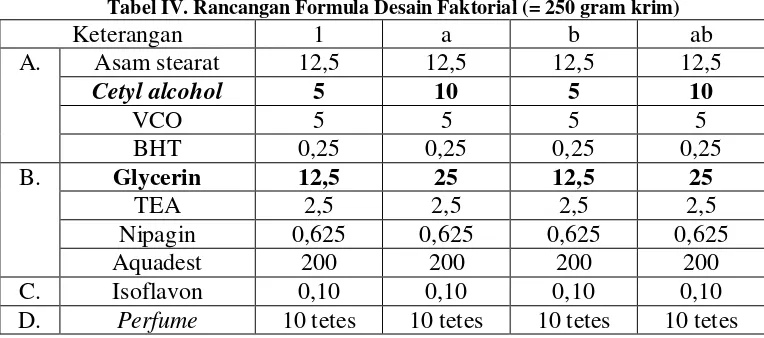
Tabel IV. Rancangan Formula Desain Faktorial (= 250 gram krim)
Keterangan 1 a b ab
Asam stearat 12,5 12,5 12,5 12,5
Cetyl alcohol 5 10 5 10
VCO 5 5 5 5
A.
BHT 0,25 0,25 0,25 0,25
Glycerin 12,5 25 12,5 25
TEA 2,5 2,5 2,5 2,5
Nipagin 0,625 0,625 0,625 0,625
B.
Aquadest 200 200 200 200
C. Isoflavon 0,10 0,10 0,10 0,10
D. Perfume 10 tetes 10 tetes 10 tetes 10 tetes
Bagian A dipanaskan di hotplate hingga suhu 700C. Setelah semua
meleleh dan mencapai suhu 700C, maka masukkan cetyl alcohol ke dalam asam
stearat, diaduk hingga homogen. Ditambahkan BHT ke dalam VCO sebagai
emollient dan penetration enhancer, diaduk hingga homogen. Ditambahkan VCO
tersebut ke dalam campuran cetyl alcohol dengan asam stearat. Fase minyak telah
siap.
Bagian B dipanaskan di hotplate hingga suhu 700C. Setelah semua
homogen. Ditambahkan nipagin ke dalam gliserin, aduk hingga homogen.
Ditambahkan gliserin ke dalam aquadest yang telah ditambahkan TEA. Campuran
tersebut kemudian diaduk. Fase air telah siap.
Fase air yang telah siap ditambahkan ke dalam fase minyak dengan suhu
pencampuran 700C di atas waterbath, diaduk dengan mixer selama sepuluh menit
(Young, 1972). Ditambahkan isoflavon pada saat pencampuran dengan mixer,
pada saat pencampuran telah berjalan selama lima menit. Setelah 10 menit,
dituangkan krim ke dalam wadah dan tunggu hingga suhu krim 450C, pada saat
suhu tersebut ditambahkan parfum kemudian diaduk hingga homogen.
5. Uji Sifat Fisik dan Stabilitas Sediaan Krim
a.Uji daya sebar. Ditimbang krim seberat 1 gram dan diletakkan di tengah
kaca bulat berskala. Di atas krim diletakkan kaca bulat lain dan pemberat
dengan berat total 125 gram, didiamkan selama 1 menit, dicatat diameter
penyebarannya.
b.Uji Viskositas. Pengukuran viskositas menggunakan Viscotester Rion seri
VT 04 dengan cara: krim dimasukkan dalam wadah dan dipasang pada
portable viscotester. Viskositas krim diketahui dengan mengamati
gerakan jarum penunjuk viskositas.
c.Uji Mikromeritik (Ukuran Droplet). Dioleskan sejumlah krim pada gelas
objek kemudian diletakkan meja benda pada mikroskop. Diamati ukuran
droplet yang terdispersi pada krim. Gunakan perbesaran lemah untuk
menentukan objek yang akan diamati kemudian ganti dengan perbesaran
27
Dalam penelitian ini pengamatan mikromeritik dilakukan dengan
mengambil beberapa foto preparat krim dan tampak adanya
droplet-droplet yang akan ditentukan diameternya. Selanjutnya pengukuran
diameter droplet dilakukan dengan menggunakan software Motic image
plus 2.0 hingga didapatkan µm diameter dari 500 droplet yang akan
diukur.
d.Uji Tipe Emulsi (Metode Warna). Beberapa tetes biru metilen
dicampurkan ke dalam suatu formula krim. Jika seluruh krim berwarna
seragam, maka terdapat suatu emulsi dari jenis m/a, oleh karena air adalah
fase luar (Voigt, 1994).
F. Analisis Hasil
Data daya sebar, viskositas, dan pergeseran viskositas dianalisis dengan
perhitungan efek menurut desain faktorial untuk mengetahui efek yang paling
dominan dalam menentukan sifat fisik dan stabilitas krim. Untuk mengetahui
komposisi basis cetyl alcohol dan humektan gliserin yang optimum dengan
penggabungan contour plot masing-masing respon yang dikenal dengan contour
plot superimpossed.
Untuk mengetahui signifikansi dari setiap faktor dan interaksi dalam
mempengaruhi respon maka dilakukan analisis dengan Yate’s Treatment.
Berdasarkan analisis tersebut maka dapat ditentukan signifikansi efek dominan
Sebelumnya ditentukan hipotesis terlebih dahulu, hipotesis alternatif
(H1) menyatakan adanya signifikansi efek dominan faktor terhadap respon,
sedangkan H0 merupakan negasi dari H1 yang menyatakan tidak adanya
signifikansi efek dominan faktor terhadap respon. H1 diterima dan H0 ditolak
apabila harga F hitung lebih besar daripada harga F tabel, yang berarti bahwa
29
BAB IV
HASIL dan PEMBAHASAN
A. Isolasi dan Identifikasi Ekstrak Etil Asetat Isoflavon Tempe 1. Isolasi Ekstak Etil Asetat Isoflavon Tempe
Diperoleh sebanyak 1 kg tempe yang telah dikumpulkan dari produsen
yang sama di pasar STAN setiap pagi hari, dengan bentuk tempe persegi panjang
yang dibungkus dengan daun pisang. Sebanyak 600 gram tempe selanjutnya
diolah sesuai dengan tata cara penelitian untuk mendapatkan ekstrak etil asetat
isoflavon.
Tempe yang telah dihaluskan kemudian ditambah dengan metanol
sehingga diperoleh ekstrak metanol sebanyak 1.200 mL dan di maserasi. Ekstrak
metanol tersebut selanjutnya dipekatkan dengan rotary vacuum evaporator
sehingga didapatkan ekstrak kental metanol sebanyak 100 mL.
Setelah mendapatkan ekstrak kental metanol, dilanjutkan dengan
ekstraksi pelarut petroleum eter dan diambil fase bagian bawah untuk selanjutnya
diekstraksi kembali dengan petroleum eter sampai 5 kali. Sehingga akan diperoleh
ekstrak petroleum eter kurang lebih 750 mL.
Selanjutnya ekstrak petroleum eter tersebut diekstraksi lagi menggunakan
pelarut etil asetat dan diambil fase bagian atas, sedangkan fase bagian bawah
diekstraksi kembali dengan etil asetat sampai 5 kali. Sehingga akan diperoleh
kemudian dipekatkan menggunakan vacuum rotary evaporator sehingga akan
diperoleh ekstrak kental etil asetat isoflavon kurang lebih 70 ml.
2. Identifikasi Ekstrak Etil Asetat Isoflavon Tempe
Isolasi isoflavon tempe pada penelitian ini didasarkan pada penelitian
yang dilakukan oleh Ariani, 2003. Pada penelitian tersebut diperoleh hasil yang
menunjukkan bahwa ekstrak etil asetat mengandung isoflavon. Sedangkan pada
penelitian ini, dilakukan pula identifikasi ekstrak etil asetat isoflavon tempe
dengan menggunakan sistem yang sama dengan penelitan Ariani, 2003. Hasil
yang diperoleh pada penelitian ini adalah sbb :
Fase gerak = metanol : kloroform = 3 : 1 Fase diam = silica gel GF 254
Detektor : UV 254 nm
Gambar 7. Hasil Uji KLT
Tabel IV. Perhitungan Rf Uji KLT Ekstrak Etil Asetat Isoflavon
Bercak Rf Bercak
Bercak I 0,0867
Bercak II 0,6734
Bercak III 0,7334
B. Uji Antioksidan Ekstrak Etil Asetat Isoflavon dengan Metode DPPH (2,2-difenil-1-pikrilhidrazil)
Pengujian ini dilakukan dengan mengukur penangkapan radikal sintetik
DPPH dalam pelarut organik, yaitu metanol yang digunakan dalam penelitian ini.
31
menangkap radikal sintetik DPPH yang akan memberikan warna ungu pada
panjang gelombang 517 nm. Setelah itu, didiamkan selama 30 menit pada suhu
kamar dan ruangan yang gelap, supaya sampel (ekstrak etil asetat isoflavon
tempe) dapat bereaksi dengan DPPH. Adanya aktivitas antioksidan dari sampel
dapat dilihat dengan adanya perubahan warna pada larutan DPPH yang semula
ungu pekat jadi kuning pucat (Andayani dkk, 2008). Penghilangan warna ini
terjadi akibat adanya peristiwa penangkapan elektron radikal bebas DPPH oleh
atom hidrogen dari isoflavon yang menyebabkan elektron menjadi berpasangan
dapat secara ringkas digambarkan dengan skema, seperti ditunjukkan pada
gambar 8. Penghilangan warna yang terjadi juga sebanding dengan jumlah
elektron radikal bebas yang diikat oleh atom hidrogen isoflavon. Oleh karena itu
semakin besar konsentrasi antioksidan isoflavon serapan yang dihasilkan akan
semakin kecil.
DPPH → mempunyai elektron bebas yang reaktif (radikal bebas) ↓
Absorbansi maksimal 517 nm berwarna ungu ↓
Penambahan isofavon sebagai antioksidan ↓
Didiamkan dalam ruangan gelap selama 30 menit ↓
Atom H dari isoflavon menangkap radikal bebas ↓
Menjadi elektron yang berpasangan ↓
Absorbansi maksimal 517 nm berwarna kuning pucat
Gambar 8. Skema Tahapan Reaksi Isoflavon sebagai Antioksidan
Uji antioksidan ekstrak etil asetat isoflavon dilakukan dengan metode
DPPH didahului dengan uji antioksidan BHT dengan metode DPPH. Hal ini
dilakukan untuk mengetahui ketepatan metode yang kita pilih, sebab BHT
merupakan bahan yang sudah terbukti sebagai antioksidan karena memiliki %
scavenging lebih besar dari 50%.
Dari uji yang dilakukan, membuktikan bahwa ekstrak etil asetat isoflavon
dari tempe terbukti mempunyai daya antioksidan dengan data % scavenging lebih
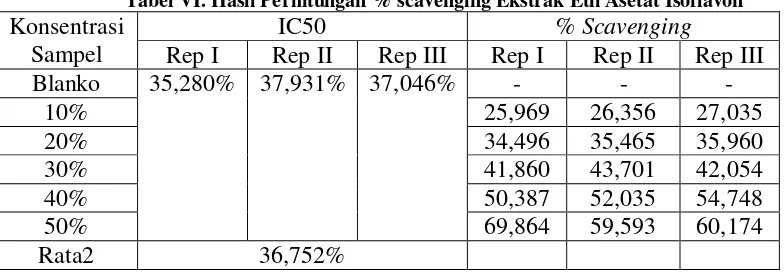
dari 50%. Pada tabel VI ditunjukkan bahwa nilai IC50 rata-rata dari tiga replikasi
isoflavon adalah sebesar 36,752%. Hasil ini menunjukkan bahwa untuk
menangkap elektron radikal bebas sebanyak 50% dibutuhkan isoflavon dengan
konsentrasi sebesar 36,752% dalam formula. Ketiga replikasi yang kami lakukan
memiliki nilai CV sebesar 0,037% sehingga memenuhi persyaratan kurang dari
2%.
Tabel VI. Hasil Perhitungan % scavenging Ekstrak Etil Asetat Isoflavon
IC50 % Scavenging
Konsentrasi
Sampel Rep I Rep II Rep III Rep I Rep II Rep III
Blanko - - -
10% 25,969 26,356 27,035
20% 34,496 35,465 35,960
30% 41,860 43,701 42,054
40% 50,387 52,035 54,748
50%
35,280% 37,931% 37,046%
69,864 59,593 60,174
Rata2 36,752%
C. Pembuatan Krim
Krim yang dibuat pada penelitian ini terdiri dari dua fase, yaitu fase
minyak yang terdiri dari asam stearat, cetyl alcohol, VCO, dan BHT. Sedangkan
33
dipanaskan hingga suhu 700C. Pemanasan ini bertujuan untuk melelehkan asam
stearat dan cetyl alcohol yang merupakan fase minyak, sehingga memudahkan
terjadinya reaksi dengan basa yang larut dalam fase air sebab jika leleh maka luas
permukaan kontak menjadi lebih besar. Pemanasan juga berfungsi untuk
menurunkan tegangan permukaan antara fase air dan fase minyak sehingga emulsi
akan terbentuk dengan baik. Selain kedua tujuan di atas, pemanasan juga
berfungsi untuk mempercepat reaksi penyabunan asam stearat oleh basa TEA.
Setelah semua bahan leleh dan kedua fase mempunyai suhu yang sama,
campuran tersebut dicampur dengan mixer di dalam bekker glass yang telah
dihangatkan terlebih dahulu sampai ± 700C. Hal ini bertujuan untuk mencegah
terjadinya perubahan suhu yang mendadak sehingga akan menyebabkan asam
stearat membeku kembali dan mengurangi kehomogenan krim.
Asam stearat dalam fase minyak akan bereaksi dengan TEA yang bersifat
basa terlarut dalam fase air, sehingga akan terjadi reaksi penyabunan yang
menghasilkan garam/sabun amin yaitu Trietanolaminstearat (Voigt, 2004). Sabun
Trietanolaminstearat ini akan berfungsi sebagai emulgator yang akan
menyelubungi droplet-droplet fase minyak, sehingga dapat didispersikan ke dalam
fase air dan terbentuklah sistem emulsi.
Pembuatan krim dalam penelitian ini, dilakukan dengan pengadukan
menggunakan mixer. Hal ini bertujuan supaya pengadukan yang terjadi konstan
dan kontinyu. Pengadukan yang terjadi harus kontinyu dan konstan supaya emulsi
yang terbentuk stabil ditandai salah satunya dengan tidak terjadi pemisahan fase
Setelah kedua fase tersebut dicampur dan telah terbentuk basis krim,
isoflavon didispersikan sesuai konsentrasi yang biasa digunakan dalam kosmetik
antara 1-500 mg/kg (Zulli, 2002), sedangkan dalam formula ini yang ditambahkan
adalah 400 mg/kg.
D. Sifat Fisik dan Stabilitas Krim Anti-Aging Ekstrak Etil Asetat Isoflavon Tempe
1. Pengujian Tipe Krim
Hasil pengujian tipe krim dengan metode warna menggunakan metylen
blue, yang terlihat fase kontinyu berwarna biru dan fase terdispersi tidak
berwarna. Dari gambar terlihat bahwa krim merupakan tipe m/a. Hal ini terkait
dengan sifat metylen blue yang merupakan pewarna larut air. Dengan adanya
penambahan metylen blue menyebabkan fase air berwarna biru dan fase minyak
tidak berwarna seperti ditunjukkan pada gambar 9.
Formula 1
Formula a
Formula b Formula ab
Gambar 9. Hasil Pengujian Mikroskopik Tipe Krim Tiap Formula (perbesaran 40x)
Fase air
35
2. Karakteristik Ukuran Droplet dengan Metode Mikroskopik
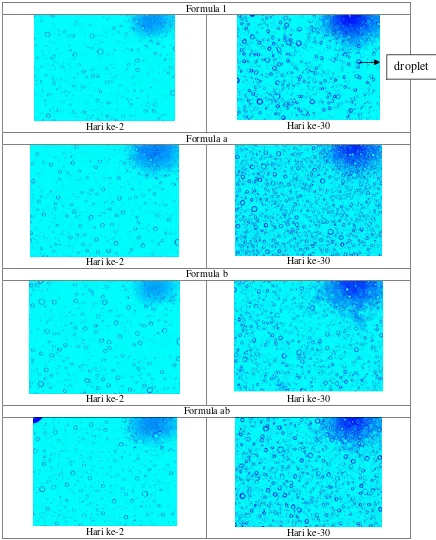
Karakteristik gambaran droplet selama 30 hari penyimpanan adalah
sebagai berikut :
Formula 1
Hari ke-2 Hari ke-30
Formula a
Hari ke-2 Hari ke-30
Formula b
Hari ke-2 Hari ke-30
Formula ab
Hari ke-2 Hari ke-30
Gambar 10. Karakteristik Ukuran Droplet Tiap Formula Hari ke-2 dan Hari ke-30
Stabilitas krim yang merupakan sistem emulsi dapat dilihat dari
gambaran ukuran droplet selama kurun waktu penyimpanan. Kondisi yang stabil
dan ideal adalah tidak terjadi perubahan ukuran droplet ke arah yang lebih besar.
Dari gambar 10, menunjukkan gambar secara visualisasi ukuran droplet yang
terlihat bahwa tidak terjadi perubahan ukuran droplet ke arah yang lebih besar,
sehingga dapat dikatakan bahwa sistem emulsi formula 1, a, b, dan ab adalah
stabil secara visual.
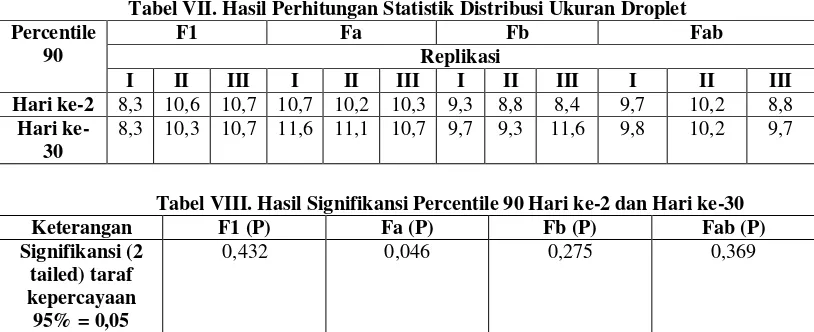
Tabel VII. Hasil Perhitungan Statistik Distribusi Ukuran Droplet
F1 Fa Fb Fab
Replikasi Percentile
90
I II III I II III I II III I II III
Hari ke-2 8,3 10,6 10,7 10,7 10,2 10,3 9,3 8,8 8,4 9,7 10,2 8,8
Hari ke-30
8,3 10,3 10,7 11,6 11,1 10,7 9,7 9,3 11,6 9,8 10,2 9,7
Tabel VIII. Hasil Signifikansi Percentile 90 Hari ke-2 dan Hari ke-30
Keterangan F1 (P) Fa (P) Fb (P) Fab (P)
Signifikansi (2 tailed) taraf kepercayaan 95% = 0,05
0,432 0,046 0,275 0,369
Hal ini juga dibuktikan dengan hasil uji statistik yang ditunjukkan dalam
tabel VII. Bahwa nilai percentile 90 formula 1, b, dan ab untuk hari ke-2 dan hari
ke-30 tidak berbeda signifikan dibuktikan dengan uji statistik paired T-test yang
ditunjukkan pada tabel VIII, sehingga dapat dikatakan bahwa ukuran droplet
stabil karena tidak tejadi perubahan ukuran droplet ke arah yang lebih besar yang
menyebabkan sistem emulsi tidak stabil pada formula 1, b, dan ab. Percentile 90
merupakan suatu parameter nilai yang menunjukkan sejumlah 90% partikel
mempunyai ukuran droplet kurang dari nilai yang tertera. Parameter percentile 90
37
Adanya kestabilan sistem emulsi pada ketiga formula tersebut dapat
disebabkan oleh elastisitas emulgator yang terdiri dari asam stearat dan TEA
menjadi sabun amin, trietanolaminstearat, adalah cukup baik. Kelebihan dari
emulgator sabun amin ini adalah dapat menghasilkan dispersi halus dan emulsi
yang stabil dan bersifat netral sehingga aman digunakan topikal (Voigt, 2004).
Selain itu, kestabilan sistem emulsi yang dihasilkan oleh krim isoflavon ini terkait
dengan tingginya viskositas krim yang disebabkan oleh adanya TEA sebagai
emulgator dan cetyl alcohol sebagai basis. TEA merupakan basa yang dapat
meningkatkan viskositas, sedangkan cetyl alcohol merupakan basis yang bersifat
sebagai thickening agent. Menurut hukum Stoke, penggabungan droplet dapat
dicegah dengan meningkatkan viskositas sehingga gerak partikel terdispersi akan
semakin lambat sehingga akan meningkatkan tingkat dispersitas (Voigt, 2004).
Namun, terjadi keridakstabilan pada formula a, hal ini terlihat dari nilai
percentile 90 yang menunjukkan perbedaan signifikan menjadi partikel yang
berukuran lebih besar dari hari ke-2 dan hari ke-30. Hal ini dapat disebabkan oleh
adanya fenomena ketidakstabilan emulsi yaitu koalesens dan ostwald ripening
seperti ditunjukkan pada gambar 11 :
Gambar 11. Fenomena Ketidakstabilan Sistem Emulsi Formula a koalesens Ostwald
Fenomena koalesens adalah bergabungnya droplet kecil membentuk suatu droplet
yang lebih besar dan lapisan film di sekitar droplet kecil itu akan menghilang,
sedangkan ostwald rippening adalah suatu fenomen ketidakstabilan emulsi di
mana droplet-droplet kecil bergabung dengan droplet yang berukuran lebih besar
sehingga akan membentuk droplet yang berukuran besar. Ketidakstabilan formula
a ini disebabkan oleh ukuran droplet yang dari awal yaitu pada hari ke-2 sudah
cukup besar, sehingga akan membuat sistem emulsi tersebut menjadi tidak stabil.
Namun, karena adanya keterbatasan penelitian maka tidak dapat diketahui kapan
saat emulsi tersebut mulai tidak stabil. Oleh karena itu, pada penelitian
selanjutnya, hendaklah dilakukan pengamatan setiap minggu sehingga kita dapat
mengetahui kapan emulsi tersebut mulai tidak stabil.
3. Uji Sifat Fisis dan Stabilitas Krim
Krim yang baik harus memenuhi sifat fisik dan stabilitas sediaan
semisolid, yaitu daya sebar, viskositas, dan pergeseran viskositas. Keberhasilan
terapi suatu sediaan semisolid sangat ditentukan oleh faktor daya sebar (Garg
et.al, 2002) karena daya sebar merupakan gambaran mudah atau tidaknya pasien
dalam mengaplikasikan (mengoleskan) sediaan. Uji daya sebar pada penelitian ini
bertujuan untuk melihat seberapa mudah 1 g sampel krim dapat menyebar bila
ditekan dengan pemberat 125 g. Parameter yang dihitung adalah rata-rata dua
diameter penyebaran krim setelah pemberian beban selama 1 menit. Krim
tergolong bersifat semifluid dengan daya sebar antara 5 -7 cm (Garg et. al, 2002).
Viskositas krim perlu diuji sebab terkait dengan konsistensi dari suatu
39
sesuai ketika krim digunakan. Viskositas berbanding terbalik dengan daya sebar
yaitu ketika viskositas lebih tinggi, daya sebar krim kebih kecil, dan sebaliknya
(Garg et.al, 2002).
Pergeseran viskositas merupakan parameter stabilitas krim, sebab ada
banyak faktor dari dalam maupun luar luar yang dapat mempengaruhi stabilitas
sediaan selama penyimpanan. Pergeseran viskositas ini erat kaitannya dengan
konsistensi sediaan dan penerimaan pasien. Diperoleh data sifat fisik krim
anti-ageing ekstrak etil asetat isoflavon adalah sbb :
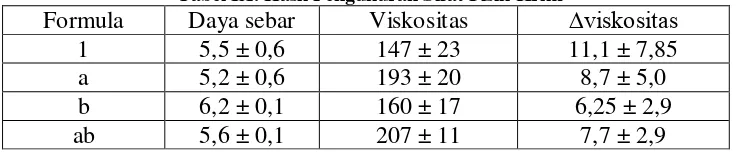
Tabel IX. Hasil Pengukuran Sifat Fisik Krim
Formula Daya sebar Viskositas ∆viskositas
1 5,5 ± 0,6 147 ± 23 11,1 ± 7,85
a 5,2 ± 0,6 193 ± 20 8,7 ± 5,0
b 6,2 ± 0,1 160 ± 17 6,25 ± 2,9
ab 5,6 ± 0,1 207 ± 11 7,7 ± 2,9
Tabel X. Efek Cetyl alcohol, Efek Gliserin, dan Efek Interaksi Cetyl alcohol -Gliserin dalam Menentukan Sifat Fisik Krim
Efek Daya sebar Viskositas ∆viskositas
Cetyl alcohol 0,45 46 0,475
Gliserin 0,55 13 2,929
Interaksi 0,15 0 1,925
a. Daya Sebar
Berdasarkan tabel IX, dapat diketahui hasil uji sifat fisik daya sebar krim
yang menunjukkan bahwa krim termasuk sediaan semifluid karena memiliki daya
sebar 5-7 cm (Garg, et al., 2002) hasil uji sifat fisik krim. Sedangkan dari nilai SD
kurang dari 10% maka dapat dikatakan bahwa data kita homogen dan bersifat
reprodusible.
Berdasarkan tabel X, gliserin diprediksi memberikan efek paling
interaksi. Faktor cetyl alcohol dan interaksi berespon negatif terhadap
daya sebar yang berarti akan menurunkan respon daya sebar, sedangkan faktor
gliserin sebagai faktor paling dominan dalam menentukan efek berespon positif
yang berarti akan menaikkan respon daya sebar. Untuk mengetahui signifikansi
dari dominansi efek faktor cetyl alcohol, gliserin, dan interaksi terhadap respon
daya sebar krim dapat dilakukan uji statistik yate’s treatment.
Hasil uji yate’s treatment pada tabel IX, efek dominan gliserin tidak
signifikan dalam mempengaruhi peningkatan respon daya sebar. Hal ini dapat
dianalisis dari nilai F hitung faktor cetyl alcohol, gliserin, dan interaksi lebih kecil
daripada F tabel yaitu 5,32. Sehingga dapat disimpulkan bahwa faktor cetyl
alcohol, gliserin, dan interaksi tidak berpengaruh signifikan dalam menentukan
respon daya sebar krim.
Tabel XI. Hasil Perhitungan Yate’s Treatmen untuk Respon Daya Sebar
Source pf variation
Degree of Freedom
Sum of Squares
Mean Squares
F
Replicates 2 0,665 0,3325
Treatment 3 1,33 0,443
a 1 0,743 0,743 4,5583
b 1 0,601 0,601 3,6871
ab 1 -0,041 -0,041 -0,2515
Experimental error
8 1,305 0,163
Total 11 3,3
Untuk melihat hubungan pengaruh pengingkatan level cetyl alcohol dan