SKRIPSI
Oleh :
NPM.0633010010 Syirhan Anas Bobsaid
PROGRAM STUDI TEKNOLOGI PANGAN FAKULTAS TEKNOLOGI INDUSTRI
SKRIPSI
Diajukan Untuk Memenuhi Sebagian Persyaratan
Dalam Memperoleh Gelar Sarjana Teknik
Jurusan Teknologi Pangan
Oleh :
NPM.0633010010 Syirhan Anas Bobsaid
PROGRAM STUDI TEKNOLOGI PANGAN FAKULTAS TEKNOLOGI INDUSTRI
SKRIPSI
KAJIAN PENAMBAHAN KITOSAN DAN LAMA WAKTU
PENGENDAPAN TERHADAP AKTIVITAS ANTIOKSIDAN
SARI BUAH DELIMA (Punica granatum L)
Oleh :
NPM. 0633010010 Syirhan Anas Bobsaid
Surabaya, November 2010
Telah disetujui dan diterima dengan baik oleh :
Dosen Pembimbing ke-1 Dosen Pembimbing ke-2
Ir. Rudi Nurismanto, Msi
ix
NPM. 0633010010 SYIRHAN ANAS BOBSAID
INTISARI
Delima merupakan salah satu jenis buah-buahan yang mempunyai kandungan polifenol yang tinggi, dimana senyawa polifenol merupakan agensia antioksidan. Di Indonesia pemanfaatan buah delima masih terbatas, hal ini karena kurangnya pengetahuan masyarakat akan manfaat delima. Salah satu alternative pengolahan buah delima ialah dijadikan sari buah, karena sari buah yang dihasilkan cenderung keruh dan sepat. Maka ditambahkan kitosan sebagai agensia penjernih. Kitosan mampu mengikat senyawa tanin penyebab rasa sepat , mengikat kotoran, menurunkan kadar asam,serta dapat berfungsi sebagai pengawet. Tujuan dari penelitian ini untuk mengetahui pengaruh perlakuan penambahan kitosan dan lama waktu pengendapan terhadap aktivitas antioksidan sari buah delima.
Penelitian ini menggunakan metode Rancangan Acak Lengkap (RAL) pola faktorian yang terdiri dari 2 faktor dengan 2 kali ulangan, faktor I adalah penambahan kitosan (0 ;0,5 ;1 dan 1,5 % v/v) dan faktor II adalah lama waktu pengendapan (0, 60, 90 dan 120 menit).
1 PBAB I
PENDAHULUAN
A. Latar Belakang
Delima (Punica granatum L.) merupakan buah yang berasal dari Timur Tengah, tersebar di daerah subtropik sampai tropik, dari dataran rendah sampai di bawah 1.000 m dari permukaan laut. Tumbuhan ini menyukai tanah gembur yang tidak terendam air, dengan air tanah yang tidak dalam. Delima sering ditanam di kebun-kebun sebagai tanaman hias,tanaman obat dan buahnya pun dapat dikonsumsi. Buah delima dapat dimakan dalam keadaan segar, sebagai campuran rujak buah, salad buah, jus atau sari buah (Huriyah, 2010).
Di Indonesia, buah delima kurang mendapat perhatian secara lebih. Pada umumnya buah delima hanya ditanam sebagai tanaman hias dan terakhir buah delima sudah tidak lagi dibudidayakan secara umum di indonesia. Hal ini dikarenakan kurangnya pengetahuan masyarakat akan manfaat dari buah delima itu sendiri sedangkan di Amerika bagian California buah delima telah di budidayakan secara besar-besaran sebagai lahan perkebunan, karena buah ini mempunyai kandungan polifenol yang tinggi dimana polifenol merupakan agensia antioksidan. Di Amerika, produk sari buah delima dikenal sebagai tren minuman kesehatan terkini (Wijanarko, 2008). Di Asia, buah delima diolah menjadi sari buah (Huriyah, 2010).
Universitas Pembangunan Nasional “Veteran” Jawa Timur
itu proses penjernihan juga dimaksudkan untuk mengurangi rasa sepat yang dihasilkan oleh senyawa tanin. Oleh karena itu, dilakukan proses penjernihan untuk menghasilkan sari buah yang jernih. Beberapa jenis bahan penjernih yang umum digunakan sebagai bahan penjernih ialah kitosan, gelatin, CMC, kasein, putih telur (Muljoharjo, 1999; Mulyono et al.,2001).
Universitas Pembangunan Nasional “Veteran” Jawa Timur
lama waktu pengendapan untuk menghasilkan sari buah dengan aktivitas antioksidan tinggi.
B. Tujuan Penelitian
a. Untuk mengetahui pengaruh perlakuan penambahan kitosan dan lama waktu pengendapan terhadap aktivitas antioksidan sari buah delima.
b. Untuk mengetahui kombinasi perlakuan terbaik terhadap sari buah delima yang memiliki aktivitas antioksidan tinggi.
C. Manfaat Penelitian
a. Sebagai informasi kepada masyarakat pada umumnya tentang potensi buah delima sebagai agensia antioksidan.
4
A. Definisi dan komposisi gizi delima
Delima (Punica granatum L.) merupakan tanaman yang sering ditanam di
pekarangan rumah sebagai tanaman hias, sekaligus untuk dimakan buahnya.
Beberapa kultivarnya yang kerdil bahkan telah dikembangkan khusus sebagai
tanaman hias. Delima merah memiliki rasa yang lebih manis dan segar.
Komposisi gizi per 100 gram bagian yang dapat dimakan dari buah delima adalah:
energi 68 kkal, air 81 g; protein 0,95 g; lemak 0,3 g; karbohidrat 17,2 g;Vitamin
C 6,1 mg; serat 0,6 gram . Kandungan lainnya adalah gula inversi 20 persen (5-10
persen di antaranya berupa glukosa), asam sitrat (0,5-3,5 persen),asam borat, dan
asam malat. Mineral yang paling dominan adalah kalium (259 mg/ 100 g).
Kandungan mineral lainnya ialah magnesium(3mg/100gr), fosfor(8mg/100gr),
seng(0,12mg/100gr), tembaga(0,07mg/100gr), kalsium(3mg/100gr) serta besi (0,3
mg/100gr) (Astawan, 2010). Berdasarkan penelitian Harverson et al. (2008) buah
delima memiliki konsentrasi antioksidan yang paling tinggi yaitu 11, 33 mmol /
100 gram lalu diikuti oleh buah anggur diurutan kedua yang hanya memiliki
konsentrasi antioksidan sebesar 2,42 mmol/ 100 gram.
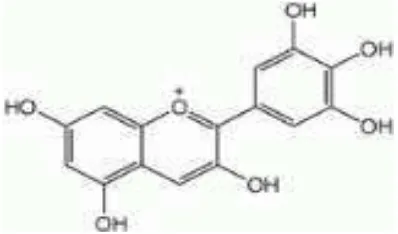
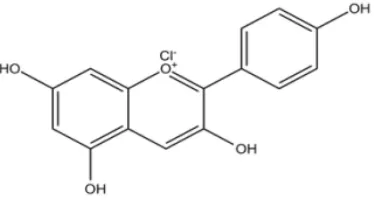
Buah delima merupakan buah yang kaya akan 2 jenis sumber polifenol,
yaitu antosianin yang terdiri atas delphinidin, cyanidin, dan pelargonidin dimana
komponen inilah yang memberikan warna merah pada buah dan minuman sari
buah delima; komponen tanin larut air seperti punicalin, galat pedunculagin , galat
Universitas Pembangunan Nasional “Veteran” Jawa Timur
pada buah utuh, dimana komponen polifenol yang larut pada sari buah delima itu
berkisar anatar 0,2 % – 1 % ( Nar Ben, 1996 dalam Louba, 2007).selain itu
senyawa fitokimia lain yang terdapat dalam delima ialah katekin dan galokatekin
(Plumb dkk.,2002)
Sari buah delima mengandung sumber penting dari kelompok polifenol,
terutama antosianin yang mengandung 3-glukosida dan 3,5-diglukosida dari
delphinidin, cyanidin, and pelargonidin (Du, 1975 dalam Miguel, 2004). Selain itu
dengan adanya gallat tipe tanin, turunan asam elagat serta komponen tanin lain
yang larut air juga memberikan sebuah kontribusi sebagai agensia antioksidan
dalam sari buah delima ( Gil, 2000 dalam Miguel, 2004).
Kandungan ekstrak delima mampu menangkal radikal bebas dan mampu
menurunkan makromolekul oksidatif dan lipida peroksida dalam tubuh hewan
(Rosenblat dkk.. 2006; Jurenka, 2008) serta mampu meningkatkan kapasitas
plasma antioksidan di dalam sel manusia (Guo dkk., 2008 dalam Jurenka,2008)
B. Manfaat delima
a.
Beberapa penelitian menunjukkan bahwa tanin yang terkandung pada
tanaman delima tidak hanya aktif sebagai antibakteri, tetapi juga melawan virus,
antara lain penyebab penyakit cacar. Penelitian terbaru melaporkan bahwa delima
dapat digunakan sebagai obat antidiabetes melitus atau kencing manis. Tanin juga
mampu untuk mereduksi risiko penyakit jantung. Hal itu, disebabkan oleh
kemampuan tannin untuk mereduksi oksidasi kolesterol LDL (Astawan, 2010).
Beberapa manfaat tanin dalam buah delima :
penghambatan terhadap pertumbuhan sel kanker.
Berdasarkan penelitian di University of California, AS, buah delima
Universitas Pembangunan Nasional “Veteran” Jawa Timur
mencegah kanker pada organ-organ reproduksi. Satu gelas jus delima setiap hari,
kita akan mendapatkan asupan senyawa antioksidan polifenol sebanyak 100 mg.
Ekstrak buah delima merah secara in vitro (uji di luar tubuh) terbukti memiliki
aktivitas antioksidan yang kuat, sehingga dapat bersifat kemopreventif
(mencegah) atau kemoterapis (mengobati) sel kanker prostat (Malik et al, 2005
dalam Astawan, 2010). beberapa penelitian lain menunjukkan bahwa ekstrak
delima juga berkhasiat untuk mencegah kanker payudara dan kanker kolon
(Astawan, 2010).
b. Penundaan terhadap penuaan kulit dan menurunkan kolesterol.
Buah delima juga kaya akan fitosterol. Fitosterol merupakan komponen
fitokimia yang mempunyai fungsi berlawanan dengan kolesterol bila dikonsumsi
oleh manusia. Pada tahun 1970-an, fitosterol diketahui berfungsi menurunkan
kadar kolesterol di dalam darah dan mencegah penyakit jantung, sehingga sangat
bermanfaat bagi kesehatan manusia (Astawan, 2010). Selain itu buah delima juga
kaya akan antioksidan golongan flavonoid, dimana secara signifikan
mekanismnenya ialah mengurangi stres oksidasi dengan menghambat oksidasi
dari LDL lipoprotein dan macromolekul lipid peroksida dan dengan mekanisme
ini artheroghenesis dapat dikurangi (Louba, 2007).
C. Kandungan kimia dalam delima yang berfungsi sebagai antioksidan
Komponen antioksidan yang terkandung dalam buah delima ialah jenis
polifenol, yaitu terdiri dari antosianin dan tanin. Selain itu buah delima juga kaya
Universitas Pembangunan Nasional “Veteran” Jawa Timur
a. Antosianin
1.
Antosianin tergolong dalam pigmen yang disebut flavonoid yang pada
umumnya larut dalam air. Dimana warna pigmen antosianin itu sendiri ialah
berwarna merah, biru, violet dan biasanya dijumpai pada bunga, buah-buahan dan
sayur-sayuran. Dalam tanaman terdapat dalam bentuk glikosida yaitu membentuk
ester dengan monosakarida (glukosa, galaktosa, ramnosa dan kadang-kadang
pentosa). Sewaktu pemanasan dalam asam mineral pekat, antosianin pecah
menjadi antosianidin dan gula. Pada pH rendah (asam) pigmen ini berwarna
merah dan pada pH tinggi akan berubah menjadi violet dan kemudian menjadi
biru .Pigmen antosianin meningkat dengan meningkatnya pH (Laleh dkk, 2006).
Menurut Rosso (2006), kandungan vitamin C yang tinggi akan menurunkan
stabilitas antosianin. Konsentrasi pigmen juga berperan dalam menentukan warna.
Pada konsentrasi yang encer antosianin berwarna biru, sebalinya pada konsentrasi
pekat antosianin akan berwarna merah, dan pada konsentrasi biasa akan berwarna
ungu. Dimana dengan adanya tanin akan banyak mengubah warna antosianin.
Dengan ion logam, antosianin membentuk senyawa komplek berwarna abu-abu
violet. Karena itu pada proses pengalengan bahan yang mengandung antosianin,
kalengnya perlu mendapat lapisan khusus (Winarno, 2002). Jenis antosianin yang
terkandung dalam buah delima adalah sebagai berikut :
Delphinidin
Delphinidin termasuk kedalam kelompok antosianin, delphinidin ialah
pigmen utama dalam tanaman dan juga bersifat sebagai antioksidan. Delphidin
Universitas Pembangunan Nasional “Veteran” Jawa Timur
selain itu delpnidin juga memberikan warna pada buah delima. Delphinidin, sama
seperti jenis antosianin lainnya yaitu sangat sensitive akan perubahan pH
(Anonima, 2010). Delpnidin pada buah delima ialah delphinidin 3-glukosida
delphinidin yang umumnya terdapat pada buah blueberis dengan rumus kimia
C21H21O12Cl dan berat molekul 500,8 g/mol (Anonimb, 2010).
2.
Gambar 1. Gambar struktur delpinidin secara umum.
Cyanidin
Cyanidin adalah pigmen antosianin yang larut dalam air, dimana warna dari
cyanidin ini terhantung dari pH larutan. Pada pH sekitar 3 cyanidin akan berwarna
merah, pada pH kisaran 11 cyandin akan berwarna biru sedangkan pada pH netral
cyadin akan berwarna ungu. Cyanidin umumnya ditemukan pada tanaman dalam
bentuk molekul gula dalam bentuk cyandin 3-0-β-glukosida (Anonimc, 2010).
Cyanidin dalam buah delima terdiri atas 2 jenis cyanidin, yaitu 3-glukosida
cyanidin yang biasa ditemukan dalam buah blueberies, dimana memiliki struktur
kimia C21H21O11Cl dengan berat molekul 484.8 g/mol (Anonimd, 2010).
Sedangkan unutk 3,5-cyanidin diglukosida biasa ditemukan dalam buah anggur
merah, 3,5-cyanidin diglukosida ini memiliki struktur kimiaC27H31O16Cl dengan
Universitas Pembangunan Nasional “Veteran” Jawa Timur
3.
Gambar 2. Gambar struktur cyanidin secara umum
Pelargonidin
Pelargonidin umumnya dihasilkan dari hasil hidrolisa buah strawberry atau
jenis buah dan bunga lainnya, yang menghasilkan derivat pelargonidin.
Pelargonodin bersifat higroskopis. Pelargonidin mempunyai struktur kimia
C15H11O5Cl dan memiliki berat molekul sebesar 306, 7 g / mol. Pelargonidin ini
memiliki kelarutan yang tinggi dalam air dan mudah mengalami pemecahan
dengan hidrolisis pada temperatur > 40oC (Anonimf, 2010)
Gambar 3. Gambar struktur pelargonidin secara umum.
b. Tanin
Tanin disebut juga sebagai asam tanat atau asam galotanat. Tanin dapat
tidak berwarna sampai berwarna kuning atau coklat. Istilah tanin yang digunakan
pada kalangan ahli pangan ada dua yaitu condensed tannin yang merupakan dimer
Universitas Pembangunan Nasional “Veteran” Jawa Timur
yang disebut hydrolized tannin, termasuk didalmnya galotanin dan elogitanin.
Senyawa-senyawa tersebut biasanya digunakan untuk menyamak kulit dan
masing-masing merupakan polimer asam galat dan asam elagat (ellagic acid).
Disamping itu ada tanin yang tidak dapat dimasukan kedalam salah satu dari
kelompok tanin diatas (Winarno, 2002).
Menurut Najib (2009), sifat-sifat tanin ialah sebagai berikut:
1. Dalam air membentuk larutan koloidal yang bereaksi asam dan sepat .
2. Mengendapkan larutan gelatin dan larutan alkaloid.
3. Tidak dapat mengkristal.
4. Larutan alkali mampu mengoksidasi oksigen.
5. Mengendapkan protein dari larutannya dan bersenyawa dengan protein
tersebut sehingga tidak dipengaruhi oleh enzim protiolitik.
Adanya tanin dalam bahan makanan dapat ikut menentukan cita rasa bahan
makanan tersebut. Rasa sepat pada bahan makanan biasanya disebabkan oleh
tanin (Winarno, 2002). Rasa sepat tanin yang terdapat di dalam berbagai bagian
tanaman disebabkan karena tanin dapat mengendapkan protein, sehingga kalau
tanin kontak dengan lidah maka reaksi pengendapan protein ditandai dengan rasa
sepat atau astringen (Wiryowidagdo,2008).
1.
Kelompok tanin yang terkandung dalam buah delima ialah sebagai berikut :
Asam galat
Asam galat merupakan asam organik dan dikenal juga sebagai
3,4,5-trihydroxybenzoic asam, banyak ditemukan pada daun teh, kulit pohon oak, dan
Universitas Pembangunan Nasional “Veteran” Jawa Timur
baik dalam bentuk bebas dan sebagai bagian dari tanin. Garam dan ester dari asam
galat disebut gallat. Asam galat merupakan agensia antioksidan yang membantu
dalam melindungi sel-sel kita terhadap kerusakan oksidatif. (Anonimg
2.
, 2010).
Asam elagat
Asam elagat biasanya ditemukan dalam bentuk elagitanin dalam
buah-buahan seperti rasberry, strawberry, delima dan pada tanaman lainnya, dimana
asam elagat tersebut ditemukan dalam bentuk molekul gula. Asam elagat
merupakan dimer turunan dari asam galat, terjadi pada buah-buahan dan
kacang-kacangan baik dalam bentuk bebas, sebagai EA-glikosida, atau terikat sebagai
3.
ellagitannins (Seram dkk. 2004).
Asam galagat
Asam galagat merupakan kelompok polifenol yang termasuk dalam
senyawa tanin yang biasanya ditemukan pada buah delima. Asam galagat ini
mempunyai rumus molekul C28H14O18 dengan berat moekul 638.39 g/mol. Asam
galagat mempunyai sifat yang hampir sama dengan asam elagat (Anonimh
4.
, 2010)
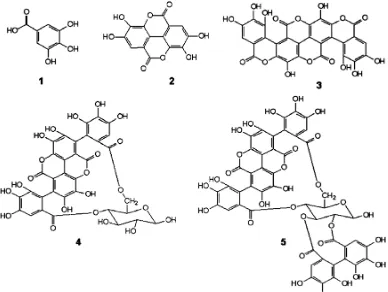
Punicalin dan Punicalagin
Punicalin dan Punicalagin adalah senyawa tanin yang mempunyai kelarutan
dan bioavabilitas yang tinggi. Punicalin dan punicalagin merupakan komponen
tanin larut air yang terikat dalam senyawa ellagitanin. Punicalagin termasuk
kelompok senyawa polifenol besar yang merupakan isomer dari
2,3-(S)-hexahydroxydiphenoyl-4, 6-(S,S)-gallagyl-D-glukosa, hydrolysable tanin dengan
berat molekul 1084. Punicalagin ditemukan dalam bentuk alfa dan beta dalam
Universitas Pembangunan Nasional “Veteran” Jawa Timur
Gambar 4. Gambar struktur senyawa tanin pada delima antara lain asam galat (1), Asam elagat (2), asam galagic (3), punicalin (4) dan punicalagin (5).
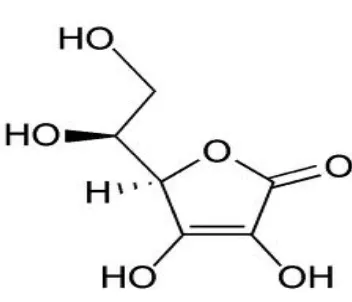
c. Vitamin C
Vitamin C adalah vitamin yang tergolong larut dalam air, dimana vitamin C
ini dapat berbentuk asam L-askorbat dan asam L-dehidroaskorbat, keduanya
mempunya keaktifan sebagai vitamin C. Asam askorbat sangat mudah teroksidasi
secara reversible manjadi asam L-dehidroaskorbat. Asam L-dehidroaskorbat
secara kimia sangat labil dan dapat mengalami perubahan lebih lanjut menjadi
asam L-diketogulonat yang tidak memiliki keaktifan sebagai vitamin C
lagi.vitamin C dapat terserap secara cepat dari alat pencernaan kita masuk
kedalam saluran darah dan dibagikan keseluruh jaringan tubuh. Kelebihan vitamin
C akan dibuang melalui air kemih. Karena itu bilaseseorang mengkonsumsi
Universitas Pembangunan Nasional “Veteran” Jawa Timur
terutama bila seseorang tersebut biasa mengkonsumsi makanan yang bergizi
tinggi. Tetapi sebaliknya, bila sebelumnya orang tersebut jelek keadaa gizinya,
maka sebagian besar dari jumlah itu dapat ditahan oleh jaringan tubuh (Winarno,
2002).
Gambar 5. Gambar struktur vitamin C
D. Antioksidan
Antioksidan sebenarnya didefinisikan sebagai inhibitor yang bekerja
menghambat oksidasi dengan cara bereaksi dengan radikal bebas reaktif
membentuk radikal bebas tak reaktif yang relatif stabil. Tetapi mengenai radikal
bebas yang berkaitan dengan penyakit, akan lebih sesuai jika antioksidan
didefinisikan sebagai senyawa-senyawa yang melindungi sel dari efek berbahaya
radikal bebas oksigen reaktif (Fery, 2007).
a. Penggolongan dan sumber antioksidan
Berdasarkan jenisnya sebagai sistem pertahanan dalam tubuh antioksidan
digolongkan menjadi 3 jenis yaitu antioksidan primer / enzimatis, antioksidan
Universitas Pembangunan Nasional “Veteran” Jawa Timur
1. Antioksidan primer (antioksidan enzimatis)
Antioksidan primer yaitu antioksidan yang diproduksi oleh tubuh sendiri
dimana antioksidan primer merupakan antioksidan yang dapat menghalangi
pembentukan radikal bebas baru. Senyawa antioksidan dapat memberikan atom
hidrogen secara cepat ke radikal lipida (R*, ROO*) atau mengubahnya ke bentuk
lebih stabil, sementara turunan radikal antioksidan (A*) tersebut memiliki
keadaan lebih stabil dibanding radikal lipida. Secara alami tubuh mampu
menghasilkan antioksidan sendiri, tetapi kemampuan ini pun ada batasnya.
Sejalan bertambahnya usia, kemampuan tubuh untuk memproduksi antioksidan
alami pun akan semakin berkurang. Hal ini lah yang menyebabkan stres oksidatif,
yaitu suatu keadaan dimana jumlah radikal bebas melebihi kapasitas kemampuan
netralisasi antioksidan. Yang termasuk Antioksidan primer ini adalah Super Oxide
Dismutase (SOD), Gluthation Peroxidase (GSH.Prx) dan Katalase (Sadhonohadi,
2010).
2. Antioksidan sekunder
Antioksidan sekunder ialah antioksidan yang tidak dihasilkan oleh tubuh
tetapi berasal dari makanan, merupakan antioksidan yang dapat menekan
terjadinya reaksi rantai baik pada awal pembentukan rantai maupun pada fase
propagasi. Antioksidan sekunder memperlambat laju autooksidasi dengan
berbagai mekanisme diluar mekanisme pemutusan rantai autooksidasi dengan
pengubahan radikal lipida ke bentuk lebih stabil Anti oksidan ini disebut juga
Universitas Pembangunan Nasional “Veteran” Jawa Timur
seperti Vitamin E, vitamin A, beta karoten, Vitamin C, Selenium, Flavonoid,
fenol dll (Sadhonohadi, 2010).
3. Antioksidan tersier
Antioksidan tersier yaitu antioksidan yang memperbaiki
kerusakan-kerusakan yang terjadi karena efek radikal bebas. Contohnya enzim DNA-repair
dan metionin sulfoksida reduktase yang berperan dalam perbaikan biomolekul
yang disebabkan oleh radikal bebas (Winarsi, 2005; Pribadi, 2009).
E. Radikal Bebas
a. Pengertian radikal bebas
Radikal bebas adalah setiap senyawa kimia yang mempunyai satu atau lebih
elektron yang tidak berpasangan dalam srtukturnya, sehingga bersifat tidak stabil
dan sangat reaktif. Untuk mencapai kestabilan atom atau molekul, radikal bebas
akan bereaksi dengan molekul disekitarnya untuk memperoleh pasangan elektron.
Reaksi ini akan berlangsung terus-menerus dalam tubuh dan bila tidak dihentikan
akan menimbulkan berbagai penyakit seperti kanker, jantung, katarak, penuaan
dini, serta penyakit degeneratif lainnya (Kikuzaki, dkk..2002; Sibuea, 2003;
Halliwell, 2000; Andayani,2008). Radikal bebas berada di dalam tubuh akibat
proses respirasi aerobik dengan bentuk yang berbeda-beda seperti superoksid,
hidroksil, hidroperoksil, peroksil, dan alkosil radikal (Teow dkk.. 2006; Pribadi,
2009).
b. Efek radikal bebas
Radikal bebas bersifat destruktif, sangat reaktif dan mampu bereaksi dengan
Universitas Pembangunan Nasional “Veteran” Jawa Timur
Pratimasari, 2009). Reaksi antara radikal bebas dan molekul itu berujung pada
timbulnya suatu penyakit, yaitu antara lain:
1. Kerusakan DNA pada inti sel
Senyawa radikal bebas merupakan salah satu faktor penyebab kerusakan
DNA dengan mengoksidasi DNA. Sel yang mengandung DNA rusak (damaged
DNA) tersebut bila membelah sebelum DNA tersebut diperbaiki, akan
mengakibatkan perubahan genetik secara permanen, hal tersebut merupakan
langkah pertama dalam karsinogenesis. Oksidasi DNA oleh senyawa radikal
bebas dapat menginisiasi terjadinya kanker (Reynertson, 2007; Pratimasari, 2009).
2. Kerusakan protein
Perubahan LDL (low density lipoprotein) menjadi bentuk LDL teroksidasi
yang diperantarai oleh radikal bebas dapat menyebabkan kerusakan dinding arteri
dan kerusakan bagian arteri lainnya. Meningkatnya kadar LDL oleh oksigen
reaktif dapat merusak dinding arteri yang menyebabkan aterosklerosis (Langseth,
1995; Pratimasari, 2009).
3. Kerusakan lipid peroksida
Radikal bebas dapat menyebabkan kerusakan oksidatif pada ikatan lemak
tak jenuh dalam fosfolipid membran biologi (lipid peroksidasi) (Josephy, 1997;
Pratimasari, 2009). Peroksidasi lipid pada membran merusak struktur membran
dan menyebabkan hilangnya fungsi dari organel sel (Kappus, 1985 cit Madhavi
Universitas Pembangunan Nasional “Veteran” Jawa Timur
F. Mekanisme radikal bebas
a. Mekanisme antioksidan dalam menangkap radikal bebas
Radikal bebas terjadi melalui proses autooksidasi lipid, dimana proses
autooksidasi lipid terjadi melalui tiga tahap reaksi yaitu reaksi inisiasi, propagasi,
dan terminasi. Inisiasi dimulai dengan terlepasnya atom hidrogen dari molekul
asam lemak sehingga terbentuk radikal bebas alkil. Inisiasi dikatalis oleh adanya
cahaya, panas dan ion logam. Pada tahap propagasi, radikal bebas alkil yang
terbentuk pada tahap inisiasi bereraksi dengan oksigen atmosfer membentuk
radikal bebas peroksi yang tidak stabil. Radikal bebas peroksi yang terbentuk
bereaksi dengan atom hidrogen yang terlepas dari asam lemak tidak jenuh yang
lain membentuk hidroperioksida (ROOH) dan radikal bebas yang baru. Radikal
bebas alkil yang baru akan bereaksi dengan oksigen atmosfer membentuk radikal
bebas peroksi. Pada tahap terminasi terjadi penggabungan radikal-radikal beba
baru membentuk produk non radikal yang stabil ( Pokorny dkk.. 2001)
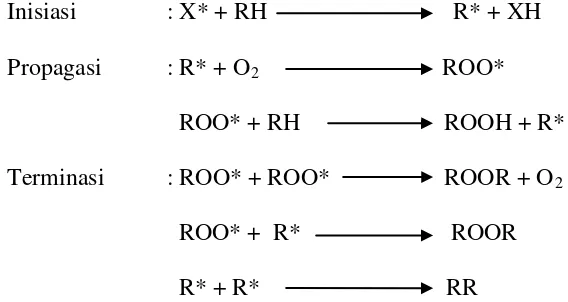
Menurut pokorny, 2001, mekanisme oksidasi lipid ialah sebagai berikut :
Inisiasi : X* + RH R* + XH
Propagasi : R* + O2
ROO* + RH ROOH + R*
ROO*
Terminasi : ROO* + ROO* ROOR + O
ROO* + R* ROOR
2
R* + R* RR
Universitas Pembangunan Nasional “Veteran” Jawa Timur
Reaksi antara antioksidan primer dengan lipid dari radikal peroksi dirubah
menjadi produk konversinya yang lebih stabil dan non radikal. Antioksidan
primer mendonasikan atom hidrogen ke lemak radikal dan menghasilkan turunan
lemak dan radikal antioksidan (A*) yang lebih stabil dan mempunyai kemampuan
lebih rendah pada proses autoksidasi. Antioksidan mempunyai afinitas lebih tinggi
untuk mendonorkan hidrogen terhadap radikal peroksi dibanding lemak. Radikal
bebas dan radikal peroksi yang terbentuk selama tahap propagasi pada proses
autooksidasi ditangkap oleh antioksidan primer. Antioksidan kemungkinan juga
bereaksi langsung dengan radikal lemak (Pokorny dkk.. 2001).
Mekanisme antioksidan dalam menangkap radikal bebas menurut Shahidi
dan Wanasundara (2002) dalam Novitasari (2009) ialah sebagai berikut :
ROO* + AH ROOH + A*
RO* + AH ROH + A*
R + AH RH + A*
Gambar 7. Mekanisme antioksidan dalam menangkap radikal bebas (Shahidi dan Wanasundara, 2002; Novitasari, 2009)
Hasil radikal antioksidan oleh donasi hidrogen mempunyai reaksi sangat
rendah terhadap lemak, dimana reaksi yang rendah akan mengurangi laju tahap
propagasi. Radikal antioksidan yang stabil disebabkan oleh pelokasian kembali
elektron yang tidak bisa diperbaiki pada sekitar cincin fenol yang stabil. Radikal
antioksidan mempunyai kemampuan dalam reaksi terminasi dengan peroksi dan
radikal antioksidan lainnya (Pokorny dkk.. 2001).
Antioksidan bekerja dalam 2 langkah, pertama antioksidan primer bekerja
Universitas Pembangunan Nasional “Veteran” Jawa Timur
terbentuklah radikal bebas yang stabil. Antioksidan primer ini juga menghambat
reaksi inisiasi dengan cara bereaksi dengan lipid radikal bebas atau menghambat
reaksi propagasi dengan cara bereaksi dengan peroksi atau radikal alkoxsi. Berikut
ialah mekanisme reaksi yang terjadi :
Pada reaksi inisiasi : AH + L* A* + LH
AH + LOO* A* + LOOH
AH + LO* A* + LOH
Pada reaksi propagasi : A* + LOO* LOOA
A* + LO* LOA
Gambar 8. Mekanisme antioksidan dalam mendonorkan atom H pada tahap
inisiasi dan propagasi (Madhevi et al. 2006)
b. Mekanisme DPPH (1,1-diphenyl-2-picrylhydrazil) dalam menangkap
radikal bebas
Kedua ialah dengan sistem sinergisme antioksidan, dimana dalam sistem ini
antioksidan dikelompokan menjadi pengikat oksigen dan sebagai chelator.
Antioksidan primer dapat digunakan pada level yang rendah jika digabungkan
dengan penambahan zat yang bersifat stimulus dari produk makanan tersebut.
Sinergisme ini biasanya terjadi pada medium yang asam yang dapat memperbaiki
stabilitas dari antioksidan primer dan sebagai pengikat oksigen, dimana asam
askorbat akan bereaksi dengan oksigen bebas yang ada di udara dan reaksi
tersebut akan menghasilkan suatu sistem yang tertutup. (Madhevi dkk.. 2006).
Radikal DPPH (1,1-diphenyl-2-picrylhydrazil)adalah suatu senyawa organik
yang mengandung nitrogen tidak stabil dengan absorbansi kuat pada λmax 517
Universitas Pembangunan Nasional “Veteran” Jawa Timur
DPPH tersebut akan tereduksi dan warnanya akan berubah menjadi kuning.
Dimana warna kuning yang terbentuk terjadi apabila larutan DPPH dicampur
dengan suatu zat yang dapat menyumbangkan atom hidrogen, maka reaksi inilah
yang menimbulkan bentuk pengurangan dengan kehilangan warna ungu
(Molyneux, 2004).
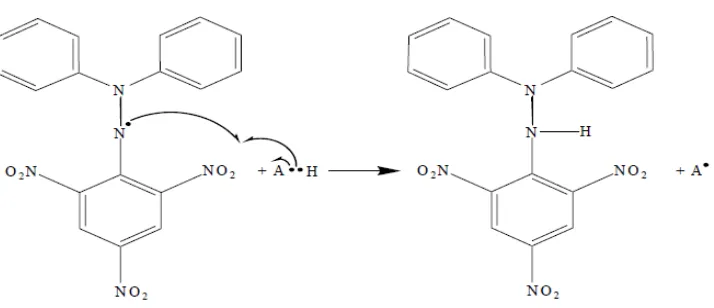
Mekanisme yang terbentuk antara reaksi radikal DPPH dengan antioksidan
ialah sebagai berikut :
Perubahan tersebut dapat diukur dengan spektrofotometer, dan
diplotkan terhadap konsentrasi (Reynertson, 2007; Pribadi, 2009). Penurunan
intensitas warna yang terjadi disebabkan oleh berkurangnya ikatan rangkap
terkonjugasi pada DPPH. Hal ini dapat terjadi apabila adanya penangkapan satu
elektron oleh zat antioksidan, menyebabkan tidak adanya kesempatan elektron
tersebut untuk beresonansi (Gambar 9.) (Pratimasari, 2009).
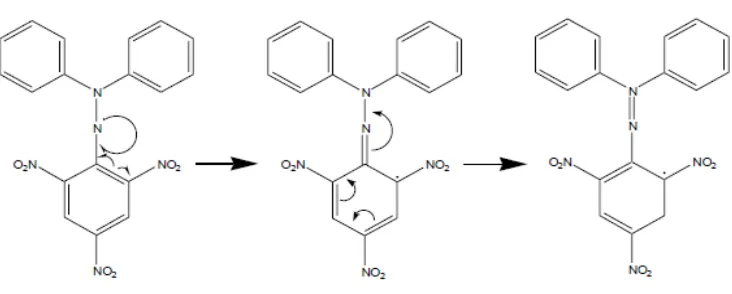
Gambar 9. Mekanisme reaksi radikal DPPH dengan antioksidan (Windono dkk..
Universitas Pembangunan Nasional “Veteran” Jawa Timur
Gambar 10. Resonansi pada struktur DPPH (Windono dkk.. 2001; Pratimasari,
2009)
G.
Sari buah adalah cairan yang dihasilkan dari pemerasan atau penghancuran
buah segar yang telah masak (Esti dan Sediadi, 2000). Sedangkan menurut Satuhu
(1996) dalam Sudarmantosastro (2008) , sari buah merupakan larutan inti daging
buah yang diencerkan, sehingga memiliki cita rasa yang sama dengan buah
aslinya.
Sari Buah
Menurut Esti dan Sediadi (2000), pada prinsipnya dikenal 2 (dua) macam
sari buah, yaitu :
1. Sari buah encer (dapat langsung diminum), yaitu cairan buah yang
diperolehdari pengepresan daging buah, biasanya dilanjutkan dengan penambahan
air dan gula pasir.
2. Sari buah pekat / sirup yaitu cairan yang dihasilkan dari pengepresan daging
buah dan dilanjutkan dengan proses pemekatan, baik dengan cara pendidihan
Universitas Pembangunan Nasional “Veteran” Jawa Timur
lain. Sirup ini tidak dapat langsung diminum, tetapi harus diencerkan dulu dengan
air (1 bagian sirup dengan 5 bagian air).
Proses pengolahan produk sari buah umumnya masih dilakukan secara
sederhana. Sari buah yang dihasilkan masih bersifat keruh dan mengandung
endapan, akibat tingginya kadar pektin buah. Sehingga berdasarkan tingkat
kekeruhannya, maka dikenal ada dua jenis sari buah, yaitu sari buah jernih dan
sari buah keruh (Astawan, 1991; Sudarmantosastro, 2008).
Sari buah biasanya memiliki pH rendah karena kaya akan asam organik,
total kandungan asam organik dalam sari buah biasanya berkisar antara 0,2 %
dalam sari buah pir sampai dengan 8,5 % dalam jeruk limau sedangkan nilai pH
sebagian besar sari buah berkisar antara 3,0 dan 4,0 (Tressler dan Joslyn, 1961;
Sudarmantosastro, 2008)
Mekanisme pembuatan sari buah menurut Sudarmantosastro (2008), ialah
sebagai berikut :
1. Pemilihan dan penentuan kemasakan buah
Umumnya industri pengolah sari buah dan juga industri pengalengan buah,
yang dipertimbangkan dalam pemilihan buah adalah bentuk buah, ukuran, warna,
banyak sedikitnya noda yang merupakan kerusakan. Berbagai jenis buah
mempunyai kandungan air cukup banyak atau rata-rata kandungan airnya 60 %.
Untuk mendapatkan sari buah yang baik sebaiknya dipilih buah yang masak. Buah
yang kurang masak, lewat masak atau busuk akan menghasilkan sari buah yang
kualitasnya rendah. Setiap pabrik mempunyai cara dan standar tersendiri serta ahli
Universitas Pembangunan Nasional “Veteran” Jawa Timur
buah yang diolah. Sehingga hal ini merupakan faktor penentu aspek kualitas dari
produk sari buah yang akan dibuat.
2. Sortasi dan pengupasan
Sortasi dilakukan sebagai pemilihan ulang agar didapat hasil yang seragam.
Serta dilakukan pengupasan dengan tujuan untuk bagian-bagian yang tidak
dikehendaki maupun bagian yang tidak bisa dimanfaatkan.
3. Pemotongan dan pencucian
Pemotongan dilakukan dengan tujuan untuk memperoleh
potongan-potongan buah, sehingga pada saat diekstrak, cairan yang ada didalam buah dapat
secara optimum terekstrak. Pencucian dimaksudkan untuk menghilangkan
kotoran-kotoran atau noda debu yang tidak dikehendaki.
4. Ekstraksi
Ekstraksi adalah salah satu cara pemisahan komponen-komponen dari suatu
sistem campuran, baik yang berupa campuran padatan-padatan, padatan-cairan
maupun cairan-cairan. Produk utama yang dikehendaki dari ekstraksi adalah
ekstraknya sedangkan ampas atau residunya merupakan hasil samping.
Ekstraksi dengan cara mekanis prinsipnya adalah pemberian tekanan pada
sejumlah bahan tertentu sehingga komponen terdorong terpisah dan keluar dari
sistem campuran. Ekstraksi ini dipengaruhi oleh sifat mengalir atau fluiditas
bahan yang diproses, tekanan yang digunakan, dan waktu yang diberikan.
Pada proses ekstraksi, Frekuensi ekstraksi yang diberikan juga sangat
mempengaruhi volume ekstrak yang dihasilkan. Semakin besar frekuensi
Universitas Pembangunan Nasional “Veteran” Jawa Timur
jumlah senyawa yang terkstrak di dalamnya juga akan semakin meningkat.
Ekstraksi mekanis sangat memperhatikan jumlah ekstrak yang dapat dihasilkan
dengan mengetahui rendemen pengempaan tersebut, yaitu perbandingan antara
jumlah ekstrak (sari buah) yang dapat dihasilkan dengan jumlah bahan awal yang
diekstrak. Selain rendemen, diperhatikan juga recovery
5. Pemisahan / penyaringan
-nya yaitu jumlah ekstrak
yang dikeluarkan dibandingkan dengan jumlah kandungan air (cairan) dalam
bahan.
Sari buah yang diperoleh biasanya masih mengandung partikel padat.
Sehingga perlu dihilangkan agar mendapatkan sari buah yang jernih.
Penghilangan dapat dilakukan dengan penyaringan. Pemisahan dengan didiamkan
beberapa waktu akan terjadi pengendapan padat karena adanya gaya gravitasi
partikel padat, kemudian dapat diambil bagian jernihnya. Selain itu untuk
mempercepat proses pemisahan juga dapat dilakukan dengan penambahan bahan
penjernih pada minuman sari buah tersebut. Penyaringan dapat dilakukan dengan
menggunakan kain atau kertas saring.
6. Pencampuran
Sari buah yang didapat tidak hanya dari satu kali pengepresan, namun dari
berbagai pengepresan, dimana hasil dari masing-masing pengepresan tidak sama.
Maka agar mendapatkan hasil sari buah yang seragam maka harus dicampur.
Keseragaman komposisi dan bau sangat diharapkan agar mendapat standart
kualitas yang tetap.
Universitas Pembangunan Nasional “Veteran” Jawa Timur
Pembotolan sari buah apel dilakukan dengan botol gelas sebagai wadah.
Karena botol gelas mempunyao sifat inert (tidak bereaksi dengan bahan, tahan
asam, tidak korosif, dan bersifat transparan). Sebelumnya botol-botol yang
digunakan sudah disterilisasi terlebih dahulu sehingga botol-botol yang digunakan
dapat mempertahankan mutu dari produk sari buah tersebut.
8. Pasteurisasi
Pasteurisasi adalah proses yang bertujuan untuk mengurangi jumlah
mikroorganisme dalam produk dengan pemanasan. Pasteurisasi hanya cocok
dilakukan untuk produk makanan dengan pH di bawah 4,2. Pasteurisasi dilakukan
pada suhu 71,1-750C selama 15-16 detik (High Temperature Short Time) atau
pada suhu 610
9. Pendinginan
C selama 30 menit (Low Temperature Long Time).
Tahap ini dilakukan untuk mengkondisikan agar sari buah lebih awet. Untuk
mempertahankan kualitas dari sari buah yang dibuat maka sari buah tersebut dapat
disimpan pada suhu refrigerator antara 4-10°C. Karena pada suhu tersebut
Universitas Pembangunan Nasional “Veteran” Jawa Timur
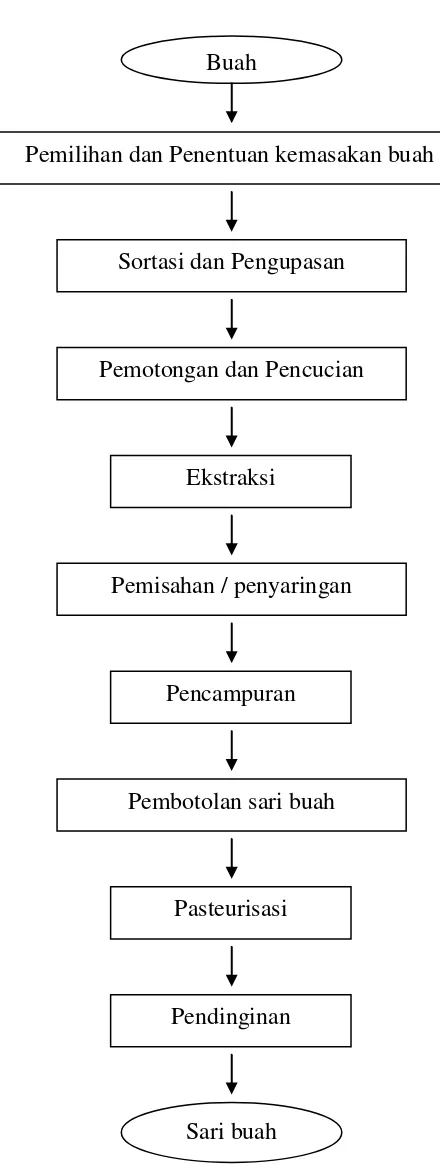
Gambar 11. Diagram alir pembuatan sari buah pada umumnya (Sudarmantosastro, 2008)
Buah
Pemilihan dan Penentuan kemasakan buah
Sortasi dan Pengupasan
Pemotongan dan Pencucian
Ekstraksi
Pemisahan / penyaringan
Pencampuran
Pembotolan sari buah
Pasteurisasi
Pendinginan
Universitas Pembangunan Nasional “Veteran” Jawa Timur
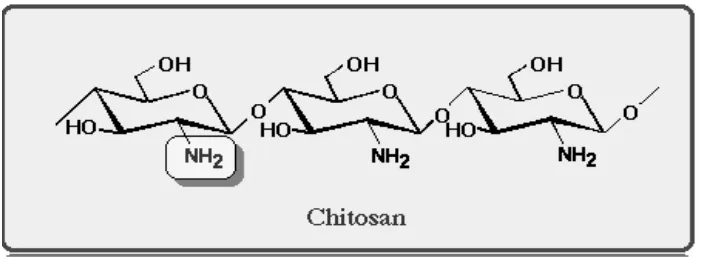
H. Kitosan
Kitosan merupakan limbah atau produk samping dari pengolahan udang dan
rajungan. Secara alami bahan ini dapat ditemukan pada dinding sel ragi, jamur
dan kulit Crustacea (udang-udangan) seperti kepiting, udang dan lobster. Selain
itu juga terdapat pada kerangka luar (Eksoskeleton) zooplankton, coral dan
ubur-ubur (Saparinto dan Diana, 2006).
Kitosan adalah nama yang digunakan untuk bentuk asetil terkecil dari kitin
yang utamanya terkomposisi atas glukosamin, 2-amino-2-deaksi-D-glukosa.
Kitosan memiliki tiga gugus reaktif, yaitu sebuah gugus amina serta dua buah
gugus hidroksil primer dan sekunder yang masing-masing terletak pada atom C-2,
C-3 dan C-6 (Pamungkas, 2008). Menurut Hardjito (2006), karakteristik
fisika-kimia kitosan berwarna putih dan berbentuk kristal, dapat larut dalam larutan
asam organik, tetapi tidak larut dalam pelarut organik lainnya. Kitosan sedikit
mudah larut dalam air dan mempunyai muatan positif yang kuat. Sifat kelarutan
kitosan dipengaruhi oleh berat molekul, derajat deasetilasi, rotasi spesifik yang
bervariasi serta tergantung dari sumber dan metode isolasinya (Austin,1984
dalam Latar, 2007).
Universitas Pembangunan Nasional “Veteran” Jawa Timur
Kitosan berbeda dengan polisakarida lainnya seperti selulosa, alginate dan
pectin yang memiliki sifat netral atau asam. Kitosan bersifat basa karena memiliki
gugus amina dalam jumlah besar (Mak dan Sun, 2008 dalam Nasution, 2010).
Gugus ini dapat mengalami protonasi pada pH kurang dari 6,5 dan ini menjadikan
kitosan bersifat polimer kationik (Nasution, 2010).
Beberapa peneliti melaporkan bahwa kitosan berfungsi sebagai antioksidan
(Kim & Thomas, 2007 dalam Pamungkas, 2008). Yen dkk (2008) dalam
Pamungkas 2008 melaporkan bahwa dengan menggunakan metode konjugasi
diena, kitosan yang berasal dari kepiting memperlihatkan aktivitas antioksidan
yaitu sebesar 58,3-70,2% pada konsentrasi 1 mg/ml dan 79,9-85,2% pada
konsentrasi 10 mg/ml. Kitosan dapat bertindak sebagai antioksidan primer dan
sekunder. Mekanisme antioksidan sekunder pada kitosan adalah adanya
kemampuan dalam mengkhelat logam dan mengikat lipid. Meningkatkan
konsentrasi kitosan akan meningkatkan aktivitas antioksidan.
Xie dkk (2001) menjelaskan bahwa mekanisme pengikatan radikal bebas
oleh kitosan berhubungan dengan fakta bahwa gugus radikal OH- dari proses
oksidasi lipid dapat bereaksi dengan ion hydrogen dari gugus amonium (NH3+)
pada kitosan membentuk suatu molekul yang lebih stabil. Aktivitas pengikat oleh
kitosan terhadap gugus radikal OH
-1. Gugus hidroksil di dalam unit polisakarida pada kitosan dapat bereaksi
dengan OH
dapat terjadi sebagai berikut :
–
2. Gugus OH
pada tipe reaksi pumutusan gugus atom H.
dapat bereaksi dengan gugus amina bebas (NH2) membentuk
Universitas Pembangunan Nasional “Veteran” Jawa Timur
3. Gugus NH2 dapat membentuk gugus ammonium NH3+ dengan
mengabsorbsi ion H+
Menurut Sandford dan Hutchins (1987) dalam Meriatna (2008) sifat
kationik, biologi dan sifat kimia kitosan adalah sebagai berikut :
dari larutan, kemudian bereaksi dengan OH melalui
reaksi lanjutan.
1. Sifat kationik
a. Linier polielektrolit pada pH asam.
b. Jumlah muatan positif tinggi : satu muatan atau unit gugus
glukosamin, jika banyak material yang bermuatan negatif maka
muatan positif kitosan berinteraksi kuat dengan permukaan negatif.
c. Flokulan yang baik : gugus NH3+
d. Mengikat ion-ion logam ( Fe, Cu, Cd, Hg, Pb, Cr, Ni, Zn, Pt, dan U)
berinteraksi dengan muatan negatif
dari koloid.
2. Sifat biologi
a. Dapat terdegradasi secara alami.
b. Polimer alam.
c. Non toksik
3. Sifat kimia
a. Linier oliamin (poli D_glukosamin) yang memiliki gugus amino yang
baik untuk reaksi kimia serta pembentuk garam dan asam.
b. Gugus amino yang reaktif.
Universitas Pembangunan Nasional “Veteran” Jawa Timur
Menurut Sandford (1989) dalam Danggi (2010), pada suasana asam, gugus
amina bebas (NH2) dari kitosan akan terprotonasi membentuk gugus amina
kationik (NH3
Menurut Suhartono (2006) dalam Irianto dan Soesilo (2007), dalam bidang
pangan kitosan biasanya digunakan sebagai senyawa penyerap lemak, flavour,
pengawet, pembentuk tekstur, emulsifier, dan penjernih minuman. Dosis
penggunaan kitosan yang diperbolehkan adalah 1,5 % (Saparinto dan Diana,
2006).
). Kation dalam kitosan akan bereaksi dengan polimer anion
membentuk kompleks elektrolit dan kitosan akan menggumpal.
I. Koagulasi
Koagulasi merupakan penyerapan bagian-bagian dari suatu koloid menjadi
berbagai bentuk yang lebih besar sehingga mampu untuk mengendap. Koloid
dikategorikan manjadi dua yaitu koloid hidrofobik dan hidrofilik. Koloid
hidrofobik tidak beraksi dengan air, sedangkan koloid hidrofilik bereaksi dengan
air. Ukuran partikel koloid cenderung mempengaruhi endapan partikel dalam
suatu media. Koloid sering memerlukan koagulasi untuk mencapai ukuran partikel
tertentu agar dapat terbentuk suatu endapan (Murniati, 2007)
Kitosan dapat digunakan sebagai penjernih minuman karena kitosan
memiliki sifat sebagai koagulan, dimana cangkang rajungan mengandung bahan
polikarbohidrat yang berfungsi mengendapkan kotoran-kotoran yang terkandung
Universitas Pembangunan Nasional “Veteran” Jawa Timur
Proses terjadinya koagulasi menurut Cherimisinoff (1989) dalam Murniati
(2007) adalah sebagai berikut :
1. Partikel koloid (suspensi) yang bermuatan negatif menarik partikel koagulan
(polimer) yang bermuatan positif.
2. Ion-ion positif kemudian menyelubungi partikel koloid dan membentuk
lapisan rapat muatan didekat permukaannya yang disebut lapisan kokoh /
tetap (fixed layer).
3. Lapisan kokoh dikelilingi lagi oleh sejumlah ion-ion yang berlawanan
muatan yang disebut sebagai difusi (difussed layer)
4. Didalam lapisan difusi terdapat bagian geser (shear plane) batas dimana
ion-ion yang berlawanan muatan dapat tersapu dari permukaan partikel karena
gerakan fluida.
5. Kumpulan ion-ion berlawanan akan mengelilingi partikel koloid dan
muatan-muatan permukaannya itu disebut lapisan ganda listrik.
6. Potensial listrik diantara bidang geser dan badan cairan disebut potensial
zeta. Potensial zeta ini berhubungan dengan muatan partikel dan ketebalan
lapisan ganda. Ketebalan lapisan bergantung dari konsentrasi ion, semakin
besar konsentrasi ion maka semakin kecil ketebalan lapisan ganda dan
berarti semakin rapat muatan. Penambahan kation sampai jumlah tertentu
akan merubah besar potensial zeta sehingga akan melampaui besar gaya
tolak-menolak yang ada, dengan demikian partikel koloid dapat saling
Universitas Pembangunan Nasional “Veteran” Jawa Timur
pemampatan lapisan ganda, sehingga tidak akan terbentuknya suatu endapan
lagi.
J. Landasan teori
Delima merupakan buah yang kaya akan kandungan gizi, tetapi di Indonesia
buah delima kurang mendapat perhatian secara lebih. Pada umumnya buah delima
hanya ditanam sebagai tanaman hias dan terakhir buah delima sudah tidak lagi
dibudidayakan secara umum. Di Amerika buah delima sudah dibudidayakan
secara besar-besaran dan diolah menjadi sari buah delima (Wijanarko, 2008).
Sari buah adalah cairan yang dihasilkan dari pemerasan atau penghancuran
buah segar yang telah masak (Esti dan Sediadi, 2000). Menurut Mazza (1993)
dalam Ekşi (2009). Sari buah delima memiliki kapasitas antioksidan yang tinggi
karena mengandung komponen antosianin seperti delfinidin, cyanidin dan
pelargonidin. Komponen lainnya ialah dari komponen ellagitanin seperti asam
elagat, punicalagin, dan punicalin (Lansky, 2007 dalam Ekşi dkk.. 2009).
Sari buah delima yang dihasilkan umumnya keruh, karena buah delima
mengandung senyawa katekin (Plumb dkk., 2002), beberapa jenis mineral serta
serat sebesar 0,6 gram per 100 gram delima (Astawan, 2010). Oleh karena itu
diperlukan perlakuan dengan penambahan bahan penjernih. Kitosan merupakan
bahan penjernih alamiah yang bersifat tidak beracun dan mudah luruh secara
alami (biodegradable) (Koesumo dan Digwijaya, 2008), kitosan juga bersifat
sebagai pengawet (Saparinto dan Diana, 2006), antioksidan(Kim & Thomas, 2007
dalam Pamungkas,2008) serta mampu menurunkan kadar asam (Shofyan, 2008).
Universitas Pembangunan Nasional “Veteran” Jawa Timur
bebas yang bersifat polikationik dan gugus amino bebas inilah yang memberikan
banyak kegunaan pada kitosan dan dengan adanya gugus amina inilah kitosan
dapat digunakan sebagai penjernih minuman.
Dosis penggunaan kitosan yang diperbolehkan adalah 1,5 % (Saparinto dan
Diana, 2006) tetapi berdasarkan penelitian Firdaus dkk.. (2007), Penggunaan 1 %
larutan kitosan dalam waktu pengendapan 90 menit pada proses penjernihan air
memberikan hasil yang terbaik, yaitu mengurangi 98,8 % kekeruhan dan 97,9 %
bentuk padatan terlarut. Berdasarkan penelitian Oszmianski dan Aneta (2007)
menyatakan bahwa penambahan kitosan sebesar 0,015 g/ml pada sari buah anggur
mampu mengurangi total asam sebanyak 52,6 % yang terdiri dari asam sitrat,
asam tartarat, asam malat, asam oksalat dan asam askorbat. Pada penelitian
pembuatan sari buah mete menggunakan gelatin 5% diperlukan waktu
penjernihan selama 60 menit (Mulyono dkk., 2001).
Penambahan kitosan pada sari buah menghasilkan sari buah yang jernih
sedangkan katekin, protein, serat, dan ion negative akan mengendap karena akan
bereaksi dengan kitosan
Proses pengendapan terjadi karena partikel koloid (suspensi) yang
bermuatan negatif menarik partikel koagulan (polimer) yang bermuatan positif
sehingga membentuk lapisan yang dikelilingi oleh muatan yang berlawanan
sehingga terbentuk suatu batas zona potensial yang menyebabkan terjadinya suatu
endapan (Cherimisinoff, 1989; Murniati 2007)
membentuk kompleks elektrolit dan akhirnya kitosan
Universitas Pembangunan Nasional “Veteran” Jawa Timur
Kitosan bersifat basa, maka dengan adanya kitosan akan menurunkan kadar
asam (Mak & Sun, 2008; Nasution, 2010), Peningkatan pH dan vitamin C akan
berpengaruh terhadap senyawa antioksidan (antosianin) (Miguel dkk, 2004; Rosso
dkk, 2006) selain itu akan berpengaruh pada aktivitas antioksidan (Yen,dkk. 2008
dalam pamungkas, 2008). Reaksi antara kitosan dengan mineral akan menurunkan
Total Padatan Terlarut dalam sari buah delima dan dengan terdapat bagian yang
mengendap maka akan mempengaruhi kenampakan yaitu kejerrnihan dan warna
sari buah yang dihasilkan. Permasalahan yang terjadi ialah berapa penambahan
kitosan dan lama waktu pengendapan yang dibutuhkan untuk menghasilkan sari
buah dengan aktivitas antioksidan tinggi dan disukai konsumen.
K. Hipotesa
Diduga penambahan kitosan dan lama waktu pengendapan akan berpengaruh
41
Berdasarkan hasil pengamatan yang dilakukan terhadap sampel sari buah
delima dengan perlakuan penambahan kitosan dengan lama waktu pengendapan
menunjukan bahwa terdapat perbedaan yang nyata (p≤ 0,05 ) pada parameter total
asam, tingkat intensitas warna, total fenol, aktivitas antioksidan (DPPH), uji
organoleptik rasa dan warna, sedangkan pada parameter nilai pH, kadar vitamin C,
Total Padatan Terlarut (TPT) tidak berpengaruh secara nyata (p≤ 0,05 ) antar
perlakuan, namun masing-masing perlakuan berpengaruh nyata dan untuk uji
organoleptik aroma juga menunjukan tidak berbeda nyata(p≤ 0,05).
(a) (b)
Universitas Pembangunan Nasional “Veteran” Jawa Timur
(c) (d)
Gambar 15. Gambar sari buah delima pada perlakuan lama waktu pengendapan 90 (c) dan lama waktu pengendapan 120 menit (d) pada penambahan kitosan 0%; 0,5%; 1%; 1,5% (pembacaan : kanan ke kiri).
a. Analisis pH
Berdasarkan analisis ragam pH (Lampiran 3) menunjukan bahwa perlakuan
penambahan kitosan dan lama waktu pengendapan menunjukan tidak ada interaksi
yang nyata (p≤ 0,05), tetapi masing-masing perlakuan berbeda nyata (p≤ 0,05)
terhadap nilai pH yang dihasilkan meskipun tidak mampu memberikan perbedaan
yang signifikan.
Pengaruh nilai pH yang dihasilkan dari perlakuan penambahan kitosan dapat
dilihat pada Tabel 1 dan untuk pengaruh nilai pH yang dihasilkan dari perlakuan
Universitas Pembangunan Nasional “Veteran” Jawa Timur
Tabel 1. Pengaruh nilai pH sari buah delima yang dihasilkan dari perlakuan penambahan kitosan.
Penambahan
Berdasarkan Tabel 1 menunjukan bahwa pH pada perlakuan penambahan
kitosan dan tanpa penambahan kitosan berbeda nyata (p≤0,05). Hasil penelitian
terhadap pH pada perlakuan penambahan kitosan menunjukan kenaikan pH tetapi
secara statistik tidak berbada secara signifikan. Hal ini diduga karena kitosan
mengandung gugus amina, dimana gugus amina mempunyai sifat basa. selain itu
kitosan juga bersifat larut dalam asam, oleh karena itu pH yang dihasilkan pada
perlakuan penambahan kitosan mengalami peningkatan. Hal ini sesuai dengan
pendapat Hardjito (2006), bahwa kitosan dapat larut dalam larutan asam organik.
Mak & Sun (2008) dalam Nasution (2010) juga menyatakan bahwa kitosan berbeda
dengan jenis polisakarida pada umumnya yang bersifat netral atau asam, kitosan
bersifat basa, karena mengandung gugus amina.
Tabel 2. Pengaruh nilai pH sari buah delima yang dihasilkan dari perlakuan lama waktu pengendapan.
Universitas Pembangunan Nasional “Veteran” Jawa Timur
Berdasarkan Tabel 2 menunjukan bahwa pH pada perlakuan lama waktu
pengendapan dan tanpa waktu pengendapan berbeda nyata (p≤0,05) . Hasil penelitian
terhadap pH pada perlakuan lama waktu pengendapan menunjukan kenaikan pH
meskipun secara statistik tidak berbeda secara signifikan. Hal ini diduga karena
dengan semakin lama waktu pengendapan, maka reaksi yang terjadi antara komponen
basa dari kitosan dengan komponen asam dari sari buah akan semakin lama, maka
basa yang beraksi dengan asam akan makin banyak, sehingga pH sari buah akan
meningkat. Menurut Murniati (2007), dengan semakin lama proses pengendapan
yang terjadi maka akan semakin banyak gugus amina bebas yang terprotonasi,
sehingga keasaman larutan akan berkurang.
b. Analisis vitamin C
Berdasarkan analisis ragam kadar vitamin C (Lampiran 4) menunjukan bahwa
perlakuan penambahan kitosan dan lama waktu pengendapan menujukan tidak ada
interaksi yang nyata (p≤ 0,05), tetapi masing -masing perlakuan memberikan nilai
yang berbeda terhadap kadar vitamin C sari buah delima yang dihasilkan meskipun
secara statistik (p≤ 0,05) tidak memberikan perbedaan yang signifikan.
Nilai kadar vitamin C (mg/100 gr) yang dihasilkan dari perlakuan penambahan
kitosan dapat dilihat pada Tabel 3 dan untuk Pengaruh nilai (mg/100 gr) vitamin C
yang dihasilkan dari perlakuan lama waktu pengendapan dapat dilihat pada Tabel 4.
Universitas Pembangunan Nasional “Veteran” Jawa Timur
Tabel 3. Pengaruh kadar vitamin C (mg/ 100 gr) sari buah delima yang dihasilkan dari perlakuan penambahan kitosan.
Penambahan
Berdasarkan Tabel 3 menunjukan bahwa vitamin C pada penambahan kitosan
dan tanpa penambahan kitosan berbeda nyata(p≤0,05), sedangkan kadar vitamin C
pada perlakuan penambahan kitosan menunjukan penurunan kadar vitamin C
meskipun secara statistik tidak berbeda secara signifikan. Berdasarkan statistik,
analisis vitamin C pada perlakuan penambahan kitosan tidak berbeda nyata (p≤0,05)
tetapi untuk perlakuan penambahan kitosan 0,5% dan 1% juga menunjukan
perbedaan yang tidak signifikan dengan perlakuan tanpa penambahan kitosan. Pada
penambahan kitosan 1,5% yang mampu mebrikan perbedaan kadar vitamin C yang
signifikan. Penambahan kitosan memberikan penurunan terhadap vitamin C yang
dihasilkan. Hal ini karena vitamin C merupakan salah satu komponen asam, yaitu
asam askorbat sedangkan kitosan merupakan komponen basa, sehingga dengan
penambahan kitosan maka akan terjadi reaksi antara asam dan basa. Menurut
Murniati (2007), kitosan merupakan larutan yang bersifat basa kuat karena
mengandung gugus amina yang bersifat reaktif, maka jika suatu asam ditambahkan
dengan basa, maka keasamanya akan berkurang dan akan bereaksi membentuk garam
Universitas Pembangunan Nasional “Veteran” Jawa Timur
Tabel 4. Pengaruh kadar vitamin C (mg/ 100 gr) sari buah delima yang dihasilkan dari perlakuan lama waktu pengendapan.
Lama waktu
Berdasarkan Tabel 4 menunjukan bahwa vitamin C pada perlakuan lama waktu
pengendapan dan tanpa waktu pengendapan berbeda nyata (p≤0,05). Perlakuan lama
waktu pengendapan berbeda secara signifikan dibanding dengan perlakuan tanpa
lama pengendapan, artinya ialah bahwa perlakuan lama waktu pengendapan mampu
menurunkan kadar vitamin C. Hal ini karena dengan semakin lama waktu
pengendapan, maka makin banyak gugus hydrogen pada asam askorbat yang akan
bereaksi dengan gugus amina dan hidroksil dari kitosan. Menurut Pamungkas (2008),
kitosan memiliki tiga gugus reaktif yaitu gugus amina serta dua buah gugus hidroksil
primer dan sekunder yang masing-masing terletak pada atom C-2, C-3 dan C-6.
Gugus reaktif ini akan bereaksi dengan gugus hydrogen dari molekul asam askorbat.
Semakin lama waktu pengendapan maka makin banyak komponen asam askorbat
Universitas Pembangunan Nasional “Veteran” Jawa Timur c. Analisis total asam
Berdasarkan analisis ragam total asam (Lampiran 5) menunjukan bahwa
perlakuan penambahan kitosan dan lama waktu pengendapan menunjukan ada
interaksi yang nyata (p ≤ 0,05) terhadap kadar total asam sari buah delima.
Pengaruh nilai (%) total asam yang dihasilkan dari perlakuan penambahan
kitosan dan lama waktu pengendapan dapat dilihat pada Tabel 5.
Tabel 5. Pengaruh total asam (%) sari buah delima yang dihasilkan dari kombinasi perlakuan penambahan kitosan dengan lama waktu pengendapan.
Perlakuan
Berdasarkan Tabel 3 menunjukan bahwa kandungan total asam tertinggi ialah
Universitas Pembangunan Nasional “Veteran” Jawa Timur
pengendapan (0 menit) sedangkan nilai total asam terendah ialah sebesar 0,44% pada
perlakuan penambahan kitosan sebesar 1,5 % dan lama waktu pengendapan selama
120 menit.
Gambar 16. Hubungan antara penambahan kitosan dan lama waktu pengendapan dengan total asam (%) sari buah delima yang dihasilkan.
Berdasarkan Gambar 16 menunjukkan bahwa semakin tinggi penambahan
kitosan dan makin lama waktu pengendapan maka nilai total asam yang dihasilkan
oleh sari buah delima akan menurun. Hal ini disebabkan karena kitosan bersifat basa
maka secara tidak langsung akan mereduksi kandungan asam dalam sari buah
delima. Diduga komponen asam-asam lain (asam malat, asam borat, asam sitrat,
asam galat, asam galagat, asam elagat) terdegradasi lebih banyak dibandingkan
degradasi vitamin C yang tidak berpengaruh nyata dan semakin lama waktu
pengendapan, maka makin banyak basa yang bereaksi dengan asam, sehingga total
R² = 0,993
Lama waktu Pengendapan (menit)
Universitas Pembangunan Nasional “Veteran” Jawa Timur
asam yang dihasilkan oleh sari buah menurun. Hal ini sesuai dengan pendapat
Argin-Sofyan et al. (2007) dalam Nasution (2010),bahwa pada pH asam, kitosan akan
terprotonasi dengan mengikat atom hidrogen dari asam, sehingga keasaman sample
akan berkurang dan dengan semakin lama waktu pengendapan maka makin banyak
atom hidrogen yang terikat oleh kitosan sehingga total asamnya juga akan berkurang.
d. Analisis Total Padatan Terlarut (TPT)
Berdasarkan analisis ragam (Lampiran 6) menujukan bahwa perlakuan
penambahan kitosan dan lama waktu pengendapan menunjukan tidak ada interaksi
yang nyata (p≤ 0,05), namun masing-masing perlakuan berpengaruh nyata (p≤ 0,05)
terhadap total padatan terlarut (TPT) yang dihasilkan oleh sari buah delima.
Pengaruh nilai Total Padatan Terlarut (TPT) yang dihasilkan dari perlakuan
penambahan kitosan dapat dilihat pada Tabel 6 dan untuk Pengaruh nilai Total
Padatan Terlarut (TPT) yang dihasilkan dari perlakuan lama waktu pengendapan
dapat dilihat pada Tabel 7.
Tabel 6. Pengaruh Total Padatan Terlarut (TPT) sari buah delima yang dihasilkan dari perlakuan penambahan kitosan.
Penambahan
Pada Tabel 6 menunjukan bahwa Total Padatan Terlarut (TPT) pada
Universitas Pembangunan Nasional “Veteran” Jawa Timur
dengan perlakuan penambahan kitosan 1% dan 1,5 %. Hasil penelitian terhadap Total
Padatan Terlarut (TPT) pada perlakuan penambahan kitosan menunjukan penurunan
TPT meskipun secara statistik tidak signifikan. Hal ini diduga karena pada analisis
TPT adanya komponen yang terlarut sehingga komponen tersebut tidak tampak dan
sampel dianggap homogen. Kitosan mampu mengikat partikel-partikel koloid,
mineral dan kotoran yang ada dalam sari buah yang akan membentuk gumpalan.
Menurut Danggi (2008) kitosan bereaksi dengan jenis polisakarida tertentu yang
bermuatan negative, serta bereaksi pula dengan larutan bervalensi 2 dari ion mineral.
Jika kitosan bereaksi dengan gugus bermutan negative maka akan terjadinya
penggumpalan kitosan.
Tabel 7. Pengaruh Total Padatan Terlarut (TPT) sari buah delima yang dihasilkan dari perlakuan lama waktu pengendapan.
Lama waktu
Berdasarkan Tabel 7 menunjukan bahwa Total Padatan Terlarut (TPT) pada
perlakuan lama waktu pengendapan dan tanpa waktu pengendapan berbeda nyata
(p≤0,05). Hasil penelitian terhadap Total Padatan Terlarut (TPT) menunjukan
penurunan Total Padatan Terlarut (TPT) meskipun secara statistik tidak signifikan.
pada nilai analisis TPT. Hal ini karena dengan semakin lama waktu pengendapan,
Universitas Pembangunan Nasional “Veteran” Jawa Timur
ion mineral. Hal ini sesuai dengan pendapat Danggi (2008), bahwa kitosan sebagai
molekul polikationik akan mengikat molekul lain sebagai pembawa muatan negatif
dan makin lama waktu pengendapan, maka komponen negatif dan kotoran yang
terikat akan semakin banyak.
e. Analisis intensitas warna
Berdasarkan analisis ragam intensitas warna (Lampiran 7 dan 8) diketahui
bahwa perlakuan penambahan kitosan dan lama waktu pengendapan berbeda nyata
(p≤ 0,05) terhadap analisis tingkat kejernihan dan tingkat kemerahan.
Pengaruh nilai intensitas warna (tingkat kejernihan dan tingkat kemerahan)
Universitas Pembangunan Nasional “Veteran” Jawa Timur
Tabel 8. Pengaruh perlakuan penambahan kitosan dan lama waktu pengendapan terhadap intensitas warna (tingkat kejernihan dan tingkat kemerahan).
Pada Tabel 8 menunjukan bahwa tingkat kejernihan tertinggi ialah sebesar
45,2 pada perlakuan penambahan kitosan 1,5 % dan lama waktu pengendapan 120
menit sedangkan untuk tingkat kejernihan terendah ialah sebesar 30,55 pada
perlakuan penambahan kitosan (0%) dan tanpa waktu pengendapan (0 menit). Pada
Tabel 8 juga menunjukan bahwa tingkat kemerahan tertinggi ialah sebesar 24,3 pada
perlakuan penambahan kitosan sebesar 1,5 % dan lama waktu pengendapan 90 menit
sedangkan untuk tingkat kemerahan terendah ialah sebesar 14,6 pada perlakuan tanpa
penambahan kitosan (0 %) dan tanpa waktu pengendapan (0 menit).
Perlakuan Tingkat kejernihan Tingkat Kemerahan
Universitas Pembangunan Nasional “Veteran” Jawa Timur
Gambar 17. Hubungan antara perlakuan penambahan kitosan dan lama waktu pengendapan dengan tingkat kejernihan sari buah delima yang dihasilkan.
Gambar 18. Hubungan antara perlakuan penambahan kitosan dan lama waktu pengendapan dengan tingkat kemerahan sari buah delima yang dihasilkan.
R² = 0,872
Lama waktu pengendapan (menit)
kitosan 0 %
Lama waktu pengendapan (menit)
Universitas Pembangunan Nasional “Veteran” Jawa Timur
Berdasarkan Gambar 17 dan 18 semakin tinggi penambahan kitosan dan makin
lama waktu pengendapan yang dilakukan maka sari buah yang dihasilkan akan
berwarna merah jernih. Peningkatan kejernihan dan kemerahan ini dikarenakan
kitosan merupakan salah satu agensia penjernih, dimana kitosan mampu mengikat
komponen penyebab kekeruhan yaitu kotoran, senyawa bermuatan negatif dan
senyawa yang bersifat koloidal sehingga warna merah yang dihasilkan juga semakin
meningkat karena sudah tidak terselubungi lagi, selain itu dengan semakin lama
waktu pengendapan, maka makin banyak komponen aktif kitosan yang bereaksi
sehingga kekeruhan juga akan berkurang. Menurut Latar (2007), kitosan mempunyai
sifat polikationik, kitosan akan menggumpal jika bertemu dengan molekul lain
sebagai pembawa muatan negatif selain itu senyawa koloidal juga akan terikat dan
selanjutnya mereka mengendap bersama kotoran lain.
f. Analisis total fenol
Berdasarkan analisis ragam total fenol (Lampiran 10) menunjukan bahwa
perlakuan penambahan kitosan dan lama waktu pengendapan berbeda nyata
(p≤ 0,05) terhadap total fenol sari buah delima.
Pengaruh nilai total fenol yang dihasilkan dari perlakuan penambahan kitosan
Universitas Pembangunan Nasional “Veteran” Jawa Timur
Tabel 10. Pengaruh total fenol (ppm) sari buah delima yang dihasilkan dari perlakuan penambahan kitosan dengan lama waktu pengendapan.
Perlakuan
Berdasarkan Tabel 9 diketahui bahwa total fenol tertinggi ialah sebesar
4680,331 ppm pada perlakuan penambahan kitosan 1,5% dan lama waktu
pengendapan selama 120 menit sedangkan nilai total fenol terendah ialah sebesar
3542,672 ppm pada perlakuan tanpa penambahan kitosan (0%) dan tanpa waktu
pengendapan (0 menit). Pengujian senyawa fenol ini menggunakan senyawa katekin
Universitas Pembangunan Nasional “Veteran” Jawa Timur
Gambar 19. Hubungan antara perlakuan penambahan kitosan dan lama waktu pengendapan dengan total fenol (ppm) sari buah delima yang dihasilkan.
Berdasarkan Gambar 19 menujukan bahwa semakin tinggi penambahan
kitosan dan makin lama waktu pengendapan maka total senyawa fenol yang
terkandung dalam sari buah meningkat, hal ini karena kitosan mengikat
senyawa-senyawa koloidal, tanin, kotoran serta ion bermuatan negarif. Peningkatan total fenol
pada perlakuan lama waktu pengendapan karena semakin lama waktu pengendapan
maka akan semakin banyak pula senyawa kolidal, tanin dan kotoran yang terikat
sehingga endapan yang dihasilkan juga semakin banyak, dimana hal ini menyebabkan
Total Padatan Terlarut dari sari buah menurun. Adanya senyawa lain yang terikat,
menyebabkan sample menjadi lebih pekat, karena adanya bagian yang mengendap,
jadi didapatkan proporsi total fenol yang lebih tinggi, karena massa cairan berkurang.
Kitosan bereaksi dengan senyawa polifenol menyebabkan turunnya total fenol sari
R² = 0,955
Lama waktu Pengendapan (menit)
Universitas Pembangunan Nasional “Veteran” Jawa Timur
buah yang dihasilkan, tetapi kitosan juga mampu melindungi senyawa polifenol
karena kandungan total fenol dalam sari buah delima menurun kurang dari 20 %.
Menurut Oszmianski dan Aneta (2007), Proses penjernihan akan menurunkan
kandungan fenol pada sari buah yang akan menyebabkan nilai gizinya berkurang.
Penggunaan kitosan sebagai penjernih mampu untuk meminimalkan kehilangan
komponen fenol kurang dari 20 %. Pada proses penjernihan juice apel didapatkan
data bahwa komponen polifenol epikatekin pada control sebesar 16,57± 0,94 b dan
setelah dijernihkan dengan kitosan epikatekin yang dihasilkan sebesar 16,26± 0,48 c.
Kitosan juga dilaporkan mampu untuk melindungi senyawa aktif polifenol.
g. Analisis aktivitas antioksidan (DPPH)
Berdasarkan analisis ragam aktivitas antioksidan (DPPH) (Lampiran 9)
menunjukan bahwa perlakuan penambahan kitosan dan lama waktu pengendapan
berpengaruh nyata (p≤ 0,05) terhadap kemampuan menangkap radikal bebas (DPPH)
yang diukur sebagai prosentaseaktivitas antioksidan sari buah delima.
Pengaruh nilai aktivitas antioksidan dari perlakuan penambahan kitosan
Universitas Pembangunan Nasional “Veteran” Jawa Timur
Tabel 10. Pengaruh aktivitas antioksidan (DPPH) sari buah delima yang dihasilkan dari perlakuan penambahan kitosan dan lama waktu pengendapan.
Perlakuan
Berdasarkan Tabel 10 menunjukan bahwa kemampuan menangkap radikal
bebas (DPPH) tertinggi ialah sebesar 74, 625 % pada perlakuan penambahan kitosan
1,5 % dan lama waktu pengendapan 120 menit sedangkan aktivitas antioksidan
(DPPH) terendah ialah sebesar 30,475 % pada perlakuan penambahan kitosan 0 %
dan lama waktu pengendapan 0 menit. Nilai aktivitas antioksidan (DPPH) yang
dihasilkan oleh sari buah delima memang relatif lebih kecil jika dibandingkan dengan
BHT, dimana BHT 0,1 % aktivitas antioksidannya mencapai 89,56% (Lampiran 10).
Berdasarkan hasil penelitian perlakuan lama waktu pengendapan tanpa
Universitas Pembangunan Nasional “Veteran” Jawa Timur
peningkatan. Berdasarkan teori, seharusnya antioksidan yang dihasilkan ialah
mengalami penurunan karena terjadinya reaksi oksidasi atau minimal stabil karena
perlakuan lama waktu pengendapan tidak dikombinasikan dengan perlakuan lain
yang dapat mempengaruhi aktivitas antioksidan. Jadi diperlukan adanya penelitian
lebih lanjut pada perlakuan lama waktu pengendapan tanpa penambahan kitosan
(0%).
Gambar 20. Hubungan antara perlakuan penambahan kitosan dan lama waktu pengendapan dengan aktivitas antioksidan (DPPH) (%) sari buah delima yang dihasilkan.
Berdasarkan Gambar 20 menunjukan bahwa semakin tinggi penambahan
kitosan dan makin lama waktu pengendapan yang dilakukan, maka aktivitas
antioksidan yang dihasilkan makin tinggi. Hal ini karena aktivitas antioksidan
berkaitan dengan total senyawa fenol karena senyawa fenol merupakan agensia
antioksidan selain itu kitosan juga dapat berfungsi sebagai komponen antioksidan
R² = 0,956
Lama waktu pengendapan (menit)