PENENTUAN KADAR ION Br
-DENGAN TITRASI ARGENTOMETRI
(METODE VOLHARD)
Tujuan: Menentukan kadar ion Br- dalam larutan NaBr
Menentukan molaritas KSCN dengan metode titrasi balik
Widya Kusumaningrum (1112016200005), Ipa Ida Rosita, Nurul Mu’nisah Awaliyah,
Ummu Kalsum A.L, Amelia Rachmawati.
Program Studi Pendidikan Kimia
Jurusan Pendidikan Ilmu Pengetahuan Alam
Fakultas Ilmu Tarbiyah dan Keguruan
Universitas lslam Negeri Syarif Hidayatullah Jakarta
ABSTRAK
Metode volhard atau disebut juga titrasi balik adalah metode yang digunakan untuk
menentukan kaadar ion halida dalam suatu larutan. Pada percobaan ini menentukan kadar ion
bromida dan konsentrasi KSCN dengan metode titrasi balik. Dalam melakukan titrasi
menggunakan indikator FeCl
3yaitu ion Fe
3+akan bereaksi dengan ion SCN
-membentuk kompleks.
Persamaan reaksi lengkapnya yaitu :
Fe3+(aq) + SCN-(aq) [FeSCN]2+(aq)
Metode volhard juga dikenal dengan metode pembentukan kompleks berwarna. Kadar ion
bromida yang didapatkan sebesar 0,74% dan konsentrasi KSCN sebesar 0,2 M.
I. PENDAHULUAN
Titrasi pengendapan adalah golongan titrasi di mana hasil reaksi titrasinya merupakan
endapan atau garam yang sukar larut. Prinsip dasarnya adalah reaksi pengendapan yang
mencapai kesetimbangan pada setiap penambahan titran; tidak ada pengotor yang
mengganggu dan diperlukan indikator untuk melihat titik akhir titrasi. Hanya reaksi
pengendapan yang dapat digunakan pada titrasi. Akan tetapi metode tua seperti penetuan Cl-¸
Br -, I- dengan Ag(I) (disebut juga metode argentomeri) adalah sangat penting. Alasan utama
kurang digunakannya metode tersebut adalah sulitnya memperoleh indikator yang sesuai
untuk menentukan titik akhir pengendapan. Kedua, komposisi endapan tidak selalu diketahui
(S.M Khopkar, 1990: 61).
Titrasi pengendapan (argentometri) didasarkan pada reaksi:
AgNO3 + Cl- AgCl(s) + NO3-
Kalium kromat dapat digunakan sebagai indikator, menghasilkan warna merah dengan
kelebihan ion Ag+. Titrasi yang lebih banyak dapat digunakan adalah metode titrasi balik.
Kelegihan AgNO3 ditambahkan ke dalam sampel yang mengandung ion klorida atau
bromida. Kelebihan AgNO3 kemudian ditirasi dengan amonium tiosianat, dan amonium fero
sulfat digunakan sebagai indikator pada kelebihan SCN- (David G Watson, 2007).
AgNO3 + NH4SCN AgSCN (s) + NH4 NO3
Titrasi argentometri yang digunakan untuk menentukan kadar ion bromida pada suatu
Metode volhard didasari oleh pengendapan dari perak tiosianat dalam larutan asam
nitrit, dengan ion besi (III) dipergunakan untuk mendeteksi kelebihan ion tiosianat:
Metode ini dapat dipergunakan untuk titrasi langsung perak dengan larutan standar
tiosianat atau untuk titrasi tidak langsung dari ion-ion klorida, bromida dan iodida. Dalam
titrasi tidak langsung, kelebihan dari perak nitrat standar ditambahkan dan kemudian dititrasi
dengan tiosianat standar (R.A DAY, JR.& A.L. UNDERWOOD, 1998:228).
II. ALAT, BAHAN, DAN PROSEDUR KERJA
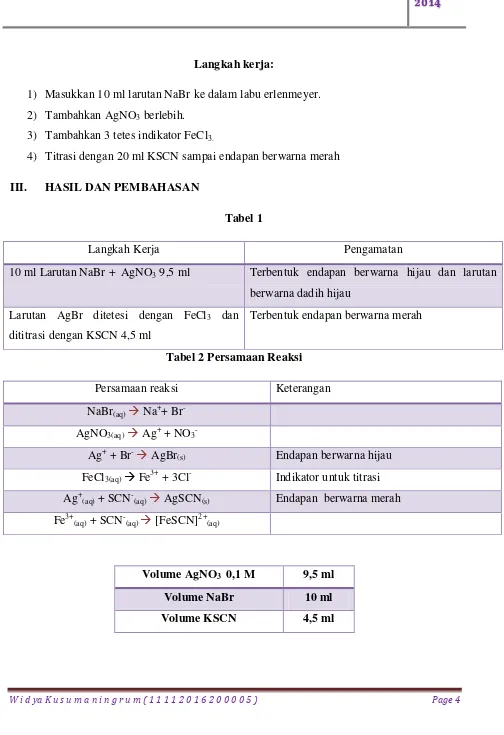
Langkah kerja:
1) Masukkan 10 ml larutan NaBr ke dalam labu erlenmeyer. 2) Tambahkan AgNO3 berlebih.
3) Tambahkan 3 tetes indikator FeCl3.
4) Titrasi dengan 20 ml KSCN sampai endapan berwarna merah
Perhitungan
A. AgNO3(aq)+ NaBr (aq) → AgBr ↓ (dadih hijau) + NaNO3 (aq)
V1xM1=V2xM2
9,5ml x 0,1 M= 10 ml x M2 M2= 0,095
Massa NaBr. . .?
Massa NaBr = 0,09785 gram
Massa Br- =
x massa NaBr
=
x 0,09785 gram
= 0,076 gram
% Massa Br- =
x 100%
=
x 100%
B. Ag+(aq) + SCN-(aq) AgSCN(s)
V1 x M1= V2 x M2
9,5 ml x 0,1 M (AgNO3) = 4,5 ml x M2 (KSCN)
M2= 0,2
Konsentrasi KSCN sebesar 0,2 M
Penentuan kadar ion bromida menggunakan metode volhard dilakukan dalam suasana asam. Sebelum melakukan titrasi balik, ion bromida yang terdapat dalam larutan NaBr yang belum diketahui konsentrasinya ditetesi dengan larutan AgNO3 0,1 M. Setelah menambahkan
AgNO3 secara berlebih, terbentuklan endapan berbentuk seperti dadih dan berwarna hijau.
Endapan ini terbentuk karena ion perak sudah berlebih, artinya tidak dapat lagi bereaksi dengan NaBr sehingga terbentuklah endapan. Persamaan reaksinya sebagai berikut:
AgNO3 (aq)+ NaBr (aq) → AgBr ↓ (dadih hijau) + NaNO3 (aq)
Setelah terbentuk endapan, pemberian AgNO3 dihentikan. Volume AgNO3 yang
dibutuhkan ialah 190 tetes atau 9,5 ml. Kemudian dapat ditentukan kadar ion bromida pada larutan NaBr dengan mencari molaritas NaBr yaitu 0,095 M, kemudian mencari massa NaBr yaitu 0,09785 gram, didapatlah massa Br- 0,076 gram. Sehingga dengan menggunakan persamaan berikut:
% Massa Br- =
x 100%
Dapat ditentukan bahwa kadar ion bromida dalam larutan NaBr sebesar 0,74 %.
Metode volhard harus dilakukan dalam suasana asam. Penambahan FeCl3 sebagai
Ag+(aq) + SCN-(aq) AgSCN(s)
Fe3+(aq) + SCN-(aq) [FeSCN]2+(aq)
Warna merah bata yang dihasilkan karena ion Fe3+ bereaksi dengan ion SCN- pada larutan. Warna ini merupakan warna pembentukan kompleks. Apabila saat dititrasi terbentuk kompleks berwarna merah, maka titrasi sudah mencapai titik ekuivalen. Sementara itu, ion Ag+ dalam larutan AgBr berekasi dengan ion SCN- pada larutan KSCN. Dalam hal ini untuk menentukan konsentrasi KSCN maka menggunakan Volume dan Molaritas AgNO3 dan
volume KSCN saat titrasi. Didapatlah molaritas KSCN sebesar 0,2 M.
IV. KESIMPULAN
Berdasarkan data hasil percobaan dan pembahasan di atas, maka dapat disimpulkan bahwa:
1)
Penentuan kadar ion bromida dengan metode volhard menggunakan AgNO3 secaraberlebih.
2)
Molaritas NaBr yaitu 0,095 M, massa NaBr yaitu 0,09785 gram, dan % massa Br -dalam NaBr yaitu 0,076 gram.V. DAFTAR PUSTAKA
Underwood, A.L. dkk. 1998.ANALISIS KIMIA KUANTITATIF Edisi Keenam. Jakarta: Erlangga
Khopkar, S.M. 1990. KONSEP DASAR KIMIA ANALITIK. Penerbit: UI-Press.