OPTIMASI WAKTU REAKSI, SUHU REAKSI
DAN KONSENTRASI KATALIS PADA SINTESIS GLISEROL
TERT-BUTYL ETER (GTBE)
Oleh :
AMRI SOLECHAN
F34050706
2010
FAKULTAS TEKNOLOGI PERTANIAN
INSTITUT PERTANIAN BOGOR
BOGOR
OPTIMASI WAKTU REAKSI, SUHU REAKSI
DAN KONSENTRASI KATALIS PADA SINTESIS GLISEROL
TERT-BUTYL ETER (GTBE)
Oleh :
AMRI SOLECHAN
F34050706
2010
FAKULTAS TEKNOLOGI PERTANIAN
INSTITUT PERTANIAN BOGOR
BOGOR
OPTIMASI WAKTU REAKSI, SUHU REAKSI
DAN KONSENTRASI KATALIS PADA SINTESIS GLISEROL
TERT-BUTYL ETER (GTBE)
Oleh :
AMRI SOLECHAN
F34050706
2010
FAKULTAS TEKNOLOGI PERTANIAN
INSTITUT PERTANIAN BOGOR
OPTIMASI WAKTU REAKSI, SUHU REAKSI
DAN KONSENTRASI KATALIS PADA SINTESIS GLISEROL
TERT-BUTYL ETER (GTBE)
SKRIPSI
Sebagai Salah Satu Syarat Untuk Mendapatkan Gelar
SARJANA TEKNOLOGI PERTANIAN
Pada Departemen Teknologi Ind ustri Pertanian
Institut Pertanian Bogor
Oleh :
AMRI SOLECHAN
F34050706
2010
FAKULTAS TEKNOLOGI PERTANIAN
INSTITUT PERTANIAN BOGOR
Judul Skripsi : Optimasi Waktu Reaksi, Suhu Reaksi dan Konsentrasi Katalis
pada Sintesis Gliserol Tert-Butyl Eter (GTBE).
Nama
: Amri Solechan
NIM
: F34050706
Menyetujui :
Dr. Dwi Setyaningsih, M.Si
NIP : 19700103 199412 2 001
Mengetahui :
Ketua Departemen
Prof. Dr. Nastiti Siswi Indrasti
NIP : 19621009 198903 2 001
Amri Solechan. F34050706. Optimasi Waktu Reaksi, Suhu Reaksi dan Konsentrasi
Katalis pada Sintesis Gliserol Tert-butyl Eter (GTBE). Di bawah bimbingan Dr.Ir. Dwi Setyaningsih, M.Si. 2010
RINGKASAN
Biodiesel adalah salah satu sumber bahan bakar yang saa t ini banyak dikembangkan di berbagai negara karena dapat diperbaharui dan juga aman bagi lingkungan. Biodiesel digunakan untuk mengurangi penggunaan bahan bakar fosil terutama solar. Namun biodiesel masih memiliki kelemahan yaitu tingginya cloud point (titik kabut) dan pour point (titik tuang) dibandingkan solar. Hal ini dapat menimbulkan masalah pada penggunaan biodiesel terutama pada negara -negara yang memiliki musim dingin. Untuk mengatasi hal ini biasanya ditambahkan aditif tertentu pada biodiesel untu k mencegah aglomerisasi kristal -kristal yang terbentuk dalam biodiesel pada suhu rendah.
Produksi biodiesel yang semakin meningkat, mengakibatkan produk -produk hasil sampingnya seperti gliserol juga semakin meningkat. Gliserol mempunyai karakteristik sebagai zat anti beku (krioprotektan), tetapi gliserol tidak dapat ditambahkan ke dalam
bahan bakar secara langsung karena perbedaan kepolaran dan akan mengalami
dekomposisi, polimerisasi serta menyebabkan masalah pada mesin pada suhu yang tinggi. Gliserol harus dimodifikasi sehingga dapat ditambahkan ke dalam bahan bakar. Modifikasi gliserol yang sangat jelas dapat dianalogikan dengan gasolin yang diformulasi ulang (oxygenated gasoline).
Gliserol dapat dieterifikasi dengan isobutilen sehingga terbentuk eter b ercabang yang dapat ditambahkan ke dalam biodiesel agar menghasilkan bahan bakar yang memiliki viskositas lebih rendah dan titik awan di bawah 0ºC. Selain dengan menggunakan isobutilen, eterifikasi gliserol juga dapat dilakukan dengan tert-butyl alkohol (TBA). Katalis yang biasa digunakan pada reaksi eterifikasi gliserol adalah katalis asam kuat penukar ion, yaitu Amberlist. Namun karena harganya yang mahal maka dalam penelitian ini digunakan katalis bentonit alam yang terlebih dahulu diaktivasi dengan meng gunakan asam.
Penelitian ini mengkaji pengaruh dan optimasi waktu reaksi, suhu reaksi dan konsentrasi katalis terhadap rendemen GTBE yang terbentuk. Rancangan percobaan yang digunakan adalah central composite design yang merupakan salah satu jenis response
surface methodology (RSM). Batas bawah untuk waktu reaksi adalah selama 6 jam, untuk
suhu reaksi sebesar 60°C, dan untuk konsentrasi katalis adalah sebesar 2,5 % (b/b). Sedangkan atas atas untuk waktu reaksi adalah selama 8 jam, untuk suhu reaksi sebes ar 80°C dan untuk konsentrasi katalis sebesar 7,5 % (b/b).
Hasil penelitian menunjukkan bahwa waktu reaksi tidak berpengaruh secara signifikan pada selang kepercayaan 95 %. Sedangkan, suhu reaksi dan konsentrasi katalis berpengaruh secara signifikan pada selang kepercayaan 95 %. Hasil analisa menggunakan
software Design Expert 7.1.6 (free trial) menunjukkan model hubungan dari faktor waktu
reaksi (X1), suhu reaksi (X2) dan konsentrasi katalis (X3) terhadap respon sqrt GTBE
menunjukkan model yang berbentuk saddle point. Dari uji optimasi didapatkan nilai optimasi sqrt GTBE perkiraan sebesar 613,10 dengan kondisi waktu reaksi selama 4,9 jam,
suhu reaksi sebesar 66,2°C, dan konsentrasi katalis sebesar 9,7 % (b/b). Dari hasil verifikasi pada kondisi tersebut di dapatkan nilai sqrt GTBE yang lebih besar yaitu 980,86. Hal ini menandakan model yang didapatkan tidak dapat memprediksi kondisi yang menghasilkan konsentrasi GTBE optimum pada kisaran yang telah ditentukan. Kondisi optimum diperkirakan berada pada kondisi waktu reaksi kurang dari 8 jam, suhu reaksi lebih dari 60°C dan konsentrasi katalis lebih dari 7,5 %.
Uji efektivitas GTBE dalam menurunkan titik kabut dan titik tuang biodiesel dilakukan dengan cara mencampurkan GTBE ke dalam biodiesel dengan perbanding an volume sebesar 1:10. Hasil dari uji ini menunjukkan bahwa biodiesel yang ditambahkan GTBE sebanyak 10 % (v/v) mempunyai titik kabut dan titik tuang yang lebih rendah 3°C daripada biodiesel yang tidak ditambahkan GTBE. GTBE yang dihasilkan masih kurang efektif untuk menurunkan titik kabut dan titik tuang biodiesel karena GTBE yang terbentuk sebagian besar adalah mono-tert-butyl eter gliserol (MTBG) yang kurang larut dalam biodiesel.
Amri Solechan. F34050706. Optimization of Reaction Time, Temperature and Concentration of Catalyst in Glycerol Tert -Butyl Ether (GTBE) Synthesis. Supervised by Dr. Ir. Dwi Setyaningsih, M.Si. 2010.
SUMMARY
Biodiesel is one of the fuels that many countries develop because it’s renewable
and eco-friendly. Biodiesel is used to substitute petroleum fuel especially diesel fuel.
However, biodiesel still have disadvantages, that is the biodiesel’s cloud point and pour
point is higher than petroleum based diesel fuel. This disadvantage becomes a problem on biodiesel utilization especially in subtropical countries. This problem can be solved by addition of chemicals to prevent agglomeration of crystals that are formed in biodiesel in low temperature.
Increasing production of biodiesel cause increasing biodiesel by products as well, one of the biodiesel by products is glycerol. Glycerol has characteristic as anti -freezing
(cryoprotectant) but it can’t be added directly to fuel because of polarity difference,
decomposition, and polymerization can rise consequential engine problems at high temparatures. Glycerol must be modified to derivatives that are compatible with diesel and biodiesel prior to be added to the fuel. The most obvious derivative of glycerol has an analogy in gasoline reformulation (oxygenated gasoline).
Etherification of glycerol with isobutylene produce branched ether that can be mixed with biodiesel to make a fuel with lower viscosity and cloud point value below 0°C. Beside of using isobutylene, etherification of glycerol also can be done with tert -butyl alcohol (TBA). The commonly used catalyst in etherification of glycerol is commercial strong acid ion-exchange catalyst, such as Amberlist. In this research, the possibility to replace expensive Amberlist with local bentonite was evaluated. Natural bentonite was activated by hydrochloric acid (HCl) prior to use as catalyst.
The effect and optimization of reaction time, temperature and concentration of catalyst to the concentration of produced GTBE was studied. Experimental design that used is central composite design, it is one kind of the Response Surface Methodology
(RSM). Lower level for reaction time is 6 hour s, temperature is 60C, and concentration of
catalyst is 2.5%. Higher level for reaction time is 10 hour s, temperature is 80C, and
concentration of catalyst is 7.5%.
The result showed that reaction time doesn’t have signification influence to
concentration of GTBE in confidence interval 95 %. Whereas , temperature and concentration of catalyst have signification influence s to concentration of GTBE in confidence interval 95 %. The result from analysis with software Design Expert 7.1.6 (free
trial) shows that the relationship between reaction time (X1), temperature (X2), and
concentration of catalyst (X3) generate saddle point model. From optimization t est, the sqrt
GTBE’s value is predicted 613.10 with reaction time is 4.9 hours, temperature is 66. 2C
and concentration of catalyst is 9 .7 %. Verification of that prediction of optimum condition
resulted in sqrt GTBE’s value of 980.86. This result showed that the model couldn’t
range. Optimum concentration of GTBE was predicted when reaction time below 6 hours, temperature above 60°C, and concentration of catalyst above 7 .5 %.
The GTBEeffectiveness test to reduce biodiesel’s cloud point and pour point was
done by mixing GTBE in biodiesel with volume ratio 1:10. The result from this test showed that biodiesel which has been mixed with GTBE has cloud point and pour point
3C lower than biodiesel alone. GTBE that has been produced is still less effective to
reduce biodiesel’s cloud point and pour point because GTBE that has been formed mainly
SURAT PERNYATAAN
Saya menyatakan dengan sebenar -benarnya bahwa skripsi dengan Judul “Optimasi
Waktu Reaksi, Suhu Reaksi dan Konsentrasi Katalis pada Sintesis Gliserol Tert-Butyl Eter (GTBE)” adalah hasil karya saya sendiri dengan arahan Dosen Pembimbing Akademik, kecuali yang dengan jelas ditunjukkan rujukannya.
Bogor, Januari 2010 Yang membuat pernyataan,
Amri Solechan NRP. F34050706
BIODATA
Penulis dilahirkan di Banjarnegara pada tanggal 29 April 1988 dari ayah bernama Nurudin dan ibu bernama Misni. Penulis merupakan putra keempat dari empat bersaudara.
Penulis memulai pendidikan formal pertamanya di SD Negeri 1 Pingit pada tahun 1993 dan lulus pada tahun 1999 sebagai lulusan terbaik. Penulis menyelesaikan pendidikan menengahnya di SLTP Negeri 1 Rakit pada tahun 2002 dan di SMU Negeri 1 Bawang, Banjarnegara pada tahun 2005. Tahun 2005 penulis diterima di IPB melalui jalur Undangan Seleksi Masuk IPB. Penulis memilih Departemen Teknologi Industri Pertanian, Fakultas Teknologi Pertanian pada pemilihan mayor tahun 2006.
Selama mengikuti perkuliahan, penulis aktif di beberapa organisasi. Pada tahun 2006/2007 penulis adalah staff biro in ternal departemen Public Relation HIMALOGIN. Pada tahun 2007/2008 penulis adalah staff departemen Minat dan Bakat Mahasiswa BEM Fateta. Pada tahun 2007 penulis menjadi assisten praktikum mata kuliah Penerapan Komputer.
Penulis melakukan praktek lapang di P T Indo Acidatama, Tbk., Karanganyar dan
menyusun laporan praktek lapang dengan judul “Mempelajari Proses Produksi di PT Indo
Acidatama, Tbk.”. Sebagai tugas akhir untuk memperoleh gelar Sarjana Teknologi
Pertanian, penulis menulis skripsi dengan judul “Optimasi Waktu Reaksi, Suhu Reaksi dan
Konsentrasi Katalis pada Sintesis Gliserol Tert-Butyl Eter (GTBE)” dengan bimbingan
KATA PENGANTAR
Alhamdulillah, puji syukur penulis panjatkan kehadirat Allah SWT atas segala limpahan rahmat, karunia, dan nikmat -Nya, sehingga penulis dapat menyelesaikan skripsi
yang berjudul “Optimasi Waktu Reaksi, Suhu Reaksi, dan Konsentrasi Katalis pada
Sintesis Gliserol Tert-Butyl Eter (GTBE)”. Skripsi ini merupakan salah satu syarat untuk menyelesaikan tugas akhir pada departemen Teknologi Industri Pertanian, Fakultas Teknologi Pertanian, Institu Pertanian Bogor.
Banyak kendala yang penulis hadapi dalam menyelesaikan skripsi ini, namun berkat rahmat dan karunia Allah SWT, serta bimbingan dan bantuan dari berbagai pihak, Alhamdulillah skripsi ini dapat diselesaikan. Oleh karena itu, pada kesempatan ini, penulis mengucapkan terima kasih kepada :
1. Ibu, bapak, kakak, serta seluruh keluarga besar penulis atas dukungan, doa, dan kasih
sayangnya.
2. Ibu Dr. Ir. Dwi Setyaningsih, M.Si, selaku dosen pembimbing akademik yang telah
memberikan waktu dan perhatiannya dalam memberikan petunjuk, arahan, bimbingan, dan pemikirannya kepada penulis dalam menyelesaikan skripsi ini.
3. Prof.Dr. Ani Suryani, DEA dan Dr. Ika Amalia Kartika, M.T, selaku dosen penguji
yang telah memberikan masukan, koreksi dan saran yang sangat berguna dalam menyelesaikan skripsi ini.
4. Seluruh Staff SBRC, terutama Mas Saiful, Mba Wiwin, dan Mas Obi atas bantuannya
selama penulis melakukan penelitian.
5. Teman-teman seperjuangan penelitian di SBRC : Fikri, Efrat, Ahsan, Mas Fanani, Ovi,
Ninda dan Nutri. Terima kasih atas kebersamaan, bantuan dan motivas inya.
6. Alfian, Tika, Arif, Deni, Shafeeg, dan O2n atas bantuan dan motivasinya.
7. Teman-teman “Pondok Botax” : Iqbal, Amri, C-bay, Adit dan Ketuk atas kecerian dan
kebersamaannya.
8. Rekan-rekan TIN 42 atas persaudaraan dan kebersamaannya. Saya bangga menjadi
bagian dari kalian.
9. Semua pihak yang tidak dapat disebutkan satu per satu, yang telah membantu dan
Penulis menyadari, skripsi ini tidaklah sempurna. Oleh karena itu pen ulis menerima kritik dan saran yang membangun untuk skripsi ini. Akhirnya penulis mengharapkan skripsi ini dapat bermanfaat bagi pen ulis pada khususnya dan pembaca pada umumnya.
Bogor, Januari 2010
DAFTAR ISI
Halaman
KATA PENGANTAR ... ... ... i
DAFTAR ISI ... ... ... ... iii
DAFTAR TABEL ... ... ... ... v
DAFTAR GAMBAR ... ... ... . vi
DAFTAR LAMPIRAN ... ... ... vii
I. PENDAHULUAN A. LATAR BELAKANG ... ... ... 1
B. TUJUAN ... ... ... ... 1
II. TINJAUAN PUSTAKA A. BIODIESEL ... ... ... .... 2
B. GLISEROL ... ... ... ... 3
C. BENTONIT ... ... ... .... 5
D. GLISEROL TERT-BUTYL ETER... ... .... 7
E. KUALITAS BIODIESEL PADA SUHU RENDAH ... ... 8
III. METODOLOGI A. BAHAN DAN ALAT... ... ... 10
B. METODE PENELITIAN ... ... ... 10
1. Tahap Sintesis GTBE ... ... ... 10
2. Optimasi Sintesis GTBE ... ... ... 12
3. Uji Efektivitas GTBE ... ... ... 12
C. RANCANGAN PERCOBAAN ... ... ... 13
IV. HASIL DAN PEMBAHASAN A. SINTESIS GLISEROL TERT-BUTYL ETER (GTBE) ... ... 15
B. ANALISIS RESPONSE SURFACE METHODOLOGY (RSM)... 19
1. Analisis Pengaruh Faktor ... ... ... 22
2. Optimasi Konsentrasi GTBE ... ... ... 26
C. EFEKTIVITAS GTBE DALAM MENURUNKAN TITIK KABUT DAN TITIK TUANG BIODIESEL ... ... ... 30
V. KESIMPULAN DAN SARAN
A. KESIMPULAN ... ... ... 34
B. SARAN... ... ... ... 35
DAFTAR PUSTAKA ... ... ... 36
DAFTAR TABEL
Halaman
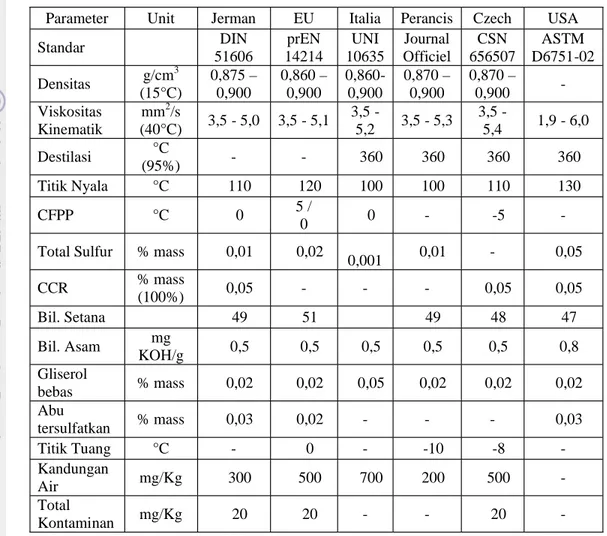
Tabel 1. Standar mutu biodiesel internasional ... ... 3
Tabel 2. Sifat fisika-kimia gliserol ... ... ... 4
Tabel 3. Komposisi kimia bentonit ... ... ... 6
Tabel 4. Batasan dan level berubah ... ... ... 14
Tabel 5. Rancangan percobaan ... ... ... 14
Tabel 6. Karakteristik bentonit ... ... ... 16
Tabel 7. Data hasil sintesis GTBE ... ... ... 19
Tabel 8. Hasil transformasi data konsentrasi GTBE ... ... 21
Tabel 9. Nilai titik kabut dan titik tuang campuran biodiesel dengan GTB... 32
DAFTAR GAMBAR
Halaman
Gambar 1. Reaksi Transesterifikasi trigeliserida dengan alkohol ... 2
Gambar 2. Struktur kimia gliserol ... ... ... 4
Gambar 3. Skema montmorillonite dua layer ... ... 6
Gambar 4. Reaksi eterifikasi gliserol ... ... ... 7
Gambar 5. Reaktor eterifikasi gliserol ... ... ... 10
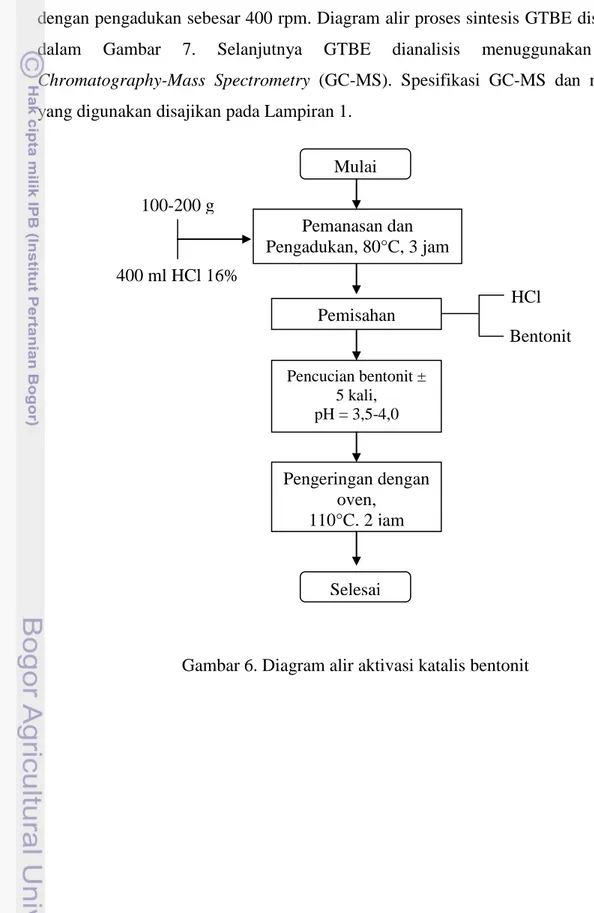
Gambar 6. Diagram alir aktivasi katalis bentonit ... ... 11
Gambar 7. Diagram alir sintesis GTBE ... ... ... 12
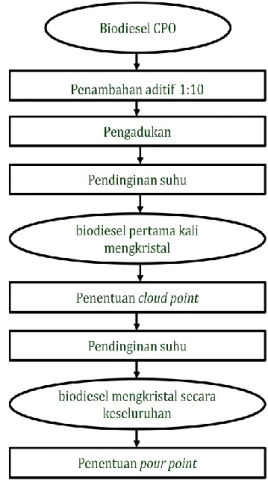
Gambar 8. Diagram pengujian efektivitas GTBE ... ... 13
Gambar 9. Hasil GC-MS GTBE ... ... ... 16
Gambar 10. Foto bentonit alam dan bentonit teraktivasi ... ... 17
Gambar 11. Plot pengaruh waktu reaksi terhadap sqrt GTBE ... ... 22
Gambar 12. Plot pengaruh suhu reaksi terhadap sqrt GTBE ... ... 23
Gambar 13. Plot pengaruh konsentrasi katalis terhadap sqrt GTBE ... 24
Gambar 14. Plot pengaruh interaksi suhu dan waktu reaksi terhadap sqrt GTBE ... 24
Gambar 15. Plot pengaruh interaksi waktu dan konsentrasi katalis terhadap sqrt GTBE ... ... ... ... 25
Gambar 16. Plot pengaruh interaksi suhu dan konsentrasi katalis terhadap sqrt GTBE ... ... ... ... 26
Gambar 17. Grafik permukaan respon sqrt GBTE sebagai fungsi dari faktor waktu dan suhu reaksi ... ... ... 27
Gambar 18. Kontur sqrt GTBE dengan faktor waktu dan suhu reaksi ... 27
Gambar 19. Grafik permukaan respon sqrt GBTE sebagai fungsi dari faktor waktu reaksi dan konsentrasi katalis ... ... ... 28
Gambar 20. Kontur sqrt GTBE dengan faktor waktu reaksi dan konsentrasi katalis... 28
Gambar 21. Grafik permukaan respon sqrt GBTE sebagai fungsi dari faktor suhu reaksi dan konsentrasi katalis ... ... .. 29
Gambar 22. Kontur sqrt GTBE dengan faktor suhu reaksi dan konsentrasi katalis... 29
DAFTAR LAMPIRAN
Halaman
Lampiran 1. Spesifikasi dan metode Gas Chromatography-Mass Spectrometry
(GC-MS)... ... ... 39
Lampiran 2. Prosedur analisa cold properties biodesel ... ... 40
Lampiran 3. Hasil GC-MS ... ... ... 42
Lampiran 4. Hasil analisis ANOVA menggunakan Design Expert 7.1.6 ... 51
Lampiran 5. Analisis sebaran normal ... ... .... 52
Lampiran 6. Analisis ANOVA data hasil transformasi ... ... 53
I. PENDAHULUAN
A. LATAR BELAKANG
Cadangan minyak mentah dunia yang semakin berkurang memaksa manusia untuk mencari sumber energi yang terbarukan. Selain itu, perubahan iklim global juga mendorong manusia untuk mencari sumber energi yang aman terhadap lingkungan. Biodiesel adalah salah satu sumber bahan bakar yang saat ini banyak dikembangkan di berbagai negara karena dapat diperbaharui dan juga aman bagi lingkungan karena tidak mengandung sulfur.
Namun biodiesel masih memiliki kelemahan yaitu tingginya titik kabut dan titik tuang dibandingkan solar. Hal ini dapat menimbulkan masalah pada penggunaan biodiesel terutama pada negara -negara yang memiliki musim dingin. Untuk mengatasi hal ini biasanya ditambahkan aditif tertentu pada biodiesel untuk mencegah aglomerisasi kristal-kristal yang terbentuk dalam biodiesel pada suhu rendah.
Peningkatan produksi biodiesel juga akan meningkatkan produk hasil sampin g produksi biodiesel yaitu gliserol. Menurut Noureddini et al. (1998), gliserol dapat dimanfaatkan sebagai aditif pada bahan bakar diesel. Namun gliserol tidak dapat ditambahkan ke bahan bakar secara langsung , karena akan mengalami dekomposisi, polimerisasi dan menyebabkan masalah pada mesin pada suhu yang tinggi. Gliserol harus dimodifikasi sehingga dapat ditambahkan ke dalam bahan bakar. Modifikasi gliserol yang sangat jelas dapat dianalogikan dengan reformulasi gasolin menjadi gasolin teroksigenasi (oxygenated gasoline), yaitu dengan penambahan Methyl Tertiary
Butyl Ethers (MTBEs) sebagai bahan aditif ke dalam gasolin .
Gliserol dapat dieterifikasi dengan senyawa isobutilen ataupun tert-butyl alkohol
dengan katalis asam kuat sehingga dihasilkan gliserol tert-butyl eter (GTBE).
Konsentrasi GTBE yang terbentuk dipengaruhi oleh beberapa faktor, antara lain suhu reaksi, waktu reaksi, jenis dan jumlah katalis dan rasio molar antara gliserol dengan TBA ataupun isobutilen (Noureddini et al., 1998).
B. TUJUAN PENELITIAN
Tujuan dilakukannya penelitian ini adalah untuk mengetahui pengaruh waktu reaksi, suhu reaksi dan konsentrasi katalis terhadap konse ntrasi GTBE yang terbentuk dan mendapatkan kondisi reaksi GTBE yang optimum. GTBE yang diperoleh diuji aktivitasnya dalam menurunkan titik awan dan titik tuang biodiesel.
II. TINJAUAN PUSTAKA
A. BIODIESEL
Biodiesel adalah bahan bakar nabati yang dibuat dari minyak nabati, baik minyak baru maupun bekas penggorengan melalui proses transesterifikasi, esterifiasi, atau proses esterifikasi-transesterifikasi (Hambali et al., 2007). Secara kimiawi, biodiesel adalah monoalkil ester dari rantai panjang asam lemak yang berasal dari bahan baku yang dapat diperbaharui, seperti minyak nabati atau lemak hewani, untuk digunakan dalam mesin diesel (Meher et al., 2004).
Biodiesel terdiri atas asam-asam lemak metil ester yang dapat diperoleh dari trigliserida dalam minyak nabati melelui proses transestrifikasi dengan metanol. Biodiesel akhir yang diperoleh dari proses ini memiliki karakteristik utama yang sama dengan bahan bakar diesel konves ional (Meher et al., 2004).
Trasnsesterifikasi atau disebut juga alkoholisis adalah proses penggantian alkohol dari ester dengan alkohol lain dalam proses yang serupa dengan hidrolisis. Alkohol yang sering digunakan yaitu metanol, karena harganya lebih m urah dibandingkan dengan turunan alkohol lainnya (Lotero et al., 2004). Transesterifikasi secara luas digunakan untuk mengurangi viskositas trigliserida dengan meningkatkan ka ndungan fisik bahan bakar terbarukan untuk meningkatkan kinerja mesin (Fukada et al., 2001). Reaksi transesterifikasi trigliserida dengan metanol disajikan dalam gambar berikut.
Gambar 1. Reaksi Transesterifikasi trigeliserida dengan alkohol
Proses transesterifikasi dipengaruhi oleh beberapa faktor tergantung kondisi reaksinya. Faktor tersebut diantaranya adalah kandungan asam lemak bebas dan kadar air minyak, jenis katalis dan konsentrasinya, perbandingan molar antara alkohol dengan minyak dan jenis alkohol, suhu dan lamanya reaksi, intensitas pencampuran dan penggunaan co-solvent organik (Meher et al., 2004).
Kualitas biodiesel dipengaruhi oleh kualitas minyak ( feedstock), komposisi asam lemak dari minyak, proses produksi dan bahan lain yang digunakan dalam proses dan parameter pasca-produksi seperti kontaminan. Kontaminan tersebut diantaranya adalah
bahan tak tersabunkan, air, gliserin terikat, alkohol, asam lemak bebas, sabun, residu katalis (Gerpen, 2004). Standar mutu dari biodisel dapat dilihat dalam Tabel 1 berikut.
Tabel 1. Standar mutu biodiesel internasional
Parameter Unit Jerman EU Italia Perancis Czech USA
Standar DIN 51606 prEN 14214 UNI 10635 Journal Officiel CSN 656507 ASTM D6751-02 Densitas g/cm 3 (15°C) 0,875– 0,900 0,860– 0,900 0,860-0,900 0,870– 0,900 0,870– 0,900 -Viskositas Kinematik mm2/s (40°C) 3,5 - 5,0 3,5 - 5,1 3,5 -5,2 3,5 - 5,3 3,5 -5,4 1,9 - 6,0 Destilasi °C (95%) - - ≤ 360 ≤360 ≤ 360 ≤ 360 Titik Nyala °C ≥ 110 ≥ 120 ≥ 100 ≥ 100 ≥ 110 ≥ 130 CFPP °C ≤ 0 ≤ 5 / ≤ 0 ≤ 0 - ≤-5
-Total Sulfur % mass ≤ 0,01 ≤ 0,02 ≤
0,001 ≤ 0,01 - ≤ 0,05 CCR % mass (100%) ≤ 0,05 - - - ≤ 0,05 ≤ 0,05 Bil. Setana ≥ 49 ≥ 51 ≥ 49 ≥ 48 ≥ 47 Bil. Asam mg KOH/g ≤ 0,5 ≤ 0,5 ≤ 0,5 ≤ 0,5 ≤ 0,5 ≤ 0,8 Gliserol bebas % mass ≤ 0,02 ≤ 0,02 ≤ 0,05 ≤ 0,02 ≤ 0,02 ≤ 0,02 Abu tersulfatkan % mass ≤ 0,03 ≤ 0,02 - - - ≤ 0,03 Titik Tuang °C - ≤ 0 - ≤-10 ≤-8 -Kandungan Air mg/Kg ≤300 ≤500 ≤700 ≤200 ≤500 -Total Kontaminan mg/Kg ≤ 20 ≤ 20 - - ≤ 20
-Sumber : Hambali et al. (2006)
B. GLISEROL
Gliserol adalah senyawa golongan alkohol polihidrat dengan tiga buah gugus
hidroksi dalam satu molekul (alkohol trivalen). Rumus kimia gliserol adalah C3H8O
dengan nama kimia 1,2,3-propanatriol. Berat molekul gliserol adalah 92,10 g/mol
dengan massa jenis 1,23 g/cm3(Winarno, 1992). Gliserol bersifat mudah larut dalam air,
dapat meningkatkan viskositas larutan, mengikat air, menurunkan aw bahan, merupakan
cairan dengan rasa pahit-manis yang mempunyai kelarutan tinggi, yaitu sebesar 71 g/100 g air pada suhu 250 ºC (Gaman dan Sherrington, 1992).
Gambar 2. Struktur kimia gliserol Tabel 2. Sifat fisika-kimia gliserol
Sifat Nilai Titik Leleh (°C) 18,17 Titik Didih (°C) 0,53 kPa 14,9 1,33 kPa 166,1 13,33 kPa 222,4 101,3 kPa 290 Spesific Gravity, 25/25 °C 1,262
Tekanan Uap (Pa)
50°C 0,33 100°C 526 150°C 573 200°C 6100 Tegangan Permukaan (20°C,nM/m) 63,4 Viskositas (20°C, mPa-s) 1499 Konduktivitas panas [W/(m-K)] 0,28 Titik Nyala (°C)
Cleveland Open Cup 177
Pensky-Martens Closed Cup 199
Titik Api (°C) 204
Sumber : Gerpen dan Knothe (2004)
Menurut Kirk dan Othmer (1964) di dalam Agustina (2004), gliserol dapat berasal dari industri sabun, oleokimia, dan dapat juga dari industri kimia. Penggunaan gliserol sangat kompleks, terutama dalam industri. Sebagian gliserol digunakan dalam obat -obatan, kosmetika, busa uretan, resin sintetik , produk-produk personal care dan gum ester.
Gliserol merupakan produk samping yang prospektif dari proses pembuatan biodiesel karena harganya lebih tinggi daripada reaktan metanol. Fase gliserol dihasilkan dari proses transesterifikasi minyak dan alkohol , dimana pada akhir proses akan terpisah dengan metil ester (biodiesel) akibat adanya perbedaan berat jenis (Gerpen dan Knothe, 2004).
Gliserol harus dipisahkan dari biodiesel karena gliserol dapat membentuk senyawa plastis yang agak padat. Senyawa ini ak an membentuk deposit pada pompa injektor sehingga menyebabkan kerusakan pada mesin diesel (Prihandana et al., 2006). Gliserol hasil samping produksi biodiesel memiliki kualitas yang sangat rendah akibat adanya pengotor. Pemanfaatan gliserol kasar menjadi b entuk murni memerlukan pemurnian (Pachauri dan He, 2006).
Gliserol sebagai hasil samping produksi biodiesel dapat diesterifikasi dengan isobutilen dan eter bercabang sehingga jika ditambahkan ke dalam biodiesel dapat menghasilkan biodiesel yang viskositasnya lebih rendah dan titik awan di bawah 0 ºC (Noureddini, 1998).
C. BENTONIT
Bentonit adalah jenis tanah liat yang kandungan mineral utamanya ada lah
montmorillonite. Bentonit diklasifikasikan ke dalam dua tipe, yaitu tipe Ca dan tipe Na
berdasarkan ion dominan yang dapat berubah. Kualitas bento nit ditentukan dari kemampuan adsorbsinya, luas permukaan, kapasitas swelling (mengembang) dan kapasitas pertukaran kation (cation exchange capacity ) (Zhansheng et al., 2006).
Montmorillonite tergolong ke dalam kelompok smektit dan mempunyai komposisi
kimia yang beragam. Smektit adalah golongan mineral tanah yang disusun oleh lapisan oktahedral tunggal di antara dua lapisan tetrahedral (tipe 2:1). Rumus montmorillonite
sering dinyatakan sebagai Al2O3.4SiO2.xH2O. Nama montmorillite dikhususkan untuk
anggota smektit yang subtitusi terutama pada lembar oktahedral. Montmorillite
mempunyai Mg dan ion -ion feri dalam posisi oktahedral (Tan, 1993).
Priatna (1982) dalam Rahendas (2005), menyatakan bentonit mempunyai warna dasar putih dengan sedikit kecoklatan atau kemerahaan atau kehijauan tergantung dari jenis dan jumlah fragmen mineralnya. Bentonit bersifat sangat lunak, ringan, mudah pecah, terasa seperti sabun, mudah menyerap air dan melakukan pertukaran ion. Berat jenis bentonit berkisar antara 2,4 -2,8. Ukuran partikel koloid bentonit sangat k ecil dan mempunyai kapasitas pert ukaran ion yang tinggi. Sifat bentonit sebagai penukar ion karena adanya kation logam alkali dan alkali tanah. Kation tersebut dapat bergerak bebas di dalam rongga dan dapat dipertukarkan dengan kation logam lain dengan jumlah yang sama. Akibat struktur bentonit berongga, anion atau molekul berukuran lebih kecil atau sama dengan rongga dapat masuk dan terjebak .
Tabel 3. Komposisi kimia bentonit
Komponen Mineral Kandungan (%)
SiO2 65,24 Al2O3 15,12 Fe2O3 5,27 MgO 2,04 CaO 1,67 Na2O 2,71 K20 2,07 TiO2 0,68 MnO2 0,21 Loss 4,92
Sumber : Zhansheng et al. (2006)
Gambar 3. Skema montmorillonite dua layer
Aktivasi asam pada bentonit akan merubah luas permukaan, pori -pori dan keasaman bentonit. Perubahan ini tergantung pada smektit mineral, komposisi mineral tanah liat lain yang ada pada bentonit dan tanah liat non -mineral, tipe kation antar layer, jenis asam yang digunakan, banyaknya asam, suhu proses dan lama proses aktivasi (Onal et al., 2001).
Dalam montmorillonite, strukturnya bertingkat -tingkat dan bagian yang paling aktif dalam pertukaran ion adalah bagian paling dasar. Tujuan aktivasi bentonit dengan asam
adalah untuk menukar kation Ca++, Na+ dan K+ yang merupakan struktur bagian dasar
dalam bentonit menjadi ion H dan melepas ion Al, Mg, dan Fe serta pengotor-pengotor lainnya dari kisi-kisi struktur sehingga secara fisik bentonit tersebut menjadi lebih aktif (David dan Messer 1992 dalam Rahendas 2005).
Aktivasi bentonit menggunakan asam digunakan secara luas pada banyak bidang, misalnya pada penggunaan bentonit sebagai katalis di industri kimia. Penggunaan
bentonit yang paling penting adalah pada proses pemurni an, penghilangan warna, dan penyetabilan pada minyak nabati (Zhansheng et al., 2006).
D. GLISEROL TERT-BUTYL ETER (GTBE)
Gliserol eter adalah senyawa yang dihasilkan dari proses eterifikasi gliserol dengan alkohol (TBA) atau dengan alkena ( isobutilen) yang mengandung komponen oksigen yang bercabang yang cocok digunakan pada bahan bakar ataupun pelarut. Penggunaan GTBE dalam bahan bakar me mpunyai kelebihan yaitu dapat diperbaharui dan dapat menurunkan cold properties-nya (Karinen dan Krause, 2006).
Eterifikasi gliserol (O-alkylation) dengan menggunakan katalis asam akan menghasilkan formasi mono-, di-, dan tri-tert butyl eter gliserol. Struktur gliserol eter sebagai bahan aditif dapat berupa 1,3 butyl gliserol atau perpaduan 2,3
di-tert-butyl gliserol dengan 1,2 di-tert-di-tert-butyl gliserol dan 1,2,3 tri-tert-di-tert-butyl gliserol. Namun,
formasi 1,3-eter (ikatan pada –OH primer) lebih mungkin terbentuk dibanding 2 ,3 dan
1,2 eter (Klepacova et al., 2005).
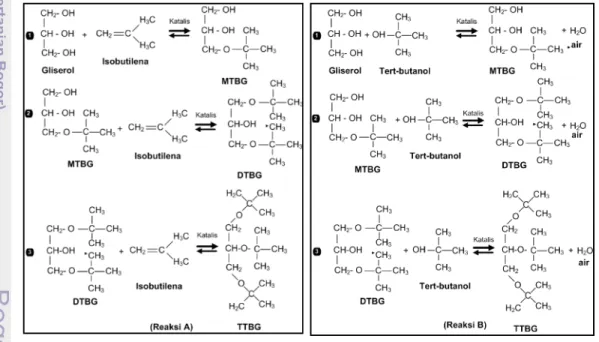
Gambar 4. Reaksi eterifikasi gliserol dengan butilena (reaksi A) dan eterifikasi gliserol dengan tert-butyl alkohol (reaksi B)
Reaksi eterifikasi gliserol dengan isobutilen akan menghasilkan mono-tert-butyl eter gliserol (MTBG). MTBG akan bereaksi kembali dengan isobutilen sehingga terbentuk di-tert-butyl eter gliserol (DTBG). DTBG akan bereaksi dengan isobut ilen dan membentuk tri-butyl eter gliserol (TTBG). Hasil eterifikasi gliserol dengan
tert-butyl alkohol (TBA) sama seperti eterifikasi gliserol dengan isobutilen, hanya saja pada
reaksi eterifikasi gliserol dengan TBA dihasilkan air.
Di- dan tri-tert-butyl eter gliserol dapat digunakan sebagai oxygenate additives
pada biodiesel yang sangat potensial karena kelarutannya dalam biodiesel.
Mono-tert-butyl eter gliserol (MTBG) mempunyai kelarutan yang rendah dalam biodiesel,
sehingga proses eterifikasi gli serol harus diarahkan untuk memaksimalkan formasi di-dan tri- eter (Klepacova et al., 2005). Katalis homogen (seperti asam sulfat, di-dan
p-toluene sulphonic acid ) dapat digunakan pada proses eterifikasi gliserol, namun lebih
disarankan untuk menggunakan kat alis heterogen yang ramah lingkungan yaitu resin penukar ion asam kuat (Klepacova et al., 2003).
Penambahan GTBE berpengaruh secara positif pada kualitas bahan bakar diesel, mengurangi partikulat emisi, komponen karbon pada gas buang (Kesling et al.,1994). Selain itu, GTBE jika ditambahkan ke dalam biodiesel dapat menurunkan titik kabut. Tingginya tingkat perubahan senyawa isobutilen tidak berpengaruh terhadap besarnya perubahan gliserol menjadi gliserol eter, melainkan jumlah isobutilen yang dikonsumsi untuk membentuk eter (Noureddini et al., 1998).
Tingkat konversi gliserol menjadi gli serol eter dipengaruhi oleh berbagai faktor, yaitu suhu, rasio mol n(IB)/n(G), air dan pengembangan gel serta tipe katalis pada reaksi eterifikasi. Konversi gliserol dan rendemen gliserol eter meningkat seiring dengan peningkatan rasio mol n(IB)/n(G). Kata lis dalam bentuk asam kuat, kering, makroretikular serta memiliki tingkat ikatan bercabang yang tinggi merupakan katalis aktif dalam reaksi eterifikasi karena memiliki pori -pori yang cukup besar sehingga gliserol eter yang terbentuk sangat besar. Reaksi et erifikasi gliserol dengan isobutilen dalam kondisi non-aqueous memberikan hasil terbaik pada rendemen eter (Pagliaro dan Rossi, 2008).
E. KUALITAS BIODIESEL PADA SUHU RENDAH
Karakteristik biodiesel pada suhu rendah merupakan sifat bahan bakar terhadap perubahan suhu yang menjadi hal yang sangat berpengaruh pada daerah -daerah yang memiliki iklim dingin atau daerah subtropis. Pada umumnya yang menjadi parameter pengukuran karakteristik tersebut diantaranya adalah : Titik Kabut (cloud point, CP), Titik Tuang (pour point, PP), Cold-Filter Pludging Point (CFPP), Low-Temperature
Flow Test (LTFT), dan Cristalization Onset Temperature (Tco) (Mittelbach dan
Seperti halnya bahan bakar solar yang merupakan fraksi minyak bumi, biodiesel juga akan menjadi berkabut ( cloudy) pada saat udara dingin, minyak akan berubah menjadi kristal lilin yang akan menyumbat saluran filter bahan bakar. Bila udara menjadi lebih dingin, mak a kristal lilin tersebut akan menjadi gel dan memadat sehingga
tidak dapat mengalir. Bahan bakar yang telah mengalami proses winterisasi
(penghilangan senyawa jenuh) atau bahan bakar dengan kualitas no mor 1 dapat digunakan pada udara yang lebih dingin ( Anonim, 2005).
Titik kabut adalah suhu dimana bahan bakar diesel pertama kali mengalami kristalisasi yang ditandai dengan timbulnya kabut pada bahan bakar diesel tesebut. Titik tuang adalah suhu dimana bahan bakar sudah tidak dapat mengalir jika wadah dimiringkan selama 5 detik (Noureddini, 1998).
Bergantung pada jenis minyak, biodiesel yang berasal dari minyak murni asli (virgin oil) memiliki titik tuang yang lebih rendah bila dibandingkan dengan biodiesel yang berasal dari minyak goreng bekas ( used cooking oil- waste vegetable oil), sehingga masih dapat digunakan dengan baik pada suhu beberapa derajat di bawah beku yaitu
sekitar -5oC. Biodiesel dari minyak goreng bekas mulai mengalami perubahan menjadi
gel pada suhu 4-5oC. Hal itu terjadi karena asam lemak minyak atau lemak jenuh telah
mengalami kritalisasi pada suhu yang lebih tinggi bila dibandingkan dengan asam lemak yang tidak jenuh, yang pada akhirnya akan memisah dan menyumbat saluran f ilter. Hal ini terjadi pada lemak babi, lemak domba dan minyak sawit (Anonim, 2005).
Molekul alkana (petrodiesel) dan FAME (biodiesel) memiliki rantai hidrokarbon lurus yang tidak cocok pada musim dingin, karena membentuk kristal padat yang menyumbat saluran filter dan mengganggu pompa bahan bakar. Namun biodiesel memiliki kecenderungan yang lebih kuat karena gugus esternya relatif bersifat polar sehingga meningkatkan gaya intermolekuler Van der Walls, sehingga secara efektif menguatkan proses kristalisasi. Angka setana (cetane number), panas pembakaran (heat
of combustion), titik cair dan titik didih, dan viskositas akan meningkat dengan
meningkatnya panjang rantai dan kejenuhan dan menurun dengan meningkatnya ketidakjenuhan asam lemak (Prakash, 1998).
III. METODOLOGI
A.
BAHAN DAN ALAT
Bahan-bahan yang digunakan pada penelitian ini adalah biodiesel CPO dan jarak
pagar, gliserol,
tert-butyl
alkohol (TBA), bentonit, zeolit, asam fosfat, HCl, alkohol,
aquades dan bahan kimia lainnya.
Peralatan yang dibutuhkan adalah timbangan, timer, hot plate, termometer,
stirrer, batang magnet, sudip, magnetic stirrer-heater, labu pemisah, erlenmeyer,
peralatan analisis seperti pH-meter, buret, spektrofotometer,
gas chromatography
mass spectrometry
(GC-MS), peralatan gelas dan pendukung lainnya.
Gambar 5. Reaktor eterifikasi gliserol
B.
METODE PENELITIAN
Penelitian ini dilakukan di laboratorium
Surfactant and Bioenergy Research
Center
(SBRC). Adapun tahapan penelitian yang dilakukan adalah sebagai berikut :
1.
Tahap Sintesis GTBE
Tahap ini diawali dengan aktivasi katalis yang akan digunakan yaitu bentonit
dengan cara aktivasi asam dengan menggunakan HCl. Metode aktivasi bentonit
disajikan pada Gambar 6.
Aktivasi bentonit dilakukan dengan mencampurkan 200 g bentonit dengan 400
ml HCl 16% ke dalam labu leher 4 yang dihubungkan dengan kondensor. Kondisi
reaksi diatur pada suhu 80°C selama 3 jam dengan pengadukan. Selanjutnya
dilakukan pemisahan dengan menggunakan saringan vakum. Bentonit yang telah
terpisah dengan HCl kemudian dicuci menggunakan aquades sampai pH-nya 3-4.
Bentonit kemudian dikeringkan menggunakan oven.
Mulai
Pemanasan dan
Pengadukan, 80°C, 3 jam
Pemisahan
HCl
Bentonit
Pencucian bentonit ± 5 kali, pH = 3,5-4,0Pengeringan dengan
oven,
110°C, 2 jam
Selesai
100-200 g
Bentonit
400 ml HCl 16%
Proses produksi GTBE (eterifikasi) dilakukan dengan mereaksikan gliserol
dengan
Tert-butyl
Alkohol (TBA) dengan perbandingan molar sebesar 1:6 dalam
labu leher 3 yang dihubungkan dengan kondensor. Bentonit yang telah diaktivasi
digunakan sebagai katalis. Zeolit 3
Åditambahkan sebagai pengikat air hasil
samping reaksi eterifikasi. Kondisi reaksi diatur pada suhu 60-80°C selama 6-8 jam
dengan pengadukan sebesar 400 rpm. Diagram alir proses sintesis GTBE disajikan
dalam
Gambar
7.
Selanjutnya
GTBE
dianalisis
menuggunakan
Gas
Chromatography-Mass Spectrometry
(GC-MS). Spesifikasi GC-MS dan metode
yang digunakan disajikan pada Lampiran 1.
Gambar 7. Diagram alir sintesis GTBE
2.
Optimasi Sintesis GTBE
Pada penelitian ini digunakan
central composite rotatable design
(CCRD)
tiga faktor. Variabel berubah yang dipilih dalam penelitian ini adalah
perbandingan waktu reaksi, suhu reaksi dan konsentrasi katalis. Parameter uji
untuk optimasi ini adalah konsentrasi GTBE yang dihasilkan. Kondisi optimum
yang diperoleh kemudian diverifikasi dengan menggunakan analisis GC-MS.
3.
Uji efektivitas GTBE
GTBE yang dihasilkan dari pada penelitian ini kemudian diuji
efektivitasnya dalam menurunkan titik kabut dan titik tuang biodiesel CPO dan
jarak. Uji ini dilakukan dengan mencampurkan GTBE ke dalam biodiesel CPO
dan jarak dengan perbandingan volume 1:10. Prosedur uji titik kabut dan titik
tuang disajikan pada Lampiran 2.
Gliserol : TBA (1:6) Eterifikasi 60-80°C, 6-8 jam, 400 rpm Zeolit 3Å 5% (b/b) Bentonit 2,5-7,5 % (b/b)
Analisis kandungan
GTBE dengan GC-MS
Gambar 8. Diagram pengujian efektivitas GTBE
C.
RANCANGAN PERCOBAAN
Rancangan percobaan optimasi sintesis gliserol
tert-butyl
eter (GTBE)
menggunakan rancangan
central composite rotatable design
yang merupakan salah
satu jenis metode permukaan respon (
Response Surface Methodology
). Faktor yang
dianalisis adalah waktu reaksi (X
1), suhu reaksi (X
2), dan konsentrasi katalis (X
3).
Batasan dan level yang digunakan untuk tiap variabel diberikan dalam Tabel 4.
Harga α (titik kritis) untuk desain rotatable adalah :
α = (F)
1/4... (1)
dimana F=2
k, k merupakan jumlah faktor (variabel). Karena dalam penelitian ini
terdapat tiga variabel, maka nilai F = 8, sehingga dari persamaan (1) didapatkan
α =
1.68
Tabel 4. Batasan dan level berubah
Variabel (X)
Batasan dan Level
- α =
1,68
-1
0
+1
+ α =
1,68
Waktu reaksi (jam)
4,64
6
8
10
11,46
Suhu Reaksi (ºC)
53,18
60
70
80
86,82
Konsentrasi bentonit (% b/w)
0,80
2,5
5
7,5
9,20
Tabel 5. Rancangan percobaan
Run Kode
Faktor terkode Faktor tak terkode
X1 X2 X3 Waktu (jam) Suhu (°C) Katalis (% b/b) 1 W1T1K1 −1 −1 −1 6 60 2.5 2 W3T1K1 1 −1 −1 10 60 2.5 3 W1T3K1 −1 1 −1 6 80 2.5 4 W3T3K1 1 1 −1 10 80 2.5 5 W1T1K3 −1 −1 1 6 60 7.5 6 W3T1K3 1 −1 1 10 60 7.5 7 W1T3K3 −1 1 1 6 80 7.5 8 W3T3K3 1 1 1 10 80 7.5 9 W4T2K2 −1,68 0 0 4,64 70 5 10 W5T2K2 1,68 0 0 11,36 70 5 11 W2T4K2 0 −1,68 0 8 53,18 5 12 W2T5K2 0 1,68 0 8 86,82 5 13 W2T2K4 0 0 −1,68 8 70 0,80 14 W2T2K5 0 0 1,68 8 70 9,20 15 W2T2K2 A 0 0 0 8 70 5 16 W2T2K2 B 0 0 0 8 70 5 17 W2T2K2 C 0 0 0 8 70 5
Model orde kedua yang bisa digunakan adalah sebagai berikut :
Dimana :
Y
:
Response
β
ij:
Interaction term
β
0:
Offset term
x
i:
Coded level
untuk faktor i
β
i:
Linear term
x
j:
Coded level
untuk faktor j
β
ii:
Squared term
IV. HASIL DAN PEMBAHASAN
A. Sintesis Gliserol Tert-butyl Eter (GTBE)
Gliserol tert-butyl eter (GTBE) disintesis melalui proses eterifikasi antara gliserol dengan tert-butyl alkohol (TBA) ataupun dengan isobutilen . GTBE pertama kali disintesis oleh Malinavskii dan Vedenskii pada tahun 1950. Malinavskii dan Vedenskii memanaskan gliserol dengan TBA dengan ditambahkan asam sulfat dan menghasilkan
mono-tert-butyl eter gliserol.
Selain dengan katalis homogen seperti asam sulfat, katalis heterogen juga dap at digunakan dalam mensintesis GTBE. Penggunaan katalis heterogen lebih disenangi daripada katalis homogen karena lebih ramah lingkungan dan dapat diperbarui. Katalis heterogen yang sering digunakan adalah katalis resin asam kuat penukar ion, seperti
Amberlist.
Amberlist adalah katalis resin yang umum digunakan dalam reaksi eterifikasi
untuk mesitesis aditif bahan bakar, misalnya Metyl Tert-Butyl Eter (MTBE). Amberlist
merupakan polimer bahan organik yang mengandung gugus aktif SO3H+. Amberlist
memiliki pori-pori yang lebar dan kapasitas tukar ion yang tinggi, sehingga baik digunakan sebagai katalis.
Selain menggunakan Amberlist, GTBE dapat disintesis menggunakan katalis heterogen lain seperti zeolit ( Klepacova et al., 2005). Penggunaan zeolit sebagai kat alis dalam reaksi eterifikasi gliserol kurang begitu baik, karena formasi tri- eter susah terbentuk. Amberlist mempunyai pori-pori yang lebih besar daripada zeolit, sehingga GTBE yang terbentuk lebih ba nyak, terutama formasi di- dan tri- eter.
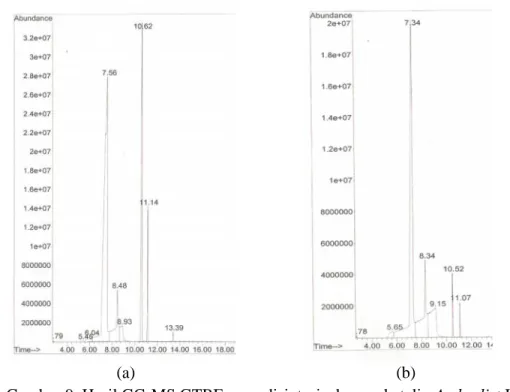
Setyaningsih et al. (2008) melakukan penelitian mengenai sintesis gliserol eter menggunakan berbagai katalis lokal. Katalis yang digunakan adalah bentonit alam, silika, dan alumina teraktivasi asam, serta Amberlist IR 120 sebagai pembanding. Dari ketiga katalis lokal yang diuji, ternyata bentonit yang paling mendekati Amberlist IR 120. Dari penelitian tersebut juga terlihat bahwa pada sintesis GTBE menggunakan katalis bentonit dengan perbandingan molar antara gliserol dengan TBA sebesar 1:6 lebih efektif dibandingkan 1:4. Gambar 9 menunjukkan perbandingan GTBE hasil sintesis menggunakan katalis Amberlist IR 120 dan bentonit alam teraktivasi.
(a) (b)
Gambar 9. Hasil GC-MS GTBE yang disintesis dengan katalis Amberlist IR 120 (a) dan bentonit alam teraktivasi (b)
Bentonit yang telah diaktivasi dengan asam akan mengalami perubahan.
Perubahan tersebut antara lain adalah luas permukaan yang semakin bertambah, memperbesar pori-pori dan juga merubah keasaman bentonit. Aktivasi asam juga mengakibatkan terjadinya pertukaraan ion -ion seperti Ca, K, dan Na dengan ion H. Aktivasi asam menjadikan bentonit dapat digunakan sebagai katalis pada sintesis GTBE karena perubaha n-perubahan tersebut. Hal ini dikarenakan aktivasi akan membuat struktur permukaan bentonit lebih berpori dengan menghilangkan sisa pengotor mineral yang tidak dapat hilang selama proses pemurnian. Larutan asam
dengan konsentrasi yang cukup besar mampu menggantikan ion K+, Na+, dan Ca2+
dengan H+ serta melepaskan ion Al3+, Fe3+, dan Mg2+, sehingga meningkatkan daya
adsorpsi bentonit (Nurliana, 2006 dalam Firdaus, 2009). Perubahan-perubahan tersebut disajikan dalam Tabel 6.
Tabel 6. Karakteristik bentonit
Karakteristik Bentonit alam Bentonit teraktivasi
pH 8,1A 3,2A
Luas permukaan (m2/g) 64,7A 267,5A
Warna Putih kecokelatan Putih kekuningan
Kehalusan Halus Agak kasar
A
Al-Zahrani et al. (2000)
(a) (b)
Gambar 9. Hasil GC-MS GTBE yang disintesis dengan katalis Amberlist IR 120 (a) dan bentonit alam teraktivasi (b)
Bentonit yang telah diaktivasi dengan asam akan mengalami perubahan.
Perubahan tersebut antara lain adalah luas permukaan yang semakin bertambah, memperbesar pori-pori dan juga merubah keasaman bentonit. Aktivasi asam juga mengakibatkan terjadinya pertukaraan ion -ion seperti Ca, K, dan Na dengan ion H. Aktivasi asam menjadikan bentonit dapat digunakan sebagai katalis pada sintesis GTBE karena perubaha n-perubahan tersebut. Hal ini dikarenakan aktivasi akan membuat struktur permukaan bentonit lebih berpori dengan menghilangkan sisa pengotor mineral yang tidak dapat hilang selama proses pemurnian. Larutan asam
dengan konsentrasi yang cukup besar mampu menggantikan ion K+, Na+, dan Ca2+
dengan H+ serta melepaskan ion Al3+, Fe3+, dan Mg2+, sehingga meningkatkan daya
adsorpsi bentonit (Nurliana, 2006 dalam Firdaus, 2009). Perubahan-perubahan tersebut disajikan dalam Tabel 6.
Tabel 6. Karakteristik bentonit
Karakteristik Bentonit alam Bentonit teraktivasi
pH 8,1A 3,2A
Luas permukaan (m2/g) 64,7A 267,5A
Warna Putih kecokelatan Putih kekuningan
Kehalusan Halus Agak kasar
A
Al-Zahrani et al. (2000)
(a) (b)
Gambar 9. Hasil GC-MS GTBE yang disintesis dengan katalis Amberlist IR 120 (a) dan bentonit alam teraktivasi (b)
Bentonit yang telah diaktivasi dengan asam akan mengalami perubahan.
Perubahan tersebut antara lain adalah luas permukaan yang semakin bertambah, memperbesar pori-pori dan juga merubah keasaman bentonit. Aktivasi asam juga mengakibatkan terjadinya pertukaraan ion -ion seperti Ca, K, dan Na dengan ion H. Aktivasi asam menjadikan bentonit dapat digunakan sebagai katalis pada sintesis GTBE karena perubaha n-perubahan tersebut. Hal ini dikarenakan aktivasi akan membuat struktur permukaan bentonit lebih berpori dengan menghilangkan sisa pengotor mineral yang tidak dapat hilang selama proses pemurnian. Larutan asam
dengan konsentrasi yang cukup besar mampu menggantikan ion K+, Na+, dan Ca2+
dengan H+ serta melepaskan ion Al3+, Fe3+, dan Mg2+, sehingga meningkatkan daya
adsorpsi bentonit (Nurliana, 2006 dalam Firdaus, 2009). Perubahan-perubahan tersebut disajikan dalam Tabel 6.
Tabel 6. Karakteristik bentonit
Karakteristik Bentonit alam Bentonit teraktivasi
pH 8,1A 3,2A
Luas permukaan (m2/g) 64,7A 267,5A
Warna Putih kecokelatan Putih kekuningan
Kehalusan Halus Agak kasar
A
Gambar 10. Foto bentonit alam (A) dan bentonit teraktivasi (B)
Ketaren (1986) menjelaskan bahwa aktivasi menggunakan asam mineral akan menimbulkan tiga macam reaksi sebagai berikut :
1. Mula-mula asam akan melarutkan komponen Fe2O3, Al2O3, CaO, dan MgO yang
mengisi pori-pori adsorben. Proses ini menyeba bkan terbukanya pori-pori yang tertutup sehingga menambah luas permukaan adsorben.
2. Kemudian ion-ion Ca2+ dan Mg2+ yang berada pada permukaan kristal adsorben
secara berangsur-angsur digantikan oleh ion H+dari asam mineral.
3. Sebagian ion H+yang telah menggantikan ion Ca2+dan Mg2+akan ditukar oleh ion
Al3+yang telah larut dalam larutan asam.
Reaksi eterifikasi gliserol dengan TBA akan menghasilkan air, sedangkan air akan mengganggu reaksi eterifikasi gliserol . Hal ini dikarenakan reaksi eterifikasi
gliserol merupakan reaksi bolak balik sehingga GTBE yang terbentuk dapat
terhidrolisis kembali. Oleh karena itu air tersebut harus diminimalisir agar reaksi eterifikasi tidak terganggu. Untuk megatasi hal tersebut maka pada penelitian ini digunakan zeolit 3 Å guna menyerap air hasil samping reaksi eterifikasi. Jika zeolit tidak ditambahkan, air hasil samping eterifikasi akan diadsorb oleh bentonit sehingga akan menutupi pori-pori bentonit sehingga gliserol dan TBA tidak dapat masuk dan reaksi eterifikasi akan terhambat.
Zeolit mempunyai pori -pori seperti halnya pada bentonit. Pori-pori ini
menyebabkan zeolit memiliki sifat sebagai adsorben. Pada zeolit alam ukuran pori -pori ini bervariasi, namun pada zeolit sintetis ukuran pori -pori ini dapat dibuat seragam. Pada penelitian ini digunakan zeolit dengan ukuran pori 3 Å. Hal ini bertujuan agar
B
molekul-molekul yang berukuran kurang dari 3 Å dapat diserap oleh zeolit , misalnya air yang mempunyai ukuran molekul 2,8 Å.
Reaksi eterifikasi terjadi karena molekul gliserol dan TBA diadsorpsi oleh bentonit sehingga masuk ke d alam pori-pori bentonit. Di dalam pori -pori tersebut kemudian gliserol dan TBA bereaksi sehingga terbentuk GTBE. Setelah GTBE terbentuk, GTBE akan dilepas bentonit karena terjadi proses desorbsi. Desorpsi adalah proses penjerapan yang arahnya keluar fasa. Karena terjadi desorpsi, pori-pori bentonit akan kosong kembali sehingga bentonit dapat mengadsorpsi gliserol dan TBA lagi sehingga terbentuk GTBE. Jika terdapat air, gliserol dan TBA susah masuk ke dalam pori-pori bentonit karena air lebih mudah diadsorb dibandingkan gliserol. Terjadinya adsorpis dan desorpsi dikarenakan adanya perbedaan konsentrasi di dalam pori -pori bentonit dengan di luar pori -pori bentonit. Substrat akan bergerak dari konsentrasi tinggi ke konsentrasi rendah. Saat adsorpsi terjadi, gli serol dan TBA akan bergerak ke dalam pori-pori bentonit. Saat desorpsi terjadi, GTBE yang telah terbentuk ke luar dari pori-pori bentonit.
Hasil sintesis GTBE selanjutnya dianalisis menggunakan Gas
Chromotography-Mass Spectroscopy (GC-MS). Hasil dari analisis ini disajikan pada Lampiran 3. Dari
hasil tersebut terlihat bahwa proses yang dilakukan berhasil mensitesis senyawa gliserol tert-butyl eter. GTBE yang terbentuk berupa mono-tert-butyl eter gliserol (MTBG), di-tert-butyl eter gliserol (DTBG), dan tri-tert-butyl eter gliserol (TTBG).
Eterifikasi gliserol (O-alkylation) dengan menggunakan katalis asam akan menghasilkan formasi mono-, di-, dan tri-tert-butyl eter gliserol. Struktur gliserol eter sebagai bahan aditif dapat berupa 1,3 tert-butyl eter gliserol atau perpaduan 2,3
di-tert-butyl eter gliserol dengan 1,2 di-di-tert-butyl eter gliserol dan 1,2,3 tri-di-tert-butyl eter
gliserol. Klepacova et al. (2005), menyebutkan bahwa proses eterifikasi pada gliserol cenderung terjadi pada gugus hidroksil primer (formasi 1 -tert-butyl gliserol dan
1,3-di-tert-butyl gliserol).
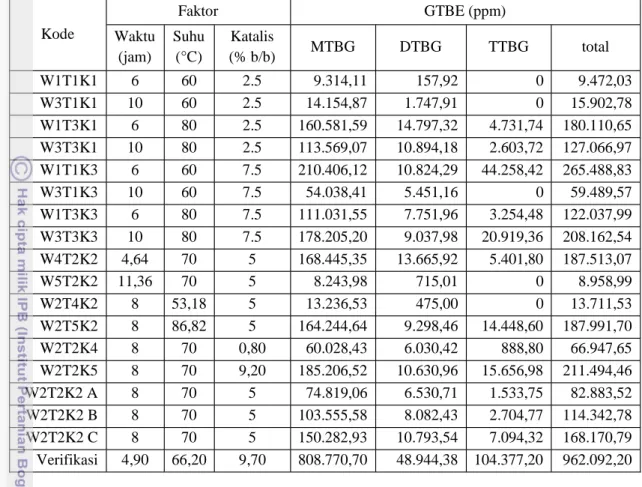
Dari hasil GC-MS dapat diketahui konsentrasi GTBE yang terbentuk. Konsentrasi GTBE dihitung dengan cara membandingkan luas area peak GTBE dengan luas area standar yang telah diketahui konsentrasinya. Untuk mengetahui konsentrasi GTBE yang terbentuk, gliserol dipakai seb agai standar. Konsentrasi GTBE yang terbentuk disajikan pada Tabel 7.
Tabel 7. Data hasil sintesis GTBE Kode Faktor GTBE (ppm) Waktu (jam) Suhu (°C) Katalis (% b/b) MTBG DTBG TTBG total W1T1K1 6 60 2.5 9.314,11 157,92 0 9.472,03 W3T1K1 10 60 2.5 14.154,87 1.747,91 0 15.902,78 W1T3K1 6 80 2.5 160.581,59 14.797,32 4.731,74 180.110,65 W3T3K1 10 80 2.5 113.569,07 10.894,18 2.603,72 127.066,97 W1T1K3 6 60 7.5 210.406,12 10.824,29 44.258,42 265.488,83 W3T1K3 10 60 7.5 54.038,41 5.451,16 0 59.489,57 W1T3K3 6 80 7.5 111.031,55 7.751,96 3.254,48 122.037,99 W3T3K3 10 80 7.5 178.205,20 9.037,98 20.919,36 208.162,54 W4T2K2 4,64 70 5 168.445,35 13.665,92 5.401,80 187.513,07 W5T2K2 11,36 70 5 8.243,98 715,01 0 8.958,99 W2T4K2 8 53,18 5 13.236,53 475,00 0 13.711,53 W2T5K2 8 86,82 5 164.244,64 9.298,46 14.448,60 187.991,70 W2T2K4 8 70 0,80 60.028,43 6.030,42 888,80 66.947,65 W2T2K5 8 70 9,20 185.206,52 10.630,96 15.656,98 211.494,46 W2T2K2 A 8 70 5 74.819,06 6.530,71 1.533,75 82.883,52 W2T2K2 B 8 70 5 103.555,58 8.082,43 2.704,77 114.342,78 W2T2K2 C 8 70 5 150.282,93 10.793,54 7.094,32 168.170,79 Verifikasi 4,90 66,20 9,70 808.770,70 48.944,38 104.377,20 962.092,20
Dari Tabel 7 terlihat bahwa GTBE yang dominan terbentuk adalah
mono-tert-butyl eter gliserol (MTBG). Hal ini terjadi karena pori -pori bentonit yang ukurannya
relatif kecil sehingga molekul -molekul di-tert-butyl eter gliserol (DTBG) dan
tri-tert-butyl eter gliserol (TTBG) yang ukuran molekulnya lebih besar dari MTBG susah
terbentuk. Adanya air dalam reaksi eterifikasi juga menghambat terbentuknya DTBG dan TTBG. Hal ini dijelaskan oleh Klepacova et al. (2005) yang menerangkan bahwa adanya air akan menghalangi gliserol memasuki daerah permukaan inti katalis atau menghalangi reaksi pembentukan molekul gliserol eter yang mempunyai ukuran molekul lebih besar sehingga reaksi berjalan sangat lambat atau reaksi terjadi di daerah permukaan katalis.
B. Analisis Response Surface Methodology (RSM)
Analisis yang bertujuan untuk mendapa tkan kondisi optimum pada umumya meggunakan metode permukaan respons ( response surface methodology ). Penggunaan metode permukaan respon pada penelitian ini diharapkan dapat menentukan fungsi yang tepat untuk meramalkan respon yang diinginkan dan dapat mengurangi jumlah
percobaan yang dilakukan. Respon yang akan dioptimalkan adalah konsentrasi gliserol
tert-butyl eter (GTBE) sedangkan faktor-faktor yang dikaji adalah waktu reaksi, suhu
reaksi dan konsentrasi katalis.
Faktor waktu reaksi (X1) yang dikaji adalah pada kisaran 4,64 – 11,36 jam.
Faktor suhu reaksi (X2) yang dikaji adalah pada kisaran 53,18– 86,82 ºC. Sedangkan
faktor konsentrasi katalis (X3) yang dikaji adalah pada kisaran 0,80–9,20% (b/b).
Hasil analisis ragam (ANOVA) dengan menggunakan software Design Expert 7.1.6 (free trial) disajikan pada Lampiran 4. Analisis ragam dari model kuadratik yang dipilih mempunyai nilai F hitung 2,7067 dan nilai p = 0,1014; waktu reaksi mempunyai nilai F hitung 4,6743 dan nilai p = 0,0647; suhu reaksi mempunyai F hi tung sebesar 7,2200 dan nilai p = 0,0312; dan konsentrasi katalis mempuyai nilai F hitung sebesar 6,8659 dan nilai p = 0,0344. Nilai p < 0,05 menunjukkan pengaruh signifikan pada respon pada tingkat kepercayaan 95 %. Hal ini menunjukkan bahwa suhu reaksi dan konsentrasi katalis berpengaruh signifikan terhadap respon. Model dan waktu reaksi tidak berpengaruh signifikan terhadap respon. Model yang tidak signifikan terjadi
karena data yang didapatkan kurang menyebar secara normal. Nilai R2 dari data
tersebut adalah 0,77. Nilai R2 ini menandakan data menyebar mengikuti sebaran
normal sebesar 77%.
Analisa normalitas data konsentrasi GTBE disajikan pada Lampiran 5. Hasil grafik plot residual menunjukkan data menyebar kurang mengikuti sebaran normal. Metode Box Cox digunakan untuk mengetahui transformasi data yang sesuai. Hasil pengujian Box Cox menunjukkan lamda terbaik adalah sebesar 0,46, maka data harus ditransformasikan dengan square root (akar kuadrat) untuk menggeser nilai lamda pada 0,5 yang mendekati lamda terbaiknya . Data hasil transformasi disajik an pada Tabel 7. Melalui transformasi diharapkan kestabilan ragam akan terpenuhi dan data menyebar
mengikuti sebaran normal (Mattjik dan Sumertajaya, 2002). Transformasi data
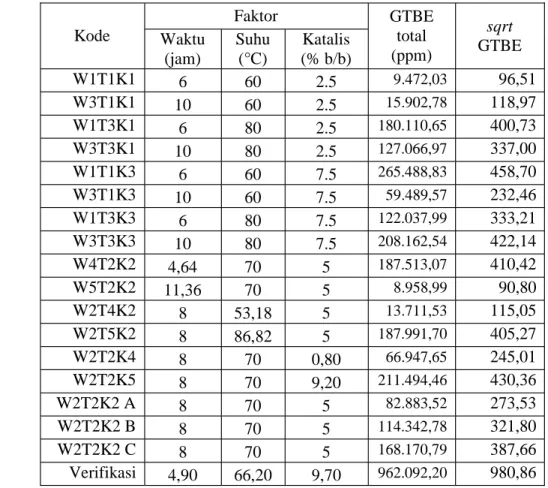
Tabel 8. Hasil transformasi data konsentrasi GTBE Kode Faktor GTBE total (ppm) sqrt GTBE Waktu (jam) Suhu (°C) Katalis (% b/b) W1T1K1 6 60 2.5 9.472,03 96,51 W3T1K1 10 60 2.5 15.902,78 118,97 W1T3K1 6 80 2.5 180.110,65 400,73 W3T3K1 10 80 2.5 127.066,97 337,00 W1T1K3 6 60 7.5 265.488,83 458,70 W3T1K3 10 60 7.5 59.489,57 232,46 W1T3K3 6 80 7.5 122.037,99 333,21 W3T3K3 10 80 7.5 208.162,54 422,14 W4T2K2 4,64 70 5 187.513,07 410,42 W5T2K2 11,36 70 5 8.958,99 90,80 W2T4K2 8 53,18 5 13.711,53 115,05 W2T5K2 8 86,82 5 187.991,70 405,27 W2T2K4 8 70 0,80 66.947,65 245,01 W2T2K5 8 70 9,20 211.494,46 430,36 W2T2K2 A 8 70 5 82.883,52 273,53 W2T2K2 B 8 70 5 114.342,78 321,80 W2T2K2 C 8 70 5 168.170,79 387,66 Verifikasi 4,90 66,20 9,70 962.092,20 980,86
Data hasil transformasi kemudian dijadikan input data. Hasil analisis ragam data yang telah ditransformasi disajikan pada Lampiran 6. Hasil analisis tersebut menunjukkan model kuadratik yang dipilih mempunyai F hitung sebesar 3,4312 dan nilai p = 0,05191; waktu reaksi mempunyai nilai F hitung sebesar 5,2893 dan nilai p = 0,0550; suhu reaksi mempunyai ni lai F hitung sebesar 11,4355 dan nilai p = 0,0117; dan konsentrasi katalis mempunyai nilai F hitung sebesar 7,1561 dan p = 0,0318 . Nilai p < 0,05 menunjukkan pengaruh signifikan pada res pon pada tingkat kepercayaan 95 %. Hal ini menunjukkan bahwa suhu reaksi dan konsentrasi katalis berpengaruh signifikan terhadap respon. Model dan waktu reaksi tidak berpengaruh signifikan terhadap respon. Model persamaan kuadratik yang dihasilkan adalah sebagai berikut :
Sqrt (Y) = 343.8021909 - 56.5773333 X1+ 83.1901288 X2+ 65.8086841 X3+
35.1935542 X1X2-15.6617795 X1X3-63.8752049 X2X3
Dengan sqrt (Y) adalah nilai akar kuadrat dari GTBE; X1 adalah waktu reaksi; X2
adalah suhu reaksi; dan X3adalah konsentrasi katalis.
1. Analisis Pengaruh Faktor
Noureddini et al. (1998) menyatakan bahwa reaksi eterifikasi gliserol dengan isobutilen dipengaruhi oleh kemurnian gliserol, rasio mol gliserol dengan mol isobutilen, waktu reaksi, suhu reaksi, serta jenis dan jumlah katalis.
Waktu Reaksi
Hasil analisis ragam menunjukkan bahwa pada rentang waktu 4,6 4 - 11,36 jam, waktu reaksi tidak berpengaruh signifikan terhadap respon. Profil waktu reaksi terhadap besaran konsentr asi GTBE disajikan pada Gambar 11.
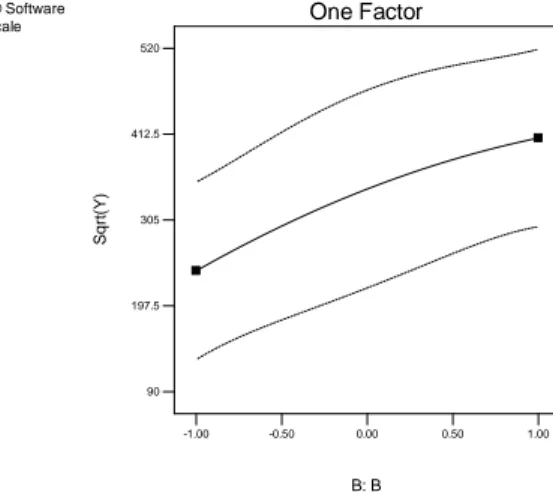
Gambar 11. Plot pengaruh waktu reaksi terhadap sqrt GTBE
Gambar 11 menunjukkan bahwa peningkatan waktu reaksi (pada suhu 70°C dan konsentrasi katalis 5%) mulai 6 jam sampai 10 jam menunjukkan penurunan konsentrasi GTBE pada waktu reaksi yang paling lama. Dari analisis ragam terlihat bahwa koefisien parameter waktu reaksi menunjukkan nilai negatif. Hal ini berarti
waktu reaksi berpengaruh negatif terhadap nilai sqrt GTBE atau dengan
peningkatan waktu reaksi, konsentrasi GTBE semakin menurun karena nilai sqrt GTBE berbanding lurus dengan konsentrasi GTBE. Konsentrasi GTBE yang semakin menurun seiring bertambahnya waktu dikarenakan reaksi eterifikasi GTBE adalah reaksi bolak-balik sehingga kemungkinan GTBE yang terbentuk akan terhidrolisis kembali oleh air yang tidak terikat oleh zeolit sehingga semak in lama reaksi berlangsung kons entrasi GTBE akan semakin menurun.
Design-Expert® Software Transformed Scale Sqrt(Y) X1 = A: A Actual Factors B: B = 0.00 C: C = 0.00 -1.00 -0.50 0.00 0.50 1.00 90 197.5 305 412.5 520 A: A S q rt (Y ) One Factor
Suhu Reaksi
Hasil analisis ragam menunjukkan bahwa pada rentang suhu 53.18 –
86.82°C suhu reaksi berpengaruh signifikan terhdap respon. Nilai koefisien yang positif menunjukkan bahwa suhu berpengaruh positif terhadap konsentrasi GTBE yang terbentuk. Semakin tinggi suhu reaksi maka ko nsentrasi GTBE yang terbentuk semakin tinggi. Gambar 1 2 menunjukkan pengaruh kenaikan suhu dengan waktu reaksi dan konsentrasi yang tetap terhadap sqrt GTBE.
Klepacova et al. (2005) menyatakan bahwa laju reaksi eterifikasi gliserol berbanding lurus dengan suhu reaksi, semakin tinggi suhu maka laju reaksi semakin
tinggi, sehingga GTBE yang terbentuk semakin banyak. Kenaikan suhu
mempengaruhi tenaga kinetis yang dimiliki oleh molekul -molekul zat pereaksi sehingga semakin besar hasil reaksinya. Dengan demikian semakin banyak molekul-molekul yang memiliki energi pengaktif, s emakin banyak tumbukan antar molekul yang berlanjut dengan reaksi. Sykes ( 1989) dalam Anwar (2008) menyatakan bahwa kecepatan reaksi berbanding lurus dengan jumlah tumbukan yang terjadi di antara molekul -molekul zat yang melakukan reaksi.
Gambar 12. Plot pengaruh suhu reaksi terhadap sqrt GTBE Konsentrasi Katalis
Hasil analisis ragam menunjukkan bahwa konsentrasi katalis pada rentang
0,80– 9,20% (b/b) berpengaruh secara signifikan terhadap sqrt GTBE pada selang
kepercayaan 95%. Nilai koefisien yang positif menunjukkan pengaruh konsentrasi katalis terhadap konsentasi GTBE juga positif. Semakin besar konsentrasi katalis yang dipakai, maka semakin tinggi konsentrasi GTBE yang terbentuk. Gambar 1 3
Design-Expert® Software Transformed Scale Sqrt(Y) X1 = B: B Actual Factors A: A = 0.00 C: C = 0.00 -1.00 -0.50 0.00 0.50 1.00 90 197.5 305 412.5 520 B: B S q rt (Y ) One Factor
menunjukkan pengaruh penambahan k onsentrasi katalis terhadap sqrt GTBE dengan waktu dan suhu reaksi yang tetap.
Klepacova et al. (2005), menyatakan penggunaan katalis sebesa r 7,5% (b/b) menghasilkan konsentrasi GTBE tertinggi pada etrifikasi gliserol dengan isobutilen. Semakin banyak katalis yang digunakan akan menyebabkan luas permukaan katalis yang semakin besar . Luas permukaan yang besar mengakibatkan lebih banyak katalis yang kontak dengan larutan sehingga proses reaksi eterifikasi yang menghasilkna GTBE akan lebih banyak terjadi.
Gambar 13. Plot pengaruh konsentrasi katalis terhadap sqrt GTBE Interaksi antar Faktor
Analisis ragam yang disajikan pada Lampiran 6 menunjukkan bahwa tidak ada interaksi antar faktor yang berpengaruh signifikan terhadap respon. Gambar interaksi antar faktor disajikan pada Gambar 13-15.
Gambar 14. Plot pengaruh interaksi suhu dan waktu reaksi terhadap sqrt GTBE
Design-Expert® Software Transformed Scale Sqrt(Y) X1 = C: C Actual Factors A: A = 0.00 B: B = 0.00 -1.00 -0.50 0.00 0.50 1.00 90 200.272 310.544 420.816 531.088 C: C S q rt (Y ) One Factor Design-Expert® Software Transformed Scale Sqrt(Y) B- -1.000 B+ 1.000 X1 = A: A X2 = B: B Actual Factor C: C = 0.00 B: B -1.00 -0.50 0.00 0.50 1.00 Interaction A: A S q rt (Y ) -6.39813 129.731 265.86 401.989 538.118
Dari Gambar 14 terlihat bahwa pada suhu reaksi rendah (60°C), perubahan waktu reaksi memberikan efek negatif terhadap konsentrasi GTBE yang dihasilkan. Hal ini ditandai dengan grafik yang menurun seiring bertambahnya waktu reaksi dengan suhu reaksi tetap. Pada suhu reaksi tinggi (80°C), perubahan waktu reaksi juga memberikan pengaruh negatif terhadap konsentrasi GTBE y ang dihasilkan, namun penurunannya tidak sebesar pada suhu reaksi rendah. Hal ini terlihat dari grafik yang relatif datar.
Gambar 15. Plot pengaruh interaksi waktu dan konsentrasi katalis terhadap
sqrt GTBE
Dari Gambar 15 terlihat bahwa pada konsentrasi katalis rendah (2,5 %), waktu reaksi berpengaruh negatif terhadap konsentrasi GTBE yang dihasilkan. Hal ini terlihat dari grafik yang menurun seiring bertambahnya waktu reaksi eterifikasi, namun penurunan ini tidak terlalu curam. Pada konsentrasi katalis tinggi (7 ,5 %), waktu reaksi juga berpengaruh negatif terhadap konsentrasi GTBE yang dihasilkan. Hal ini terlihat dari grafik yang menurun curam seiring bertambahnya waktu reaksi.
Design-Expert® Software Transformed Scale Sqrt(Y) C- -1.000 C+ 1.000 X1 = A: A X2 = C: C Actual Factor B: B = 0.00 C: C -1.00 -0.50 0.00 0.50 1.00 Interaction A: A S q rt (Y ) 90 217.82 345.641 473.461 601.282
Gambar 16. Plot pengaruh interaksi suhu dan konsentrasi katalis terhadap sqrt GTBE
Dari Gambar 16 terlihat bahwa pada konsentrasi katalis rendah (2,5 %), suhu reaksi berpengaruh positif terhadap konsentrasi GTBE yang dihasilkan. Hal ini terlihat dari grafik yang meningkat tajam seiring bertambahnya waktu reaksi eterifikasi. Pada konsentrasi katalis tinggi (7,5 %), waktu reaksi juga berpengaruh positif terhadap konsentrasi GTBE, namun peningkatan nya relatif kecil. Hal ini ditandai dengan grafik yang meningkat secara landai.
2. Optimasi konsentrasi GTBE
Optimasi konsentrasi GTBE menggunakan Response Surface Methodology (RSM) dengan faktor yang dikaji adalah waktu reaksi, suhu reaksi dan konsentrasi katalis. Nilai konsentrasi gliserol tert-butyl eter (GTBE) dari hasil sintesis disajikan pada Tabel 7. Konsentrasi GTBE yang diperoleh berkisar antara 8.958,99 ppm sampai 265.488,83 ppm. Nilai konsentrasi GTBE terendah adalah 8 .958,99 ppm dihasilkan pada saat waktu reaksi 11,364 jam dengan suhu reaksi 70°C dan konsentrasi katalis yang ditambahkan sebanyak 5 % (b/b). Nilai GTBE tertinggi adalah 265.488,83 ppm didapatkan pada saat reaksi berlangsung selama 6 jam dengan suhu reaksi sebesar 60°C dan konsentrasi katalis yang ditambahkan sebanyak 7,5 % (b/b). Grafik permukaan respon dan kontur dari hubungan antar faktor disajikan pada Gambar 17 - 22.
Design-Expert® Software Transformed Scale Sqrt(Y) C- -1.000 C+ 1.000 X1 = B: B X2 = C: C Actual Factor A: A = 0.00 C: C -1.00 -0.50 0.00 0.50 1.00 Interaction B: B S q rt (Y ) -10.556 130.189 270.934 411.678 552.423
Gambar 17. Grafik permukaan respon sqrt GBTE sebagai fungsi dari faktor waktu dan suhu reaksi
Gambar 18. Kontur sqrt GBTE dengan faktor waktu dan suhu reaksi Gambar 17 menunjukkan hubungan waktu reaksi dengan suhu reaksi terhadap respon sqrt GTBE. Gambar 18 menunjukkan kontur dari sqrt GTBE dengan faktor waktu dan suhu reaksi. Dari grafik permukaan respon dan kontur terlihat bahwa
sqrt GTBE tidak mencapai titik optimal pada selang waktu 4,6 4 – 11,26 jam dan
selang suhu 53,18°C – 86,82°C. Kemungkinan titik optimum tercapai pada selang
waktu 4,64 – 6 jam. Hal ini terlihat dari nilai sqrt GTBE tertinggi tercapai pada
rentang waktu reaksi tersebut.
Design-Expert® Software Transformed Scale Sqrt(Y) 515.256 94.6519 X1 = A: Waktu X2 = B: Suhu Actual Factor C: Konsentrasi Katalis = 0.00 -1.68 -0.84 0.00 0.84 1.68 -1.68 -0.84 0.00 0.84 1.68 -120 17.5 155 292.5 430 S q rt (Y ) A: W aktu B: Suhu Design-Expert® Software Transformed Scale Sqrt(Y) Design Points 515.256 94.6519 X1 = A: Waktu X2 = B: Suhu Actual Factor C: Konsentrasi Katalis = 0.00 -2.00 -1.00 0.00 1.00 2.00 -2.00 -1.00 0.00 1.00 2.00 Sqrt(Y) A: Waktu B : S u h u 264.815 305.610 346.405 346.405 387.201 427.996 3