BAB 2
TINJAUAN KEPUSTAKAAN
2.1. Metabolisme Besi
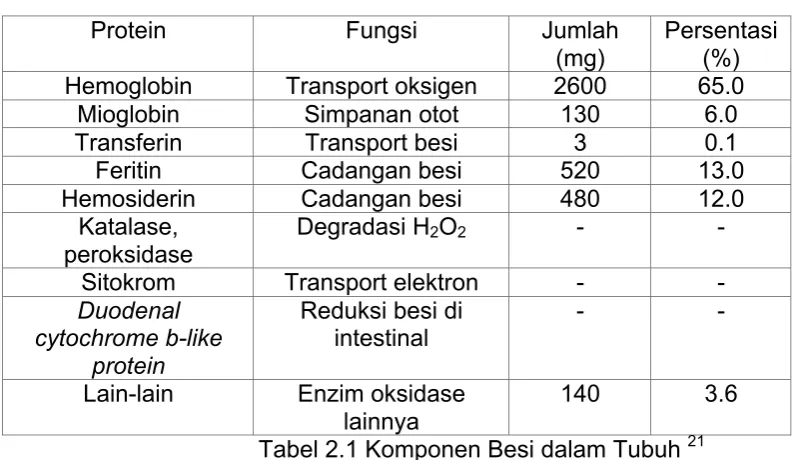
2.1.1. Komposisi Besi dalam Tubuh
Besi merupakan mineral penting bagi semua sel tubuh manusia.
Kemampuan besi untuk berubah pada reaksi oksidasi stabil, yaitu Fe2+
dan Fe3+, dalam kondisi fisiologis membuatnya ideal untuk reaksi katalisis
biokimia dan sejumlah besar enzim tergantung pada besi untuk fungsi
biologis mereka. Dampak negatifnya adalah logam ini mampu
mengkatalisis reaksi yang mengarah ke produksi radikal bebas, terutama
ketika berada dalam jumlah yang berlebihan.
Sangatlah penting untuk memasok zat besi yang cukup untuk
memenuhi persyaratan metabolisme sel, tetapi juga penting untuk
mencegah kelebihan zat besi karena hal ini dapat menempatkan sel di
bawah tekanan stress oksidatif.18 Pada orang dewasa, jumlah besi yang
hilang dari tubuh relatif kecil. Laki-laki kehilangan kira-kira 0.6 mg/hari,
sedangkan pada perempuan kehilangannya lebih besar dengan rata-rata
dua kali angka tersebut karena penambahan kehilangan besi dalam darah
selama mensturasi.19 Kadar besi dalam tubuh seorang dewasa normal
berkisar antara 35-45 mg/kgBB, dimana laki-laki lebih tinggi daripada
Besi terdapat dalam berbagai jaringan dalam tubuh, berupa
senyawa besi fungsional, yaitu besi yang membentuk senyawa yang
berfungsi dalam tubuh, besi cadangan, yaitu senyawa besi yang
dipersiapkan bila masukan besi berkurang, besi transport, yaitu besi yang
berikatan dengan protein tertentu dalam fungsinya untuk mengangkut besi
dari satu kompartemen ke kompartemen lainnya.
Besi terdapat dalam dua bentuk yaitu heme dan non heme. Sekitar
70% zat besi dalam tubuh ditemukan dalam bentuk heme, khususnya
hemoglobin dan mioglobin, walaupun dapat juga ditemukan pada enzim
hidroperoksidase dan sitokrom. Zat besi nonheme paling banyak disimpan
sebagai feritin (sekitar 1 g pada pria dewasa) atau hemosiderin dalam
makrofag dan hepatosit. Hanya sebagian kecil (sekitar 0,1%) berada
transit dalam plasma, terikat dengan protein pembawanya transferin.
Jumlah yang sangat kecil terdapat dalam enzim peroksidase dan
Hemoglobin Transport oksigen 2600 65.0
Mioglobin Simpanan otot 130 6.0
Transferin Transport besi 3 0.1
Feritin Cadangan besi 520 13.0
Hemosiderin Cadangan besi 480 12.0
Katalase,
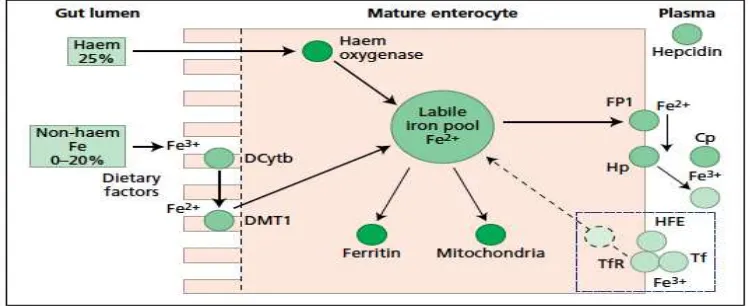
2.1.2. Absorpsi Besi
Besi lebih mudah diserap dalam bentuk Ferro (Fe2+) tetapi
kebanyakan besi yang dimakan berada dalam bentuk Ferri (Fe3+).19
Hanya sedikit sekali besi yang diserap dalam lambung, tetapi di dalam
lambung besi dalam bentuk Ferri (Fe+3) akan diubah menjadi Ferro (Fe+2)
oleh ferric reductase dengan bantuan kofaktor duodenal cytochrom b-like
(DCYTB).20
Perubahan ini sangat penting, karena duedonal metal transporter 1
(DMT1) memungkinkan hanya divalen logam (terutama besi, tetapi juga
Cu, Pb, dan Mn) yang dapat melalui membran apikal enterosit duedonal.
Namun, DMT1 bukan molekul satu-satunya yang memfasilitasi
transportasi besi melalui membran enterosit. Heme carrier protein
merupakan molekul penting yang mengangkut besi heme dari permukaan
apikal ke enterosit. Besi heme akan terikat oleh reseptor heme di
membran brush border dan didalam sel akan dilepaskan oleh heme
oxygenase sebelum memasuki penampungan besi labil dan kemudian
akan mengikuti jalur yang sama dengan besi non-heme. 22
Di dalam enterosit sebagian besi disimpan sebagai feritin, dan
sebagian lagi menuju ke membrane basolateral ke sirkulasi melalui
basolateral transporter dalam bentuk Fe2+ yang disebut ferroportin.20
Ferroportin juga dapat ditemukan pada permukaan membran makrofag.
Jika total besi dalam tubuh tinggi, sintesis hati terhadap hepsidin akan
menyebabkan internalisasi, ubiquitinasi dan degradasi dari ferroportin.
Akibatnya, besi yang ditransfer ke sirkulasi akan menurun. Ferroportin,
seperti DMT1 bersifat permeabel hanya untuk besi dalam bentuk Ferro
(Fe+2). Di sisi lain, besi harus berada dalam bentuk Ferri (Fe+3) agar dapat
terikat dengan transferin. Oleh karena itu, oksidasi besi dari bentuk Ferro
(Fe+2 ) menjadi Ferri (Fe+3 ) oleh ferrooxidase atau hephaestin sangat
diperlukan.20,22
Seruloplasmin adalah homolog hephaestin menetap di membran
makrofag dekat dengan ferroportin, melakukan kerja yang sama dengan
hephaestin. Singkatnya, besi ferro yang berasal dari enterosit dioksidasi
oleh hephaestin, dan besi ferro yang berasal dari makrofag akan
dioksidasi oleh seruloplasmin dengan cara yang sama.22
Gambar 2.1. Mekanisme absorpsi besi 23
2.1.3. Transport Besi
Transferin (Tf) adalah protein utama yang mengikat dan
menyalurkan zat besi ke jaringan. Setiap molekul transferin dapat
salah satu transferrin reseptor (TfR) pada membran sel, TfR1 atau TfR2.
Setiap reseptor transferin mengikat 2 molekul transferin.20,22 Transferrin
reseptor 1 ada dalam semua jaringan kecuali eritrosit yang matang.
Transferrin reseptor 2 paling banyak berada di hati. Meskipun struktur
protein dari TfR1 dan TfR2 hampir sama tetapi fungsi dan regulasinya
berbeda. Ekspresi dari TfR1 diatur sangat ketat oleh kadar zat besi seluler
melalui human hemochromathosis protein (HFE). Namun, kadar zat besi
seluler tidak berpengaruh pada TfR2. TfR2 diatur oleh saturasi transferin
dan berfungsi meregulasi ekspresi hepsidin.
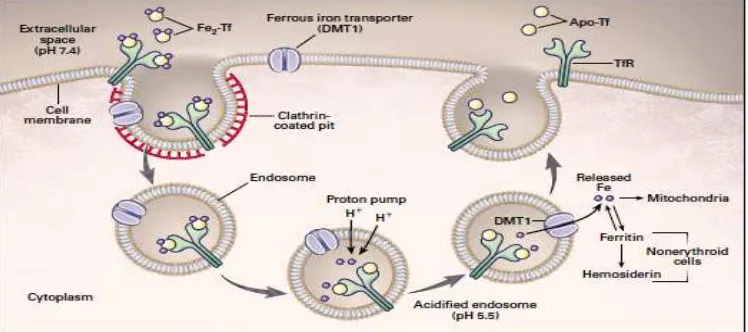
Setelah pengikatan diferric-Tf ke TFR, kompleks diferric-Tf/TFR
bersama dengan DMT 1 pada membran sel yang dilapisi clathrin akan
diinternalisasi secara endositosis. Dalam endosome, proses pengasaman
melalui pompa proton ATPase (pH 5,5-6) akan mengakibatkan ikatan Fe3+
dan Tf terlepas. Sebuah protein disebut STEAP3 (Six-Transmembrane
Epithelial Antigen of Prostate 3) akan mengubah Fe+3 menjadi Fe+2 di
dalam prekursor sel eritroid. Konversi ini diperlukan karena DMT1 hanya
mengangkut divalent logam dari endosome ke sitoplasma seperti pada
enterosit.22,24 Besi di dalam sel eritroid hampir seluruhnya akan menuju
mitokondria dimana akan bergabung dengan protoporphyrin membentuk
heme, sedangkan pada sel lain besi akan disimpan dalam bentuk feritin
dan hemosiderin.25 Kompleks tansferin/TfR yang sudah tidak berikatan
dengan besi (Apotransferrin) akan didaur ulang ke permukaan sel di
perubahan pH ini mengakibatkan terlepasnya ikatan antara apotransferrin
dari TfR. Apotransferin akan dilepaskan keluar dari sel menuju sirkulasi
dan berfungsi kembali menjadi pengangkut besi, sedangkan TfR akan
menjadi truncated transferrin receptor atau soluble transferrin receptor
(sTfR).20,26 Seluruh siklus diselesaikan dalam hitungan menit dan terjadi
sekitar 100-200 dalam durasi hidup sebuah molekul transferin.24
Gambar 2.2. Siklus transferin 25
2.1.4. Besi di dalam Sel Eritroid
2.1.4.1. Pengambilan Besi oleh Sel Eritroid
Nasib besi yang terikat dengan plasma transferin telah
dipelajari dengan menyuntikkan sejumlah radioaktif 59Fe yang
diikat dengan transferin. Sekitar 85% dari 59Fe memasuki sel
prekursor eritroid untuk digunakan dalam pembentukan
hemoglobin.
Dua sampai tiga juta sel darah merah diproduksi setiap detik
per sel. Jumlah zat besi yang dikirim ke masing-masing prekursor
eritroid tergantung pada jumlah monoferric dan diferric transferrin
yang ditemukan dalam sirkulasi serta kepadatan TfR1 pada
permukaan sel. Biasanya, setiap prekursor eritroid memiliki lebih
dari satu juta TfR1 pada membran karena kebutuhan yang tinggi
untuk sintesis hemoglobin.
Bentuk terlarut dari reseptor ini dapat terdeteksi dalam
serum. Konsentrasi sTfR1 pada serum biasanya ditemukan
sebanding dengan jumlah yang ditemukan pada permukaan sel.
Pada anemia defisiensi besi, kepadatan TfR1 pada permukaan sel
meningkat sehingga meningkatkan konsentrasi soluble TfR1
(sTfR1). 23,24
Dalam keadaan normal, afinitas TfR1 dengan diferric
transferrin lebih besar daripada monoferric transferrin. Namun,
afinitas ini akan berkurang apabila pasokan zat besi berkurang.
Monoferric transferrin adalah bentuk dominan transferin yang
beredar saat saturasi transferin menurun. Molekul monoferric
transferrin menghantarkan zat besi yang lebih sedikit ke prekursor
eritroid dibandingkan diferric transferrin. Hal ini memungkinkan
sejumlah besar prekursor eritroid untuk menerima sebagian kecil
dari besi. Penemuan ini konsisten dengan fakta bahwa MCV akan
besi. Transfer besi langsung dari makrofag ke eritroblas
(rhopheocytosis) kini dianggap tidak begitu signifikan.24
Pada keadaan normal, sekitar 80 sampai 90% dari besi yang
masuk ke prekursor eritroid akan diambil oleh mitokondria dan
dimasukkan ke dalam heme, sisanya akan disimpan dalam bentuk
feritin.23,25 Granul feritin dalam eritrosit dapat kadang-kadang dapat
dideteksi dengan cara reaksi Prusisian blue.21
Semua sel darah merah yang imatur sampai retikulosit
memiliki kemampuan untuk mengambil besi, sedangkan eritrosit
matur tidak. Pronormoblast dan basofilik normoblast memiliki
kapasitas terbesar untuk menyerap zat besi. Secara in vitro,
transfer besi dari transferin ke eritrosit imatur akan menurun apabila
saturasi transferin menurun sampai di bawah 30%.27
2.1.4.2. Penggunaan Besi dalam Pembentukan Heme
Hampir 80-90% besi yang dibawa ke eritroblast akan
dikonversi menjadi heme dalam waktu 1 jam. Setiap besi yang
melebihi kebutuhan untuk sintesis heme akan disimpan dalam
bentuk feritin. Oleh karena itu feritin akan meningkat ketika sintesis
hemoglobin terganggu, seperti dalam thalassemia atau anemia
sideroblastik. 23
Heme terdiri dari sebuah cincin protoporfirin dengan atom
besi di pusatnya. Heme disintesis dari prekursor suksinil CoA dan
(ALA). Enzim yang mengkatalisis reaksi ini, ALA-synthase (ALAS)
tampaknya merupakan enzim penentu kecepatan jalur metabolik
ini. Piridoksal fosfat (vitamin B6) adalah koenzim untuk reaksi ini.
Reaksi ini dirangsang oleh adanya hormon eritropoetin dan
dihambat oleh pembentukan heme. Jalur ini dimulai di mitokondria.
Dua molekul ALA menyatu untuk membentuk porphobilinogen.21
Empat molekul porphobilinogen akan terkondensasi di
bawah pengaruh deaminase porphobilinogen (PBGD) dan
uroporphyrinogen cosynthase untuk membentuk cincin tetrapyrrole
yang disebut uroporphyrinogen III. Senyawa ini akan diubah
menjadi coproporphyrinogen dan akan diubah menjadi
protoporphyrin IX. Akhirnya zat besi dalam bentuk ferro dengan
bantuan enzim ferrochelatase akan berikatan dengan
protoporphyrin IX membentuk heme.
Mitokondria memegang peranan utama dalam sintesis heme
karena mengandung enzim synthase, coproporphyrinogen oksidase
dan ferrochelatase. Urutan-urutan enzim dari ALA menjadi
coproporphyrinogen terletak di sitoplasma. Sel darah merah yang
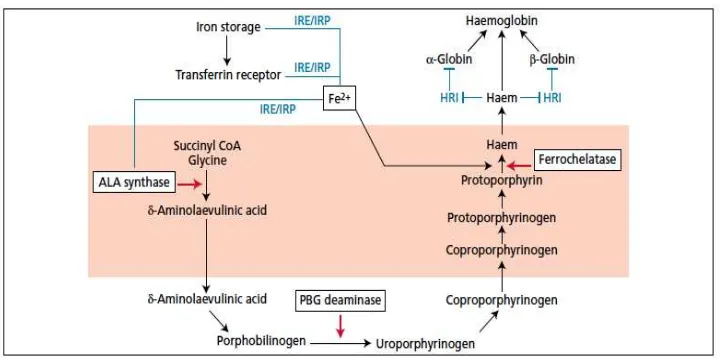
matang tidak memiliki mitokondria, oleh karena itu tidak dapat
Gambar 2.3. Skema pembentukan hemoglobin 23
2.4.1.3. Penghancuran Eritrosit
Eritrosit yang sudah tua akan dihancurkan oleh sistem
retikuloendotelial, terutama dalam hati dan limpa. Kemampuan
penghancuran ini sekitar 20% dalam beberapa jam.28,29 Di dalam
RES eritrosit akan difagositosis oleh makrofag, heme akan dipecah
oleh heme oxygenase (HMOX1) untuk melepaskan besi. Besi
kemudian bisa disimpan dalam bentuk feritin atau melalui
Ferroportin 1 dilepas ke dalam plasma. Di dalam plasma, untuk
dapat berikatan dengan transferin, besi harus berada dalam
bentuk ferri, perubahan ini difasilitasi oleh enzim ferrooxidase
seruloplasmin. Pelepasan besi dari makrofag dikendalikan oleh
hepsidin dimana apabila hepsidin terdapat dalam kadar yang tinggi,
seperti dalam peradangan atau kelebihan zat besi, terjadi
pengurangan dari pelepasan besi. Perubahan dalam pelepasan
dimana konsentrasi besi serum tertinggi terdapat pada pagi hari
dan terendah di malam hari.23
2.2. Retikulosit
Sel darah merah manusia dimulai dari sel berinti dan akhirnya
menjadi tidak berinti. Perkembangan ini berada didalam sum-sum tulang
dan membutuhkan waktu 5 hari sampai akhirnya sel-sel prekursor
menghasilkan sel yang lebih kecil. Beberapa bentuk dari sel darah merah
yang berubah secara dramatis adalah berkurangnya perbandingan inti :
sitoplasma (N:C), kromatin menjadi lebih padat dan warna sitoplasma juga
berubah sesuai dengan proses hemoglobinisasi yang semakin dominan.30
Prekursor-prekursor eritroid berasal dari CFU-GEMM. Prekursor
selanjutnya yang secara spesifik bekerja dalam lini eritroid adalah
Burst-Forming-Unit (BFU-E), diikuti oleh pembentukan Colony-Forming-Unit
(CFU-E). Prekursor eritrosit awal yang dapat dikenali adalah rubriblast,
yang ditandai dengan nukleus yang menempati hampir 80% dari sel, dan
pinggir sitoplasma yang basofilik. Pada tahap ini hanya sedikit jumlah
hemoglobin yang ditemukan.21 Tahap pematangan selanjutnya adalah
prorubrisit kemudian menjadi rubrisit. Prekursor bernukleus terakhir adalah
metarubrisit dimana sitoplasmanya hampir penuh dengan hemoglobin.
Setelah inti diekstrusi, sel ini dikenal sebagai retikulosit. Sel-sel ini agak
lebih besar dari eritrosit dengan diameter 7-10 µm, mungkin volumenya
ribonukleat (RNA). Retikulosit mungkin tetap dalam sumsum tulang
selama 3 hari untuk kemudian dilepaskan ke sirkulasi.26
2.3. Pemeriksaan Status Besi
2.3.1. Retikulosit Hemoglobin (RET-HE)
Penilaian besi yang terkait eritropoiesis dapat dilakukan dengan
penilaian pada sum-sum tulang tetapi tindakan ini terlalu invasif . Sel-sel
darah merah yang secara aktif menggunakan besi untuk sintesa
hemoglobin berada di dalam sumsum tulang, tidak di dalam sirkulasi
perifer. Retikulosit adalah sel-sel darah merah yang belum matang tetapi
yang paling dekat yang dapat dengan mudah dinilai dan diidentifikasi di
darah perifer.30 Ketika produksi sel darah merah dalam keadaan normal,
retikulosit akan berada dalam sirkulasi hanya 1 sampai 2 hari tapi
mencerminkan status besi yang ada 3 sampai 4 hari sebelum
penggabungan besi ke hemoglobin berada pada saat maksimum.11,14,16
Dengan demikian, ketersediaan besi fungsional untuk dimasukkan ke
dalam sel darah merah pada sumsum tulang selama proses pembentukan
sel darah merah beberapa hari sebelumnya tercermin dari jumlah
hemoglobin dalam retikulosit.30,31 Hal ini lebih berguna daripada
pewarnaan besi yang merupakan perkiraan deposit di sistem
retikuloendotelial.12
Dengan demikian, jumlah hemoglobin dalam retikulosit adalah
refleksi yang cukup baik dari seberapa banyak zat besi yang tersedia.
mungkin berada di mana saja antara 1 sampai 120 hari, hemoglobin
retikulosit akan memberikan gambaran berapa banyak besi tersedia untuk
produksi sel darah merah dalam jangka waktu yang relevan secara klinis.
Oleh karena itu, secara teoritis retikulosit hemoglobin merupakan penanda
yang cukup baik.31
Karena ukuran rata-rata sel digunakan untuk perhitungan retikulosit
hemoglobin maka pengukuran ini memiliki keterbatasan diagnostik.
Retikulosit hemoglobin sering rendah pada pasien thalasemia yang
sedang diberi terapi besi dan hemoglobinopati yang dapat menyebabkan
anemia mikrositer. Retikulosit hemoglobin dapat pula meningkat pada
pasien defisiensi besi yang bersamaan dengan anemia megalobastik
karena MCV tinggi yang terkait dengan megaloblastik.16
2.3.2. Feritin
Besi seluler yang tidak langsung digunakan akan disimpan dalam
bentuk feritin. Feritin adalah protein yang memiliki berat 480 kDa yang
terdiri dari 24 monomer apoferitin. Feritin dapat mengikat hingga 4500
atom besi yang tersimpan dalam bentuk Fe3+. Feritin ditemukan hampir di
seluruh sel walaupun umumnya akan ditemukan di dalam sel hepatosit
hati, makrofag pada sum-sum tulang dan limfa yang berfungsi untuk
menyediakan besi untuk sintesa hemoglobin..32,33
Feritin dalam jumlah kecil juga akan terdapat di dalam darah. Pada
orang sehat dan penderita defisiensi besi tahap awal, konsentrasi feritin di
setiap 1 µg/L serum feritin mengindikasikan kurang lebih 8 mg dari besi
yang tersimpan. Meskipun demikian, hubungan langsung antara besi yang
dikonsumsi dengan feritin tidak begitu baik. Hal ini disebabkan oleh
karena feritin juga merupakan protein reaktan fase akut yang kadarnya
akan meningkat apabila terjadi proses infeksi, inflamasi, keganasan dan
penyakit hati. Cut-off feritin untuk defisiensi besi menurut WHO adalah
<15 µg/L, tetapi apabila didapati infeksi cut off defisiensi besi adalah < 30
µg/L.1,20,24
2.3.3. Serum Iron
Serum iron adalah banyaknya besi yang diangkut oleh
apotransferin.13 Secara fisiologis, konsentrasi besi serum memiliki irama
diurnal, dimana besi serum akan berkurang di sore dan malam hari,
mencapai titik nadir dekat pukul 9 malam dan meningkat menjadi
maksimum antara pukul 7 dan 10 pagi. Meskipun berbagai penelitian
menunjukkan bahwa variasi diurnal terjadi, sangat diragukan apakah hal
ini cukup penting secara klinis untuk mewajibkan semua nilai besi serum
diambil pada pagi hari. Konsentrasi besi serum berkurang dengan adanya
proses inflamasi baik akut maupun kronis, infeksi, dan keganasan.26,28,34
2.3.4. Total Iron Binding Capacity (TIBC)
Besi akan ditransportasikan di dalam plasma dan cairan
ekstraseluler oleh transferin. Metaloprotein ini memiliki afinitas yang
sangat tinggi terhadap besi. Hampir seluruh besi dalam plasma akan diikat
plasma transferin secara indirek dengan mengukur jumlah total iron
binding capacity (TIBC) yang merupakan jumlah total ikatan besi dengan
tranferin.24 Hanya sepertiga bagian dari transferin yang berikatan dengan
besi, sehingga masih tersedia cadangan yang cukup banyak untuk
berikatan dengan besi apabila terjadi kelebihan besi.20 TIBC akan
meningkat apabila terjadi pengurangan simpanan besi. TIBC akan
berkurang apabila terjadi infeksi, inflamasi ataupun keganasan.29
2.3.5. Saturasi Transferin (TfSat)
Konsentrasi besi dalam serum dan saturasi transferin akan turun
seiring dengan pasokan besi yang menurun. Level saturasi dibawah 16%
mengindikasikan ketidakcukupan besi untuk mempertahankan sintesa
hemoglobin dalam kadar yang normal. 29 Persen saturasi transferin
dengan besi ditentukan dengan membagi serum besi dengan TIBC dikali
100. 20
% !"#$%"&' !"#$% =
!"#$% !"#$
!"!#$ !"#$ !"#$"#% !!"!#$%& × 100%
2.4. Perubahan-Perubahan pada Wanita Hamil
2.4.1. Kebutuhan Besi selama Kehamilan
Ketersediaan besi sangat penting bagi proses pematangan janin.
Hampir 1000 mg besi diperlukan untuk mendukung pertumbuhan dan
pematangan janin selama kehamilan. Untuk mengatasi kebutuhan besi,
penyerapan besi di duodenum meningkat lebih dari dua kali lipat selama
Kebutuhan janin terhadap besi sangat tinggi, oleh karena itu
plasenta akan mengambil besi dari plasma ibu sejauh yang diperlukan
untuk memenuhi kebutuhan janin. Mobilisasi cadangan besi ibu
membantu memenuhi kebutuhan itu apabila absorpsi besi pada saluran
pencernaan tidak cukup. Rata-rata terjadi mobilisasi sekitar 8% dari
cadangan besi terjadi selama usia kehamilan 280 hari. Hasilnya adalah
menipisnya cadangan zat besi ibu sampai dapat menimbulkan defisiensi
besi.
Transferin dalam sirkulasi akan mengikat dan mentransportasikan
besi ke semua sel dalam tubuh. Umumnya, sumsum tulang adalah tujuan
utama sebab hampir 90% besi digunakan untuk produksi heme. Pada
kehamilan, plasenta merupakan tujuan kedua. Besi yang dikirim ke
plasenta meningkat seiring usia kehamilan.21,35
2.4.2. Perubahan Hematologi selama Kehamilan
Terdapat dua perubahan hematologi yang paling menonjol selama
kehamilan yaitu, peningkatan volume plasma dan jumlah sel darah merah.
Volume plasma meningkat sekitar 30% sedangkan jumlah sel darah
merah meningkat hanya sekitar 20%, hasilnya adalah penurunan
hematokrit, karena variabel ini didefinisikan sebagai volume sel darah
merah dalam volume plasma tertentu. 21,35
Penurunan hematokrit ini disebut anemia fisiologis atau dilutional
anemia. Kenaikan volume plasma dimulai sekitar minggu ke-6
sekitar minggu ke-30. Volume plasma sekitar 1200 mL (hampir 50%) lebih
besar daripada di saat tidak hamil. Jumlah sel darah merah juga
meningkat pada waktu ini, dengan kenaikan sekitar 250 sampai 400 mL
(20% sampai 30%) dibandingkan saat tidak hamil.
Hematokrit biasanya menurun sampai trimester kedua, tapi naik
perlahan-lahan setelahnya. Akibatnya, nilai hemoglobin akan berfluktuasi
selama kehamilan, sehingga dapat menimbulkan kebingungan. Cara yang
paling baik adalah untuk menetapkan kadar hemoglobin 11 g/dL sebagai
batas bawah dari nilai hemoglobin normal selama kehamilan.
Kenaikan nilai eritropoietin tampaknya menjadi faktor kunci
terjadinya peningkatan jumlah sel merah selama kehamilan. Eritropoietin
dapat meningkat sekitar 50% saat trimester kedua sampai akhir semester
tiga. Kenaikan eritropoietin lebih tinggi pada wanita yang kekurangan
besi.21,35
2.4.3. Penilaian Defisiensi Besi selama Kehamilan
Sama seperti perubahan pada jumlah sel darah merah dan volume
plasma yang diakibatkan oleh kehamilan, perubahan juga terjadi pada
parameter penilaian cadangan besi. Kehamilan meningkatkan nilai serum
feritin, sehingga menurunkan nilai diagnostiknya dalam menilai cadangan
besi. Penggunaan besi dalam pembentukan heme sebagai akibat dari
ekspansi jumlah sel darah merah ibu akan mengakibatkan penurunan
kehamilan ini mengurangi penggunaan dua kunci parameter laboratorium
dalam menganalisa defisiensi besi.
Peningkatan jumlah prekursor eritroid akan meningkatkan jumlah
transferin reseptor dalam tubuh serta jumlah soluble transferin reseptor
dalam sirkulasi. Kehamilan hanya sedikit mengganggu kadar soluble
trasnferin reseptor, membuat indeks ini menjadi penanda penting dalam
deteksi defisiensi besi pada ibu hamil.37
Defisiensi besi menghambat sintesis hemoglobin oleh prekursor
eritroid sehingga menurunkan mean corpuscular hemoglobin
concentration (MCHC) dan mean corpuscular volume (MCV). Namun
penilaian MCHC dalam mendeteksi defisiensi besi bukan merupakan
indeks yang baik. Kesulitannya terletak dalam waktu paruh sel darah
merah. Seiring dengan perkembangan defisiensi besi, sel-sel merah
dengan nilai MCHC rendah bercampur dengan sel-sel yang sudah lebih
tua dalam sirkulasi dengan nilai MCHC normal.
Penilaian retikulosit hemoglobin menghilangkan masalah ini.
Retikulosit berada di sirkulasi selama 2-3 hari sebelum menjadi eritrosit
matang. Karena retikulosit baru saja muncul dari sumsum tulang,
retikulosit adalah jendela untuk status eritropoiesis saat ini. Kekurangan
zat besi untuk proses eritropoesis menghasilkan retikulosit dengan kadar
hemoglobin rendah. Retikulosit hemoglobin menyediakan ketersediaan
2.5. Defisiensi Besi
Defisiensi besi merupakan suatu keadaan yang disebabkan oleh
berkurangnya cadangan besi tubuh akibat asupan yang tidak adekuat,
kebutuhan meningkat, atau perdarahan menahun.
2.5.1. Penyebab Defisiensi Besi
Defisiensi besi umumnya terjadi oleh karena tiga faktor yang
mempengaruhi keseimbangan zat besi, yaitu :
1. Kehilangan darah
Kehilangan darah umumnya merupakan penyebab paling
utama dari anemia defisiensi besi di nengara-negara berkembang.
Perdarahan gastrointestinal merupakan penyebab tersering pada
pria dan wanita postmenapause. Perdarahan menstrual yang berat
merupakan penyebab yang sering pda wanita-wanita usia
reproduksi.
2. Diet
Kekurangan zat besi terjadi ketika asupan tidak seimbang
dengan penggunaan dan kehilangan zat besi. Di seluruh dunia,
penyebab paling umum adalah rendahnya kadar zat besi makanan,
terutama dalam bentuk yang mudah diserap seperti daging.
Kejadian kekurangan zat besi relatif tinggi pada wanita remaja,
seiring dengan meningkatnya kebutuhan zat besi karena
3. Malabsorpsi
Malabsorpsi adalah penyebab defisiensi besi yang kurang
umum. Beberapa pasien dengan short bowel syndrome, dan
dengan riwayat gastrektomi tidak dapat menyerap zat besi secara
normal. 30,38
2.5.2. Tahapan Defisiensi Besi
Perjalanan defisiensi besi melalui 3 tahapan, tahap :
1. Tahap iron depletion
Ketika tubuh berada dalam kekurangan besi, peristiwa
pertama yang terjadi adalah pengurangan dari penyimpanan besi
tubuh, yang digunakan untuk produksi hemoglobin. Penyerapan zat
besi meningkat ketika simpanan dikurangi, sebelum anemia
berkembang dan bahkan ketika tingkat zat besi dalam serum masih
normal, meskipun serum feritin sudah turun.
2. Tahap iron deficient erythropoiesis
Apabila kekurangan zat besi terus berlanjut saturasi
transferin akan menurun hingga dibawah 15% karena peningkatan
konsentrasi transferin dan penurunan besi serum. Hal ini akan
berkembang menjadi tahap kekurangan besi untuk eritropoiesis.
Terjadi pula peningkatkan konsentrasi reseptor transferin dan red
cell protoporfirin. Pada tahap ini, hemoglobin, MCV dan MCH
mungkin masih dalam batas normal meskipun dapat meningkat
3. Tahap iron deficiency anemia
Tahap selanjutnya adalah tahapan anemia defisiensi besi.
Sel-sel darah merah menjadi jelas mikrositik hipokromik dan
poikilositosis lebih nyata dijumpai. MCV dan MCH berkurang dan
dapat pula dijumpai sel target. Saturasi transferin biasanya kurang
dari 10% diakibatkan jumlah besi serum yang semakin menurun
dan kenaikan TIBC. Jumlah eritroblast yang mengandung besi
(sideroblas) berkurang pada tahap awal sampai akhirnya sama
sekali tidak dijumpai pada tahap ini. 21,26,38,39
2.5.3. Diagnosa
Diagnosa defisiensi besi adalah sebagai berikut :
Jenis kelamin/Umur (tahun) Hemoglobin <g/dL Laki-laki dewasa < 13
Perempuan dewasa tidak hamil < 12 Perempuan hamil < 11 Anak umur 6 - 12 tahun < 12 Anak umur 6 bulan - 6 tahun < 11
Feritin < 15 µg/L sTfR > 8.5 mg/L Saturasi Transferin < 16% Mean cell volume (MCV) < 82/85 fL* RDW > 14% Eritrosit protoporfirin > 70 µg/dL * <15tahun/ >15 tahun
2.6. Kerangka Konseptual
Cadangan Besi : Feritin dan Hemosiderin
Besi dalam plasma : Serum Iron, TIBC,
Saturasi Transferin
Eritropoesis
: sTfR, MCV,MCH,Hb,Ht, RDW, Eritrosit Protoporphrin, RET-HE
Usia Kehamilan Inhibitor
Intake
Enhancer