PEMISAHAN DENGAN CARA DESTILASI
I. Tujuan
Tujuan dari praktikum ini adalah melakukan pemisahan senyawa dari pengotornya dan atau pelarutnya melalui jalan destilasi.
II. Landasan Teori
Destilasi atau penyulingan adalah suatu metode pemisahan bahan kimia berdasarkan pada perbedaan kecepatan atau kemudahan menguap (volatilitas) bahan atau zat. Dalam penyulingan, campuran zat dididihkan sehingga menguap, dan uap ini kemudian didinginkan kembali ke dalam bentuk cairan. Zat yang memiliki titik didih lebih rendah akan menguap lebih dulu.
(Syukri,2007). Prinsip destilasi adalah penguapan cairan dan pengembunan kembali uap tersebut pada suhu titik didih. Titik didih suatu cairan adalah suhu dimana tekanan uapnya sama dengan tekanan atmosfer. Cairan yang diembunkan kembali disebut destilat. Tujuan destilasi adalah pemurnian zat cair pada titik didihnya, dan memisahkan cairan tersebut dari zat padat yang terlarut atau dari zat cair lainnya yang mempunyai perbedaan titik didih cairan murni. Pada destilasi biasa, tekanan uap di atas cairan adalah tekanan atmosfer (titik didih normal). Untuk senyawa murni, suhu yang tercatat pada termometer yang ditempatkan pada tempat terjadinya proses destilasi adalah sama dengan titik didih destilat.
Proses destilasi dilakukan dengan menggunakan seperangkat alat destilasi yang terdiri dari labu dasar bulat, kondensor, dan labu destilat. Larutan atau campuran zat ditempatkan dalam labu dasar bulat dan biasanya ditambahkan batu didih untuk mencegah golakan gelembung udara. Ketika larutan tersebut dipanaskan secara perlahan tekanan uap masing-masing zat akan naik hingga mencapai 1 Atm dan selanjutnya panas yang diberikan digunakan zat untuk mengubah fasa cair menjadi fasa gas/uap.
(Tim Kimia Analitik, 2014) Dalam proses destilasi terdapat dua tahap proses yaitu tahap penguapan dan dilanjutkan dengan tahap pengembangan kembali uap menjadi cair atau padatan. Atas dasar ini maka perangkat peralatan destilasi menggunakan alat pemanas dan alat pendingin.
Proses destilasi diawali dengan pemanasan, zat yang memiliki titik didih lebih rendah akan menguap. Uap tersebut bergerak menuju kondenser yaitu alat pendingin. Proses pendinginan tersebut kemudian mengkondensasikan uap air tersebut dengan kemurnian yang relatif tinggi. Proses ini berjalan terus menerus dan akhirnya kita dapat memisahkan seluruh senyawa-senyawa yang ada dalam campuran homogen tersebut.
pemisahan dengan cara destilasi digunakan untuk memisahkan campuran alkohol dari air.
(Wahyu, 2013). Ada 6 jenis destilasi yang akan dibahas disini, yaitu destilasi sederhana, destilasi fraksionasi, destilasi uap, destilasi vakum, destilasi kering dan destilasi azeotropik.
1. Destilasi Sederhana
Pada destilasi sederhana, dasar pemisahannya adalah perbedaan titik didih yang jauh atau dengan salah satu komponen bersifat volatil. Jika campuran dipanaskan maka komponen yang titik didihnya lebih rendah akan menguap lebih dulu. Selain perbedaan titik didih, juga perbedaan kevolatilan, yaitu kecenderungan sebuah substansi untuk menjadi gas. Destilasi ini dilakukan pada tekanan atmosfer. Aplikasi destilasi sederhana digunakan untuk memisahkan campuran air dan alkohol.
2. Destilasi Fraksionasi
Fungsi destilasi fraksionasi adalah memisahkan komponen-komponen cair, dua atau lebih, dari suatu larutan berdasarkan perbedaan titik didihnya. Destilasi ini juga dapat digunakan untuk campuran dengan perbedaan titik didih kurang dari 20 °C dan bekerja pada tekanan atmosfer atau dengan tekanan rendah.
3. Destilasi Azeotrop
Azeotrop adalah campuran dari dua atau lebih komponen yang memiliki titik didih yang konstan. Campuran azeotrop merupakan penyimpangan dari hukum Raoult.
4. Destilasi Vakum
Destilasi vakum biasanya digunakan jika senyawa yang ingin didestilasi tidak stabil, dengan pengertian dapat terdekomposisi sebelum atau mendekati titik didihnya atau campuran yang memiliki titik didih di atas 150 °C.
Destilasi uap digunakan pada campuran senyawa-senyawa yang memiliki titik didih mencapai 200 °C atau lebih. Distilasi uap dapat menguapkan senyawa-senyawa ini dengan suhu mendekati 100 °C dalam tekanan atmosfer dengan menggunakan uap atau air mendidih
6. Destilasi kering
Destilasi kering merupakan destilasi yang dilakukan dengan cara memanaskan material padat untuk mendapatkan fase uap dan cairnya, biasanya digunakan untuk mengambil cairan bahan bakar dari kayu atau batu bara.
III. Prosedur Kerja 3.1 Alat dan Bahan
Alat
Seperangkat alat destilasi Lampu spirtus
Termometer Batu didih atau
padatan berpori Mentel pemanas Rotary Evaporator
Gelas ukur Corong pisah Pompa vaccum
Bahan
Anilin yang kotor Benzena
Akuades
3.2 Skema Kerja 3.3
3.3.1 Pemisahan anilin dari
didestilasi
dipisahkan menggunakan corong pisah diamati
didestilasi
diamati dicatat
diukur volume destilat yang diperoleh
3.3.2 Pemisahan benzena dari campuran air dan benzena
Ditempatkan dalam labu dasar bulatdestilasi
Diatur tekanan dalam labu (0,5 Atm) Mengunakan alat vaccum
Dilaksanakan destilasi vaccum Diatur panas yang digunakan
Diamati suhu pada termometer Dicatat
Diukur volume destilat yang dihasilkan 50 ml benzena
Hasil 2 ml air
Hasil
IV. Hasil dan Pembahasan 4.1 Hasil
1. Pemisahan anilin dari pengotornya
Perlakuan Hasil Pengamatan
50 ml anilin kotor didestilasi, hasil dipisahkan menggunakan corong pisah, diukur volume anilin yang diperoleh
Tidak dipraktikumkan
2. Pemisahan Benzena dari campuran air-benzena
Jumlah tetesan Menit ke- T (⁰C)
32 1 56
74 2 57
76 3 58
110 4 58
110 5 58
58 6 59
Volume benzena yang dihasilkan = 37 ml
%rendemen=volume hasilvolume awal x100 %=3750mlml x100 %=74 %
4.2 Pembahasan
Pada praktikum ini, praktikan akan melakukan prosedur pemisahan dengan cara destilasi. Percobaan yang dilakukan oleh praktikan ada dua bagian yaitu pemisahan anilin dari pengotorannya dan pemisahan benzena dari campuran air dan benzena.
Destilasi adalah suatu proses pemurnian yang didahului dengan penguapan senyawa cair dengan cara memanaskannya, kemudian mengembunkan uap yang terbentuk. Destilasi merupakan suatu proses pemisahan dua atau lebih komponen zat cair berdasarkan pada titik didih. Secara sederhana destilasi dilakukan dengan memanaskan/menguapkan zat cair lalu uap tersebut didinginkan kembali supaya jadi cair dengan bantuan kondensor.
terendah akan menguap lebih dahulu, kemudian apabila didinginkan akan mengembun dan menetes sebagai zat murni (destilat).
1. Pemisahan anilin dari pengotornya
Pada praktikum ini praktikan tidak melaksanakan kegiatan praktikum dikarenakan sampel bahan anilin yang dibutuhkan tidak tersedia, sehingga pada pembahasan ini hanya dibahas sesuai literatur yang praktikum temukan.
Sebanyak 50 ml anilin kotor dimasukkan ke dalam labu dasar bulat dan ditambahkan batu didih di dalamnya. Fungsi dari batu didih ini adadlah agar meratakan panas yang diterima sampel dan agar tidak menimbulkan percikan saat pemanasan. Kemudian didestilasi dengan menggunakan metode destilasi sederhana.
Destilasi sederhana merupakan prosedur pemisahan atau pemurnian zat yang menggunakan tekanan yang sama dengan tekanan atmosfer disekitarnya. Destilasi ini baik digunaka dalam pemisahkan atau memurnikan zat yang memiliki perbedaan titik didih yang cukup besar. Selain itu dalam prosedur ini dipengaruhi sifat kevolatilan ( kemudahan untuk menguap) dari zat yang akan didestilasi.
Berdasarkan literatur senyawa anilin (C6H5-NH2) merupakan senyawa aromatik dari turunan benzena. Anilin memiliki sifat fisik dan kimia antara lain:
Sifat Fisika Anilin
Berat molekul : 93,128 g/mol
Temperatur kritis : 699 K
Titik lebur : 267,13 K
Titik didih : 457,6 K
Tekanan kritis : 53,09 bar
Volume kritis : 270 cm3/mol
Indeks bias : 1.58
Sifat Kimia Anilin
Larut pada pelarut organik dengan baik, larut pada air dengan tingkat kelarutan 3,5 % pada 25 C
Anilin adalah basa lemah (Kb = 3,8 x 10^ -10)
Halogenasi senyawa anilin dengan brom dalam larutan sangat encer
menghasilkan endapan 2,4,6 tribromanilin; sedangkan halogenasi dengan klorin menghasilkan trikloroanilin
Anilin beraksi dengan gliserol membentuk quinoline dengan adanya
nitrobenzen dan asam sulfat
Anilin bereaksi dengan hidrogen peroksida dan arctonitril dalam larutan metanol membentuk azoxybenzene
Hidrogenasi anilin dengan menggunakan brom menghasilkan 2,4,6
tribromoanilin
Sebagaimana prinsip dasar dari destilasi adalah memisahkan zat berdasarkan perbedaan titik didihnya, maka komponen zat yang memiliki titik didih yang rendah akan lebih dulu menguap sedangkan yang lebih tinggi titik didihnya akan tetap tertampung pada labu destilasi. Proses penguapan komponen zat ini dilakukan dengan pemanasan pada labu destilasi sehingga komponen zat yang memiliki titik didih yang lebih rendah akan menguap dan uap tersebut melewati kondensor atau pendingin yang mendinginkan komponen zat tersebut sehingga akan terkondensasi atau berubah dari berwujud uap menjadi berwujud cair sehingga dapat ditampung di labu destilat atau labu Erlenmeyer.
Anilin yang dihasilkan melalui desdtilasi ini kemudian dipisahkan menggunakan corong pisah menggunakan metode ekstraksi cair-cair. Hal ini dikarenakan hasil destilat yang dihasilkan terdiri dari dua fase larutan yang berbeda. Kemungikan akibat perbedaan massa jenis dari kedua senyawa atau sifat kepolarannnya. Kemudian diukur volume anilin yang dihasilkan.
2. Pemisahan benzena dari campuran air-benzena
Pada percobaan pemisahan benzana dari campuran air dan benzena, dilakukan dengan cara destilasi vaccum. Langkah pertama pada percobaan ini yaitu, praktikan memasukkan 2 ml air dan 50 ml benzene dalam labu dasar bulat. Kemudian dihidupkan pompa vaccum, dan dilakukan proses destilasi.
Destilasi vakum adalah destilasi yang tekanan operasinya 0,4 atm (≤300 mmHg absolut). Proses distillasi dengan tekanan dibawah tekanan atmosfer. Fungsinya yaitu untuk menurunkan titik didih pada minyak berat atau long residu sehingga menghasilkan produk - produknya.
Destilasi vakum biasanya digunakan jika senyawa yang ingin didestilasi tidak stabil, dengan pengertian dapat terdekomposisi sebelum atau mendekati titik didihnya atau campuran yang memiliki titik didih di atas 150 °C. Metode distilasi ini tidak dapat digunakan pada pelarut dengan titik didih yang rendah jika kondensornya menggunakan air dingin, karena komponen yang menguap tidak dapat dikondensasi oleh air. Untuk mengurangi tekanan digunakan pompa vakum atau aspirator. Aspirator berfungsi sebagai penurun tekanan pada sistem distilasi ini.
Benzena juga bahan dasar dalam produksi obat-obatan, plastik, bensin, karet buatan, dan pewarna. Selain itu, benzena adalah kandungan alami dalam minyak bumi, namun biasanya diperoleh dari senyawa lainnya yang terdapat dalam minyak bumi. Karena bersifat karsinogenik, maka pemakaiannya selain bidang non-industri menjadi sangat terbatas.
Sifat fisik benzena:
Rumus molekul : C6H6
Massa molar : 78,1121 g/mol
Penampilan : cairan tak berwarna
Densitas : 0,8786 g/ml, zat cair
Titik lebur : 5,5 ⁰C (278,6 K)
Titik didih : 80,1 ⁰C (353,2 K)
Kelarutan dalam air : 0,8 g/l (25⁰C)
Air adalah senyawa kimia yang paling banyak digunakan oleh kehidupan manusia. Air merupakan elemen/unsur pembangun kehidupan di bumi, sehingga perlu dijaga dan dilestarikan.
Air mempunyai rumus moleku H2O dan merupakan pelarut yang paling banyak digunakan dalam kegiatan kimia karena sifatnya yang terdisosiasi membentuk Ion H+ dan ion OH-.
Sifat fisik air:
Rumus molekul : H2O
Massa molar : 18,0153 g/mol
Densitas : 0,998 g/cm3 (cairan pada 20⁰C)
0,92 g/cm3 (padatan)
Titik lebur : 0⁰C (273,15 K)
Titik didh : 100⁰C (373,15 K)
Kalor jenis : 4184 J/kg.K
tersebut. Senyawa benzena memilki sifat non polar, sedangkan air adalah senyawa polar. Karena ketidaklarutan tersebut, maka campuran benzena-air dapat dipisahkan melalui destilasi.
Sebagaimana prinsip dasar dari destilasi adalah memisahkan zat berdasarkan perbedaan titik didihnya, maka komponen zat yang memiliki titik didih yang rendah akan lebih dulu menguap sedangkan yang lebih tinggi titik didihnya akan tetap tertampung pada labu destilasi. Benzena memliki titik didih sekitar 80,1 ⁰C lebih rendah dari pada titik didih air yang berkisar 100⁰C pada tekanan atmosfer, sehingga berdasarkan perbedaan titik didih yang cukup besar ini dapa dilakukan prosedur pemisahan menggunakan metode destilasi.
Destilasi yang digunakan dalam prosedur pemisahan benzena-air ini adalah destilasi vakum, artinya praktikan akan memisahkan komponen benzena dibawah titik didih normalnya akibat berkurangnya tekanan dalam alat destilasi. Kemudian praktikan membuat grafik temperatur titik didh terhadap volume
grafk hubungan volume destilat vs waktu
20 30 40 50 60 70 80 90 100 110 120
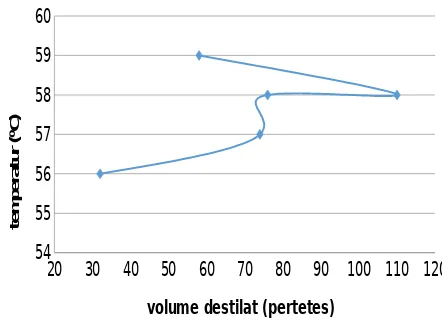
grafk pengaruh temperatur terhadap volume destilat
volume destilat (pertetes)
Grafik pertama (hubungan volume destilat terhadap waktu) menunjukkan sejak awal tetesan pertama, destilat mengalami penambahan volume setiap menitnya. Hal ini dikarenakan ketika pemanasan berlangsung, temperatur larutan mengalami kenaikan sehingga mendekati titik didihnya dan mengakibatkan semakin banyak cairan yang mengalami perubahan fasa menjadi uap. Hal ini terus berlangsung selama volume cairan yang akan dipisahkan (benzena) masih ada sehingga hanya menyisakan air.
Grafik kedua (hubungan temperatur terhadap volume destilat) menunjukkan bahwa semakin tinggi temperatur dari larutan maka akan semakin banyak volmue destilat yang dihasilkan. Dikarenakan kondisi destilasi ini dibuat vakum, maka destilat akan menguap di bawah titik didid normalnya. Tempertur ini akan terus naik hingga mencapai titik didihnya sehingga hanya menyisakan senyawa campurannya karena titik didihnya berada lebih tinggi dari senyawa yang akan dipisahkan.
Dari hasil pengukuran volume destilat yang dihasilkan, didapatlah volume benzena yang berhasil dipisahkan dari larutan campuran sebanyak 37 ml. Sehingga persentase keberhasilan destilasi in berkisar 74%.
V. Kesimpulan dan Saran 5.1 Kesimpulan
Berdasarkan praktikum yang dilaksanakan, maka dapat disimpulkan: 1. Destilasi adalah pemisahan campuran cairan-cairan berdasarkan titik
didih. Apabila titik didih dari suatu campuran yang akan dipisahkan rendah maka campuran itu akan mudah di distilasi.
2. Prinsip dasar dari destilasi adalah perbedaan titik didih dari zat-zat cair dalam campuran zat cair tersebut sehingga zat (senyawa) yang memiliki titik didih terendah akan menguap lebih dahulu, kemudian apabila didinginkan akan mengembun dan menetes sebagai zat murni (destilat). 3. Destilasi vakum Destilasi vakum adalah destilasi yang tekanan
operasinya 0,4 atm (≤300 mmHg absolut). Proses distillasi dengan tekanan dibawah tekanan atmosfer. Fungsinya yaitu untuk menurunkan titik didih pada minyak berat atau long residu sehingga menghasilkan produk - produknya.
4. Volume benzena yang berhasil dipisahkan dari senyawa campurannya berkisar 37 ml, sehingga persentase hasilnya sebesar 74%
5.2 Saran
Pada percobaan ini, ketersediaan alat di laboratorium sangat minim. Ketika praktikum pun, praktikan harus melakukannya di laboratorium lainnya karena di laboratorium pertama alatnya tidak bisa dipakai. Praktika pun mengharapkan agar peralatan yang dibutuhkan ketika praktikum dapat tersedia dengan baik sehingga praktikum dapat berjalan dengan baik dan sesuai dengan prosedur.
VI. Daftar Pustaka
Harizul, Rivai. 1995. Asas Pemeriksaan Kimia. Jakarta : UI Press Soebagio, dkk. 2005. Kimia Analitik II. Malang : UM Pres
Syukri.2007. Kimia Dasar 2. Bandung : ITB
LAMPIRAN
Pertanyaan PraPraktikum
1. Faktor-faktor apakah yang mempengaruhi tinggi rendahnya titik didih dan tekanan upa suatu zat, serta bagaimana keterkaitan antara keduanya? Jawab :
Titik didih zat cair dipengaruhi oleh dua faktor yaitu tekanan di atas permukaan zat cair dan ketidakmurnian zat cair. Faktor-faktor yang mempengaruhi tekanan uap salah satunya adalah suhu. Semakin tinggi suhu zat cair, semakin besar tekanan uapnya.
Apabila sebuah larutan mempunyai tekanan uap yang tinggi pada suhu tertentu, maka molekul-molekul yang berada dalam larutan tersebut mudah untuk melepaskan diri dari permukaan larutan atau dapat dikatakan pada suhu yang sama sebuah larutan mempunyai tekanan uap yang rendah, maka molekul molekul dalam larutan tersebut tidak dapat dengan mudah melepaskan diri dari larutan.
Jadi larutan dengan tekanan uap yang lebih tinggi pada suhu tertentu akan memiliki titik didih yang lebih rendah. Cairan akan mendidih ketika tekanan uapnya menjadi sama dengan tekanan udara luar. Titik didih cairan pada tekanan udara 760 mmHg disebut titik didih standar atau titik didih normal. Jadi yang dimaksud dengan titik didih adalah suhu pada saat tekanan uap jenuh cairan itu sama dengan tekanan udara luar (tekanan pada permukaan cairan ).
2. Buatlah table yang memperlihatkan perbedaan antara Ke-4 teknik destilasi yaitu destilasi biasa, vaccum, uap, dan destilasi fraksional?
Jawab :
Table 1 koaparasi beberapa teknik destilasi
titik didih
3. Beberapa titik didih dari senyawa anilin dan benzene ini pada tekanan 1 Atm?
Jawab : titik didih anilin 457,6 K sedangkan titik didih benzen 80,1 °C (353,2 K)
4. Jelaskan penggunaan Hukum Raoult dalam kaitannya dengan proses destilasi?
Jawab : Destilasi adalah pemisahan campuran cairan-cairan berdasarkan titik didih. Apabila titik didih dari suatu campuran yang akan dipisahkan rendah maka campuran itu akan mudah di distilasi. Penerapan hukum dalam destilasi yaitu hukum raoult
Menurut Raoult, tekanan parsial suatu komponen setara dengan hasil kali
tekanan uap komponen murni dengan fraksi mol komponen tersebut di
dalam suatu campuran, sesuai dengan Hukum Raoult:
Di mana, PA = tekanan parsial komponen A dalam campuran
PA0 = tekanan uap zat A dalam keadaan murni
XA = fraksi mol komponen A dalam campuran
Pascapraktek
1. Apakah fungsi batu didih dapat digantikan dengan bahan lain, jelaskan jawaban saudara?
Jawab:
Fungsi batu didih merupakan alat yang digunakan untuk meratakan panas pada larutan yang akan didestilasi. Selain itu batu didih ini digunakan agar tidak terjadi percikan yang dapat merusak perlatan destilasi selama destilasi berlangsung. Pori-pori dalam batu didih akan membantu penangkapan udara pada larutan dan melepaskannya ke permukaan larutan (ini akan menyebabkan timbulnya gelembung-gelembung kecil pada batu didih). Tanpa batu didih, maka larutan yang dipanaskan akan menjadi superheated pada bagian tertentu, lalu tiba-tiba akan mengeluarkan uap panas yang bisa menimbulkan letupan/ledakan (bumping).
Fungsi batu didih dapat digantikan dengan media lain yang terbuat dari keramik, pecahan kaca, maupun batu kapur selama media tersebut berisifat inert atau tidak bereaksi dengan larutan yang digunakan.
2. Tentukan presentasi anilin yang diperoleh? Jawab:
Volume benzena yang dihasilkan = 37 ml
%rendemen=volume hasilvolume awal x100 %=3750mlml x100 %=74 %
Jawab:
DAFTAR ISI
I. Tujuan... 1
II. Landasan Teori... 1
III. Prosedur Kerja... 4
III.1Alat dan Bahan... 4
III.2Skema Kerja... 4
IV. Hasil dan Pembahasan... 6
IV.1 Hasil dan Perhitungan... 6 IV.2 Pembahasan... 6 V. Kesimpulan dan Saran... 13
V.1 Kesimpulan... 13
V.2 Saran... 13