Pestisida secara umum mencakup bahan kimia yang digunakan untuk
membunuh atau mengendalikan organisme yang merugikan manusia, tumbuhan,
ternak dan sebagainya yang diusahakan manusia. Insektisida diazinon merupakan
salah satu pestisida untuk racun serangga, termasuk golongan organofosfat dari
grup fosforotioat/fosforotionat mengandung unsur karbon dan fosfor serta dapat
mengganggu sistem syaraf manusia. Insektisida golongan ini bekerja sangat efektif
menghambat aktifitas enzim asetilkolinesterase (AchE) sebagian besar serangga,
dan mengakibatkan akumulasi asetilkolin (Ach) dan tidak dapat berfungsi lagi
sebagai neurotransmitter, kemudian akan mengakibatkan kontraksi otot yang diikuti
dengan kelemahan, hilangnya refleksi (kelumpuhan) dan paralisis jaringan.
Asetilkolin berlebihan menyebabkan tremor, kejang-kejang dan kematian. Enzim
asetilkolinesterase dibutuhkan untuk fungsi sistem syaraf (Lu 1995; Zhang &
Pehkonen 1999).
Diazinon merupakan insektisida yang sangat efektif digunakan untuk
memberantas dan membasmi, ataupun mengendalikan hama-hama tanaman
seperti kutu daun, lalat, wereng, kumbang penggerek padi, dan sebagainya.
Diazinon umumnya digunakan pada tanaman buah, padi, tebu, jagung, tembakau
dan tanaman hortikultura.
Insektisida dengan bahan aktif diazinon mempunyai nama dagang yang
beragam diantaranya : basazinon 45 EC, basminon 60 EC, basudin 60 EC, basudin
10 G, brantasan 450 EC, diazinon 60 EC, sidazinon 600 EC, dazzel, nucidol,
agrostar 600 EC, gardentox, kayazol, knox out, spectracide dan prozinon 600 EC
(Frederick 2003). Insektisida ini sudah dilarang penggunaannya untuk tanaman
padi berdasarkan Instruksi Presiden Republik Indonesia No. 3 Tahun 1986 (Anonim
1987), namun sampai tanggal 1 Mei tahun 1997, saat masa beredarnya habis,
sesuai dengan Keputusan Menteri Pertanian No. 473/KPTS/TP.270/6/96,
insektisida tersebut masih beredar dan masih digunakan oleh petani. Hal ini
terbukti hasil penelitian pada akhir 1997 (Ngabekti 1998) yang ternyata masih
ditemukan residu diazinon pada sayuran kubis, selada dan tomat yang dipasarkan
di Kota Semarang dengan residu 0.0069-0.0591 ppm.
Insektisida golongan ini
cukup stabil di lingkungan, sehingga mengakibatkan masalah kesehatan manusia
dan lingkungan.
Diazinon memiliki nama kimia (0.0-dietil
0-2-isopropyl-6-metilpyrimidin-4-methyl pyrimidinyl fosfosrotionat) dengan rumus empiris C
12H
21N
2O
3P
5adalah
insektisida dan nematisida non sistemik berspektrum luas (broad spectrum) dan
bertindak sebagai inhibitor asetilkolinesterase berakibat pada kolin (Sumner et al.
1988; EXTONET 1996). Rumus bangunnya disajikan pada Gambar 2.
Gambar 2. Rumus bangun diazinon (Zhang & Pehkonen 1999)
2.1.2. Sifat Fisik, Kimia dan Biologi Diazinon
Sifat fisik diazinon yang berkaitan dengan lingkungan adalah mempunyai
titik didih 83-84
oC, tekanan uap 1.4 10
-4mmHg pada 20
oC, koefisien partisi
oktanol-air adalah 4, kelarutan dalam oktanol-air 40 µg ml
-1pada 25
oC, sedikit larut dalam air
(kira-kira 0.04%) dan dapat dicampur dengan pelarut organik (Merck Index 1998). Stabil
dalam lingkungan alkali lemah tetapi sedikit terhidrolisis dalam air dan asam encer.
Diazinon sangat sensitif terhadap oksidasi dan suhu tinggi, serta cepat terurai pada
suhu di atas 100
oC (Hayes & Laws 1991).
Matsumura (1976) menyatakan bahwa sebagian besar diazinon mengalami
degradasi membentuk asam dietiltiofosfonat. Persisten diazinon dalam air tawar
dan air laut masing-masing adalah 11% dan 30% setelah aplikasi 17 hari,
sedangkan residu dalam lumpur permukaan (2 mm) masih terdapat 0.05-2%
setelah 21 hari aplikasi.
Diazinon sangat mobil pada tanah dengan kandungan bahan organik
rendah sampai sedang, dan immobil pada kandungan bahan organik tinggi
(Arienzo et al. 1994). Koefisien partisi oktanol-air mengindikasikan diazinon bisa
diakumulasi secara biologis dalam organisme, dan ini telah dijumpai pada ikan
pada konsentrasi maksimum 300-360 kali konsentrasi di air. Volatilitas diazinon
adalah 2.4 mg m
-3pada 20
oC dan 18.6 mg m
-3pada 40
oC. Diazinon mempunyai
waktu paruh (half-life) 30 hari dan koefisien serap oleh tanah K
oc=1.000 E
(Wauchope et al. 1992), sedangkan konsentrasi diazinon sebesar 0.2-5.2 mg l
-1dapat membunuh ikan (Smith et al. 2007)
Diazinon mempunyai spektrum daya bunuh yang luas terhadap serangga
dan berbagai cacing tanah. Toksisitas diazinon terhadap mamalia adalah sedang
(II), dengan lethal doses (LD
50) oral akut masing-masing 96-967 mg kg
-1pada tikus
jantan dan 66-635 mg kg
-1pada tikus betina dan LD
50dermal akut masing-masing
tikus adalah >2000 mg kg
-1(katagori III), LD
50inhalasi akut pada tikus 3.5 mg l
-1termasuk kategori III (Pesticide Fact Handbook 1986). LD
50untuk beberapa spesies
burung 3-40 mg kg
-1dan spesies ikan 0.4-8 µg ml
-1(Sumner et al. 1985 laporan
CIBA-GEIGY tidak dipublikasi).
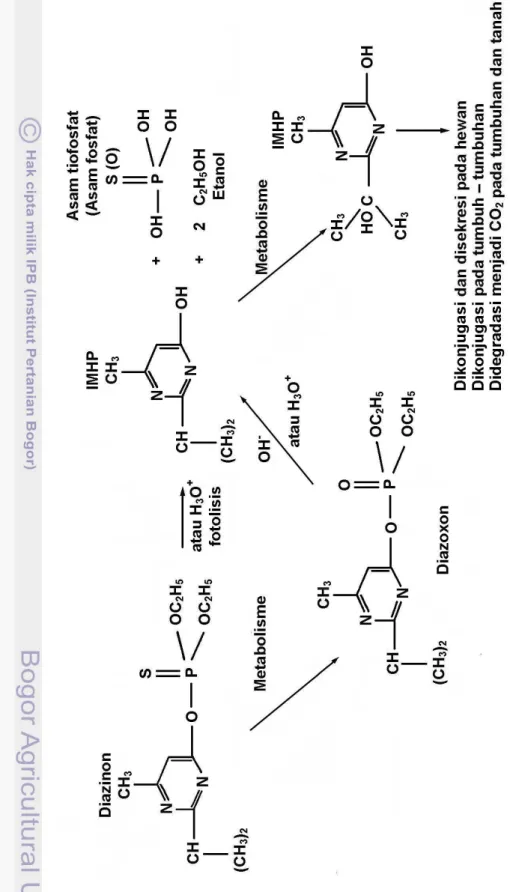
2.1.3. Alur Biokimia pada Reduksi Diazinon di Alam
Residu pestisida secara alamiah dapat hilang atau terurai dengan baik
dalam lingkungan abiotik maupun lingkungan biotik. Faktor-faktor yang
berpengaruh dalam penguraian pestisida adalah penguapan, pencucian, pelapukan
dan dengan degradasi baik secara kimia, biologi maupun fotokimia. Hidrolisis
diazinon menjadi IMPH (2-isopropyl-4-methyl-6-hydroxy pyrimidine) terutama diatur
oleh proses abiotik, degradasi dari diazinon meningkat oleh mikroorganisme tanah,
sehingga mikroorganisme menjadi faktor yang lebih dominan dari faktor abiotik
(Leland 1998).
Formulasi diazinon terdegradasi menjadi sejumlah tetraetilpirofosfat,
menghasilkan sulfotepp (S,S-TEPP) dan monothiotepp (O,S-TEPP), kedua
senyawa tersebut mempunyai sifat toksik yang lebih tinggi dibandingkan diazinon
dan merupakan inhibitor enzim kolinesterase terutama O,S-TEPP yaitu 14000 kali
lebih toksik dari diazinon (Allender & Britt 1994). Oksidasi diazinon menjadi bentuk
diazoxon yang lebih toksik, terjadi pada jaringan hewan dan tumbuhan (Mc Ewen &
Stevenson 1989). Pada vertebrata, oksidasi terjadi di mikrosom hati, dalam kondisi
ada oksigen dan NADPH
2. Pada insekta, oksidasi terjadi dalam lemak tubuh dan
metabolitnya dikeluarkan. Kecepatan oksidasi diazinon menjadi diazoxon, dua kali
lipat untuk setiap kenaikan suhu 10
oC dari 10
o–60
oC, diazoxon tidak bisa diisolasi
dari tanah (Leland 1998). Selanjutnya dikatakan bahwa degradasi diazinon lebih
cepat pada air dengan suhu lebih hangat, maka degradasi menjadi 2-4 kali lebih
cepat pada air dengan suhu 21
oC dibandingkan pada air dengan suhu (Moore et
al. 2007).
Proses pembentukan metabolit diazinon (reaksi transformasi enzimatik)
terjadi melalui reaksi primer yaitu hidrolisis yang diikuti oleh reaksi pemecahan
rantai cincin diazinon, sehingga diazinon terdegradasi pada reaksi primer menjadi
2-isopropyl-4-methyl-6-pyrimidinol (IMP) dan tiofosfonat. Menurut Ku et al. (1997)
bahwa diazinon mengalami dekomposisi secara fotolisis pada pH 3 menghasilkan
bentuk organik antara yang bisa diekspresikan sebagai jumlah dari
2-isopropyl-4-methyl-6-pyrimidinol (IMP) dan tiofosfonat sebagai C diikuti dengan pembentukan
ion SO
4-2. Produk hidrolisis dan fotolisis tersebut diidentifikasi sebagai senyawa
yang sifat toksiknya lebih rendah dibandingkan senyawa diazinon (Bollag 1974).
Degradasi diazinon di air disebabkan oleh hydrolisis, terutama pada kondisi
asam. Pada kondisi air streril half life diazinon selama 12 hari pada pH 5 dan pada
air netral half life selama 138 hari pada pH 7 (US-EPA 2006). Diazinon mengalami
degradasi dengan cahaya membutuhkan waktu 17.3-37.4 jam (Howard 1991) dan
di tanah akan terurai menghasilkan CO
2(Roberts & Hutson 1999). Degradasi
diazoxon yang diaplikasi pada tanah silt loam pada pH 8.1 dan suhu 25
oC
ditemukan mengikuti kurva linier dan half-life dalam tanah ditemukan 18 jam
(Getzin 1968). Half-life diazinon studi laboratorium di tanah dengan pH 7.8 selama
39 hari (US-EPA 2007).
Diazinon
dan
diazoxon
dihidrolisis
menjadi
2-isopropyl-4-metil-6-hydroxypyrimidine (IMHP) yang memiliki toksisitas sangat rendah dan ada dalam
dua bentuk isomer yaitu keton dan enol. Pada pH 8.4 kecepatan hidrolisis
diazoxon, adalah 10 kali diazinon. Diazinon dan diazoxon masing-masing dikatalis
dalam kondisi asam dan basa. Pada kondisi pH air alami 5.5-8.5 dan suhu kurang
dari 25
oC, residu diazinon akan bertahan lama Gomma et al. (1969). Hidrolisis di
dalam tanah, nampaknya diadsorpsi dari pada dikatalisis asam (Konrad et al.
1967). Degradasi diazinon yang terjadi melalui proses biotik dan abiotik ditunjukan
pada Gambar 3.
G
a
m
b
a
r 3
. D
e
g
radas
i di
a
zi
n
o
n
y
ang
ter
ja
di
m
el
al
u
i
pr
os
e
s
b
iot
ik
dan ab
io
ti
k
(Lel
and 1998)
2.1.4. Keberadaan Diazinon di Lingkungan
Interaksi senyawa pestisida dan lingkungan tanah diatur oleh tiga faktor
penting yaitu: 1) Proses sorpsi atau desorpsi; 2) Difusi – pencucian; 3) Degradasi.
Perpindahan dan penghilangan senyawa pestisida dalam tanah terjadi karena:
pencucian
(leaching),
aliran
buangan,
penguapan,
degradasi
kimia,
fotodekomposisi dan biodegradasi (Connel 1995).
Aplikasi insektisida di lingkungan tidak hanya mempengaruhi jumlah dan
aktifitas metabolik mikroorganisme, tetapi juga bisa merubah struktur komunitas
mikroorganisme dalam tanah, beberapa mikroorganisme bisa tertekan dan lainnya
berkembangbiak (Johansen et al. 2001). Akumulasi pestisida disebabkan adanya
adsorbsi oleh alam melalui tanah, air dan makhluk hidup lainnya (Tarumingkeng
1992). Diazinon bisa diserap oleh akar tanaman dan di translokasikan pada
tanaman dan cepat didegradasi di daun, buah dan rumput-rumputan dengan half
life berkisar 2-14 hari (Kamrin 1997). Diazinon di tanaman mengalami metabolisis
menghasilkan produk hidrolisis pyrimidinol (hydroxyl pyrimidinol) dan diazoxon
(Robert & Hutson 1999).
Selanjutnya dikatakan bahwa pestisida yang tertinggal di biosfer harus
didegradasi agar menjadi berkurang atau hilang secara keseluruhan. Diazinon
dilepas ke air permukan atau tanah melalui volatilisasi, fotolisis, hidrolisis dan
biodegradasi. Biodegradasi pada kondisi aerob merupakan alur proses utama
diazinon di tanah dan air (ATSDR 2008) dan degradasi diazinon pada kondisi
anaerob juga berlangsung baik. Half life diazinon di tanah dipengaruhi oleh pH
pada tanah dan tipe tanah, pada pH 4, 7 dan 10, half life diazinon adalah 66, 209
dan 153 hari. Kecepatan degradasi di alam maupun di dalam tumbuhan mengikuti
kimia ordo pertama yaitu kecepatan degradasi dipengaruhi oleh banyaknya
pestisida dan faktor waktu. Proses degradasi berlangsung dalam dua tahap yaitu
proses dissipasi dan persistensi. Residu pestisida dalam tanaman atau hewan
menurun atau hilang akibat metabolisme yang berkaitan dengan pertumbuhan
tanaman atau hewan tersebut (Leland 1998).
Secara alamiah di lingkungan yang tercemar diazinon, mengandung aneka
ragam mikroorganisme, sehingga polutan yang ada di lingkungan tersebut dapat
didegradasi. Degradasi diazinon di alam tidak hanya dilakukan oleh
mikroorganisme yang ada di lingkungan (mikroorganisme indigenous), tetapi
dengan adanya cahaya diazinon juga dapat terdegradasi. Mikroorganisme butuh
waktu yang sangat lama untuk beradaptasi dengan bahan/senyawa pencemar
(residu pestisida), yang disebabkan karena mikroorganisme tersebut tidak pernah
berhubungan langsung dengan residu pestisida tersebut. Oleh karena itu perlu
suatu adaptasi dimana dalam proses adaptasi mikroorganisme tersebut berusaha
mengeluarkan enzim atau plasmid yang dapat mendetoksifikasi senyawa yang
akan didegradasi.
2.2. Teknik Pengolahan Diazinon dalam Limbah Cair
Ada beberapa teknik penanganan yang digunakan untuk mengolah limbah
cair yang meliputi metode fisika, kimia dan biologi. Cara-cara yang digunakan yaitu
penyaringan/filtrasi,
absorbsi,
sedimentasi/pengendapan,
elektrodialisis,
penambahan zat pereaksi (seperti CaO, logam hidroksida), bioremediasi,
fitoremediasi, bioremediasi kompos dan biofilter (US-EPA 1998). Upaya
meningkatkan kemampuan degradasi residu diazinon bisa dilakukan dengan
mempertahankan kondisi optimal untuk kelangsungan bioremediasi dan
penambahan mikroorganisme yang mampu mendegradasi diazinon (Leland 1998)
Pengolahan residu diazinon secara biologi bisa dilakukan dengan
bioremediasi, yaitu penambahan mikroorganisme pada air yang tercemar diazinon,
atau dengan memperkaya mikroorganisme indigenous, misalnya Arthobacter sp.
dan Streptomyces sp. secara sinergis keduanya mampu mendegradasi diazinon
(Leland 1998). Selanjutnya Leland (1998) mengisolasi Flavobacterium sp. dari air
irigasi sawah yang menggunakan diazinon, mengatakan spesies ini mempunyai
keistimewaan bisa memetabolis diazinon sebagai sumber karbon, selanjutnya
diazinon dalam air irigasi yang diinkubasi diubah menjadi metabolit dalam 3 hari
dan kemudian mineralisasi menjadi CO
2dalam waktu 2 hari berikutnya.
Beberapa spesies bakteri bisa memanfaatkan diazinon sebagai sumber
karbon dan energi, seperti Pseudomonas sp. (Ramanathan & Lalithakumari 1999),
Agrobacterium sp. (Ghassempour et al. 2002; Yasouri 2006), Arthrobacter sp.
(Ohshiro et al. 1996) dan Flavobacterium sp. (Ghassempour et al. 2002). Bakteri
Serratia sp juga mempunyai kemampuan mendegradasi insektisida organofosfor
lainnya secara sempurna (Cycon et al. 2009; Lakshmi et al. 2008; Rani et al. 2008).
Di tanah tercemar diazinon terdapat isolate bakteri Bacillus, Pseudomonas mampu
menurunkan konsentrasi diazinon 3 ppm dirombak selama 12 hari (Setyobudiarso
2008).
2.3. Bioremediasi dan Biodegradasi
Akhir-akhir ini, teknik bioremediasi banyak digunakan untuk penanganan
pengolahan limbah di industri. Teknik bioremediasi dinilai efektif dan ekonomis
untuk membersihkan tanah, permukaan air dan kontaminasi tanah yang
mengandung sejumlah bahan beracun seperti rekalsitran, senyawa kimia.
Bioremediasi merupakan bagian dari bioteknologi lingkungan yang memanfaatkan
proses alami biodegredasi dengan menggunakan aktifitas mikroorganisme yang
dapat memulihkan lahan tanah, air dan sendimen dari kontaminan terutama
senyawa organik (Yani et al. 2003), teknik teknologi rendah, mudah diterima
masyarakat dan bisa digunakan dimana saja (Kamuludeen et al. 2003).
Biodegradasi umumnya dilakukan oleh kelompok utama mikroorganisme
tanah (fungi, bakteri dan actynomycetes) yang dapat secara mudah menyesuaikan
diri atau mendegradasi pestisida melalui proses oksidasi, pemutusan-ester,
hidrolisis ester, dan amida, oksidasi alkohol dan aldehida, dealkilasi, hidroksilasi,
dehidrogenasi, epoksidasi, dehalogenasi, reduksi dan dealkilasi (Matsumura 1973,
Strong & Burges 2008). Biodegradasi merupakan penguraian suatu senyawa
menjadi yang lebih sederhana melalui aktifitas mikroorganisme (Onshiro et al.
1996). Said dan Fauzi (1996) menerangkan bahwa biodegradasi merupakan
transformasi struktur dalam senyawa oleh pengaruh biologis sehingga terjadi
perubahan integritas molekuler. Dalam proses degradasi, kondisi lingkungan
harus sesuai dengan pertumbuhan dan perkembangan mikroorganisme.
Bioremediasi merupakan proses degradasi bahan organik berbahaya
secara biologi menjadi senyawa lain misalnya CO
2, metan, air, garam organik,
biomassa dan hasil samping yang sedikit lebih sederhana dari senyawa semula
(Citroreksoko 1996). Berbagai bahan pencemar umumnya senyawa senobiotik
(asing di alam) misalnya residu pestisida, deterjen, limbah eksplorasi dari
pengolahan minyak bumi dan residu amunisi. Senyawa tersebut bersifat rekalsitran
(sulit didegradasi) sehingga memiliki ketahanan yang tinggi di alam.
Manfaat lain dari bioremediasi selain mendegradasi polutan, juga dapat
menjerap bahan-bahan logam dan mineral serta memisahkan zat-zat yang tidak
diinginkan dalam udara, air, tanah dan bahan baku proses produksi dalam industri
(US-EPA 1998). Bioremediasi dapat dilakukan secara in situ dan ex situ. In situ
yaitu bioremediasi dilakukan langsung di lingkungan yang tercemar (contohnya
pengggunaan kompos dan penambahan mikroorganisme yang sesuai langsung
pada tanah tercemar), sedangkan ex situ yaitu bioremediasi dilakukan di luar
lingkungan yang tercemar dengan membuat lingkungan baru bioreaktor yang
dikondisikan dengan menggunakan inokulan yang dapat mendegradasi cemaran
kontaminan organik, misalnya penggunaan biofilter untuk reduksi limbah cair di
bidang pertanian (Citroreksoko 1996). Teknologi bioremediasi dapat dimanfaatkan
sebagai salah satu teknik dalam penanganan limbah senyawa kimia termasuk
pestisida.
Beberapa penelitian terdahulu dilaporkan bahwa penggunaan kompos
dalam proses bioremediasi telah terbukti efektif untuk mendegradasi banyak jenis
kontaminan seperti hidrokarbon terklorinasi dan tidak terklorinasi, bahan-bahan
kimia pengawet kayu, pelarut, logam berat, pestisida produk minyak, bahan
peledak dan senyawa-senyawa senobiotik lainnya (US-EPA 1999; Gray et al. 1999;
Baker & Bryson 2002). Bakteri aerob dari kompos seperti Pseudomonas sp,
Alcaligenes
sphingomonas,
Rhodococcus
dan
Mycobacterium,
mampu
mendegradasi pestisida, hidrokarbon, senyawa alkana dan poliaromatik (fenol,
benzoate, benzene dan turunannya), bakteri ini menggunakan kontaminan sebagai
sumber karbon dan energi (Haigler et al. 1992; Vidali 2001).
Kompos limbah pertanian dan kotoran ternak dapat mengurangi DDT dari
tanah tercemar di atas 600 ppm DDT (1.1.1-trichloro-2.2-bis (p-chlorophenyI ethan)
menjadi kurang dari 140 ppm setelah pengomposan 4 minggu, tanpa dihasilkan
DDD (1.2 dichloro-2.2-bis (p-chlorophenyl ethan) dan DDE (2.2-bis (p-chlorophenyl)
1.1 dichloroethylene) (Bernier et al. 1997). Tanah yang tercemar lebih dari satu
senyawa nitro seperti TNT (trinitrotoluene), RDX (hexahydro-1.3.5 trinitro-1.3.5
triazine) dan HMX (octahydro-1.3.5.7 tetranitro-1.3.5.7 tetrazocine) dengan
konsentrasi di atas 20.000 ppm, konsentrasinya berkurang 90% dengan
menggunakan kompos campuran (Moser et al. 1999). Selanjutnya menurut Gray et
al. (2000) bahwa kompos limbah pertanian berhasil mengurangi konsentrasi khlorin
dari tanah tercemar senyawa klorin (methoxychlor) 600 ppm berkurang menjadi
140 ppm setelah pengomposan 4 minggu.
Kompos digunakan untuk memperbaiki tanah yang terkontaminasi dengan
berbagai polutan organic (Fermor et al. 2001). Kompos juga digunakan untuk
bioremediasi limbah hidrokarbon, mampu mendegradasi minyak pelumas 75%
(Suortti et al. 2000); minyak diesel 85% (Ryckeboer et al. 2003); minyak 88.25%
(Munawar et al. 2007). Bakteri yang ditemukan pada tanah yang terkontaminasi
minyak hidrokarbon yaitu: Azotobacter sp., Bacillus alvei, B. macerans, B.
laterosporus, B. larvae, B. megaterium, Pseudomonas putida, Micrococcus roseus,
dan bakteri yang terdapat dalam kompos dari sampah kota, yang terkontaminasi
minyak hidrokarbon yaitu: Azotobacter sp., Bacillus cereus, Pseudomonas
aeruginosa, Micrococcus agalis, M. roseus, Mycobacterium sp., Nocardia sp.,
(Pagoray 2009).
2.3.1. Faktor-faktor yang mempengaruhi Biodegradasi
Mengingat mikroorganisme sangat berperan penting dalam proses
degradasi, maka kondisi lingkungan yang maksimal mendukung aktifitas
mikroorganisme akan memaksimalkan proses biodegradasi. Keberhasilan proses
biodegradasi banyak ditentukan oleh aktifitas enzim dalam mikroorganisme.
Kemudian aktifitas mikroorganisme dioptimasikan dengan pengaturan kondisi dan
pemberian suplemen yang sesuai. (Vidali 2001).
Keberadaan oksigen dibutuhkan untuk pertumbuhan bakteri aerob dan
merupakan faktor pembatas laju degradasi hidrokarbon. Oksigen digunakan untuk
mengkatabolisme senyawa hidrokarbon dengan cara mengoksidasi substrat
dengan katalisis enzim oksidase (Vidali 2001). Tingkat keasaman (pH) juga
merupakan faktor yang mempengaruhi laju pertumbuhan mikroorganisme.
Umumnya bakteri tumbuh baik pada kisaran pH netral (pH 6.5–7.5), seperti P.
aeruginosa yang tumbuh pada kisaran pH 6.6–7.0 dan mampu bertahan pada
kisaran pH 5.6–8.0. Suhu akan berpengaruh terhadap sifat fisik dan kimia,
kecepatan degradasi oleh mikroorganisme serta komposisi mikroorganisme selama
proses degradasi. Pertumbuhan efektif untuk mikroorganisme berkisar antara 45
o–
59
oC (US-EPA 1994).
Mikroorganisme membutuhkan nutrisi sebagai sumber karbon, energi dan
keseimbangan metabolisme sel. Menurut Boopathy (2000), kemampuan
mendegradasi
tergantung
pada
mikroorganisme
(konsentrasi
biomassa,
keanekaragaman populasi dan aktifitas enzim), substrat (karakteristik fisikokimia,
struktur molekul dan konsentrasi), serta faktor lingkungan (pH, suhu, kelembaban,
tersedianya akseptor elektron sebagai sumber karbon dan energi). Selain itu
struktur molekul dan konsentrasi kontaminan berpengaruh sangat kuat dalam
proses bioremediasi. Bakteri pendegradasi diazinon, Serratia sp. mampu
memanfaatkan diazinon sebagai sumber karbon dan fosfor pada keadaan pH
7.0-8.0 dan degradasi terhambat pada pH 5, 6 dan 9, 10. Bakteri ini juga mampu
mendegradasi diazinon secara sempurna dalam waktu 11 hari pada suhu 25
o-30
oC,
tetapi dalam waktu 13 hari pada suhu 20
oC (Amer 2011).
2.4. Biofilter Kompos
Biofilter adalah teknologi inovatif untuk menangani air atau udara yang
tercemar kontaminan melalui media filter untuk tempat hidup mikrooganisme pada
reaktor, dan diharapkan kontaminan diuraikan menjadi senyawa yang lebih
sederhana dan tidak berbahaya yaitu H
2O dan CO
2. Umumnya pada biofilter
diinokulasi dengan mikroorganisme kultur campuran dimana akan terjadi seleksi
alamiah sehingga diperoleh satu jenis/lebih mikroorganisme yang dapat
beradaptasi dengan lingkungan (US-EPA 1998).
Teknologi biofilter yang umum digunakan adalah penggunaan campuran
pasir dan krikil yang dibungkus atau karbon aktif kemudian ditambahkan
mikroorganisme. Masalah yang timbul umumnya pasir dan krikil mempunyai
kemampuan menjerap rendah, sehingga bahan ini tidak baik digunakan sebagai
media untuk hidup mikroorganisme. Kemudian berkembang teknologi penggunaan
kompos sebagai media filter untuk reduksi limbah cair. Biofilter kompos lebih
menguntungkan dibandingkan karbon aktif granular karena masa pakai panjang 1-
1.5 tahun sedangkan karbon aktif granular sangat singkat (Casucci et al. 2004).
Pada biofilter kompos, kompos berperan sebagai penyaring (filter), dan
penyerap (absorben) zat kimia yang akan dilewatkan pada biofilter tersebut.
Fungsi ini dapat dianalogikan dengan fungsi tanah dan sendimen sebagai bahan
yang dapat menghilangkan pencemar di lingkungan, melalui proses penyerapan
pada permukaan sehingga menstabilkan pH, selanjutnya menguraikan zat
pencemar (Connell 1995).
Kelebihan kompos sebagai media filter (biasanya untuk aliran limbah cair)
adalah karena memiliki porositas tinggi, kapasitas absorbsi tinggi terhadap
senyawa organik dan anorganik, retensi kelembaban baik, dan kemampuan
mendukung kecepatan degradasi tinggi (US-EPA 1998). Kapasitas absorbsi
kompos terhadap senyawa organik dan anorganik bisa melalui beberapa
mekanisme penyerapan seperti: gaya vander waal, ikatan hidrofobik, ikatan
hidrogen, pertukaran ligan, pertukaran ion elekrostatik, interaksi tertutup dan
penyerapan kimia (Connell 1995). Kemampuan penyerapan terhadap suatu zat
kimia ditunjukkan oleh koefisien penyerapan (Haque et al. 1980). Selanjutnya
menurut Connell (1995) faktor-faktor yang mempengaruhi penyerapan senyawa
kimia adalah struktur zat kimia, kandungan bahan organik, pH media, ukuran
partikel, kapasitas tukar elektron dan suhu.
Karakteristik biofilter kompos sebagai berikut: kapasitas pegang air (water
holding capacity) dan total porositas tinggi; kinerja bertambah baik dengan
bertambahnya waktu; terjadi penambahan nutrien; kelembaban antara 50-70%;
suhu antara 20
o–30
oC; waktu tinggal (residence time) singkat; dan kedalaman filter
satu meter (Leson 1991; Haug 1993; Toffey 1997). Pada awalnya aplikasi biofilter
kompos untuk menguraikan gas hydrogen sulfite (83-99%) dan beberapa senyawa
aromatik sederhana. Selanjutnya aplikasi biofilter kompos berkembang untuk
menguraikan larutan chlorin alifatik dan senyawa mudah menguap lainnya/VOC
(Ergas 1995).
2.5.
Kompos dari Limbah Media Jamur Tiram
Kompos sebagai hasil akhir pengomposan, memiliki kandungan bahan
organik tinggi dan mineral yang penting untuk pertumbuhan tanaman. Kompos
juga digunakan sebagai bahan penyerap (absorben) yang baik, terutama untuk
senyawa kimia organik dan anorganik (US-EPA 1994). Hasil samping produksi
jamur adalah limbah media budidaya jamur yang masih bisa digunakan sebagai
kompos/pupuk dan makanan ternak. Maher dan Magette (1997) mengemukakan
bahwa hasil analisis ekstrak kompos jamur di Irlandia mengandung bahan organik
65%, makro nutrien tinggi (nitrogen, phosphor, kalium dan kalsium), pH 6.6, dan
electricity conductifity/konduktifitas listrik tinggi (7.500 µS cm
-1).
SMC (spent mushroom compost) adalah kompos dari limbah media
budidaya jamur, mengandung konsorsium mikroorganisme di antaranya
Paenibacillus lentimorphus, Bacillus lecheniformis, B. subtilis, Pseudomonas
meralanii,
Klebsiella
enterobacter
sp.
Sphingobacterium
multivarum,
Microbacterium, Stenophomonas sp. (Watabe et al. 2004). Bakteri tersebut bisa
mengganggu kesehatan manusia dan hewan, contohnya Bacillus sp. merupakan
pathogen pada debu, menimbulkan alergi, hipersensitif, pneumonitis. Kompos dari
bekas media jamur P. pulmonarius yang mendegradasi substrat dengan bahan
dasar dedak padi mengandung chitin 25% merupakan polimer
N-asetil-d-glukosamin (Law et al. 2003) dan sebagian besar komponen dari dinding sel fungi
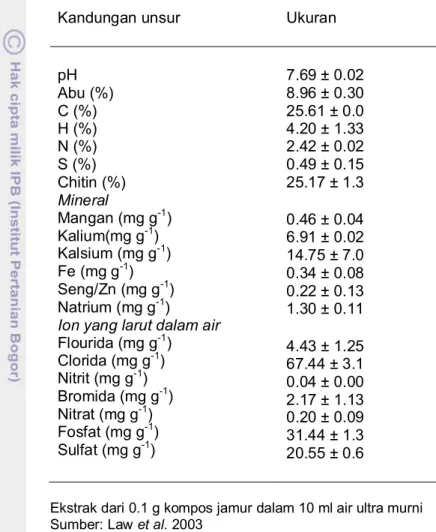
dan kandungan unsur lainnya tertera pada Tabel 1.
Kompos jamur mempunyai beberapa keuntungan jika ditambahkan ke
tanah, yaitu menambah nutrisi esensial bagi tanaman; menggantikan pupuk
organik; sumber fosfor, kalium dan elemen trace juga nitrogen; kandungan bahan
organik tinggi, sehingga penting untuk memperbaiki struktur tanah; meningkatkan
aktifitas
mikroorganisme
tanah
dan
cacing
tanah;
dan
memudahkan
menghancurkan struktur tanah pada saat pengolahan tanah (Glass 2003).
Tabel 1 Sifat fisika-kimia kompos jamur media Pleurotus pulmonarius
Kandungan unsur
Ukuran
pH
Abu (%)
C (%)
H (%)
N (%)
S (%)
Chitin (%)
Mineral
Mangan (mg g
-1)
Kalium(mg g
-1)
Kalsium (mg g
-1)
Fe (mg g
-1)
Seng/Zn (mg g
-1)
Natrium (mg g
-1)
Ion yang larut dalam air
Flourida (mg g
-1)
Clorida (mg g
-1)
Nitrit (mg g
-1)
Bromida (mg g
-1)
Nitrat (mg g
-1)
Fosfat (mg g
-1)
Sulfat (mg g
-1)
7.69 ± 0.02
8.96 ± 0.30
25.61 ± 0.0
4.20 ± 1.33
2.42 ± 0.02
0.49 ± 0.15
25.17 ± 1.3
0.46 ± 0.04
6.91 ± 0.02
14.75 ± 7.0
0.34 ± 0.08
0.22 ± 0.13
1.30 ± 0.11
4.43 ± 1.25
67.44 ± 3.1
0.04 ± 0.00
2.17 ± 1.13
0.20 ± 0.09
31.44 ± 1.3
20.55 ± 0.6
Ekstrak dari 0.1 g kompos jamur dalam 10 ml air ultra murni Sumber: Law et al. 2003
Kompos jamur mempunyai karakteristik sebagai berikut: secara fisik
mengandung 65% bahan organik, sehingga bermanfaat untuk memperbaiki struktur
dan tekstur tanah, memperbaiki aerasi dan drainase, menambah kapasitas pegang
air (water holding capacity/WHC), menambah aktifitas biologis tanah; bebas dari
kontaminan benih gulma dan patogen tumbuhan; penampakan yaitu halus dan
berbau tanah; sumber nitrogen, fosfor, kalium, kalsium, sulfur; sumber elemen trace
seperti besi, natrium, mangan, boron, tembaga dan seng (Glass 2003).
Karakteristik kompos limbah media jamur dapat dilihat pada Tabel 2.
Tabel 2 Karakteristik kompos limbah media jamur
Sifat fisik
Keuntungan
Bahan organik 65%
Bebas dari polutan
Kandungan nutrisi utama
Unsur lain (dalam jumlah
kecil)
Meningkatkan struktur dan tekstur tanah.
Meningkatkan aktivitas biologis tanah
Berasal dari rerumputan dan tanaman patogen
Sumber bahan organik N, P, K, Ca, dan S
Sumber bahan organik Fe, Na, Mn, Br, Cu dan
Zn.
Sumber: Glass (2003)