SINTESIS LAKTOGENIN SUATU SENYAWA ANALOG ASETOGENIN DARI TETRAHIDRO 3 FURANKARBOKSALDEHID
DAN 2 ASETIL γ BUTIROLAKTON DALAM SUASANA BASA ETILENDIAMIN
SKRIPSI
Diajukan untuk Memenuhi Salah Satu Syarat Memperoleh Gelar Sarjana Farmasi (S. Farm)
Program Studi Farmasi
Diajukan oleh : Elya Findawati NIM : 088114053
FAKULTAS FARMASI
UNIVERSITAS SANATA DHARMA YOGYAKARTA
ii
SINTESIS LAKTOGENIN SUATU SENYAWA ANALOG ASETOGENIN DARI TETRAHIDRO 3 FURANKARBOKSALDEHID
DAN 2 ASETIL γ BUTIROLAKTON DALAM SUASANA BASA ETILENDIAMIN
SKRIPSI
Diajukan untuk Memenuhi Salah Satu Syarat Memperoleh Gelar Sarjana Farmasi (S. Farm)
Program Studi Farmasi
Diajukan oleh : Elya Findawati NIM : 088114053
FAKULTAS FARMASI
UNIVERSITAS SANATA DHARMA YOGYAKARTA
2011
PLAGIAT MERUPAKAN TINDAKAN TIDAK TERPUJI
iv
PLAGIAT MERUPAKAN TINDAKAN TIDAK TERPUJI
v
HALAMAN PERSEMBAHAN
“
! " !
LEMBAR PERNYAT
ngan di bawah ini, saya mahasiswa Universitas San : Elya Findawati
Mahasiswa : 08 8114 053
ngan ilmu pengetahuan, saya memberikan kepada ta Dharma karya ilmiah saya yang berjudul:
TOGENIN SUATU SENYAWA ANALOG A HIDRO939FURANKARBOKSALDEHID DAN
DALAM SUASANA BASA ETILENDIAMIN t yang diperlukan (bila ada). Dengan demikian say akaan Universitas Sanata Dharma hak untuk lam bentuk media lain, mengelolanya dalam ben ikan secara terbatas, dan mempublikasikannya d k kepentingan akademis tanpa perlu meminta ri royalti kepada saya selama tetap mencantumk
vii
PRAKATA
Puji syukur kepada Tuhan Yang Maha Esa atas anugerah dan berkat yang melimpah, sehingga penulis dapat menyelesaikan penelitian dan penyusunan skripsi yang berjudul ”SINTESIS LAKTOGENIN SUATU SENYAWA
ANALOG ASETOGENIN DARI TETRAHIDRO939
FURANKARBOKSALDEHID DAN 29ASETIL9γ9BUTIROLAKTON DALAM SUASANA BASA ETILENDIAMIN”
Penulis menyadari bahwa penulis tidak dapat menyelesaikan skripsi ini seorang diri. Oleh karena adanya dukungan, bimbingan, kritik, dan saran dari berbagai pihak, penulis akhirnya dapat menyelesaikan skripsi ini. Maka pada kesempatan ini penulis hendak menyampaikan ungkapan terimakasih yang sebesar9besarnya kepada:
1. Ipang Djunarko, M.Si., Apt., selaku Dekan Fakultas Farmasi, Universitas Sanata Dharma Yogyakarta.
2. Jeffry Julianus, M.Si., selaku dosen pembimbing yang telah memberikan bimbingan dan pengarahan kepada penulis sekaligus sebagai dosen penguji atas segala masukan, kritik, dan sarannya.
3. Dra. M. M. Yetty Tjandrawati, M. Si. selaku dosen penguji atas segala masukan, kritik dan sarannya.
viii
5. Rini Dwi Astuti, M.Si, Apt., selaku kepala laboratorium Farmasi, atas ijin yang diberikan kepada penulis untuk melakukan penelitian di Laboratorium Farmasi.
6. Seluruh staf laboran Laboratorium Farmasi khususnya Pak Parlan, Pak Kunto, dan Mas Bimo yang telah banyak menemani dan membantu penulis selama melakukan penelitian.
7. Widi dan Rika sebagai sahabat dan rekan satu tim penelitian yang telah banyak membantu penulis selama melakukan penelitian dan selalu memberikan dukungan terbaik dalam suka maupun duka.
8. Helen, Lala, Tere, Sari, Heppi, Adi sebagai sahabat, teman berpetualang dan tempat berbagi cerita baik dalam suka maupun duka.
9. Natalia, Dea, Cynthia, Fajar sebagai teman kelompok praktikum A3 yang banyak membantu penulis selama kegiatan praktikum berlangsung.
10. Susi, Nona, Susan, Dina, Prasilya, Sasa, Felicia, Novi, Bravo, Winarti, Sisca, Yesi atas kebersamaan di kelompok praktikum A yang selalu menginspirasi.
11. Teman9teman angkatan 2008, khususnya minat FST yang sangat kompak selama menjalani proses perkuliahan.
12. Bernadus Meymoriardi E., S.Si. yang selalu memberikan nasihat dan dukungan baik dalam suka maupun duka.
13. Semua pihak yang tidak dapat disebutkan satu per satu, atas segala dukungan dan doa yang diberikan.
PLAGIAT MERUPAKAN TINDAKAN TIDAK TERPUJI
ix
Penulis menyadari bahwa dalam penulisan naskah skripsi ini penulis tidak luput dari kekurangan mengingat segala keterbatasan wawasan dan kemampuan penulis. Oleh karena itu, penulis membuka diri untuk menerima kritik dan saran yang membangun sehingga skripsi ini menjadi lebih baik. Akhir kata, penulis berharap semoga tulisan ini berguna bagi semua pihak, terutama untuk kemajuan ilmu pengetahuan dalam bidang Farmasi.
PE
enyatakan dengan sesungguhnya bahwa skripsi yan rya atau bagian karya orang lain, kecuali yang te n daftar pustaka, sebagaimana layaknya karya ilmi di kemudian hari ditemukan indikasi plagiarisme ersedia menanggung segala sanksi sesuai peratur erlaku
Yogyakarta, 20 Pe
Elya F
xi
DAFTAR ISI
Halaman
HALAMAN SAMPUL i
HALAMAN JUDUL ii
HALAMAN PERSETUJUAN PEMBIMBING iii
HALAMAN PENGESAHAN iv
HALAMAN PERSEMBAHAN v
LEMBAR PERNYATAAN PERSETUJUAN PUBLIKASI KARYA ILMIAH
UNTUK KEPENTINGAN AKADEMIS vi
3. Manfaat Penelitian 4
B. Tujuan Penelitian 4
xii
2. Uji Kemurnian Menggunakan Kromatografi Lapis Tipis (KLT) 11
3. Spektrofotometri UV 12
4. Kromatografi Gas 13
E. Elusidasi Struktur Senyawa Hasil Sintesis 13
1. Spektrofotometri Inframerah 13
2. Spektrometri Massa 15
F. Landasan Teori 16
G. Hipotesis 17
BAB III METODE PENELITIAN 18
A. Jenis dan Rancangan Penelitian 18
B. Variabel dan Definisi Operasional 18
C. Bahan Penelitian 19
D. Alat Penelitian 19
E. Tata Cara Penelitian 19
1. Pengenceran Etilendiamin 19
2. Sintesis Laktogenin 19
3. Uji Pendahuluan 20
a) Organoleptis 20
b) Uji Kemurnian Menggunakan Kromatografi Lapis Tipis (KLT)20 c) Uji Penentuan Panjang Gelombang Maksimum 20
d) Kromatografi Gas 21
4. Elusidasi Struktur Senyawa Hasil Sintesis 21
a) Spektrofotometri Inframerah 21
b) Spektrometri Massa 22
F. Analisis Hasil 22
1. Analisis Pendahuluan 22
2. Pemeriksaan Kemurnian Senyawa Hasil Sintesis 22
3. Elusidasi Struktur 22
BAB IV PEMBAHASAN 23
A. Sintesis Senyawa Laktogenin 23
B. Analisis Pendahuluan 27
PLAGIAT MERUPAKAN TINDAKAN TIDAK TERPUJI
xiii
1. Uji Organoleptis 27
2. Uji Kromatografi Lapis Tipis 27
3. Uji Panjang Gelombang Maksimum 30
C. Elusidasi Struktur Senyawa Hasil Sintesis 33
1. Spektrofotometri Inframerah 33
2. Spektrometri Massa 39
D. Pembentukan Produk Reaksi Samping 44
BAB V KESIMPULAN DAN SARAN 48
xiv
DAFTAR TABEL
Tabel 1. Tabel perbandingan data organoleptis starting material dengan senyawa
hasil sintesis 27
Tabel 2. Perbandingan nilai Rf antara 29asetil9γ9butirolakton dan senyawa hasil
sintesis 29
Tabel 3. Perbandingan panjang gelombang maksimum starting material dan
senyawa hasil sintesis 32
Tabel 4. Interpretasi spektra inframerah senyawa hasil sintesis 35 Tabel 5. Perbandingan interpretasi spektra inframerah senyawa hasil sintesis dan
starting material 38
PLAGIAT MERUPAKAN TINDAKAN TIDAK TERPUJI
xv
DAFTAR GAMBAR
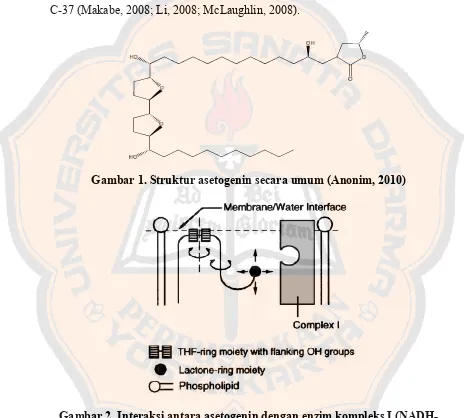
Gambar 1. Struktur asetogenin secara umum 6
Gambar 2. Interaksi antara asetogenin dengan enzim kompleks I (NADH9
ubiquinone oksidoreduktase) 6
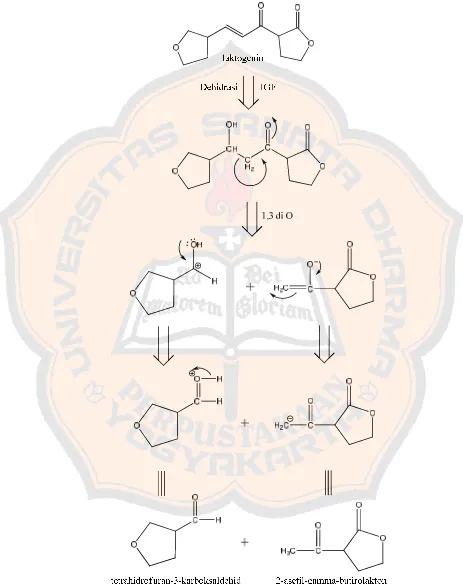
Gambar 3. Analisis diskoneksi senyawa laktogenin 10 Gambar 4. Mekanisme reaksi sintesis senyawa laktogenin secara umum 16 Gambar 5. Posisi hidrogen alfa pada 29asetil9γ9butirolakton 23
Gambar 6. Mekanisme reaksi sintesis senyawa laktogenin 25 Gambar 7. Posisi hidrogen alfa pada tetrahidro939furankarboksaldehid 26
Gambar 8. Kromatogram KLT senyawa hasil sintesis 29 Gambar 9. Ikatan hidrogen antara fase diam dengan 29asetil9γ9butirolakton 30 Gambar 10. Ikatan hidrogen antara fase diam dengan senyawa sintesis 31 Gambar 11. Spektra UV 29asetil9γ9butirolakton 31 Gambar 12. Spektra UV Tetrahidro939furankarboksaldehid 32
Gambar 13. Spektra UV senyawa hasil sintesis 33
Gambar 14. Gugus kromofor pada laktogenin 34
xvi
Gambar 21. Hasil spektra massa senyawa produk samping 44 Gambar 22. Usulan mekanisme fragmentasi senyawa produk samping 45 Gambar 23. Perkiraan struktur senyawa produk samping 46 Gambar 24. Mekanisme reaksi pembentukan senyawa produk samping 47
PLAGIAT MERUPAKAN TINDAKAN TIDAK TERPUJI
xvii
DAFTAR LAMPIRAN
Lampiran 1. Perhitungan bahan dan persamaan reaksi 52 Lampiran 2. Kromatogram KLT senyawa hasil sintesis 54 Lampiran 3. Perhitungan nilai Rf senyawa hasil sintesis 55 Lampiran 4. Perhitungan kepolaran fase gerak KLT dan log P senyawa hasil
sintesis 56
Lampiran 5. Kromatogram GC senyawa hasil sintesis 57
Lampiran 6. Kondisi setting alat GC9MS 58
Lampiran 7. Spektra massa senyawa hasil sintesis 59 Lampiran 8. Spektra massa senyawa produk reaksi samping 60 Lampiran 9. Spektra inframerah senyawa hasil sintesis 61 Lampiran 10. Spektra inframerah (IR) 29asetil9γ9butirolakton 62 Lampiran 11. Spektra inframerah (IR) tetrahidro939furankarboksaldehid 63 Lampiran 12.Keelektronegatifan 29asetil9γ9butirolakton dengan program Marvin
Sketch 64
Lampiran 13.Keelektronegatifan tetrahidro939furankarboksaldehid dengan
xviii
INTISARI
Asetogenin merupakan senyawa alam yang berasal dari golongan
Annonaceous, memiliki aktivitas antikanker melalui mekanisme inhibitor enzim
kompleks I (NADH9ubiquinone oksidoreduktase). Lipofilisitas asetogenin yang
tinggi dengan nilai log P 8,84 membuatnya memiliki kelarutan yang rendah dalam air sehingga sulit untuk digunakan secara per oral. Modifikasi yang dapat
dilakukan yaitu dengan memperpendek rantai alkilnya namun tetap mempertahankan gugus aktif γ9lakton dan tetrahidrofuran. Senyawa hasil modifikasi adalah laktogenin (39(39(tetrahidrofuran939il)akriloil)dihidrofuran9 2(3H)9on) yang mempunyai lipofilisitas lebih kecil dengan nilai log P 0,90, sehingga dapat diformulasikan dalam bentuk sediaan per oral.
Penelitian ini termasuk dalam penelitian non9eksperimental deskriptif non9analitik. Sintesis dilakukan dengan mereaksikan tetrahidro939 furankarboksaldehid 5,53 mmol (1 mL) dan 29asetil9γ9butirolakton 5,53 mmol (0,5943 mL), dalam suasana basa etilendiamin melalui reaksi kondensasi aldol silang. Analisis hasil dilakukan melalui uji organoleptis, uji kromatografi lapis tipis (KLT) dengan fase diam silika gel GF254 danfase gerak toluen : metanol (1 :
3), serta elusidasi struktur dengan spektrofotometri inframerah dan spektrometri massa.
Uji organoleptis menunjukkan bahwa senyawa hasil sintesis berupa larutan, berwarna kuning pekat, dan berbau menyengat. Hasil uji KLT menunjukkan senyawa hasil sintesis memiliki nilai Rf sebesar 0,71. Berdasarkan
hasil kromatogram GC, senyawa laktogenin memiliki kemurnian sebesar 1,72%. Hasil elusidasi struktur dengan spektrofotometri inframerah dan spektrometri massa (MS) menunjukkan bahwa senyawa hasil sintesis adalah laktogenin.
Kata kunci : laktogenin, asetogenin, antikanker, reaksi kondensasi aldol silang.
PLAGIAT MERUPAKAN TINDAKAN TIDAK TERPUJI
xix
ABSTRACT
Acetogenin is a natural compound derived from the class of Annonaceous, has an anticancer activity through the mechanism by inhibitors of complex I (NADH9ubiquinone oksidoreduktase) enzyme. Acetogenin has a high lipophilicity with log P value 8,84 makes it has a low solubility in water, so difficult to be used orally. One modification that can be done by shortening the alkyl chain is a modified structure called lactogenin (39(39(tetrahydrofurane939 yl)akriloyl)dihydrofurane92(3H)9on) that have a smaller lipophilicity with log P value 0,90, so it can be used orally.
This study is a non9experimental descriptive studies of non9analytic. Synthesis carried out by reacting 5,53 mmol (1 mL) tetrahydro939 furanecarboxaldehyde and 5,53 mmol (0,5943 mL) 29acetyl9γ9butyrolactone, using ethylenediamine through cross9aldol condensation reaction. Analysis of the results has done through organoleptis test, thin9layer chromatography (TLC) test with silica gel GF254 as stationary phase and toluene: methanol (1: 3) as mobile
phase, the determination of the maximum wavelength, and structure elucidation by infrared spectrophotometry and mass spectrometry.
Organoleptis test showed that the compounds synthesized in the form of the solution, thick yellow and smelly. TLC test results indicate compounds synthesized have a value of Rf 0,71. Based on the results of the GC
chromatogram, lactogenin compounds have a purity of 1,72%. The results of structure elucidation by infrared spectrophotometry (IR) and mass spectrometry (MS) showed that the compound is lactogenin.
1
BAB I
PENGANTAR
A. Latar Belakang
Kanker (karsinoma) merupakan suatu penyakit yang dicirikan dengan adanya pertumbuhan dan penyebaran sel yang tidak teratur ke bagian anggota tubuh lain (Corner, 2001; Balmain, Gray, and Ponder, 2003). Perkembangan sel yang tidak teratur dan terjadi dalam waktu singkat ini menyebabkan tumor tumbuh baik menjadi tumor yang bersifat jinak (benign) serta ganas (malignant
atau kanker) (Gabriel, 2007). Tumor yang bersifat ganas atau disebut dengan kanker dapat menginvasi dan menyebar ke jaringan lain (metastasis) bahkan jika
melampaui level tertentu dapat menimbulkan kematian.
Asetogenin merupakan salah satu komponen yang berasal dari tumbuhan golongan Annonaceous, sering disebut dengan Annonaceous acetogenin (Piret,
2008). Annonaceous acetogenins merupakan kelompok metabolit sekunder
dengan beberapa aktifitas biologi dan telah digunakan sebagai salah satu alternatif pilihan untuk pengembangan obat antikanker baru (Wikstrom and Saraste, 1984; Ragan, 1985; Walker, 1992; Ohnishi, 1993) karena memiliki kemampuan yakni dapat menghambat enzim NADH9ubiquinone oksidoreduktase pada rantai
respirasi sel (kompleks I mitokondria), yang merupakan gerbang utama produksi energi di dalam sel (Zeng et al., 1996; Tormo et al., 2001; Bermejo et al., 2005).
Menurut Morré et al (1995), senyawa ini juga merupakan inhibitor kuat dari
NADH oksidase yang terdapat di dalam membran plasma sel tumor. Dengan
PLAGIAT MERUPAKAN TINDAKAN TIDAK TERPUJI
dihambatnya enzim NADH9ubiquinone oksireduktase maka rantai respirasi sel
akan terputus (Gonzalez et al., 2002), sehingga ATP yang merupakan sumber
energi bagi sel tidak akan terbentuk lagi, jika hal ini berlangsung terus menerus maka sel kanker akan kekurangan pasokan energi dan kemudian lisis.
Asetogenin memiliki rantai alkil yang panjang dan strukturnya meruah sehingga mengakibatkan asetogenin bersifat sangat lipofil (Hongda, 2006). Lipofilisitas asetogenin yang tinggi dengan nilai log P 8,84 ini membuatnya memiliki kelarutan yang rendah sehingga sulit untuk digunakan secara per oral,
oleh karena itu perlu dilakukan modifikasi pada struktur agar dapat diformulasikan ke dalam sediaan per oral. Salah satu modifikasi yang dapat
dilakukan yaitu dengan memperpendek rantai alkilnya namun tetap mempertahankan gugus aktif γ9lakton dan tetrahidrofuran. Senyawa hasil modifikasi adalah laktogenin (39(39(tetrahidrofuran939il)akriloil)dihidrofuran9 2(3H)9on) yang mempunyai lipofilisitas lebih kecil dengan nilai log P 0,90, sehingga dapat diformulasikan ke dalam bentuk sediaan per oral. Bentuk sediaan per oral merupakan bentuk sediaan obat yang mudah untuk diaplikasikan ke
pasien sehingga akan meningkatkan nilai acceptabilitas.
Sintesis senyawa laktogenin dilakukan berdasarkan prinsip reaksi kondensasi aldol silang dengan starting material tetrahidro939furankarboksaldehid
dan 29asetil9γ9butirolakton. Kondensasi aldol silang merupakan suatu reaksi antara sebuah aldehida dengan suatu senyawa yang memiliki sebuah hidrogen alfa
3
tetrahidro939furankarboksaldehid merupakan senyawa golongan aldehid yang berperan sebagai elektrofil, sedangkan 29asetil9γ9butirolakton merupakan senyawa golongan keton yang berperan sebagai nukleofil.
Etilendiamin merupakan basa jenis amin primer diperlukan dalam sintesis senyawa laktogenin untuk menyediakan suasana basa sehingga dapat meningkatkan nukleofilisitas C alfa pada 29asetil9γ9butirolakton. Adanya
pasangan elektron bebas pada gugus amina (9NH2) membuatnya bersifat
elektronegatif sehingga akan mengambil hidrogen alfa pada 29asetil9γ9
butirolakton yang bersifat asam dan akan terbentuk ion enolat. Produk intermediet ion enolat bersifat reaktif sehingga diharapkan dapat mempercepat reaksi dan produk yang dihasilkan lebih banyak. Alasan pemilihan penggunaan suasana basa etilendiamin karena menurut Jose´ A et al. (2005) lakton merupakan golongan
ester yang mudah terhidrolisis oleh basa kuat terutama basa golongan hidroksida, namun γ9butirolakton merupakan jenis yang paling stabil diantara jenis lakton yang lain seperti α9asetolakton, β9propiolakton, dan δ9valerolakton. Oleh karena itu digunakan etilendiamin dengan pKb 4,02 yang merupakan suatu basa organik agar 29asetil9γ9butirolakton tidak terhidrolisis dan nukleofilisitas dari C alfa pada
29asetil9γ9butirolakton semakin meningkat sehingga dapat dihasilkan senyawa laktogenin.
PLAGIAT MERUPAKAN TINDAKAN TIDAK TERPUJI
1. Permasalahan
Apakah senyawa laktogenin dapat disintesis dari tetrahidro939 furankarboksaldehid dan 29asetil9γ9butirolakton dalam suasana basa etilendiamin?
2. Keaslian Penulisan
Sejauh pengetahuan penulis, penelitian tentang sintesis laktogenin sebagai senyawa analog asetogenin dalam suasana basa etilendiamin belum pernah dilakukan sebelumnya. Penelitian sejenis pernah dilakukan oleh Oasa et al. (2010)
dengan judul “Synthesis of Annonacin Isolated from Annona densicoma”.
3. Manfaat Penelitian
a) Manfaat teoritis
Untuk menambah faedah bagi perkembangan dunia farmasi terkait sintesis senyawa laktogenin dalam suasana basa etilendiamin.
b) Manfaat metodologis
Untuk memberikan pengetahuan tentang cara sintesis senyawa laktogenin dengan reaksi kondensasi aldol silang.
c) Manfaat praktis
Untuk memberikan informasi adanya senyawa yang berpotensi sebagai antikanker.
B. Tujuan Penelitian
5
BAB II
PENELAAHAN PUSTAKA
A. Kanker
Kanker merupakan kumpulan sel abnormal yang terbentuk oleh sel9sel yang tumbuh secara terus9menerus, tidak terbatas, tidak terkoordinasi dengan jaringan sekitarnya dan tidak berfungsi fisiologis. Kanker terjadi karena timbul dan berkembang biaknya jaringan sekitarnya (infiltratif) sambil merusaknya (destruktif), dapat menyebar kebagian lain tubuh, dan umumnya fatal jika dibiarkan (Dalimartha, 2004).
Pertumbuhan sel9sel kanker akan menyebabkan jaringan menjadi besar dan disebut sebagai tumor. Tumor merupakan istilah yang dipakai untuk semua bentuk pembengkakan atau benjolan dalam tubuh. Sel9sel kanker yang tumbuh cepat dan menyebar melalui pembuluh darah dan pembuluh getah bening. Penjalarannya ke jaringan lain disebut sebagai metastasis (Bustan, 1997).
B. Asetogenin
Annonaceous acetogenin (ACGs) merupakan senyawa alam yang berasal
dari tanaman golongan annoaceae dimana memiliki kekayaan fungsi biologis
seperti sitotoksik, antitumor, pestisida, anti9infeksi dan aktivitas antifedant. Dari hasil studi biokimia menunjukkan bahwa asetogenin merupakan inhibitor yang paling kuat terhadap enzim kompleks I (NADH9ubiquinone oksireduktase) pada
rantai respirasi sel mitokondria. Sampai saat ini lebih dari 430 komponen yang
PLAGIAT MERUPAKAN TINDAKAN TIDAK TERPUJI
termasuk dalam golongan annonaceae telah berhasil diisolasi, dan sebagian besar
memiliki sebuah cincin tetrahidropiran (THP) atau tetrahidrofuran (THF), gugus hidroksil, gugus keto dan gugus epoksi dua sampai tiga ikatan yang dihubungkan dengan α,β unsaturated γ lactone yang menyatu dalam rantai panjang C935 atau
C937 (Makabe, 2008; Li, 2008; McLaughlin, 2008).
Gambar 1. Struktur asetogenin secara umum (Anonim, 2010)
Gambar 2. Interaksi antara asetogenin dengan enzim kompleks I (NADH ) (Hongda, 2006)
7
Annonaceous acetogenin sebagai antikanker. Dalam penelitian pertama yang
dilakukan oleh Shimada (1998) tentang isolasi Annonaceous acetogenin alami,
tetrahidrofuran yang diapit oleh gugus hidroksil dipercaya berperan sebagai jangkar hidrofilik yang akan menempel pada permukaan membran sel, sedangkan γ9lakton akan berinteraksi langsung dengan sisi target enzim kompleks I dan menuju ke reseptor melalui difusi lateral. Oleh karena itu, diyakini bahwa struktur yang berbeda akan mempengaruhi lokasi, konformasi dan orientasi dari cincin lakton fungsional sehingga dapat mempengaruhi aktivitas biologis Annonaceous acetogenin (Hongda, 2006).
C. Sintesis Senyawa Laktogenin
Senyawa laktogenin (39(39(tetrahidrofuran939il)akriloil)dihidrofuran9 2(3H)9on) adalah salah satu senyawa analog asetogenin yang berpotensi sebagai inhibitor enzim kompleks I yang poten. Seperti yang dijelaskan oleh Mauro (1994), bahwa senyawa9senyawa lakton yang merupakan analog asetogenin berperan sebagai inhibitor NADH9ubiquinone oksidoreduktase pada rantai
respirasi sel (kompleks I mitokondria). Senyawa laktogenin diperkirakan memiliki aktifitas inhibitor enzim NADH9ubiquinone oksidoreduktase yang tingkat
kekuatannya tidak berbeda jauh dari asetogenin. Hal ini dikarenakan oleh adanya gugus lakton dan tetrahidrofuran pada senyawa laktogenin berarti memiliki dua sisi aktif yang dapat bekerja sebagai inhibitor enzim NADH9ubiquinone oksidoreduktase. Keunggulan lain yang diinginkan dari senyawa ini adalah rantai
alkil yang lebih pendek dari asetogenin pada umumnya, dengan upaya
PLAGIAT MERUPAKAN TINDAKAN TIDAK TERPUJI
memperpendek rantai alkil diharapkan dapat meningkatnya sifat hidrofilisitasnya. Sehingga diharapkan aktivitasnya sebagai antikanker akan meningkat melalui mekanisme penghambatan respirasi sel pada mitokondria yang akan menyebabkan penurunan produksi ATP, dan pada akhirnya sel9sel kanker akan mengalami apoptosis dan mati.
Senyawa laktogenin disintesis dari starting material 29asetil9γ9
butirolakton yang merupakan senyawa golongan keton dengan hidrogen alfa dan
tetrahidro939furankarboksaldehid yang merupakan senyawa golongan aldehida dengan etilendiamin sebagai penyedia suasana basa. Reaksi yang mendasari sintesis senyawa laktogenin adalah reaksi kondensasi aldol silang. Prinsip reaksi kondensasi aldol silang adalah suatu aldehid yang tidak memiliki hidrogen alfa
bila direaksikan dengan suatu aldehid atau keton yang memiliki hidrogen alfa,
maka akan terjadi dimerisasi (Fessenden dan Fessenden, 1994). Dalam suasana basa, hidrogen alfa pada 29asetil9γ9butirolakton akan terdeprotonasi membentuk
karbanion lalu beresonansi menjadi ion enolat yang berperan sebagai nukleofil. Pembentukan ion enolat akan meningkatkan nukleofilisitas dari C alfa 29asetil9γ9
butirolakton yang kemudian menyerang atom C karbonil dari tetrahidro939 furankarboksaldehid yang bersifat elektrofil. Dari reaksi tersebut akan terbentuk produk senyawa yang mudah terdehidrasi sehingga menghasilkan senyawa dengan struktur afa beta unsaturated yaitu laktogenin.
9
hidrogen alfa dapat berlangsung dalam suasana asam maupun basa. Dalam
suasana asam, suatu karbonil akan membentuk enol. Sedangkan dalam suasana basa akan terbentuk enolat yang memiliki reaktifitas yang lebih tinggi dibandingkan enol. Reaksi pembentukan laktogenin berjalan dalam suasana basa dengan adanya etilendiamin. Etilendiamin merupakan basa jenis amin primer, berfungsi untuk mengambil hidrogen alfa yang bersifat asam sehingga akan
terbentuk ion enolat. Amina adalah turunan organik dari ammonia dimana satu atau lebih atom hidrogen pada nitrogen telah tergantikan oleh gugus alkil atau aril. Karena itu amina memiliki sifat mirip dengan ammonia seperti alkohol dan eter terhadap air yang bersifat sebagai pendonor elektron. Adanya pasangan elektron bebas pada NH2 membuat etilendiamin mudah dalam mengambil hidrogen alfa
pada 29asetil9γ9butirolakton.
PLAGIAT MERUPAKAN TINDAKAN TIDAK TERPUJI
Berikut ini mekanisme analisis diskoneksi senyawa laktogenin :
11
D. Uji Pendahuluan
1. Pemeriksaan organoleptis
Uji organoleptis merupakan uji pendahuluan yang bertujuan untuk mengetahui sifat fisik dari senyawa hasil sintesis yang meliputi bentuk, warna dan bau. Uji ini merupakan uji yang sangat sederhana, bisa dilakukan tanpa bantuan alat, dan dilakukan dengan membandingkan antara senyawa hasil sintesis dengan
starting material yang digunakan (Dirjen POM RI, 1995).
2. Uji kemurnian menggunakan Kromatografi Lapis Tipis (KLT)
Kromatografi Lapis Tipis (KLT) digunakan untuk menguji kemurnian secara kualitatif dari campuran suatu senyawa untuk pembuktian ada tidaknya komponen yang dicari atau kemurnian komponen tersebut. Uji ini dilakukan dengan cara membandingkan senyawa hasil sintesis dengan senyawa standar. Senyawa yang murni akan memberikan bercak tunggal pada berbagai fase gerak dengan berbagai tingkat kepolaran (Gasparic dan Churacek, 1978).
Metode ini menggunakan dua fase, yaitu fase diam dan fase gerak yang memiliki kepolaran yang berbeda. Fase gerak akan bergerak naik melalui fase diam oleh karena gaya kapilaritas. Berdasarkan hal tersebut dapat dinyatakan jarak rambat senyawa pada fase diam (Rf) dapat digunakan sebagai cerminan
polaritas suatu senyawa (Bresnick, 2004).
Jika fase diam yang digunakan bersifat polar maka senyawa yang bersifat polar akan melekat lebih kuat pada lempeng daripada senyawa non9polar akibat interaksi tarik menarik dipo9dipol. Senyawa non9polar kurang melekat pada fase diam polar sehingga terelusi lebih cepat. Berdasarkan hal tersebut dapat
PLAGIAT MERUPAKAN TINDAKAN TIDAK TERPUJI
disimpulkan bahwa jarak rambat senyawa pada lempengan dapat digunakan sebagai cerminan polaritas suatu senyawa (Bresnick, 2004).
3. Spektrofotometri UV
Spektrofotometri UV adalah teknik analisis spektroskopik yang memakai sumber radiasi elektromagnetik UV dekat (1909380nm) dengan memakai instrumen spektrofotometer. Spektrofotometri UV melibatkan energi elektronik yang cukup besar pada molekul yang dianalisis, sehingga spektrofotometri UV lebih banyak dipakai untuk analisis kuantitatif dibandingkan kualitatif (Mulja dan Suharman, 1995).
13
4. Kromatografi Gas
Kromatografi gas merupakan teknik pemisahan dimana solut9solut yang mudah menguap (dan stabil terhadap panas) bermigrasi melalui kolom yang mengandung fase diam dengan suatu kecepatan yang tergantung pada rasio distribusinya. Pada umumnya solut akan terelusi berdasarkan pada peningkatan titik didihnya, kecuali jika ada interaksi khusus antara solut dengan fase diam. Pemisahan pada kromatografi gas didasarkan pada titik didih suatu senyawa dikurangi dengan semua interaksi yang mungkin terjadi antara solut dengan fase diam (Sudjadi, 2009).
Kromatografi gas merupakan instrumen analitis yang memberikan informasi baik kualitatif maupun kuantitatif mengenai komponen suatu sampel. Sampel akan mengalami proses pemisahan dalam kolom kemudian dideteksi dan direkam sebagi pita elusi (Day and Underwood, 1996).
Data kromatografi gas biasanya terdiri atas waktu retensi berbagai komponen campuran. Waktu retensi diukur mulai dari titik penyuntikan sampai titik maksimum puncak dan sangat khas untuk senyawa tertentu pada kondisi tertentu (kolom, suhu, gas pembawa, laju aliran) (Gritter, 1991).
E. Elusidasi Struktur
1. Spektrofotometri Inframerah
Semua ikatan kimia memiliki frekuensi khas yang dapat membuat ikatan mengulir (stretch) atau menekuk (blend). Apabila frekuensi energi
elektromagnetik inframerah yang dilewatkan pada suatu molekul sama dengan
PLAGIAT MERUPAKAN TINDAKAN TIDAK TERPUJI
frekuensi mengulur atau menekuknya ikatan, maka energi tersebut akan diserap. Serapan inilah yang dapat direkam oleh detektor pada spektrofotometri inframerah (Bresnick, 1996).
Penggunaan spektrofotometri inframerah pada bidang kimia organik hampir menggunakan daerah 65094000 cm91. Daerah dengan frekuensi lebih
rendah dari 650 cm91 disebut inframerah jauh dan daerah dengan frekuensi lebih
tinggi dari 4000 cm91 disebut inframerah dekat (Sastrohamidjojo, 2007).
Ahli kimia telah mempelajari banyak sekali senyawa organik dan telah dapat menghubungkan macamnya ikatan dengan panjang gelombang atau frekuensi dari absorbs sinar infra merahnya. Karena itu, untuk dapat menentukan apakan suatu senyawa mengandung suatu macam ikatan, misalnya O9H, perlu dilakukan pengukuran energi absorpsi dari senyawa tersebut pada panjang gelombang atau frekuensi yang sesuai untuk ikatan tersebut. Apabila senyawa yang diukur tersebut mengabsorpsi energi yang ditentukan, hal itu berarti ikatan O9H ada dalam struktur senyawa, akan tetapi jika energi tidak diabsorpsi maka ikatan O9H tidak ada dalam struktur senyawa (Fessenden dan Fessenden, 1994)
Absorpsi dalam daerah inframerah mengakibatkan eksitasi vibrasi dari ikatan9ikatan. Inti9inti atom yang terikat oleh ikatan kovalen dapat mengalami getaran (vibrasi) atau osilasi (oscillation). Beragam ikatan membutuhkan energi
15
C=O menunjukkan absorpsi yang kuat. Setiap jenis gugus fungsi dalam sebuah molekul mempunyai rentang daerah serapan yang berbeda9beda, sebagai contohnya adalah pada gugus OH (alkohol), absorpsi inframerahnya menunjukan pola yang jelas pada 320093500 cm91; gugus –O9CH3 (eter) menunjukkan peak
pada 283092815 dan 146091450 cm91 dengan intensitas lemah9sedang; senyawa
yang mengandung gugus C=O (karbonil) menunjukkan absorpsi yang kuat dan nyata pada frekuensi 165091800 cm91, dan masih banyak lagi (Fessenden dan Fessenden, 1994).
2. Spektrometri Massa
Spektrometri massa memberikan informasi tentang hasil fragmen9 fragmen yang dinyatakan sebagai perbandingan massa dengan muatan (m/z). Dalam spektrometri massa, molekul9molekul dari senyawa organik dalam bentuk gas akan diubah menjadi ion9ion yang bermuatan positif yang bertenaga tinggi. Ion molekul yang dihasilkan ini tidak stabil dan akan terpecah menjadi fragmen9 fragmen kecil, baik dalam bentuk radikal bebas maupun ion9ion lain. Fragmen yang bermuatan positif ini akan terdeteksi, sedangkan fragmen yang bersifat netral tidak dapat dideteksi dalam spektrometer massa (Sastrohamidjojo, 2001).
Suatu molekul atau ion pecah menjadi fragmen9fragmen bergantung pada kerangka karbon dan gugus fungsional yang ada. Oleh karena itu, struktur dan massa fragmen memberi petunjuk mengenai struktur molekul induknya dan seringkali digunakan untuk menentukan bobot molekul suatu senyawa (Fessenden dan Fessenden, 1994).
PLAGIAT MERUPAKAN TINDAKAN TIDAK TERPUJI
Dalam spektrum massa, setiap peak menyatakan suatu fragmen molekul
secara spesifik. Fragmen9fragmen tersebut disusun sedemikian rupa sehingga
peak peak tertata menurut kenaikan m/z dari kiri ke kanan dalam spektra.
Intensitas peak sebanding dengan kelimpahan relatif dari fragmen9fragmen, dan
tergantung pada stabilitas relatif fragmenya. Peak yang tertinggi pada spektra
disebut peak dasar (base peak) dan intensitasnya sebesar 100%. Peak dasar
dihasilkan dari ion molekul, akan tetapi lebih sering dihasilkan dari suatu fragmen yang lebih kecil (Silverstein, R.M., Bassler G.C, dan Morril T.C, 1991).
F. Landasan Teori
Reaksi kondensasi aldol silang adalah reaksi antara senyawa karbonil dengan sedikitnya satu hidrogen alfa dengan senyawa karbonil lain yang tidak
memiliki hidrogen alfa dalam suasana basa. Oleh karena itu dengan mereaksikan
29asetil9γ9butirolakton yang memiliki hidrogen alfa dengan tetrahidro939
furankarboksaldehid yang merupakan senyawa golongan keton, menggunakan suasana basa seperti etilendiamin akan menghasilkan senyawa laktogenin.
Gambar 4. Mekanisme reaksi sintesis senyawa laktogenin secara umum
Etilendiamin berfungsi untuk meningkatkan nukelofilisitas C alfa dari 29
17
amina (9NH2) akan mengambil hidrogen alfa yang bersifat asam sehingga akan
terbentuk ion enolat. Pembentukan ion enolat akan meningkatkan nukleofilisitas dari C alfa 29asetil9γ9butirolakton yang kemudian menyerang atom C karbonil
dari tetrahidro939furankarboksaldehid sehingga dihasilkan senyawa laktogenin.
G. Hipotesis
Senyawa laktogenin dapat disintesis dari tetrahidro939furankarboksaldehid dan 29asetil9γ9butirolakton dalam suasana basa etilendiamin.
PLAGIAT MERUPAKAN TINDAKAN TIDAK TERPUJI
18
BAB III
METODE PENELITIAN
A. Jenis dan Rancangan Penelitian
Penelitian ini termasuk dalam penelitian non9eksperimental deskriptif non9 analitik. Pada penelitian ini tidak ada perlakuan pada subjek uji dan hanya dipaparkan fenomena yang terjadi yang tidak terdapat hubungan sebab akibat.
B. Variabel dan Definisi Operasional
1. Variabel
a) Variabel bebas dalam penelitian ini adalah perbandingan mol pada starting material yang digunakan.
b) Variabel tergantung dalam penelitian ini adalah jumlah rendemen senyawa laktogenin karena merupakan obyek yang kehadirannya akibat reaksi antara 29asetil9γ9butirolakton dan tetrahidro939furankarboksaldehid.
c) Variabel pengganggu terkendali pada penelitian ini adalah suhu pencampuran dan kondisi peralatan.
2. Definisi Operasional
a) Starting material adalah senyawa awal yang digunakan dalam proses
sintesis dengan tujuan untuk mendapatkan senyawa hasil sintesis. Starting material yang digunakan dalam penelitian ini adalah 29asetil9γ9
19
b) Senyawa target adalah senyawa yang diharapkan terbentuk dari reaksi. Senyawa target yang diharapkan terbentuk adalah senyawa laktogenin.
C. Bahan Penelitian
29asetil9γ9butirolakton (for synthesis, Merck), tetrahidro939
furankarboksaldehid (for synthesis, Sigma9aldrich), etilendiamin (p.a., Merck),
metanol (p.a., Merck), aquadest, silika gel GF254.
D. Alat Penelitian
Pengaduk magnetik, pemanas listrik (Herdolph MR 2002), pengering (Memmert Oven Model 400), neraca analitik (Mextler PM 100), seperangkat alat gelas, klem, statif, termometer, corong Buchner, kromatografi gas9spektrometer massa (Shimadzu QP 2010 SE), spektrometer IR (IR Shimadzu Prestige 21),
lampu UV254 nm, mikropipet, baskom, kertas saring.
E. Tata Cara Penelitian
1. Pengenceran etilendiamin
Etilendiamin sebanyak 0,370 mL dimasukkan ke dalam labu takar 10 mL lalu ditambah aquadest hingga tanda.
2. Sintesis senyawa laktogenin
29asetil9γ9butirolakton 5,53 mmol (0,5943 mL) dimasukkan ke dalam labu erlenmeyer. Etilendiamin sebanyak 10 mL (5,53 mmol) ditambahkan dalam
PLAGIAT MERUPAKAN TINDAKAN TIDAK TERPUJI
larutan tersebut. Tetrahidro939furankarboksaldehid 5,53 mmol (1 mL) ditambahkan ke dalam campuran tetes demi tetes. Campuran diaduk dengan pengaduk magnetik pada kecepatan 750 putaran per menit pada suhu kamar selama 180 menit.
3. Uji Pendahuluan a. Organoleptis
Senyawa hasil sintesis diamati sifat9sifat fisiknya, meliputi bentuk, warna, dan bau. Kemudian hasil pengamatan dibandingkan dengan reaktan yang digunakan dalam penelitian yaitu 29asetil9γ9butirolakton dan tetrahidro939 furankarboksaldehid.
b. Uji kemurnian menggunakan Kromatografi Lapis Tipis (KLT)
Senyawa hasil sintesis dan starting material masing9masing ditotolkan
sebanyak 2 RL menggunakan mikropipet pada lempeng silika gel GF254 yang
sudah diaktifkan pada suhu 100oC selama 30 menit. Pengembangan dilakukan
dengan jarak rambat 15 cm dengan fase gerak yang digunakan yaitu toluen : metanol (1:3).
c. Uji penentuan panjang gelombang maksimum
Sebanyak 1 mL 0,001% (v/v) senyawa hasil sintesis dan 1 mL 0,001% (v/v) starting material masing9masing dilarutkan dalam metanol lalu di masukkan
ke dalam kuvet. Larutan tersebut di scan pada rentang panjang gelombang 1909
380nm. Ditentukan panjang gelombang maksimumnya pada area peak dengan
21
senyawa hasil sintesis dan starting material dibandingkan dan dilihat
perbedaannya dari profil spektra dan panjang gelombang maksimum yang dihasilkan.
d. Kromatografi Gas dan Spektrometri Massa (GC9MS)
Pemeriksaan kemurnian senyawa hasil sintesis dilakukan dengan kromatografi gas dengan kondisi alat: suhu injektor 310°C, jenis kolom Rastek Rxi95MS, panjang kolom 30 meter, suhu kolom diprogram 80°C, gas pembawa helium, tekanan 16,5 kPa, kecepatan alir fase gerak 0,5 ml/menit, dan detektor ionisasi nyala. Cuplikan senyawa hasil sintesis dilarutkan dalam kloroform, kemudian diinjeksikan ke dalam injektor pada alat kromatografi gas. Aliran gas dari gas pengangkut helium akan membawa cuplikan yang sudah diuapkan masuk kedalam kolom RXi95MS yang dilapisi fase cair dimetilpolisiloksan. Selanjutnya cuplikan diukur oleh detektor hingga diperoleh suatu kromatogram.
4. Elusidasi struktur senyawa hasil sintesis a. Spektrofotometri inframerah
Senyawa yang berwujud cairan ditempatkan dalam film tipis di antara dua lapis NaCl yang transparan terhadap inframerah. Cahaya inframerah dari sumber dilewatkan melalui cuplikan, kemudian dipecah menjadi frekuensi9 frekuensi individunya dalam monokromator dan intensitas relatif dari frekuensi individu diukur oleh detektor hingga didapat spektra inframerah dari senyawa yang bersangkutan. Bilangan gelombang yang digunakan 40094000 nm.
PLAGIAT MERUPAKAN TINDAKAN TIDAK TERPUJI
b. Spektrometri massa
Uap cuplikan senyawa hasil sintesis yang keluar dari kolom kromatografi gas dialirkan ke dalam kamar pengion pada spektrometer massa untuk ditembak dengan seberkas elektron hingga terfragmentasi. Jenis pengionan yang digunakan adalah EI (Electron Impact) 70 eV. Fragmen9fragmen akan melewati lempeng
mempercepat ion dan didorong menuju tabung analisator, dimana partikel9partikel akan dibelokkan dalam medan magnet dan menimbulkan arus pada kolektor yang sebanding dengan kelimpahan relatif setiap fragmennya. Kelimpahan relatif setiap fragmen akan dicatat dan menghasilkan data spektra massa.
F. Analisis Hasil
1. Analisis Pendahuluan
Analisis pendahuluan senyawa hasil sintesis berdasarkan data organoleptis dan spektra UV.
2. Pemeriksaan Kemurnian Senyawa Hasil Sintesis
Pemeriksaan kemurnian senyawa hasil sintesis berdasarkan data kromatografi lapis tipis (KLT) dan kromatografi gas.
3. Elusidasi Struktur
23
BAB IV
HASIL DAN PEMBAHASAN
A. Sintesis senyawa laktogenin
Sintesis senyawa laktogenin (39(39(tetrahidrofuran939 il)akriloil)dihidrofuran92(3H)9on) dilakukan dengan cara mereaksikan kedua
starting material yaitu tetrahidro939furankarboksaldehid dan 29asetil9γ9
butirolakton melalui reaksi kondensasi aldol silang. Tetrahidro939 furankarboksaldehid merupakan senyawa golongan aldehid yang berperan sebagai elektrofil, sedangkan 29asetil9γ9butirolakton merupakan senyawa golongan keton dengan hidrogen alfa yang bersifat asam dan berperan sebagai nukleofil.
Gambar 5. Posisi hidrogen pada 2 asetil γ butirolakton
Terdapat dua buah posisi hidrogen alfa pada 29asetil9γ9butirolakton,
dimana hidrogen alfa pada posisi 1 bersifat lebih asam daripada hidrogen alfa
pada posisi 2. Hidrogen alfa pada posisi 1 memiliki halangan stearik yang lebih
besar jika dibandingkan dengan hidrogen alfa pada posisi 2 sehingga hidrogen alfa pada posisi 2 inilah yang lebih memungkinkan untuk bereaksi dengan katalis
basa. Berdasarkan analisis komputasi menggunakan program marvin sketch,
PLAGIAT MERUPAKAN TINDAKAN TIDAK TERPUJI
diperoleh nilai muatan atom C alfa posisi 1 sebesar 0,09 sedangkan pada atom C alfa posisi 2 sebesar 90,01. Dari analisa tersebut, hidrogen alfa pada posisi 2
bersifat lebih asam sehingga akan lebih mudah dilepaskan dan terbentuk suatu atom karbon alfa yang bermuatan negatif yang disebut dengan ion enolat. Dengan
terbentuknya ion enolat, maka 29asetil9γ9butirolakton bersifat sebagai nukleofil yang akan menyerang atom karbon karbonil pada tetrahidro939 furankarboksaldehid. Atom karbon karbonil ini bermuatan parsial positif karena adanya resonansi dan induksi elektron oleh oksigen.
Pada tahap pembentukan ion enolat dibutuhkan suatu kondisi basa. Etilendiamin digunakan untuk menyediakan suasana basa sekaligus sebagai katalis. Pada reaksi ini, etilendiamin berfungsi untuk mendeprotonasi 29asetil9γ9 butirolakton sehingga terbentuk ion enolat yang akan menyerang gugus karbonil pada tetrahidro939furankarboksaldehid.
Penyerangan gugus karbonil oleh ion enolat ini akan menghasilkan suatu senyawa β9OH9karbonil yang merupakan senyawa antara dan kemudian
25
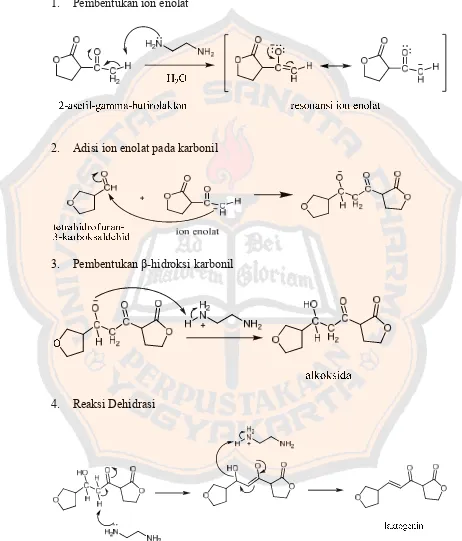
Sintesis senyawa laktogenin terjadi dengan beberapa tahap sebagai berikut :
1. Pembentukan ion enolat
2. Adisi ion enolat pada karbonil
3. Pembentukan β9hidroksi karbonil
4. Reaksi Dehidrasi
Gambar 6. Mekanisme reaksi sintesis senyawa laktogenin
PLAGIAT MERUPAKAN TINDAKAN TIDAK TERPUJI
Pada proses sintesis dilakukan pencampuran kedua macam starting material dan etilendiamin dengan cara mencampurkan 29asetil9γ9butirolakton
dengan etilendiamin terlebih dahulu, hal ini bertujuan untuk mengoptimalkan pembentukan ion enolat. Setelah itu baru tetrahidro939furankarboksaldehid ditambahkan kemudian tetes demi tetes, hal ini karena pada tetrahidro939 furankarboksaldehid juga terdapat atom H pada posisi alfa yang bersifat asam
sehingga dengan penambahan pada saat akhir diharapkan hidrogen alfa dari
tetrahidro939furankarboksaldehid tidak turut bereaksi dengan katalis etilendiamin. Pencampuran dilakukan pada suhu kamar untuk menghindari peristiwa hidrolisis gugus ester pada 29asetil9γ9butirolakton yang menurut Jose´ A et all (2005)
peristiwa hidrolisis lakton dapat dihindari dengan melakukan pencampuran pada pH netral dan suhu kamar. Setelah proses sintesis selesai kemudian dilakukan pengecekan pH campuran larutan, dan diperoleh pH larutan sebesar 8.
Gambar 7. Posisi hidrogen pada tetrahidro 3 furankarboksaldehid
B. Analisis Pendahuluan
1. Uji Oganoleptis
27
material yang digunakan, yaitu 29asetil9γ9butirolakton dan tetrahidro939
furankarboksaldehid.
Tabel 1. Tabel perbandingan data organoleptis
dengan senyawa hasil sintesis
Warna Kuning pekat Kuning muda Putih
Bau Menyengat Tidak berbau Menyengat
Dari hasil pemeriksaan organoleptis yang meliputi bentuk, warna, dan bau di atas, maka dapat disimpulkan bahwa senyawa hasil sintesis memiliki profil organoleptis yang berbeda dengan starting material nya. Maka diperkirakan telah
terbentuk senyawa baru yang merupakan hasil reaksi antara kedua starting material. Untuk mempertegas senyawa hasil sintesis maka dilakukan serangkaian
uji lebih lanjut.
2. Uji Kromatografi Lapis Tipis (KLT)
Kromatografi lapis tipis (KLT) merupakan uji yang dapat digunakan untuk mengetahui kemurnian dari senyawa hasil sintesis. Parameter yang digunakan dalam pengujian menggunakan KLT adalah nilai Rf untuk masing9masing
senyawa pada pelarut yang sama dan banyaknya bercak yang dihasilkan dari proses elusi. Uji KLT pada penelitian ini dilakukan dengan menggunakan fase gerak toluen : metanol (1 : 3), fase diam silika gel GF254 dan jarak pengelusian 15
cm. Pembanding yang digunakan adalah 29asetil9γ9butirolakton yang merupakan
PLAGIAT MERUPAKAN TINDAKAN TIDAK TERPUJI
starting material, hal ini karena laktogenin merupakan senyawa baru sehingga
belum ada baku pembandingnya. Starting material yang digunakan sebagai
pembanding hanya 29asetil9γ9butirolakton karena pada saat orientasi, bercak tetrahidro939furankarboksaldehid tidak dapat terlihat saat dideteksi dengan sinar UV 254 nm. Setelah diperoleh profil KLT, apabila terdapat bercak baru yang berbeda dari starting material maka bercak tersebut dianggap sebagai senyawa
baru sehingga dapat dilakukan pengujian lebih lanjut melalui kromatografi gas9 spektrometri massa (MS) dan spektrofotometri inframerah (IR).
Silika Gel GF254 sebagai fase diam, mengandung Gips (CaSO4) yang
berfungsi untuk melekatkan silika gel pada lempeng KLT. Pada fase diam ini juga terkandung indikator yang dapat berfluoresensi pada panjang gelombang 254nm, adanya indikator ini akan menyebabkan peredaman pada bercak dengan latar belakangnya berfluoresensi warna hijau, sehingga membuat bercak senyawa mudah terdeteksi. Pada saat dilakukan deteksi bercak, sinar UV akan diabsorbsi oleh senyawa tersebut sehingga tidak ada cahaya yang dipancarkan oleh bercak tersebut. Untuk fase gerak yang digunakan adalah toluen : metanol (1 : 3), pemilihan fase gerak ini merupakan hasil orientasi dimana pada komposisi fase gerak inilah dihasilkan pemisahan bercak yang optimal. Nilai indeks polaritas campuran fase gerak ini adalah 4,43.
Hasil Rf yang diperoleh pada senyawa sintesis adalah sebesar 0,71 untuk
replikasi 1 dan 0,70 untuk replikasi 2, sedangkan pada 29asetil9γ9butirolakton sebesar 0,78. Berdasarkan perbedaan nilai Rf pada kedua bercak tersebut maka
29
materialnya dan kemungkinan telah terbentuk senyawa baru. Bercak yang
dihasilkan setelah elusi merupakan bercak tunggal namun belum dapat dipastikan sepenuhnya apakah senyawa ini sudah murni atau belum, maka perlu dilakukan uji selanjutnya.
A = 29asetil9γ9butirolakton
B = senyawa hasil sintesis replikasi 1 C = senyawa hasil sintesis replikasi 2
Gambar 8. Kromatogram KLT senyawa hasil sintesis
Tabel 2. Perbandingan nilai 2 asetil γ butirolakton dan senyawa hasil sintesis
Bercak Senyawa Rf
A 29asetil9γ9butirolakton 0,78
B senyawa hasil sintesis replikasi 1 0,71 C senyawa hasil sintesis replikasi 2 0,70
Dari hasil nilai Rf antara senyawa hasil sintesis dengan 29asetil9γ9
butirolakton tidak terlihat perbedaan yang signifikan, hal ini dikarenakan adanya kemungkinan interaksi antara kedua senyawa tersebut dengan fase diam. Interaksi
PLAGIAT MERUPAKAN TINDAKAN TIDAK TERPUJI
antara senyawa hasil sintesis dengan fase diam dan 29asetil9γ9butirolakton dengan fase diam memiliki profil interaksi yang sama sehingga diperlukan uji lebih lanjut apakah senyawa hasil sintesis merupakan senyawa baru atau bukan.
Gambar 9. Interaksi hidrogen antara fase diam dengan 2 asetil γ butirolakton
Gambar 10. Interaksi hidrogen antara fase diam dengan senyawa sintesis
3. Uji Penentuan Panjang Gelombang Maksimum
dilakukan di daerah pa pengujian ini hanya be yang dihasilkan, mak
starting material denga
Ga
Gambar
panjang gelombang daerah UV (190 – 380 n nya bersifat kualitiatif dari profil spektra dan panja , maka dapat dibandingkan apakah terdapat per
dengan senyawa hasil sintesis.
Gambar 11. Spektra UV 2 asetil γ butirolakton
mbar 12. Spektra UV tetrahidro 3 furankarboksaldehid
31
80 nm). Oleh karena panjang gelombang at perbedaan antara
ldehid
PLAGIAT MERUPAKAN TINDAKAN TIDAK TERPUJI
Gambar 13. Spektra UV senyawa hasil sintesis
Tabel 3. Perbandingan panjang gelombang maksimum
dan senyawa hasil sintesis
Senyawa λ maks Abs
29asetil9γ9butirolakton 254 0,538
Tetrahidro939furankarboksaldehid 207 0,404
Senyawa hasil sintesis 9 206
9 297
0,669 0,228
33
hasil sintesis ini menunjukkan kemungkinan telah terbentuk senyawa baru. Terbentuknya senyawa baru ini ditandai dengan munculnya spektra pada panjang gelombang 297 nm yang bukan merupakan spektra dari kedua macam starting material (29asetil9γ9butirolakton dan tetrahidro939furankarboksaldehid),
diperkirakan terbentuk senyawa baru yang memiliki gugus kromofor lebih panjang daripada kedua starting material sehingga panjang gelombang
maksimumnya lebih panjang. Namun hal ini masih harus dibuktikan dengan pengujian lebih lanjut karena pengecekan spektra panjang gelombang maksimum disini hanya bersifat kualitatif. Berikut ini gambar gugus kromofor pada senyawa hasil sintesis:
Gambar 14. Gugus kromofor pada laktogenin
C. Elusidasi Struktur Senyawa Hasil Sintesis
1. Spektrofotometri inframerah
Spektrofotometri inframerah (IR) digunakan untuk mengetahui gugus9 gugus fungsional yang terdapat dalam suatu senyawa.
Gugus kromofor
PLAGIAT MERUPAKAN TINDAKAN TIDAK TERPUJI
Spektra IR seny cm91 dengan intensitas yang terkonjugasi deng
R senyawa hasil sintesis ditujukkan pada gambar be
Gambar 15. Spektra inframerah senyawa hasil sintesis
il spektra IR yang diperoleh tersebut terdapat em g menunjukkan adanya gugus9gugus fungsional sintesis. Pita A pada bilangan gelombang anya vibrasi ulur C=C tak jenuh dengan intensit apan ini diperkuat dengan adanya pita D intensitas ang 1010,7 cm91. Pita D ini merupakan pita overto
an adanya gugus C=C. Gugus karbonil juga yang ntesis ditunjukkan pada pita B pada bilangan gelom nsitas kuat. Pada pita ini terlihat adanya serapan d si dengan suatu alkena. Sedangkan pita C merupak
bar berikut ini:
pat empat buah pita sional pada struktur bang 3140,11 cm91 ntensitas sedang dan
35
yang menunjukkan adanya gugus C9O ester yang khas dengan intensitas sedang pada bilangan gelombang 1242,16 cm91.
Tabel 4. Interpretasi spektra inframerah senyawa hasil sintesis
Bilangan gelombang (cm91) Intensitas Gugus fungsi 9 3140,11
9 1010,7 (overtone)
Sedang dan melebar
Sedang Ikatan C=C
9 1643,35 Kuat Ikata C=O terkonjugasi
suatu alkena
9 1242,16 Lemah Ikatan C9O ester
(Sastrohamidjojo, 2007)
Dari hasil elusidasi struktur inframerah (IR) menunjukkan adanya beberapa gugus fungsional yang penting pada struktur senyawa hasil sintesis yakni gugus C=O yang terkonjugasi pada gugus alkena serta adanya gugus C9O ester. Spektra senyawa hasil sintesis kemudian dibandigkan dengan spektra inframerah (IR) pada kedua macam starting material untuk mengetahui perbedaan
profil antara senyawa hasil sintesis.
PLAGIAT MERUPAKAN TINDAKAN TIDAK TERPUJI
Berikut ini gam
Gamba
Pada spektra merepresentasikan gug B menginterpretasikan lakton pada bilangan terlihat pada pita D da cm91. Sedangkan adan dimana pada bilangan g
i gambar spektra inframerah (IR) 29asetil9γ9butirol
mbar 16. Spektra inframerah 2 asetil γ butirolakton
ektra inframerah diatas, terdapat 5 buah an gugus fungsi yang terdapat 29asetil9γ9butirolakt
asikan adanya ikatan C=O yang spesifik pada gu ngan gelombang 1776 dan 1712 cm91. Ikatan C
a D dan E yaitu pada bilangan gelombang 2993,5 adanya gugus C9O ester juga ditandai dengan ngan gelombang 1026,13 cm91 dengan intensitas ku
37
Gambar 17. Spektra inframerah senyawa tetrahidro 3 furankarboksaldehid
Pada gambar 17, terdapat 4 buah spektra yang menginterpretasikan adanya gugus fungsional seperti yang terdapat pada tetrahidro939furankarboksaldehid. Pita A menunjukkan adanya gugus C=O aldehid pada bilangan gelombang 1712,19 cm91 dengan intensitas kuat. Gugus C9H alkana alifatik juga ditunjukkan oleh pita B dan C pada bilangan gelombang 2978,09 dan 2885,51 cm91 dengan intensitas sedang. Sedangkan pita D pada bilangan gelombang 1056,99 cm91 dengan intensitas kuat menunjukkan adanya gugus C9O.
PLAGIAT MERUPAKAN TINDAKAN TIDAK TERPUJI
Tabel 5. Perbandingan interpretasi spektra inframerah senyawa hasil sintesis
dan
Gugus fungsi Senyawa hasil sintesis
Berdasarkan tabel 5 mengenai perbandingan interpretasi spektra senyawa hasil sintesis dan starting material terlihat adanya perbedaan gugus fungsi pada
masing9masing senyawa. Pada senyawa hasil sintesis terdapat ikatan C=C yang tidak dimiliki oleh kedua starting material ini begitu juga dengan adanya gugus
2. Spektrometri ma
struktur senyawa hasil sintesis dilakukan deng rafi gas (GC) – spektrometri massa (MS). Kromato
mengetahui kemurnian dari senyawa hasil sinte amaan dengan spektrometri massa. Hasil peng data, yaitu kromatogram GC dan spektra MS
romatogram GC senyawa hasil sintesis dan
ektra MS senyawa hasil sintesis.
ar 18. Kromatogram kromatografi gas senyawa hasil sin
yang dihasilkan, Area Under Curve (AUC) terbesar ada pada waktu retensi
18,491 menit. Munculnya tujuh buah peak pada kromatogram GC menunjukkan
bahwa senyawa hasil sintesis belum murni dan masih terdapat banyak campuran senyawa.
Kemurnian peak yang menunjukkan senyawa laktogenin adalah sebesar
1,72%. Nilai kemurnian yang diperoleh berdasarkan data GC ini tergolong rendah, hal ini karena banyak faktor yang sangat mempengaruhi berjalannya reaksi. Prinsip reaksi sintesis senyawa laktogenin ini adalah kondensasi aldol dengan menggunakan katalis basa. Salah satu faktor yang sangat penting pada kondensasi aldol adalah pembentukan ion enolat oleh katalis basa, ion enolat ini berperan sebagai nukleofil. Kemampuan pembentukan ion enolat sangat dipengaruhi oleh kekuatan basa yang dimiliki oleh katalis. Jika suatu katalis memiliki kemampuan yang cukup untuk mengambil H alfa pada 29asetil9γ9
butirolakton maka langkah reaksi selanjutnya juga akan berjalan sehingga senyawa target mudah terbentuk dan dihasilkan rendemen yang sesuai dengan teoritis.
Seperti yang dijelaskan oleh Jose´ A et al. (2005) γ9lakton merupakan
dengan pKb 4,02, tinggi sehingga salah elektron berenergi tin disebut sebagi ion radi hasil sintesis pada wak
, sehingga kemampuan terbentuknya nukl kurangnya jumlah nukleofil yang terbentuk, ula jumlah nukelofil yang menyerang atom C nkarboksaldehid yang bersifat elektrofil sehin
anyak dihasilkan. Etilendiamin yang berperan seb aligus sebagai katalis juga tidak dapat terdeteksi ofotometri inframerah dan spektrometri ma tilendiamin turut bereaksi dengan 2 starting materi
emilihan katalis yang sesuai.
l spektra massa senyawa hasil sintesis pada waktu retens
mbar 19 menunjukkan spektra MS senyawa hasi ,725 menit. Prinsip elusidasi struktur dengan spek kan molekul senyawa hasil sintesis dengan elek salah satu elektron valensinya lepas. Hasil penem
gi tinggi adalah suatu ion molekuler dengan mu n radikal positif. Dari hasil spektra massa terlihat b
a waktu retensi 24,725 menit memiliki ion moleku
211, dimana m/z tersebut sesuai dengan bobot molekul senyawa laktogenin sebesar 211g/mol.
Mekanisme fragmentasi dari senyawa hasil sintesis adalah sebagai berikut :
43
Senyawa hasil sintesis ditembak dengan elektron berenergi tinggi yang menghasilkan peak A dengan nilai m/z = 211. Peak ion molekuler ini merupakan peak yang tidak stabil oleh karena itu dapat pecah menjadi fragmen9fragmen yang
lebih kecil. Ion molekuler ini kemudian akan terpecah menjadi fragmen9fragmen yang lebih kecil baik dalam bentuk radikal bebas maupun dalam bentuk ion (+) /ion (9). Namun hanya fragmen yang bermuatan radikal positif dan positif saja yang akan terdeteksi oleh spektrometer massa.
Senyawa laktogenin mengalami fragmentasi oleh elektron berenergi tinggi dan terbentuk beberapa potongan fragmen. Senyawa hasil sintesis ini memiliki dua buah kemungkinan jalur fragmentasi. Pada jalur yang pertama, terbentuk 2 fragmen yang sesuai dengan hasil pada spektra massa. Peak D dengan
nilai m/z = 113 merupakan fragmen C5H5O3+. Peak D kemudian mengalami
fragmentasi lebih lanjut menghasilkan kation C4H5O2+, peak kation ini
menunjukkan nilai m/z = 86 sesuai dengan peak F.
Pada jalur yang kedua, dihasilkan 4 buah fragmen yang sesuai dengan spektra massa yang dihasilkan. Peak B dengan nilai m/z = 168 yang merupakan fragmen C11H14O4+. Peak B ini kemudian mengalami fragmentasi lebih lanjut
menghasilkan kation C7H11O2+ dengan nilai m/z = 128 seperti yang ditunjukkan
pada peak C. Peak C ini mempunyai intensitas 100% jika dibandingkan dengan peak peak yang lain sehingga disebut sebagai base peak (peak dasar). Peak C
kemudian akan mengalami fragmentasi lebih lanjut menghasilkan kation C6H9O+. Peak ini menunjukkan nilai m/z = 98 sesuai dengan peak E. Fragmentasi lebih
PLAGIAT MERUPAKAN TINDAKAN TIDAK TERPUJI
lanjut yang dihasilkan dari kation peak E adalah kation C2H3O+ dengan nilai m/z =
44 seperti yang terlihat pada peak G.
D. Pembentukan Produk Reaksi Samping
Dari hasil uji kromatografi gas9spektrometri massa, diperoleh juga spektra yang menunjukkan adanya hasil reaksi samping dari proses sintesis. Hasil reaksi samping yang terbesar tampak pada peak kelima, pada waktu retensi
18,491 menit (dilihat dari besar AUC pada kromatogram GC, peak kelima ini
memiliki AUC paling besar yaitu 70,54%). Berdasarkan hasil spektrometri
massanya, pada peak ketiga ini memiliki ion molekul dengan m/z = 223, oleh
karena itu, senyawa ini memiliki bobot molekul sebesar 223 g/mol.
Gambar 21. Hasil spektra massa produk samping pada waktu retensi 18,492 menit
45
Berikut ini merupakan gambar usulan mekanisme fragmentasi senyawa produk reaksi samping :
m/z: 223
m/z: 112
m/z: 42 EI
70 ev
m/z : 181
C10H11O3+ C6H7O2+
C3H5+
C11H12O5•+
Gambar 22. Usulan mekanisme fragmentasi dari produk reaksi samping
Pada mekanisme fragmentasi di atas dihasilkan 4 buah fragmen yang sesuai dengan spektra massa yang dihasilkan. Peak B dengan nilai m/z = 181 merupakan fragmen C10H11O3+. Peak B ini kemudian mengalami fragmentasi
lebih lanjut menghasilkan kation C6H7O2+ dengan nilai m/z = 112 seperti yang
PLAGIAT MERUPAKAN TINDAKAN TIDAK TERPUJI
ditunjukkan pada peak C. Peak C kemudian akan mengalami fragmentasi lebih
lanjut menghasilkan kation C3H5+. Peak ini menunjukkan nilai m/z = 42 sesuai
dengan peak D.
Produk reaksi samping ini merupakan senyawa yang terbentuk dari reaksi
self kondensasi 29asetil9γ9butirolakton. Gambar di bawah ini merupakan perkiraan
struktur senyawa yang merupakan hasil reaksi samping dari proses sintesis:
Gambar 23. Perkiraan struktur senyawa produk samping
Reaksi self kondensasi ini terjadi karena pada senyawa 29asetil9γ9
butirolakton memiliki atom C pada posisi alfa yang bermuatan negatif dan atom C
karbonil yang bermuatan parsial positif sehingga memungkinkan terbentuknya suatu elektrofil dan nukleofil pada 29asetil9γ9butirolakton. Nukleofil terbentuk karena adanya ion enolat, dimana atom C pada posisi alfa bermuatan negatif
47
Mekanisme reaksi pembentukan senyawa produk samping adalah sebagai berikut :
Gambar 24. Mekanisme reaksi pembentukan senyawa produk samping
PLAGIAT MERUPAKAN TINDAKAN TIDAK TERPUJI
48
BAB V
KESIMPULAN DAN SARAN
Kesimpulan
Berdasarkan hasil penelitian, dapat diambil kesimpulan bahwa laktogenin dapat disintesis dari tetrahidro939furankarboksaldehid dan 29asetil9γ9butirolakton dalam suasana basa etilendiamin. Dengan metode kromatografi9gas (GC), senyawa hasil sintesis memiliki kermurnian sebesar 1,72%.
Saran
49
DAFTAR PUSTAKA
Anonim, 2010, Acetogenin, http://www.biofunc9chem.kais.kyoto9
u.ac.jp/projects/compound/compound.html diakses pada tanggal 22 Februari 2011.
Balmain, A., Gray, J. and Ponder, B., 2003, The genetics and genomics of cancer, Journal of Natural Genetic, 33 Suppl: 238−44.
Bermejo, A., Figadere, B., Zafra9Polo, M.C., Barrachina, I., Estornell, E., Cortes D., 2005, Acetogenins from annonaceous: recent progress in isolation, synthesis and mechanisms of action, Journal of Natural Product, Rep 22:
2699303.
Bresnick, M.D., 2004, Intisari Kimia Organik, 96997, 1019107, Hipokrates
Jakarta.
Bustan, M.N., 1997, Epidemologi Penyakit Tidak Menular, 24927, Rineka Cipta,
Jakarta.
Corner, J., 2001, What is cancer? In: Cancer Nursing Care in Context (eds J.
Corner and C. Bailey), Blackwell Publishing, Oxford.
Dalimartha, S., 2004, Deteksi Dini Kanker dan Simplisia Anti Kanker, Penerbit
Swadaya, Jakarta.
Day, Jr., R. A., and Underwood, A. L., 1996, Analisis Kimia Kuantitatif,
diterjemahkan oleh Pudjaatmaka, A. H., Edisi IV, 519, Penerbit Erlangga, Jakarta.
Direktorat Jenderal Pengawasan Obat dan Makanan RI, 1995, Farmakope Indonesia, jilid IV, Departemen Kesehatan Republik Indonesia, Jakarta,
1125.
Fessenden, R.J. and Fessenden, J.S., 1994, Organic Chemistry, Fifth Edition, 209
42, 6959697, Wadsworth, Inc., Belmont, USA.
Gabriel, J., 2007, The Biology of Cancer 2nd edition, 63, John Wiley and Sons
Ltd, Inggris.
Gasparic, J., and Churacek J., 1978, Laboratory Handbook of Paper and Thin Layer Chromatography, 63, Ellis Horwood Limited, England.
PLAGIAT MERUPAKAN TINDAKAN TIDAK TERPUJI
Gonzalez, A., Cavé, A., Granell, S., Cortes, D., Zafra9Polo, Tormo, J., Estornell, E., Gallardo, T., 2002, Selective action of acetogenin mitochondrial complex I inhibitors, Journal Z. Naturforsch, 57(11912): 1028934.
Gritter, R.J., Bobit, J.M., dan Schwarting, A.E., 1991, Pengantar Kromatografi,
diterjemahkan oleh Kosasih Padmawinata, edisi 2, 1099112, ITB.
Hongda, Z., 2006, Stereospecific Alkynylation at the More Hindered Carbon of Trisubstituted Epoxides and Concise Syntheses of Bis9THF Acetogenins and Analogues, Desertation, 63, Faculty of the Graduate School of The
University of Texas at Austin.
Jose´, A., Manso, M., Teresa, Pe´rez9Prior, M., del Pilar Garcı´a9Santos, Emilio, C., and Julio, C., 2005, A Kinetic Approach to the Alkylating Potential of Carcinogenic Lactones, Universidad de Salamanca, Spanyol.
Li, N., Shi, Z., Tang, Y., Chen, J., dan Li, X., 2008, Beilstein Jurnal Organic Chemistry, 4.
Makabe H., Konno H., and Miyoshi H., 2008, Journal Drug Discovey Technology, 5, 2139229.
Mauro, 1994, Natural substances (acetogenins) from the family Annonaceae are powerful inhibitors of mitochondrial NADH dehidrogenase (Complex I),
Biochemistry Journal, 301, 1619167.
McLaughlin, J.L., 2008, Journal of Natural Product, 71, 131191321.
Morré, D.J, Cabo, R., Farley, C., Oberlies, N.H., McLaughlin, J.L., Yenkin, 1995, Mode action of bullatacin, a potent antitumor acetogenin: inhibition of NADH oxidase activity of HeLa and HL960; but not liver; plasma membranes, Journal of Natural Product, 56: 3439348.
Mulja, H.M, dan Suharman, 1995, Analisis Instrumental, hal 28, Airlangga
University Press, Surabaya.
Oasa, M., Yasunao, H., Hiroyuki, K., and Hidefumi, M.M, 2010, Synthesis of Annonacin Isolated from Annona densicoma, Biosci. Biotechnol.Biochem.,
74 (6), 127491275.
Ohnishi, T., 1993, Biomembran, Journal of Bioenergetic edisi 25, 3259329.
Piret, V., 2008, Synthesis of Acetogenin Analogue, Thesis, 10912, University of
Tartu Faculty of Science and Technology Institute of Technology.