5
II. TINJAUAN PUSTAKA
2.1. Tanaman Kakao
Kakao (Theobroma cacao Linn) adalah tanaman tahunan dari famili Sterculiaceae, berupa pohon dengan percabangan agak rendah dengan tinggi 3-15 meter. Bunga muncul dari batang dan cabang yang tua. Buah berbentuk lonjong dengan kulit beralur-alur dan daging buah yang lunak. Pada waktu muda, biji-biji menempel pada bagian dalam kulit buah, setelah matang akan lepas dan berbunyi jika diguncang. Biji-biji inilah yang akan dimanfaatkan dalam industri makanan. Kakao merupakan satu-satunya dari 22 jenis marga Theobroma, suku Sterculiaceae, yang diusahakan secara komersial. Menurut Tjitrosoepomo (1988) sistematika tanaman ini sebagai berikut:
Divisi : Spermatophyta Anak divisi : Angioospermae Kelas : Dicotyledoneae Anak kelas : Dialypetalae Bangsa : Malvales Suku : Sterculiaceae Marga : Theobroma
Jenis : Theobroma cacao L
Ada bermacam-macam kakao, namun yang umum dibudidayakan adalah
Criollo, Forestero, dan Trinitario yang merupakan varietas dari Theobroma
cacao. Varietas Criollo menghasilkan biji kakao yang bermutu baik, buahnya
6
permukaan kulit buah kasar, biji buahnya besar-besar dengan kotiledonnya berwarna putih atau jingga. Varietas Forestero menghasilkan biji yang bermutu rendah (bulk cacao), namun tanamannya kuat, produksinya tinggi, buahnya berbentuk gerigi, berdinding buah tebal, berwarna kuning jika cukup masak, biji buahnya kecil, berwarna jingga tua, kulitnya lebih halus, dan alur rusuknya tidak dalam. Varietas Trinitario merupakan hasil silangan alami antara Criollo dan Forestero (Susanto, 1994).
2.2 Buah Kakao
Buah kakao dapat dipanen apabila telah mencapai umur buah 160-175 hari atau sekitar 5-6 bulan sejak dari fase penyerbukan dan terjadi perubahan warna kulit buah (Haryadi dan Supriyanto, 1991; Bucheli et al., 2001). Menurut Sunanto (1992), kakao masak pohon dan siap panen dicirikan dengan perubahan warna buah, yaitu: (a) warna buah sebelum masak hijau, setelah masak warna alur buah menjadi kuning, atau (b) warna buah sebelum masak merah tua, setelah masak warna buah merah muda, jingga atau kuning.
Buah kakao masak berisi sekitar 30-40 biji yang terbungkus oleh lapisan lendir (pulpa). Menurut Haryadi dan Supriyanto (1991), berat biji kakao yang diperoleh dipengaruhi oleh curah hujan selama periode pemasakan, berkisar antara 92,2 – 103,5 g biji kakao basah segar setiap buah (pod) tergantung dari besarnya curah hujan. Pada musim hujan diperoleh buah kakao yang lebih besar dibandingkan pada musim kemarau (Wardojo, 1991).
Pemanenan buah kakao umumnya berlangsung antara bulan Mei sampai dengan Oktober tiap tahunnya. Di Jawa Tengah panen besar biasanya pada bulan Mei-Juni dan penen tambahan pada bulan Agustus-Oktober. Sedangkan di
7
Sumatra Utara, panen besar pada bulan Mei-Juni dan panen tambahan pada bulan September-Oktober. Rotasi pemanenan biasanya dilakukan dengan selang waktu antara 7-14 hari, dimaksudkan untuk memperoleh hasil panen tepat masak dengan tingkat masak relatif homogen (Haryadi dan Supriyanto, 1991).
Pulpa biji kakao, yaitu selaput berlendir berwarna putih yang membungkus biji kakao, mengandung : 82-87% air, 10-13% gula, 2-3% pentosan, 1-2% asam sitrat dan 8-10% garam-garam (Lopez, 1986). Pembentukan senyawa gula pada pulpa mencapai maksimal pada buah masak optimal (170 hari), begitu pula dengan peningkatan kandungan asam-asam organik. Pada buah masih muda, senyawa gula yang terbentuk masih sangat rendah sehingga mungkin akan ber-pengaruh pada kondisi pulpa untuk difermentasi (Haryadi dan Supriyanto, 1991). Selama pemasakan buah, pada keping biji terjadi peningkatan kandungan tanin dan karbohidrat serta terjadi konversi asam-asam lemak bebas menjadi trigeliserida (Lopez,1986). Haryadi dan Supriyanto (1991) menambahkan bahwa lemak netral baru terbentuk pada tahap akhir pemasakan.
2.3 Pengolahan Kakao
Pengolahan kakao pada dasarnya adalah suatu usaha untuk memisahkan biji dari buah dan selaput berlendir (pulpa) yang membungkus dan memperlakukannya sedemikian rupa sehingga diperoleh biji kakao kering dengan karakteristik khas yang sesuai dengan standar mutunya. Setiap buah kakao berisi sekitar 30-40 biji dan masing-masing biji diselubungi oleh pulpa (Wood and Lass, 1985; Beckett, 1988). Buah yang telah dipetik kemudian dipecah untuk dipisahkan bijinya. Menurut Askindo (1990), dikenalkan cara lain yaitu melakukan penyimpanan buah selama 9-15 hari sebelum biji dipecah. Hasil
8
penelitian Said et al. (1990), menyarankan agar penyimpanan buah dilakukan selama 6 hari, sedangkan Yusianto dan Wahyudi (1991) mengatakan bahwa waktu penyimpanan buah optimum adalah 8 hari untuk meningkatkan mutu biji kakao. Perlakuan penyimpanan buah tersebut akan mempengaruhi kondisi pulpa biji kakao sebelum difermentasi.
Biji yang sudah dipisahkan selanjutnya difermentasi. Fermentasi dapat dilakukan dengan menumpuk biji kakao pada kotak kayu (peti), ember plastik, keranjang bambu atau hanya sekedar dionggokkan di atas lantai dengan dialasi dan ditutupi dengan daun pisang. Ukuran wadah fermentasi bervariasi antara 1.500 – 2.000 kg biji kakao segar. Lama fermentasi juga bervariasi antara 2 - 8 hari, tergantung dari jenis kakao dan kebiasaan setempat (Nasution et al., 1980). Amin (2004a) menambahkan bahwa lama fermentasi adalah 5 hari, sesuai dengan kebiasaan yang dilakukan di perkebunan Indonesia atau sama dengan hasil penelitian Sime-Cadbury. Sedangkan menurut Wood and Lass (1985) lama fermentasi adalah 5 hari untuk varietas Forastero dan 2-3 hari untuk Criollo, tetapi menurut penelitian Schwan (1998) fermentasi dilakukan selama 7 hari dan biji diaduk setiap hari untuk meningkatkan aerasi.
Perendaman dan pencucian dilakukan setelah proses fermentasi, tetapi tidak semua pengolah melakukan tahapan proses ini. Perendaman dan pencucian selain untuk membersihkan sisa-sisa pulpa yang masih menempel juga dapat mencegah fermentasi lebih lanjut. Perendaman dalam air dapat dilakukan selama 2 jam, selanjutnya dilakukan pencucian secara manual pada air mengalir atau semi mekanis dengan mesin pencuci (Nasution et al., 1980).
9
Kadar air biji kakao hasil fermentasi berkisar 60%, sehingga untuk menurunkan kadar air hingga 6-7% diperlukan pengeringan. Pengeringan biji kakao lebih baik dilakukan dengan penjemuran, tetapi saat ini cenderung digantikan dengan pengering buatan karena lebih cepat. Di perkebunan besar biasanya digunakan kombinasi antara penjemuran dengan pengering buatan. Pengeringan dengan sistem mekanis sebaiknya dilakukan pada suhu antara 50-60oC, karena jika dilakukan di atas suhu tersebut akan menyebabkan bau hangus (Hardiman dan Kartika, 1980). Guritno dan Hardjosuwito (1984) menambahkan bahwa suhu pengeringan dianjurkan tidak lebih dari 55oC untuk mendapatkan hasil biji kakao kering yang bermutu baik.
2.4 Mekanisme Fermentasi Kakao
Fermentasi biji kakao bertujuan untuk menghancurkan pulpa (eskternal) dan mengusahakan kondisi untuk terjadinya reaksi kimia dan biokimia dalam keping biji (internal). Pulpa yang telah hancur akan mudah lepas dari biji sehingga biji kakao menjadi bersih dan cepat kering. Selanjutnya reaksi kimia dan biokimia dalam keping biji dimaksudkan untuk pembentukan prekursor cita rasa dan warna coklat. Reaksi tersebut baru akan terjadi setelah biji kakao mati. Faktor-faktor yang mempengaruhi proses fermentasi tersebut, diantaranya: waktu fermentasi, pengadukan dan aerasi, ukuran tumpukan biji dalam wadah fermentasi, penundaan pengolahan, kemasakan buah, dan varietas kakao (Haryadi dan Supriyanto, 1991).
Mekanisme proses fermentasi bermula dari adanya pulpa yang membungkus biji kakao segar. Ketika baru dipecah pulpa dalam keadaan steril, tetapi kemudian terkontaminasi oleh mikroorganisme dari kulit buah, serangga,
10
alat angkut maupun manusia sebagai perkerjanya. Menurut Lopez (1986), kandungan gula yang relatif tinggi, pH rendah dan suplai oksigen yang rendah pada tumpukan biji selama tahap awal fermentasi menyebabkan yeast mampu berkembang dengan baik. Lebih lanjut menurut Amin (2004b), aktivitas utama dari yeast tersebut adalah: (a) disimilasi sukrosa, glukosa dan fruktosa menjadi etanol dan CO2, (b) kemungkinan terjadi pemecahan pektin dalam pulpa, dan (c) memetabolisme asam-asam organik (asam sitrat) yang terdapat dalam jumlah relatif banyak pada pulpa biji kakao.
Jenis yeast tertentu juga dapat menghasilkan enzim pektolitik, yang dapat merombak pektin dalam pulpa. Perubahan komposisi pulpa sebelum dan setelah fermentasi (Case, 2004), disajikan seperti Tabel 1.
Tabel 1. Perubahan komposisi pulpa
Komposisi Sebelum fermentasi Setelah fermentasi
Sukrosa 12 % 0 % Asam sitrat 1 – 3 % 0.5 % Pektin 1 - 1.5 % - pH 3.7 6.5 Etil alkohol - 0.5 % Asam asetat - 1.6 % Sumber : Case (2004).
Selanjutnya menurut Chong et al. (1978), desimilasi asam sitrat oleh yeast menyebabkan naiknya pH yang disertai dengan naiknya suhu karena panas yang timbul pada fermentasi alkohol, menjadikan kondisi ini cocok untuk pertumbuhan bakteri asam laktat meskipun masih dalam keadaan anaerob. Bakteri asam laktat yang mempunyai sifat homo- dan hetero-fermentatif dapat menghidrolisis substrat gula menghasilkan asam laktat, asam asetat, etanol dan CO2 disertai dengan
11
pembebasan panas. Amin (2004b) menambahkan bahwa produksi asam laktat dari gula heksosa oleh bakteri asam laktat akan membantu dalam peningkatan suhu.
Kemudian dengan semakin naiknya suhu mencapai 45-50oC dan adanya aerasi karena proses pengadukan menyebabkan pertumbuhan bakteri asam asetat menjadi dominan. Proses ini berlangsung pada 24-48 jam pada awal fermentasi (Schwan, 1998). Asam asetat dan panas yang dihasilkan dari oksidasi etanol dapat menyebabkan biji mati, dikenal sebagai fermentasi fase I.
Kematian biji dikehendaki untuk berlangsungnya perubahan-perubahan fisik, kimia dan biokimia (enzimatis) di dalam keping biji (Sulistyowati, 1988; Alamsyah, 1991). Pada biji yang sudah mati (fermentasi fase II), enzim dan subtrat yang sebelumnya terpisah menjadi mudah bertemu. Etanol, asam asetat dan air yang berdifusi ke dalam keping biji bertindak sebagai pelarut dan mem-bawa subtrat ke tempat yang aktif. Perubahan dalam keping biji berdampak pada pengembangan cita rasa khas kakao dan pembentukan warna coklat (Lopez, 1986).
2.5 Penghancuran Pulpa
Salah satu tujuan fermentasi adalah penghancuran pulpa biji kakao. Proses ini dapat berlangsung karena terjadinya depolimerisasi pektin pulpa. Depolimerisasi pektin dapat berlangsung karena adanya aktivitas enzim pektolitik yang menghidrolisis substrat pektin, yaitu polisakarida struktural pada dinding sel primer dan ruang antar sel. Aktivitas enzim tersebut dalam menghidrolisis pektin menyebabkan jaringan pulpa rusak terdisintegrasi, membentuk cairan dan menetes keluar dari tumpukan biji (watery sweatings).
12
Pada fermentasi biji kakao secara alami, mekanisme penghancuran pulpa didasarkan atas aktivitas mikroba yang dapat menghasilkan enzim-enzim pektolitik (eksojinus). Pendapat ini didukung oleh ditemukannya strain yeast yang dapat menghasilkan enzim pektolitik pendegradasi pektin, misalnya
Kluyveromyces fragilis (dulunya Saccharomyces) (Carr, 1982; Schwan, 1998).
Buamah et al. (1997), menambahkan bahwa penggunaan kultur murni Saccharomyces chevalieri dan Kluyveromyces fragilis pada fermentasi biji kakao dapat meningkatkan volume watery sweatings. Gálvez et al. (2007), juga menemukan beberapa strain yeast yang menghasilkan enzim pektolitik pendegradsi pektin pulpa biji kakao seperti: Candida inconspicua, Hanseniaspora guillermondii dan Candida zeylanoides.
Menurut Quesnel (1967) dalam Haryadi dan Supriyanto (1991), jenis yeast tertentu juga dapat menghasilkan enzim pektolitik, diantaranya pektin metil esterase (PME) dan poligalakturonase (PG). Menurut Fox (1991); Whitaker (1996), enzim PME menghidrolisis ikatan metil ester pada pektin menjadi asam pektat dan metanol. Pelepasan metil ester menyebabkan asam pektat lebih banyak memiliki gugus karboksilat bebas. Sedangkan PG, menghidrolisis ikatan glikosidik antar unit-unit asam galakturonat (asam pektat) yang berdekatan dengan gugus karboksilat bebas. Hasil hidrolisis asam pektat akan terbentuk asam uronida (galakturonat), galaktosa, arabinosa dan asam asetat. Hal ini menyebabkan pektin mengalami depolimerisasi. Bower and Cutting (1988); Nikolic and Mojovic (2007), menambahkan bahwa proses yang didahului oleh aktivitas enzim PME dalam mendemetilasi pektin akan memberikan kondisi substrat yang lebih baik bagi aktivitas enzim PG pada depolimerisasi pektin.
13
Lebih lanjut menurut Turner et al. (2007), bahwa beberapa enzim pektolitik terlibat dalam depolimerisasi pektin, baik dengan cara hidrolisis seperti: pektinmetilgalakturonase, endo-PG dan ekso-PG yang menghidrolisis asam galakturonat, maupun dengan cara trans-β-eliminasi seperti pektin liase. Nikolic and Mojovic (2007), menambahkan bahwa degradasi pektin dikatalisis oleh enzim-enzim pektolitik, baik yang endojinus maupun yang eksojinus.
2.6 Hasil Samping Fermentasi
Limbah yang mengandung asam asetat dalam konsentrasi pekat sangat membahayakan bagi lingkungan apabila dibuang langsung tanpa proses pengelolahan terlebih dahulu. Limbah asam asetat memiliki tingkat keasaman yang sangat tinggi, disamping itu memiliki sifat korosif. Limbah tersebut dapat menyebabkan kerusakan lingkungan terutama badan air yang tercemari contohnya, akar-akar tanaman akan membusuk dan ikan-ikan akan mati serta daun tanaman akan menggulung yang menyebabkan terhambatnya proses fotosintesis (Abied, 2010).
Cairan pulpa yang merupakan hasil samping selama fermentasi biji kakao, diantaranya mengandung asam asetat atau asam cuka, asam laktat dan alkohol. Asam-asam organik tersebut terbentuk dari fermentasi gula yang terkandung dalam pulpa biji kakao. Pulpa biji kakao adalah selaput berlendir berwarna putih yang membungkus biji kakao, terdapat sekitar 25-30% dari berat biji, diantaranya mengandung gula dengan kadar yang relatif tinggi sekitar 10-13% (Lopez, 1986). Selama fermentasi dapat dihasilkan 15-20% cairan pulpa dari berat biji kakao (Ganda-Putra et al., 2008).
14
Secara umum dapat dikemukakan bahwa asam asetat dapat dihasilkan secara alami melalui fermentasi dan secara sintetis kimiawi. Bila cairan pulpa hasil fermentasi biji kakao potensial sebagai sumber bahan baku asam asetat untuk dibuat menjadi produk cuka fermentasi, tentunya akan dapat meningkatkan nilai tambah hasil perkebunan kakao dan memberi kontribusi dalam penyediaan bahan baku asam asetat. Mengingat dalam setahun, kebutuhan dunia akan asam asetat mencapai 6,5 juta ton, dimana 1.5 juta ton diperoleh dari hasil daur ulang, sisanya dari industri petrokimia dan dari sumber hayati. Asam asetat diantaranya dapat digunakan sebagai pereaksi kimia, bahan baku industri dan sebagai pemberi rasa asam dan aroma dalam makanan (Anonymous, 2011a).
Pada akhirnya, dari semua hal di atas, diharapkan akan dapat memberikan kontribusi positif dalam usaha pengembangan perkakaoan di Indonesia. Hal demikian merupakan bagian dari misi institusi Perguruan Tinggi sebagai agen pengembangan ipteks untuk membantu memecahkan permasalahan di masyarakat, khususnya masyarakat perkakaoan Indonesia. Selain itu juga untuk memberdayakan industri pengolahan kakao Indonesia agar sebesar-besarnya memanfaatkan hasil samping dari proses pengolahan kakao dalam rangka menunjang program ketahanan dan keamanan pangan. Lebih khusus pada isu
strategis penanganan pasca panen dan konsumsi dengan konsep/pemikiran untuk peningkatan nilai tambah hasil pertanian dengan mengolah menjadi produk
lanjutan. Hal demikian dapat dilakukan melalui penelitian rancang bangun dan teknologi produksi sektor hilir hasil perkebunan kakao.
15 2.7 Cuka Fermentasi
Cuka Fermentasi termasuk golongan asam asetat yang merupakan senyawa kimia asam organik yang dikenal sebagai pemberi rasa asam dan aroma dalam makanan. Asam asetat memiliki rumus empiris C2H4O2. Rumus ini seringkali ditulis dalam bentuk CH3-COOH, CH3COOH, atau CH3CO2H. Asam asetat murni (disebut asam asetat glasial) adalah cairan higroskopis tak berwarna, dan memiliki titik beku 16,7°C. Asam asetat merupakan salah satu asam karboksilat paling sederhana, setelah asam format. Larutan asam asetat dalam air merupakan sebuah asam lemah, artinya hanya terdisosiasi sebagian menjadi ion H+ dan CH3COO-. Asam asetat merupakan pereaksi kimia dan bahan baku industri yang penting. Asam asetat digunakan dalam produksi polimer seperti polietilena tereftalat, selulosa asetat, dan polivinil asetat, maupun berbagai macam serat dan kain. Dalam industri makanan, asam asetat digunakan sebagai pengatur keasaman. Di rumah tangga, asam asetat encer juga sering digunakan sebagai pelunak air. (Anonymous, 2011a).
Asam asetat diproduksi secara sintetis maupun alami melalui fermentasi mikroba. Sekarang hanya 10% dari produksi asam asetat dihasilkan melalui jalur alami, namun kebanyakan hukum yang mengatur bahwa asam asetat yang terdapat dalam cuka haruslah berasal dari proses biologis. Dari asam asetat yang diproduksi oleh industri kimia, 75% diantaranya diproduksi melalui karbonilasi metanol. Sisanya dihasilkan melalui metode-metode alternatif. Dalam setahun, kebutuhan dunia akan asam asetat mencapai 6,5 juta ton, dimana 1,5 juta ton diperoleh dari hasil daur ulang, sisanya diperoleh dari industri petrokimia maupun dari sumber hayati (Noriyki et al., 2001 dalam Anonymous, 2011a).
16
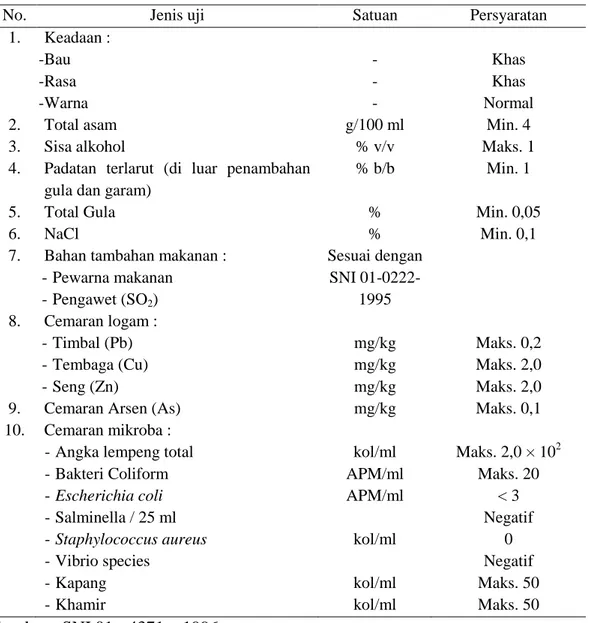
Asam asetat yang berasal dari hasil fermentasi disebut cuka fermentasi. Cuka fermentasi didefinisikan sebagai produk cair yang mengandung asam asetat, diperoleh melalui fermentasi bahan-bahan yang mengandung gula atau alkohol dengan atau tanpa penambahan bahan tambahan makanan yang diijinkan (SNI 01-4371-1996). Standar mutu cuka fermentasi menurut SNI 01- 4371-1996 ditunjukkan pada Tabel 2.
Tabel 2. Standar mutu cuka fermentasi menurut SNI 01 - 4371 – 1996
No. Jenis uji Satuan Persyaratan
1. Keadaan : -Bau -Rasa -Warna - - - Khas Khas Normal
2. Total asam g/100 ml Min. 4
3. Sisa alkohol % v/v Maks. 1
4. Padatan terlarut (di luar penambahan gula dan garam)
% b/b Min. 1
5. Total Gula % Min. 0,05
6. NaCl % Min. 0,1
7. Bahan tambahan makanan : -Pewarna makanan -Pengawet (SO2) Sesuai dengan SNI 01-0222-1995 8. Cemaran logam : -Timbal (Pb) -Tembaga (Cu) -Seng (Zn) mg/kg mg/kg mg/kg Maks. 0,2 Maks. 2,0 Maks. 2,0
9. Cemaran Arsen (As) mg/kg Maks. 0,1
10. Cemaran mikroba : -Angka lempeng total -Bakteri Coliform -Escherichia coli -Salminella / 25 ml -Staphylococcus aureus -Vibrio species -Kapang -Khamir kol/ml APM/ml APM/ml kol/ml kol/ml kol/ml Maks. 2,0 × 102 Maks. 20 < 3 Negatif 0 Negatif Maks. 50 Maks. 50 Sumber : SNI 01 - 4371 – 1996.
Asam asetat merupakan nama trivial yang paling dianjurkan oleh IUPAC. Nama ini berasal dari kata Latin acetum, yang berarti cuka. Nama sistematis dari
17
senyawa ini adalah asam etanoat sedangkan asam asetat glasial merupakan nama trivial yang merujuk pada asam asetat yang tidak bercampur air atau asam asetat murni (Hardoyo et al., 2007). Sifat fisika dan kimia asam asetat dapat dilihat pada Tabel 3.
Tabel 3. Sifat fisika dan sifat kimia asam asetat
Sifat fisika Sifat kimia
Densitas : 1,049-1,266 g/cm Asam lemah
Massa molar : 60,09 g/mol Higroskopis
Titik lebur : 16,5 oC -
Titik didih : 118,1 oC -
Titik beku : 16,7 oC -
Penampilan : cairan tidak berwarna -
Keasaman : 4, 76 pada suhu 25 oC -
Aroma : berbau khas -
Sumber : Anonymous (2012).
2.8 Proses Distilasi
Distilasi merupakan teknik pemisahan yang didasari atas perbedaan titik didih atau titik cair dari masing-masing zat penyusun dari campuran homogen. Dalam proses distilasi terdapat dua tahap proses yaitu tahap penguapan dan dilanjutkan dengan tahap pengembangan kembali uap menjadi cair. Atas dasar ini maka perangkat peralatan distilasi menggunakan alat pemanas dan alat pendingin. Zat yang memiliki titik didih lebih rendah akan menguap lebih dulu. Metode ini termasuk sebagai unit operasi kimia jenis perpindahan massa. Penerapan proses ini didasarkan pada teori bahwa pada suatu larutan, masing-masing komponen akan menguap pada titik didihnya. Ada 4 jenis distilasi, yaitu distilasi sederhana, distilasi fraksionasi, distilasi uap, dan distilasi vakum. Selain itu ada pula distilasi ekstraktif dan distilasi azeotropic homogenous, distilasi dengan menggunakan garam berion, distilasi pressure-swing, serta distilasi reaktif (Anonymous, 2011b).
18
Pada distilasi sederhana, dasar pemisahannya adalah perbedaan titik didih yang jauh atau dengan salah satu komponen bersifat volatil. Jika campuran dipanaskan maka komponen yang titik didihnya lebih rendah akan menguap lebih dulu. Selain perbedaan titik didih, juga perbedaan kevolatilan, yaitu kecenderungan sebuah substansi untuk menjadi gas. Distilasi ini dilakukan pada tekanan atmosfer. Aplikasi distilasi sederhana digunakan untuk memisahkan campuran air dan alkohol (Walangare et al., 2013).
Distilasi fraksionasi adalah memisahkan komponen-komponen cair, dua atau lebih, dari suatu larutan berdasarkan perbedaan titik didihnya. Distilasi ini juga dapat digunakan untuk campuran dengan perbedaan titik didih kurang dari 20 °C dan bekerja pada tekanan atmosfer atau dengan tekanan rendah. Aplikasi dari distilasi jenis ini digunakan pada industri minyak mentah, untuk memisahkan komponen-komponen dalam minyak mentah. Perbedaan distilasi fraksionasi dan distilasi sederhana adalah adanya kolom fraksionasi. Di kolom ini terjadi pemanasan secara bertahap dengan suhu yang berbeda-beda pada setiap platnya. Pemanasan yang berbeda-beda ini bertujuan untuk pemurnian distilat yang lebih dari plat-plat di bawahnya. Semakin ke atas, semakin tidak volatil cairannya (Anonymous, 2011b).
Distilasi uap digunakan pada campuran senyawa-senyawa yang memiliki titik didih mencapai 200°C atau lebih. Distilasi uap dapat menguapkan senyawa-senyawa ini dengan suhu mendekati 100°C dalam tekanan atmosfer dengan menggunakan uap atau air mendidih. Sifat yang fundamental dari distilasi uap adalah dapat mendistilasi campuran senyawa di bawah titik didih dari masing-masing senyawa campurannya. Selain itu distilasi uap dapat digunakan untuk
19
campuran yang tidak larut dalam air di semua temperatur, tapi dapat didistilasi dengan air. Aplikasi dari distilasi uap adalah untuk mengekstrak beberapa produk alam seperti minyak eucalyptus dari eucalyptus, minyak sitrus dari lemon atau jeruk, dan untuk ekstraksi minyak parfum dari tumbuhan. Campuran dipanaskan melalui uap air yang dialirkan ke dalam campuran dan mungkin ditambah juga dengan pemanasan. Uap dari campuran akan naik ke atas menuju ke kondensor dan akhirnya masuk ke labu distilat (Perdana et al., 2010).
Distilasi vakum biasanya digunakan jika senyawa yang ingin didistilasi tidak stabil, dengan pengertian dapat terdekomposisi sebelum atau mendekati titik didihnya atau campuran yang memiliki titik didih di atas 150°C. Metode distilasi ini tidak dapat digunakan pada pelarut dengan titik didih yang rendah jika kondensornya menggunakan air dingin, karena komponen yang menguap tidak dapat dikondensasi oleh air. Untuk mengurangi tekanan digunakan pompa vakum atau aspirator. Aspirator berfungsi sebagai penurun tekanan pada sistem distilasi ini (Anonymous, 2011b).