BAB 2
TINJAUAN PUSTAKA
2.1 Glukosamin
Glukosamin (2-amino-2-deoxyglucose, chitosamine) adalah gula amino yang
diperoleh dari hidrolisis kitin. Kitin terutama dihasilkan dari kulit luar golongan
Crustacea, Artropoda, dan cendawan. Dalam industri, glukosamin diproduksi dengan
cara hidrolisis rangka luar golongan Crustacea seperti udang dan kepiting.
Glukosamin pertama kali diidentifikasi oleh Dr. Georg Ledderhose pada tahun 1876,
tapi struktur stereokimia tidak sepenuhnya diketahui sampai ditemukan oleh Walter
Haworth pada tahun 1939. Glukosamin dalam tubuh manusia bergabung dalam
struktur tulang rawan dan bekerja untuk merangsang dan memperbaiki fungsi sendi.
Telah terbukti keefektifan glukosamin dalam banyak uji ilmiah yang menyatakan
bahwa glukosamin dapat mengurangi rasa sakit penyakit osteoarthritis, membantu
dalam rehabilitasi tulang rawan, memperbaharui cairan sinovial, dan memperbaiki
sendi yang telah rusak. (Mojarrad, et al. 2006)
Glukosamin telah dievaluasi sebagai sebuah agen terapi untuk penyakit radang
sendi di German sejak 1969. Senyawa glukosamin sulfat dat diturunkan dari kitin.
Dapat juga dihasilkan dengan cara sintetik. Di Eropa, glukosamin tersedia sebagai
obat resep. Di UK atau Amerika Utara, glukosamin tersedia sebagai makanan
suplemen diet.
Glukosamin ditemukan hampir di semua jaringan manusia tetapi paling tinggi
konsentrasinya terdapat dalam hati, ginjal dan tulang rawan. Ini merupakan blok
bangunan yang paling mendasar yang diperlukan untuk biosintesis berbagai senyawa
termasuk glikolipid, glikoprotein, glikosaminoglikan yang mana semua senyawa erat
terlibat dengan struktur dan fungsi sendi. Glukosamin juga senyawa penting dalam
membran sel dan permukaan sel protein serta struktur molekul intertisial yang
mengontrol sel bersama-sama. Baik langsung atau tidak langsung, glukosamin
sinovial, kulit, tulang, kuku, katup jantung, pembuluh darah, sekresi lendir dalam
pencernaan, pernafasan, dan sistem kemih.
O HO
HO
NH2 CH2OH
OH HO O
HO
NH3+ Cl -CH2OH
OH
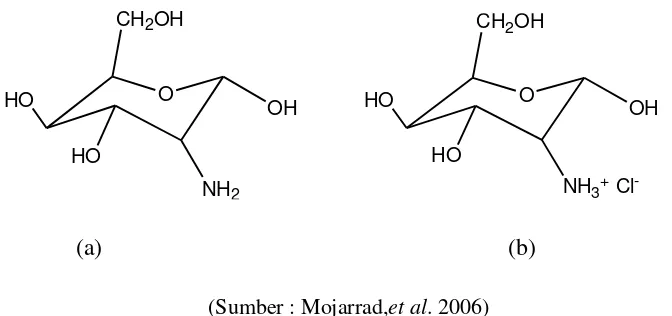
(a) (b)
(Sumber : Mojarrad,et al. 2006)
Gambar 2.1. (a) Struktur kimia glukosamin dan, (b) glukosamin hidroklorida
Dalam klinis, glukosamin dapat diberikan melalui intravena, intramuskular,
intra artikular dan rute oral. Sekitar 70% oral glukosamin sulfat diserap melalui usus
dan dikeluarkan melalui sistem ginjal. Sebagian besar uji klinis pada oral glukosamin
digunakan glukosamin dosis standar, 500 mg diminum tiga kali sehari, dengan atau
tanpa mengkonsumsi obat nyeri yang disarankan untuk pasien.
Penelitian laboratorium menunjukkan bahwa glukosamin dapat diserap melalui
saluran pencernaan. Studi radioisotop telah menunjukkan bahwa distribusi glukosamin
cepat ke seluruh tubuh dengan penyerapan selektif oleh artikular tulang rawan.
Penelitian vitro menunjukkan bahwa glukosamin dapat menstimulasi
glukosaminoglikan dan sintesis proteoglikan dalam gabungan jaringan. Dalam studi
hewan, dosis tinggi glukosamin telah terbukti memiliki efek anti inflamasi ringan.
(Martin, C.W. 2004)
2.1.1 Penyediaan Glukosamin
Produk glukosamin untuk radang sendi biasanya dirumuskan sebagai garam hidroklorida atau sulfat glukosamin dan sering menggabungkan dengan kondroitin
Glukosamin sulfat dapat dibuat dengan merefluks kitin dengan larutan asam
sulfat, namun reaksi ini memiliki hasil yang rendah. larutan asam sulfat dapat
mengoksidasi kelompok alkohol primer dan sekunder dalam kitin atau glukosamin.
Glukosamin sulfat sangat higroskopis yang sangat cepat terdegradasi (dari putih
menjadi putih kecokelatan) bila terkena uap air. Untuk menghindari masalah ini,
glukosamin sulfat dibuat dari glukosamin hidroklorida dengan menambahkan baik
kalium atau natrium sulfat dan hasil campurannya dikokristalisasi. Glukosamin sulfat,
fosfat, dan garam hidroiodin juga disiapkan dengan melewatkan larutan glukosamin
hidroklorida melalui resin penukar anion yang telah dikondisikan dengan asam sulfat,
asam fosfor, asam hidroiodin, atau garam logam dari satu asam ini. Penyusunan
glukosamin hidroklorida dari kitin merupakan reaksi hidrolisis sederhana. Selama
reaksi ini, kitin dideasetilasi dan didepolimerisasi menjadi glukosamin hidroklorida
dengan adanya larutan asam klorida.
Kamasastri dan Prabhu menyiapkan glukosamin dari kitin dengan perlakukan
penambahan klorida pekat berlebih. Kocourek, et al. kitin dihidrolisis dengan asam
klorida 37% dalam wadah air mendidih. Inoue mengusulkan 2,5 L asam klorida 20%
untuk hidrolisis 594,7 g kitin, yang telah diperoleh dari kerangka luar udang. Alphan
menggunakan asam klorida 37% pada suhu 100oC dengan larutan asam pada
perbandingan larutan 5:1. Ingle, et al. menerapkan 3 bagian asam klorida 20% pada
suhu 100oC selama 2 jam dengan pengadukan untuk hidrolisis kitin. (Mojarrad, et al.
2006).
2.2 Belangkas
Hewan mirip kepiting ini adalah hewan jenis artopoda yang hidup di perairan
dangkal dan kawasan mangrove. Kadang disebut juga dengan nama kepiting ladam,
mimi, atau mintuna. Kepiting ladam yang dalam bahasa Indonesia disebut
belangkas ialah hewan beruas yang bentuk badannya menyerupai “ladam kuda”
berekor sehingga di luar negeri, belangkas kerap dipanggil dengan nama "kepiting
tapal kuda" (horseshoe crab). Cetakan fosil hewan ini tidak mengalami perubahan
bentuk berarti sejak masa Devon (400-250 juta tahun yang lalu) dibandingkan dengan
bahasa Jawa untuk yang berkelamin jantan dan Mintuna adalah untuk yang
berkelamin betina.
Belangkas di dalam tangga klasifikasi ilmiah termasuk ke dalam filum
Arthropoda (hewan beruas-ruas) di mana hewan-hewan seperti kepiting, serangga, dan
kelabang juga termasuk ke dalam filum ini. Dasar dari penggolongan tersebut adalah
karena belangkas memiliki 6 pasang kaki dan tubuh yang beruas-ruas. Ada 4 spesies
belangkas yang diketahui oleh manusia dan masih hidup di masa kini di mana
keempat spesies tersebut digolongkan ke dalam famili Limulidae.
(Sumber : Abbas, 2012)
Gambar 2.2. Belangkas
Klasifikasi Belangkas
Kingdom : Animalia
Filum : Arthropoda
Kelas : Merostomata
Ordo : Xiphosura
Jenis-jenis :
1. Genus Carcinoscorpius
Carcinoscorpius rotundicauda, hidup di perairan mangrove Asia Tenggara
2. Genus Limulus
Limulus polyphemus, menghuni pantai-pantai timur Amerika Utara
3. Genus Tachypleus
- Tachypleus gigas, menghuni pantai Asia Tenggara dan Asia Selatan
- Tachypleus tridentatus, menghuni pantai-pantai Asia Timur (Abbas, 2012)
2.3 Kitin
Kitin merupakan poli (2-asetamido-2-deoksi-β-(1→4)-D-glukopiranosa)
dengan rumus molekul (C8H13NO5)n yang tersusun atas 47% C, 6% H, 7% N, dan
40% O. struktur kitin menyerupai struktur selulosa dan hanya berbeda pada gugus
yang terikat di posisi atom C-2 kitin adalah gugus N-asetil (-NHCOCH3, asetamida).
O HOH2C
HO
O NHCOCH3 *
* n
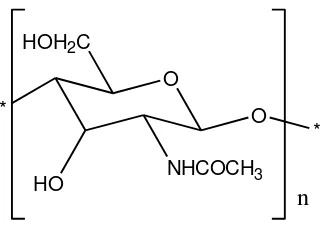
(Sumber : Mojarrad,et al. 2006) Gambar 2.3. Struktur kimia kitin
Di alam, kitin dikenal sebagai polisakarida yang paling melimpah setelah
jamur dari gugus Mucor, Phycomyces, dan Saccharomyces (Hirano, 1986; Knorr,
1991). Keberadaan kitin di alam umumnya terikat dengan protein, mineral, dan
berbagai macam pigmen. Sebagai contoh, kulit udang mengandung 25-40% protein,
40-50% CaCO3, dan 15-20% kitin, tetapi besarnya komponen tersebut masih
bergantung pada jenis udangnya (Altschul, 1976). Sebagian besar kelompok
Crustacea, seperti kepiting, udang, dan lobster, merupakan sumber utama kitin
komersial. Di dunia, kitin yang diproduksi secara komersial 120 ribu ton per tahun.
Kitin yang berasal dari kepiting dan udang besar 39 ribu ton (32,5%) dan dari jamur
32 ribu ton (26,7%)(Knorr, 1991).
Tabel 2.1. Kandungan kitin pada berbagai Crustacea
Sumber : Hirano, 1986
Jenis Organisme Kandungan Kitin (%)
Kepiting Cancer 72, 1c
Kepiting (Carcinus) 0,4-3,3
Kepiting Biru (Callinectes) 14a
Kepiting Matsuba (Chionecetes) 25,9d
Kepiting (Erimacrus) 18,4d
Hemigraprapsus 10,6d
Kepiting Raja (Paralithodes) 35b 10,4a
Kepiting Merah (Pleuroncodes) 1,3 1,8b
Udang Alaska 28d
Udang Crangon 5,8b 11,6d 69,1c
Metapenaeus 32,4d
Lobster (Nephrops) 69,8c
Lobster (Homarus) 60,8-77,0c
Penaeus 25d
Keterangan:
Berdasarkan bobot bahan organik pada kulit luar
d
Berdasarkan bobot kering total kulit luar
2.3.1 Sifat Kitin
Kitin merupakan bahan yang tidak beracun dan bahkan mudah terurai secara
hayati (biodegradable). Bentuk fisiknya merupakan padatan amorf yang berwarna
putih dengan kalor spesifik 0,373 ± 0,03 kal/g/oC (Knorr, 1984) dan derajat rotasi spesifik [α]D18 +22o pada kosentrasi asam metanasulfonat 1,0%. Sebagai biopolymer
kristalin, kitin terdapat dalam 3 bentuk Kristal di alam, yaitu α, β, dan γ. Kitin- α berbentuk Kristal ortorombik dengan setiap unit selnya mengandung 4 cincin N
-asetil-D-glukosamina yang ditautkan dengan 2 ikatan glikosidik β-(1→4) dan tertara secara
antiparalel, rapat, dan kompak. Kitin-β berbentuk kristalin monoklin dan setiap
unitnya terdiri atas 2 cincin N-asetil-D-glukosamina dan 2 molekul air yang tertara
secara parallel. Sementara struktur kitin-γ diduga dalam 2 penataan, yaitu 2 rantai
paralel dan 1 antiparalel. Ketiga bentuk kristalin tersebut dapat dibedakan dengan
menggunakan spektroskopi IR pada bilangan gelombang 3160 dan 3190 cm-1.
Kitin hampir tidak larut dalam air, asam encer, dan basa, tetapi larut dalam
asam formiat, asam metanasulfonat, N,N-dimetilasetalmida yang mengandung 5%
litium klorida, heksafluoroisopropil alkohol, heksafluoroaseton dan campuran
1,2-dikloroetana-asam trikloroasetat dengan nisbah 35:65 (% [v/v])(Hirano, 1986). Asam
mineral pekat seperti H2SO4, HNO3, dan H3PO4 dapat melarutkan kitin sekaligus
menyebabkan rantai panjang kitin terdegradasi menjadi satuan-satuan yang lebih kecil
(Bastaman,1989).
2.3.2. Kegunaan Kitin dan Kitosan
Dewasa ini aplikasi kitin dan kitosan sangat banyak dan meluas. Di bidang
industri, kitin, dan kitosan berperan antara lain sebagai koagulan polielektrolit
mikroalga, pewarna, residu pestisida, lemak tanin, PCB (poliklorinasi bifenil), mineral
dan asam organik, media kromatografi afinitas, gel dan pertukaran ion, penyalut
berbagai serat alami dan sintetik, pembentukan film dan membran mulai terurai,
meningkatkan kualitas kertas, pulp, dan produk tekstil. Sementara dibidang pertanian
dan pangan kitin dan kitosan digunakan sebagai pencampur ransum pakan ternak,
antimikrob, antijamur, serat bahan pangan, penstabil, pembentuk gel, pembentuk
tekstur, pengental dan pengemulsi produk olahan pangan, pembawa zat aditif
makanan, flavor, zat gizi, pestisida, herbisida, virusida tanaman, dan deasedifikasi
buah-buahan, sayuran dan penjernih sari buah. Fungsinya sebagai antimikroba dan
antijamur juga diterapkan dibidang kedokteran kitin dan kitosan dapat mencegah
pertumbuhan Candida albican dan Staphvlacoccus aureus. Selain itu bipolimer
tersebut juga berguna sebagai antikoagulan, antitumor, antivirus, pembuluh
darah-kulit dan ginjal sintetik, bahan pembuat lensa kontak, aditif kosmetik, membran di
alis, bahan shampoo dan kondisioner rambut, zat hemostatik, penstabil liposom,bahan
ortoprdik, pembalut luka dan benang bedah yang mudah diserap, serta mempertinggi
daya kekebalan, antiinfeksi. (Purwantiningsih,S. 2009).
2.4 Spektrofotometer Ultraviolet (UV)
Spektrum absorpsi dalam daerah-daerah ultraungu dan tampak umumnya
terdiri dari satu atau beberapa pita absorpsi yang lebar. Semua molekul dapat
menyerap radiasi dalam daerah UU-tampak, oleh karena mereka mengandung
elektron, baik yang dipakai bersama maupun tidak, yang dapat dieksitasi ke tingkat
energi yang lebih tinggi di dalam molekul. Elektron dalam satu ikatan kovalen tunggal
erat terikat, dan radiasi dengan energi tinggi, atau panjang gelombang pendek,
diperlukan untuk eksitasinya. Spektrum absorpsi dapat diperoleh dengan
menggunakan bermacam-macam bentuk contoh : gas, lapisan tipis cairan, larutan
dalam bermacam-macam pelarut, dan bahkan padat. Kebanyakan pekerjaan analitik
menyangkut larutan, dan kita mengharapkan disini untuk mengembangkan satu uraian
kuantitatifdari hubungan antara konsentrasi larutan dan kemampuannya untuk
menyerap radiasi. Pada waktu yang sama, kita harus sadar bahwa besarnya absorpsi
telah kita lihat, absorpsi juga tergantung pada panjang gelombang radiasi dan tabiat
jenis zat molekular dalam larutan.
Hubungan antara absorpsi radiasi dan panjang jalan melalui medium yang
menyerap pertama kali dirumuskan oleh Bouguer (1729), meskipun kadang-kadang
dianggap berasal dari Lambert (1768). Marilah kita membagi sebuah medium
penyerap yang homogen, seperti suatu larutan kimia, menjadi lapisan-lapisan maya,
masing-masing dengan ketebalan yang sama. Jika suatu sinar radiasi monokhromatik
(yaitu radiasi dari satu panjang gelombang tunggal) diarahkan melewati medium,
diketahui bahwa tiap lapisan menyerap bagian yang sama dari radiasi, atau tiap
lapisan mengurangi tenaga radiasi sinar dengan bagian yang sama. Pernyataan
persamaan ini dapat berbunyi: Tenaga radiasi yang ditransmisikan berkurang secara
eksponensial jika tebal medium penyerap bertambah secara aritmatik.
Hubungan antara konsentrasi macam zat penyerap dan besarnya absorpsi
dirumuskan oleh Beer dalam tahun 1859. Hukum beer analog dengan hukum Bouguer
dalam menguraikan pengurangan eksponensial dalam tenaga transmisi dengan satuan
peningkatan aritmatik dalam konsentrasi. Hukum Beer dapat digunakan dengan tepat
hanya untuk radiasi monokhromatik dan sifat macam zat yang menyerap ditetapkan di
atas jangkauan konsentrasi yang bersangkutan, maka disebut “penyimpangan” dari
hukum Beer.
Hukum-hukum Baouguer dan Beer dengan mudah digabung menjadi
pernyataan yang sesuai. Kita mengetahui bahwa dalam mempelajari akibat perubahan
konsentrasi terhadap absorpsi, jarak jalan lewat larutan harus dibuat tetap, tetapi
hasil-hasil yang diukur akan tergantung pada besarnya harga tetapan.
2.4.1 Peralatan untuk Spektrofotometer
Spektrofotometer adalah alat untuk mengukur transmitan atau absorban suatu
contoh sebagai fungsi panjang gelombang, pengukuran terhadap suatu deretan contoh
pada suatu panjang gelombang tunggal mungkin juga dapat dilakukan. Alat-alat
demikian dapat dikelompokkan baik sebagai manual atau perekam, maupun sebagai
(Sumber : Underwood,A.L. 1983)
Gambar 2.4. Bagan Alat Spektrofotometer
Unsur-unsur terpenting suatu spektrofotometer yaitu:
1. Sumber energi radiasi yang kontiniu dan meliputi daerah spektrum, dimana alat
ditujukan untuk dijalankan.
2. Monokhromator, yang merupakan suatu alat untuk mengisolasi suatu berkas
sempit dari panjang gelombang-panjang gelombang dari spektrum yang luas yang
disiarkan oleh sumber.
3. Wadah untuk contoh
4. Detektor yang merupakan suatu transducer yang mengubah energi radiasi menjadi
isyarat listrik.
5. Penguat dan rangkaian yang bersangkutan yang membuat isyarat listrik cocok
untuk diamati.
6. Sistem pembacaan yang dapat mempertunjukkan besarnya isyarat listrik.
(Underwood,A.L. 1983)
2.5 Spektroskopi FTIR
Pancaran inframerah pada umumnya mengacu pada bagian spektrum
elektromagnet yang terletak di antara daerah tampak dan daerah gelombang mikro.
Bagi kimiawan organik, sebagian besar kegunaannya terbatas di antara 4000 cm-1 dan
Sumber Monokhromator Sampel Detektor
666 cm-1 (2,5 – 15,0 μm). Sebuah molekul yang paling sederhana sekalipun dapat
memberikan spektrum yang sangat rumit. Kimiawan organik mengambil keuntungan
dari kerumitan spektrum itu dengan membandingkan spektrum senyawa yang tidak
diketahui terhadap spektrum cuplikan yang asli. Suatu kesesuaian puncak demi
puncak merupakan bukti yang kuat tentang identitasnya. Selain enantiomer, dua
senyawa tidak mungkin memberikan spektrum inframerah yang sama.
Pancaran infra-merah terbatas di antara 4000 cm-1 dan 666 cm-1 (2,5 – 15,0 μm), diserap oleh sebuah molekul organik dan diubah menjadi energi getaran molekul. Penyerapan ini juga tercatu, namun spektrum getaran tampak bukan sebagai
garis-garis melainkan berupa pita-pita. Letak pita dalam spektrum inframerah disajikan
sebagai bilangan gelombang atau panjang gelombang. Satuan bilangan gelombang
(cm-1, kebalikan sentimeter). Terdapat dua macam getaran molekul yaitu getaran ulur
dan getaran tekuk. Getaran ulur adalah suatu gerakan berirama di sepanjang sumbu
ikatan sehingga jarak antar atom bertambah atau berkurang. Getaran tekuk dapat
terjadi karena perubahan sudut-sudut ikatan antara ikatan-ikatan pada sebuah atom.
(Silverstein, R.M. 1986)
Spektroskopi IR juga digunakan untuk penentuan struktur, khususnya senyawa
organik dan juga untuk analisa kuantitatif. Spektrum infra merah memberikan puncak
maksimal yang jelas sebaik puncak minimumnya. Spektrum absorpsi dibuat dengan
bilangan gelombang pada sumbu X dan persentase transmitan (T) pada sumbu Y. Bila
dibandingkan dengan daerah UV-tampak, dimana energi dalam daerah ini dibutuhkan
untuk transisi elektronik, maka radiasi infra merah hanya terbatas pada perubahan
energi setingkat molekul. Untuk tingkat molekul, perbedaan dalam keadaan vibrasi
dan rotasi digunakan untuk mengabsorpi sinar inframerah. Jadi, untuk dapat
mengabsorpi, molekul harus memiliki perubahan momen dipole sebagai akibat dari
vibrasi. Berarti radiasi medan listrik yang berubah-ubah akan berinteraksi dengan
molekul dan akan menyebabkan perubahan amplitude salah satu gerakan molekul.
(Khopkar,S.M.2008)
2.5.1 Peralatan untuk Spektrofotometer Inframerah
Komponen dasar spektrofotometer IR sama dengan UV-tampak, tetapi sumber,
dilewatkan melalui sampel dan larutan pembanding, kemudian dilewatkan pada
monokromator untuk menghilangkan sinar yang tidak diinginkan (stray radiation).
Berkas ini kemudian didispersikan melalui prisma. Dengan melewatkannya melalui
slit, sinar tersebut dapat difokuskan pada detektor. (Khopkar,S.M.2008)
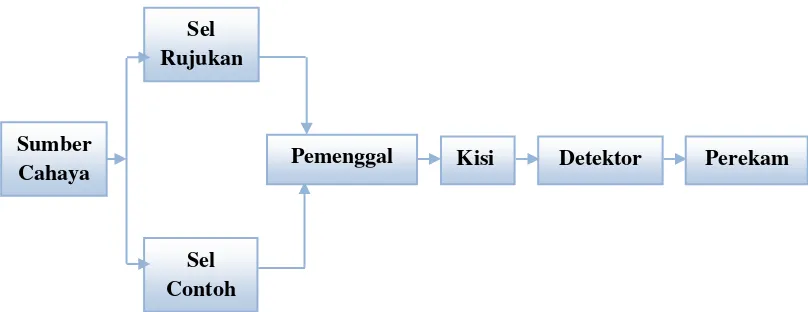
(Sumber : Fessenden,R.J.1983)
Gambar 2.5. Bagan Alat Spektroskopi Inframerah
Instrumen yang digunakan untuk mengukur resapan radiasi inframerah pada
berbagai panjang gelombang disebut spektrofotometer inframerah. Komponen alat
yang khas adalah sumber cahaya yang memancarkan cahaya inframerah pada semua
panjang gelombang. Cahaya dari sumber ini pecah oleh sistem cermin menjadi dua
berkas cahaya, berkas rujukan (referensi) dan berkas contoh. Setelah masing-masing
melewati sel rujukan (pelarut murni, jika pelarut itu digunakan dalam contoh, atau
kosong jika contoh tak menggunakan pelarut) dan sel contoh, kedua berkas ini
digabung kembali dalam pemenggal (chopper; suatu sistem cincin lain), menjadi suatu
berkas yang berasal dari kedua berkas itu, yang selang-seling bergantian. Berkas
selang-seling ini didifraksi oleh suatu kisi sehingga berkas itu terpecah menurut
panjang gelombang. Detektor mengukur beda intensitas antara kedua macam berkas
tadi pada tiap-tiap panjang gelombang dan meneruskan informasi ini ke perekam,
yang menghasilkan spektrum. Pita-pita inframerah dalam sebuah spektrum dapat
dikelompokkan menurut intensitasnya : kuat (s, strong), medium (m) dan lemah (w,
Sumber Cahaya
Sel Contoh
Sel Rujukan
weak). Suatu pita lemah yang bertumpang-tindih dengan suatu pita kuat disebut bahu
(sh, shoulder). Banyaknya gugus identik dalam sebuah molekul mengubah kekuatan
relatif pita absopsinya dalam suatu spektrum. (Fessenden,R.J.1983)
2.5.2 Spektrum Inframerah untuk Glukosamin
Karakterisasi glukosamin hidroklorida dapat ditentukan dengan menggunakan
spektroskopi inframerah. Menurut Mojarrad et al. (2006) spektrum inframerah dari
glukosamin dapat dilihat sebagai berikut:
FT-IR Kitin (KBr) : 532 (w), 565 (w), 952 (w), 1024 (m), 1074 (m), 1114 (m), 1157
(m), 1205 (w), 1261 (w), 1314 (m), 1379 (m), 1429 (m), 1559 (m), 1629 (m), 1658
(m), 2890 (m), 2930 (m), 3130 (m), 3254 (m), 3443 (s), 3471 (s) cm-1.
FT-IR Glukosamin HCl (KBr) : 570 (s), 597 (s), 698 (w), 773 (m), 854 (m), 889 (w),
912 (m), 1002 (s), 1034 (s), 1066 (s), 1095 (s), 1137 (s), 1183 (m), 1394 (m), 1421 (s),
1535 (s), 1583 (s), 1614 (s), 2943 (s), 3042 (s), 3105 (s), 3350 (s) cm-1.
Spektrum inframerah dari glukosamin hidroklorida yang diperoleh
menunjukkan deasetilasi apabila bilangan gelombang ~1700 cm-1 untuk C=O, yang
ada dalam spektrum inframerah kitin telah menghilang. Dimana gugus-gugus penting
pada glukosamin hidroklorida adalah O-H, N-H, dan ikatan glikosida.
Menurut Silverstein, R.M. (1986) gugus O-H berada di antara 3500-3200 cm-1
untuk glukosamin 3350 cm-1. Gugus N-H berada di antara 1610-1481 cm-1, untuk
glukosamin 1535 cm-1. Gugus C-N berada diantara 1342-1266 cm-1, untuk glukosamin
1334 cm-1. Dan Ikatan glukosida berada diantara 1150-1085 cm-1,untuk glukosamin
1034 cm-1.