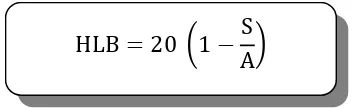Lampiran 3. Perhitungan Nilai HLB Rata-rata 1. Bilangan Penyabunan rata-rata
Bilangan penyabunan = (21,80−21,55) � 0,05 � 56,1 0,1
=
0,701250,1
= 7,0125
Bilangan penyabunan
= (21,75−21,55) � 0,05 � 56,1 0,1
=0,561 0,1
= 5,6100
Bilangan penyabunan
= (21,80−21,55) � 0,05 � 56,1 0,1
=0,70125 0,1
= 7,0125 Bilangan penyabunan Rata-rata = 7,0125 +5,61+7,0125
3 = 6,5450
2. Bilangan Asam rata-rata
Bilangan asam Rata−rata =1,0 x 0,02 x 56,1 0,1
=
1,122
0,1
Lampiran 4.Rangkaian Alat Refluks Lampiran 5. ProsesPenyaringan
Lampiran 6.Titrasi HLBLampiran 7.Serbuk
Karboksimetil selulosa(CMC)
DAFTAR PUSTAKA
Adel, A.M., Abou-Yussef, H., El-gendy A.A., Nada, A.M., (2010),Carboxy-
methylated Cellulose Hydrogel; Sorption Behavior and
Characterization. Cellulose and paper department, National research
centre, Cairo,Egypt.
Angkasa, S. dan Nazaruddin.(1994),Sukun dan Keluwih, Penebar Swadaya,Jakarta.
Atalla, R.H., (1987), Structure of cellulose, Characterization of The Solid States, ACS Symposium series , NO. 340, Washington.
Ashari, S., (2004), Biologi Reproduksi Tanaman Buah-buahan
Komersial,Edisipertama,Bayumedia Publishing, Malang.
Awalludin, A., (2004), Karboksimetilasi Selulosa Bakteri, Skripsi, Fakultas Matematika dan Ilmu Pengetahuan Alam, Bogor : Institut Pertanian Bogor.
Belitz,H.D and W.Grosch., (1987),Food Chemistry,Translation from the second German Edition by D. Hadziyev, Department of Food Science University of Alberta, Canada.
Bird, T., (1993), Kimia Fisika Untuk Universitas. Gramedia. Jakarta
Coffey, D.G., Bell, D.A., and Handerson, A., (1995), Cellulose and Cellulose
Derivate, New York.
Djaeni, M.A. Prasetyaningrum., (2010), Kelayakan Biji Durian Sebagai Bahan
Pangan Alternatif : Aspek Nutrisi Dan Tekno Ekonomi, Vol. 4,
Semarang.
Eliasson, A.C.,( 2004),Starch in Food. Structure, Function and Application, Woodhead Publishing Limited, England.
Hardjono, S. (1995), Kimia kayu dasar-dasar dan penggunaannya, Edisi kedua, Yogyakarta: Gajah Mada University Press.
Hart, H., Craine, L.E., and Hart, D.J., (2003), Kimia Organik.Edisi Kesebelas, Jakarta : Erlangga.
Haygreen, J.G & Bowyer, J.L (2007), hasil Hutan dan Hasil Kayu. UGM.Press : Yogyakarta.
Herman, T.F., (2009), Pengaruh Tingkat Pencampuran Terung Pyrus
(Cyphomandra betacea Sendt) dan Rumput Laut Dalam Pembuatan Selai Lembaran, Skripsi, Teknologi Hasil Pertanian, Fakultas
Teknologi Pertanian, Universitas Andalas, Padang.
Heydarzadeh H.D ,Najafpour G.D ,Nazari Moghaddam A.A (2009), Catalyst-
Free Conversion of Alkali Cellulose to Fine Carboxymethyl Cellulose at Mild Conditions.World apllied science journal (6). IDOSI
publication
Hong, K. M. (2013).,Preparation and Characterization of Carboxymethyl
Cellulose from Sugarcane Bagasse. (S). Departement of Cemical
Science. Faculty of Science. Universiti Tunku Abdul Rahman. Malaysia.
Klemm, D. (1998).,Fundamentals and Analytical Methods. Volume 1. New York : Wiley-VCH
Krasigg, H.A., (1993).,Cellulose Structure accessibility and reactivity, Gordon and breach science publisher,Yverdon, switzerland, Vol. 11.
Lehninger, A.L., (1988), Dasar-Dasar Biokimia, Jilid 1, Erlangga, Jakarta. Latif, A., Anwar, T., and Noor, S., (2007).,Two step synthesis and charactrization
of carboxymethylcellulose rayon grade wood and cotton linter. Pcsir
laboratories complex,material science centre, Pakistan.
Manahan, S.E., (1994), Environmental Chemistry, Sixth Edition, London, Lewis Publisher.
Martin, A.N., (1960), Physical Pharmacy. Philadelphia : lea & Febiger.
Menifie, B.W., (1989), Choclate,Cocoa,And Confectionery Science And
Technology, Third Edition, An Aspen Publication, United states Of
America.
Moore, G.K dan Roberts, G.A.F. (1980).Determination of The Degree of
Najafpour,G.D., (2009), Catalys free Convertion of Alkali Cellulose fine
Carboxymethyl Cellulose at Mild Conditions. World Applied Sciences
Journal.6.
Nisa, D, (2014), Pemanfaatan Selulosa dari Kulit Buah Kakao (Teobroma cacao
L) sebagai bahan baku pembuatan CMC (carboxymethyl Cellulose),
Malang : Universitas Brawijaya.
Phillips, G.O and P.A. Williams., (1987),Handbook of
Hydrocolloids,WoodheadPublishing Limited, Cambridge England.
Poedjiadi, A., (2006), Dasar-Dasar Biokimia, Jakarta : Universitas Indonesia. Rukmana, R. (1996). Durian Budidaya Pasca Panen.Yogyakarta: Penerbit
Kanisius.
Sastrohamidjojo, H., (1995), Kimia Organik Stereo Kimia, Karbohidrat, Lemak
dan Protein,Yogyakarta, Gajah Mada University Press.
Saxena, I.M., and Brown, R.M.Jr., (1995), Identification of a second cellulose
synthase gene (acsAll) in Acetobacter xylinum, Journal of Bacteorology.
Setiadi,. (2007), Bertanam Durian, Jakarta : Penebar Swadaya
Setiyawan, Y., (2010), Peranan Polimer Selulosa Sebagai Bahan Baku dalam
Pengembangan Produk Manufaktur Menuju Era Globalisasi. Bandung
: Universitas Islam Indonesia.
Sjostrom, E., (1995), Kimia Kayu, Edisi 2.Gajah Mada University Press.Yogyakarta.
Smook, G.A., (1982), Hand Book For Pulp And Pare Technologist. Boston : Miller Freeman, Inc.
Wijayani, A., Ummah, K., dan Siti Tjahjani.( 2005). Karakteristik Karboksimetil
Selulosa (CMC) dari Enceng Gondok (Eichorniacrassipes (Mart) Solms).Universitas Negeri Surabaya.Indo.J. Chem., 2005, 5 (3), 228 –
Winarno, F.G., (1984),Kimia Pangan dan Gizi. Gramedia Pustaka Utama, Jakarta. Wulandari, G.R.., (2014), Sintesis O-karboksimetil N-lauril kitosan melalui
eterifikasi kitosan dengan asam monokloroasetat dan diikuti asilasi dengan lauril klorida, Universitas sumatera utara, Medan.
BAB 3
METODE PENELITIAN
3.1 Alat-alat
Peralatan yang digunakan dalam penelitian ini meliputi:
- Labu leher tiga 500 ml Durrant
- Hot plate - Statif dan klem - Kondensor
- Corong pisah Durrant
- Penangas air
- Termometer 1000C
- Neraca analitis
- Beaker glass 4000 ml Pyrex
- Gelas ukur 100 ml
- Spatula
- Indikator Universal
- Oven Fisher Scientific
- Labu takar 100 ml Pyrex
- Fourier transform infra red (FT-IR) - Kaca arloji
3.2 Bahan-Bahan
5. Kulit Buah Durian
6. NaOH (pellet) p.a E.Merck
7. Isopropanol (l) p.a Fisons
8. CH3COOH (glacial) p.a Emsure
9. H2O2 (l) 30% Teknis
10. Monokloroasetat
E.Merck
11. Etanol 96% Teknis
E.Merck
3.3 Prosedur Penelitian
3.3.1Penyediaan Sampel
Bahan yang digunakan dalam penelitian adalah kulit buah durian yang diperoleh dari pinggir jalan.Kemudian dipotong-potong sedemikian rupa lalu dijemur dibawah sinar matahari, kemudian diblender hingga menjadi serbuk.
3.3.2 Pembuatan Reagen
3.3.2.1 Pembuatan Larutan NaOH 2 %
Ditimbang NaOH pellet sebanyak 2 gram dan dilarutkan dengan aquadest dalam 100 ml labu takar.
3.3.2.2 Pembuatan Larutan NaOH 30 %
Ditimbang NaOH pellet sebanyak 30 gram dan dilarutkan dengan aquadest dalam 100 ml labu takar.
3.3.2.3 Pembuatan Larutan H2O2 10 %
3.3.2.4 Pembuatan Larutan Etanol 90%
Diukur sebanyak 93,75 ml Etanol 96 % kemudian ditambahkan aquadest dalam labu takar 100 ml.
3.3.2.5 Pembuatan Larutan HCl 0,05 N
Diukur sebanyak 0,68 ml HCl 18,35 N kemudian ditambahkan aquadest dalam labu takar 250 ml.
3.3.2.6 Pembuatan Larutan KOH 0,02 N
Ditimbang KOH pellet sebanyak 0,28 gram kemudian dilarutkan dengan aquadest dalam labu takar 250 ml.
3.3.3 Isolasi Selulosa dari Kulit Buah Duriandengan Metode pemanasan
500 gram serbuk kulit durian direndam dengan NaOH 2% sebanyak 1L dalam beaker glass 4000 ml. Dipanaskan selama 1 jam dengan suhu 800C kemudian dicuci residu hingga netral (pH= 7) dengan menggunakan aquadest. Kemudian residu ditambahkan dengan H2O2 10% sebanyak 500 mldan dipanaskan selama 10 menit lalu didiamkan selama 1 malam. Selanjutnya disaring dan residu dikeringkan dalam oven pada suhu 750C selama 3 jam, ditimbang kemudian diuji secara kualitatif dengan pereaksi fehling Aditambah fehling B dan diikuti uji FT-IR (Fouriertransform infrared spectroscopy).
3.3.4 Proses Alkalisasi dan Karboksimetilasi
glasial.Kemudian disaring lalu dicuci dengan etanol 90 % kemudian dikeringkan dalam oven dengan suhu 500C.
3.3.5 Prosedur AnalisisHasil Karboksimetilasi Selulosa 3.3.5.1 Derajat Substitusi (DS)
Derajat substitusi dapat dievaluasi dengan metode FT-IR dari perbandigan absorbansi pada 1573,91(dianggap berasal dari pita karbonil) dan absorbansi 3425,58 (berasal dari pita hidroksil), dihitung dengan meggunakan persamaan2.1perhitungan Derajat Substitusi.
3.3.5.2 Viskositas
Untuk menentukan Viskositas dari CMC terlebih dahulu dilarutkan dengan aquadest kemudian dimasukkan larutan kedalam alat viskosimeter ostwald (10 ml).
Adapun tahapannya sebagai berikut :
Untuk aquadest :
l0 ml aquadest dimasukkan kedalam alat viskosimeter Ostwald kemudian dihisap larutan dengan bola karet sampai garis tanda atas ,dihentikan hisapan kemudian diukur waktu aquadest untuk turun dari batas atas sampai batas bawah dengan stopwatch dan diulangi sebanyak 3 kali.
Untuk CMC :
diukur waktu larutan turun dari batas atas sampai batas bawah dengan stopwatch. Diulangi sebanyak 3 kali dan dilakukan hal yang sama untuk CMC 0,02 gram; 0,03 gram; 0,04 gram; 0,05 gram.
3.3.5.3 Penentuan Harga HLB
Analisis ini dilakukan terhadap Karboksimetil selulosa (CMC).Sebelum harga HLB ditentukan, terlebih dahulu ditentukan bilangan penyabunan dan bilangan asam.
3.3.5.3.1 Analisis Bilangan Penyabunan (S)
Ditimbang sampel sebanyak 0,1 gram dan dimasukkan kedalam Erlenmeyer. kemudian ditambahkan 25 ml larutan KOH-alkohol 0,5 N dan dipanaskan hingga mendidih. kemudian didinginkan dan ditambahkan 3 tetes indikator fenolftalein (pp) kemudian dititrasi dengan larutan HCl 0,05 N hingga warna merah muda hilang. dilakukan titrasi terhadap larutan blanko pada kondisi yang sama. Dicatat volume HCl 0,05 N yang terpakai dan dihitung bilangan penyabunan dengan menggunakan persamaan 2.2 penentuan bilangan penyabunan sebagai berikut ;
Persamaan 2.3 Penentuan bilangan penyabunan
3.3.5.3.2 Analisis Bilangan Asam (A)
Ditimbang sampel 0,1 gram dan dimasukkan kedalam Erlenmeyer. kemudian ditambahkan 10 ml larutan etanol netral. Erlenmeyer tersebut ditutup dengan
terpakai dan dihitung bilangan asam dengan menggunakan persamaan 2.3penentuan bilangan asam sebagai berikut ;
Persamaan 2.4 Penentuan bilangan asam
Setelah bilangan asam dan bilangan penyabunan telah ditentukan,maka dapat ditentukan harga HLB (Hidrofi-lifofil balancel) dengan menggunakan rumus persamaan 2.2 sebagai berikut ;
Persamaan 2.2 Penentuan HLB
Dimana : S = Bilangan penyabunan A = Bilangan asam
3.3.5.4 Analisis Spektrofotometer FT-IR
Untuk masing-masing cuplikan selulosa dan karboksimetil selulosa (CMC) berwujud padat dioleskan pada plat KBr hingga terbentuk lapisan tipis yang transparan dan diukur spektrumnya dengan alat Spektrofotometer FT-IR model Shimadzu.
Bilangan asam = VKOH x NKOH x 56,1 massa sampel (gram)
3.4 Bagan Penelitian
3.4.1 Isolasi Selulosa dari Kulit Durian
dimasukkan kedalam beaker glass 4000 ml
ditambahkan 1 liter larutan NaOH 2%
dipanaskan pada suhu 800C selama 4 jamsambil diaduk diatas hotplate
disaring
dicuci hingga netral (pH = 7)
dibleaching dengan H2O2 10 % sebanyak 500 ml dipanaskan pada suhu 600C selama 15 menit sambil diaduk diatas hotplate
dibiarkan selama 1 malam
dikeringkan pada suhu 750C dalam oven selama 4 jam
analisa FT-IR uji kualitatif
500 gram serbuk kulit durian
Filtrat Residu
Hasil
3.4.2 Uji Kualitatif Selulosa
Ditambahkan 1 ml Fehling A
Ditambahkan 1 ml Fehling B
Dimasukkan kedalam tabung reaksi yang mengandungselulosa sebanyak 1 gram
Dipanaskan hingga terjadi perubahan warna 1 gram
S l l
3.4.3 Proses Alkalisasi Dan Karboksimetilasi
dimasukkan kedalam labu leher tiga
ditambahkan 30 ml isopropanol dan 30 ml NaOH 30 % dipanaskan pada suhu 600 C selama 1 jam
ditambahkan 40 ml isopropanol yang mengandung gram monokloroasetat melalui corong penetes selama 1 jam diaduk selama 4 jam pada suhu 600 C
dinetralkan dengan asam asetat glasial disaring
dicuci dengan etanol 90 % dikeringkan pada suhu 500C
4 gram selulosa kulit durian
Residu Filtrat
Hasil analisa
FT-IR
Derajat Substitusi
(DS)
Viskositas analisis HLB
BAB 4
HASIL DAN PEMBAHASAN
4.1 Hasil
Selulosa yang digunakan dalam penelitian ini adalah berasal dari kulit buah durian. Dari 500 gram serbuk kulit buah durian yang diisolasi diperoleh selulosa kulit buah durian sebanyak 463,78 gram (92,756 %).
Karboksimetil selulosa yang diperoleh dari 4 gram selulosa kulit buah durian yang direaksikan dengan asam monokloroasetat (MCA) diperoleh sebanyak 4,725 gram.
4.1.1 Analisis Spektrofotometer FT-IR Selulosa
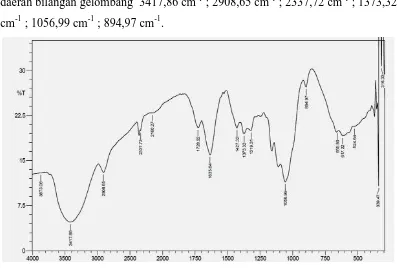
Dari data spektroskopi FT-IR selulosa memberikan puncak-puncak vibrasi pada daerah bilangan gelombang 3417,86 cm-1 ; 2908,65 cm-1 ; 2337,72 cm-1 ; 1373,32 cm-1 ; 1056,99 cm-1 ; 894,97 cm-1.
4.1.2 Analisis Spektrofotometer FT-IR CMC
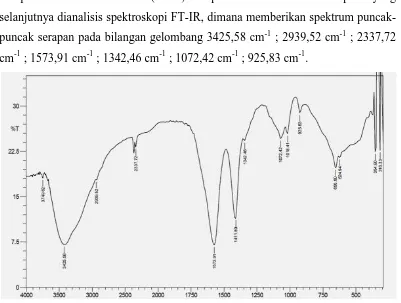
Karboksimetil selulosa (CMC) merupakan hasil reaksi antara selulosa yang sudah dialkalisasi terlebih dahulu dengan NaOH sehingga suasananya menjadi alkali yang kemudian direaksikan dengan asam monokloroasetat yang dilarutkan terlebih dahulu dengan isopropanol dengan pemanasan 600C selama 4 jam.Kemudian dicuci dengan alkohol 90% lalu dikeringkan. Hasil yang diperoleh berupa karboksimetil selulosa (CMC) berupa serbuk halus berwaran putih yang selanjutnya dianalisis spektroskopi FT-IR, dimana memberikan spektrum puncak-puncak serapan pada bilangan gelombang 3425,58 cm-1 ; 2939,52 cm-1 ; 2337,72 cm-1 ; 1573,91 cm-1 ; 1342,46 cm-1 ; 1072,42 cm-1 ; 925,83 cm-1.
4.1.3 Harga HLB
Harga HLB (Hydrophylic Lyphopylic Balance) dari karboksimetil selulosa dilakukan dengan cara menghitung bilangan penyabunan dan bilangan asamnya terlebih dahulu dengan metode titrasi. Data dan perhitungannya dapat dilihat sebagai berikut (Lampiran C):
Tabel 4.1. Data Penentuan Bilangan Penyabunan
Sampel Massa sampel (gram) Volume titrasi (ml) Bilangan penyabunan Bilangan penyabunan rata-rata Blanko
- 21,80 -
-
- 21,75 -
- 21,75 -
CMC
0,104 21,55 7,0125
6,545
0,104 21,55 5,61
0,102 21,50 7,0125
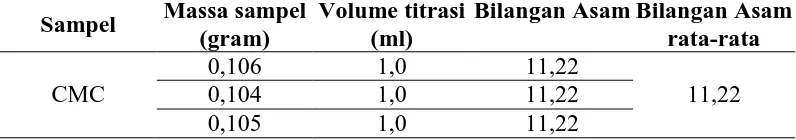
Tabel 4.2. Data Penentuan Bilangan Asam
Sampel Massa sampel (gram)
Volume titrasi (ml)
Bilangan Asam Bilangan Asam rata-rata
CMC
0,106 1,0 11,22
11,22
0,104 1,0 11,22
0,105 1,0 11,22
4.1.4 Penentuan Derajat Substitusi
Penentuan derajat substitusi dari CMC yang dihasilkan berdasarkan analisis spektrum FT-IR. Nilai intensitas %T pada bilangan gelombang 1573,91 cm-1 dan 3425,58 cm-1 masing-masing adalah 6,97 dan 7,03 yang dapat dilihat pada Lampiran B.
Perhitungan nilai derajat substitusinya dapat dihitung berdasarkan persamaan 2.1penentuan derajat substitusi dibawah ini :
Adsorbansi pada bilangan gelombang 1573,91 cm-1 (A1573,91) %T = 6,97
T = 0,0697
�1573 ,91 = ���
1 �= ���
1
0,0697 = 1,1567
Adsorbansi pada bilangan gelombang 3425,58 cm-1(A3425,58) %T = 7,03
T = 0,0703
�3425 ,58 = ���
1 � =���
1
0,0703= 1,1530
�� (%) = ��1,1567
1,1530� − 0,10� � 100
= (1,003-0,10) X 100 �� (%) =���1573
�3425� −
4.1.5 Viskositas
Pengujian Viskositas CMC
Penentuan viskositas berdasarkan viskositas ostwald menggunakan alat viskosimeter (Sibata), maka diperoleh data sebagai berikut : ( Tabel 4.3)
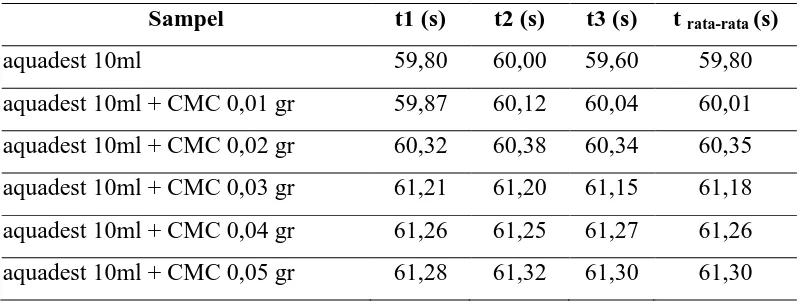
Tabel 4.3. Data Viskositas CMC
Sampel t1 (s) t2 (s) t3 (s) t rata-rata (s)
aquadest 10ml 59,80 60,00 59,60 59,80
aquadest 10ml + CMC 0,01 gr 59,87 60,12 60,04 60,01 aquadest 10ml + CMC 0,02 gr 60,32 60,38 60,34 60,35 aquadest 10ml + CMC 0,03 gr 61,21 61,20 61,15 61,18 aquadest 10ml + CMC 0,04 gr 61,26 61,25 61,27 61,26 aquadest 10ml + CMC 0,05 gr 61,28 61,32 61,30 61,30
4.2 Pembahasan
4.2.1 Isolasi Selulosa
Pemanasan pada suhu 800 C bertujuan dimana pada tahap ini dapat mempenetrasi NaOH kedalam struktur selulosa.Langkah ini disebut alkali selulosa yang mana nantinya memberikan sifat reaktif ketika bereaksi dengan asam monokloroasetat ataupun NaOCl yang mana nantinya diikuti dengan reaksi eterifikasi.reaksi antara alkali selulosa dengan eterifikasi normalnya terjadi pada rentan suhu 50-70 0C (Krasigg, 1993)
4.2.2 Pembuatan Karboksimetil Selulosa
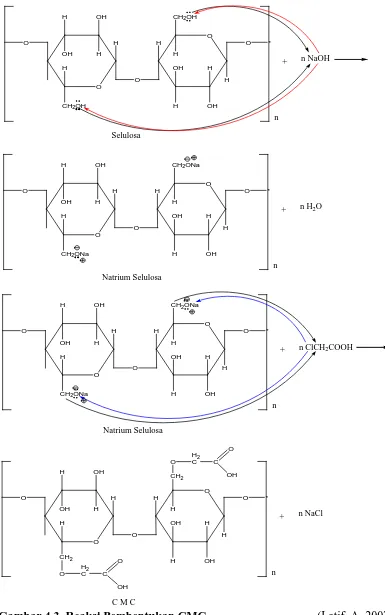
Karboksimetil selulosa merupakan hasil reaksi antara selulosa alkalisasi dengan asam monokloroasetat dengan melarutkan asam monokloroasetat terlebih dahulu dengan isopropanol membentuk karboksimetil selulosa dan garamnya.Kemudian dicuci dengan asam asetat dan dilanjutkan dengan mencucinya dengan alkohol 90% dan kemudian dikeringkan. Terbentuknya karboksimetil selulosa ditandai dengan munculnya bilangan gelombang 1573,91 cm-1 merupakan gugus karbonil (C=O) dari asam monokloroasetat serta didukung oleh puncak serapan pada bilangan gelombang 1072,42 cm-1 merupakan vibrasi dari gugus C-O-C dan didukung dengan munculnya serapan pada daerah bilangan gelombang 3425,58 cm-1 yang merupakan vibrasi OH streching dari selulosa dan puncak serapan pada daerah bilangan gelombang 2939,52 cm-1 menunjukkan vibrasi streching dari C-H sp3 yang didukung oleh puncak serapan pada bilangan gelombang 1342,46 cm-1 yang merupakan vibrasi bending C-H. serta munculnya bilangan gelombang 2337,72 cm-1 merupakan vibrasi C-Cstreching dan didukung dengan bilangan gelombang 925,83 cm-1 yang merupakan C-Cbending.
O H
OH H
CH2OH OH
H
O H
O
O CH2OH
H OH
H OH
H H
H O *
n
+ n NaOH
O H
OH H
CH2ONa OH
H
O H
O
O CH2ONa
H OH
H OH
H H
H O *
n
+ n H2O
O H
OH H
CH2ONa OH
H
O H
O
O CH2ONa
H OH
H OH
H H
H O *
n
+ n ClCH2COOH
O H OH H CH2 OH H O H O O CH2 H OH H OH H H
H O *
n
+ n NaCl
O HC2 C O OH O H2 C C O OH Selulosa Natrium Selulosa Natrium Selulosa
C M C
Gambar 4.3. Reaksi Pembentukan CMC (Latif, A. 2007)
4.2.3 Penentuan HLB
Harga HLB (Hidrofil-lifofil balance) dari karboksimetil selulosa dapat dihitung berdasarkan persamaan 2.2berikut :
dimana : S = Bilangan penyabunan A = Bilangan asam
Dari hasil perhitungan nilai bilangan asam dan bilangan penyabunan (Lampiran C) maka diperoleh nilai HLB dari senyawa karboksimetil selulosa (CMC) :
HLB = 20 �1−6,545
11,22� = 8,34
Berdasarkan Skala rentang nilai HLB untuk bebrapa zat permukaan aktif sebesar 8,34w/o, maka CMC yang diperoleh dapat dinyatakan sebagai zat penyebar dan pembasah.
4.2.4 Derajat Substitusi
Derajat substitusi sebesar 90,3 % menunjukkan bahwa hanya 90,3 % asam monokloroasetat tersubstitusi kegugus H yang terikat pada CH2OH sedangkan selebihnya 9,7 % tidak bereaksi.
4.2.5 Viskositas
Dari data diatas (Tabel 4.3) dapat dilihat untuk waktu rata-rata alir diperoleh HLB = 20 �1−S
A�
δ
δ
δ δ δ
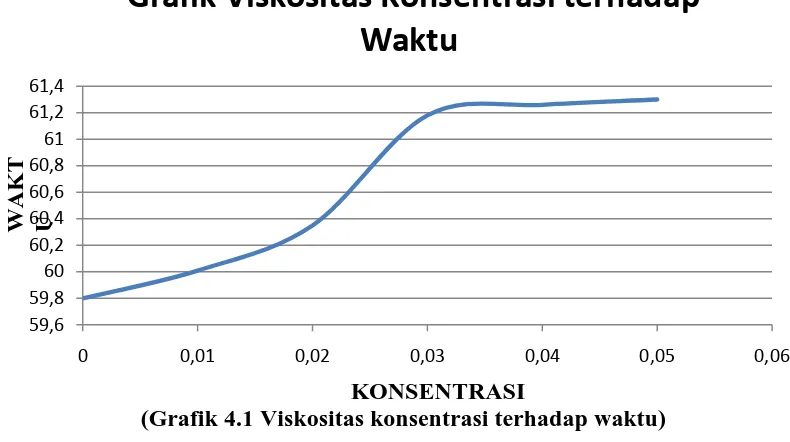
(Grafik 4.1 Viskositas konsentrasi terhadap waktu)
Dari data diatas terbukti viskositas dari CMC semakin meningkat dengan penambahan konsentrasi CMC yang semakin besar.
59,6 59,8 60 60,2 60,4 60,6 60,8 61 61,2 61,4
0 0,01 0,02 0,03 0,04 0,05 0,06
Grafik Viskositas Konsentrasi terhadap
Waktu
KONSENTRASI
WA
K
T
BAB 5
KESIMPULAN DAN SARAN
5.1. Kesimpulan
1. Dari penelitian yang dilakukan, maka diperoleh hasil sebagai berikut ;
• Dari 500 gram kulit buah Durian yang diisolasi diperoleh selulosa kulit buah durian sebanyak 463,78 gram (92,756 %).
• Dari 4 gram selulosa kulit Durian yang direaksikan dengan asam monokloroasetat diperoleh CMC sebanyak 4,725 gram
• Nilai HLB (hidrofil-lifofil balance) dari karboksimetil selulosa (CMC) yang diperoleh adalah 8,34. Berdasarkan skalarentan nilai HLB, CMC yang diperoleh dapat dinyatakan sebagai surfaktan.
• Pada penentuan Viskositas, CMC yang dilarutkan pada aquades tidak larut sempurna. Hal ini dikarenakan asam monokloroasetat tidak tersubstitusi sempurna terhadap selulosa dari kulit buah durian. Berdasarkan penentuan derajat substitusi (DS) nilai yang diperoleh sebesar 90,3% yang mana berarti hanya 90,3% saja asam monoloroasetat yang tersubstitusi ke dalam selulosa selebihnya 9,7% merupakan selulosa murni yang tidak bereaksi.
2. Karakteristik Karboksimetil selulosa (CMC) yang diperoleh berbentuk serbuk putih, tidak berbau.
5.2. Saran
BAB 2
TINJAUAN PUSTAKA
2.1 Buah Durian (Durio zibethinus Murr)
Tanaman durian diduga berasal dari kawasan Asia Tenggara terutama Indonesia, Thailand, dan Malaysia.Sementara itu, di Indonesia, terutama dipulau Sumatera dan pulau Kalimantan masih terdapat beberapa jenis durian liar.Agrobisnis durian ditanah air sudah dimulai beberapa tahun yang lalu, misalnya didaerah Bogor.Disana, tanaman durian sudah diperkebunkan dengan perawatan yang cukup intensif (Ashari, 2004).
Buah durianmerupakan tanaman daerah tropis, karenanya dapattumbuhbaik di Indonesia.Panjang buah durian yang matang bisa mencapai30-45 cmdengan lebar 20-25 cm, dan beratantara1,5-2,5 kg.Setiap buah berisi 5 juringyang di dalamnya terletak 1-5 biji yang diselimuti daging buah yang berwarnaputih, krem, kuning, atau kuning tua.Tiap varietas durianmenentukan besarkecilnya ukuran buah, rasa, tekstur, dan ketebalan daging(Angkasa ,S Dan Nazaruddin, 1994).Dalam sistematika (taksonomi) tumbuhan, tanaman durian diklasifikasikan sebagai berikut :
Kingdom : Plantae (tumbuh-tumbuhan) Divisi : Spermatophyta (tumbuhan berbiji) Sub-divisi : Angiospermae (berbiji tertutup) Kelas : Dicotyledonae (biji berkeping dua) Ordo : Bombacales
Famili : Bombacacaeae Genus : Durio
Gambar 2.1.Kulit Durian yang digunakan dalam penelitian.
Tanaman durian ( Durio zibethinus Murr ), merupakan salah satu jenis buah-buahan yang produksinya melimpah. Buah durian disebut juga The King of Fruit sangat digemari oleh berbagai kalangan masyarakat karena rasanya yang khas. Bagian buah yang dapat dimakan (persentase bobot daging buah) tergolong rendah yaitu hanya 20,52%. Hal ini berarti ada sekitar 79,08% yang merupakan bagian yang tidak termanfaatkan untuk dikonsumsi seperti kulit dan biji durian (Setiadi, 2007 ).
2.2 Selulosa
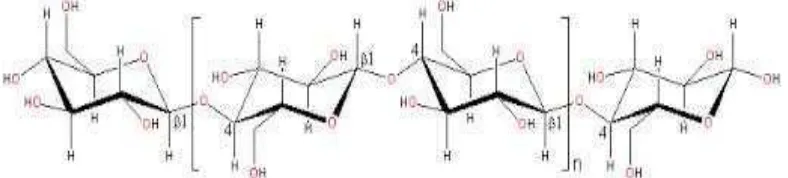
Selulosa adalah polimer glukosa yang berbentuk rantai linier dan dihubungkan
oleh ikatan β-1,4 glikosidik. Struktur yang linier menyebabkan selulosa bersifat kristalin dan tidak mudah larut.Selulosa tidak mudah didegradasi secara kimia maupun mekanis(Holtzapple et.al 2003).
Selulosa tidak pernah ditemukan dalam keadaan murni di alam, tetapi selalu berasosiasi dengan polisakarida lain seperti lignin, pectin, hemiselulosa, dan xilan (Goyskor dan Eriksen 1980 dalam Fitriani 2003).
Kebanyakan selulosa berasosiasi dengan lignin sehingga sering disebut sebagai lignoselulosa. Selulosa, hemiselulosa dan lignin dihasilkan dari proses fotosintesis. Di dalam tumbuhan molekul selulosa tersusun dalam bentuk fibril yang terdiri atas beberapa molekul paralel yang dihubungkan oleh ikatan glikosidik sehingga sulit diuraikan (Goyskor dan Eriksen 1980 dalam Fitriani 2003).Komponen-komponen tersebut dapat diuraikan oleh aktifitas mikroorganisme.Beberapa mikroorganisme mampu menghidrolisis selulosa untuk digunakan sebagai sumber energi, seperti bakteri dan fungi (Sukumaran et.al 2005).
Selulosa adalah komponen utama dari kayu dan merupakan polisakarida linier dengan rantai yang cukup panjang yang terdiri dari glukosa-glukosa yang kemudian berhubungan satu sama lain (Fegel. D. Dan Wegner. G. 1995)
Selulosa dibuat langsung dari unit-unit glukosa. Sebagai langkah pertama dalam proses tersebut, pohon mengangkut glukosa ke pusat-pusat pengolahan yang terletak pada pucuk-pucuk cabang dan akar (meristem ujung) dan ke lapisan kambium yang menyelubungi batang utama, cabang dan akar. Kemudian dalam suatu proses yang kompleks, glukosa mengalami modifikasi secara kimia dengan dipindahkannya satumolekul air dari setiap unit dan terbentuklah suatu anhidrid glukosa: C6H12O6 (glukosa) –H2O = C6H12O5 (anhidrid glukosa). Unit-unit anhidrid glukosa kemudian salingbersambungan ujung-ujungnya membentuk polimer berantai panjang yaitu selulosa(C6H12O5)n(derajat polimerisasi) sama dengan 500-10000(Haygreen. J. G. dan Bowyer.J. L. 2007).
Rantai selulosa terdiri dari satuan glukosa anhidrida yang saling berikatan melalui atom karbon pertama dan ke empat. Ikatan yang terjadi adalah ikatan ß- 1,4-glikosidik. Secara alamiah molekul-molekul selulosa tersusun dalam bentuk fibril-fibril yang terdiri dari beberapa molekul selulosa yang dihubungkan dengan ikatan glikosidik. Fibril-fibril ini membentuk struktur kristal yang dibungkus oleh lignin. Komposisi kimia dan struktur yang demikian membuat kebanyakan bahan yang mengandung selulosa bersifat kuat dan keras.Sifat kuat dan keras yang dimiliki oleh sebagian besar bahan berselulosa membuat bahan tersebut tahan terhadap peruraian secara enzimatik.Secara alamiah peruraian selulosa berlangsung sangat lambat (Fan et al., 1982).
Selulosa adalah senyawa seperti serabut, liat, tidak larut dalam air dan ditemukan didalam dinding sel pelindung tumbuhan, terutama pada tangkai, batang, dahan dan semua bagian berkayu dari jaringan tumbuhan. Kayu terutama mengandung selulosa dan senyawa polimer lain. Selulosa tidak hanya merupakan polisakarida struktural ekstrasellular yang paling banyak dijumpai pada dunia tumbuhan, tetapi juga merupakan senyawa yang paling banyak diantara semua biomolekul pada tumbuhan atau hewan. Karena selulosa merupakan homopolisakarida linear tidak bercabang, terdiri dari 10.000 atau lebih unit D-glukosa yang dihubungkan oleh ikatan 1 4 glikosida senyawa ini akan kelihatan seperti amilosa, dan rantai utama glikogen (Lehninger, A.L., 1988).
Selulosa merupakan salah satu jenis polisakarida yang tersusun dari molekul glukosa dalam bentuk rantai panjang tidak bercabang yang mirip dengan amilosa. Bagaimanapun, unit-unit dari glukosa dalam selulosa terikat pada ikatan
Gambar 2.2.Struktur Selulosa(dalam Setiyawan, 2010).
Selulosa adalah suatu polisakarida yang juga disusun dari unit-unit C6H10O5.Molekul-molekul dari selulosa besar, dengan berat molekul sekitar 40.000. Struktur selulosa sama dengan pati. Selulosa dihasilkan oleh tanaman dalam bentuk struktural bahan ini adalah dari dinding sel tanaman. Kayu mengandung kira-kira 60 % selulosa dan kapas mengandung lebih dari 90 % bahan ini.Serat-serat selulosa diekstrak dari kayu dan dicetak bersamaan untuk membuat kertas.
Manusia dan kebanyakan hewan tidak dapat mencerna selulosa karena kekurangan enzim yang dibutuhkan untuk menghidrolisa ikatan-ikatan oksigen diantara molekul-molekul glukosa. Hewan pemamah biak (lembu, domba, kambing dan rusa) mempunyai bakteri dalam perut mereka yang dapat memecah selulosa menjadi produk yang dapat digunakan oleh hewan (Stanley, 1994 ).
Molekul-molekul selulosa seluruhnya berbentuk linier dan mempunyai kecenderungan kuat membentuk ikatan-ikatan hidrogen intra dan intermolekul.Jadi berkas-berkas selulosa membentuk agregat dalam bentuk mikrofibril, dimana daerah kristalin diselingi dengan daerah amorf.Mikrofibril membentuk fibril-fibril dan akhirnya serat-serat selulosa.Sebagai akibat dari struktur yang berserat dan ikatan hidrogen yang kuat, selulosa mempunyai kekuatan tarik yang tinggi dan tidak larut dalam kebanyakan pelarut (Atalla, 1987).
Selulosa pada daun, pembuluh xylem dan floem akan terletak berdampingan dan jaringannya tersusun pada tulang daun. Meskipun susunan jala yang tampak pada daun, kedua jarigan ini akan disatukan dalam berkas-berkas yang direkatkan oleh pecktin dan selulosa. Selulosa pada hewan tingkat rendah terdapat didalam organisme primitif, seperti rumput laut, flagelata, dan bakteri, misalnya pada bakteri Acetobacter xylinum.Nata de coco merupakan sumberselulosa yang diproduksi sebagai hasil proses fermentasi dalam substrat air kelapa dengan menggunakan bakteri Acetobacter xylinum. Kelebihan selulosa yang dihasilkan dari nata de coco adalah tidak bercampur dengan lignin dan hemiselulosa (Saxena, 1995).
Selulosa merupakan biopolimer yang berlimpah dialam yang bersifat dapat diperbaharui, mudah terurai, tidak beracun, dan juga merupakan polimer
karbohidrat yang tersusun atas β-D glukopiranosa dan terdiri dari tiga gugus hidroksi per anhidro glukosa menjadikan selulosa memiliki derajat fungsionalitas yang tinggi. Sebagai materi yang diperbaharui, selulosa dan turunannya dapat dipelajari dengan baik (Coffey et al, 1995).
Setiap unit β-D-glikopiranosa didalam rantai selulosa mempunyai tiga gugus hidroksil reaktif, dua sekunder 2 dan HO-3) dan satu primer (HO-6).Untuk eterifikasi, gugus hidroksil sekunder (HO-2) biasanya paling mudah bereterifikasi sedangkan untuk esterifikasi, gugus hidroksil primer (HO-6) memiliki reaktifitas yang lebih tinggi.
Walaupun manusia dan hewan lain dapat mencerna pati dan glikogen, mereka tidak dapat mencerna selulosa. Ini merupakan contoh yang baik mengenai spesifisitas reaksi biokimiawi.Satu-satunya perbedaan kimia antara pati dan selulosa ialah stereokimia tautan glikosidik tepatnya stereokimia pada C-1 dari setiap unit glukosa. Sistem pencernaan manusia mengandung enzim yang dapat mengkatalisis hidrolisis ikatan α-glikosidik (Hart,H., dkk., 2003).
Berdasarkan derajat polimerisasi dan kelarutan dalam senyawa natrium hidroksida (NaOH) 17,5%, selulosa dapat dibedakan atas tiga jenis yaitu :
1. Selulosa α (Alpha Cellulose) adalah selulosa berantai panjang, tidak larut
dalam larutan NaOH 17,5% atau larutan basa kuat dengan derajat polimerisasi 600 - 1500. Selulosa α dipakai sebagai penduga dan atau penentu tingkat
kemurnian selulosa. Selulosa α merupakan kualitas selulosa yang paling tinggi (murni). Selulosa α > 92% memenuhi syarat untuk digunakan sebagai bahan baku utama pembuatan propelan dan atau bahan peledak, sedangkan selulosa kualitas dibawahnya digunakan sebagai bahan baku pada industri kertas dan industri sandang/kain. Semakin tinggi kadar alfa selulosa, maka semakin baik mutu bahannya (Nuringtyas 2010).
2. Selulosa β (Betha Cellulose) adalah selulosa berantai pendek, larut dalam
larutan NaOH 17,5% atau basa kuat dengan derajat polimerisasi 15 - 90, dapat mengendap bila dinetralkan.
3. Selulosa γ (Gamma cellulose) adalah sama dengan selulosa β, tetapi derajat
polimerisasinya kurang dari 15.
Bervariasinya struktur kimia selulosa (α, β, γ) mempunyai pengaruh yang
Rantai-rantai selulosa akan bergabung menjadi satu kesatuan membentuk mikrofibril, bagian kristalin akan bergabung dengan bagian nonkristalin. Mikrofibril-mikrofibril akan bergabung membentuk fibril, selanjutnya gabungan fibril akan membentuk serat (Klemm 1998).
2.2.1 Lignin
Kebanyakan selulosa berasosiasi dengan lignin sehingga sering disebut sebagai lignoselulosa. Pada saat yang sama, komponen-komponen utama penyusun tanaman ini diuraikan oleh aktivitas mikroorganisme. Beberapa mikroorganisme mampu menghidrolisis selulosa untuk digunakan sebagai sumber energi, seperti bakteri dan kapang (Enary, 1983).
Lignin adalah suatu polimer yang kompleks dengan berat molekul tinggi, tersusun atasunit-unit fenilpropan.Meskipun tersusun atas karbon, hidrogen, dan oksigen, ligninbukanlah suatu karbohidrat suatu karbohidrat dan bukan tidak ada hubungannyadengan golongan senyawa tersebut.Sebaliknya lignin pada dasarnya adalah suatufenol.lignin sangat stabil dan sukar dipisahkan dan mempunyai bentuk yangbermacam-macam karena susunan lignin yang pasti didalam kayu tetap tidakmenentu.
(bersama-samadengan karbohidrat-karbohidrat tertentu) lama-kelamaan lignin cenderungmenjadi kuning, karenanya kertas koran yang terbuat dari serat-serat yang diperolehsecara mekanis dengan lignin yang belum dipisahkan, tidak berumur panjang karenakecenderungannya untuk menjadi kuning, kertas koran juga kasar, massanya besar dankekuatanya rendah karena serat-seratnya yang kaku memilki ikatan antar serat yanglemah.
Lignin bersifat termoplastik artinya lignin akan menjadi lunak dan dapatdibentuk pada suhu yang lebih tinggi dan keras kembali apabila menjadi dingin. Sifat termoplastik lignin menjadi dasar pembuatan papan kertas
(Hardboard) dan lain-lainproduk kayu yang dimampatkan ( Haygreen, 1987).
Lignin adalah suatu polimer yang kompleks dengan berat molekul tinggi, tersusun atas unit-unit fenilpropan.Meskipun tersusun atas karbon, hidrogen dan oksigen, lignin bukanlah suatu karbohidrat dan bahkan tidak ada hubungannya dengan golongan senyawa tesebut.Lignin sangat stabil dan sukar dipisahkan dan mempunyai bentuk yang bermacam-macam karenanya susunan lignin yang pasti di dalam kayu tetap tidak menentu.(Haygreen. J. G. dan Bowyer. J. L. 2007)
2.2.2 Hemiselulosa
Hemiselulosa semula diduga merupakan senyawa antara dalam biosintesis selulosa.Namun saat ini diketahui bahwa hemiselulosa termasuk dalam polisakarida heterogenyang dibentuk melalui jalan biosintesis yang berbeda dari selulosa.Berbeda denganselulosa yang merupakan homopolisakarida, Hemiselulosa merupakanheteropolisakarida. Seperti halnya selulosa kebanyakan hemiselulosa berfungsisebagai bahan pendukung dalam dinding sel. Hemiselulosa relatif mudah dihidrolisisoleh asam menjadi komponen– komponen monomernya, yang terdiri dari D-Glukosa,D-manosa, D-galaktosa, D-xilosa, L-arabinosa, dan sejumlah kecil L-ramnosa disamping menjadi asam D-glukuronat, asam 4-0-metil-D-glukuronat, dan asam D-galakturonat.
Kebanyakan hemiselulosa mempunyai derajat polimerisasi hanya 200.Sejumlah polisakarida kayu banyak bercabang dan mudah larut dalam air.Khasuntuk pohon-pohon tropika tertentu adalah pembentukan spontan getah-getah yangmenetes, yang adalah pembentukan spontan getah-getah-getah-getah yang menetes , yang menetessebagai cair kental pada tempat –tempat yang terluka dan setelah terdehidrasimenjadi bintil –bintil yang keras dan jernih yang keras dan jernih yang kaya akanpolisakarida. Getah –getah ini misalnya, getah arabika, terdiri atas polisakrida yangbanyak bercabang yang larut dalam air.Jumlah hemiselulosa dari berat kering biasanya antara 20-30%.Komposisi dan struktur hemiselulosa dalam kayu keras. Perbedaan-perbedaan yang besar jugaterdapat dalam kandungan dan komposisi hemiselulosa antara batang, cabang-cabang akar dan kulit kayu (Sjostrom,1995).
Rantai hemiselulosa lebih pendek dari pada rantai selulosa.Hemiselulosa adalah polimer bercabang atau tidak linier.Selama pembuatan pulp, hemiselulosa bereaksi lebih cepat dengan larutan pemasak dibandingkan dengan selulosa.Hemiselulosa bersifat hidrofil (mudah menyerap air) yang mengakibatkan strukturnya jadi kurang teratur.Kadar hemiselulosa dalam pulp jauh lebih kecil dibandingkan dengan serat asal, karena selama pemasakan hemiselulosa bereaksi dengan bahan pemasak dan lebih mudah terlarut daripada selulosa (Sjostrom.Eeoro. 1995).
2.3 CarboxyMethyl Cellulose(CMC)
Carboxy Methyl Cellulose adalah turunan dari selulosa dan ini sering dipakai
dalam industri makanan untuk mendapatkan tekstur yang baik.Fungsi CMC ada beberapa terpenting yaitu sebagai pengental, stabilisator, pembentuk gel, sebagai pengemulsi dan dalam beberapa hal dapat meratakan penyebaran antibiotik (Winarno, 1984).
Sebagai pengemulsi, CMC sangat baik digunakan untuk memperbaiki kenampakan tekstur dari produk berkadar gula tinggi.Sebagai pengental, CMC mampu mengikat air sehingga molekul-molekul air terperangkap dalam struktur gel yang dibentuk oleh CMC (Fardiaz, 1986).
Polisakarida stabilizer meliputi berbagai jenis hidrokoloid, diantaranya yaitu karboksimetil selulosa yang sering digunakan pada produk makanan beku untuk mengontrol pembentukan kristal-kristal es dan menghasilkan tekstur produk yang baik (Eliasson, 2004).
Senyawa CMC merupakan senyawa turunan selulosa yang paling penting, yang memiliki kepentingan yang sangat besar dalam industri dan kehidupan kita sehari-hari.Senyawa ini memiliki struktur yang linear, berantai panjang, tidak larut dalam air, dan polisakarida anionik yang diturunkan dari selulosa (Hong, 2013).
CMC dapat disintesis dari selulosa serat kayu,kapas,pohon pisang dan ampas tebu. Langkah pertama dari pembuatan karboksimetil selulosa adalah reaksi pembentukan selulosa alkali,yang mana dibentuk dari serbuk selulsa yang kuat. selulosa ditambahkan dengan NaOH. CMC terdiri dari eter yang mana bagian hidroksil dari glukosa anhidrat digantikan oleh karboksimetil dari bagian monokloroasetat (MCA). Dalam kondisi alkali, bagian hidroksil dari selulosa menunjukkan aktivitas tinggi.Untuk memproduksi CMC ada dua langkah penting yang dilakukan untuk reaksi ini.reaksipembasaan (Alkalisasi) dan reaksi eterifikasi,yang mengikuti ;
1. Reaksi pembasaan (Alkalisasi)
[C6H7O2(OH3)n] + nNaOH [C6H7O2(OH)2ONa]n + nH2O 2. Reaksi eterifikasi (Karboksimetilasi)
[C6H7O2(OH)2ONa] + nClCH2COONa
[C6H7O2(OH)2OCH COONa]n + nNaCl(Adel, A.M, 2010)
Reaksi diatas tidak dapat berjalan tanpa menggunakan pelarut.Isopropanol digunakan sebagai pelarut.reaksi pertama disebut endotermik reaksi kedua disebut eksotermik. Sintesis CMC ini umumnya digunakan dalam farmasi dan produk makanan. suasana basa dan eterifikasi adalah reaksi dengan menggunakan NaOH dan MCA (Heydarzadeh, H.D ,2009).
2.3.1 Alkalisasi Dan Karboksimetilasi a. proses alkalisasi
b. proses karboksimetilasi
proses karboksimetilasi ini sebenarnya adalah proses eterifikasi. Pada tahap ini merupakan proses peletakan gugus karboksilat pada kerangka selulosa. Gugus karboksilat yang dimaksud terdapat pada asam monokloroasetat.
2.4 Sifat-sifat CMC
CMC tidak berwarna dan tidak berbau, mudah larut dalam air panas dan air dingin. Kekentalan dihasilkan oleh kontribusi dari CMC untuk stabilisasi produk-produk beku seperti es krim. CMC juga dapat digunakan sebagai
stabilizer utama dalam es krim untuk mengontrol ukuran kristal es dan
pembentukan kristal es selama pembekuan dan penyimpanan untuk memberikan tekstur lembut saat dimakan(Phillips and Williams, 1987).
Sifat CMC yangbiodegradabledanfood grade relatif aman untuk digunakan dalam aplikasiberbagaiproduk makanan atau minuman.CMCsebagai pengemulsi sangat baikuntuk memperbaiki kenampakan tekstur dari produk berkadar gula tinggisedangkan sebagai pengentalsifatnya mampu mengikat air sehinggamolekul-molekul air terperangkap dalam struktur gel yang dibentuk olehCMC (Minifie, 1989).
2.5 Kegunaan Karboksimetil Selulosa (CMC)
2.5.1 Surfaktan
Berdasarkan muatannya, surfaktan dapat dikasifikasikan atas 4 golongan, yaitu surfaktan anionik, kationik, non-ionik dan amfoter. Surfaktan anionik yaitu surfaktan yang rantai hidrokarbonnya terikat pada suatu anion, seperti : COO- , OSO3- atau SO3-. surfaktan kationik yaitu surfaktan yang rantai hidrokarbonnya terikat pada suatu kation, seperti Na+. Surfaktan nonionik yaitu surfaktan yang rantai hidrokarbonnya tidak bermuatan, seperti –(OCH2-CH2)-OH. Selanjutnya adalah surfaktan amfoter, dimana pada rantai hidrokarbonnya ada muatan positif dan muatan negatif (swern and baylei, 1979).
Zat aditif pada permukaan yang teradsorbsi pada antarmuka air-minyak adalah sebagai akibat adanya gugus hidrofilik (menyukai air) atau gugus polar dan lipofilik (menyukai minyak) atau gugus non polar(Griffin, 1949).
Suatu surfaktan sangat bergantung pada gugus hidrofilik dan hidrofobik yang terdapat didalam molekulnya.Secara umum surfaktan memiliki sifat sebagai detergen, pembasah, pengemulsi dan pendispersi (Sharp and Harper, 1983).
[image:42.595.132.514.619.724.2]Senyawa CMC telah banyak digunakan dalam bidang industri dan kehidupan sehari-hari.Sebagai contoh senyawa ini digunakan dalam bidang makanan, farmasi, detergen, dan kosmetik (Najafpour et al., 2009).Selain itu, senyawa ini juga berguna dalam sistem koloid hidrofilik (Krishnaiah et al., 2009). Contoh kegunaan CMC yang lain dapat dilihat pada Tabel 1. berikut :
Tabel 2.1. Kegunaan CMC
Industri Aplikasi Fungsi
2.6 Derajat Substitusi
Derajat substitusi dapat dievaluasi dengan metode FT-IR dari perbandigan absorbansi pada 1573,91 (dianggap berasal dari pita karbonil) dan absorbansi 3425,58 (berasal dari pita hidroksil), dihitung dengan meggunakan persamaan 2.1 berikut ;
Persamaan 2.1 Derajat Substitusi
Dimana DS adalah derajat substitusi dan nilai 0,10 mewakili gugus yang spesifik dari selulosa asli (Moore dan Roberts, 1980).
2.7 Viskositas
Viskositas adalah ukuran yang menyatakan kekentala suatu cairan atau fluida.kekentalan merupakan sifat cairan yang berhubungan erat dengan hambatan untuk mengalir. Beberapa cairan ada yang dapat mengalir cepat, sedangkan yang lainnya mengalir secara lambat.Cairan yang mengalir cepat seperti air, alkohol dan bensin mempunyai viskositas kecil.Sedangkan cairan yang mengalir lambat seperti gliserin, minyak dan madu mempunyai viskositas besar. Jadi viskositas tidak lain menentukan kecepatan mengalirnya suatu cairan. Viskoaitas (kekentalan) cairan akan menimbulkan gesekan antara bagian-bagian atau lapisan-lapisan cairan yang bergerak satu terhadap yang lain.
Secara umum, viskositas cairan dapat ditentukan dengan dua metode, yaitu : 3. Viskosimeter Ostwald
Metode ini ditentukan berdasarkan hukum poiseuille menggunakan alat Viskosimeter Ostwald. Penetapannya dilakukan dengan jalan mengukur waktu yang diperlukan untuk mengalirnya cairan dalam pipa kapiler dari a ke b. Sejumlah cairan yang akan diukur viskositasnya dimasukkan kedalam viskosimeter yang diletakkan pada termostat(Yazid, 2005).
Pada metode Ostwald yang diukur adalah waktu yang diperlukan oleh sejumlah tertentu cairan untuk mengalir melalui pipa kapiler dengan gaya yang disebabka oleh berat cairan itu sendiri. Pada percobaan, sejumlah tertentu cairan dipipet ke dalam viskosimeter.Cairan kemudian dihisapmelalui labu pengukur dari viskosimeter sampai permukaan cairan
�� (%) =���1573
lebih tinggi dari batas “a” dan “b” dapat ditentukan.Tekanan P merupakan perbedaan tekanan antara kedua ujung pipa U dan besarnya diasumsikan sebanding dengan berat jenis cairan (Bird Tony, 1993).
4. Viskosimeter bola jatuh
Viskositas cairan dapat ditentukan dengan metode bola jatuh berdasarkan
hukum stokes.Penetapanya diperlukan bola kelereng dari logam dan alat
gelas silinder berupa tabung. Bola kelereng dengan rapatan d dan jari-jari r dijatuhkan kedalam tabung berisi cairan yang akan ditentukan viskositasnya. Waktu yang diperlukan bola untuk jatuh melalui cairan dengan tinggi tertentu kemudian dicatat dengan stopwatch (Bird Tony, 1993).
2.8 HLB (hidrofilik-lipofilik balance)
Untuk penentuan uji nilai HLB, Griffin merancang suatu skala sembarang dari berbagai angka untuk dipakai sebagai suatu ukuran keseimbangan
hidrofilik-lipofilik balance(HLB) dari zat-zat aktif permukaan. Dengan bantuan angka ini,
memungkinkan untuk membentuk suatu jarak HLB untuk efesiensi optimum atau terbaik dari masing-masing golongan surfaktan. HLB dari sejumlah senyawa dapat dihitung dengan menggunakan persamaan 2.4 ;
Persamaan 2.2 Penentuan HLB
Dimana S adalah bilangan penyabunan dan A adalah bilangan asam. zat aditif tersebut harus diimbangi dengan jumlah yang tepat antara gugus yang larut dalam air dan gugus yang larut dalam minyak sehingga dapat terorientasi pada antarmuka dan fase menurunkan tegangan. Jika molekul terlalu hidrofilik, itu berarti tetap dalam fase cairan dan tidak berpengaruh pada antarmuka.jika terlalu
sistem nomor ini, kemungkinan untuk membuat berbagai rentang HLB yang optimal untuk setiap kelas surfaktan dapat dilihat pada Gambar 2.3 berikut ;
Gambar 2.3 Skala Rentang Nilai HLB untuk beberapa Zat Aktif Permukaan
18
15
12
9
6
3
Skala HLB
Hidrofilik
Lipofilik
Zat Pelarut
Detergen
Zat Pengemulsi o/w
Zat Penyebar dan Pembasah
Zat Pengemulsi w/o
Kebanyakan Zat Antibusa
BAB 1
PENDAHULUAN
1. Latar Belakang
Durian (Durio zibethinus Murr) merupakan salah satu tanaman hasil perkebunan yang telah lama dikenal oleh masyarakat yang pada umumnya dimanfaatkan sebagai buah saja. Sebagian sumber literatur menyebutkan tanaman durian adalah salah satu jenis buah tropis asli Indonesia (Rukmana, 1996).
Kenyataannya, kulit dan biji buah hanya dibuang begitu saja tanpa dimanfaatkan menjadi lebih berguna.Jika dilihat, persentase bagian dagingnya termasuk rendah yaitu hanya 20-35%, sedangkan kulit (60-75%), dan biji (5-15%) belum termanfaatkan secara maksimal (Djaeni dan Prasetya, 2010).
Hasil penelitian Hatta (2007) menunjukkan bahwa kulit durian mengandung unsur selulosa yang tinggi (50-60%) dan kandungan lignin (5%) serta kandungan pati yang rendah (5%) sehingga dapat diindikasikan sebagai campuran bahan baku pangan olahan serta produk lainnya yang dimampatkan (Herman, 2009).
Wijayani,A (2005) telah meneliti tentang karboksimetil selulosa (CMC) dari eceng gondok dengan menggunakan metode perbandingan pada penambahan Natrium Monokloroasetat dan perbandingan penambahan NaOH. Nisa,D (2014) telah meneliti tentang CMC dari kulit buah kakao dengan metode perbandingan penambahan Trikoloroasetat dan perbandingan variasi waktu. Wulandari,G (2014) telah meneliti tentang sintesis O-karboksimetil N-lauril kitosan melalui eterifikasi kitosan dengan asam monokloroasetat dan diikuti asilasi dengan lauroil klorida.Dari uraian diatas, penulis bermaksud mengisolasi selulosa dari kulit durian yang digunakan sebagai pembuatan karboksimetil selulosa (CMC) dengan menggunakan asam monokloroasetat.
1.2 Permasalahan
1. Bagaimanakah hasil CMC (Carboxymethyl cellulose) dari selulosa hasil isolasi dari kulit buah durian berdasarkan sifat fisik serta berdasarkan penentuan Derajat substitusi (DS), Hidrofil-lifofil balance (HLB) dan Viskositas.
1.3 Pembatasan Masalah
1. Sampel yang digunakan adalah limbah kulit buah durian yang matang. 2. Selulosa yang diperoleh dari pemisahan selulosa kulit buah durian yang
diuji kualitatif kemudian digunakan untuk membuat CMC.
1.4 Tujuan Penelitian
1. Untuk mengetahui hasil karboksimetilasi (CMC) dari selulosa hasil isolasi kulit buah durian (Durio zibethinus Murr) melalui reaksi dengan asam monokloroasetat berdasarkan Derajat Substitusi (DS), (hidrofil lifofil
balance) HLB dan Viskositas.
2. Untuk mengetahui karakteristik CMC dari selulosa hasil isolasi kulit buah durian yang dihasilkan.
Penelitian ini diharapkan dapat memberikan informasi mengenai sintesis karboksimetil selulosa (CMC) dari selulosa hasil isolasi kulit durian (Durio
zibethinus Murr) dengan asam monokloroasetat.
1.6Lokasi Penelitian
Penelitian ini dilakukan di Laboratorium Kimia Organik FMIPA-USU Medan.Analisa spektrofotometer FT-IR dilakukan di Laboratorium Kimia Organik UGM.
1.7 Metodologi Penelitian
Penelitian ini bersifat eksperimen laboratorium dimana pada tahap pertama dilakukan isolasi selulosa dari kulit buah durian dengan melakukan perendaman dengan reagent NaOH 2% dalam beaker glass dan dipanaskan pada suhu 800C kemudian dicuci dengan aquadest hingga pH = 7. Selanjutnya dilakukan proses bleaching dengan menggunakan reagent H2O2 10% residunya dikeringkan dengan suhu 750C. Tahap selanjutnya dilakukan proses alkalisasi dengan menggunakan pelarut isopropanol dan ditambahkan reagent NaOH 30%. Kemudian dilakukan proses karboksimetilasi dengan menambahkan asam monokloroasetat yang berlangsung selama 1 jam dan dilakukan pengadukan selama 4 jam pada suhu 600C.
Karboksimetil selulosa hasil isolasi dari kulit durian ini ditentukan derajat substitusinya (DS), viskositas, penentuan harga HLB (Hydrophylic-lypophylic
Balance) dan kemudian dianalisis dengan spektrofotometer FTIR (Fourier
SINTESIS KARBOKSIMETIL SELULOSA (CMC) DARI
SELULOSA HASIL ISOLASI KULIT BUAH DURIAN
(Duriozibethinus Murr) MELALUI REAKSI DENGAN
ASAM MONOKLOROASETAT
ABSTRAK
Telah dilakukan penelitian mengenai sintesis Karboksimetil selulosa (CMC) dari selulosa hasil isolasi kulit durian (Duriozibethinus Murr) dengan asam monokloroasetat. Reaksi sintesis dilakukan dengan metode pemanasan dan reaksi alkalisasi menggunakan NaOH diikuti reaksi karboksimetilasi sehingga diperoleh karboksimetil selulosa (CMC). Hasil senyawa CMC didukung dengan spektrum FT-IR yang menunjukkan adanya serapan pada bilangan gelombang 1573,91 cm-1 yang merupakan serapan dari C=O dan adanya vibrasi C-O-C pada bilangan gelombang 1072,42 cm-1 serta bilangan gelombang OH pada 3425,58 cm-1 yang menunjukkan serapan dari karboksimetil selulosa (CMC). Pada penentuan HLB
(Hidrofilik Lipofilik Balance) diperoleh nilai 8,34 serta penentuan nilai viskositas
SYNTHESIS CARBOXYMETHYL CELLULOSE (CMC)
FROM CELLULOSE ISOLATION DURIAN’s PEEL
(Duriozibethinus Murr) THROUGH REACTION WITH
MONOCHLOROACETATE
ABSTRACT
We report the synthesis of carboxymethyl cellulose (CMC) of cellulose isolation results durian’s peel (Duriozibethinus Murr) using monocloroacetate acid. Synthesis reaction carried out by the method of heating and alkalization reaction using NaOH followed carboxymethylation reaction in order to obtain carboxymethyl cellulose (CMC). this is supported bt FT-IR spectrum to showed absorption at wave number 1573,91 cm-1 which is the absorption of C=O and the vibration wave number C-O-C at 1072,42 cm-1 and wave number of –OH 3425,58 cm-1 which shows the uptake of carboxymethyl cellulose (CMC). Determination of HLB (Hydrophilic lipophilic balance) which has a value of 8,34 which is expressed as a surfactant (w/o), as well as the determination of the viscosity value state viscosity of CMC supported by the value of the time’s 61,30 secon with mixing a concentration a CMC 0,05%. As well as the determination of degree of substitution (DS) a 90,3 % by acid monochloroacetate (MCA) of the cellulose insulation results of durian peel.
SINTESIS KARBOKSIMETIL SELULOSA (CMC) DARI
SELULOSA HASIL ISOLASI KULIT BUAH DURIAN (Durio
zibethinus Murr) MELALUI REAKSI DENGAN ASAM
MONOKLOROASETAT
SKRIPSI
DEDY SAH PUTRA MELIALA
100802050
DEPARTEMEN KIMIA
FAKULTAS MATEMATIKA DAN ILMU PENGETAHUAN
ALAM
UNIVERSITAS SUMATERA UTARA
MEDAN
SINTESIS KARBOKSIMETIL SELULOSA (CMC) DARI
SELULOSA HASIL ISOLASI KULIT BUAH DURIAN (Durio
zibethinus Murr) MELALUI REAKSI DENGAN ASAM
MONOKLOROASETAT
SKRIPSI
Diajukan untuk melengkapi tugas dan memenuhi syarat mencapai gelar sarjana sains
DEDY SAH PUTRA MELIALA
100802050
DEPARTEMEN KIMIA
FAKULTAS MATEMATIKA DAN ILMU PENGETAHUAN
ALAM
PERSETUJUAN
Judul : Sintesis karboksimetil selulosa (cmc) dari selulosa hasil isolasi kulit buah durian (duriozibethinus murr) melalui reaksi dengan asam monokloroasetat
Kategori : Skripsi
Nama : Dedy sah putra Meliala
NomorIndukMahasiswa : 100802050
Program : Sarjana (s1) kimia
Departemen : Kimia
Fakultas : Matematika dan ilmu pengetahuan alam (fmipa) universitas sumatera utara
Disetujui di
Medan, Januari 2016
KomisiPembimbing :
Pembimbing II Pembimbing I
Drs. Darwis Surbakti, MS Dr. Adil Ginting, M.Sc NIP.1953070719830301001 NIP. 195307041980031002
Diketahui/ Disetujui oleh
Departemen Kimia FMIPA USU Ketua,
PERNYATAAN
SINTESIS KARBOKSIMETIL SELULOSA (CMC) DARI
SELULOSA HASIL ISOLASI KULIT BUAH DURIAN
(Durio zibethinus Murr) MELALUI REAKSI DENGAN
ASAM MONOKLOROASETAT
SKRIPSI
Saya mengakui bahwa skripsi ini adalah hasil karya saya sendiri, kecuali beberapa kutipan dan ringkasan yang masing-masing disebutkan sumbernya.
Medan, Januari 2016
PENGHARGAAN
Puji dan syukur penulis panjatkan kepada Tuhan Yang Maha Esa, yang telah melimpahkan kasih dan karunian-Nya sehingga penulis dapat menyelesaikan skripsi ini sebagai salah satu syarat untuk menyelesaikan pendidikan sarjana sains di FMIPA USU dengan judul “SINTESIS KARBOKSIMETIL SELULOSA
(CMC) DARI SELULOSA HASIL ISOLASI KULIT BUAH DURIAN (Durio zibethinus Murr) MELALUI REAKSI DENGAN ASAM MONOKLOROASETAT”
Pada kesempatan ini penulis menyampaikan terima kasih kepada berbagai pihak yang telah membantu dalam penulisan skripsi ini kepada:
1. Bapak Dr. Adil Ginting, M.Sc selaku pembimbing I dan Bapak Drs.Darwis Surbakti, M.S selaku pembimbing II yang telah banyak meluangkan waktu untuk membimbing penulis dalam penelitian dan menyelesaikan skripsi ini hingga selesai.
2. Ibu Dr. Rumodang Bulan MS dan Bapak Drs. Albert Pasaribu M.Sc selaku ketua dan sekretaris departemen Kimia FMIPA USU, serta kepada Bapak Drs. Albert Pasaribu M.Sc selaku dosen PA penulis dan kepada semua staff dosen Departemen Kimia FMIPA USU.
3. Bapak Dr. Mimpin Ginting MS selaku Kepala Laboratorium Kimia Organik FMIPA USU
4. Seluruh staff pengajar FMIPA USU
5. Seluruh asisten Lab.Organik FMIPA USU
6. Sahabat-sahabat penulis : Rekan 2010 (Dedi Sinurat,Roympus Manalu, Mars Bronson Siburian,Gani simanjuntak, Abdi Surbakti, Thamrin Pakpahan,Idealisman,Ricky Sitinjak), rekan 2011 (Sahat Sihaloho,Dendy Sitepu, Choliq Doloksaribu)
7. Dan semua pihak yang tidak dapat disebutkan satu per satu.
Secara khusus, penulis mengucapakan terima kasih yang sebesar-besarnya kepada kedua orang tua penulis, Ayah tercinta J. Meliala dan Ibu tercinta P. Br Barus yang senantiasa memberikan doa atas dukungan moril dan materil hingga akhirnya penulis menyelesaikan studi. Penulis juga ucapkan terimakasih kepada adik-adik penulis Ivo Andreanta Meliala dan Greace Br Meliala, yang telah memberikan doa dan motivasi dalam menyelesaikan skripsi ini. Penulis meyadari bahwa skripsi ini masih jauh dari kesempurnaan karena keterbatasan penulis. Untuk itu dengan segala kerendahan hati, penulis mengharapkan saran dan kritik yang bersifat membangun demi kesempurnaan skripsi ini
Akhir kata penulis berharap semoga skripsi ini dapat bermanfaat bagi penelitian dan kemajuan ilmu pengetahuan.
SINTESIS KARBOKSIMETIL SELULOSA (CMC) DARI
SELULOSA HASIL ISOLASI KULIT BUAH DURIAN
(Duriozibethinus Murr) MELALUI REAKSI DENGAN
ASAM MONOKLOROASETAT
ABSTRAK
Telah dilakukan penelitian mengenai sintesis Karboksimetil selulosa (CMC) dari selulosa hasil isolasi kulit durian (Duriozibethinus Murr) dengan asam monokloroasetat. Reaksi sintesis dilakukan dengan metode pemanasan dan reaksi alkalisasi menggunakan NaOH diikuti reaksi karboksimetilasi sehingga diperoleh karboksimetil selulosa (CMC). Hasil senyawa CMC didukung dengan spektrum FT-IR yang menunjukkan adanya serapan pada bilangan gelombang 1573,91 cm-1 yang merupakan serapan dari C=O dan adanya vibrasi C-O-C pada bilangan gelombang 1072,42 cm-1 serta bilangan gelombang OH pada 3425,58 cm-1 yang menunjukkan serapan dari karboksimetil selulosa (CMC). Pada penentuan HLB
(Hidrofilik Lipofilik Balance) diperoleh nilai 8,34 serta penentuan nilai viskositas
SYNTHESIS CARBOXYMETHYL CELLULOSE (CMC)
FROM CELLULOSE ISOLATION DURIAN’s PEEL
(Duriozibethinus Murr) THROUGH REACTION WITH
MONOCHLOROACETATE
ABSTRACT
We report the synthesis of carboxymethyl cellulose (CMC) of cellulose isolation results durian’s peel (Duriozibethinus Murr) using monocloroacetate acid. Synthesis reaction carried out by the method of heating and alkalization reaction using NaOH followed carboxymethylation reaction in order to obtain carboxymethyl cellulose (CMC). this is supported bt FT-IR spectrum to showed absorption at wave number 1573,91 cm-1 which is the absorption of C=O and the vibration wave number C-O-C at 1072,42 cm-1 and wave number of –OH 3425,58 cm-1 which shows the uptake of carboxymethyl cellulose (CMC). Determination of HLB (Hydrophilic lipophilic balance) which has a value of 8,34 which is expressed as a surfactant (w/o), as well as the determination of the viscosity value state viscosity of CMC supported by the value of the time’s 61,30 secon with mixing a concentration a CMC 0,05%. As well as the determination of degree of substitution (DS) a 90,3 % by acid monochloroacetate (MCA) of the cellulose insulation results of durian peel.
DAFTAR ISI
Persetujuan ii
Pernyataan iii
Penghargaan iv
Abstrak v Abstrack vi Daftar Isi vii Daftar Tabel ix Daftar Gambar x Daftar Lampiran xi Daftar Grafik xii BAB 1 PENDAHULUAN 1.1 Latar Belakang 1 1.2 Permasalahan 2 1.3 Pembatasan Masalah 2 1.4 Tujuan penelitian 2 1.5 Manfaat Penelitian 3 1.6 Lokasi Penelitian 3 1.7 Metodologi Penelitian 3 BAB 2 TINJAUAN PUSTAKA 2.1 Buah Durian 4 2.2 Selulosa 5 2.2.1 Lignin 11
2.2.2 Hemiselulosa 13
2.3Karboksimetil Selulosa (CMC) 14
2.3.1 Alkalisasi dan Karboksimetilasi 15
2.4 Sifat-sifat CMC 16 2.5 Kegunaan Karboksimetil Selulosa 16 2.5.1 Surfaktan 16
2.6 Derajat Substitusi (DS) 18
2.7 Viskositas 18
2.8 HLB (hidrofilik-lipofilik balance) 19 BAB 3 METODE PENELITIAN
3.3.2.3 Pembuatan Larutan H2O2 10 % 22 3.3.2.4 Pembuatan Larutan Etanol 90 % 23 3.3.2.5 Pembuatan Larutan HCl 0,05 N 23 3.3.2.6 Pembuatan Larutan KOH 0,02 N 23 3.3.3 Isolasi selulosa dari kulit buah durian 23 3.3.4 Proses alkalisasi dan karboksimetilasi 23
3.3.5 Prosedur analisis 24
3.3.5.1Derajat Substitusi (DS) 24
3.3.5.2Viskositas 24
3.3.5.3Penentua Harga HLB 25
3.3.5.3.1 Analisis Bilangan Penyabunan 25 3.3.5.3.2 Analisis Bilangan Asam 25 3.3.5.4Analisis Spektrofotometer FT-IR 26
3.4 Bagan Penelitian 27
3.4.1 Isolasi selulosa dari kulit durian 27
3.4.2 Uji Kualitatif Selulosa 28
3.4.3 Proses alkalisasi dan karboksimetilasi 29 BAB 4 HASIL DAN PEMBAHASAN
4.1Hasil 30
4.1.1 Analisa FT-IR Selulosa 30
4.1.2 Analisa FT-IR karboksimetil Selulosa 31
4.1.3 Harga HLB 32
4.1.4 Penentuan Derajat Substitusi 33
4.1.5 Viskositas 34
4.2Pembahasan 34
4.2.1 Pembuatan Selulosa 34
4.2.2 Pembuatan Karboksimetil selulosa 35
4.2.3 Penentuan HLB 37
4.2.4 Derajat Substitusi 37
4.2.5 Viskositas 37
BAB 5 KESIMPULAN DAN SARAN
5.1 Kesimpulan 39
5.2 Saran 39
DAFTAR PUSTAKA 40
DAFTAR TABEL
Nomor Tabel
Judul Halaman
2.1 Kegunaan CMC 17
4.1 Data Penentuan Bilangan Penyabunan 32
4.2 Data Penentuan Bilangan Asam 32
DAFTAR GAMBAR
Nomor Gambar
Judul Halaman
2.1 Kulit Buah Durian 5
2.2 Struktur Selulosa 8
2.3 Skala Rentang Nilai HLB untuk beberapa zat aktif permukaan
20
4.1 Spektrum FT-IR Selulosa 30
4.2 Spektrum FT-IR Karboksimetil Selulosa 31
DAFTAR LAMPIRAN
Nomor Lampiran
Judul Halaman
1 Spektrum FT-IR selulosa 45
2 Spektrum FT-IR CMC 46
3 Perhitungan Nilai HLB Rata-rata 47
4 Gambar Rangkaian Alat Refluks 48
5 Gambar Proses penyaringan 48
6 Gambar Titrasi HLB 48
7 8
Gambar Karboksimetil Selulosa (CMC) Gambar Uji Kualitatif Selulosa
DAFTAR GRAFIK
Nomor Grafik
Judul Halaman