ISOLASI DAN IDENTIFIKASI BAKTERI ENDOFIT
TUMBUHAN NYAWAI (
Ficus variegata
Blume) SERTA
ANALISIS SENYAWA ANTIBAKTERI
SHINTA LEONITA
SEKOLAH PASCASARJANA INSTITUT PERTANIAN BOGOR
PERNYATAAN MENGENAI TESIS DAN
SUMBER INFORMASI SERTA PELIMPAHAN HAK CIPTA
Dengan ini saya menyatakan bahwa tesis berjudul Isolasi dan Identifikasi Bakteri Endofit Tumbuhan Nyawai (Ficus variegata Blume) Serta Analisis Senyawa Antibakteri adalah benar karya saya dengan arahan dari pembimbing dan belum diajukan dalam bentuk apa pun kepada perguruan tinggi mana pun. Sumber informasi yang berasal atau dikutip dari karya yang diterbitkan maupun tidak diterbitkan dari penulis lain telah disebutkan dalam teks dan dicantumkan dalam Daftar Pustaka di bagian akhir tesis ini.
Dengan ini saya melimpahkan hak cipta dari karya tulis saya kepada Institut Pertanian Bogor dan Lembaga Ilmu Pengetahuan Indonesia
.
Bogor, Agustus 2015
Shinta Leonita
RINGKASAN
SHINTA LEONITA. Isolasi dan Identifikasi Bakteri Endofit Tumbuhan Nyawai (Ficus variegata Blume) Serta Analisis Senyawa Antibakteri. Dibimbing oleh MARIA BINTANG dan FACHRIYAN HASMI PASARIBU.
Ficus variegata Blume merupakan tumbuhan obat yang mengandung
senyawa antibakteri. Bakteri endofit merupakan bakteri yang hidup bersimbiosis dengan tanaman. Beberapa spesies bakteri endofit telah diteliti memiliki kemampuan menghasilkan senyawa bioaktif, salah satunya antibakteri.
Tujuan penelitian ini adalah mengisolasi, menguji aktivitas antibakteri, mengidentifikasi bakteri endofit dari tumbuhan nyawai, serta menganalisis senyawa antibakteri yang dihasilkan oleh isolat bakteri potensial menggunakan GC-MS. Tahap awal pada penelitian ini yaitu isolasi bakteri endofit dari tumbuhan nyawai. Isolat yang dihasilkan kemudian diuji aktivitas antibakterinya terhadap Staphylococcus aureus, Escherichia coli, Bacillus subtilis, dan
Pseudomonas aeruginosa. Isolat yang mampu menghambat semua bakteri uji dinamakan isolat potensial. Identifikasi dilakukan secara morfologi, biokimia, dan molekuler berdasarkan sekuen 16S rRNA. Isolat potensial kemudian difermentasi dalam media nutrient broth (NB) selama 48 jam. Supernatan hasil fermentasi diekstraksi dengan etil asetat. Selanjutnya, analisis senyawa antibakteri yang dihasilkan oleh bakteri endofit dilakukan dengan menggunakan GC-MS.
Sebanyak 29 isolat bakteri endofit diperoleh dari Ficus variegata Blume. Berdasarkan uji aktivitas antibakteri, isolat bakteri endofit BH2 mampu menghambat pertumbuhan semua bakteri uji. Hasil identifikasi morfologi dan aktivitas biokimia menunjukkan bahwa bakteri isolat BH2 merupakan
Pseudomonas sp. Analisis sekuen 16S rRNA menggunakan BLAST menunjukkan
isolate BH2 memiliki presentase kemiripan dengan Pseudomonas aeruginosa
strain SV1 sebesar 99%. Hasil GC-MS menunjukkan bahwa senyawa aktif yang diduga berperan sebagai antibakteri dari ekstrak etil asetat isolat BH2 diantaranya asam nonanoat, dokosan, oktadekan, asam tetrakosanoat, asam heksadekanoat, asam 9-oktadekanoat, asam 1,2-benzenedikarboksilat bis (2-etilheksil) ester,
tetradekan, eikosan, nonakosan, dan triakontan.
SUMMARY
SHINTA LEONITA. Isolation and Identification of Endophytic Bacteria from
Ficus variegata Blume and Analysis of Antibacterial Compounds. Supervised by MARIA BINTANG dan FACHRIYAN HASMI PASARIBU.
Ficus variegata Blume known as medicinal plant which contains antibacterial compounds. Endophytic bacteria are bacteria that live symbiotically with plant. Some spesies of endophytic bacteria have the ability to produce bioactive compound, one of them is antibacterial.
The objectives of this research are to isolate, test antibacterial activity, identify endophytic bacteria from Ficus variegata Blume and analysis antibacterial compounds from potential isolate using Gas Chromatography-Mass Spectrometry (GC-MS). This research started with isolation of endophytic bacteria from Ficus variegata Blume. The isolate were tested antibacterial activity against Staphylococcus aureus, Escherichia coli, Bacillus subtilis, and
Pseudomonas aeruginosa. The isolate which able to inhibit the growth of all against bacteria called potential isolate. Identification of potential isolate spesies using morphological analysis, biochemical activity, and molecular analysis of 16S rRNA. Potential isolate was fermented in nutrient broth (NB) for 48 hours. The supernatant from fermentation was extracted with ethyl acetate. Analysis of antibacterial compounds which produced by endophytic bacteria are using GC-MS.
A total of 29 isolates of endophytic bacteria were obtained from Ficus variegata Blume. Based on antibacterial activity test, endophytic bacteria isolate BH2 from Ficus variegata Blume fruit had the ability to inhibit the growth of all against bacteria. The result of the identification of morphology and biochemical activity shows that bacteria isolate BH2 is Pseudomonas sp. Analysis of 16S rRNA sequence using BLAST showed that BH2 isolate was related to Pseudomonas aeruginosa strain SV1 with 99% identity. The result of GC-MC analysis showed that active compound which estimated as antibacterial from ethyl acetat extract of BH2 are : Nonanoic acid, Docosane, Octadecane, Tetracosanoic acid, Hexadecanoic acid, 9-Octadecenoic acid, 1,2-Benzenedicarboxylic acid, bis
(2-ethyhexyl) ester,Tetradecane, Eicosane, Nonacosane, and Triacontane.
Keywords: Endophytic bacteria, Ficus variegata Blume, Pseudomonas
© Hak Cipta Milik IPB, Tahun 2015
Hak Cipta Dilindungi Undang-Undang
Dilarang mengutip sebagian atau seluruh karya tulis ini tanpa mencantumkan atau menyebutkan sumbernya. Pengutipan hanya untuk kepentingan pendidikan, penelitian, penulisan karya ilmiah, penyusunan laporan, penulisan kritik, atau tinjauan suatu masalah; dan pengutipan tersebut tidak merugikan kepentingan IPB
Tesis
sebagai salah satu syarat untuk memperoleh gelar Magister Sains
pada
Program Studi Biokimia
ISOLASI DAN IDENTIFIKASI BAKTERI ENDOFIT
TUMBUHAN NYAWAI (
Ficus variegata
Blume) SERTA
ANALISIS SENYAWA ANTIBAKTERI
SEKOLAH PASCASARJANA INSTITUT PERTANIAN BOGOR
BOGOR 2015
PRAKATA
Puji dan syukur penulis panjatkan kehadirat Allah SWT atas segala rahmat dan karunia-Nya sehingga penulis dapat menyelesaikan tesis yang berjudul Isolasi dan Identifikasi Bakteri Endofit Tumbuhan Nyawai (Ficus variegata Blume) Serta Analisis Senyawa Antibakteri yang telah dilaksanakan sejak bulan September 2014 sampai Maret 2015 di Laboratorium Bakteriologi Fakultas Kedokteran Hewan-IPB.
Terima kasih penulis ucapkan kepada Prof Dr Drh Maria Bintang, MS dan Prof Dr Drh Fachriyan Hasmi Pasaribu selaku pembimbing, Staf Laboratorium Bakteriologi Fakultas Kedokteran Hewan-IPB Bapak Agus Somantri, serta teman-teman SPs Biokimia angkatan 2013 yang telah memberikan motivasi dalam menyelesaikan karya ilmiah ini. Ungkapan terima kasih juga disampaikan kepada kedua orang tua, Teguh Purwo Wastianto, Idha Yunita Rizki, serta Nur Arifin atas segala doa dan kasih sayangnya.
Penyusunan tesis ini tentunya tidak terlepas dari kekurangan. Oleh karena itu, penulis mengharapkan adanya saran dan kritik yang bersifat membangun untuk menyempurnakan penyusunan tesis ini. Semoga karya ilmiah ini dapat memberikan informasi yang bermanfaat bagi kemajuan ilmu pengetahuan.
Bogor, Agustus 2015
DAFTAR ISI
DAFTAR TABEL vi
DAFTAR GAMBAR vi
DAFTAR LAMPIRAN vi
1 PENDAHULUAN 1
Latar Belakang 1
Perumusan Masalah 3
Tujuan Penelitian 3
Manfaat Penelitian 3
Ruang Lingkup Penelitian 3
2 METODE 3
Waktu dan Tempat Penelitian 3
Bahan 4
Alat 4
Prosedur Analisis Data 4
3 HASIL 6
Isolat Bakteri Endofit 6
Penapisan Aktivitas Antibakteri 7
Identifikasi Morfologi dan Biokimia Bakteri Endofit Terpilih 8 Identifikasi Molekular 16S rRNA dan Pohon Filogenetik 8
Aktivitas Antibakteri Metabolit Isolat BH2 10
Identifikasi Senyawa dengan GC-MS 11
4 PEMBAHASAN 11
Isolat Bakteri Endofit 11
Penapisan Aktivitas Antibakteri 12
Identifikasi Morfologi dan Biokimia Bakteri Endofit Terpilih 12 Identifikasi Molekular 16S rRNA dan Pohon Filogenetik 13
Aktivitas Antibakteri Metabolit Isolat BH2 14
Identifikasi Senyawa dengan GC-MS 15
5 KESIMPULAN DAN SARAN 16
Kesimpulan 16
Saran 17
DAFTAR PUSTAKA 17
LAMPIRAN 22
DAFTAR TABEL
1 Identifikasi morfologi sel dan biokimia 8
2 Perbandingan tingkat kemiripan sekuen isolat BH2 dengan beberapa sekuen 16S rRNA pada data GenBank menggunakan program BLAST 9 3 Aktivitas antibakteri metabolit isolat BH2 10
DAFTAR GAMBAR
1 Tumbuhan nyawai 2
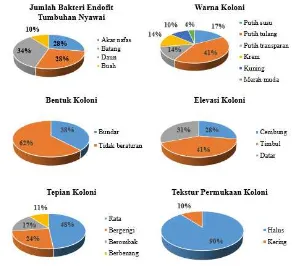
2 Presentase bakteri endofit yang diisolasi dari tumbuhan nyawai 7
3 Pembentukan zona hambat bakteri endofit 7
4 Pewarnaan Gram sel bakteri isolat BH2 8 5 Pohon filogenetik berdasarkan sekuen gen 16S rRNA dari
isolat BH2 10
6 Zona hambat yang terbentuk pada pengujian ekstrak etil
asetat 11
DAFTAR LAMPIRAN
1 Bagan Alir Penelitian 23
2 Determinasi tumbuhan nyawai 24
3 Data morfologi seluruh isolat bakteri endofit dari tumbuhan nyawai 23 4 Aktivitas antibakteri isolat bakteri endofit dari tumbuhan nyawai 26 5 Hasil sekuensing gen 16S rRNA bakteri endofit isolat BH2 27 6 Sekuen 16S rRNA isolat BH2 hasil pensejajaran 29 7 Hasil penelusuran homologi sekuen gen 16S rRNA dari bakteri endofit
isolat BH2dengan sekuen pada Genbank 30
8 Kromatogram hasil identifikasi senyawa ekstrak etil asetat isolat BH2 32
1 PENDAHULUAN
Latar Belakang
Indonesia merupakan negara yang memiliki biodiversitas tinggi dan memiliki kawasan hutan hujan tropis yang luas. Berbagai penelitian telah dilakukan untuk mengidentifikasi senyawa-senyawa bioaktif dari tumbuhan yang dapat dijadikan sebagai bahan baku obat. Penggunaan tumbuhan sebagai sumber obat meningkat seiring dengan meningkatnya resistensi bakteri penyebab infeksi terhadap berbagai jenis obat. Saat ini, banyak dilakukan pencarian tumbuhan obat yang belum teridentifikasi secara ilmiah di daerah pedalaman atau daerah hutan (Rahmadani 2014).
Spesies tumbuhan hutan yang berpotensi sebagai tumbuhan obat tetapi belum dimanfaatkan secara optimal, salah satu diantaranya adalah nyawai (Ficus variegata Blume) (Gambar 1). Nama lain tumbuhan nyawai adalah kundang, gondang (Jawa, Bali); kondang, (Sunda); ara, arah, aro, barai silai uding, haru kucing (Sumatera); hara, lua, nyawi, nyawai (Kalimantan); aga, andharahi montaha, bunta, rolli (Sulawesi); akau, andei yeva, gondal, sesem, kabato (Maluku); ganalang, kanjilu (Sumba) (Sumarni et al. 2009). Tumbuhan nyawai termasuk jenis pioner yang membutuhkan cahaya (intolerant) dan memiliki pertumbuhan cepat (fast growing). Tumbuhan ini dapat mencapai 25 meter dan mulai berbuah setelah umur 3 tahun. Buah tumbuh bergerombol pada batang atau cabang. Buah muda berwarna hijau, kemudian menjadi kuning dan setelah matang berwarna merah. Tipe buah termasuk buah periuk (Schiconium) dan berbentuk bulat (Haryjanto & Prastyono 2014).
Nyawai (Ficus variegata Blume) merupakan salah satu tumbuhan tingkat tinggi yang termasuk dalam genus Ficus. Tumbuhan genus Ficus merupakan genus terbesar dalam keluarga Moraceae yang terdistibusi di daerah tropis dan subtropis (Zheng et al. 2006). Penyebaran tumbuhan nyawai meliputi seluruh Asia Tenggara, India, Jepang, Cina, Taiwan, Australia, Kepulauan Pasifik (Zhekun & Gilbert 2003). Beberapa penelitian terbaru melaporkan tumbuhan genus Ficus
memiliki beberapa aktivitas. Akar nafas atau akar gantung Ficus bengalensis
memiliki aktivitas antipiretik (Hasti et al. 2011), Ficus religiosa berpotensi sebagai antikanker (Gulecha & Sivakuma 2011), Ficus carica memiliki aktivitas antimikroba (Jeong et al. 2009), Ficus racemosa memiliki aktivitas antioksidan (Ravishankan et al. 2013) dan antibakteri (Shaikh et al. 2011). Beberapa genus
Ficus lainnya ada yang dijadikan obat secara langsung seperti Ficus quercifolia,
Ficus septica, dan Ficus variegata untuk mengobati penyakit bisul, borok, luka, diare, eksim, dan penawar racun binatang berbisa (Aryani et al. 2009).
alkaloid dan saponin (Rijai 2013). Sedangkan pada daun nyawai telah diketahui memiliki kandungan fenol yang tinggi (Lushaini et al. 2015).
Gambar 1 Tumbuhan nyawai (Rijai 2013; Lushaini et al. 2015)
Khasiat obat dari tumbuhan nyawai tidak terlepas dari kandungan senyawa bioaktif yang dimilikinya. Senyawa bioaktif yang terkandung dalam tumbuhan nyawai diduga erat kaitannya dengan keberadaan bakteri endofit dalam tumbuhan tersebut. Beberapa studi ilmiah menunjukkan bahwa bakteri endofit mampu menghasilkan senyawa bioaktif yang sama dengan tanaman inangnya (Radji 2005; Simarmata et al. 2007).
Pseudomonas, Bacillus dan Burkholderia adalah genus bakteri endofit yang paling sering ditemui dan mampu menghasilkan senyawa bioaktif, salah satunya berpotensi sebagai senyawa antimikroba (Ryan et al. 2007). Bacillus subtilis yang diisolasi dari mulbery menunjukkan aktivitas antimikroba (Qiong-Ying et al. 2012), Bacillus Pumilus dari cassava mampu menghasilkan lipopeptida pumilacidin (Melo et al. 2009), Pseudomonas sp. yang diisolasi dari umbi tanaman dahlia mampu memproduksi senyawa antibakteri yang mampu menghambat bakteri patogen (Elita et al. 2013), serta Burkholderia cepacia
memiliki aktivitas antibakteri (Gohat et al. 2010). Jose & Christy (2013) melaporkan bahwa Serratia, Bacillus, Pseudomonas, Micrococcus, dan
Enterobacter dari tanaman Rhizopora mucronata mampu menghasilkan senyawa antimikroba yang aktif terhadap bakteri dan cendawan patogen. Beberapa hasil penelitian senyawa antibakteri dari bahan alami terutama tumbuhan dan bakteri endofit mampu memberikan hasil yang menjanjikan dalam pengembangan senyawa-senyawa antibakteri baru.
3
Perumusan Masalah
Nyawai (Ficus variegata Blume) khususnya bagian buah telah dilaporkan memiliki aktivitas antibakteri, sehingga berpotensi sebagai sumber obat antibakteri baru. Kemungkinan besar senyawa antibakteri tersebut juga dihasilkan oleh bakteri endofit yang hidup di dalam tumbuhan nyawai. Sampai saat ini, belum dilaporkan mengenai isolasi dan identifikasi bakteri endofit tumbuhan nyawai dalam menghasilkan senyawa antibakteri.
Tujuan Penelitian
Penelitian ini bertujuan mengisolasi dan mengidentifikasi bakteri endofit dari tumbuhan nyawai (Ficus variegata Blume) berdasarkan analisis morfologi, biokimia, sekuen gen 16S rRNA, serta menganalisis senyawa antibakteri yang dihasilkan oleh isolat bakteri endofit potensial menggunakan Gas
Chromatography-Mass Spectrometry (GC-MS).
Manfaat Penelitian
Penelitian ini diharapkan dapat memberikan informasi mengenai potensi bakteri endofit dari tumbuhan nyawai (Ficus variegata Blume) sebagai penghasil senyawa antibakteri yang akan memberikan konstribusi bagi pengembangan penelitian dalam bidang kesehatan.
Ruang Lingkup Penelitian
Penelitian ini mencakup isolasi bakteri endofit dari tumbuhan nyawai (Ficus variegata Blume). Isolat-isolat tersebut diseleksi untuk menentukan isolat yang memiliki aktivitas antibakteri melalui uji terhadap Staphylococcus aureus, Bacillus subtilis, Escherichia coli, dan Pseudomonas aeruginosa. Isolat bakteri endofit yang mampu menghambat pertumbuhan bakteri uji diidentifikasi secara morfologi, biokimia, molekuler dengan marka 16S rRNA, serta identifikasi senyawa antibakteri yang dihasilkan dengan GC-MS.
2 METODE
Waktu dan Tempat
Bahan
Bahan yang digunakan dalam penelitian ini adalah tumbuhan nyawai (Ficus variegata Blume) yang diperoleh dari daerah Gunung Sindur Bogor.
Tumbuhan nyawai ini telah diidentifikasi di Herbarium Bogoriense, Balitbang Biologi-LIPI Bogor (Lampiran 2). Bahan lain yang digunakan yaitu Nutrient Agar
(Oxoid), Nutrient Broth (Difco), Na-hipoklorit 5,25%, nistatin, etanol 96%, kultur bakteri uji (Staphylococcus aureus, Bacillus subtilis, Escherichia coli, dan
Pseudomonas aeruginosa), kristal violet, lugol, safranin, media untuk uji biokimia, primer 27f (5’-AGAGTTTGATCCTGGCTCAG-3’), 1492r (5’-GGTTACCTTGT TACGAC TT-3’), 518F (5’-CCAGCAGCCGCGGTAATACG-3’) dan 800R (5’ -TACCAG GGTATCTAATCC-3’), InstaGene Matrix (Bio-Rad, USA), Montage PCR Clean up kit (Milipore), Big Dye terminator cycle sequencing kit (Applied BioSystems, USA), n-heksana, etil asetat, kloroform, n-butanol dan kloramfenikol.
Alat
Alat yang digunakan dalam penelitian ini adalah pipet mikro, alat gelas, vorteks, cawan Petri, inkubator, mikroskop, mesin sentrifugasi, corong pisah, tabung eppendorf, mesin Polymerase Chain Reaction (PCR), Applied Biosystems model 3730XL automated DNA sequencing system (Applied BioSystems, USA) dan Mesin GC-MS (Shimadzu Type GCMS-QP2010).
Prosedur Penelitian
Isolasi Bakteri Endofit (Kusumawati et al. 2014 modifikasi)
Sampel berupa beberapa bagian dari tumbuhan nyawai (Ficus variegata
Blume) seperti akar nafas (AR), batang (BT), daun (DN), dan buah (BH). Sampel dicuci dengan air mengalir hingga bersih, kemudian dipotong masing-masing sekitar 1-3 cm. Potongan sampel tersebut dilakukan sterilisasi permukaan secara bertahap. Potongan sampel direndam etanol 96% selama 1 menit, dilanjutkan ke dalam Na-hipoklorit 5.25% selama 5 menit, kemudian dibilas lagi ke dalam etanol 96% sebanyak tiga kali. Sampel yang telah disterilisasi lalu ditanam pada media isolasi Nutrient Agar (NA) yang mengandung nistatin (0.01% b/v) kemudian diinkubasi di ruang gelap pada suhu ruang dan diamati sampai adanya pertumbuhan koloni. Pemurnian dilakukan dengan memindahkan 1 ose koloni bakteri ke dalam media NA. Setelah diperoleh biakan murni, bakteri endofit dipindahkan ke agar miring NA.
Penapisan Isolat Bakteri Endofit (Simarmata et al. 2007)
Peremajaan isolat bakteri endofit dan bakteri uji (Staphylococcus aureus, Bacillus subtilis, Escherichia coli, dan Pseudomonas aeruginosa) dilakukan dengan menginokulasi ke dalam media NA lalu diinkubasi pada suhu 28-300C selama 24 jam. Koloni bakteri uji yang tumbuh dipindahkan ke dalam 5 ml media
5
dituang ke dalam cawan Petri steril sebanyak ± 20 ml dan dibiarkan memadat. Isolat bakteri endofit diinokulasikan ke dalam media yang telah mengandung bakteri uji. Cawan tersebut diinkubasi selama 24-48 jam. Zona penghambat diukur berdasarkan diameter zona bening yang terbentuk di sekitar isolat bakteri endofit. Isolat bakteri endofit yang positif menunjukkan zona hambat terhadap semua bakteri uji merupakan isolat potensial.
Identifikasi Morfologi dan Biokimia Isolat Bakteri Endofit Terpilih
Isolat bakteri endofit yang menghasilkan zona hambat terluas kemudian diidentifikasi secara morfologi dan uji biokimia bakteri. Metode identifikasi bakteri yang dilakukan secara konvensional tersebut meliputi : pewarnaan Gram, uji katalase, uji oksidase, motilitas, pigmen, pertumbuhan, uji gula-gula, hidrolisis gelatin, hidrolisis kasein, urea, sitrat, dan arginine. Hasil dari karakterisasi bakteri tersebut kemudian dicocokan dengan Manual for the identification of Medical Bacteria (Cowan 1974).
Identifikasi molekuler berdasarkan sekuen 16S rRNA
Isolasi DNA Bakteri Endofit Isolat BH2. Koloni isolat BH2 disuspensikan ke dalam 0,5 ml larutan garam steril pada tabung sentrifugasi 1,5 ml, kemudian disentrifugasi dengan kecepatan 10000 rpm selama 10 menit. Pelet lalu diresuspensi dengan penambahan 0,5 ml InstaGeneMatrix (Bio-Rad, USA). Setelah itu, diinkubasi pada suhu 560C selama 30 menit, lalu dipanaskan 1000C selama 10 menit. Setelah proses pemanasan, supernatant yang berisi DNA cetakan siap untuk digunakan pada proses selanjutnya.
Amplifikasi Gen penyandi 16S rRNA. Amplifikasi DNA dilakukan menggunakan mesin PCR. Primer yang digunakan pada penelitian ini adalah 27F dan 1492R. Volume DNA cetakan yang ditambahkan adalah 1 µl dari 20 µl total larutan reaksi. Amplifikasi yang dilakukan sebanyak 35 siklus, dengan kondisi PCR sebagai berikut : denaturasi 940C selama 45 detik, annealing 550C selama 60 detik dan elongasi pada suhu 720C selama 60 detik. Selanjutnya dilakukan purifikasi produk PCR menggunakan Montage PCR Clean up kit (Milipore).
Sekuensing Gen 16S rRNA, Analisis Bioinformatik dan Konstruksi Pohon Filogenetik. Produk PCR kemudian disekuensing menggunakan dua primer (518F dan 800R) dan Big Dye terminator cycle sequencing kit (Applied BioSystems, USA) kemudian dianalisis menggunakan Applied Biosystems model 3730XL automated DNA sequencing system (Applied Biosystems, USA). Hasil sekuensing berupa urutan DNA kemudian disejajarkan menggunakan program BioEdit Sequence Aligment Editor versi 7.2.0 lalu dianalisis lebih lanjut menggunakan program BLASTN (Kusumawati 2014). Analisis filogenetik menggunakan program multiple aligment Clustal X2. Konstruksi jarak kekerabatan genetik dengan metode Neighbor joining. Konstruksi jarak evolusi dalam derajat kepercayaan menggunakan bootstrap value pada program NJ plot (Singh et al. 2011).
memisahkan bagian pelet dan supernatan. Supernatan yang dihasilkan selanjutnya diekstraksi dengan beberapa pelarut yaitu heksana, etil asetat, kloroform, n-butanol, dan etanol (1:1 v/v) menggunakan corong pisah. Ekstrak yang diperoleh selanjutnya diuapkan pelarutnya. Ekstrak kering disimpan untuk analisis selanjutnya (Garcia et al. 2012 modifikasi). Pengujian aktivitas antibakteri dilakukan dengan menggunakan metode difusi sumur dengan mengukur diameter penghambatan dari ekstrak tersebut (Garriga et al. 1993). Media NA yang mengandung bakteri uji dituangkan ke dalam cawan Petri steril dan dibiarkan memadat. Selanjutnya media tersebut dibuat lubang-lubang atau sumur dengan diameter 6 mm. Ekstrak dari fraksi teraktif dimasukkan sebanyak 50 µl ke dalam lubang tersebut dan diinkubasi dalam inkubator suhu 370C selama 24-48 jam. Identifikasi Senyawa Antibakteri dengan GC-MS
Ekstrak dari fraksi teraktif selanjutnya dianalisis menggunakan mesin GC-MS (Shimadzu tipe QP2010) untuk mengidentifikasi senyawa antibakteri dalam ekstrak tersebut. Kolom yang digunakan adalah Capiler type Phase Rtx-5MS dengan panjang 60 m dan diameter 0.25 mm. Kondisi alat meliputi : suhu kolom 50ºC, gas helium, SPL Temperature 280 ºC, MS Interface 280 ºC, pyrolisis temperature 280 ºC, dan ion surface 200 ºC.
3 HASIL
Isolat Bakteri Endofit
7
Gambar 2 Presentase bakteri endofit yang diisolasi dari tumbuhan nyawai Penapisan Aktivitas Antibakteri
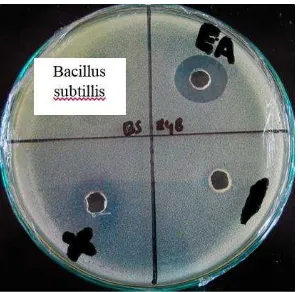
Penapisan merupakan tahap seleksi dan penentuan bakteri endofit tumbuhan nyawai yang memiliki aktivitas antibakteri. Hasil penapisan menunjukkan dari 29 isolat bakteri endofit yang berhasil diisolasi ternyata hanya 7 isolat bakteri saja yang memiliki aktivitas antibakteri yaitu isolat DN11, DN12, DN13, DN14, DN15, BT12, dan BH2. Sebanyak 6 isolat mampu menghambat pertumbuhan Staphylococcus aureus, 5 isolat mampu menghambat Eschericia coli, 4 isolat menghambat Bacillus subtilis, dan 4 isolat mampu menghambat pertumbuhan Pseudomonas aeruginosa (Lampiran 4). Pemilihan isolat potensial dilakukan dengan memilih isolat yang membentuk zona hambat paling besar dan jernih pada semua bakteri uji. Isolat BH2 menunjukan aktivitas penghambatan terhadap seluruh bakteri uji dan dipilih untuk tahap berikutnya (Gambar 3).
Identifikasi Morfologi dan Biokimia Bakteri Endofit Terpilih
Hasil pengamatan secara morfologi sel (Gambar 4), menunjukkan bahwa isolat BH2 berbentuk batang dan termasuk bakteri Gram negatif. Berdasarkan karakter morfologi dan biokimia yang diperoleh, isolat BH2 kemudian dibandingkan dengan ciri-ciri bakteri yang diuraikan oleh Cowan (1974). Hasil identifikasi isolat BH2 yaitu memiliki kemiripan dengan jenis Pseudomonas sp. Hasil identifikasi isolat BH2 secara morfologi dan biokimia dapat dilihat pada Tabel 1.
Gambar 4 Pewarnaan Gram sel bakteri endofit isolat BH2 Tabel 1 Identifikasi morfologi sel dan biokimia
Parameter uji Hasil Reaksi
Morfologi sel Gram Bentuk Negatif Batang
Katalase +
Oksidase +
Motilitas +
Pigmen +
Pertumbuhan 42
0C MacConkey
- +
Uji gula-gula Glukosa Laktosa Maltosa Manitol Salicin Xylose
+ - d d - -
Hidrolisis Gelatin Kasein
- -
Urease d
Arginin +
Keterangan : (+) = uji positif (-) = uji negatif (d) = uji dubius
Identifikasi Molekular 16S rRNA dan Pohon Filogenetik
9
(pensejajaran) dengan sekuen 16S rRNA, diperoleh pasangan basa sepanjang 1463 bp (Lampiran 6).
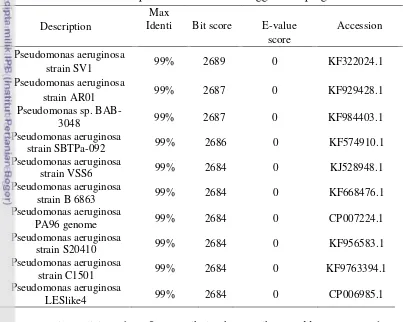
Urutan basa yang diperoleh dari hasil sekuensing selanjutnya dianalisis dengan program BLAST. Hasil analisis sekuen 16S rRNA menggunakan pogram BLAST menunjukkan isolat BH2 memiliki kemiripan dengan Pseudomonas aeruginosa strain SV1 dengan nilai bit score yang tinggi dan E-value sebesar 0 dengan nilai identiknya 99% (Tabel 2). Hasil penelusuran homologi sekuen gen 16S rRNA dari bakteri endofit isolat BH2 dengan sekuen Pseudomonas aeruginosa strain SV1 pada Genbank (Lampiran 7).
Tabel 2 Perbandingan tingkat kemiripan sekuen isolat BH2 dengan beberapa sekuen 16S rRNA pada data GenBank menggunakan program BLAST Description
Max
Identi Bit score E-value Accession
score
Hasil analisis pohon filogenetik jarak genetik (neighbor joining) dapat dilihat pada Gambar 5. Angka yang terdapat disetiap cabang pohon memperlihatkan nilai bootstrap. Berdasarkan pohon filogenetik yang mengikutsertakan beberapa data sekuen GenBank sebagai pembanding menunjukkan bahwa isolat BH2 berada dalam satu kelompok spesies
Gambar 5 Pohon filogenetik berdasarkan sekuen gen 16S rRNA dari isolat BH2 Aktivitas Antibakteri Metabolit Isolat BH2
Hasil pengamatan terhadap aktivitas antibakteri ekstrak metabolit isolat BH2 dari fraksi-fraksi pelarut disajikan pada Tabel 3. Fraksi etil asetat, kloroform, dan n-butanol yang memiliki aktivitas antibakteri, sedangkan fraksi n-heksana dan etanol tidak menunjukkan aktivitas antibakteri.
Tabel 3 Aktivitas antibakteri metabolit isolat BH2 Pelarut
Zona hambat (mm) Bacillus
subtillis
Staphylococcus aureus
Escherichia coli
Pseudomonas aeruginosa
n-heksana 0 0 0 0
Etil asetat 16.03 11.37 8.73 8.5
Kloroform 10.17 7.95 8.2 3.47
n-butanol 10.44 8.94 8.68 5.83
Etanol 0 0 0 0
11
Gambar 6 Zona hambat yang terbentuk pada pengujian ekstrak etil asetat metabolit isolat BH2 terhadap Bacillus subtillis
Identifikasi Senyawa dengan GC-MS
Hasil analisis GC-MS terhadap fraksi teraktif etil asetat metabolit isolat BH2 teridentifikasi sebanyak 30 senyawa berdasarkan penelusuran database
nama-nama senyawa yang terdapat dalam perangkat computer GC-MS (Lampiran 8). Senyawa dengan konsentrasi tertinggi adalah asam nonanoat. Senyawa yang sering muncul adalah dokosan dan oktadekan. Senyawa yang diduga berperan sebagai antibakteri dengan konsentrasi yang lebih kecil yaitu asam tetrakosanoat, asam heksadekanoat, asam 9-oktadekanoat, asam 1,2-benzenedikarboksilatbis (2-etilheksil) ester, tetradekan, eikosan, nonakosan, triakontan.
4 PEMBAHASAN
Isolat Bakteri Endofit
Bakteri endofit dapat diisolasi dari jaringan tumbuhan bagian dalam. Bakteri endofit diisolasi dari tumbuhan nyawai melalui sterilisasi permukaan. Menurut Hallman et al. (1997) bakteri endofit adalah bakteri yang hidup dalam jaringan tanaman yang dapat diisolasi melalui sterilisasi permukaan jaringan. Jumlah bakteri endofit di dalam tanaman tidak dapat ditentukan secara pasti, namun bakteri ini dapat dideteksi dengan mengisolasi pada media agar (Bacon & Hinton 2006). Media isolasi yang digunakan adalah media NA karena media ini lebih cocok untuk isolasi bakteri endofit (Sulistiyani 2014) dan ditambahkan nistatin sebagai antifungi (Kumala & Siswanto 2007).
umumnya melalui akar, namun demikian, bagian tanaman yang terpapar udara langsung seperti daun (melalui stomata), bunga, batang ranting, dan kotiledon dapat juga sebagai jalur masuk bakteri endofit. Bakteri endofit juga bisa memasuki tanaman pada saat tanaman mengalami luka yang disebabkan oleh faktor biotik dan faktor abiotik (Siddiqui & Shaukat 2003). Penelitian ini juga diperoleh bakteri endofit pada akar nafas dan buah. Hal ini membuktikan bahwa bakteri endofit dapat diisolasi dari berbagai jaringan tanaman serperti akar, daun, batang, dan buah (Hallmann et al. 1997; Simarmata et al. 2007; Bacon & Hinton 2006).
Penapisan Aktivitas Antibakteri
Penapisan merupakan tahap seleksi dan penentuan bakteri endofit tumbuhan nyawai yang memiliki aktivitas antibakteri. Isolat bakteri endofit yang mempunyai aktivitas antibakteri dapat dilihat dari zona hambat yang terbentuk pada cawan Petri. Zona hambat yang terbentuk disebabkan bahwa bakteri endofit tersebut memiliki kemampuan untuk memproduksi senyawa ekstraseluler yang bersifat antibakteri (Kusumawati 2014). Pembentukkan zona hambat juga dipengaruhi oleh jenis bakteri uji. Menurut Tortora et al. (2007) dan Pandey et al.
(2011) menjelaskan bahwa adanya perbedaan antara dinding sel bakteri Gram positif dan Gram negatif. Perbedaan ini yang menyebabkan bakteri Gram positif lebih rentan karena pada bagian luar hanya memiliki lapisan peptidoglikan yang tidak efektif sebagai penghalang, sedangkan bakteri Gram negatif memiliki membran luar polisakarida yang menyebabkan dinding sel tidak dapat ditembus oleh antibiotik, pewarna, dan deterjen.
Senyawa antibakteri yang dihasilkan oleh bakteri memiliki sifat selektif dalam menghambat pertumbuhan bakteri lain. Senyawa antibakteri kisaran luas adalah senyawa antibakteri yang mampu membunuh berbagai jenis mikroorganisme, sedangkan antibakteri kisaraan sempit ialah senyawa antibakteri yang mampu mematikan hanya beberapa jenis mikroorganisme (Levinson 2004). Pemilihan isolat potensial dilakukan dengan memilih isolat yang membentuk zona hambat paling besar dan jernih pada semua bakteri uji. Berdasarkan hasil tersebut maka isolat BH2 yang menunjukan aktivitas penghambatan terhadap seluruh bakteri uji dan dipilih untuk tahap berikutnya (Gambar 3).
Identifikasi Morfologi dan Biokimia Bakteri Endofit Terpilih
Pengamatan berdasarkan bentuk morfologi bakteri tidak cukup untuk melakukan identifikasi bakteri. Ciri lainnya seperti sifat pewarnaan dan sifat metabolisme bakteri berdasarkan serangkaian uji biokimia sangat membantu dalam identifikasi bakteri. Wilson (2014) menyatakan bahwa uji biokimia merupakan hal penting dalam identifikasi bakteri karena setiap isolat bakteri memiliki ciri fisiologis yang spesifik untuk setiap uji. Hasil pengamatan morfologi sel dan uji biokimia dapat dilihat pada Tabel 1.
13
al. (2012) menyatakan bahwa bakteri yang umum terdapat pada permukaan buah meliputi bakteri Gram positif dan Gram negatif dengan struktur morfologi yang bervariasi seperti batang, bacillary rods, dan bulat.
Beberapa uji biokimia yang penting dalam identifikasi isolat bakteri antara lain katalase, oksidase, motilitas, pigmen, pertumbuhan, penggunaan karbohidrat, hidrolisis gelatin dan kasein, urease, serta arginin. Hasil uji katalase isolat BH2 menunjukkan hasil positif. Aktivitas enzim katalase yang dimiliki oleh isolat bakteri endofit dan biasanya terdapat pada sel-sel bakteri dengan metabolisme aerobik (Wilson 2014). Hal ini menunjukkan bahwa isolat BH2 juga dapat dikatakan bakteri aerob karena mampu menghasilkan enzim katalase yang merupakan enzim yang penting bagi sel bakteri.
Tahapan uji biokimia ini sangat mempengaruhi dalam menentukan genus dan spesies dari bakteri. Menurut Cowan (1974) identifikasi bakteri dengan teknik konvensional adalah membandingkan bakteri yang sedang diidentifikasi dengan bakteri yang telah teridentifikasi sebelumnya dan tidak dapat menemukan spesies baru. Berdasarkan karakter morfologi dan biokimia yang diperoleh, isolat BH2 kemudian dibandingkan dengan ciri-ciri bakteri yang diuraikan oleh Cowan (1974). Hasil identifikasi isolat BH2 yaitu memiliki kemiripan dengan jenis
Pseudomonas sp. Genus Pseudomonas merupakan bakteri endofit yang banyak ditemukan hampir pada semua sampel tanaman. Hal ini dikarenakan bakteri ini mudah ditumbuhkan dan berpotensi sebagai agen biokontrol (Miller et al. 2012).
Pseudomonas dikenal sebagai bakteri antagonis karena menghasilkan metabolit sekunder berupa antibiotik terhadap bakteri patogen tumbuhan. Bakteri endofit
Pseudomonas yang berhasil diisolasi dari tanaman mangrove memiliki aktivitas antibakteri dan antifungi (Jose & Christy 2013). Selain itu, Elita et al. (2013) melaporkan bakteri endofit genus Pseudomonas sp. dari tanaman dahlia (Dahlia variabillis) mengandung metabolit sekunder golongan saponin yang berpotensi sebagai antibakteri karena dapat menghambat pertumbuhan Eschericia coli dan
Staphylococcus aureus.
Identifikasi Molekular 16S rRNA dan Pohon Filogenetik
Amplifikasi sekuen 16S rRNA pada penelitian ini menggunakan primer universal, yaitu primer forward dan reverse (27F dan 1492R). Daerah gen pada primer tersebut banyak digunakan dalam filogenetika, klasifikasi, dan identifikasi untuk bakteri karena sifat keberadaannya yang ubikuitas dengan fungsi yang identik pada semua bakteri. Produk DNA hasil amplifikasi kemudian digunakan untuk sekuensing.
Urutan basa yang diperoleh dari hasil sekuensing (Lampiran 6) selanjutnya dianalisis dengan program BLAST. Program bioinformatika BLAST menggunakan analisis statistik untuk menghasilkan bit score dan E-value. Homologi yang tinggi ditunjukkan dengan bit score yang semakin besar. Sedangkan nilai E-value yang semakin kecil menunjukkan tingkat homologi kedua sekuens semakin tinggi. Hasil analisis sekuen 16S rRNA menggunakan pogram BLAST menunjukkan isolat BH2 memiliki kemiripan dengan
Pseudomonas aeruginosa strain SV1 dengan nilai bit score yang tinggi dan E-value sebesar 0 dengan nilai identiknya 99% (Tabel 2). Hal ini menunjukkan bahwa tingkat homologi sekuen sampel sangat tinggi. Nilai E-value bernilai 0 menunjukkan bahwa kedua sekuen tersebut identik (Claverie & Notredame 2003). Berdasarkan pohon filogenetik yang mengikutsertakan beberapa data sekuen GenBank sebagai pembanding menunjukkan bahwa isolat BH2 berada dalam satu kelompok spesies Pseudomonas (Gambar 5). Isolat BH2 memiliki kemiripan terdekat dengan Pseudomonas aeruginosa strain SV1. Bakteri
Pseudomonas aeruginosa dapat memberikan keuntungan pada tumbuhan
inangnya. Berdasarkan hasil penelitian Hidayati (2014) membuktikan bahwa bakteri endofit pseudomonas aeruginosa yang diisolasi dari tanaman karet mampu menghasilkan hormon Indole Acetic Acid (IAA), Gliberelin dan Sitokinin. Selain itu, Charyulu et al. (2012) menunjukkan bahwa estrak metabolit sekunder
Pseudomonas aeruginosa MTCC 5210 yang diisolasi dari sendimen laut mampu menghasilkan senyawa antibakteri yang mampu penghambat pertumbuhan mikroba resisten terhadap antibiotik seperti Methicillin Resisten Staphylococcus aureus (MRSA).
Aktivitas Antibakteri Metabolit Isolat BH2
Isolasi senyawa aktif yang memiliki aktivitas antibakteri dilakukan dengan menumbuhkan isolat bakteri potensial BH2 ke dalam media NB selama 48 jam kemudian disentrifugasi untuk memisahkan sel bakteri dengan supernatan yang mengandung senyawa ekstraseluler bersifat antibakteri (Kusumawati 2014). Supernatan dari kultur bakteri endofit BH2 diekstrak menggunakan berbagai pelarut n-heksana, etil asetat, kloroform, n-butanol, dan etanol. Fraksi-fraksi pelarut tersebut selanjutnya dilakukan uji aktivitas antibakteri. Pengujian ini dilakukkan untuk mengetahui potensi antibakteri dari ekstrak metabolit isolat bakteri endofit tersebut dalam menghambat pertumbuhan bakteri uji. Zona hambat yang terbentuk disebabkan adanya senyawa metabolit isolat BH2 yang memiliki aktivitas antibakteri.
15
Staphylococcus aureus dengan rata-rata diameter zona hambat diatas 10 mm. Sedangkan fraksi etil asetat tergolong aktivitas sedang terhadap Escherichia coli
dan Pseudomonas aeruginosa. Hal ini sesuai dengan Zahro & Agustini (2013) yang menjelaskan pengelompokkan antibakteri ke dalam empat kelompok, yaitu antibakteri dengan aktivitas rendah (<5 mm), sedang (6-10 mm), kuat (11-20 mm), dan sangat kuat (>20 mm).
Hasil uji aktivitas antibakteri menunjukkan bahwa fraksi etil asetat metabolit bakteri endofit BH2 memiliki spektrum luas karena mampu menghambat pertumbuhan bakteri Gram positif dan Gram negatif. Berdasarkan hasil tersebut, menunjukkan diameter zona hambat ekstrak etil asetat metabolit bakteri endofit paling besar yaitu terhadap Bacillus subtillis yang dapat dilihat pada Gambar 6. Kontrol positif yang digunakan adalah kloramfenikol karena antibiotik ini sensitif terhadap bakteri Gram positif dan Gram negatif. Sedangkan kontrol negatif yang digunakan adalah pelarut etil asetat. Pelarut etil asetat yang diujikan sebagai kontrol negatif terhadap keempat bakteri uji tidak menunjukkan aktivitas zona hambat. Hal ini membuktikan bahwa diameter zona hambat yang dihasilkan oleh ekstrak etil asetat disebabkan oleh adanya senyawa-senyawa yang berpotensi sebagai antibakteri dan bukan pengaruh dari pelarut etil asetat (Sugara 2011).
Besarnya diameter zona hambat terhadap Bacillus subtilis menunjukkan bahwa bakteri Gram positif ini lebih sensitif terhadap fraksi etil asetat metabolit isolat BH2 yang merupakan bakteri endofit Psedomonas aeruginosa. Charyulu et al. (2012) melaporkan aktivitas antibakteri metabolit sekunder Pseudomonas aeruginosa menunjukkan aktivitas bakterisidal terhadap Bacillus subtillis. Hasil penelitian ini juga membuktikan bahwa isolat bakteri endofit Pseudomonas aeruginosa yang diisolasi dari buah nyawai juga memiliki aktivitas antibakteri seperti ekstrak tumbuhan inangnya. Rijai (2013) membuktikan bahwa zona hambat yang dihasilkan oleh ekstrak fraksi etil asetat buah nyawai memiliki aktivitas antibakteri dengan diameter zona hambat terbesar terhadap Bacillus subtilli dibandingkan dengan Staphylococcus aureus, Escherichia coli dan
Psedomonas aeruginosa.
Identifikasi Senyawa dengan GC-MS
Bakteri endofit memiliki kemampuan mensintesis senyawa metabolit sekunder yang termasuk ke dalam kelompok senyawa bioaktif (Baker & Satish 2013). Adanya aktivitas antibakteri dari ekstrak etil asetat metabolit BH2 terhadap bakteri uji mengindikasikan keberadaan suatu senyawa antibakteri yang terdapat dalam ekstrak tersebut. Untuk melihat identitas dari senyawa-senyawa yang terdapat pada ekstrak tersebut maka dilakukan pengujian menggunakan Gas
Chromatography-Mass Spectrometry (GC-MS).
mengakibatkan kematian pada bakteri patogen (Naviner et al. 1999). Menurut Murhadi (2009) asam-asam lemak yang paling dominan pada tanaman adalah asam palmitat, asam stearat, asam oleat, dan asam laurat.
Asam nonanoat merupakan senyawa yang memiliki nilai kelimpahan terbanyak yaitu 42%. Asam nonanoat atau pelargonic acid ini tidak larut air, tetapi larut dalam pelarut organik, eter dan alkohol. Asam nonanoat juga merupakan unsur utama dari minyak atsiri. Minyak atsiri dikenal memiliki aktivitas antimikroba. Turunan asam nonanoat telah dilaporkan memiliki aktivitas antimikroba yaitu mampu menghambat pertumbuhan Bacillus cereus, Salmonella typhimirium, Mycobacterium smegmatis, Sarcina lutea, dan Candida utilis (Sahin
et al. 2006).
Senyawa asam heksadekanoat (asam palmitat) dan asam 9-oktadekanoat (asam oleat) diketahui memiliki aktivitas antibakteri. Sugara (2011) melaporkan bahwa ekstrak etil asetat tanaman obat bandotan memiliki aktivitas sebagai antibakteri dengan komponen yang terkandung di dalamnya yaitu senyawa asam heksadekanoat dan asam 9-oktadekanoat. Fitriani et al. (2015) juga menyatakan ekstrak kasar bakteri endofit Pseudomonas yang diisolasi dari akar Ageratum conyzoides L. mengandung senyawa asam 9-oktadekanoat. Asam 9-oktadekanoat yang merupakan turunan dari asam oleat mampu menghambat pertumbuhan
Staphylococcus aureus dan Streptococcuspyogenes (Zheng et al. 2005).
Berdasarkan hasil analisa GC-MS didapatkan juga senyawa asam 1,2-benzenedikarboksilat bis (2-etilheksil) ester. Senyawa asam 1,2-benzenedikarboksilat juga ditemukan pada kapang endofit Taxus yunnanensis
yang mampu menghambat pertumbuhan Staphylococcus aureus, Bacillus subtilis
dan (Chen et al. 2009). Penelitian yang dilakukan oleh Gohar et al. (2010) menginformasikan keberadaan senyawa asam 1,2-benzenedikarboksilat bis (2-etilheksil) ester pada ekstrak etil asetat metabolit sekunder Burkholderia cepacia
yang memiliki aktivitas antibakteri terhadap Aeromonas hydrophila, Edwardsiella tarda dan Vibrio ordalli. Senyawa asam tetrakosanoat yang terkandung di dalam ekstrak daun Finlaysonia obovata memiliki aktivitas antibakteri dengan menghambat pertumbuhan bakteri patogen Aeromonas hydrophila, Pseudomonas aeruginosa, Vibrio alginolticus, Staphylococcus aureus Eschericia colli, Edwardsiella tarda dan Micrococcus sp. (Mishra & Sree 2007). Selain itu, senyawa yang diperoleh dari ekstrak daun Azadirachta indica seperti tetradekan, oktadekan, dokosan, eikosan, nonakosan, dan triakontan merupakan senyawa yang juga memiliki aktivitas antibakteri terhadap Salmonella typhi (Akpuaka et al.
2013).
5
KESIMPULAN DAN SARAN
Kesimpulan
Bakteri endofit dapat diisolasi dari tumbuhan nyawai (Ficus variegata
17
kemiripan dengan Pseudomonas sp. Berdasarkan analisis sekuen 16S rRNA, isolat BH2 memiliki presentase kemiripan dengan Pseudomonas aeruginosa strain SV1 sebesar 99%. Hasil GC-MS menunjukkan bahwa senyawa aktif yang diduga berperan sebagai antibakteri dari ekstrak etil asetat BH2 diantaranya asam nonanoat, dokosan, oktadekan, asam tetrakosanoat, asam heksadekanoat, asam 9-oktadekanoat, asam 1,2-benzenedikarboksilat bis (2-etilheksil) ester, tetradekan, eikosan, nonakosan, dan triakontan.
Saran
Perlu dilakukan penelitian lebih lanjut terkait optimasi media dan waktu fermentasi isolat BH2 dalam menghasilkan senyawa antibakteri dan meneliti terkait mekanisme kerja dari senyawa antibakteri tersebut dalam menghambat bakteri uji.
DAFTAR PUSTAKA
Akpuaka A, Ekwenchi EK, Dashak DA, Dildar A. 2013. Biological activities of characterized isolate of n-hexan extract of Azadirachta Indica A.Juss (Neem) leaves. New York Science Journal. 6(6): 119-124.
Aryani N, Zuhelmi Z, Hafrijal S, Jaswandi. 2009. Studi nutrisi buah ara (Ficus racemose L.) untuk pakan ikan. Jurnal Natur Indonesia. 12(1): 54-60. Bacon CW, Hinton DM. 2006. Bacterial endophytes: the endophytic niche, its
occupants, and its utility. Di dalam: Gnanamanickam SS, editor, Plant-Associated Bacteria. Netherland : Springer.
Baker S, Satish S. 2013. Bioprospeting of endophytic bacterial plethora from medicinal plant. Plant Sciences Feed. 3: 42-45.
Charyulu EM, Japyesan S, Gnanamani A. 2012. Antioxidant and antimicrobial profile of a secondary metabolite of Pseudomonas aeruginosa: ESR and spectrophotometric methods. Oxidants and Antioxidants in Medical Science. 1(2): 119-126.
Chen S, Liu J, Gong H, Yang D. 2009. Identification and antibacterial activity of secondary metabolites from Taxus endophytic fungus. Sheng Wu Gong Cheng Xue Bao. 25: 368-374.
Claverie JM, Notredame C. 2003. Bioinformatics for Dummies. Indianapolis: Wiley Publishing.
Cowan SJ. 1974. Manual for The Identification of Medical Bacteria. Cambridge: Cambridge University Press.
[Dephut] Departemen Kehutanan. 2008. Nyawai (Ficus variegata Blume). http://library.forda-mof.org/libforda/file=33Nyawai. (24 November 2014). Elita A, Saryono S, Cristine J. 2013. Penentuan waktu optimum produksi
antimikroba dan uji fitokimia ekstrak kasar fermentasi bakteri endofit
Fitriani A, Fajrul I, Yanti H, Maemunah. 2015. Antibacteria activity of
Shewanella and Pseudomonas as endophytic bacteria from the root of
Ageratum conyzoides L. Asian Journal of Applied Sciences. 3: 415-420. Garcia A, Rhoden SA, Bernardi WJ, Orlandelli RC, Azevedo JL, Pamphile JA.
2012. Antimicrobial activity of crude extract of endophytic fungi isolated from medicinal plant Sapindus saponaria L. Journal of Applied Pharmaceutical Science. 2(10): 35-40.
Garriga M, Aymerich HM, Monfort JM. 1993. Bacteriocinogenic activity of
Lactobacilli from fermentor sausages. Journal of Applied Bacteriology. 75: 142-148.
Gohar YM, El-Naggar MMA, Soliman MK, Barakat KM. 2010. Characterization of marine Burkholderia cepacia antibacterial agents. International Journal of Natural Products. 3: 86-94.
Gulecha V, Sivakuma T. 2011. Anticancer activity of Tephrosia purpurea and
Ficus religiosa using MCF 7 cell lines. Asian Pacific Journal of Tropical Medicine. 526-529.
Hallman J, Hallmann AQ, Mahaffee WF, Kloepper JW. 1997. Bacterial endophytes in agricultural crops. Canadian Journal of Microbiology. 43: 895-914.
Haryjanto L, Prastyono. 2014. Pendugaan parameter genetik semai Nyawai (Ficus variegata Blume) asal pulau Lombok. Jurnal Penelitian Kehutanan Wallacea. 3(1): 37-45.
Hasti S, Sandi NH, Srianti T. 2011. Uji efek antipiretika ekstrak etanol, fraksi etil asetat dan fraksi heksan akar gantung beringin (Ficus benjamina L.) pada tikus putih betina (Rattus norvegicus). Prociding Seminar Nasional Farmasi. Padang.
Helander M, Ahlholm J, Sieber TN, Hinneri S, Saikkonen K. 2007. Fragmented environment affects birch leaf endophytes. New Phytologist. 175: 547-553. Hidayati U. 2014. Potensi bakteri enodfit asal tanaman karet sebagai pemacu
pertumbuhan bibit batang bawah tanaman karet (Hevea brasiliensis Mull. Arg.). [Disertasi]. Bogor: Institut Pertanian Bogor.
Jeong MR, Kim HY, Cha JD. 2009. Antimicrobial activity of methanol extract from Ficus carica leaves against oral bacteria. Journal of Bacteriology and Virology. 39(2): 97-102.
Jose AC, Christy PH. 2013. Assessment of antimicrobial potential of endophytic bacteria isolated from Rhizophora mucronata. International Journal of Current Microbiology and Applied Sciences. 2(10): 188-194. Kumala S, Siswanto EB. 2007. Isolation and screening of endophytic microbes
from Morinda citrifolia and their ubility to produce antimicrobial subtances.
Microbiology Indonesia. 1: 145-148.
Kusumawati DE. 2014. Isolasi dan karakterisasi senyawa antibakteri dari bakteri endofit tanaman miana (Colens scutellariodes L. Benth.). [Thesis]. Bogor: Institut Pertanian Bogor.
Lacava PT, Arau’jo WL, Macron J, Maccheroni W, Azevedo JL. 2004. Interaction between endophytic bacteria from citrus plant and the phytopatogenic bacteria Xyllela fastidiosa, causal agent of citrus-variegated chlorosis.
19
Levinson W. 2004. Medical microbiology and immunology. Eight edition.
McGraw-Hill : New York.
Lushaini S, Muhamad AW, Puji A. 2015. Kandungan total fenol, aktivitas antioksidan dan sitotoksik daun kedadai (Ficus variegata Blume). Jurnal Kimia Khatulistiwa. 4(2): 1-5.
Madigan MT, Martinko JM, Dunlap PV, Clark DP. 2009. Microbiology of
Microorganism. USA: Pearson Benjamin Cummings.
Mano H, Tanaka F, Nakamura C, Kaba H, Morisaki H. 2007. Culturable endophyte Bacillus pumilus MAIIIM4A. Scientia Agricola. 66(5): 583-592. Miller KI, Qing C, Sze DM, Roufogalis BD, Neilan BA. 2012. Culturable
endophytes of medicinal plants and the genetic basis for their bioactivity.
Microbial Ecology. 64: 431-449.
Mishra PM, Sree A. 2007. Antibacterial activity and GCMS analysis of the extract of leaves of Finlaysonia obovate (A Mangrove Plant). Asian Journal of Plant Sciences. 6(1): 168-172.
Murhadi. 2009. Senyawa dan aktivitas antimikroba golongan asam lemak dan eternya dari tanaman. Jurnal Teknologi Industri dan Hasil Pertanian. 14(1): 97-105.
Naviner M, Bergee JP, Durand P, Le BH. 1999. Antibacterial activity of the marine diatom Skeletonema costatum against aquacultural pathogens.
Journal aquaqultur. 174: 15-24.
Pandey A, Ali I, Butola KS, Chatterji T, Singh V. 2011. Isolation and characterization of actinomycetes from soil and evaluation of antibacterial activities of actinomycetes against pathogens. The International Journal of Applied Biology and Pharmaceutical Technology. 2: 384-392.
Pareira P, Ibanez F, Rosenblueth M, Etcheverry M, Martinez-Romero E. 2011. Analysis of bacterial diversity associated with the roots of Maize (Zea mays
L.) through culture-dependent and culture-independent methods.
International Scholarly Research Network. Doi: 10.5402/2011/938546. Qiong-Ying W, Jun-Qiang J, Guang-Xiu T, Zhong-Zheng G. 2012. Isolation and
characterization of an antimicrobial endophytic bacterium ME-2 from mulberry twig in Chin. African Journal of Microbiology Research. 6: 6462-6467.
Radji M. 2005. Peranan bioteknologi dan mikroba endofit dalam pengembangan obat herbal. Majalah Ilmu Kefarmasian. 3: 113-126.
Rahmadani, A. 2014. Isolasi dan uji aktivitas antibakteri metabolit sekunder daun tendani (Goniothalamus macrophyllus Hook.f. & Thoms). [Tesis]. Yogjakarta: Universitas Gajah Mada.
Rijai, L. 2013. Potensi tumbuhan libo (Ficus variegata Blume) sebagai sumber bahan farmasi potensial. Journal of Tropical Pharmacy and Chemistry. 2(3): 166-179.
Ryan RP, Germaine K, Franks A, Ryan DJ, Dowling DN. 2007. Bacteria endophytes: recent developments and applications. Federation of European Microbiological Societies Microbiology. 278: 1-9.
Sahin N, Ibrahim K, Yunus E. 2006. Investigation of antimicrobial activities of nonanoic acid derivatives. Fresenius Environmental Bulletin. 15(2): 141-143. Seo WT, Lim WJ, Kim EJ, Yun HD, Lee YH, Cho KM. 2010. Endophytic
bacterial diversity in the Young Radish and their antimicrobial activity against pathogens. Journal of The Korean Society for Applied Biological Chemistry. 53(4): 493-503.
Shaikh T, Rub R, Bhise K, Pimprikar RB, Sufiyan A. 2010. Antibacterial activity of Ficus racemosa Linn leaves on Actinomyces viscosus. Journal of Pharmaceutical Sciences and Research. 2: 41-44.
Siddiqui IA, Shaukat SS. 2003. Endophytic bacteria: prospects and opportunities for the biological control of plant-parasitic nematodes. Nematologia Mediterranea. 31: 111-120.
Simarmata R, Lekatompessy S, Sukiman H. 2007. Isolasi mikroba endofitik dari tanaman obat sambung nyawa (Gymura procumbens) dan analisis potensinya sebagai antimikroba. Berkala Penelitian Hayati. 13: 85-90. Singh V, Chaudhary DK, Mani I. 2011. Molecular characterization and modeling
of secondary structure of 16S rRNA from aeromonas veronii. International Journal of Applied Biology and Pharmaceutical Technology. 3(1): 253-260. Sinha N, Jiwan S, Jozsef B, James W, Pilar C. 2012. Handbook of fruits and fruit
processing. Second Edition. US: Willey Blackwell.
Stackebrandt E, Goebel BM. 1994. Taxonomic note: a place for DNA-DNA reassociation and 16S rRNA sequence analysis in the present species definition in bacteriology. International Journal of Systematic and Evolutionary Microbiology. 44: 846-849.
Sugara TH. 2011. Karakterisasi senyawa aktif antibakteri dari fraksi etil asetat daun tanaman bandotan (Ageratum conyzoides L). [Tesis]. Bogor: Institut Pertanian Bogor.
Sulistiyani TR. 2014. Keragaman bakteri endofit tanaman kunyit putih (Curcuma zedoaria) dan toksisitasnya terhadap embrio ikan zebra. [Tesis]. Bogor: Institut Pertanian Bogor.
Sumarni G, Muslich M, Hadjib N, Krisdianto, Malik D, Suprapti S, Basri E, Pari G, Iskandar MI, Siagian RM. 2009. Sifat dan kegunaan kayu : 15 jenis andalan setempat Jawa Barat. Bogor: Pusat Penelitian dan Pengembangan Hasil Hutan.
Tortora GJ, Funke BR, Case CL. 2007. Microbiology: An Intoduction 9th edition. San Francisco: Pearson Education.
Wilson W. 2014. Bakteri endofit tanaman purwoceng (Pimpinella pruatjan
21
Zahro L, Agustini R. 2013. Uji efektivitas antibakteri ekstrak kasar saponin jamur tiram putih (Pleurotus ostreatus) terhadap Staphylococcus aureus dan
Escherichia coli. Journal of Chemistry. 2(2): 120-129.
Zheng CJJ, Yoo T, Lee H, Cho Y, Kimdan, Kim W. 2005. Fatty acid synthesis is a target for antibacterial activity of unsaturated fatty acids. Federation of European Biochemical Societies. 579: 5157-5162.
Zhekun Z, MG Gilbert. 2003. Moraceae. Flora ofChina. 5:21-73.
Zheng H, Wu Y, Ding J, Binion D, Fu W, Reardon R. 2006. Invasive plant of Asian origin established in the united state and their natural enemieas.
Forest Health Tecnology Enterprise Team. 1: 79.
23
Lampiran 1 Bagan alir penelitian
Isolasi Bakteri Endofit
Isolat Bakteri Endofit Peremajaan Bakteri Uji
dan Bakteri Endofit Isolat Bakteri UJi
Penapisan Aktivitas Antibakteri Bakteri
Endofit
Isolat Potensial
Identifikasi Biokimia
Identifikasi 16S rRNA
Spesies Bakteri Endofit
Fermentasi
Sentrifugasi
Supernatan Pelet
Ekstraksi
Ekstrak Fraksi Teraktif
Uji Aktivitas Antibakteri Identifikasi
GC-MS
Senyawa antibakteri
25
Lampiran 3 Data morfologi seluruh isolat bakteri endofit dari tumbuhan nyawai
No
Kode Morfologi
Isolat Warna Bentuk Elevasi Pinggiran Tekstur
Permukaan
1 AR11 kuning bundar timbul bergerigi halus
2 AR12 putih tulang tidak beraturan timbul rata halus 3 AR13 putih transparan tidak beraturan datar rata halus 4 AR21 putih tulang tidak beraturan cembung berbenang kering 5 AR22 putih tulang tidak beraturan datar rata halus
6 AR31 krem tidak beraturan datar rata halus
7 AR32 putih susu bundar cembung berombak halus
8 AR33 putih transparan tidak beraturan datar rata halus
9 BT11 putih tulang bundar timbul rata halus
10 BT12 krem bundar timbul rata halus
11 BT13 putih transparan bundar timbul rata halus
12 BT14 kuning bundar datar rata halus
13 BT15 putih tulang bundar datar rata halus
14 BT16 putih susu tidak beraturan cembung berombak halus 15 BT21 putih susu tidak beraturan datar rata halus 16 BT22 merah muda tidak beraturan datar rata halus
17 DN11 krem bundar timbul berombak halus
18 DN12 putih tulang tidak beraturan timbul bergerigi halus 19 DN13 putih tulang tidak beraturan cembung berbenang kering
20 DN14 kuning bundar timbul bergerigi halus
21 DN15 putih tulang tidak beraturan timbul bergerigi halus 22 DN21 putih tulang tidak beraturan cembung berombak halus
23 DN22 putih susu bundar timbul berombak halus
24 DN23 putih tulang tidak beraturan cembung bergerigi halus 25 DN24 putih transparan tidak beraturan datar rata halus 26 DN3 putih tulang tidak beraturan cembung bergerigi halus 27 BH1 putih susu tidak beraturan timbul bergerigi halus
28 BH2 krem bundar timbul rata halus
Lampiran 4 Aktivitas antibakteri isolat bakteri endofit dari tumbuhan nyawai
Keterangan : (-) : tidak menghambat; (+): menghambat < 2 mm; (++): < 5 mm; (+++) : > 10 mm; BS: Bacillus subtilis; SA: Staphylococcus aureus; PA: Pseudomonas aeruginosa; EC:
Escherichia coli
Isolat Bakteri Uji
BS SA EC PA
AR11 - - - -
AR12 - - - -
AR13 - - - -
AR21 - - - -
AR22 - - - -
AR31 - - - -
AR32 - - - -
AR33 - - - -
BT11 - - - -
BT12 + - + +
BT13 - - - -
BT14 - - - -
BT15 - - - -
BT16 - - - -
BT21 - - - -
BT22 - - - -
DN11 + + - -
DN12 - ++ ++ -
DN13 + ++ - -
DN14 - + ++ -
DN15 - + ++ -
DN21 - - - -
DN22 - - - -
DN23 - - - -
DN24 - - - -
DN3 - - - -
BH1 - - - -
BH2 +++ +++ + ++
27
29
Lampiran 7 Hasil penelusuran homologi sekuen gen 16S rRNA dari bakteri endofit isolat BH2dengan sekuen pada Genbank
>gb|KF322024.1| Pseudomonas aeruginosa strain SV1 16S ribosomal RNA gene, partial sequence
Length=1501
Score = 2689 bits (1456), Expect = 0.0
Identities = 1461/1463 (99%), Gaps = 2/1463 (0%) Strand=Plus/Plus
Query 3 TCAGATT-AACGCTGGCGGCAGGCCTAACACATGCAAGTCGAGCGGATGAAGGGAGCTTG 61 ||||||| |||||||||||||||||||||||||||||||||||||||||||||||||||| Sbjct 4 TCAGATTGAACGCTGGCGGCAGGCCTAACACATGCAAGTCGAGCGGATGAAGGGAGCTTG 63
Query 62 CTCCTGGATTCAGCGGCGGACGGGTGAGTAATGCCTAGGAATCTGCCTGGTAGTGGGGGA 121 |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||| Sbjct 64 CTCCTGGATTCAGCGGCGGACGGGTGAGTAATGCCTAGGAATCTGCCTGGTAGTGGGGGA 123
Query 122 TAACGTCCGGAAACGGGCGCTAATACCGCATACGTCCTGAGGGAGAAAGTGGGGGATCTT 181 |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||| Sbjct 124 TAACGTCCGGAAACGGGCGCTAATACCGCATACGTCCTGAGGGAGAAAGTGGGGGATCTT 183
Query 182 CGGACCTCACGCTATCAGATGAGCCTAGGTCGGATTAGCTAGTTGGTGGGGTAAAGGCCT 241 |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||| Sbjct 184 CGGACCTCACGCTATCAGATGAGCCTAGGTCGGATTAGCTAGTTGGTGGGGTAAAGGCCT 243
Query 242 ACCAAGGCGACGATCCGTAACTGGTCTGAGAGGATGATCAGTCACACTGGAACTGAGACA 301 |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||| Sbjct 244 ACCAAGGCGACGATCCGTAACTGGTCTGAGAGGATGATCAGTCACACTGGAACTGAGACA 303
Query 302 CGGTCCAGACTCCTACGGGAGGCAGCAGTGGGGAATATTGGACAATGGGCGAAAGCCTGA 361 |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||| Sbjct 304 CGGTCCAGACTCCTACGGGAGGCAGCAGTGGGGAATATTGGACAATGGGCGAAAGCCTGA 363
Query 362 TCCAGCCATGCCGCGTGTGTGAAGAAGGTCTTCGGATTGTAAAGCACTTTAAGTTGGGAG 421 |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||| Sbjct 364 TCCAGCCATGCCGCGTGTGTGAAGAAGGTCTTCGGATTGTAAAGCACTTTAAGTTGGGAG 423
Query 422 GAAGGGCAGTAAGTTAATACCTTGCTGTTTTGACGTTACCAACAGAATAAGCACCGGCTA 481 |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||| Sbjct 424 GAAGGGCAGTAAGTTAATACCTTGCTGTTTTGACGTTACCAACAGAATAAGCACCGGCTA 483
Query 482 ACTTCGTGCCAGCAGCCGCGGTAATACGAAGGGTGCAAGCGTTAATCGGAATTACTGGGC 541 |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||| Sbjct 484 ACTTCGTGCCAGCAGCCGCGGTAATACGAAGGGTGCAAGCGTTAATCGGAATTACTGGGC 543
Query 542 GTAAAGCGCGCGTAGGTGGTTCAGCAAGTTGGATGTGAAATCCCCGGGCTCAACCTGGGA 601 |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||| Sbjct 544 GTAAAGCGCGCGTAGGTGGTTCAGCAAGTTGGATGTGAAATCCCCGGGCTCAACCTGGGA 603
Query 602 ACTGCATCCAAAACTACTGAGCTAGAGTACGGTAGAGGGTGGTGGAATTTCCTGTGTAGC 661 |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||| Sbjct 604 ACTGCATCCAAAACTACTGAGCTAGAGTACGGTAGAGGGTGGTGGAATTTCCTGTGTAGC 663
Query 662 GGTGAAATGCGTAGATATAGGAAGGAACACCAGTGGCGAAGGCGACCACCTGGACTGATA 721 |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||| Sbjct 664 GGTGAAATGCGTAGATATAGGAAGGAACACCAGTGGCGAAGGCGACCACCTGGACTGATA 723
Query 722 CTGACACTGAGGTGCGAAAGCGTGGGGAGCAAACAGGATTAGATACCCTGGTAGTCCACG 781 |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||| Sbjct 724 CTGACACTGAGGTGCGAAAGCGTGGGGAGCAAACAGGATTAGATACCCTGGTAGTCCACG 783
31
Query 842 ATAAGTCGACCGCCTGGGGAGTACGGCCGCAAGGTTAAAACTCAAATGAATTGACGGGGG 901 |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||| Sbjct 844 ATAAGTCGACCGCCTGGGGAGTACGGCCGCAAGGTTAAAACTCAAATGAATTGACGGGGG 903
Query 902 CCCGCACAAGCGGTGGAGCATGTGGTTTAATTCGAAGCAACGCGAAGAACCTTACCTGGC 961 |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||| Sbjct 904 CCCGCACAAGCGGTGGAGCATGTGGTTTAATTCGAAGCAACGCGAAGAACCTTACCTGGC 963
Query 962 CTTGACATGCTGAGAACTTTCCAGAGATGGATTGGTGCCTTCGGGAACTCAGACACAGGT 1021 |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||| Sbjct 964 CTTGACATGCTGAGAACTTTCCAGAGATGGATTGGTGCCTTCGGGAACTCAGACACAGGT 1023
Query 1022 GCTGCATGGCTGTCGTCAGCTCGTGTCGTGAGATGTTGGGTTAAGTCCCGTAACGAGCGC 1081 |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||| Sbjct 1024 GCTGCATGGCTGTCGTCAGCTCGTGTCGTGAGATGTTGGGTTAAGTCCCGTAACGAGCGC 1083
Query 1082 AACCCTTGTCCTTAGTTACCAGCACCTCGGGTGGGCACTCTAAGGAGACTGCCGGTGACA 1141 |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||| Sbjct 1084 AACCCTTGTCCTTAGTTACCAGCACCTCGGGTGGGCACTCTAAGGAGACTGCCGGTGACA 1143
Query 1142 AACCGGAGGAAGGTGGGGATGACGTCAAGTCATCATGGCCCTTACGGCCAGGGCTACACA 1201 |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||| Sbjct 1144 AACCGGAGGAAGGTGGGGATGACGTCAAGTCATCATGGCCCTTACGGCCAGGGCTACACA 1203
Query 1202 CGTGCTACAATGGTCGGTACAAAGGGTTGCCAAGCCGCGAGGTGGAGCTAATCCCATAAA 1261 |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||| Sbjct 1204 CGTGCTACAATGGTCGGTACAAAGGGTTGCCAAGCCGCGAGGTGGAGCTAATCCCATAAA 1263
Query 1262 ACCGATCGTAGTCCGGATCGCAGTCTGCAACTCGACTGCGTGAAGTCGGAATCGCTAGTA 1321 |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||| Sbjct 1264 ACCGATCGTAGTCCGGATCGCAGTCTGCAACTCGACTGCGTGAAGTCGGAATCGCTAGTA 1323
Query 1322 ATCGTGAATCAGAATGTCACGGTGAATACGTTCCCGGGCCTTGTACACACCGCCCGTCAC 1381 |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||| Sbjct 1324 ATCGTGAATCAGAATGTCACGGTGAATACGTTCCCGGGCCTTGTACACACCGCCCGTCAC 1383
Query 1382 ACCATGGGGAGTGGGTTGCTCCAGAAGTAGCTAGTCTAACCGCAAGGGGG-ACGGTTACC 1440 |||||||||||||||||||||||||||||||||||||||||||||||||| ||||||||| Sbjct 1384 ACCATGGGGAGTGGGTTGCTCCAGAAGTAGCTAGTCTAACCGCAAGGGGGGACGGTTACC 1443
Lampiran 8 Kromatogram hasil identifikasi senyawa ekstrak etil asetat isolat
42.00 Nonanoic acid, ethyl ester (CAS) Ethyl nonanoate
5.60 1-BROMO-2,2-DICHLORO-ETHANE
0.78 Undecane, 2,6-dimethyl- (CAS) 2,6-Dimethylundecane 0.28 Dodecane (CAS) n-Dodecane
0.22 Tetradecane (CAS) n-Tetradecane
0.37 Heptadecane (CAS) n-Heptadecane
0.19 Docosane (CAS) n-Docosane
0.86 Octadecane (CAS) n-Octadecane
0.58 Octadecane (CAS) n-Octadecane
0.46 Hexamethyl-pyranoindane
0.39 Octadecane (CAS) n-Octadecane
0.49 Tetracosanoic acid, methyl ester (CAS) Methyl lignocerate 0.71 Octadecane (CAS) n-Octadecane
1.58 Hexadecanoic acid (CAS) Palmitic acid 1.81 Eicosane (CAS) n-Eicosane
0.43 1,2-Benzenedicarboxylic acid, butyl octyl ester (CAS) 0.22 Hexadecanoic acid, 1-methylethyl ester (CAS) Isopal 0.28 Hexadecane, 2,6,10,14-tetramethyl- (CAS) Phytane
1.27 Docosane (CAS) n-Docosane
0.82 9-Octadecenoic acid (Z)-, methyl ester (CAS) Methyl oleate
0.84 Nonahexacontanoic acid, methyl ester (CAS)
0.59 Nonacosane (CAS) n-Nonacosane 1.84 Docosane (CAS) n-Docosane 0.30 Tricosane (CAS) n-Tricosane 0.32 Octadecane (CAS) n-Octadecane
1.25 TRIACONTANE, 1,30-DIBROMO- 0.32 PALMITIC ACID, N-OCTYL ESTER
1.17 1,2-Benzenedicarboxylic acid, bis(2-ethylhexyl) ester (CAS)
33
RIWAYAT HIDUP
Penulis dilahirkan di Jakarta pada tanggal 22 Agustus 1990 sebagai anak kedua dari pasangan Bambang Dwi Purnomo, M.Pd dan Nyai Wastini, S.Pd. Penulis menyelesaikan pendidikan menengah atas di SMAN 97 Jakarta pada tahun 2008. Penulis meneruskan pendidikan di Program Studi Teknologi Industri Pertanian, Institut Teknologi Indonesia (ITI) dan menyelesaikan jenjang studi S1 pada tahun 2013. Setelah mendapatkan gelar akademik, penulis melanjutkan Program Kursus Pembinaan Profesi Insinyur (KPPI) yang diselenggarakan oleh Persatuan Insinyur Indonesia (PII) dan mendapatkan gelar profesi Insinyur pada tahun 2013. Pada tahun yang sama, penulis melanjutkan studi S2 di Departemen Biokimia Program Pascasarjana, Institut Pertanian Bogor (IPB).
Selama masa perkuliahan di Pascasarjana IPB, penulis juga pernah bekerja sebagai asisten riset di Laboratoria Pengembangan Teknologi Industri Agro dan Biomedika (LAPTIAB) PUSPIPTEK, Serpong. Penulis juga pernah mengikuti pelatihan dan seminar. Tahun 2014 penulis mengikuti kegiatan Pelatihan Pengenalan HACCP SNI CAC/RCP 1:2011 di Laboratorium Terpadu IPB dan Seminar Nasional Biologi Wallacea 2014 di Universitas Mataram, Lombok. Penulis telah mempublikasikan artikel yang berjudul “Isolasi dan Identifikasi Senyawa Antibakteri dari Bakteri Endofit Tumbuhan Nyawai (Ficus variegata
Blume)”. Artikel penelitian ini telah diterima dan akan dipublikasi dalam jurnal