LAPORAN PRAKTEK KERJA PROFESI APOTEKER
DI LEMBAGA FARMASI DIREKTORAT KESEHATAN
ANGKATAN DARAT
BANDUNG
Disusun Oleh :
ELLIYA YUSFITRI, S.Farm 073202124
FAKULTAS FARMASI
UNIVERSITAS SUMATERA UTARA
MEDAN
LEMBAR PENGESAHAN
LAPORAN PRAKTEK KERJA PROFESI APOTEKER
DI LEMBAGA FARMASI DIREKTORAT KESEHATAN ANGKATAN DARAT BANDUNG
Diajukan untuk melengkapi salah satu syarat untuk mencapai gelar Apoteker pada Fakultas Farmasi
Universitas Sumatera Utara
Oleh:
Elliya Yusfitri, S.Farm.
073202124
Disetujui Oleh Pembimbing
Dra. Neneng Cahyati, Apt NIP. 030 183 409
Disahkan Oleh:
Dekan, Kepala Lembaga Farmasi Ditkesad,
KATA PENGANTAR
Puji dan syukur penulis ucapkan kehadirat Tuhan Yang Maha Esa yang telah memberikan rahmat dan karuniaNya sehingga penulis dapat menyelesaikan laporan ini
sebagai hasil Praktek Kerja Profesi Apoteker di Lembaga Farmasi Direktorat Kesehatan Angkatan Darat (Lafi Ditkesad) Bandung, yang dilaksanakan pada tanggal 1 september –
23 September 2008.
Praktek Kerja Profesi di Lembaga Farmasi Direktorat Kesehatan Angkatan Darat dapat memperluas wawasan tentang gambaran sebuah industri farmasi bagaimana cara
mengelola dan manajemen dari suatu industri farmasi.
Pelaksanaan Praktek Kerja Profesi Apoteker ini beserta penyusunan laporannya tidak
terlepas dari dukungan dan bantuan berbagai pihak, untuk itu penulis mengucapkan terima kasih kepada semua pihak yang telah memberikan bantuan, dukungan, petunjuk, bimbingan, saran serta berbagai fasilitas dan kemudahan bagi penulis.
Pada kesempatan ini izinkanlah penulis mengucapkan rasa terima kasih kepada :
1. Bapak Letkol CKM Drs. Sambas Setiawan, Apt, selaku Kepala Lembaga Farmasi Direktorat Kesehatan Angkatan Darat.
2. Bapak Letkol CKM Drs.Yan Suryana Ilham, Apt, M.M selaku kepala Instalasi Penelitian dan Pengembangan Lembaga Farmasi Direktorat Kesehatan Angkatan
Darat.
4. Bapak Mayor CKM Drs. Abdul Azis, MM selaku Kepala Bagian Administrasi dan
Logistik Lembaga Farmasi Direktorat Kesehatan Angkatan Darat.
5. Bapak Mayor CKM Drs. Junaedi, Apt. selaku Lakhar Kepala Instalasi Produksi Lembaga Farmasi Direktorat Kesehatan Angkatan Darat.
6. Ibu Mayor CKM. (K). Dra. Emmy Winarni, Apt. selaku Kepala Instalasi Penyimpanan Lembaga Farmasi Direktorat Kesehatan Angkatan Darat.
7. Bapak Mayor CKM Drs. Agoes Imam Nugroho, Apt. selaku Kepala Instalasi Pemeliharaan Lembaga Farmasi Direktorat Kesehatan Angkatan Darat.
8. Bapak Mayor CKM Drs. T.P. Simorangkir, M.Si., Apt. selaku Koordinator
Mahasiswa Praktek Kerja Profesi di Lembaga Farmasi Direktorat Kesehatan Angkatan Darat dan sebagai Pembimbing.
9. Ibu Dra. Neneng Cahyati, Apt. selaku Kepala Seksi Kemas Instalasi simpan dan sebagai pembimbing.
10. Ibu Dra. Lisa Olii, Apt, M.Si. selaku Wakil Koordinator Mahasiswa Praktek Kerja
Profesi di Lembaga Farmasi Direktorat Kesehatan Angkatan Darat.
11. Ibu Dra. Tuti Sunarti, Apt. selaku Kepala Seksi Sediaan Cair dan Steril Instalasi Produksi dan sebagai pembimbing.
12. Ibu Dra. Weni Widaningsih, Apt. selaku Kepala Seksi Kimia Fisika Instalasi Pengawasan Mutu dan sebagai Pembimbing.
Semoga Tuhan membalas budi baik Bapak dan Ibu dengan balasan yang berlipat
ganda. Penulis berharap semoga tulisan ini dapat memberikan manfaat bagi kita semua.
Bandung, September 2008
DAFTAR ISI
1.2 Metodologi Praktek Kerja Profesi Apoteker ... 3
1.3 Tujuan Praktek Kerja Profesi Apoteker... 3
BAB II TINJAUAN PUSTAKA... 4
2.1 Industri Farmasi ... 4
2.2 Persyaratan Industri Farmasi... 4
2.3 Pencabutan Izin Usaha Industri Farmasi... 5
7. Pengolahan... 15
4. Pengawasan terhadap bahan awal, produk antara, produk ruahan dan produk jadi... 21
5. Produksi-produksi dan perubahannya... 21
6. Peninjauan Catatan Produksi dan Bets Produk . 21 7. Penelitian stabilitas ... 21
8. Penilaian terhadap pemasok... 22
2.4.8 Inspeksi Diri... 22
2.4.9 Penanganan Keluhan Terhadap Obat, Penarikan Kembali Obat dan Obat Kembalian... 22
2.4.10 Dokumentasi ... 23
2.4.11 Pembuatan dan Analisis Berdasarkan Kontrak... 24
2.4.12 Kualifikasi dan Validasi... 24
BAB III TINJAUAN KHUSUS LEMBAGA FARMASI DIREKTORAT KESEHATAN ANGKATAN DARAT ... 27
3.1 Sejarah... 27
3.2 Visi, Misi serta Tujuan... 28
3.3 Kedudukan, Tugas Pokok dan Fungsi Lafi Ditkesad... 28
3.3.1 Tugas melaksanakan Fungsi Utama ... 29
3.3.2 Tugas melaksanakan Fungsi Organik ... 29
3.4 Struktur Organisasi Lafi Ditkesad ... 30
3.4.1 Eselon Pimpinan ... 30
3.4.2 Eselon Pembantu Pimpinan ... 30
3.4.3 Eselon Pelayanan (Seksi Tata Usaha Urusan Dalam)... 31
3.5 Kualifikasi Tenaga Kerja Lafi Ditkesad ... 34
3.6 Sertifikasi CPOB Lafi Ditkesad... 35
3.7 Kegiatan Lafi Ditkesad ... 38
3.7.1 Kegiatan Bagminlog ... 39
3.7.2 Kegiatan Instalasi Pengawasan Mutu ... 40
3.7.3 Kegiatan Instalasi Penelitian dan Pengembangan (Installitbang)... 42
3.7.4 Kegiatan Instalasi Produksi... 43
1. Seksi Sediaan Non Betalaktam ... 44
2. Seksi Sediaan Sefalosporin ... 52
3. Seksi Sediaan Betalaktam ... 52
4. Seksi Kemas... 53
3.7.5 Kegiatan Instalasi Simpan... 53
3.7.6 Kegiatan Instalasi Pemeliharaan dan Sisjang ... 55
3.8 Pengolahan Dokumen ... 61
4.9 Penanganan Keluhan Terhadap Obat, Penarikan Kembali Obat dan Obat Kembalian... 59
4.10 Dokumentasi ... 70
BAB V KESIMPULAN DAN SARAN ... 72
5.1 Kesimpulan ... 72
5.2 Saran ... 73
DAFTAR PUSTAKA... 74
DAFTAR TABEL
Halaman Tabel 1. Data Personil Lafi Ditkesad Bulan September 2008
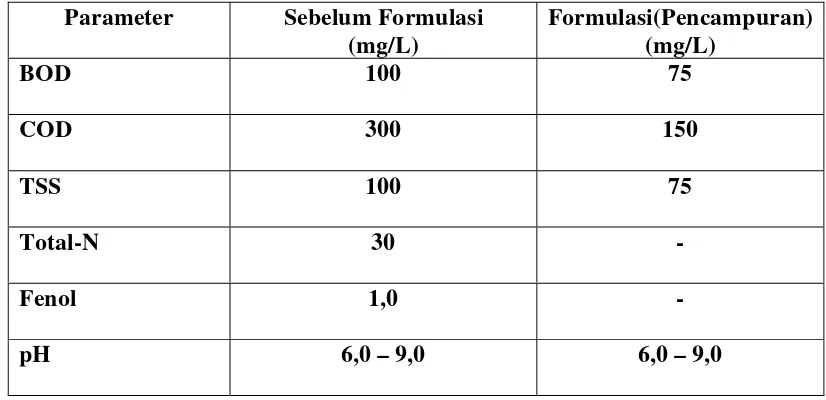
Berdasarkan Jenjang Pendidikannya... 35 2. Baku Mutu Limbah Cair untuk Industri Farmasi
DAFTAR LAMPIRAN
Halaman
Lampiran 1 Struktur Organisasi Lembaga Farmasi Ditkesad Berdasarkan Eselon dan Jabatan (Peraturan Kasad
Nomor Perkasad/219/XII/2007 Tanggal 10-12-2007) ... 75
Lampiran 2 Blanko Hasil Pengujian Laboratorium ... 76
Lampiran 3 Blanko Catatan Pengujian Tablet dan Kapsul ... 77
Lampiran 4 Blanko Laporan Hasil Pengujian Larutan/ Sirup/ Injeksi ... 78
Lampiran 5 Blanko Laporan Hasil Pengujian Salep/ Krim ... 79
BAB I
PENDAHULUAN
1.1 Latar Belakang
Industri farmasi menurut SK Menkes No. 245/Menkes/SK/V/1990 adalah industri
obat jadi dan industri bahan baku obat. Industri obat jadi adalah industri yang memproduksi suatu produk yang telah melalui seluruh tahap proses pembuatan. Obat jadi
ini dapat berupa sediaan atau paduan bahan yang siap digunakan untuk mempengaruhi sistem fisiologi atau keadaan patologi dalam rangka penetapan diagnosa, pencegahan, penyembuhan, pemulihan, peningkatan kesehatan dan kontrasepsi. Industri farmasi
merupakan salah satu tempat dimana apoteker melakukan pekerjaan kefarmasian terutama menyangkut pengadaan, pengolahan dan pengemasan, pengendalian mutu
sediaan farmasi, penyimpanan, pendistribusian dan pengembangan obat.
Sasaran utama industri farmasi adalah memproduksi obat jadi dengan mengutamakan keamanan, keefektifan, kualitas dan harga yang terjangkau oleh
masyarakat. Untuk menghasilkan obat jadi yang memenuhi persyaratan yang telah ditetapkan sesuai dengan tujuan penggunaannya, setiap industri farmasi harus menerapkan CPOB (Cara Pembuatan Obat yang Baik).
Pada saat ini industri farmasi di Indonesia telah menghasilkan berbagai produk obat yang jumlahnya semakin meningkat dan tersebar luas, sehingga diharapkan dapat
menjangkau semua lapisan masyarakat. Industri farmasi bertanggung jawab sepenuhnya dalam menjamin tersedianya produk obat yang memenuhi standar mutu. Oleh karena itu, industri farmasi harus dapat menerapkan Cara Pembuatan Obat yang Baik (CPOB) dalam
No.43/Menkes/SK/II/1988 tentang CPOB, yang kemudian direvisi dengan keputusan
Kepala Badan Pengawasan Obat dan Makanan No:HK.00.05.3.02152 tahun 2001 tentang Penerapan Pedoman Cara Pembuatan Obat yang Baik. Pedoman CPOB hendaklah diperbaiki secara berkesinambungan mengikuti perkembangan ilmu pengetahuan dan
teknologi untuk mengantisipasi era globalisasi dan harmonisasi di bidang farmasi terutama pemenuhan terhadap persyaratan dan standar produk farmasi global terkini.
Oleh karena itu, pedoman CPOB edisi 2001 direvisi kembali menjadi pedoman CPOB yang dinamis edisi tahun 2006, berdasarkan Surat Keputusan Kepala Badan Pengawas Obat dan Makanan No.HK.00.06.0511, tanggal 24 Januari 2006.
Dalam melaksanakan tugas dan tanggung jawabnya di industri farmasi, apoteker sebagai personil yang profesional harus memahami penerapan CPOB disamping adanya
pengetahuan dan keterampilan, baik yang berhubungan dengan kefarmasian ataupun kepemimpinan.
Sebagai upaya untuk memberikan wawasan yang luas tentang industri farmasi bagi
calon apoteker, maka Fakultas Farmasi Universitas Sumatera Utara Medan bekerja sama dengan Lembaga Farmasi Direktorat Kesehatan Angkatan Darat (Lafi Ditkesad) Bandung memberikan kesempatan bagi calon apoteker untuk mengenal lingkungan kerja dan
1.2 Metodologi Praktek Kerja Profesi Apoteker
Metodologi kerja praktek profesi apoteker yang dilakukan di Lembaga Farmasi Direktorat Kesehatan Angkatan Darat adalah :
1. Interaksi langsung mahasiswa dengan pihak-pihak terkait dengan cara melakukan
kunjungan langsung ke instalasi-instalasi di lingkungan Lafi Ditkesad 2. Diskusi dengan para pembimbing dan antar mahasiswa.
3. Belajar mandiri melalui data perpustakaan Lafi Ditkesad, website farmasi, data-data primer dan sekunder lainnya.
4. Pemberian materi oleh masing-masing kepala instalasi di Lafi Ditkesad.
1.3 Tujuan Praktek Kerja Profesi Apoteker
Tujuan praktek kerja profesi apoteker, sebagai berikut:
1. Memahami dan melihat secara langsung gambaran umum tentang kegiatan suatu industri farmasi
2. Mengetahui dan memahami bagaimana pengelolaan industri farmasi secara profesional serta melihat tentang penerapan aspek CPOB di industri farmasi
3. Mengetahui dan memahami tentang tugas dan tanggung jawab serta wewenang
apoteker, sehingga dapat dijadikan bekal guna mempersiapkan diri dalam menghadapi dunia kerja sesungguhnya.
4. Mengetahui perencanaan dan pelaksanaan produksi di industri farmasi khususnya di Lafi Ditkesad yang merupakan perusahaan non profit oriented.
BAB II
TINJAUAN PUSTAKA
2.1 Industri Farmasi
Industri farmasi menurut Surat Keputusan Menteri Kesehatan Republik Indonesia Nomor 245/Menkes/SK/V/1990 adalah industri obat jadi dan industri bahan baku obat.
Industri obat jadi adalah industri yang menghasilkan suatu produk yang telah melalui seluruh tahap proses pembuatan, dimana obat jadi tersebut dapat berupa sediaan atau bahan-bahan yang sering digunakan untuk mempengaruhi atau menyelidiki sistem
fisiologis atau keadaan patologi dalam rangka penetapan diagnosis, pencegahan, penyembuhan, pemulihan, peningkatan kesehatan dan kontrasepsi. Industri bahan baku
adalah industri yang memproduksi bahan baku dimana bahan baku tersebut adalah seluruh bahan, baik berkhasiat ataupun tidak berkhasiat yang digunakan dalam proses pengolahan obat.
2.2 Persyaratan Industri Farmasi
Perusahaan industri farmasi wajib memperoleh izin usaha industri farmasi, karena
itu industri tersebut wajib memenuhi persyaratan yang telah ditetapkan oleh Menteri Kesehatan. Persyaratan industri farmasi tercantum dalam Surat Keputusan Menteri
Kesehatan RI No. 245//Menkes/SK/V/1990 adalah sebagai berikut :
1. Industri farmasi merupakan suatu perusahaan umum, badan hukum berbentuk Perseroan Terbatas atau Koperasi.
3. Memiliki Nomor Pokok Wajib Pajak (NPWP).
4. Industri farmasi obat jadi dan bahan baku wajib memenuhi persyaratan CPOB sesuai dengan ketentuan SK Menteri Kesehatan No. 43/Menkes/SK/II/1988.
5. Industri farmasi obat jadi dan bahan baku, wajib mempekerjakan secara tetap
sekurang-kurangnya dua orang apoteker warga negara Indonesia, masing-masing sebagai penanggung jawab produksi dan penanggung jawab pengawasan mutu sesuai
dengan persyaratan CPOB.
6. Obat jadi yang diproduksi oleh industri farmasi hanya dapat diedarkan setelah memperoleh izin edar sesuai dengan ketentuan perundang-undangan yang berlaku.
Izin usaha industri farmasi diberikan oleh Menteri Kesehatan dan wewenang pemberian izin dilimpahkan kepada Badan Pengawasan Obat dan Makanan (BPOM). Izin
ini berlaku seterusnya selama industri tersebut berproduksi dengan perpanjangan izin setiap 5 tahun, sedangkan untuk industri farmasi Penanaman Modal Asing (PMA) masa berlakunya sesuai dengan ketentuan dalam Undang-Undang No. 1 Tahun 1967 tentang
Penanaman Modal Asing dan pelaksanaannya.
2.3 Pencabutan Izin Usaha Industri Farmasi
Izin usaha industri farmasi dapat dicabut dalam hal:
1. Melakukan pemindah tanganan hak milik izin usaha industri farmasi dan perluasan tanpa memiliki izin.
2. Tidak menyampaikan informasi mengenai perkembangan industri secara
berturut-turut tiga kali atau dengan sengaja menyampaikan informasi yang tidak benar.
4. Dengan sengaja memproduksi obat jadi atau bahan baku obat yang tidak memenuhi
persyaratan dan ketentuan yang berlaku (obat palsu).
5. Tidak memenuhi ketentuan dalam izin usaha industri farmasi.
2.4 Cara Pembuatan Obat yang Baik
Surat Keputusan Menteri Kesehatan No. 245/Men.Kes/SK/V/1990, menjelaskan
bahwa CPOB merupakan syarat wajib untuk memperoleh izin usaha industri farmasi. CPOB harus diterapkan di industri farmasi karena CPOB bertujuan untuk menjamin obat dibuat secara konsisten, memenuhi persyaratan yang ditetapkan dan sesuai dengan tujuan
penggunaannya. CPOB mencakup seluruh aspek produksi dan pengendalian mutu. Pedoman CPOB telah terbit tiga edisi, yaitu pedoman CPOB edisi 1988, 2001, dan
2006. Dibandingkan dengan edisi sebelumnya, Pedoman CPOB edisi 2006 mengandung perbaikan sesuai persyaratan CPOB dinamis, antara lain “ Kualifikasi dan Validasi “, “Pembuatan dan Analisis Obat Berdasarkan Kontrak”, “Pembuatan Produk Steril”, dan
penambahan beberapa bab yaitu “Manajemen Mutu”, “Pembuatan Produk Darah”, “Sistem Komputerisasi”, dan “Pembuatan Produk Investasi untuk UJi Klinis”. Aspek-aspek CPOB 2006 diuraikan di bawah ini.
2.4.1 Manajemen Mutu
Industri farmasi harus memberikan jaminan khasiat, keamanan dan mutu produk
yang dihasilkan agar sesuai dengan tujuan penggunaanya. Manajemen bertanggung jawab untuk mencapai tujuan ini melalui suatu kebijakan mutu dimana diperlukan manajemen mutu yang didesain secara menyeluruh dan diterapkan secara benar.
1. Sistem mutu yang tepat mencakup struktur organisasi, prosedur, proses dan sumber
daya
2. Pemastian Mutu
Pemastian mutu adalah totalitas semua pengaturan yang dibuat dengan tujuan
untuk memastikan bahwa obat dihasilkan dengan mutu yang sesuai dengan tujuan pemakaiannya, karena itu Pemastian Mutu mencakup CPOB ditambah dengan faktor lain
seperti desain dan pengembangan produk.
Cara Pembuatan Obat yang Baik (CPOB) merupakan bagian dari Pemastian Mutu yang memastikan bahwa obat dibuat dan dikendalikan secara konsisten untuk mencapai
standar mutu yang sesuai dengan tujuan penggunaan dan dipersyaratkan dalam izin edar dan spesifikasi produk. CPOB mencakup Produksi dan Pengawasan Mutu.
Pengawasan Mutu berhubungan dengan pengambilan sampel, spesifikasi dan pengujian, organisasi, dokumentasi dan prosedur pelulusan yang memastikan bahwa pengujian yang diperlukan dan relevan telah dilakukan dan bahwa bahan yang belum
diluluskan tidak digunakan serta produk yang belum diluluskan tidak dijual atau dipasok sebelum mutunya dinilai dan dinyatakan memenuhi syarat.
Pengawasan mutu secara menyeluruh mempunyai tugas lain, yaitu menetapkan,
memvalidasi dan menerapkan semua prosedur pengawasan mutu, mengevaluasi, mengawasi dan menyimpan bahan baku pembanding, memastikan kebenaran label wadah
bahan dan produk, memastikan bahwa stabilitas dari zat aktif dan obat jadi dipantau, mengambil bagian dalam investigasi keluhan yang terkait dengan mutu produk, dan ikut mengambil bagian dalam pemantauan lingkungan. Semua kegiatan tersebut hendaklah
mutu hendaklah memiliki akses ke area produksi untuk melakukan pengambilan sampel
dan investigasi bila diperlukan. Pengkajian mutu produk secara berkala biasanya dilakukan tiap tahun dan didokumentasikan dengan mempertimbangkan hasil kajian ulang sebelumnya.
2.4.2 Personalia
Jumlah personil di semua tingkat harus memadai serta memiliki pengetahuan,
keterampilan dan kemampuan yang sesuai dengan tanggung jawabnya. Kesehatan mental dan fisik yang baik harus dimiliki personil agar mampu melaksanakan tugas secara profesional. Selain itu, para personil hendaklah memiliki sikap dan kesadaran tinggi
untuk mewujudkan CPOB. Hal-hal yang harus diperhatikan dalam aspek personalia adalah :
1. Organisasi, kualifikasi, dan tanggung jawab
a. Struktur organisasi perusahaan bagian produksi dan pengawasan mutu harus dipimpin oleh apoteker yang berbeda, yang tidak saling bertanggung jawab satu
dengan yang lain. Keduanya tidak boleh mempunyai kepentingan di luar organisasi perusahaan, yang dapat menghambat atau membatasi tanggung jawabnya.
b. Manajer produksi hendaklah seorang apoteker yang terlatih serta memiliki pengalaman yang memadai, diberikan wewenang dan tanggung jawab penuh
untuk mengelola produksi obat.
jawab penuh dalam penyusunan dan pelaksanaan seluruh prosedur pengawasan
mutu.
d. Manajer produksi dan pengawasan mutu bersama-sama bertanggung jawab dalam penyusunan dan pengesahan prosedur-prosedur tertulis, pemantauan dan
pengawasan lingkungan pembuatan obat, kebersihan pabrik dan validasi proses produksi, kalibrasi alat-alat pengukur, pelatihan personalia, pemberian
persetujuan terhadap pemasok bahan dan kontraktor, pengamanan produk dan bahan terhadap kerusakan serta kemunduran mutu dan dalam penyimpanan dokumen.
e. Tersedianya tenaga yang terampil dalam jumlah memadai untuk melaksanakan supervisi langsung di bagian produksi dan pengawasan mutu obat. Setiap supervisor tersebut hendaklah terlatih dan memiliki keterampilan teknis,
pengalaman dan bertanggung jawab kepada manajer produksi dan pengawasan mutu.
f. Tersedianya tenaga yang terlatih secara teknis dalam jumlah memadai untuk melaksanakan kegiatan produksi dan pengawasan mutu sesuai prosedur dan spesifikasi yang telah ditentukan.
g. Tanggung jawab yang diberikan pada setiap personil hendaklah tidak terlalu berlebihan sehingga dapat menimbulkan resiko terhadap mutu obat.
2. Pelatihan
a. Seluruh personil yang terlibat dalam kegiatan pembuatan obat, hendaklah dilatih mengenai kegiatan yang sesuai dengan tugasnya maupun mengenai prinsip CPOB.
b. Pelatihan hendaklah diberikan oleh orang yang ahli. Perhatian khusus diberikan bagi mereka yang bekerja di daerah steril dan daerah bersih atau yang bekerja
dengan bahan yang beresiko tinggi atau yang menimbulkan sensitifitas.
c. Pelatihan mengenai CPOB dilakukan secara berkesinambungan dengan frekuensi yang memadai untuk menjamin agar personil terbiasa dengan persyaratan CPOB.
d. Pelatihan CPOB dilaksanakan menurut program tertulis yang disetujui oleh manajer produksi dan pengawasan mutu.
e. Catatan pelatihan mengenai CPOB kepada personil hendaklah disimpan dan efektivitas program pelatihan dan prestasi personil hendaklah dinilai secara berkala untuk menentukan apakah mereka telah memiliki kualifikasi yang
memadai untuk melaksanakan tugas yang diberikan.
2.4.3 Bangunan dan Fasilitas
Bangunan untuk pembuatan obat hendaklah memiliki ukuran, rancangan,
konstruksi serta letak yang memadai agar memudahkan pelaksanaan kerja, pembersihan dan pemeliharaan, tiap sarana kerja hendaklah memadai, sehingga setiap resiko terjadi
1. Lokasi bangunan hendaklah dapat mencegah terjadinya pencemaran dari lingkungan
sekelilingnya. Seperti pencemaran udara, tanah dan air maupun kegiatan di sekitarnya.
2. Bangunan dirancang dengan baik sehingga dapat terpelihara dan berfungsi
sebagaimana mestinya
3. Saluran air limbah hendaklah cukup besar dan mempunyai bak kontrol serta ventilasi
yang baik.
4. Tenaga listrik, suhu, kelembaban dan ventilasi harus tepat supaya tidak mengakibatkan dampak yang merugikan baik secara langsung ataupun tidak langsung
terhadap produk selama proses pembuatan dan penyimpanan.
2.4.4 Peralatan
Peralatan yang digunakan dalam pembuatan obat hendaklah memiliki rancangan bangunan dan konstruksi yang tepat, ukuran yang memadai serta ditempatkan dengan tepat sehingga mutu setiap produk obat terjamin secara seragam dari bets ke bets serta
untuk memudahkan pembersihan dan perawatannya
1. Rancang Bangun dan Konstruksi
a. Peralatan yang digunakan tidak bereaksi atau menimbulkan akibat terhadap bahan
yang diolah.
b. Peralatan hendaklah mudah dibersihkan baik bagian dalam maupun bagian
luarnya.
c. Peralatan yang digunakan untuk menimbang, mengukur, menguji dan mencatat hendaklah diperiksa ketelitiannya secara teratur serta ditara menurut program dan
d. Penyaring untuk cairan tidak boleh melepaskan serat ke dalam produk dan tidak
boleh mengandung asbes.
2. Pemasangan dan Penempatan
a. Peralatan hendaklah ditempatkan pada posisi yang tepat untuk memperkecil
pencemaran silang antar bahan.
b. Peralatan ditempatkan dengan jarak yang cukup renggang untuk memberikan
keleluasaan kerja.
c. Peralatan utama diberi nomor pengenal yang dipakai pada semua perintah dan catatan pembuatan betsuntuk menunjukkan unit atau alat tertentu.
d. Semua pipa, tangki, selubung hendaknya diberikan pelekat untuk memperkecil kehilangan energi.
e. Saluran pipa yang menggunakan uap bertekanan hendaknya dilengkapi dengan peralatan uap dan saluran pembuangan yang berfungsi dengan baik.
f. Sistem-sistem penunjang hendaknya divalidasi untuk memastikan fungsinya
sesuai tujuannya.
3. Pemeliharaan
a. Peralatan hendaknya dirawat sesuai jadwal yang tepat agar berfungsi dengan baik
dan mencegah pencemaran.
b. Prosedur-prosedur tertulis untuk peralatan dibuat dan dipatuhi.
c. Catatan pelaksanaan pemeliharaan pemakaian peralatan utama hendaklah dicatat dalam buku harian dan catatan untuk peralatan yang digunakan khusus untuk satu produk saja dapat dimasukkan ke catatan produksi bets produk tertentu.
Tingkat sanitasi dan higiene yang tinggi hendaklah diterapkan pada setiap aspek
pembuatan obat. Ruang lingkup sanitasi dan higiene meliputi personalia, bangunan, peralatan dan perlengkapan, bahan produksi serta wadahnya dan setiap hal yang merupakan sumber pencemaran produk. Sumber pencemaran hendaknya dihilangkan
melalui suatu program sanitasi dan higiene yang menyeluruh dan terpadu.
2.4.6 Produksi
Produksi hendaklah dilaksanakan dengan prosedur yang telah ditetapkan serta dapat menjamin produk obat jadi memenuhi spesifikasi yang ditentukan.
1. Bahan Awal
a. Setiap bahan awal hendaklah memenuhi spesifikasi dan diberi label dengan nama yang dinyatakan dalam spesifikasi sebelum dinyatakan lulus untuk digunakan.
b. Untuk setiap kiriman atau bets hendaklah diberi nomor rujukan yang menunjukkan identitas yang jelas.
c. Saat penerimaan barang selalu dilakukan pemeriksaan visual tentang kondisi
umum dan contoh untuk pengujian yang diambil oleh petugas menggunakan metode yang disetujui oleh manajer pengawasan mutu.
d. Persediaan awal hendaklah diperiksa dalam selang waktu tertentu.
e. Bahan awal yang tidak stabil oleh pengaruh suhu, hendaklah disimpan pada ruangan dengan suhu udara yang dapat diatur.
f. Pengeluaran bahan awal dilakukan oleh petugas yang berwenang.
2. Validasi Proses
a. Semua proses produksi divalidasi dengan tepat serta dilaksanakan sesuai prosedur yang telah ditentukan dan hasilnya disimpan.
b. Sebelum suatu proses pengolahan induk diterapkan hendaklah dilakukan
langkah-langkah untuk membuktikan kecocokan dengan pelaksanaan produksi. c. Perubahan peralatan atau bahan disertai dengan tindakan validasi ulang.
d. Proses dan prosedur yang kritis dievaluasi kembali secara rutin untuk memastikan bahwa proses dan prosedur tersebut tetap mampu memberikan hasil yang diinginkan.
3. Pencemaran
Pencemaran kimiawi atau mikroba terhadap suatu obat yang dapat merugikan
kesehatan atau mengurangi daya terapeutik maupun mempengaruhi kualitas suatu produk, tidak dapat diterima.
4. Sistem Penomoran bets dan Lot
a. Sistem penomoran selanjutnya hendaklah saling berkaitan.
b. Sistem penomoran hendaklah menjamin bahwa nomor tidak digunakan secara berulang.
5. Penimbangan dan Penyerahan
a. Metode penanganan, penimbangan, perhitungan dan penyerahan bahan dan
produk tercakup dalam prosedur tertulis.
c. Pada setiap penimbangan maupun pengukuran hendaklah dilakukan pembuktian
kebenarannya, ketepatan identitas, dan jumlah bahan.
d. Kebersihan tempat penimbangan dan penyerahan bahan ataupun obat hendaklah dijaga.
e. Penimbangan dan penyerahan hendaklah menggunakan peralatan yang cocok dan bersih.
f. Bahan baku produk yang diserahkan hendaknya diperiksa ulang.
6. Pengembalian
Semua bahan yang dikembalikan ke tempat penyimpanan hendaklah
didokumentasikan dengan baik.
7. Pengolahan
a. Semua bahan dan peralatan yang dipakai hendaklah diperiksa terlebih dahulu. b. Semua kegiatan pengolahan hendaklah mengikuti prosedur tertulis yang telah
ditentukan dan penyimpangan dilaporkan dengan alasan dan penjelasan.
c. Wadah dan penutup untuk bahan dan produk hendaklah selalu bersih. d. Seluruh pengawasan dalam proses harus dicatat dengan teliti.
e. Bahan dan produk kering.
Penanganannya menimbulkan masalah debu, oleh karena itu perlu dipasang sistem penghisap debu untuk mencegah penyebarannya. Produk hendaklah
dilindungi dari pencemaran dan jangan sampai ada produk yang tertinggal di dalam peralatan.
Mesin pencampur, pengayak dan pengaduk dilengkapi dengan sistem
pengendalian debu. Parameter operasional tercantum dalam Dokumen Produksi Induk. Bahan yang beresiko tinggi digunakan kantong pelindung. Pada pembuatan dan penggunaan larutan atau suspensi dicegah terjadinya pencemaran
atau pertumbuhan mikroba. g. Pencetakan tablet.
Mesin dilengkapi dengan fasilitas pengendali debu yang memadai, dilakukan pengendalian secara fisik, prosedur dan penandaan untuk menghindari campur aduk antar produk. Tersedianya alat timbang yang telah ditara. Tablet yang
diambil untuk diuji tidak boleh dikembalikan dan tablet yang ditolak atau disingkirkan hendaklah ditempatkan dalam wadah yang ditandai dengan jelas dan
dicatat pada Catatan Pengolahan bets. m. Penyalutan
Udara yang dialirkan disaring dan memiliki mutu yang tepat dan larutan penyalut
digunakan dengan cara yang dapat menekan pertumbuhan jasad renik. n. Pengisian kapsul keras.
Kapsul kosong sebagai bahan awal, disimpan dalam kondisi yang baik.
o. Pemberian tanda tablet bersalut dan kapsul.
Hendaklah dihindari terjadinya campur-baur selama proses pemberian tanda,
p. Produk cair, krim dan salep.
Proses produksi produk cair, krim, dan salep terlindung dari pencemaran. Peralatan yang digunakan dirancang dan dipasang secara tepat sehingga mudah untuk melakukan pembersihan. Kualitas kimiawi dan mikrobiologi air hendaklah
diperiksa pada awal, sesudah penghentian dan pada akhir proses pengisian untuk memastikan homogenitas produk.
8. Produk Steril
a. Cara produksi ada dua kategori yaitu aseptik dan sterilisasi akhir.
b. Semua produk steril dibuat dengan kondisi yang terkendali dan dipantau dengan
teliti, diperlukan tindakan khusus untuk meyakinkan sterilisasi akhir.
c. Untuk membuat produk steril diperlukan ruangan terpisah yang dirancang khusus.
d. Pembuatan produk steril memerlukan tiga kualitas ruangan yang berbeda yaitu ruang ganti pakaian, ruang bersih, dan ruang steril.
e. Kontaminasi jasad renik tidak melebihi nilai batas yang ditentukan.
f. Personalia.
Personil yang bekerja hendaklah dipilih dengan seksama. Standar higiene dan kebersihan perorangan sangat penting. Oleh karena itu semua personil dilatih
dalam bidang yang berkaitan dengan pembuatan produk steril. g. Pakaian.
Personil memakai pakaian khusus untuk daerah bersih dan steril. Pakaian biasa dari luar tidak boleh dibawa ke dalam. Arloji, perhiasan dan kosmetika tidak boleh dipakai dalam ruangan bersih dan steril. Pakaian ditangani dengan cepat
h. Bangunan.
Bangunan untuk ruang steril dirancang khusus, ruangan diberi aliran udara bertekanan positif secara efektif melalui saringan. Permukaan kedap air dan tidak retak. Tidak boleh ada bagian yang dapat terjadi penumpukan debu. Pipa-pipa
dipasang dengan tepat. Saluran pembuangan terpisah dan bak cuci ditiadakan. Dan semua aspek yang memungkinkan pencemaran dihindari.
i. Peralatan dirancang dan dipasang dengan tepat dan mudah dibersihkan.
j. Sterilisasi dapat dilakukan dengan cara panas basah, panas kering, cara radiasi sesuai dengan masing-masing cara yang efektif.
Selain hal-hal di atas, masalah yang perlu diperhatikan adalah masalah air, penyelesaian produk steril, kesiapan jalur pengemasan, pengawasan dalam proses,
pelaksanaan pengemasan, produk pilihan, sisa produk dan obat jadi yang dikembalikan dari gudang pabrik, obat kembalian, karantina obat jadi, pengawasan distribusi, penyimpanan bahan awal, produk antara, ruahan dan obat jadi, penyimpanan bahan baku
dan bahan pengemas, serta penyimpanan produk antara, produk ruahan dan obat jadi. Pembuatan obat berdasarkan kontrak hanya boleh diberikan kepada pabrik yang sudah memiliki sertifikat CPOB dan disertai surat perjanjian yang merinci tugas dan
tanggung jawab masing-masing pihak.
Pembuatan produk steril dilakukan di area bersih yang tingkat kebersihannya
sesuai dengan standar kebersihan dengan udara yang telah melewati filter dengan efisiensi yang sesuai. Pembuatan produk steril dibedakan menjadi 4 kelas :
Zona untuk kegiatan yang beresiko tinggi, misalnya untuk zona pengisian ampul dan
vial terbuka, penyambungan secara aseptik dan wadah tutup karet. Kondisi ini umumnya dicapai dengan memasang Laminar Air Flow (LAF).
2. Kelas B
Untuk pembuatan dan pengisian secara aseptik, kelas ini merupakan latar belakang untuk zona kelas A.
3. Kelas C dan D
Area bersih untuk melakukan tahap pembuatan produk steril dengan tingkat resiko yang lebih rendah.
2.4.7 Pengawasan Mutu
Pengawasan mutu merupakan bagian yang esensial dari cara pembuatan obat yang
baik, agar tiap obat yang dibuat memenuhi persyaratan mutu yang sesuai dengan tujuan penggunaannya. Hal-hal yang perlu dibicarakan dalam pengawasan mutu antara lain : 1. Pengawasan mutu
Pengawasan mutu hendaklah dirancang dengan tepat meliputi semua fungsi analisis yang dilakukan di laboratorium. Sistem dokumentasi dan prosedur hendaklah menjamin bahwa pemeriksaan dilakukan dengan tepat. Tugas pokok pengawasan
mutu meliputi penyusunan prosedur, penyiapan, instruksi, menyusun rencana pengambilan contoh, meluluskan atau menolak bahan-bahan dan produk, meneliti
kembalian, ikut serta dalam program inspeksi diri dan memberikan rekomendasi
untuk pembuatan obat oleh pihak lain atas dasar kontrak. 2. Laboratorium
Laboratorium pengujian meliputi bangunan dan alat-alat penunjang yang lengkap dan
memadai, personalia yang terlatih dan bertanggung jawab, peralatan instrumen yang cocok untuk prosedur dan dikalibrasi secara berkala, pereaksi dan media pembiakan
yang sesuai, baku pembanding resmi yang sesuai dengan monografi yang bersangkutan, spesifikasi dan prosedur pengujian yang divalidasi dengan fasilitas yang digunakan, catatan pengujian yang mencakup seluruh aspek yang diperlukan
dan contoh pertinggal untuk disimpan yang dipergunakan dalam pengujian selanjutnya.
3. Validasi
Bagian pengawasan mutu melakukan validasi terhadap prosedur penetapan kadar dan penerapan alat-alat instrumen yang ada, serta memberi bantuan dalam pelaksanaan
validasi di bagian produksi.
4. Pengawasan terhadap bahan awal, produk antara, produk ruahan dan obat jadi, diperhatikan dalam hal spesifikasi, cara pengambilan contoh, pengujian terhadap
bahan baku, pengemas, produk antara, produk ruahan dan obat jadi. Uji sterilitas untuk produk steril, uji pirogenitas serta pengawasan lingkungan secara berkala
terhadap mutu kimiawi dan mikrobiologi dari air dan lingkungan produksi. 5. Produksi-produksi dan perubahannya
Bagian pengawasan mutu ikut serta dalam pembuatan prosedur pengolahan induk dan
6. Peninjauan catatan produksi dan bets produk
Semua catatan produksi dan pengawasan tiap bets dilakukan oleh bagian pengawasan mutu dan bets yang menyimpang diselidiki secara tuntas.
7. Penelitian stabilitas
Penelitian dirancang untuk mengetahui stabilitas dari produk, dan program ini dipatuhi mencakup jumlah, kondisi penyimpanan dan metode pengujian. Penelitian
stabilitas dilakukan terhadap produk baru, kemasan baru, perubahan formula dan bets yang telah diluluskan.
8. Penilaian terhadap pemasok
Bagian pengawasan mutu bertanggung jawab menentukan pemasok yang dipercaya, yang sebelumnya dievaluasi dan diinspeksi bersama oleh bagian pengawasan mutu,
bagian produksi dan bagian pembelian secara berkala.
2.4.8 Inspeksi Diri
Tujuan inspeksi diri adalah untuk melakukan penilaian apakah seluruh aspek
produksi dan pengendalian mutu memenuhi standar CPOB. Program inspeksi diri dirancang untuk mendeteksi kelemahan dalam pelaksanaan CPOB dan untuk menetapkan tindakan perbaikan yang diperlukan. Inspeksi diri dilakukan secara indepeden dan dirinci
oleh petugas yang kompeten dari perusahaan. Inspeksi diri dilakukan secara rutin dan disamping itu pada situasi khusus, misalnya dalam hal terjadi penarikan kembali obat jadi
atau terjadi penolakan yang berulang. Prosedur dan catatan inspeksi diri hendaklah didokumentasikan dan dibuat program tindak lanjut yang efektif.
Inspeksi meliputi personil, bangunan, penyimpanan, bahan awal, obat jadi,
2.4.9 Penanganan Keluhan Terhadap Obat dan Penarikan Kembali Obat Serta
Obat Kembalian
Penarikan kembali obat adalah suatu proses penarikan kembali dari satu atau beberapa bets atau seluruh bets obat tertentu dari peredaran. Penarikan kembali obat
dilakukan apabila ditemukan obat yang cacat mutu atau bila ada laporan mengenai reaksi yang merugikan yang serius serta beresiko terhadap kesehatan. Obat kembalian adalah
obat jadi yang beredar yang kemudian dikembalikan ke pabrik pembuatnya karena adanya keluhan, kerusakan, kadaluwarsa, masalah keabsahan atau sebab-sebab lain mengenai kondisi obat, wadah atau kemasan sehingga menimbulkan keraguan akan
keamanan, khasiat atau mutu obat.
Semua keluhan dan informasi lain yang berkaitan dengan kemungkinan terjadi
kerusakan obat hendaklah dikaji dengan teliti sesuai dengan prosedur tertulis. Untuk menangani semua kasus yang mendesak, hendaklah disusun suatu sistem, bila perlu mencakup penarikan kembali produk yang diketahui atau diduga cacat dari peredaran
secara cepat dan efektif.
2.4.10 Dokumentasi
Dokumentasi adalah seluruh prosedur, instruksi dan catatan yang berhubungan
dengan proses pembuatan Obat. Fungsi dokumentasi adalah: 1. Merupakan bagian dari sistem manajemen mutu dalam c-GMP
2. Memastikan bahwa setiap petugas mendapat instruksi secara rinci dan jelas mengenai bidang tugas yang harus dilaksanakan
3. Menggambarkan riwayat lengkap dari setiap bets/lot produk sehingga menjamin
Dokumentasi pembuatan obat merupakan bagian dari sistem informasi
manajemen yang meliputi spesifikasi bahan baku, bahan pengemas, produk antara, produk ruahan dan obat jadi, dokumen dalam produksi, dokumen dalam pengawasan mutu, dokumen dalam penyimpanan dan distribusi, dokumen dalam pemeliharaan,
pembersihan dan pengendalian ruangan dan peralatan, dokumen dalam penanganan keluhan obat yang ditarik kembali, obat kembalian dan pemusnahan bahan baku obat dan
obat jadi, dokumen untuk peralatan khusus, prosedur dan catatan tentang inspeksi diri, pedoman dan catatan tentang pelatihan CPOB bagi personil.
2.4.11 Pembuatan dan Analisis Berdasarkan Kontrak
Pembuatan analisis berdasarkan kontrak harus dibuat secara benar, disetujui dan dikendalikan untuk menghindari kesalahpahaman yang dapat menyebabkan produk atau
pekerjaan dengan mutu yang tidak memuaskan. Kontrak tertulis antara pemberi Kontrak dan Penerima Kontrak harus dibuat secara jelas menentukan tanggung jawab dan kewajiban masing-masing pihak. Kontrak harus menyatakan secara jelas prosedur
pelulusan tiap bets produk untuk diedarkan yang menjadi tanggung jawab penuh kepala bagian Manajemen Mutu (Pemastian Mutu). Hal – hal yang harus diperhatikan dari pembuatan dan analisis berdasarkan kontrak, yaitu :
1. Hendaklah dibuat kontrak tertulis yang meliputi pembuatan dan/atau analisis obat yang dikontrakkan dan semua pengaturan teknis terkait.
3. Kontrak hendaklah mengizinkan Pemberi Kontrak untuk mengaudit sarana dari
Penerima Kontrak.
4. Dalam hal analisis berdasarkan kontrak, pelulusan akhir harus diberikan oleh kepala bagian Manajemen Mutu (Pemastian Mutu) Pemberi Kontrak
2.4.12 Kualifikasi dan Validasi
1. Perencanaan Validasi adalah sebagai berikut :
a. Seluruh kegiatan validasi hendaklah direncanakan. Unsur utama program validasi hendaklah dirinci dengan jelas dan didokumentasikan di dalam Rencana Induk Validasi (RIV) atau dokumen setara.
b. RIV hendaklah merupakan dokumen yang singkat, tepat dan jelas. c. RIV hendaklah mencakup sekurang-kurangnya data sebagai berikut:
1) Kebijakan validasi.
2) Struktur organisasi kegiatan validasi.
3) Ringkasan fasilitas, sistem, peralatan dan proses yang akan divalidasi.
4) Format dokumen, format protokol dan laporan validasi, perencanaan dan jadwal pelaksanaan.
5) Pengendalian perubahan, dan
6) Acuan dokumen yang digunakan.
d. RIV terpisah mungkin diperlukan untuk suatu proyek besar.
2. Kualifikasi terdiri dari : a. Kualifikasi Desain
Kualifikasi Desain adalah unsur pertama dalam melakukan validasi terhadap
b. Kualifikasi Instalasi
Kualifikasi Instalasi hendaklah dilakukan terhadap fasilitas, sistem dan peralatan baru atau yang dimodifikasi.
c. Kualifikasi Operasional
Kualifikasi Operasional hendaklah dilakukan setelah Kualifikasi Instalasi selesai dilaksanakan, dikaji dan disetujui.
d. Kualifikasi Kinerja
BAB III
TINJAUAN KHUSUS LEMBAGA FARMASI
DIREKTORAT KESEHATAN ANGKATAN DARAT
3.1. Sejarah Perkembangan Lafi Ditkesad
Lembaga Farmasi Direktorat Kesehatan Angkatan Darat (Lafi Ditkesad) berasal
dari MSL (Militaire Scheikundig Laboratorium). Lembaga ini berfungsi sebagai tempat pemeriksaan obat-obatan bagi kebutuhan tentara Belanda.
Pada tanggal 23 Januari 1950 dibentuk panitia pengalihan, sehingga pada tanggal
1 Juni 1950 dilakukan serah terima dari MSL kepada TNI AD yang menjadi dasar dalam penetapan hari jadi Lafi Ditkesad melalui SK No. Kep/23/I/1997 tanggal 31 Januari 1997.
Setelah serah terima pada tanggal 1 Juni 1950 MSL terbagi menjadi dua :
1. Laboratorium Kimia Tentara (LKT) yang kemudian berkembang menjadi Laboratorium Kimia Angkatan Darat (LKAD).
2. Depot Obat Tentara Pusat (DOTP) yang berkembang menjadi Depot Obat Angkatan Darat (DOAD).
Berdasarkan SK Ditkesad No. Kpts/61/10/IX/1960 tanggal 13 September 1960
terhitung mulai tanggal 8 Juni 1960 LKAD dan DOAD disatukan menjadi Lembaga Farmasi Angkatan Darat (LAFIAD). Pada tanggal 15 Oktober 1970 LAFIAD dipisah
kembali menjadi :
2. Depot Obat Angkatan Darat (DOAD) berkembang menjadi Depot Alat Peralatan
Kesehatan (Dopalkes) dan berakhir menjadi Depot Pusat Perbekalan Kesehatan (Dopusbekkes) Jankesad
Selanjutnya tahun 1985 antara Lafi Jankesad dan Dopusbekkes Jankesad disatukan
kembali menjadi Lafi Ditkesad hingga 31 Maret 2005 dan mulai 1 April 2005 dipisah lagi menjadi Lafi Ditkesad dan Gudang Pusat II Ditkesad.
3.2 Visi dan Misi LAFI DITKESAD
Visi Lafi Ditkesad adalah menjadi satu-satunya lembaga produksi yang mampu
memenuhi kebutuhan obat yang bermutu bagi TNI AD. Lafi Ditkesad mempunyai misi sebagai berikut :
1. Mampu memenuhi kebutuhan obat TNI AD 2. Pusat litbang dan informasi obat TNI AD.
3. Mampu menjadi mitra industri farmasi lain dalam memenuhi kebutuhan obat
nasional.
3.3 Kedudukan, Tugas Pokok dan Fungsi Lafi Ditkesad
Lembaga Farmasi Direktorat Kesehatan Angkatan Darat (Lafi Ditkesad) adalah badan pelaksana di tingkat Ditkesad yang berkedudukan langsung di bawah Direktur
Dalam melaksanakan tugas pokok tersebut Lafi Ditkesad menyelenggarakan
tugas-tugas sebagai berikut :
3.3.1 Tugas dalam melaksanakan fungsi utama
1. Penelitian dan Pengembangan; meliputi segala usaha, pekerjaan, kegiatan di bidang
penelitian dan pengembangan produk, sistem metode dan personel dalam rangka penyelenggaraan produksi obat.
2. Produksi; meliputi segala usaha, pekerjaan dan kegiatan di bidang produksi obat 3. Pengawasan mutu; meliputi segala usaha, pekerjaan dan kegiatan pemeriksaan fisika,
kimia, mikrobiologi, terhadap bahan baku, bahan pendukung produksi, pengawasan
selama proses, produk antara, produk ruahan dan produk jadi.
4. Pemeliharaan; meliputi segala usaha, pekerjaan, kegiatan di bidang pemeliharaan dan
perbaikan peralatan produksi, pengawasan mutu dan sistem penunjang.
5. Penyimpanan; meliputi segala usaha, pekerjaan, dan kegiatan di bidang penerimaan, penyimpanan dan pengeluaran bahan baku, bahan pendukung produksi, peralatan dan
obat jadi.
3.3.2 Tugas Melaksanakan Fungsi Organik
1. Fungsi Organik Militer
Meliputi segala usaha, pekerjaan dan kegiatan di bidang intelijen, operasi, personil, logistik, teritorial, perencanaan dan pengawasan serta pemeriksaan dalam rangka
mendukung tugas pokok LAFI Ditkesad. 2. Fungsi Organik Pembinaan
Meliputi segala usaha, pekerjaan dan kegiatan di bidang latihan kesatuan dalam
3.4 Struktur Organisasi Lafi Ditkesad
Peraturan Kepala Staf TNI AD No. Perkasad/219/XII/2007 tanggal 10 Desember 2007 tentang organisasi dan tugas Lafi Ditkesad telah mengalami perkembangan mengenai struktur organisasi yang bertujuan untuk lebih mengoptimalkan
kinerja personil dalam menghadapi kemajuan ilmu pengetahuan dan teknologi. Struktur organisasi Lafi Ditkesad dapat dilihat pada lampiran 1. Susunan organisasi adalah
sebagai berikut:
3.4.1 Eselon Pimpinan
1. Kepala Lembaga Farmasi, disingkat Kalafi
Kalafi dijabat oleh seorang Pamen TNI Angkatan Darat berpangkat Letnan Kolonel CKM, dalam melaksanakan tugas kewajibannya bertanggung jawab kepada
Direktur Kesehatan Angkatan Darat.
2. Wakil Kepala Lembaga Farmasi, disingkat Wakalafi
Wakalafi dijabat oleh seorang Pamen TNI Angkatan Darat, berpangkat Letnan
Kolonel CKM, dalam melaksanakan tugas kewajibannya bertanggung jawab kepada Kalafi.
3.4.2 Eselon Pembantu Pimpinan
1. Perwira Ahli Lembaga Farmasi, disingkat Pa ahli Lafi
Pa Ahli Lafi dijabat oleh Pamen TNl Angkatan Darat berpangkat Letnan Kolonel
CKM, dalam melaksanakan tugas kewajibannya bertanggung jawab kepada Kalafi. Pa Ahli terdiri dari:
a. Perwira Ahli Madya Manajemen Mutu, disingkat Paahli Madya Jemen Mutu.
c. Perwira Ahli Madya Analisa Mengenai Dampak Lingkungan, disingkat Paahli
Madya Amdal.
2. Bagian Administrasi Logistik, disingkat Bagminlog.
Kabagminlog dijabat oleh Pamen TNI Angkatan Darat berpangkat Letnan
Kolonel CKM, dalam pelaksanaaan tugas kewajibannya bertanggung jawab kepada Kalafi. Kabagminlog dalam melaksanakan tugasnya dibantu oleh dua kepala seksi
yang masing-masing dijabat oleh Pamen TNI Angkatan Darat berpangkat Mayor CKM, terdiri dari:
a. Kepala Seksi Perencanaan Program dan Anggaran, disingkat Kasirengarprogar.
b. Kepala Seksi Pengendalian Materil, disingkat Kasidalmat.
3.4.3 Eselon Pelayanan (Seksi Tata Usaha dan Urusan Dalam, disingkat Si TUUD)
Kasi TUUD dijabat oleh seorang Pamen TNI Angkatan Darat berpangkat Mayor CKM dalam melaksanakan tugas kewajibannya bertanggung jawab kepada Kalafi. Kasi TUUD dalam melaksanakan tugasnya dibantu oleh tiga kepala urusan yang
masing-masing dijabat oleh Pama TNI Angkatan Darat berpangkat Kapten CKM dan PNS golongan tiga serta satu perwira urusan yang dijabat oleh Pama TNI Angkatan Darat berpangkat Letnan CKM terdiri dari:
1. Kepala Urusan Administrasi Personil dan Logistik, disingkat Kaurminperslog. 2. Kepala Urusan Tata Usaha, disingkat Kaurtu.
3. Kepala Urusan Dalam, disingkat Kaurdal. 4. Perwira Urusan Pengamanan, disingkat Paurpam.
3.4.4 Eselon Pelaksana
KaInstallitbang dijabat oleh seorang Pamen TNI Angkatan Darat berpangkat Letnan
Kolonel CKM, dalam melaksanakan tugasnya dibantu oleh dua Kepala Seksi yang masing-masing dijabat oleh Pamen TNI Angkatan Darat berpangkat Mayor CKM, terdiri dari:
a. Kepala Seksi Penelitian dan Pengembangan Produksi, disingkat Kasilitbangprod.
b. Kepala Seksi Penelitian dan Pengembangan Sistem Metode dan Personel, disingkat Kasilitbangsistodapers.
KaInstallitbang dalam pelaksanaan tugas kewajibannya bertanggung jawab kepada
Kalafi.
2. Instalasi Produksi, disingkat Instalprod.
KaInstalprod dijabat oleh seorang Pamen TNI Angkatan Darat berpangkat Letnan Kolonel CKM (Berkualifikasi Apoteker), dalam pelaksanaan tugas kewajibannya bertanggung jawab kepada Kalafi. Ka Instalprod dalam melaksanakan tugasnya
dibantu oleh empat Kepala Seksi yang masing-masing dijabat oleh Pamen TNI Angkatan Darat berpangkat Mayor CKM, terdiri dari:
a. Kepala Seksi Sediaan Non Betalaktam, disingkat Kasidia Non Betalaktam
b. Kepala Seksi Sediaan Betalaktam, disingkat Kasidia Betalaktam c. Kepala Seksi Sediaan Sefalosforin disingkat Kasidia Sefalosforin.
d. Kepala Seksi Kemas, disingkat Kasi Kemas. 3. Instalasi Pengawasan Mutu, disingkat Instal wastu
KaInstal wastu dijabat oleh seorang Pamen TNI Angkatan Darat berpangkat Letnan
Seksi yang masing-masing dijabat oleh Pamen TNI Angkatan Darat berpangkat
Mayor CKM, terdiri dari:
a. Kepala Seksi Pengujian Kimia, Fisika dan mikrobiologi, disingkat Kasiuji Kifis dan Mikro
b. Kepala Seksi Inspeksi, disingkat Kasiinspek.
KaInstal wastu dalam pelaksanaan tugas kewajibannya bertanggung jawab
kepada Kalafi.
4. Instalasi Pemeliharaan dan sistem penunjang, disingkat Instalhar dan Sisjang.
Kainstalhar dan Sisjang dijabat oleh Pamen TNI Angkatan Darat berpangkat Mayor
CKM yang dalam melaksanakan tugasnya dibantu oleh dua Kepala Urusan yang masing-masing dijabat oleh Pama TNI Angkatan Darat berpangkat Kapten CKM,
terdiri dari:
a. Kepala Urusan Pemeliharaan, disingkat Kaurhar.
b. Kepala Urusan Sistem Penunjang, disingkat Kaursisjang.
Kainstalhar dan Sisjang dalam pelaksanaan tugas kewajibannya bertanggung jawab kepada Kalafi.
5. Instalasi Simpan, disingkat Instal simpan
Kainstalsimpan di.jabat oieh Pamen TNI Angkatan Darat berpangkat Mayor CKM, dalam melaksanakan tugasnya dibantu oleh satu Kepala Urusan yang dijabat oleh
Pama TNI Angkatan Darat berpangkat Kapten CKM dan satu Perwira Urusan yang dijabat oleh Pama TNI Angkatan Darat berpangkat Letnan CKM, terdiri dari:
a. Kepala Urusan Penyimpanan Material Produksi, disingkat Kaur simpanmatprod.
Kainstalsimpan dalam pelaksanaan tugas kewajibannya bertanggung jawab kepada
Kalafi.
3.5 Kualifikasi Tenaga Kerja Lafi Ditkesad
Berdasarkan statusnya, personil Lafi Ditkesad terdiri dari militer dan Pegawai Negeri Sipil (PNS). Adapun data personil Lafi Ditkesad Bulan Februari 2009 berdasarkan
jenjang pendidikannya dapat dilihat pada Tabel 1.
Tabel 1. Data Personil Lafi Ditkesad Bulan September 2008 Berdasarkan Jenjang Pendidikannya.
No Kualifikasi Militer PNS Jumlah
1 S2 Farmasi 2 1 3
2 S2 Manajemen 1 - 1
3 Apoteker 7 3 10
4 S1 Kimia / Sarjana lain-lain 5 3 8
5 Sarjana Muda Kimia 1 - 1
6 D3 Analisis Medis / Kesehatan 2 1 3
7 Asisten Apoteker 2 6 8
8 Analis - 2 2
9 Perawat Umum/Bidan 1 - 1
10 Perawat Veteriner - - -
11 STM Alkes - 2 2
12 SLTA (SMA, SMEA, STM) 21 75 96
14 SD - 3 3
Jumlah 44 111 155
3.6 Sertifikasi CPOB Lafi Ditkesad
Lembaga Farmasi Angkatan Darat merupakan salah satu badan pelaksana di
tingkat Ditkesad yang bertugas melaksanakan fungsi penelitian, pengembangan dan produksi obat-obatan, yang mengharuskan lembaga ini mengikuti peraturan pemerintah
melalui keputusan MenKes RI No. 43/MenKes/SK/II/1988 tentang Cara Pembuatan Obat Yang Baik yang mengharuskan seluruh industri farmasi melaksanakan seluruh kegiatan sesuai dengan tuntunan CPOB.
Dengan pertimbangan efisiensi dan efektifitas maka dimulailah pembangunan gedung baru di Jl. Gudang Utara No. 26 Bandung dengan rancang bangun sesuai CPOB
dan perkembangan teknologi di bidang industri farmasi. Pembangunan gedung baru ini dilaksanakan setelah Rencana Induk Pembangunan (RIP) dalam rangka sertifikasi CPOB Lafi Ditkesad mendapatkan persetujuan dari Dirjen POM Depkes RI dengan surat
keputusan No. 02.01.2.4.96.665 tanggal 28 Februari 1996.
Pembangunan dan pekerjaan yang sudah dilaksanakan Lafi Ditkesad pada saat ini
adalah : 1. Bangunan
a. Bangunan Instalasi Produksi Betalaktam.
d. Fasilitas sumber air PDAM dan air baku farmasi untuk seluruh kebutuhan
Instalasi Produksi (Betalaktam dan non Betalaktam), Instalasi Pengawasan Mutu dan perkantoran.
e. Fasilitas gardu listrik mencakup seluruh kebutuhan Instalasi Produksi, Instalasi
Pengawasan Mutu dan perkantoran.
f. Fasilitas Instalasi Pengolahan Air Limbah (IPAL) yang mampu mengolah limbah
pabrik.
g. Unit ketel uap yang mencakup kebutuhan seluruh pabrik.
h. Kompresor udara bertekanan yang mampu mendukung seluruh kebutuhan pabrik.
i. Air Handling System (AHS) untuk unit produksi Betalaktam, ruang laboratorium mikrobiologi dan Instalasi Pengawasan Mutu dan sebagian unit produksi Non
Betalaktam sudah terpasang dan memenuhi syarat CPOB. 2. Peralatan
Peralatan untuk Betalaktam, sebagian non Betalaktam dan Instalasi Pengawasan Mutu
sudah terpasang dan memenuhi syarat CPOB. 3. Dokumen Prosedur Tetap (Protap)
Dokumen protap untuk sediaan Betalaktam dan non Betalaktam yang telah dibuat
sudah dilaksanakan sesuai aturan CPOB 4. Pelatihan CPOB
Pelatihan CPOB umum dan khusus baik untuk Betalaktam dan Non Beta laktam telah dilaksanakan secara berkala.
Sertifikasi CPOB yang telah diterima oleh Lafi Ditkesad sampai bulan Februari 2007
ditujukan untuk sediaan Betalaktam dan non Betalaktam. a. Sertifikat CPOB untuk Sediaan Betalaktam :
1) Tablet antibiotika turunan Penisilin.
Kaplet Amoxicillin 500 mg dan Ampicillin 500 mg 2) Tablet salut antibiotika turunan Penisilin
Amoxicillin 500 mg dan Ampicillin 500 mg
3) Kapsul keras antibiotika turunan Penisilin
Ampicillin 250 mg dan Amoxicillin 250 mg 4) Suspensi kering oral antibiotika turunan Penisilin
Sirup kering Ampicillin 125 mg dan Amoxicillin 125 mg 5) Serbuk steril injeksi antibiotika turunan Penisilin
Amoxicillin dan Ampicillin.
b. Sertifikat CPOB untuk Sediaan non Betalaktam : 1) Tablet biasa non antibiotik
Fimol 500 mg, Dexamethason, Lafihistin, Lafimag, Lafiten, Neuralgad
2) Tablet salut non antibiotik Imodiad, Neurobiad, Buscofiad
3) Kapsul keras non antibiotik Yaitu Sangobiad
4) Sirop oral non antibiotik
5) Cairan obat luar non antibiotik
Lafiodin 15 mL dan Lafiodin 1 L
Sertifikasi ini merupakan pengakuan Badan Pengawas Obat dan Makanan yang berlaku selama industri menjalankan prinsip CPOB yang telah ditetapkan.
3.7 Kegiatan Lafi Ditkesad
Kegiatan Lafi Ditkesad dalam melaksanakan tugas dan fungsi produksi obat-obatan meliputi perencanaan dan pengadaan barang, penyimpanan barang, proses produksi, pengawasan mutu, penelitian dan pengembangan, pemeliharaan dan kegiatan
administrasi.
3.7.1 Kegiatan Bagian Administrasi dan logistik (Bagminlog)
Perencanaan dan pengadaan barang untuk produksi obat Lafi Ditkesad dilakukan berdasarkan data dari Sub Direktorat Pembinaan Pelayanan Kesehatan (Subditbinyankes) yang disusun berdasarkan masukan pola penyakit dari daerah dan laporan dari
masing-masing Kesehatan Daerah Militer (Kesdam), Satuan Kesehatan (Satkes) dan Rumah Sakit Pusat Angkatan Darat (RSPAD). Rencana pengadaan obat kemudian dibuat dengan melakukan penyesuaian antara daftar kebutuhan obat dengan anggaran yang tersedia dan
selanjutnya dianalisa dan dievaluasi oleh Subditbinyankes yang dilakukan setahun sebelum pelaksanaan.
Surat Keputusan Kasad No. Skep/336/X/2005 tanggal 17 Oktober 2005 tentang Pengadaan Barang/Material dan Jasa di Lingkungan Angkatan Darat mengatur tata cara pengadaan obat yang dilakukan dengan cara pembuatan obat jadi dan produksi di Lafi
terdiri dari rencana kebutuhan bahan aktif, bahan pembantu dan bahan pengemas
(embalage). Perencanaan tersebut disusun berdasarkan formula dan spesifikasi obat yang telah ditentukan oleh Lafi Ditkesad, disamping itu Bagminlog juga menyusun rencana dan anggaran untuk pemeliharaan sarana operasional yang digunakan di tiap instalasi
atau bagian di Lafi Ditkesad.
Pengadaan barang dilakukan oleh Ditkesad melalui panitia pengadaan atau lelang,
kemudian Dirkesad membentuk tim komisi penerimaan barang yang bertugas memeriksa keadaan barang secara administrasi dan fisik, uji kimia dan uji mutu dilakukan oleh Instal Wastu setelah barang lulus uji mutu maka dibuat Laporan Hasil Pengujian (LHP) dan
Berita Acara (BA) penerimaan. Bila barang yang dikirimkan tidak sesuai dengan spesifikasi diminta atau tidak memenuhi syarat, maka barang akan dikembalikan untuk
diganti, kemudian barang yang lolos administrasi dan uji mutu dikirim ke Gudang Pusat II yang disertai dengan surat Perintah Penerimaan Material (PPnM).
3.7.2 Kegiatan Instalasi Pengawasan Mutu (Instal wastu)
Pengawasan mutu merupakan bagian integral dari suatu produksi obat. Instal wastu bertanggung jawab terhadap setiap hal yang menyangkut kualitas bahan baku obat, bahan pembantu, bahan pengemas, produk antara, produk ruahan, dan obat jadi yang dihasilkan
sampai dengan pemantauan kualitas setelah didistribusikan (dengan standar waktu kadaluarsa). Instal wastu juga bertanggung jawab terhadap kualitas lingkungan kerja
yang menyangkut pengawasan bangunan, ruangan dan peralatan serta fasilitas penunjang lainnya seperti pemeriksaan kualitas udara, pengendalian mutu air dan pemeriksaan limbah. Pelaksanaan kegiatan di Instal wastu ditunjang oleh fasilitas Instrumen HPLC,
(pembaca jumlah bakteri), Climatic Chamber, Dissolution Tester serta berbagai fasilitas
penunjang lainnya.
Dalam menjalankan tugasnya, Instal wastu didukung oleh personel yang terdiri dari apoteker dan analis yang terlatih dan berpengalaman dalam menjalankan tugasnya.
Kegiatan Instal wastu tersebut dilaksanakan pada tahap persiapan, selama proses produksi dan setelah proses produksi.
Beberapa kegiatan Instal wastu diantaranya:
1. Menyiapkan metode pemeriksaan, pengujian dan validasi metoda analisa yang sesuai dengan acuan standar resmi seperti Farmakope Indonesia.
2. Menyiapkan prosedur pengambilan sampel untuk pemeriksaan dan pengujian, dimana setiap sampel yang diambil dicatat dan didokumentasikan.
3. Menyiapkan dan menyimpan baku pembanding kerja untuk pengujian.
4. Menyimpan contoh pertinggal obat jadi dan bahan baku serta Catatan Pengujian atau Pemeriksaan.
5. Meluluskan atau menolak bahan yang akan digunakan dalam produksi meliputi bahan baku obat, bahan baku pembantu dan embalage. Hasilnya dapat dicatat pada Laporan Hasil Pengujian (Laporan Hasil Pengujian dapat dilihat pada Lampiran 2).
6. Melaksanakan In Process Control (IPC) selama proses produksi dan memberikan keputusan atas diluluskan atau tidaknya hasil suatu tahap produksi sampai hasil
produk akhirnya.
7. Melaksanakan pengujian terhadap hasil jadi suatu sediaan yang diperoleh. Dicatat pada Catatan Pengujian sediaan jadi (Blanko Hasil Pengujian Laboratorium dapat
8. Meneliti dokumen produksi (Catatan Pengolahan Bets dan Catatan Pengemasan Bets)
sebelum obat diluluskan.
9. Melaksanakan uji stabilitas dipercepat untuk menetapkan kondisi penyimpanan dan masa edar suatu produk.
10.Membantu pelaksanaan validasi proses produksi.
11.Memantau stabilitas produk-produk yang telah dikeluarkan atau didistribusikan
sampai beberapa waktu setelah batas kadaluarsa terutama untuk sediaan antibiotika. 12.Hasil pengujian laboratorium yang dilaksanakan diringkas, dicatat dan
didokumentasikan dalam lembaran yang disebut Laporan Hasil Pengujian.
3.7.3 Kegiatan Instalasi Penelitian dan Pengembangan (Installitbang)
Dalam menjalankan perannya Installitbang melakukan penelitian terhadap produk
baru dan pengembangan produk lama untuk memperoleh kualitas yang lebih baik. Pelaksanaan kegiatan dimulai dengan pengajuan rencana penelitian dan pengembangan produk Lafi Ditkesad yang meliputi :
1. Membuat spesifikasi teknis bahan baku obat, bahan pembantu dan bahan pengemas (embalage).
2. Mencari dan meneliti formula yang dapat dikembangkan sebagai produk Lafi
Ditkesad.
3. Merevisi ulang suatu formula yang sudah ditetapkan bila suatu saat terjadi perubahan
alat, bahan baku dan komponen produksi lainnya.
Penelitian dan pengembangan dimulai dari penelusuran pustaka, pengadaan bahan,
penelitian skala laboratorium dan skala produksi, selanjutnya dilakukan validasi proses produksi dan pengawasan mutu dengan kerjasama antara Insproduksi dan Instal wastu.
3.7.4 Kegiatan Instalasi Produksi (Instalprod)
Kegiatan produksi obat-obatan dilaksanakan oleh Instalprod yang meliputi perencanaan, pengaturan, pelaksanaan dan pengendalian. Produk yang dihasilkan oleh
Lafi Ditkesad berupa produk Betalaktam dan produk non Betalaktam, dimana masing-masing produk dikerjakan pada gedung yang berbeda. Pada Instalprod terdapat empat seksi yaitu: seksi non Betalaktam, seksi sediaan Betalaktam, dan seksi kemas.
Masing-masing seksi dikepalai oleh seorang Apoteker.
Obat-obat yang diproduksi oleh Lafi Ditkesad tidak diperdagangkan bagi
masyarakat umum, dan belum memiliki nomor registrasi, namun demikian proses produksinya tetap dilaksanakan sesuai dengan Pedoman CPOB yang dikeluarkan oleh Badan POM.
Rencana produksi dibuat berdasarkan pada banyaknya jenis obat yang diminta, jenis peralatan yang dimiliki (kapasitas dan spesifikasi mesin), jumlah sumber daya manusia dan jam kerja serta waktu produksi yang tersedia.
Seluruh proses produksi yang dilaksanakan, dicatat dan didokumentasikan dalam Catatan Pengolahan Bets dan Catatan Pengemasan Bets (Batch Record) yang disusun
oleh tim CPOB dan disetujui oleh Kainstal prod dan Kainstal wastu, kemudian didistribusikan dan didokumentasikan. Hal yang diuraikan dalam catatan pengolahan bets dan catatan pengemasan bets adalah kode produk, nama produk, nomor bets, besar bets,
Selain itu dalam catatan pengolahan bets diuraikan mengenai komposisi,
spesifikasi, peralatan, penimbangan bahan dan prosedur pengolahan. Pada catatan pengemasan bets di cantumkan tentang penerimaan bahan pengemas, prosedur pengemasan primer, prosedur pengemasan sekunder dan pelulusan oleh pengawasan
mutu.
Proses produksi dimulai dari penimbangan bahan baku yang akan digunakan dan
dikeluarkan dari Instalsimpan berdasarkan catatan pengolahan bets dan catatan pengemasan bets untuk setiap produk. Barang yang telah dikeluarkan dari Ins. Simpan selanjutnya memasuki tahap pengolahan pada masing-masing seksi produksi, yaitu seksi
sediaan non Betalaktam atau seksi sediaan Betalaktam.
Berikut ini adalah uraian mengenai proses produksi pada masing-masing seksi
yang ada di Instalasi Produksi :
1. Seksi Sediaan Non Betalaktam (Sidia Non Betalaktam)
Seksi sediaan Non Betalaktam adalah seorang Apoteker yang bertanggung jawab
kepada Kepala Instalasi produksi. Pada seksi ini memproduksi obat-obatan yang terdiri dari: sediaan tablet, sediaan kapsul dan sediaan sirup kering, salep dan sirup basah
a. Sediaan Tablet
Pembuatan tablet meliputi kegiatan pencampuran, granulasi, pengeringan,
Tablet merupakan sediaan padat kompak yang dibuat secara kempa cetak dalam
bentuk tabung pipih atau sirkuler, kedua permukaan rata atau cembung, mengandung satu jenis bahan obat atau lebih dengan atau tanpa zat tambahan. Peralatan yang digunakan oleh seksi sediaan padat untuk pembuatan tablet
diantaranya adalah mesin pembuat mucilago dengan energi panas dari uap, mesin pencampur basah sekaligus campur kering, oven pengering, granulator, mesin
cetak tablet, mesin salut film serta mesin strip tablet.
Metoda pembuatan tablet yang biasa digunakan adalah metoda cetak langsung dan metoda granulasi basah. Tablet yang diproduksi adalah tablet biasa dan tablet
salut
Alur proses produksi tablet di Lafi Ditkesad dengan menggunakan metoda
granulasi basah dimulai dengan urutan sebagai berikut: 1) Penimbangan bahan baku
Bahan yang ditimbang diambil dari Instalasi simpan. Bahan yang dibawa ke
ruang timbang hanya boleh terbungkus oleh kemasan primernya, sedangkan kemasan sekundernya tidak disertakan. Proses penimbangan dilakukan di ruang kelas III. Ruang timbang dilengkapi dengan dust collector dan meja
timbang yang kuat dan tahan getar. Bahan baku yang akan digunakan adalah bahan baku yang sudah dinyatakan lulus.
2) Proses pencampuran bahan berkhasiat dengan fase dalam
Bahan berkhasiat dicampurkan dengan fase dalam, diaduk sampai homogen. Pada pencampuran ini yang harus diperhatikan adalah waktu pencampuran
3) Proses pembuatan bahan pengikat (mucilago)
Bahan pengikat ini harus dibuat baru dengan menambahkan air pada bahan pengikat contohnya Amylum, lalu dipanaskan Kemudian dilakukan pengadukan sampai terbentuk massa bening. Pembuatan mucilago ini
dilakukan di dalam tangki pemanas double jacket. 4) Proses granulasi basah
Pada proses granulasi ditambahkan sejumlah bahan pengikat (mucilago) ke dalam hasil campuran zat berkhasiat dengan fase dalam dan diaduk hingga homogen sampai terbentuk massa yang dapat dikepal. Proses granulasi ini
dilakukan didalam Mixer Planetary. 5) Proses pengeringan
Massa yang diperoleh dikeringkan pada suhu 600C, sampai terbentuk massa setengah kering (tergantung jenis tablet yang dibuat).
6) Proses pengayakan
Massa setengah kering diayak dengan ayakan mesh tertentu tergantung dari jenis dan ukuran tablet yang akan dibuat. Hasil pengayakan disebut dengan granul setengah kering.
7) Pada granul dilakukan IPC yang meliputi pemeriksaan kadar air granul 8) Proses pembuatan massa cetak
Setelah granul lulus pemeriksaan uji mutu dibuat massa cetak yaitu dengan penambahan bahan pelincir dan bahan pengembang luar. Diaduk sampai homogen.
Sebelum proses pencetakan, dilakukan IPC terhadap massa cetak yang
meliputi pemeriksaan homogenitas dan kadar zat aktif. 10) Proses pencetakan
Pencetakan tablet dilakukan sesuai dengan ukuran diameter dan berat tablet.
11) Pengawasan mutu (In process control)
Sebelum dikemas, dilakukan pemeriksaan keseragaman bobot, kekerasan,
kerapuhan, dan kadar zat aktif. 12) Proses penyalutan
Jika tablet memerlukan penyalutan maka dapat dilakukan penyalutan dengan
mencampurkan larutan penyalut dengan tablet jadi. 13) Proses penyetripan
Setelah tablet selesai dicetak atau disalut (untuk tablet salut) maka dilakukan proses pengemasan primer yakni proses penyetripan (stripping).
14) Pengawasan mutu (In process control)
Pada hasil penyetripan dilakukan uji mutu (IPC) meliputi tes kebocoran strip. Tablet yang telah lulus uji mutu siap dikemas dan dikirim ke Instalasi simpan.
Untuk pembuatan tablet metode cetak langsung, dimulai dari proses penimbangan bahan baku, selanjutnya mengikuti proses pencampuran massa cetak sampai
dengan proses penyetripan dan pengemasan tanpa melalui proses granulasi. b. Sediaan Kapsul
Ruang produksi kapsul terdiri dari ruang pencampuran, ruang pengisian dan
kapsul diantaranya adalah mesin pencampur, mesin pengisi kapsul, mesin polishing dan mesin strip.
Alur proses produksi kapsul terdiri dari tahapan sebagai berikut: 1) Penimbangan bahan baku
Penimbangan bahan baku antara lain penimbangan bahan aktif, bahan pengisi, bahan pelincir dilakukan oleh personil Instalsimpan.
2) Pencampuran/granulasi
Proses pencampuran dilakukan hingga seluruh bahan yang dicampurkan homogen. Bahan yang diisikan ke dalam kapsul ada yang harus digranulasi
terlebih dahulu untuk memperbaiki sifat alirnya, sedangkan untuk bahan yang tidak digranulasi langsung diisikan pada cangkang kapsul.
3) Pengawasan mutu
Hasil pencampuran massa kapsul dilakukan IPC oleh Instal wastu yang meliputi pemeriksaan homogenitas kadar zat aktifnya.
4) Pengisian kapsul
Setelah massa kapsul diluluskan oleh Instal wastu maka massa kapsul diisikan ke dalam cangkang kapsul. Selama pengisian harus diperhatikan
suhu dan kelembaban ruangan. 5) Polishing
Polishing dilakukan untuk menghilangkan debu yang masih menempel pada dinding luar kapsul.
Pemeriksaan dilakukan pada hasil pengisian ke dalam cangkang kapsul yang
meliputi pemeriksaan kadar zat aktif, keseragaman bobot, uji waktu hancur dan uji disolusi.
7) Stripping
Proses stripping kapsul sama dengan proses stripping pada tablet. 8) Pengawasan mutu
Pada hasil stripping dilakukan tes kebocoran strip. Kapsul yang telah di strip siap untuk dikemas dan dikirim ke Instalsimpan.
c. Sirup Kering
Alur proses produksi sirup kering hampir sama dengan alur proses produksi tablet, yang membedakan hanya pada proses pencetakan, stripping dan
pengemasan. d. Sediaan Salep
Ruang produksi salep terdiri dari ruang pencampuran dan ruang pengisian.
Peralatan yang digunakan antara lain mesin peleleh basis (Double Jacket), mesin pencampur salep dan mesin pengisi-penutup salep otomatis.
Alur proses produksi salep terdiri dari tahapan sebagai berikut:
1) Penimbangan bahan baku
Penimbangan bahan baku dilakukan di ruang kelas III, oleh personil instalasi
simpan.
2) Pelelehan basis
Basis dilelehkan pada tangki pemanas double jacket, disaring kemudian
3) Pencampuran
Bahan basis yang telah dilelehkan lalu dicampur dengan zat aktif dan diaduk terus sampai homogen pada suhu 400C di dalam Homomixer.
4) Pengawasan mutu
Pada hasil proses pencampuran dilakukan uji mutu (IPC) terhadap homogenitas, pH dan kadar zat aktif.
5) Pengisian tube
Setelah lulus uji mutu, massa salep diisikan ke dalam tube dengan suhu yang terjaga sekitar 400C.
6) Pengawasan mutu
Pada hasil pengisian dilakukan uji mutu (IPC) untuk diperiksa keseragaman
isi tube dengan cara menimbang tube satu persatu yang dilakukan setiap 15 menit selain itu juga dilakukan uji mutu (IPC) yang meliputi pemeriksaan pH, massa salep dan kadar zat aktif tiap tube. Setelah lulus uji mutu, tube
siap dikemas dan dikirim ke Ins.simpan. e. Sediaan Sirup
Ruang produksi sirup merupakan ruang kelas III yang terdiri dari ruang
pencampuran, ruang pengisian, ruang pencucian alat. Peralatan yang digunakan antara lain mixer, tangki pemanas (double jacket), filter, drum stainless, mesin
pengisi sirup, penutup botol dan pemasangan etiket yang merupakan satu rangkaian (In Line Process).