ANALISIS KANDUNGAN TIMBAL (Pb) DAN KADMIUM (Cd) PADA KANGKUNG AIR (Ipomoea aquatica Forssk) DAN KANGKUNG
DARAT (Ipomoea reptans Poir) DI DAERAH MABAR-KIM SECARA SPEKTROFOTOMETRI SERAPAN ATOM
SKRIPSI
OLEH: ARISA DIAN SARI
NIM 091524048
PROGRAM EKSTENSI SARJANA FARMASI FAKULTAS FARMASI
UNIVERSITAS SUMATERA UTARA MEDAN
ANALISIS KANDUNGAN TIMBAL (Pb) DAN KADMIUM (Cd) PADA KANGKUNG AIR (Ipomoea aquatica Forssk) DAN KANGKUNG
DARAT (Ipomoea reptans Poir) DI DAERAH MABAR-KIM SECARA SPEKTROFOTOMETRI SERAPAN ATOM
SKRIPSI
Diajukan untuk Melengkapi Salah Satu Syarat untuk Memperoleh Gelar Sarjana Farmasi pada Fakultas Farmasi
Universitas Sumatera Utara
OLEH: ARISA DIAN SARI
NIM 091524048
PROGRAM EKSTENSI SARJANA FARMASI FAKULTAS FARMASI
PENGESAHAN SKRIPSI
ANALISIS KANDUNGAN TIMBAL (Pb) DAN KADMIUM (Cd) PADA KANGKUNG AIR (Ipomoea aquatica Forssk) DAN KANGKUNG
DARAT (Ipomoea reptans Poir) DI DAERAH MABAR-KIM SECARA SPEKTROFOTOMETRI SERAPAN ATOM
OLEH: ARISA DIAN SARI
NIM 091524048
Dipertahankan di Hadapan Panitia Penguji Skripsi Fakultas Farmasi
Universitas Sumatera Utara Pada tanggal: Juli 2011
Pembimbing I, Panitia Penguji,
Dra. Tuty Roida Pardede, M.Si., Apt. Drs. Chairul Azhar Dalimunthe, M.Sc., Apt. NIP 195401101980032001 NIP 194907061980021001
Pembimbing II, Dra. Tuty Roida Pardede, M.Si., Apt. NIP 195401101980032001
Drs. Fathur Rahman Harun, M.Si., Apt. Drs. Maralaut Batubara, M.Phill., Apt. NIP 195201041980031002 NIP 195101311976031003
Dra. Sudarmi, M.Si., Apt. NIP 195409101983032001
Dekan,
KATA PENGANTAR Bismillahirrahmanirrahiim,
Puji syukur penulis ucapkan kepada Allah SWT atas segala limpahan
rahmat dan karunia-Nya, sehingga penulis dapat menyelesaikan penelitian dan
penyusunan skripsi ini, serta shalawat beriring salam untuk Rasulullah
Muhammad SAW sebagai suri tauladan dalam kehidupan.
Skripsi ini disusun untuk melengkapi salah satu syarat mencapai gelar
Sarjana Farmasi pada Fakultas Farmasi Universitas Sumatera Utara, dengan judul
”Analisis Kandungan Timbal (Pb) dan Kadmium (Cd) pada Kangkung Air (Ipomoea aquatica Forssk) dan Kangkung Darat (Ipomoea reptans Poir) di Daerah Mabar-KIM Secara Spektrofotometri Serapan Atom”.
Pada kesempatan ini dengan segala kerendahan hati penulis mengucapkan
terima kasih yang sebesar-besarnya kepada:
1. Ayahanda Drs.H.M.Rasyid dan Ibunda Hj.Syafrida Lubis serta Adik dan Ferry
Fadli yang selalu mendo’akan dan memberikan motivasi.
2. Ibu Dra.Tuty Roida Pardede, M.Si., Apt dan Drs. Fathur Rahman Harun, M.Si.,
Apt yang telah membimbing dan memberikan petunjuk serta saran-saran
selama penelitian hingga selesainya skripsi ini.
3. Bapak Prof. Dr. Sumadio Hadisahputra., Apt selaku Dekan Fakultas Farmasi
USU Medan, yang telah memberikan bantuan dan fasilitas selama masa
pendidikan.
4. Bapak Drs. Chairul Azhar D., M.Sc., Apt., Ibu Dra.Sudarmi, M.Si., Apt dan
Bapak Drs. Maralaut Batubara, M.Phill., Apt., selaku dosen penguji yang telah
5. Bapak Drs, Panal Sitorus, M.Si., Apt selaku penasihat akademik yang telah
memberikan bimbingan kepada penulis selama masa perkuliahan.
6. Ibu Dra. Masfria, M.Si, Apt selaku Kepala Laboratorium Kimia Farmasi
Kualitatif Farmasi USU yang telah memberikan izin dan fasilitas untuk penulis
sehingga dapat mengerjakan dan menyelesaikan penelitian.
7. Bapak Emil Salim selaku Operator Laboratorium Majelis Ulama Indonesia
(MUI) Kota Medan yang telah memberikan fasilitas kepada penulis selama
melaksanakan penelitian.
8. Sahabat-sahabatku sari, dewi, oliv dan teman-teman seperjungan dinda, ade,
liana, kak afni, sri, serta teman-teman Farmasi Ekstensi 2009 terima kasih
untuk perhatian, semangat, doa, dan kebersamaannya selama ini.
10.Serta seluruh pihak yang telah ikut membantu penulis namun tidak tercantum
namanya.
Penulis menyadari sepenuhnya bahwa dalam penulisan skripsi ini masih
jauh dari kesempurnaan, oleh karena itu dengan segala kerendahan hati, penulis
menerima kritik dan saran demi kesempurnaan skripsi ini.
Akhirnya, penulis berharap semoga skripsi ini dapat memberi manfaat
bagi kita semua.
Medan, Juli 2011
Penulis
ANALISIS KANDUNGAN TIMBAL (Pb) DAN KADMIUM (Cd) PADA KANGKUNG AIR (Ipomoea aquatica Forssk) DAN KANGKUNG
DARAT (Ipomoea reptans Poir) DI DAERAH MABAR-KIM SECARA SPEKTROFOTOMETRI SERAPAN ATOM
ABSTRAK
Kangkung merupakan jenis sayuran yang banyak dikonsumsi oleh masyarakat dan sayuran ini merupakan sumber vitamin A yang sangat baik. Kawasan Industri Medan seperti di daerah Mabar, banyak masyarakat menanam berbagai jenis sayuran, diantaranya adalah sayur kangkung. Banyaknya industri di sekitar pertanian penduduk tersebut sayuran ini dikhawatirkan telah terpapar oleh logam timbal dan kadmium. Tujuan dari penelitian ini yaitu untuk mengetahui kadar logam Pb dan Cd pada tanaman kangkung air dan kangkung darat yang ditanam disekitar Mabar Kawasan Industri Medan ( KIM ).
Analisis kedua logam ini dilakukan secara kualitatif dan kuantitatif. Analisis kualitatif menggunakan pereaksi dithizon 0,005% b/v pada pH yang berbeda, di mana akan terbentuk warna merah tua untuk logam Pb pada pH 8 dan warna merah muda untuk logam Cd pada pH 12. Analisis kuantitatif kedua logam di lakukan dengan menggunakan metode Spektrofotometri Serapan Atom pada panjang gelombang yang berbeda. Logam Pb di ukur pada panjang gelombang 283,3 nm dan logam Cd di ukur pada panjang gelombang 228,8 nm. Konsentrasi logam di tentukan dengan metode Least Square.
Hasil analisis di peroleh kadar logam Pb pada kangkung air dan kangkung darat masing-masing sebesar 6,8500 ± 0,3905 µg/g dan 4,2322 ± 0,2928 µg/g, sedangkan kadar logam Cd pada kangkung air dan kangkung darat masing-masing sebesar 1,3004 ± 0,0024 µg/g dan 1,1948 ± 0,0103 µg/g.
Kadar cemaran timbal dan kadmium di dalam kedua sampel ini melebihi batas maksimum yang diperbolehkan berdasarkan SNI No.7387-2009. Batas maksimum cemaran logam berat yang diperbolehkan dalam sayuran adalah 0,5 µg/g untuk timbal dan 0,2 µg/g untuk kadmium. Uji validasi yang dilakukan terhadap metode yang dipakai memberikan hasil perolehan kembali yaitu 98,18% dengan Relatif Standar Deviasi (RSD) 1,32%. Ini menunjukkan metode ini memberikan akurasi dan presisi yang baik dengan batas deteksi (LOD) 0,40 µg/g dan batas kuantitasi (LOQ) 1,34 µg/g.
LEAD (Pb) AND CADMIUM (Cd) CONTENT ANALYSES OF WATER KANGKUNG ( Ipomoea aquatica Forssk ) AND LAND
KANGKUNG ( Ipomoea reptans Poir ) IN MABAR-KIM BY ATOMIC ABSORBTION SPECTROPHOTOMETRY
ABSTRACT
Kangkung is a kind of vegetables that is commonly consumed by people and it contains a lot of vitamin A. Surrounding the Industry Area in Medan such as Mabar, vegetables are planted by people, one of them is kangkung. Since the industries growth in the area of the vegetables are expanded, it is wondered that the kangkung has been contaminated by lead and cadmium metals. The purpose of this research is to know the lead and cadmium metals of water kangkung and land kangkung planted in Mabar the Industries Area of Medan.
The analyses to the both of metals are applied qualitatively and quantitatively. The qualitative analysis uses dithizon reagent 0.005% b/v of different pH, it conduces dark red color of Pb on pH 8 and light red color of Cd on pH 12. The quantitative analysis of the metal is applied by using Atomic Absorbtion Spectrophotometry of different length. Pb is measured in wave-length 283.3 nm and Cd that of 228.8 nm. Metal consentration is determined by using Least Square method.
The result of analyses show that lead metal of water kangkung and land kangkung are 6.8500 ± 0.3905 µg/g and 4.2322 ± 0.2928 µg/g, meanwhile the cadmium metal of water kangkung and land kangkung are 1.3004 ± 0.0024 µg/g and 1.1948 ± 0.0103 µg/g.
The level of contaminated water kangkung and land kangkung by lead and cadmium metals are over maximum level allowed by SNI No. 7387-2009. The maximum metal limit of contaminated vegetables is allowed 0.5 µg/g for lead and 0.2 µg/g for cadmium. Validation test of the method applied shows the recovery result 98.18% and Standard Deviation Relativity (RSD) 1.32%. It shows that the method applied is fine and precisely accurate by the Limit of Detection (LOD) 0.40 µg/g and Limit of Quantitation (LOQ) 1.34 µg/g.
DAFTAR ISI
Halaman
JUDUL ... i
HALAMAN PENGESAHAN ... iii
KATA PENGANTAR ... iv
ABSTRAK ... vi
ABSTRACT ... vii
DAFTAR ISI ... viii
DAFTAR TABEL ... xii
DAFTAR GAMBAR ... xiii
DAFTAR LAMPIRAN ... xiv
BAB I PENDAHULUAN ... 1
1.1. Latar Belakang ... 1
1.2 Perumusan Masalah ... 3
1.3 Hipotesis ... 3
1.4 Tujuan Penelitian ... 4
1.5 Manfaat Penelitian ... 4
BAB II TINJAUAN PUSTAKA ... 5
2.1 Uraian Tanaman ... 5
2.2 Logam Berat ... 6
2.3 Cemaran Logam Berat ... 6
2.4 Toksisitas Logam Berat ... 7
2.5 Timbal ... 7
2.5.2 Toksisitas Timbal ... 8
2.6 Kadmium ... 9
2.6.1 Penggunaan Kadmium ... 9
2.6.2 Toksisitas Kadmium ... 10
2.7 Spektrofotometri Serapan Atom ... 10
2.7.1 Teori Spektrofotometri Serapan Atom ... 10
2.7.2 Instrumen Spektrofotometer Serapan Atom ... 11
2.7.3 Gangguan Pada Spektrofotometer Serapan Atom ... 13
2.8 Validasi metode Analisis ... 14
2.8.1 Kecermatan ( Akurasi ) ... 14
2.8.2 Ketepatan ( Presisi ) ... 15
2.8.3 Batas Deteksi dan Batas Kuantitasi ... 15
BAB III METODE PENELITIAN ... 16
3.1 Lokasi dan Waktu Penelitian ... 16
3.2 Bahan-bahan ... 16
3.3 Alat-alat ... 16
3.4 Pembuatan pereaksi ... 17
3.4.1 Larutan HNO3 5 N ... 17
3.4.2 Larutan Dithizon 0,005% b/v ... 17
3.4.3 Larutan NH4OH 1 N ... 17
3.5 Rancangan Penelitian ... 17
3.5.1 Sampel ... 17
3.5.1.1 Pengambilan Sampel ... 17
3.5.2 Penyiapan Sampel ... 18
3.5.3 Proses Destruksi Logam Timbal dan Kadmium ... 18
3.5.3.1 Proses Dekstruksi Basah ... 18
3.6 Pemeriksaan Kualitatif ... 18
3.6.1 Pemeriksaan Kualitatif untuk Timbal ... 18
3.6.2 Pemeriksaan Kualitatif untuk Kadmium ... 19
3.7 Pemeriksaan Kuantitatif ... 19
3.7.1 Penentuan Linieritas Kurva Kalibrasi Timbal ... 19
3.7.2 Penentuan Linieritas Kurva kalibrasi Kadmium ... 19
3.7.3 Penetapan Kadar Logam Pb dan Cd pada Sampel ... 20
3.7.4 Perhitungan Kadar Logam Pb dan Cd dalam Sampel ... 20
3.8 Analisa Data Secara Statistik ... 21
3.8.1 Uji Penolakan Hasil Analisis ... 21
3.8.2 Rata-rata Kadar logam Pb dan Cd dalam Sampel ... 22
3.8.3 Pengujian Beda Nilai Rata-rata Kadar logam Pb dan Cd pada Sampel ... 22
3.9 Uji ketepatan(Recovery Test) ... 23
3.9.1 Prosedur Uji perolehan kembali (Recovery) ... 23
3.9.2 Uji Ketelitian ... 24
3.9.3 Penentuan Limit of Detection (LOD) and Limit of Quantitation (LOQ) ... 25
BAB IV HASIL DAN PEMBAHASAN ... 26
4.1 Pemeriksaan Kualitatif ... 26
4.2 Pemeriksaan Kuantitatif ... 27
4.3 Analisis Kadar Logam Pb dan Cd pada Sampel ... 28
4.4 Pengujian Beda Nilai Rata-Rata Kadar Logam Pb dan Cd pada Sampel ... 29
4.5 Uji Ketepatan dan Ketelitian ... 30
4.6 Batas Deteksi (LOD) dan Batas Kuantitasi (LOQ) ... 31
BAB V KESIMPULAN DAN SARAN ... 32
5.1 Kesimpulan ... 32
5.2 Saran ... 32
DAFTAR PUSTAKA ... 33
DAFTAR TABEL
Halaman Tabel 1. Hasil Uji Kualitatif Logam Pb dan Cd dalam Sampel dengan Pereaksi
Dithizon 0,005 % b/v ... 26
Tabel 2. Data Kadar Logam Pb dan Cd pada Kangkung Air dan Kangkung Darat ... 29
Tabel 3. Hasil Uji Ketepatan (% Uji Perolehan Kembali (recovery)) dan
DAFTAR GAMBAR
Halaman
Gambar 1. Kurva Kalibrasi Larutan Baku Pb ... 27
DAFTAR LAMPIRAN
Halaman
Lampiran 1 Flowsheet Proses Dekstruksi Basah ... 35
Lampiran 2. Hasil Pengukuran Absorbansi Larutan Standar Timbal (Pb), Perhitungan Persamaan Garis Regresi dan Koefesien Korelasi (r) dari Data Kalibrasi Pb ... 36
Lampiran 3. Hasil Pengukuran Absorbansi Larutan Standar Kadmium (Cd), Perhitungan Persamaan Garis Regresi dan Koefesien Korelasi (r) dari Data Kalibrasi Cd .. ... 38
Lampiran 4. Hasil Analisis Logam Pb dan Cd dan Kadar Sebenarnya pada Sampel Kangkung Darat dan Kangkung Air ... 40
Lampiran 5. Contoh Perhitungan Kadar Timbal dalam Sampel Kangkung Darat ... 41
Lampiran 6. Contoh Perhitungan Kadar Kadmium dalam Sampel Kangkung Darat ... 42
Lampiran 7. Perhitungan Statistik Kadar Logam Timbal pada Kangkung Darat ... 43
Lampiran 8. Perhitungan Statistik Kadar Logam Timbal pada Kangkung Air ... 45
Lampiran 9. Perhitungan Statistik Kadar Logam Kadmium pada Kangkung Darat ... 47
Lampiran 10. Perhitungan Statistik Kadar Logam Kadmium pada Kangkung Air ... 49
Lampiran 11. Pengujian beda Nilai Rata-rata Kadar Logam Pb antara Kangkung Darat dan Kangkung Air ... 51
Lampiran 12. Pengujian Beda Nilai Rata-rata Kadar Logam Cd antara Kangkung Darat dan Kangkung Air ... 53
Lampiran 13. Contoh perhitungan Uji Perolehan Kembali untuk Pb ... 55
Lampiran 14. Contoh perhitungan Uji Perolehan Kembali untuk Cd ... 56
Lampiran 15. Data % Recovery Logam Timbal pada Kangkung Darat ... 57
Lampiran 17. Perhitungan Relatif Standar Deviasi (%RSD) Timbal
Kangkung Darat ... 58
Lampiran 18. Perhitungan Relatif Standar Deviasi (%RSD) Kadmium Kangkung Darat ... 58
Lampiran 19. Perhitungan Limit of Detection (LOD) dan Limit of Quantitation (LOQ) Timbal ... 59
Lampiran 20. Perhitungan Limit of Detection (LOD) dan Limit of Quantitation (LOQ) Kadmium ... 60
Lampiran 21. Hasil Identifikasi Kangkung Air ... 61
Lampiran 22. Hasil Identifikasi kangkung Darat ... 62
Lampiran 23. Daftar Tabel Konsentrasi dan Absorbansi Pb dan Cd dari Kurva Kalibrasi ... ... 63
Lampiran 24. Gambar Lokasi Pengambilan Kangkung Air ... 64
Lampiran 25. Gambar Lokasi Pengambilan Kangkung Darat ... 64
Lampiran 26. Gambar Alat Spektrofotometer Serapan Atom ... 65
Lampiran 27. Gambar hasil Uji Kualitatif Pb dan Cd pada Kangkung Darat dan Kangkung Air ... 66
Lampiran 28. Nilai Distribusi t ... 67
ANALISIS KANDUNGAN TIMBAL (Pb) DAN KADMIUM (Cd) PADA KANGKUNG AIR (Ipomoea aquatica Forssk) DAN KANGKUNG
DARAT (Ipomoea reptans Poir) DI DAERAH MABAR-KIM SECARA SPEKTROFOTOMETRI SERAPAN ATOM
ABSTRAK
Kangkung merupakan jenis sayuran yang banyak dikonsumsi oleh masyarakat dan sayuran ini merupakan sumber vitamin A yang sangat baik. Kawasan Industri Medan seperti di daerah Mabar, banyak masyarakat menanam berbagai jenis sayuran, diantaranya adalah sayur kangkung. Banyaknya industri di sekitar pertanian penduduk tersebut sayuran ini dikhawatirkan telah terpapar oleh logam timbal dan kadmium. Tujuan dari penelitian ini yaitu untuk mengetahui kadar logam Pb dan Cd pada tanaman kangkung air dan kangkung darat yang ditanam disekitar Mabar Kawasan Industri Medan ( KIM ).
Analisis kedua logam ini dilakukan secara kualitatif dan kuantitatif. Analisis kualitatif menggunakan pereaksi dithizon 0,005% b/v pada pH yang berbeda, di mana akan terbentuk warna merah tua untuk logam Pb pada pH 8 dan warna merah muda untuk logam Cd pada pH 12. Analisis kuantitatif kedua logam di lakukan dengan menggunakan metode Spektrofotometri Serapan Atom pada panjang gelombang yang berbeda. Logam Pb di ukur pada panjang gelombang 283,3 nm dan logam Cd di ukur pada panjang gelombang 228,8 nm. Konsentrasi logam di tentukan dengan metode Least Square.
Hasil analisis di peroleh kadar logam Pb pada kangkung air dan kangkung darat masing-masing sebesar 6,8500 ± 0,3905 µg/g dan 4,2322 ± 0,2928 µg/g, sedangkan kadar logam Cd pada kangkung air dan kangkung darat masing-masing sebesar 1,3004 ± 0,0024 µg/g dan 1,1948 ± 0,0103 µg/g.
Kadar cemaran timbal dan kadmium di dalam kedua sampel ini melebihi batas maksimum yang diperbolehkan berdasarkan SNI No.7387-2009. Batas maksimum cemaran logam berat yang diperbolehkan dalam sayuran adalah 0,5 µg/g untuk timbal dan 0,2 µg/g untuk kadmium. Uji validasi yang dilakukan terhadap metode yang dipakai memberikan hasil perolehan kembali yaitu 98,18% dengan Relatif Standar Deviasi (RSD) 1,32%. Ini menunjukkan metode ini memberikan akurasi dan presisi yang baik dengan batas deteksi (LOD) 0,40 µg/g dan batas kuantitasi (LOQ) 1,34 µg/g.
LEAD (Pb) AND CADMIUM (Cd) CONTENT ANALYSES OF WATER KANGKUNG ( Ipomoea aquatica Forssk ) AND LAND
KANGKUNG ( Ipomoea reptans Poir ) IN MABAR-KIM BY ATOMIC ABSORBTION SPECTROPHOTOMETRY
ABSTRACT
Kangkung is a kind of vegetables that is commonly consumed by people and it contains a lot of vitamin A. Surrounding the Industry Area in Medan such as Mabar, vegetables are planted by people, one of them is kangkung. Since the industries growth in the area of the vegetables are expanded, it is wondered that the kangkung has been contaminated by lead and cadmium metals. The purpose of this research is to know the lead and cadmium metals of water kangkung and land kangkung planted in Mabar the Industries Area of Medan.
The analyses to the both of metals are applied qualitatively and quantitatively. The qualitative analysis uses dithizon reagent 0.005% b/v of different pH, it conduces dark red color of Pb on pH 8 and light red color of Cd on pH 12. The quantitative analysis of the metal is applied by using Atomic Absorbtion Spectrophotometry of different length. Pb is measured in wave-length 283.3 nm and Cd that of 228.8 nm. Metal consentration is determined by using Least Square method.
The result of analyses show that lead metal of water kangkung and land kangkung are 6.8500 ± 0.3905 µg/g and 4.2322 ± 0.2928 µg/g, meanwhile the cadmium metal of water kangkung and land kangkung are 1.3004 ± 0.0024 µg/g and 1.1948 ± 0.0103 µg/g.
The level of contaminated water kangkung and land kangkung by lead and cadmium metals are over maximum level allowed by SNI No. 7387-2009. The maximum metal limit of contaminated vegetables is allowed 0.5 µg/g for lead and 0.2 µg/g for cadmium. Validation test of the method applied shows the recovery result 98.18% and Standard Deviation Relativity (RSD) 1.32%. It shows that the method applied is fine and precisely accurate by the Limit of Detection (LOD) 0.40 µg/g and Limit of Quantitation (LOQ) 1.34 µg/g.
BAB I PENDAHULUAN
1.1Latar Belakang
Tumbuhan termasuk sayur-sayuran seperti kangkung dan mahluk hidup
lainnya dapat terpapar oleh zat-zat pencemar seperti partikel maupun gas. Partikel
yang banyak dilepaskan oleh industri adalah timbal dan kadmium.
Tanaman dapat menjadi mediator penyebaran logam berat pada mahluk
hidup karena masuknya logam tersebut pada tumbuhan melalui akar dan mulut
daun (stoma). Sayur-sayuran sebagai pakan baik pada manusia maupun hewan
menyebabkan berpindahnya logam yang terpapar didalamnya seperti timbal,
kadmium, kromium dan seng masuk kedalam tubuh mahluk hidup lainnya
( Farida, 2004 )
Kawasan Industri Medan seperti di daerah Mabar, banyak masyarakat
menanam berbagai jenis sayuran, diantaranya adalah sayur kangkung.
Sehubungan banyaknya industri di sekitar pertanian penduduk tersebut sayuran ini
dikhawatirkan telah tercemar oleh logam timbal dan kadmium. Sumber
pencemaran berasal dari tanah, udara dan air. Dari udara yaitu berasal dari asap
pabrik dan kendaraan bermotor sedangkan dari air yaitu berasal dari air hujan
yang telah tercemar oleh asap dari pabrik selain itu pencemaran air juga
disebabkan oleh hasil pembuangan limbah industri yang berasal dari pabrik.
Pencemaran logam di air diduga lebih tinggi di bandingkan di darat.
Pencemaran air biasanya terjadi karena pembuangan limbah dari industri
bahan yang mengandung logam itu sendiri (pestisida, insektisida) selain itu
berasal dari partikel logam berat yang beterbangan di udara akan terbawa oleh air
hujan ( Darmono, 1995 ). Menurut SNI No.7387-2009, batas maksimum cemaran
logam berat yang diperbolehkan dalam sayuran adalah 0,5 µg/g untuk timbal dan
0,2 µg/g untuk kadmium.
Pemeriksaan kuantitatif kandungan logam dalam sampel dapat di lakukan
dengan menggunakan metode Spektrofotometri Serapan Atom, Spektrofotometri
Emisi Nyala dan Spektrofotometri Visibel. Dalam hal ini, penetapan kadar Pb dan
Cd dilakukan dengan metode Spektrofotometri Serapan Atom, pemilihan metode
ini karena memilki beberapa keuntungan antara lain kecepatan analisisnya,
ketelitiannya, tidak memerlukan pemisahan pendahuluan dan dapat menentukan
konsentrasi unsur dalam jumlah yang sangat rendah yaitu kurang dari 1 ppm
(Khopkar, 1990).
Berdasarkan uraian di atas, peneliti tertarik untuk memeriksa logam timbal
dan kadmium pada kangkung air (Ipomoea aquatica Forssk) dan kangkung darat
(Ipomoea reptans Poir) yang ada di wilayah sekitar Mabar-Kawasan Industri
1.2 Perumusan Masalah
Berdasarkan uraian di atas, maka permasalahan dalam penelitian ini dapat
dirumuskan sebagai berikut :
a. Apakah kangkung air dan kangkung darat yang ditanam di kawasan sekitar
daerah Mabar KIM mengandung cemaran logam Timbal (Pb) dan
Kadmium (Cd)?
b. Apakah kadar logam Timbal (Pb) dan Kadmium (Cd) di dalam kangkung
air dan kangkung darat melewati batas cemaran maksimum yang
ditetapkan oleh Badan Standarisasi Nasional dalam SNI No. 7387-2009?
c. Apakah ada perbedaan kadar logam Timbal (Pb) dan Kadmium (Cd) pada
tanaman kangkung air dan kangkung darat?
1.3Hipotesis
a. Tanaman kangkung air dan kangkung darat yang ditanam di kawasan
Mabar KIM mengandung cemaran logam Timbal (Pb) dan Kadmium (Cd).
b. Kadar logam Timbal (Pb) dan Kadmium (Cd) pada kangkung air dan
kangkung darat yang berada di lingkungan sekitar Mabar KIM melewati
ambang batas.
c. Terdapat perbedaan kadar logam Timbal (Pb) dan Kadmium (Cd) pada
1.4Tujuan Penelitian
a. Mengidentifikasi logam Timbal (Pb) dan Kadmium (Cd) pada tanaman
kangkung air dan kangkung darat.
b. Menentukan kadar Timbal (Pb) dan Kadmium (Cd) pada tanaman
kangkung air dan kangkung darat.
c. Untuk mengetahui adanya perbedaan kadar logam Timbal (Pb) dan
Kadmium (Cd) pada tanaman kangkung air dan kangkung darat.
1.5 Manfaat Penelitian
Memberikan informasi kepada masyarakat mengenai besarnya kandungan
logam Timbal (Pb) dan Kadmium (Cd) pada tanaman kangkung air dan kangkung
darat yang ditanam disekitar Mabar KIM dan aman tidaknya sayur tersebut
BAB II
TINJAUAN PUSTAKA
2.1 Uraian Tanaman
Taksonomi tumbuhan kangkung :
Kingdom : Plantae
Divisi : Spermatophyta
Subdivisio : Angiospermae
Class : Dicotyledoneae
Ordo : Solanales
Family : Convolvulaceae
Genus : Ipomoea
Species : Ipomoea aquatica Forssk (kangkung air)
Ipomoea reptans Poir (kangkung darat)
Kangkung merupakan tanaman tahunan yang banyak ditanam di daerah
tropis maupun subtropis. Tanaman ini termasuk dalam famili Convolvulaceae atau
kangkung-kangkungan yang dicirikan dengan batang bergetah dan berlubang di
dalamnya.
Jenis kangkung yang umumnya dibudidayakan terdiri dari dua macam
yaitu kangkung air dan kangkung darat. Bagian dari tanaman kangkung yang
paling banyak dimanfaatkan ialah batang muda dan daun-daunnya. Daun dan
batang kangkung merupakan sumber vitamin A yang sangat baik (Purwandari,
2.2 Logam Berat
Logam berat adalah unsur logam yang mempunyai massa jenis lebih besar
dari 5 g/cm3, antara lain Cd, Hg, Pb, Zn dan Ni. Logam berat Cd, Hg dan Pb
dinamakan sebagai logam non esensial dan pada tingkat tertentu menjadi logam
beracun bagi makhluk hidup (Darmono, 1995).
Logam berat umumnya berbahaya karena memiliki kerapatan massa tinggi
dan dalam jumlah konsentrasi kecil dapat bersifat racun dan berbahaya. Beberapa
dari logam ini merupakan logam Bahan Berbahaya dan Beracun (logam B3) yang
pada umumnya secara alami merupakan komponen tanah. Logam ini dapat masuk
ke dalam tubuh manusia melalui makanan, air minum, atau melalui udara.
Arsen (As), merkuri (Hg), kadmium (Cd), timbal (Pb), adalah jenis logam
yang termasuk dalam kelompok logam yang berbahaya dan beracun bagi
kehidupan makhluk hidup. Beberapa logam lain yang juga cukup berbahaya
antara lain aluminium (Al), kromium (Cr), dan ada juga beberapa jenis logam
yang termasuk kelompok logam esensial yang dibutuhkan oleh tubuh untuk
membantu kinerja metabolisme misalnya, seng (Zn) dan tembaga (Cu). Logam
berat yang non esensial dapat bersenyawa dengan protein jaringan dan tertimbun
serta berikatan dengan protein, sehingga senyawanya disebut metalotionein yang
dapat menyebabkan toksik (Darmono, 1995).
2.3 Cemaran Logam Berat
Logam berat yang terdapat di lingkungan tanah, air dan udara dengan
suatu mekanisme dapat masuk ke dalam mahluk hidup. Tanaman dapat menjadi
mediator penyebaran logam berat pada mahluk hidup karena masuknya logam
partikulat (Charlena, 2004). Partikulat adalah bahan padatan atau likuid di udara
dalam bentuk asap, debu dan uap, yang dapat tinggal di atmosfer dalam waktu
yang lama. Asap merupakan pencemar yang paling jelas terlihat keluar dari
cerobong pabrik sebagai asap hitam tebal. Partikulat yang paling berbahaya adalah
partikel-partikel halus yang begitu kecil sehingga dapat menembus bagian
terdalam paru-paru (Prana, 2010).
2.4 Toksisitas Logam Berat
Besarnya tingkat keracunan logam berat menurut WHO (2004)
dipengaruhi oleh :
1. Umur
Anak-anak lebih rentan dari orang dewasa karena pengaruh dari volume
darah.
2. Jenis kelamin
Wanita lebih rentan dibandingkan dengan pria
3. Musim panas akan meningkatkan daya racun logam berat
Di musim panas logam berat akan terus berada diatmosfer
4. Peningkatan asam lambung akan meningkatkan absorbsi logam berat
5. Peminum alkohol lebih rentan terhadap logam berat
2.5 Timbal
Menurut Lawrence (1957), karakterisasi dari timbal adalah :
Pemerian : Timbal adalah logam berwarna kebiru-biruan sampai abu-abu
Kelarutan : Larut dalam HNO3 encer dan pekat, sedikit larut dalam HCl dan
H2SO4 pekat.
Nomor/Berat : 82/207,2
Berat Jenis : 11,34
Titik lebur : 327,5oC
Titik didih : 1740oC
Timbal merupakan bahan kimia yang termasuk dalam kelompok logam
berat. Logam ini merupakan bahan kimia golongan logam yang sama sekali tidak
dibutuhkan oleh tubuh. Bila masuk ke dalam tubuh organisme hidup dalam jumlah
yang berlebihan akan menimbulkan efek negatif terhadap fungsi fisiologis tubuh
(Palar, 1994).
2.5.1 Penggunaan Timbal
Dalam industri baterai, timbal digunakan sebagai grid yang merupakan
alloy (suatu persenyawaan) dengan logam Bismut (Pb-Bi) dengan perbandingan
93:7 (Palar, 1994). Timbal oksida (PbO4) dan logam timbal dalam industri baterai
digunakan sebagai bahan yang aktif dalam pengaliran arus elektron. Alloy Pb yang
mengandung 1% b/b Stibium (Sb) banyak digunakan sebagai kabel telepon (Palar,
1994).
2.5.2 Toksisitas Timbal
Toksisitas yang ditimbulkan oleh persenyawaan logam Pb dapat terjadi
karena masuknya persenyawaan logam tersebut ke dalam tubuh. Proses masuknya
logam ini ke dalam tubuh dapat melalui beberapa jalur, yaitu melalui makanan
dan minuman, udara dan perembesan atau penetrasi pada selaput atau lapisan kulit
Timbal yang masuk melalui makanan, masuk ke saluran cerna dan dapat
masuk ke dalam darah. Pada anak-anak, tingkat penyerapan timbal mencapai
53%. Hal ini jauh berbeda pada tingkat penyerapan orang dewasa yaitu sekitar
10%. Peningkatan asam lambung dapat meningkatkan absorbsi usus sehingga
absorbsi timbal juga meningkat (Riyadina, 1997).
Keracunan timbal dalam tubuh dapat menyebabkan gangguan terhadap
sistem syaraf, rongga mulut dan sistem rangka. Secara visual akan muncul gejala
dampak keterpaparan timbal secara akut maupun kronis. Keterpaparan secara akut
melalui udara yang terhirup dapat menimbulkan gejala rasa lemah, lelah,
gangguan tidur, sakit kepala, nyeri otot dan tulang. Dampak kronis keracunan
logam ini diawali dengan kelelahan, kelesuan dan gangguan gastrointestinal.
Keterpaparan yang terus-menerus pada sistem syaraf pusat menunjukkan gejala
insomnia (susah tidur), bingung dan gangguan ingatan.
2.6 Kadmium
Menurut Anonim (2008), karakterisasi Kadmium adalah :
Pemerian : Logam berwarna putih keperak-perakkan
Kelarutan : Larut dalam HNO3 pekat dan HCl panas
Nomor/Berat : 48/112,4
Berat Jenis : 8,65
Titik lebur : 321,07oC
Titik didih : 767oC
2.6.1 Penggunaan Kadmium
Kadmium murni banyak digunakan oleh industri pelapisan logam dan
fotografi, produksi foto-elektrik, foto-konduktor dan produksi gelas. Bentuk
garam asetatnya banyak digunakan pada proses industri porselen dan keramik
(Darmono, 2001).
2.6.2 Toksisitas Kadmium
Keracunan akut dari kadmium dapat terjadi melalui oral maupun inhalasi.
Efek keracunan yang umum adalah iritasi pada saluran pencernaan dan paru-paru,
tenggorokan terasa kering, mual, muntah, salivasi dan diare serta kejang pada
perut dan sakit pada otot.
Efek keracunan yang kronis ditandai dengan kehilangan indera perasa dan
penciuman, batuk, berkurangnya berat badan, gigi menjadi kuning dan dapat juga
terjadi kerusakan pada hati dan ginjal (Palar, 1994). Kasus keracunan Cd kronis
juga menyebabkan gangguan kardiovaskuler dan hipertensi. Hal tersebut terjadi
karena tingginya afinitas jaringan ginjal terhadap kadmium. Selain itu, logam ini
juga dapat menyebabkan terjadinya gejala osteomalasia karena terjadi kerusakan
daya keseimbangan kandungan kalsium dan fosfat dalam ginjal.
2.7 Spektrofotometri Serapan Atom
2.7.1 Teori Spektrofotometri Serapan Atom
Spektrofotometri serapan atom merupakan suatu metode analisis yang
digunakan untuk penentuan unsur-unsur logam dan metaloid yang berdasarkan
pada proses penyerapan energi radiasi atom-atom yang berada pada tingkat energi
dasar (ground state) pada panjang gelombang tertentu tergantung jenis unsur yang
dianalisis (Haswell, 1991).
Prinsip dasar spektrometri serapan atom adalah interaksi antara radiasi
absorbansi dari uap atom larutan sampel. Interaksi ini diperoleh dari proses
penguapan sampel yang dirubah menjadi atom bebas. Atom ini akan
mengabsorpsi radiasi dari sumber cahaya yang dipancarkan dari lampu katoda
(Hallow cathode lamp) yang mengandung unsur dari logam yang akan ditentukan.
Banyaknya penyerapan radiasi kemudian di ukur pada panjang gelombang
tertentu menurut jenis logamnya (Darmono, 1995).
Ada 4 cara pembentukan atom dalam spektrofotometri serapan atom yaitu: 1. Dengan menggunakan nyala campuran gas (Flame-AAS).
2. Melalui pembentukan senyawa hidrida diikuti pemanasan. 3. Dengan tanpa nyala untuk analisis merkuri.
4. Menggunakan pemanasan oleh listrik
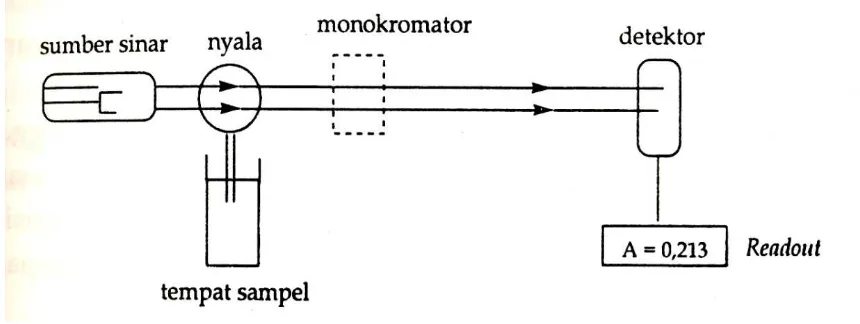
2.7.2 Instrumen Spektrofotometer Serapan Atom
Gambar 2. Komponen Spektrofotometer Serapan Atom
Gambar : Diagram Blok Instrumen Spektrofotometer Serapan
a. Sumber Sinar
Sumber sinar yang lazim dipakai adalah lampu katoda berongga (hollow cathoda lamp). Lampu ini terdiri atas tabung kaca tertutup yang mengandung suatu katoda dan anoda. Katoda berbentuk silinder berongga yang terbuat dari mineral atau dilapisi dengan mineral tertentu. Tabung mineral ini diisi dengan gas mulia (neon atau argon). Bila antara anoda dan katoda diberi selisih tegangan yang tinggi (600 volt), maka katoda akan memancarkan beras-berkas elektron yang bergerak menuju anoda yang mana kecepatan dan energinya sangat tinggi. Elektron-elektron dengan energi tinggi ini dalam perjalanannya menuju anoda akan bertabrakan dengan gas-gas mulia yang diisikan tadi. Akibat dari tabrakan-tabrakan ini membuat unsur-unsur gas mulia akan kehilangan elektron dan menjadi bermuatan positif. Ion-ion gas mulia yang bermuatan positif ini selanjutnya akan bergerak ke katoda dengan kecepatan dan energi yang tinggi pula. Pada katoda terdapat unsur-unsur yang sesuai dengan unsur yang dianalisis. Unsur-unsur ini akan ditabrak oleh ion-ion positif gas mulia. Akibat tabrakan ini, unsur-unsur akan terlempar ke luar dari permukaan katoda. Atom-atom unsur dari katoda ini mungkin akan mengalami eksitasi ke tingkat energi-energi elektron yang lebih tinggi dan akan memancarkan spektrum pencaran dari unsur yang sama dengan unsur yang akan dianalisis (Gandjar dan Rohman, 2007).
b. Tempat Sampel
sampel menjadi uap atom-atom yaitu : dengan nyala (flame) dan dengan tanpa nyala (flameless) (Gandjar dan Rohman, 2007).
c. Monokromator
Monokromator dimaksudkan untuk memisahkan dan memilih panjang gelombang yang digunakan dalam analisis. Dalam monokromator terdapat chopper (pemecah sinar), suatu alat yang berputar dengan frekuensi atau kecepatan perputaran tertentu (Gandjar dan Rohman, 2007).
d. Detektor
Detektor digunakan untuk mengukur intensitas cahaya yang melalui tempat pengatoman. Biasanya digunakan tabung penggandaan foton (photomultiplier tube). Ada 2 cara yang dapat digunakan dalam sistem deteksi yaitu: (a) yang memberikan respon terhadap radiasi resonanasi dan radiasi kontinyu; dan (b) yang hanya memberikan respon terhadap radiasi resonansi (Gandjar dan Rohman, 2007).
e. Readout
Readout merupakan suatu alat penunjuk atau dapat juga diartikan sebagai pencatat hasil. Hasil pembacaan dapat berupa angka atau berupa kurva yang menggambarkan absorbansi atau intensitas emisi (Gandjar dan Rohman, 2007).
2.7.3 Gangguan Pada Spektrofotometer Serapan Atom
Gangguan-gangguan yang dapat terjadi dalam spektrofotometer serapan atom (Gandjar dan Rohman, 2007) adalah sebagai berikut:
2. Gangguan kimia yang dapat mempengaruhi jumlah atau banyaknya atom yang terjadi dalam nyala.
2.8 Validasi Metode Analisis
Validasi metode analisis adalah suatu tindakan penilaian terhadap parameter tertentu, berdasarkan percobaan laboratorium untuk membuktikan bahwa parameter tersebut memenuhi persyaratan untuk penggunaannya (Harmita, 2004). Parameter yang digunakan dalam hal ini adalah ketepatan, kecermatan dan batas deteksi serta batas kuantifikasi.
2.8.1 Kecermatan (akurasi)
Kecermatan adalah ukuran yang menunjukkan derajat kedekatan hasil
analisis dengan kadar analit yang sebenarnya. Kecermatan dinyatakan sebagai
perses perolehan kembali (recovery) analit yang ditambahkan (Harmita, 2004).
Perolehan kembali dapat ditentukan dengan cara membuat sampel plasebo
(eksipien obat, cairan biologis) kemudian ditambahkan analit dengan konsentrasi
tertentu (biasanya 80% sampai 120% dari kadar analit yang diperkirakan),
kemudian dianalisis dengan metode yang akan divalidasi (Ermer dan Miler,
2005).
Tetapi bila tidak memungkinkan membuat sampel plasebo, maka dapat
dipakai metode adisi. Metode adisi dapat dilakukan dengan menambahkan
sejumlah analit dengan konsentrasi tertentu pada sampel yang diperiksa, lalu
2.8.2 Ketepatan (presisi)
Presisi merupakan ukuran keterulangan metode analisis dan biasanya
diekspresikan sebagai simpangan baku relatif (Relative Standard Deviation, RSD)
dari sejumlah sampel yang berbeda secara statistik (Rohman, 2007).
Dalam analisis, nilai RSD antara 1-2% biasanya dipersyaratkan untuk
senyawa aktif dalam jumlah yang banyak, sedangkan untuk
senyawa-senyawa dengan kadar kecil RSD-nya berkisar antara 5-15% (Rohman, 2007).
2.8.3 Batas Deteksi (Limit of Detection, LOD) dan Batas Kuantifikasi (Limit of Quantification, LOQ)
Batas deteksi didefenisikan sebagai konsentrasi analit terendah dalam
sampel yang masih dapat dideteksi, tetapi tidak dikuantifikasi pada kondisi
percobaan yang dilakukan. Batas deteksi dinyatakan dalam konsentrasi analit
(persen, bagian per juta) dalam sampel (Satiadarma, dkk, 2004).
Batas kuantifikasi didefenisikan sebagai konsentrasi analit terendah dalam
sampel yang dapat ditentukan dengan presisi dan akurasi. Batas ini dinyatakan
dalam konsentrasi analit (persen, bagian per juta) dalam sampel (Satiadarma, dkk.,
BAB III
METODE PENELITIAN
Penelitian ini menggunakan metode deskriptif yang bertujuan untuk
menggambarkan sifat dari suatu keadaan dalam hal ini menentukan kandungan
logam Pb dan Cd pada kangkung air dan kangkung darat.
3.1Lokasi dan Waktu penelitian
Penelitian dilakukan di laboratorium Kimia Farmasi Kualitatif Fakultas
Farmasi USU, Laboratorium Majelis Ulama Indonesia ( MUI ) Kota Medan. Dan
penelitian dilakukan pada bulan Februari 2011 – Maret 2011.
3.2Bahan – Bahan
Bahan yang digunakan adalah pro analisis keluaran E.Merck kecuali
disebutkan lain yaitu Asam Nitrat 65% b/v, Kloroform, Dithizon 99% b/b,
Ammonium hidroksida 25% b/b, Kalium Sianida, Akuabides, larutan baku Pb dan
Cd masing-masing dengan konsentrasi 1000 µg/ml.
3.3Alat-Alat
Alat-alat yang digunakan yaitu Spektrofotometer Serapan Atom
(AA-6300) dengan nyala Udara-Asetilen, Neraca Listrik (AND GF-200), lampu katoda
3.4 Pembuatan Pereaksi 3.4.1 Larutan HNO3 5 N
Dibuat dengan mengencerkan 340 ml HNO3 65% b/v dengan air suling
hingga 1000 ml (Ditjen POM, 1995).
3.4.2 Larutan Dithizon 0,005% b/v
Dithizon sebanyak 5 mg dilarutkan dalam 100 ml kloroform (Vogel,
1990).
3.4.3 Larutan NH4OH 1 N
Di encerkan NH4OH 25% b/b sebanyak 7,4 ml dengan akuadest dalam 100
ml (Ditjen POM, 1979).
3.5 Rancangan Penelitian 3.5.1 Sampel
3.5.1.1 Pengambilan Sampel
Metode pengambilan sampel dilakukan secara sampling purposif yang
dikenal juga sebagai sampling pertimbangan dimana sampel ditentukan atas
pertimbangan bahwa populasi sampel adalah homogen dan sampel yang tidak
diambil mempunyai karakteristik yang sama (Sudjana, 2002).
3.5.1.2 Identifikasi Sampel
Identifikasi sampel dilakukan oleh bagian herbarium Fakultas MIPA
Biologi Universitas Sumatera Utara. Hasil identifikasi sampel yaitu kangkung air
(Ipomoea aquatica Forssk) dan kangkung darat (Ipomoea reptans Poir). Hasil
3.5.2 Penyiapan Sampel
Sampel yang digunakan adalah kangkung yang ditanam di daerah
Mabar-KIM Medan. Sampel sebanyak ± 2 kg, dicuci bersih kemudian dipotong
kecil-kecil dan ditiriskan. Dikeringkan di dalam oven pada suhu 35-400C lalu
dihaluskan dengan blender.
3.5.3 Proses Dekstruksi Logam Pb dan Cd 3.5.3.1 Proses Dekstruksi Basah
Timbang ±20 g serbuk kangkung, tambahkan 25 ml asam nitrat 65% b/v lalu didiamkan selama 24 jam, kemudian sampel di panaskan di atas hotplate pada temperatur sekitar 100°C sampai mengering, tambahkan tetes demi tetes asam nitrat 65% b/v hingga larutan bewarna kuning jernih (± selama 5 jam ). Kemudian dipindahkan ke dalam labu tentukur 25 ml dan volumenya ditepatkan sampai garis tanda dengan akuabides, lalu disaring dengan kertas saring Whatman No.42 dengan membuang 2 ml larutan pertama hasil penyaringan. Larutan ini digunakan untuk analisis kualitatif dan kuantitatif dengan spektrofotometer serapan atom (Haswell,1991).
3.6 Pemeriksaan Kualitatif
3.6.1 Pemeriksaan Kualitatif untuk Timbal
Ke dalam tabung reaksi dimasukkan 5 ml larutan sampel, diatur pH-nya 8
dengan penambahan ammonium hidroksida 1N, di masukan kalium sianida,
kemudian ditambahkan 5 ml dithizon 0,005% b/v kocok kuat, dibiarkan lapisan
memisah dan terbentuk warna merah tua berarti positif mengandung Pb (Fries,
3.6.2 Pemeriksaan Kualitatif untuk Kadmium
Ke dalam tabung reaksi dimasukkan 5 ml larutan sampel, diatur pH-nya 12
dengan penambahan ammonium hidroksida 1N, kemudian ditambahkan 5 ml
dithizon 0,005% b/v kocok kuat, dibiarkan lapisan memisah dan terbentuk warna
merah muda berarti positif mengandung Cd (Fries, 1977).
3.7 Pemeriksaan Kuantitatif
3.7.1 Penentuan Linieritas Kurva Kalibrasi Logam Timbal
Larutan standar Timbal (1000 μg/ml) dipipet sebanyak 10 ml, dimasukkan ke dalam labu tentukur 100 ml, kemudian ditambahkan 10 ml HNO3 5N,
ditepatkan sampai garis tanda dengan akuabides (konsentrasi 100 μg/ml).
Larutan kurva kalibrasi Timbal dibuat dengan memipet 2,0 ml; 4,0 ml ; 6,0 ml; 8,0 ml; 10 ml larutan baku 100 μg/ml, dimasukkan kedalam labu tentukur 100 ml, ditambahkan 10 ml HNO3 5N kemudian ditepatkan sampai garis tanda dengan
akuabides, diperoleh larutan dengan konsentrasi 2 μg/ml; 4 μg/ml; 6 μg/ml; 8 μg/ml; dan 10 μg/ml lalu diukur pada panjang gelombang 283,3 nm.
3.7.2 Penentuan Linieritas Kurva Kalibrasi Logam Kadmium
Larutan standar Kadmium (1000 μg/ml) dipipet sebanyak 10 ml, dimasukkan ke dalam labu tentukur 100 ml, kemudian ditambahkan 10 ml HNO3
5N, ditepatkan sampai garis tanda dengan akuabides (konsentrasi 100 μg/ml). Larutan standar Kadmium (100 μg/ml) dipipet sebanyak 10 ml, dimasukkan kedalam labu tentukur 100 ml, kemudian ditambahkan 10 ml HNO3
100 ml, ditambahkan 10 ml HNO3 5N kemudian ditepatkan sampai garis tanda
dengan akuabides, diperoleh larutan dengan konsentrasi 0,4 μg/ml; 0,8 μg/ml; 1,2 μg/ml; 1,6 μg/ml; dan 2 μg/ml lalu diukur pada panjang gelombang 228,8 nm. Data hasil pengukuran absorbansi larutan standar Pb dan Cd dan contoh perhitungan persamaan regresinya dapat dilihat pada lampiran 2 sampai 3
halaman 36 sampai 39.
3.7.3 Penetapan Kadar Logam Pb dan Cd pada Sampel
Sampel yang telah di dekstruksi lalu dipindahkan ke dalam labu tentukur
25 ml dan volumenya ditepatkan sampai garis tanda dengan akuabides, lalu
disaring dengan kertas saring Whatman No.42 dengan membuang 2 ml larutan
pertama hasil penyaringan. Lalu di ukur absorbansinya dengan alat
spektrofotometer serapan atom. Logam Pb di ukur pada panjang gelombang 283,3
nm dan logam Cd 228,8 nm. Pengukuran ini di lakukan terhadap sampel yang
telah di destruksi. Nilai absorbansinya yang diperoleh berada dalam rentang
kalibrasi.
3.7.4 Perhitungan Kadar Logam Pb dan Cd dalam Sampel
Kadar Timbal dan Kadmium dihitung dengan mensubstitusikan absorbansi ke dalam persamaan regresi yang diperoleh dari kurva kalibrasi seperti di bawah ini :
Y = aX + b
Dari perhitungan regresi linear, maka dapat diketahui kadar dari sampel dengan menggunakan rumus :
Kadar Sebenarnya μg/g =
(g) Sampel Berat n pengencera Faktor x (ml) sampel Volume x ) / ( i
Konsentras µg ml
Hasil analisis logam Pb dan Cd pada sampel dapat di lihat pada lampiran
4 halaman 40, sedangkan contoh perhitungan kadar logam pada lampiran 5 sampai 6 halaman 41 sampai 42.
3.8 Analisa Data Secara Statistik 3.8.1 Uji penolakan Hasil Analisis
Untuk mengetahui di terima atau tidaknya data penelitian, maka data yang
di peroleh di analisis secara statistik dengan uji distribusi t.
Untuk mencari t hitung digunakan rumus :
t hitung =
n SD X Xi / −
SD =
( )
1 -n X -Xi 2
∑
Keterangan : Xi = Kadar sampel
−
X = Kadar rata-rata
n = jumlah perlakuan
3.8.2 Rata – Rata kadar Logam Pb dan Cd dalam Sampel
Untuk menentukan kadar logam dalam sampel dengan taraf kepercayaan
95%, α= 0,05, dk= n-1, dapat digunakan rumus (Sudjana, 2002).
Kadar Logam: µ = X ± t(α/2, dk) x ( SD / )
Keterangan : −
X = Kadar rata-rata sampel
SD = Standar Deviasi
dk = Derajat kebebasan (dk = n-1)
α = interval kepercayaan
n = jumlah perlakuan
Hasil perhitungan statistik kadar logam pada sampel dapat di lihat pada lampiran
7 sampai 10 halaman 43 sampai 50.
3.8.3. Pengujian Beda Nilai Rata- Rata kadar Logam Pb dan Cd pada Sampel
Sampel yang di bandingkan adalah independen dan jumlah pengamatan
masing- masing lebih kecil dari 30 sehingga variansi (σ) tidak di ketahui dan di
lakukan uji F untuk mengetahui apakah variansi populasi sama (σ1 = σ2) atau
berbeda (σ1 ≠ σ2) dengan menggunakan rumus:
S
S
2 2 2 1 F=Data berbeda secara signifikan jika F hitung > F tabel.
Dimana:
F = beda nilai yang diterima
S1 = standar deviasi sampel 1
Apabila dari hasilnya di peroleh Fο ≤ Fkritis, maka di simpulkan bahwa σ1
= σ2, kemudian di lanjutkan dengan uji beda rata- rata menggunakan uji t dengan
rumus:
(
)
( ) ( )
n
n
x
x
Sp 1 2
2 1 o 1 1 t + − =
dan jika Fo≥ F kritis maka dilanjutkan dengan uji t dengan rumus :
(
)
( ) ( )
s
n
s
n
x
x
2 2 2 1 2 1 2 1 o / t + − =Kedua sampel dinyatakan berbeda apabila to yang diperoleh melewati nilai kritis t, dan sebaliknya.
(Sabri dan Hastono, 2006)
Hasil Pengujian beda nilai rata-rata kadar logam pada sampel dapat dilihat
pada Lampiran 11 sampai 12 halaman 51 sampai 54.
3.9 Uji Ketepatan (Recovery Test)
Ketepatan adalah ukuran yang menunjukan kedekatan hasil analisis
dengan kadar analit yang sebenarnya. Ketepatan di nyatakan sebagai persen
perolehan kembali (recovery) yang di tentukan dengan menentukan berapa persen
analit yang di tambahkan dapat di peroleh kembali pada suatu pengukuran
(Rohman,2007).
3.9.1 Prosedur Uji Perolehan Kembali (Recovery)
Sampel di timbang seksama lebih kurang 20 gram dalam erlenmeyer yang
telah di ketahui beratnya. Di tambahkan 10 ml larutan standar Pb dengan
konsentrasi 8 µg/ml dan 2 ml larutan standar Cd dengan konsentrasi 0,4 µg/ml
pada sampel. Selanjutnya di lakukan cara yang sama seperti 3.5.3.1 dan di hitung
persentase uji perolehan kembali (uji recovery) dengan rumus.(Harmita,2004)
Keterangan :
Cf =konsentrasi sampel yang di peroleh setelah penambahan larutan baku
CA =konsentrasi sampel yang di peroleh sebelum penambahan larutan baku
C*A = konsentrasi larutan baku yang di tambahkan
Data hasil perolehan kembali dapat di lihat pada lampiran 15 sampai 16
halaman 57 dan contoh perhitungannya pada lampiran 13 sampai 14 halaman 55 sampai 56.
3.9.2 Uji Ketelitian
Uji ketelitian dilakukan untuk mengetahui derajat kesesuaian antara hasil
uji individual yang diterapkan secara berulang pada sampel. Adapun parameter uji
ketelitian yaitu Koefesien Variasi (KV) atau Relative Standard Deviation (%
RSD). (Harmita,2004) Harga persentase Relative Standard Deviation (% RSD) di
tentukan dengan rumus
Keterangan : SD = Standar Deviasi
X = Kadar rata-rata setelah telah ditambah larutan baku
Data hasil Perhitungan Uji Ketelitian dapat dilihat pada Lampiran 17 sampai 18
halaman 58.
Batas deteksi atau limit of detection (LOD) adalah jumlah terkecil analit
dalam sampel yang dapat di deteksi yang masih memberikan respon signifikan,
sedangkan batas kuantitasi merupakan kuantitas terkecil analit dalam sampel yang
masih dapat memenuhi kriteria cermat dan seksama (Rohman, 2007).
Batas deteksi dan batas kuantitasi ini dapat di hitung berdasarkan pada
standar deviasi (SD) respon dan kemiringan (slope) linieritas baku ( Harmita,
2004 ) dengan rumus:
SY =
( )
2 -n
Y
-Yi 2
∑
Batas deteksi (LOD) = slope
SY x 3
Batas kuantitasi (LOQ )= slope
SY x 10
Hasil perhitungan LOD dan LOQ dapat di lihat pada lampiran 19 sampai 20
BAB IV
HASIL DAN PEMBAHASAN
4.1 Analisis Kualitatif
Adanya logam Pb dan Cd pada kangkung darat dan kangkung air,
dilakukan secara uji kualitatif dengan pereaksi dithizon 0,005% b/v. Hasil
reaksinya dapat di lihat pada tabel di bawah ini:
Tabel 1. Hasil Uji Kualitatif Logam Pb dan Cd dalam sampel dengan menggunakan Pereaksi Dithizon 0,005% b/v
No. Logam pH Reaksi dengan larutan Dithizon 0,005% b/v
Kode
Sampel Hasil
1. Pb
8 Merah tua
KD +
KA +
2. Cd 12 Merah muda
KD +
KA +
Keterangan :
[image:43.595.117.519.328.488.2]+ = Mengandung logam KD = Kangkung darat KA = Kangkung air
Tabel di atas menunjukkan kangkung darat dan kangkung air mengandung
logam Pb dan Cd, karena menghasilkan reaksi warna yang positif dengan
reagensia dithizon 0,005% b/v. Warna yang di hasilkan masing-masing logam
berbeda pada pH yang berbeda pula, yakni logam Pb bewarna merah tua pada pH
8 dan logam Cd bewarna merah muda pada pH 12. Warna yang terjadi ini karena
terbentuknya senyawa logam–dithizonat pada pH Reaksi pada tiap pH yang
berbeda (Fries,1977). Hasil uji kualitatif dapat dilihat pada Lampiran 27
4.2 Pemeriksaan Kuantitatif
4.2.1 Penentuan Linearitas Kurva Kalibrasi Timbal dan Kadmium
Kurva kalibrasi logam Pb dan Cd diperoleh dengan cara mengukur
absorbansi dari larutan standar kedua logam tersebut. Berdasarkan hasil
pengukuran kurva kalibrasi untuk Logam Pb diukur pada rentang konsentrasi 2
µg/ml sampai 10 µg/ml di peroleh persamaan regresi Y = 0,00087X + 0,0001
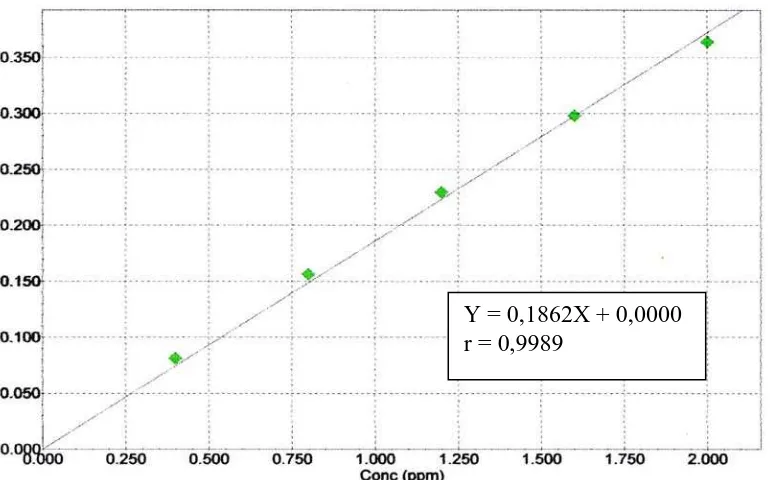
dan untuk Logam Cd pada rentang konsentrasi 0,4 µg/ml sampai 2 µg/ml,
persamaan regresi yang di peroleh yaitu Y = 0,1862X + 0,0000.
Kurva kalibrasi larutan standar Pb dan Cd dapat di lihat pada Gambar 1 dan
[image:44.595.120.516.403.591.2]Gambar 2 dan data hasil konsentrasi dan absorbansi Pb dan Cd dapat dilihat pada Lampiran 23 halaman 63.
Gambar 1. Kurva kalibrasi larutan baku Pb
Gambar 2. Kurva kalibrasi larutan baku Cd
Berdasarkan gambar kedua kurva kalibrasi diatas diperoleh serapan nilai
koefisien korelasi ( r ) untuk Pb sebesar 0,9995 dan Cd sebesar 0,9989. Koefisien
korelasi yang diperoleh dari kedua logam dapat diterima karena sesuai persyaratan
untuk koefisien korelasi tidak boleh lebih kecil dari 0,995 ( Badan POM, 2003 ).
Kedua koefisien diatas menyatakan adanya hubungan linier antara konsentrasi
logam dan serapannya ( absorbansi ).
4.3 Analisis kadar Logam Pb dan Cd pada sampel
Konsentrasi logam Pb dan Cd dalam sampel di hitung berdasarkan
persamaan garis regresi linier kurva kalibrasi larutan standar masing-masing
logam. Kadar kedua logam di hitung secara statistik dengan distribusi t pada taraf
kepercayaan 95% (α = 0,05). Berdasarkan hasil perhitungan statistik tersebut, di
peroleh kesimpulan bahwa rata-rata kadar logam Pb dan Cd pada kangkung air Y = 0,1862X + 0,0000
lebih tinggi di bandingkan kangkung darat, seperti yang di cantumkan pada tabel
[image:46.595.113.517.164.283.2]berikut:
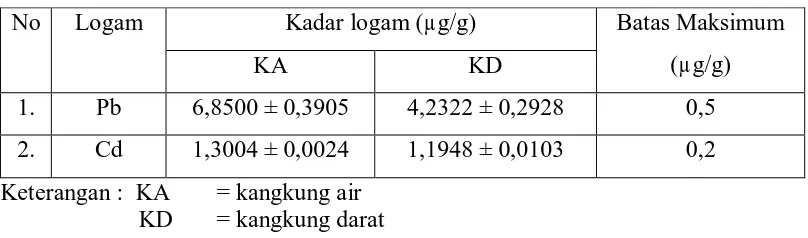
Tabel 2 . Data kadar logam Pb dan Cd pada kangkung air dan kangkng darat
No Logam Kadar logam (µg/g) Batas Maksimum
(µg/g)
KA KD
1. Pb 6,8500 ± 0,3905 4,2322 ± 0,2928 0,5
2. Cd 1,3004 ± 0,0024 1,1948 ± 0,0103 0,2
Keterangan : KA = kangkung air KD = kangkung darat
Tabel di atas menunjukkan bahwa kadar logam Pb dan Cd pada kangkung
air lebih tinggi kadarnya di bandingkan kangkung darat. Ini disebabkan karena
kangkung air selain mengalami pencemaran dari tanah, udara seperti asap-asap
dari pabrik juga melalui air yaitu dari air hujan yang telah tercemar oleh asap
pabrik dan dari pembuangan limbah-limbah industri. Kadar kangkung air dan
kangkung darat telah melewati batas maksimum yang di izinkan SNI No.
7387-2009.
4.4 Pengujian Beda Nilai Rata-Rata Kadar Logam Pb dan Cd pada Sampel Pengujian beda nilai rata-rata kadar logam Pb dan Cd pada sampel
bertujuan untuk melihat apakah ada perbedaan yang signifikan pada rata-rata
kadar logam Pb dan Cd antara kangkung air dan kangkung darat. Berdasarkan
asumsi bahwa sampel berasal dari varians yang sama maka di lakukan uji F ,
apabila dari hasilnya di peroleh F0≤ Fkritis maka di lanjutkan dengan uji beda
rata-rata menggunakan uji t pada taraf kepercayaan 95%. Pengujian menunjukkan
bahwa terdapat perbedaan yang signifikan rata-rata kadar logam Pb dan Cd pada
4.5 Uji Ketepatan dan Ketelitian
Untuk melihat sejauh mana metode yang digunakan ini memberikan
ketepatan dan ketelitian yang baik maka dilakukan uji ketepatan dengan parameter
% Uji Perolehan Kembali dan uji ketelitian dengan parameter % RSD. Hasil Uji
ketepatan dan ketelitian dapat dilihat pada Tabel 3.
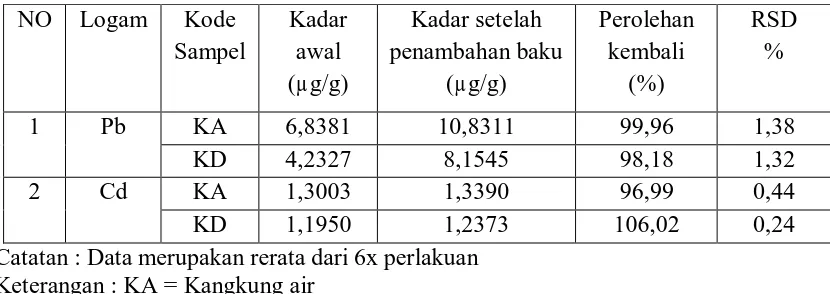
Tabel 3. Hasil Uji ketepatan (% Uji Perolehan Kembali) dan ketelitian (%RSD)
NO Logam Kode
Sampel
Kadar awal (µg/g)
Kadar setelah penambahan baku
(µg/g)
Perolehan kembali
(%)
RSD %
1 Pb KA 6,8381 10,8311 99,96 1,38
KD 4,2327 8,1545 98,18 1,32
2 Cd KA 1,3003 1,3390 96,99 0,44
KD 1,1950 1,2373 106,02 0,24
Catatan : Data merupakan rerata dari 6x perlakuan Keterangan : KA = Kangkung air
KD = Kangkung darat
Hasil yang di peroleh dari % uji perolehan kembali menunjukkan bahwa
metode yang digunakan memberikan ketepatan yang memenuhi syarat. Ini berarti
metode ini memberikan ketepatan yang baik. Menurut Miller (2005), suatu
metode dikatakan tepat jika nilai recovery-nya antara 80-120%.
Dari hasil Relatif Standar Deviasi (RSD) juga memberikan ketelitian yang
memuaskan. Hasil ini telah memenuhi batas yang telah di tetapkan yaitu kriteria
seksama atau teliti yang diberikan jika metode memberikan koefesien variasi 2%
[image:47.595.116.531.276.423.2]4.6 Batas Deteksi (LOD) dan Batas Kuantitasi (LOQ)
Berdasarkan hasil perhitungan standar deviasi (SD) yang di lakukan, maka
di peroleh batas deteksi (LOD) untuk logam Pb dan Cd masing-masing sebesar
0,4000 µg/ml dan 0,0474 µg/ml sedangkan batas kuantitasi (LOQ) untuk logam
Pb dan Cd masing-masing sebesar 1,3400 µg/ml dan 0,1579 µg/ml. Dari hasil
pengukuran, semua konsentrasi sampel berada diatas konsentrasi dari batas
BAB V
KESIMPULAN DAN SARAN
5.1Kesimpulan
1. Kangkung air dan kangkung darat yang ditanam di daerah Mabar-KIM
mengandung logam Timbal (Pb) dan Kadmium (Cd)
2. Kadar Logam Timbal (Pb) dan Kadmium (Cd) pada kangkung air dan
kangkung darat melewati batas maksimum cemaran logam berat yang
ditetapkan oleh Badan Standarisasi Nasional dalam SNI No.7387-2009
yaitu 0,5 µg/g untuk Timbal dan 0,2 µg/g untuk Kadmium.
3. Dari hasil pengujian beda nilai rata-rata menggunakan distribusi t pada
taraf kepercayaan 95% di peroleh bahwa terdapat perbedaan yang
signifikan rata-rata kadar logam Pb dan Cd pada kangkung air dan
kangkung darat.
5.2Saran
1. Disarankan kepada masyarakat untuk mengurangi mengkonsumsi sayuran
yang ditanam di daerah perindustrian
2. Di sarankan kepada peneliti selanjutnya agar dapat meneliti jenis sayuran
DAFTAR PUSTAKA
Anonim. (2008) Kadmium (Cd).
http://www.wikipediaindonesia.com/bahan logam/html.
Badan Pengawasan Obat dan Makanan. (2003). Cara Pembuatan Obat yang Baik. Bandung: Badan Pengawasan Obat dan Makanan. Hal. 1-21.
Darmono. (1995). Logam dalam Sistem Biologi Mahluk Hidup. Cetakan pertama. Jakarta: UI-Press. Hal. 10-12, 21-23, 26-27.
Ditjen POM. (1995). Farmakope Indonesia. Edisi IV. Departemen Kesehatan RI. Jakarta.
Farida. (2004). Pencemaran Udara dan Permasalahannya.
Fries, J,.and Getrost, H. (1977). Organic Reagents For Trace Analysis. E. Merck Darmstadt. Page. 243-249.
Gandjar, I. G., dan Rohman, A. (2007). Kimia Farmasi Analisis. Cetakan Pertama. Yogyakarta: Pustaka Belajar. Hlm. 27, 463
Haswell, S.J. (1991). Atomic Absorption Spectrometry. Amsterdam: Elsevier. page.202, 207-208
Harmita.(2004). Petunjuk Pelaksanaan Validasi Metode dan Cara Perhitungannya. Review Artikel. Majalah Ilmu Kefarmasian. Vol 1 (3): 117-135.
J. Ermer, J. H. McB. Miller. (2005). Method Validation in Pharmaceutical Analysis. Weinheim : WILEY-VCH Verlag GmbH & Co. KGaA. Page. 117 -135
Khopkar, S. M. (1990). Konsep Dasar Kimia Analitik. Penerjemah: Saptohardjo. Jakarta: UI-Press. Hlm. 274-275
Lawrence. (1957) Timbal dan sifat-sifatnya.
Palar. (1994). Pencemaran dan Toksikologi Logam Berat. Penerbit Rineka Cipta. Jakarta.
Prana. (2010). Cemaran Logam Berat.
Purwandari, A. W. (2006). Budidaya Tanaman Kangkung. Jakarta: Ganeca Exact. Hal 5-8
Riyadina, W. (1997). Pengaruh Pencemaran Plumbum Terhadap Kesehatan. Media Litbangkes Balitbang Dep. Kes RI Jakarta.
Sabri, L. dan Hastono, S.P. (2006). Statistik Kesehatan. Jakarta: PT Raja Grafindo Persada. Halaman 112-118
Satiadarma, K., M. Mulja, D. H. Tjahjono, R. E. Kartasasmita. 2004. Asas Pengembangan Prosedur Analisis. Edisi Pertama. Surabaya: Airlangga University Press. Hal. 46-49.
Sudjana.(2002). Metode Statistika. Edisi Statistika. Edisi Keenam. Bandung: Penerbit Tarsito. Hal. 168,371.
Lampiran 1. Flowsheet proses Dekstruksi Basah
Dicuci Bersih Dipotong kecil-kecil Dikeringkan didalam oven Dihaluskan dengan blender
Ditimbang 20 gram
Dimasukkan kedalam erlenmeyer Ditambahkan 25 ml HNO3 (p) Didiamkan selama 24 jam
Didestruksi sampai larutan berwarna kuning jernih (±selama 5 jam)
Didinginkan
Dimasukkan kedalam labu ukur 25 ml
Ditepatkan dengan akuabides sampai garis tanda
Disaring dengan kertas saring whatman no.42 dengan membuang 2 ml larutan pertama hasil penyaringan
Diuji kualitatif
Diuji kuantitatif dengan
Spektrofotometer Serapan Atom
untuk timbal pada 283,3 nm dan
untuk kadmium pada 228,8 nm Sayur kangkung
sebanyak 2 kg
Sampel + HNO3 (p)
25 ml larutan sampel
Larutan sampel
Lampiran 2. Data Hasil Pengukuran Absorbansi Larutan Standar Timbal (Pb), Perhitungan Persamaan Garis Regresi dan Koefisien Korelasi (r)
dari Data Kalibrasi Pb
1. Hasil pengukuran absorbansi larutan standar Pb
No Konsentrasi (µg/ml) Absorbansi (A)
1
0,0000 0,0000
2
2,0000 0,0019
3
4,0000 0,0037
4
6,0000 0,0052
5
8,0000 0,0071
6
10,0000 0,0087
2. Perhitungan Persamaan Garis Regresi dan Koefisien Korelasi (r)
No X Y XY X2 Y2
1
0,0000 0,0000 0,0000 0,0000 0,0000
2
2,0000 0,0019 0,0038 4,0000 0,00000361
3
4,0000 0,0037 0,0148 16,0000 0,00001369
4
6,0000 0,0052 0,0312 36,0000 0,00002704
5
8,0000 0,0071 0,0568 64,0000 0,00005041
6
10,0000 0,0087 0,0870 100,0000 0,00007569
∑
30,0000 0,0266 0,1936 220,0000 0,00017044
Rata-rata
a
–
a
–
a = 0,00087
b - a
b = 0,0044 – (0,00087) ( 5 )
b = 0,0001
Maka persamaan regresinya adalah : Y= 0,00087
r
– –
r
– –
r
Lampiran 3. Data Hasil Pengukuran Absorbansi Larutan Standar Kadmium (Cd), Perhitungan Persamaan Garis Regresi dan Koefisien Korelasi
(r) dari Data Kalibrasi Cd
1. Hasil Pengukuran Absorbansi Larutan Standar Cd
No Konsentrasi (µg/ml) Absorbansi (A)
1
0,0000 0,0000
2
0,4000 0,0811
3
0,8000 0,1564
4
1,2000 0,2297
5
1,6000 0,2982
6
2,0000 0,3641
2. Perhitungan Persamaan Garis Regresi dan Koefisien Korelasi (r)
No X Y XY X2 Y2
1
0,0000 0,0000 0,0000 0,0000 0,0000
2
0,4000 0,0811 0,0324 0,1600 0,0066
3
0,8000 0,1564 0,1251 0,6400 0,0245
4
1,2000 0,2297 0,2756 1,4400 0,0528
5
1,6000 0,2982 0,4771 2,5600 0,0890
6
2,0000 0,3641 0,7282 4,0000 0,1326
∑
6,0000 1,1172 1,6385 8,80000 0,3053
Rata-rata
a
–
a –
–
a = 0,1862
b - a
b = 0,1862 – (0,1862) ( 1 )
b = 0,0000
Maka persamaan regresinya adalah : Y= 0,1862 X
r
– –
r
– –
r
Lampiran 4. Hasil analisis logam Pb dan Cd dan kadar sebenarnya pada sampel Kangkung Darat dan Kangkung Air.
No Sampel Logam Berat Sampel
(gram)
Absorbansi Konsentrasi (µg/ml)
Kadar sampel (µg/g)
Kadar sebenarnya (µg/g)
1 Kangkung Darat
Timbal 20,0299 0,0031 3,4483 4,3039 20,0250 0,0033 3,6782 4,5920
20,0259 0,0029 3,2184 4,0178 4,2322±0,2928 20,0241 0,0030 3,3333 4,1617
20,0390 0,0032 3,5632 4,4454 20,0210 0,0028 3,1034 3,8752 Kadar rata –rata 4,2327
Kadmium 20,0299 0,1795 0,9460 1,2032 20,0250 0,1780 0,9560 1,1935
20,0259 0,1801 0,9672 1,2075 1,1948±0,0103 20,0241 0,1765 0,9479 1,1835
20,0390 0,1772 0,9517 1,1873 20,0210 0,1782 0,9570 1,1949 Kadar rata- rata 1,1950
2. Kangkung Air
Timbal 20,0380 0,0052 5,8621 7,3137
20,0281 0,0047 5,2874 6,5999 6,8500 ±0,3905 20,0350 0,0049 5,5172 6,8845
20,0350 0,0048 5,4023 6,7414 20,0272 0,0051 5,7471 7,1742 20,0210 0,0045 5,0575 6,3152 Kadar rata rata 6,8381
Kadmium 20,0380 0,1945 1,0446 1,3032 20,0281 0,1937 1,0403 1,2985 20,0350 0,1940 1,0419 1,3001 20,0350 0,1935 1,0392 1,2968
20,0272 0,1942 1,0430 1,3019 1,3004± 0,0024 20,0210 0,1940 1,0419 1,3010
Lampiran 5. Contoh Perhitungan kadar logam Timbal dalam sampel Kangkung Darat.
Misalnya untuk kadar Timbal dalam sampel kangkung darat dengan berat
20,0299 gram, absorbansi 0,0031
X = Konsentrasi sampel
Y = Absorbansi sampel
Persamaan garis regresi yang diperoleh dari kurva kalibrasi adalah
y = 0,00087x + 0,0001
x =
x = 3,4483 µg/ml
Maka konsentrasi sampel tersebut adalah 3,4483 µg/ml
Kadar = W CxVxFp
Keterangan : C = Konsentrasi larutan sampel (µg/ml)
V = Volume larutan sampel (ml)
Fp = Faktor pengenceran
W = Berat sampel sampel (gram)
Maka:
Kadar timbal dalam sampel =
Lampiran 6. Contoh Perhitungan kadar logam Kadmium dalam sampel
Kangkung darat
Misalnya untuk kadar Kadmium dalam sampel kangkung darat dengan berat
20,0299 ,absorbansi 0,1795
X = Konsentrasi sampel
Y = Absorbansi sampel
Persamaan garis regresi yang diperoleh dari kurva kalibrasi adalah
y = 0,1862x + 0,0000
x =
x = 0,9640 µg/ml
Maka konsentrasi sampel tersebut adalah 0,9640 µg/ml
Kadar = W CxVxFp
Keterangan : C = Konsentrasi larutan sampel (µg/ml)
V = Volume larutan sampel (ml)
Fp = Faktor pengenceran
W = Berat sampel (gram)
Maka:
Kadar kadmium dalam sampel =
Lampiran 7. Perhitungan Statistik Kadar Timbal pada Kangkung darat
No. X
Kadar (µg/g) X – X (X – X)
2
1 4,3039 0,0712 0,00506944
2 4,5920 0,3593 0,12909649
3 4,0178 0,2149 0,04618201
4 4,1617 0,0710 0,00504100
5 4,4454 0,2127 0,04524129
6 3,8752 0,3575 0,12780625
4,2327 ∑(X – X)2 = 0,35843648
SD = 0,2677
Pada interval kepercayaan 95% dengan nilai α = 0,05, df = 5 diperoleh nilai t tabel = α
/2,dk = 2,5706. Data ditolak jika t hitung ≥ t tabel atau t hitung ≤ - t table
t hitung =
n SD X X / −
t hitung data 1 =
6 / 0,2677 0712 , 0 = 0,6514
t hitung data 2 =
6 / 0,2677 3593 , 0
= 3,2873 (data ditolak)
t hitung data 3 =
6 / 0,2677 2149 , 0 = 1,9661
t hitung data 4 =
6 / 0,2677 0710 , 0 = 0,6496
t hitung data 5 =
6 / 0,2677 2127 , 0 = 1,9460
t hitung data 6 =
6 / 0,2677 3575 , 0
Untuk itu perhitungan diulangi dengan cara yang sama tanpa mengikutsertakan
data ke 2 dan data ke 6.
No. X
Kadar (µg/g)
X – X (X – X)2
1 4,3039 0,0717 0,00514089
3 4,0178 0,2144 0,04596736
4 4,1617 0,0705 0,00497025
5 4,4454 0,2132 0,04545424
4,2322 ∑(X – X)2 = 0,10153274
SD =
(
)
1 2 − −
∑
n X X = 3 0,10153274 = 0,1840Pada interval kepercayaan 95% dengan nilai α = 0,05, df = 3 diperoleh nilai t tabel = α
/2,dk = 3,1824. Data ditolak jika t hitung ≥ t tabel atau t hitung ≤ - t table
t hitung =
n SD X X / −
t hitung data 1 =
6 / 0,1840 0717 , 0 = 0,7793
t hitung data 3 =
6 / 0,1840 2144 , 0 = 2,3304
t hitung data 4 =
6 / 0,1840 0705 , 0 = 0,7663
t hitung data 5 =
6 / 0,1840 2132 , 0 = 2,3174
Karena t hitung < t tabel, maka semua data tersebut diterima.
Rata-rata kadar Timbal pada Kangkung darat adalah:
)
(
X
t
(α 2,df)SD
n
µ
=
±
μ = 4,2322 ± 3,1824 (0,1840 / √4)
Lampiran 8. Perhitungan Statistik Kadar Timbal pada Kangkung air
No. X
Kadar (µg/g) X – X (X – X)2
1 7,3137 0,4756 0,22619536
2 6,5999 0,2382 0,05673924
3 6,8845 0,0464 0,00215296
4 6,7414 0,0967 0,00935089
5 7,1742 0,3361 0,11296321
6 6,3152 0,5229 0,27342441
X 6,8381 ∑(X – X)2 = 0,68082607
SD = 0,3690
Pada interval kepercayaan 95% dengan nilai α = 0,05, df = 5 diperoleh nilai t tabel = α
/2,dk = 2,5706. Data ditolak jika t hitung ≥ t tabel atau t hitung ≤ - t table
t hitung =
n SD X X / −
t hitung data 1 =
6 / 0,3690 4756 , 0
= 3,1580 (data ditolak)
t hitung data 2 =
6 / 0,3690 2382 , 0 = 1,5817
t hitung data 3 =
6 / 0,3690 0464 , 0 = 0,3081
t hitung data 4 =
6 / 0,3690 0967 , 0 = 0,6421
t hitung data 5 =
6 / 0,3609 3361 , 0
= 2,2317
t hitung data 6 =
6 / 0,3609 5229 , 0
Untuk itu perhitungan diulangi dengan cara yang sama tanpa mengikut