68 Lampiran 1. Flowsheet pembuatan VCO
Diparut Ditimbang
Ditambahkan air, diperas Didiamkan selama 1 jam
Ditampung krim santan Ditambahkan dengan ragi tempe
Diaduk sampai homogen
Dimasukkan dalam corong pisah Didiamkan 24 jam sampai terbentuk
3 lapisan
Ditampung bagian atas (minyak)
disentrifuse selama 20 menit dengan kecepatan 2000 rpm Daging buah kelapa
Krim santan dan air
Minyak, protein dan air
69
Lampiran 2. Gambar proses pembuatan VCO sampai jadi emulsi VCO
Krim Santan
Air
Santan dan Ragi tempe Minyak Protein
Air
Minyak Protein
70 Lampiran 3. Flowsheet uji kualitas VCO
a. Kadar air
Ditimbang 5 g dalam botol timbang
Dipanaskan dalam oven T=105℃ selama 2 jam Didinginkan dalam desikator, selama 30 menit Ditimbang
b. Berat Jenis
Ditimbang
Dimasukkan VCO dalam piknometer Ditimbang kembali
Direndam dalam waterbath T= 25±0,2℃,30 menit Ditimbang
VCO
Berat konstan
Piknometer
71 c. Bilangan asam
Ditimbang sebanyak 5 g
Dimasukkan dalam erlenmeyer 250 ml
Ditambahkan alkohol 95% 50 ml, dipanaskan dan diaduk dengan hot plate
Dititrasi dengan KOH 0,1 N menggunakan indikator fenolftalein sampai warna merah jambu
VCO
72
Lampiran 4. Perhitungan rendemen minyak, berat jenis VCO
Kelapa = 4 buah
Berat Kelapa Parut = 2 Kg
Berat Jenis = 0,9072 g/ml
�=� �⁄
0,9072= ��900 ��
= 816, 48 g
�����������=(Berat Minyak)
(Berat Sampel) x 100%
����������� =816, 48 g
2000 g x 100%
= 40, 824%
Perhitungan berat jenis VCO
Berat piknometer = 11,731 g
Sampel+ piknometer = 16,267
���������� =(Berat piknometer + minyak)−(berat piknometer)
Volume air pada piknometer 5 (ml)
���������� =16,267 g−11,731 g
5 ml
73
Lampiran 5. Perhitungan kadar air dan bilangan asam VCO Berat Awal = 5 g
Berat Akhir = 4,999 g
Kadar air =Berat awal−berat akhir
Berat sampel x 100%
Kadar air =5 g−4,999 g
5 g x 100%
= 0,0333%
Perhitungan bilangan asam
NKOH = 0,0946N
BM KOH = 56,1
Massa Sampel (g) :M1 = 5,029 M2 = 5,030
M3 = 5,027
Volume KOH (ml) : V1 = 0,13 V2 = 0,13 V3 = 0,13
Bilangan Asam = ml KOH x NKOH x MrKOH Berat sampel
Bilangan Asam =0,13 � 0,0946�� 56,1 5, 029
74
Lampiran 6. Flowsheet pembuatan sediaan emulsi VCO
Diformulasi dengan dasar emulsi VCO
Sediaan uji (emulsi VCO) konsentrasi Tween 80 0,25%, 0,5%, 0,75%, 1%
Diuji mutu fisik
pH, tipe emulsi, viskositas, pemisahan fase, redispersibilitas,ukuran partikel dan
75 Lampiran 7. Perhitungan creaming
Waktu (minggu)
Pemisahan fase (creaming)
F1 F2 F3 F4 F5
V0 VU R V0 VU R V0 VU R V0 VU R V0 VU R
0 - - - -
1 5 2,3 0,46 - - - -
2 5 2,3 0,46 - - - -
3 5 2,3 0,46 - - - -
4 5 2,3 0,46 - - - -
5 5 2,3 0,46 - - - -
6 5 2,3 0,46 5 1,5 0,3 5 1,3 0,26 5 1 0,2 - - -
7 5 2,5 0,5 5 2,3 0,34 5 1,5 0,3 5 1,3 0,26 5 0,5 0,1
8 5 2,5 0,5 5 2,3 0,34 5 1,5 0,3 5 1,3 0,26 5 0,5 0,1
R = Vu / V0 Keterangan:
R : Perbandingan volume fase air terhadap volume total emulsi Vu : Volume fase air (ml)
76
78 Lampiran 8. (Lanjutan)
Cara perhitungan ukuran partikel
1 pixel = 0,026458334 cm = 264,58334 µm
Perbesaran Mikroskop = 10 x 40
2 pixel = 2 x 264, 58334 µm
= 528 µm/ 40
= 13,2 µm
Jumlah partikel 2 pixel = 100
= 100 x 13,2 µm
=1320 µm per lapangan pandang
Jumlah partikel total = 315 per lapangan pandang
Jumlah total ukuran pertikel = 11510,4 µm per lapangan pandang
Rata-rata = 11510,4 µm per lapangan pandang / 315 /
per lapangan pandang
79
Lampiran 9. Gambar buah kelapa, ragi tempe, alat peras kelapa
a.Buah kelapa b. Ragi tempe
80
Lampiran 10. Gambar pH meter , viskometer brookfield, neraca analitik dan mikroskop digital
a.pH meter Hanna b. Viskometer Brookfield
81
Lampiran 11. Gambar uji tipe emulsi, pengukuran pH, dan uji viskositas
a.Uji tipe emulsi b.Pengukuran pH emulsi
64
DAFTAR PUSTAKA
Ansel, H.C. (1989). Pengantar Bentuk Sediaan Farmasi. Edisi keempat. Jakarta: UI-Press. Halaman 326 - 342.
APCC. (2008). APCC Standards for Virgin Coconut Oil. http://
Bawalan, D.D. (2011). Processing Manual for Virgin Coconot Oil, its Products and By-Products for Pacific Island Countries and Territories. Secretariat of the Pacific Community Noumea, New Caledonia. Halaman 32 - 34. Cahyono., dan Untari, L. (2009). Proses Pembuatan Virgin Coconut Oil dengan
fermentasi Menggunakan Starter Ragi Tempe. Semarang: Jurusan Teknik Kimia, Universitas Diponegoro.
Campo, I., Yagmur, A., Garti, N., leser, M.E., Folmer, B dan Glatter, O. (2004). Five componenr food-grade microemulsions: structural characterization by SANS. Journal of Colloid Interface Science. 274(4): 251 - 267.
Darmoyuono, W. (2006). Gaya Hidup Sehat Dengan Virgin Coconut Oil. Jakarta: Gramedia. Halaman 61.
Ditjen POM. (1995). Farmakope Indonesia. Edisi Ke IV. Jakarta: Departemen Kesehatan RI. Halaman 749.
Febrina, E., Gozalih, D., dan Rusdiana, T. (2007). Formulasi Sediaan Emulsi
Buah Merah sebagai Produk Antioksidan Alami. Bandung: Fakultas
Farmasi, Universitas Padjadjaran. Halaman 39 – 50.
Florence, A.T., dan Attwood, D. (2006). Physicochemical Principles of
Pharmacy. Fourth Edition. United Kingdom: Pharmaceutical Press.
Halaman 229 – 239.
Friberg, S.E. (1997). Emulsion Stability. Dalam: Food Emulsion, Friberg, S.E. and K. Larrson (Eds). Marcel Dekker, New York. Halaman 1 - 4.
Gani, Z., Yuni., dan Dede. (2005). Bebas Segala Penyakit dengan VCO (Virgin Coconut Oil). Jakarta: Penebar Swadaya. Halaman 1, 4.
Gennaro, R.A. (1990). Remington’s Pharmaceutical Sciences. 18 th Edition.
USA: Marck Printing Company Easton. Halaman 712.
65
Gupta, A., Malav, A., Singh, A., Gupta, M.K., Khinchi, M.P., Sharma, N., dan Agrawal, D. (2010). Coconut Oil: The Healthiest Oil on Earth.
International Journal of Pharmaceutical Sciences and Research. 1(6): 19-26.
Hedge, B.M. (2006). Coconut Oil-Ideal fat next only to Mother’s Milk. J. Indian Academy of Clinical Medicine. 7(1):16-19.
Ishwanto, T.I.L.G. (2001). Bioproses Enzimatik dan Purifikasi Minyak Kelapa Fermentasi (femikel). Bogor: Fakultas Teknologi Pertanian, Universitas Djuanda. Halaman 91.
Joshi, H.C., Pandey, I.P., Kumar, A., Garg, N. (2012). A Study of Various Factors Determining The Stability of Molecules. Advances in Pure and Appl Chem. 1(1): 7 - 11.
Ketaren, S. (1986). Pengantar Teknologi Minyak dan Lemak Pangan. Jakarta: UI-Press. Halaman 113.
Ketaren, S. (2005). Minyak dan Lemak Pangan. Jakarta: Universitas Indonesia. Halaman 49 - 65.
Kim, H.J., Decker, E.A., dan Mcclements, D.J. (2003). Influence of Sucrose on Droplet Flocculation in Hexadecane oil-in-water Emulsions Stablilized by β-Lactoglobulin. Agriculture and Food Chemistry. 51(3): 766 – 772.
Kulshreshtha, A.K., Singh, O.N., dan Wall, G.M. (2010). Pharmaceutical Suspensions. London: AAPS Press. Halaman 4 – 10.
Lachman, L., Lieberman, H.A., dan Kanig, J.L. ( 1994). Teori dan Praktek Farmasi Industri. Edisi ke III. Jakarta: Universitas Indonesia. Halaman 760.
Lieberman, S., Enig, M.G., dan Preuss, H.G. (2006). A Review of Monolaurin and Lauric Acid. Alternative and Complementary Therapies. 12(5): 310 – 312. Marchaban. (2005). Kemampuan Solubilisasi Surfaktan karena Perbedaan
Panjang Rantai Lifofil dan Hidrofil. Majalah Farmasi Indonesia. 16(2):105 - 109
Martin, A., Swarbrik, J., Cammarata, A. (1993). Dasar-dasar Farmasi Fisik dalam Ilmu Farmasetik. Alih Bahasa Yoshita. Edisi Ketiga. Jakarta: UI Press. Halaman 924 - 950, 1255.
66
Mentawai, I. (2005). Ringkasan Manfaat Kesehatan Virgin Coconut Oil. http:// indo-coco.com/ (9 Februari 2005).
Murtiningrum., Sarungallo, Z.L., Cepeda, G.N., dan Olong, N. (2013). Stabilitas Emulsi Minyak Buah Merah pada berbagai Nilai HLB Pengemulsi. Jurnal Teknik Industri Pertanian. 23(1): 30 - 37.
Nawansih, O., dan Nurainy, F. (2007). Efek Pateurisasi terhadap Karakteristik
Santan yang Distabilkann dengan CMC Selama Penyimpanan Dingin.
Prosiding Seeminar Hasil Penelitian dan Pengabdian Kepada Masyarakat. Universitas Lampung.
Nevin, K.G., dan Rajamohan, T. (2006). Virgin Coconut Oil Supplemented Diet Increase the Antioxidant Status in Rats. Food Chem. 99: 260 – 266.
Purba, E.M. (2012). Pembuatan Minyak Kelapa Murni Dengan Metode Fermentasi. Skripsi. Medan: Fakultas Farmasi.
Rawlins, E.A. (2003). Bentley’s textbook of Pharmaceutics. Edisi ke-18. London: Bailierre Tindall. Halaman 22, 355.
Rohman, A., Che Man, Y.B., dan Norviana, E. (2012). Analysis of Emulsifier in Food Using Chromatograpic Techniques. J. Food Pharm Sci. 1(20): 1-6. Rowe, R. C., Paul, J.S., dan Marian, E.Q. (2009). Handbook of Pharmaceuutical
Expients. Six edition. Pharmaceutical Press. London. Hal. 1, 75, 442, 550, 704.
Setiaji, B., dan Prayugo., S. (2006). Membuat VCO Berkualitas Tinggi. Seri Agriteknologi. Cetakan Kedua. Jakarta: Penebar Swadaya. Halaman 43, 50, 55.
Silalahi, J. (2012). Manfaat Minyak Kelapa untuk Meningkatkan Kesehatan. Dalam: Pemikiran Guru Besar Universitas Sumatera Utara dalam Pembangunan nasional. Medan: USU Press. Halaman 30 – 35.
Silalahi, J., dan Nurbaya, S. (2011). Komposisi, Distribusi dan Sifat aterogenik Asam Lemak di dalam Minyak Kelapa dan Kelapa Sawit. Majalah Kedokteran Indonesia. 61(11): 456.
Standarisasi Nasional Indonesia. (2008). Minyak Kelapa Murni. SNI 7381:2008 Jakarta: Departemen Perindustrian RI. Halaman 2.
67
Subroto, A. (2006). VCO Dosis Tepat Taklukkan Penyakit. Cetakan Pertama. Jakarta: Penebara Swadaya. Halaman 7.
Sukmadi, B., dan Nugroho, N.B. (2002). Kajian Penggunaan Inokulum Pada Produksi Minyak Kelapa Secara Fermentasi. J Biosains Bioteknol Indones. 10(2): 12 - 17
Surtami., dan Rozaline, H. (2005). Takulukan Penyakit Denagn VCO. Seri Agrisehat. Cetakan Ketiga. Jakarta: Penebar Swadaya. Halaman 5, 9, 22, 28.
Syukri, Y., Sari, F., dan Zahliyatul, S. (2009). Stabilitas Fisik Emulsi Ganda Virgin Coconot Oil Menggunakan Emulgator Span 80 dan Tween 40.
Skripsi. Jakarta: Jurusan Farmasi FMIPA, Universitas Islam Indonesia. Halaman 33 – 41.
Villarino, B.J., dan Lizada, M.A.C.C. (2007). Descriptive Sensory Evaluation of Virgin Coconut Oil and Refined, Bleached dan Deodorized Coconut Oil.
Food Science and Technology. 40(5): 193 – 199.
Viyoch J, Klinthong N., dan Siripaisal W. (2003). Development of Oil-in Water Emulsion Containing Tamarind Fruit Pulp Extract. Naresuan University J. 21(4): Halaman 29 - 49.
Wang, L.L., dan Johnson, E.A. (1992). Inhibition of Listeria Monocytogenes by Fatty Acids and Monoglycerides. Applied and Environmental Microbiologi. 19(3): Halaman 58.
Wardani, I.E. (2007). Uji Kualitas VCO Berdasarkan Cara Pembuatan dan Proses Pengadukan Tanpa Pemancingan dan Proses Pengadukan dengan Pemancingan. Skripsi. Fakultas MIPA UNS. Halaman 2.
Wathoni, N., Soebagio, B., Rusdiana, T. (2007). Efektivitas Lecithin sebagai
Emulgator dalam Sediaan Emulsi Minyak Ikan. Jatinangor: Fakultas
Farmasi, Universitas Padjadjaran. Halaman 22 – 31.
31
BAB III
METODOLOGI PENELITIAN
3.1 Metode Penelitian
Metode penelitian ini dilakukan secara eksperimental yaitu melihat pengaruh variasi konsentrasi Tween 80 yang dikombinasi dengan gom arab dalam stabilitas sediaan emulsi VCO. Penelitian ini meliputi pemeriksaan organoleptis, berat jenis, kadar air, bilangan asam, rendemen minyak dari VCO, uji pH, uji tipe emulsi, pengamatan creaming, uji viskositas, uji redispersibilitas (pengocokan), ukuran partikel dan distribusi partikel emulsi VCO. Penelitian ini dilaksanakan di laboratorium Farmasi Fisik Fakultas Farmasi Universitas Sumatera Utara.
3.2 Alat-alat
Alat-alat yang digunakan adalah stoples transparan, botol timbang, oven (Fisher Isotem 500 Series), desikator, labu ukur (Pyrex), erlenmeyer (Pyrex), buret (Pyrex), klaim, statif, gelas ukur (Pyrex), pipet tetes, piknometer (Pyrex), corong pisah (Interkey), batang pengaduk, spatel, lumpang, stamfer, objek gelas (Pyrex), neraca analitik (Boeco), pH meter (Hanna), mikroskop, dan viskometer brookfield.
3.3 Bahan-bahan
32
(Merck), Tween 80 (Merck), sukrosa, nipagin (Merck), butil hidroksi toluen (Merck), aquadest.
3.4Prosedur Kerja 3.4.1. Pembuatan VCO
Empat buah kelapa diparut dan diperoleh berat 2 kg kelapa parut lalu ditambahkan air dengan perbandingan 1:1 artinya 2 kg kelapa parut dicampur dengan 2 liter air, kemudian diperas dan disaring untuk memperoleh santan. Santan dimasukkan kedalam stoples transparan kemudian didiamkan selama 1 jam hingga terbentuk 2 lapisan, lapisan atas yaitu krim santan dan lapisan bawah yaitu air. Krim santan diambil dan diperolah sebanyak 1 liter. Selanjutnya ditambahkan ragi tempe dengan perbandingan 5:1 artinya 1000 ml krim santan dan 200 g ragi tempe. Kemudian diaduk, dimasukkan kedalam corong pisah, didiamkan selama 24 jam pada suhu kamar, sesudah pendiaman terbentuk tiga lapisan yaitu lapisan atas (minyak), lapisan tengah (protein) dan lapisan bawah (air). Selanjutnya dilakukan pemisahan terhadap lapisan-lapisan yang terbentuk yaitu lapisan minyak, protein, air dengan cara membuka krannya dan menampung masing-masing lapisan. Lapisan minyak yang diperoleh di sentrifuge selama 20 menit dengan kecepatan 2000 rpm untuk mendapat minyak yang baik (Cahyono dan Untari, 2009).
3.4.2.4 Kadar minyak
33
Kadar minyak =Berat Minyak
Berat Sampel x 100%
3.4.2 Uji mutu VCO 3.4.2.1 Kadar air
Ditimbang VCO sebanyak 5 g dalam botol timbang, kemudian dimasukkan kedalam oven pada suhu 1050C selama 2 jam lalu didinginkan dalam desikator selama 30 menit. Ditimbang kembali botol timbang untuk memperoleh berat konstan (Standarisasi Nasional Indonesia, 2008).
Kadar air =Berat awal−Berat akhir
Berat sampel x 100%
3.4.2.2Bilangan Asam
Ditimbang VCO sebanyak 5 g kemudian dimasukkan kedalam erlenmeyer 250 ml. Ditambahkan alkohol 95% sebanyak 50 ml lalu dipanaskan dan diaduk dengan hot plate. Setelah dingin dititrasi dengan KOH 0,1 N menggunakan indikator fenolftalein sampai berwarna merah jambu (Standarisasi Nasional Indonesia, 2008).
Bilangan asam =ml KOH x N KOH x Mr KOH Berat Sampel
3.4.2.3Berat jenis
Ditimbang berat piknometer kosong lalu masukkan VCO kedalam piknometer dan ditimbang kembali. Setelah itu direndam dalam waterbath pada suhu 25 ± 0,20C selama 30 menit dan ditimbang berat piknometer tersebut (Ketaren, 1986).
34
3.5 Penentuan Emulgator dan Formulasi Emulsi VCO 3.5.1 Penentuan emulgator
Untuk menentukan emulgator yang cocok dalam pembuatan sediaan emulsi VCO, dibuat suatu basis emulsi dengan menggunakan beberapa emulgator yang biasa digunakan diantaranya gom arab, CMC Na, Span 60, Tween 80 dan diamati kestabilannya seperti terlihat pada Tabel 3.1. Emulgator yang menghasilkan basis emulsi paling baik digunakan untuk membuat formula selanjutnya.
Tabel 3.1 Formula basis emulsi VCO
Bahan (%) F1 F2 F3 F4 F5
VCO 25 25 25 25 25
Gom arab 20 - 20 - 20
Tween 80 - 1 1 1 -
Span 60 - - - 20 -
CMC Na - - - - 2
Akuades sampai 100 100 100 100 100
Cara Pembuatan: Formula 1
35
Formula 2
Dibuat dengan menggunakan metode gom kering. Di dalam mortir minyak bersama Tween 80 yang telah dilarutkan dengan sedikit air diaduk sampai homogen, kemudian ditambahkan air sekaligus sambil diaduk cepat sampai terbentuk inti emulsi lalu ditambahkan air sampai jumlah yang ditentukan (Ansel, 1989).
Formula 3
Dibuat dengan menggunakan metode gom kering. Di dalam mortir minyak bersama gom diaduk sampai homogen, kemudian ditambahkan air sekaligus sambil diaduk cepat sampai terbentuk inti emulsi lalu ditambahkan Tween 80 sedikit demi sedikit kemudian ditambahkan air sampai jumlah yang ditentukan (Ansel, 1989).
Formula 4
Dibuat dengan menggunakan metode gom kering. Di dalam mortir minyak bersama Span 60 diaduk sampai homogen, kemudian ditambahkan air sekaligus sambil diaduk cepat sampai terbentuk inti emulsi lalu ditambahkan Tween 80 sedikit demi sedikit kemudian ditambahkan air sampai jumlah yang ditentukan (Ansel, 1989).
Formula 5
36
Masing-masing formula diamati meliputi warna, bau dan pemisahan fase. 3.5.2 Formulasi emulsi VCO
Hasil pengamatan dari penentuan emulgator menunjukkan bahwa formula basis emulsi dengan menggunakan emulgator Tween 80 dan gom arab merupakan basis emulsi kombinasi terbaik di antara keempat basis emulsi yang lain. Oleh karena itu dibuat variasi konsentrasi Tween 80 0,25, 0,5, 0,75 dan 1% yang dikombinasi dengan gom arab 20%, nipagin 0,1%, sukrosa 20%, butil hidroksi toluen 0,1% (Rowe, et al., 2009). Formula emulsi VCO dapat dilihat pada Tabel 3.2.
Tabel 3.2 Formula emulsi VCO
Bahan (%) F1 F2 F3 F4 F5
VCO 25 25 25 25 25
Gom arab 20 20 20 20 20
Tween 80 - 0,25 0,5 0,75 1
Nipagin 0,1 0,1 0,1 0,1 0,1
Sukrosa 20 20 20 20 20
Butil hidroksi toluen 0,1 0,1 0,1 0,1 0,1
Akuades sampai 100 100 100 100 100
3.6 Cara Pembuatan Emulsi VCO
37
3.7 Evaluasi terhadap Sediaan 3.7.1 Pengamatan organoleptis
Pengamatan organoleptis yang diamati meliputi pengamatan bentuk, konsistensi, warna, rasa serta bau dari emulsi VCO secara visual (Ditjen POM, 1995).
3.7.2 Pengukuran pH
Penentuan pH sediaan dilakukan dengan menggunakan alat pH meter. Alat terlebih dahulu dikalibrasi dengan menggunakan larutan dapar standar netral (pH 7,01) dan larutan dapar pH asam (pH 4,01) hingga alat menunjukkan harga pH tersebut. Kemudian elektroda dicuci dengan aquadest, lalu dikeringkan dengan tissue. Sampel dibuat dalam konsentrasi 1% yaitu ditimbang 1 g sediaan dan dilarutkan dalam 100 ml aquadest. Kemudian elektroda dicelupkan dalam larutan tersebut. Dibiarkan alat menunjukkan nilai pH sampai konstan. Angka yang ditunjukkan pH meter merupakan pH sediaan (Rawlins, 2003).
3.7.3 Penentuan tipe emulsi
Penentuan tipe emulsi sediaan dilakukan dengan penambahan sedikit metilen biru pada permukaan emulsi. Jika air merupakan fase eksternal m/a, bahan pewarna akan terlarut dan berdifusi merata dalam air. Jika emulsi bertipe a/m, partikel-partikel bahan pewarna akan menggumpal pada permukaan (Martin, et al., 2011).
3.7.4 Pengamatan creaming
38
3.7.5 Penentuan viskositas
Pengukuran viskositas dilakukan dengan menggunakan viskometer Brookfield. Viskometer disiapkan, dipasang spindle no.61, diukur viskositas sediaan pada kecepatan putar spindle 12 rpm, kemudian hasil pembacaan dikalikan dengan faktor koreksi yang ada pada alat tersebut.
3.7.6 Uji redispersibilitas
Uji redispersibilitas dilakukan dengan cara mengocok masing-masing sediaan uji, kemudian dihitung jumlah pengocokan yang diperlukan sampai sediaan emulsi terdispersi kembali.
3.7.7 Ukuran partikel dan distribusi partikel terdispersi
Pemeriksaan stabilitas sediaan meliputi ukuran partikel dan distribusi partikel terdispersi menggunakan mikroskop. Ukuran partikel terdispersi ditentukan dengan pengamatan dibawah mikroskop yang diproyeksikan ke sebuah layar dan dilakukan pemotretan dari slide yang sudah disiapkkan. Pada sistem ini akan muncul ukuran partikel dalam bentuk pixel selanjutnya diubah kedalam bentuk µm (1 pixel= 264, 58334 µm). Dari hasil pengamatan kemudian di plot
grafik waktu versus ukuran partikel terdispersi sehingga diamati perubahan ukuran partikel terdispersi. Ukuran rata-rata partikel terdispersi yang semakin kecil menandakan produk emulsi semakin stabil.
39
BAB IV
HASIL DAN PEMBAHASAN
4.1 Hasil Uji Mutu VCO
4.1.1 Karakteristik organoleptis VCO
VCO berbentuk cairan encer berwarna bening, mempunyai rasa tawar serta bau yang khas. Saat diminum VCO mempunyai rasa khas minyak nabati serta rasa yang tidak enak sebab cairan berbentuk minyak ini tidak larut air sehingga tetap meninggalkan bekas minyak di lidah yang menimbulkan rasa tidak nyaman bagi penggunanya.
4.1.2 Kadar air, bilangan asam dan bobot jenis VCO
Data perhitungan hasil penelitian dapat dilihat pada Lampiran 4 dan 5. Hasil penelitian tentang pembuatan VCO dengan ragi tempe secara fermentasi secara keseluruhan dapat dilihat pada Tabel 4.1.
Tabel 4.1. Data kadar air, bilangan asam dan bobot jenis VCO
No Parameter Hasil
1 Kadar air 0,03%
2 Bilangan asam 0,1389%
3 Bobot Jenis 0,915
4 Rendemen Minyak 40,82%
40
1986). Penelitian yang dilakukan oleh Purba (2012), menggunakan ragi tempe dan ragi roti untuk uji kualitas kadar air diperoleh sebesar 0,1193%.
Bilangan asam VCO yang diperoleh dalam penelitian ini memenuhi standar SNI yaitu 0,2%. Semakin tinggi bilangan asam maka semakin rendah kualitasnya. Penelitian yang dilakukan oleh Purba (2012), menggunakan ragi tempe dan ragi roti untuk uji bilangan asam diperoleh sebesar 0,1373%. Sedangkan penelitian yang dilakukan oleh Cahyono dan Untari (2009), menggunakan ragi tempe diperoleh bilangan asam 0,483%.
Berat jenis VCO yang diperoleh dalam penelitian ini memenuhi standart APCC (Asian Pacific Coconut Community) yaitu sebesar 0,915 - 0,920. Penelitian yang dilakukan oleh Cahyono dan Untari (2009), untuk uji kualitas berat jenis menggunakan ragi tempe diperoleh berat jenis 0,914.
4.2 Penentuan Emulgator dan Formulasi Emulsi VCO 4.2.1 Penentuan emulgator (basis emulsi)
Sebelum dipilih emulgator yang cocok untuk pembuatan emulsi VCO, maka terlebih dahulu dilakukan pengamatan terhadap beberapa basis emulsi seperti yang terlihat pada Gambar 4.1. Hasil pengamatan basis emulsi dapat dilihat pada Tabel 4.2.
Gambar 4.1. Basis emulsi VCO
F5
F4
F3
41
Tabel 4.2. Pengamatan basis emulsi VCO
Formula Pengamatan
Warna Bau Sifat fisik
F1 Putih Kekuningan Khas Creaming, mudah didispersikan kembali
F2 Putih Khas Creaming, agak sukar didispersikan kembali
F3 Putih Khas Tidak memisah
F4 Putih Khas Creaming, sukar didispersikan kembali
F5 Putih Khas Creaming, mudah dididpersikan kembali
Basis emulsi dengan emulgator Span 60 dan Tween 80 mempunyai konsistensi yang buruk karena pemisahannya sangat cepat (sejak hari pertama pembuatan sudah terjadi pemisahan) dan membutuhkan pengocokan yang lama agar terdispersi kembali. Basis emulsi F1 (gom arab), F2 (Tween 80), F5 (gom arab dan CMC Na) menghasilkan emulsi yang lebih baik walaupun memisah namun masih lebih mudah didispersikan kembali. Basis emulsi F3 (gom arab dan Tween 80) merupakan basis yang terbaik di antara basis yang lain dengan warna dan konsistensi yang lebih homogen serta mudah didispersikan kembali membentuk massa yang homogen. Dalam pembuatan emulsi oral masih diperbolehkan pembentukan cream karena sifatnya yang reversible dan mudah didispersikan kembali (Ansel, 1989).
42
monomolekular. Tween 80 bersifat hidrofilik karena keberadaan gugus hidroksil dan oksietilen. Gugus tersebut mengakibatkan pengemulsi mampu membentuk ikatan hidrogen dengan molekul air (Marchaban, 2005; Joshi, et al., 2012).
Gom arab bekerjanya sebagai zat pengemulsi terutama karena dapat membentuk suatu lapisan multimolekuler pada antarmuka dan lapisan yang terbentuk tersebut kuat dan menghambat terjadinya penggabungan. Efek tambahan yang mendorong emulsinya menjadi stabil adalah kenaikan viskositas yang bermakna dari medium dispers. Karena zat pengemulsi itu membentuk lapisan-lapisan multilayer sekeliling tetesan yang bersifat hidrofilik, maka zat ini cenderung untuk membentuk emulsi m/a (Martin, et al., 1993).
Tween 80 dan gom arab banyak digunakan secara luas dalam pembuatan emulsi minyak-minyak lemak serta mempunyai sifat lebih mudah larut dalam air. Oleh karena itu, berdasarkan sifat-sifat di atas serta hasil orientasi basis emulsi maka emulgator kombinasi Tween 80 dengan gom arab dipilih untuk membuat formula selanjutnya. Pada penelitian ini dipilih jenis emulsi minyak dalam air (m/a) untuk memudahkan penggunaan serta untuk kenyamanan pada waktu digunakan (Martin, et al., 2011).
4.2.2 Formulasi emulsi VCO
Formula emulsi VCO yang dibuat dapat dilihat pada Tabel 3.2. Jumlah gom arab yang biasa digunakan dalam pembuatan emulsi adalah sebanyak 10 - 20% (Rowe, et al., 2009). Berdasarkan Rowe gom arab yang digunakan dalam formula di bawah adalah 20% (b/b).
43
mencegah kerusakan pada sediaan emulsi yang dapat disebabkan oleh mikroba ataupun oksidasi oleh udara. Pengawet yang digunakan untuk fase air yang bekerja sebagai antimikroba yaitu nipagin, sedangkan untuk fase minyak biasanya digunakan antioksidan untuk mencegah ketengikan. Nipagin sebagai antimikroba untuk fase air sebanyak 0,015% - 0,2%. BHT sebagai antioksidan untuk fase minyak sebanyak 0,01% - 0,1%. (Rowe, et al., 2009). Nipagin dan BHT yang digunakan dalam formula di atas adalah masing-masing 0,1%. Hasil emulsi VCO dapat dilihat pada Gambar 4.2.
Gambar 4.2. Emulsi VCO
Keterangan:
F1 : Tween 80 0% dan gom arab 20% F2 : Tween 80 0,25% dan gom arab 20%
44
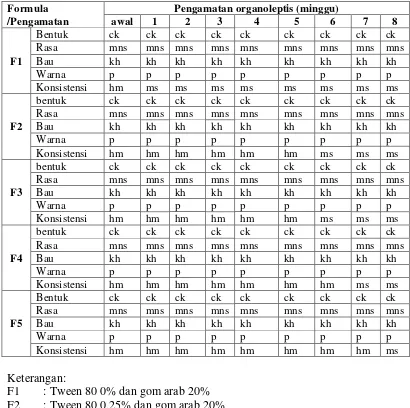
4.3 Hasil Evaluasi Emulsi VCO 4.3.1 Pengamatan organoleptis
Hasil data pengamatan dapat dilihat pada Tabel 4.3.
Tabel 4.3. Data pengamatan organoleptis selama 8 minggu penyimpanan
Formula /Pengamatan
Pengamatan organoleptis (minggu)
45
Hasil pengamatan organoleptis menunjukkan bahwa sediaan emulsi tidak mengalami perubahan selama 8 minggu penyimpanan, baik dari segi bentuk, rasa, bau, warna, tetapi dari segi konsistensinya sediaan formula 5 memisah pada 7 minggu penyimpanan dan formula yang lain lebih awal memisah. Hasil pengamatan ini juga membuktikan bahwa zat - zat lain yang ditambahkan ke dalam sediaan emulsi seperti pemanis, pengawet, antioksidan tercampurkan secara baik satu sama lain. Warna sediaan emulsi antara formula yang satu dengan yang lain sedikit berbeda sesuai dengan banyaknya penambahan Tween 80. Semakin banyak penambahan Tween 80 maka sediaan emulsi akan menghasilkan warna yang lebih cerah.
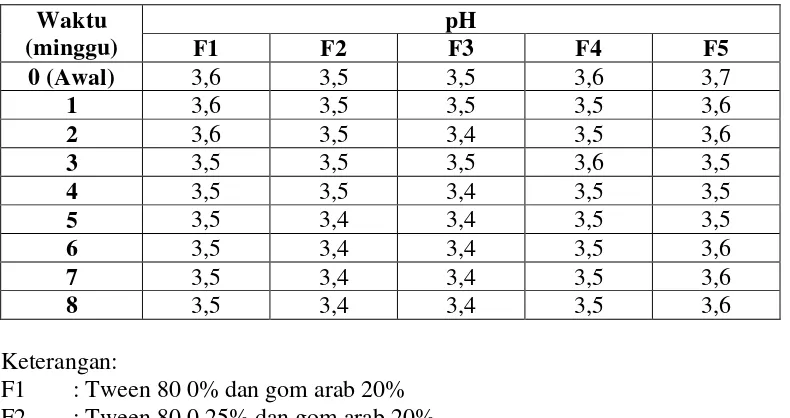
4.3.2 Pengukuran pH
Hasil pengukuran pH emulsi VCO yang disimpan pada suhu kamar ditunjukkan pada Tabel 4.4.
46
Pada Tabel 4.4 terlihat bahwa masing-masing formula emulsi memiliki pH asam yaitu 3,4 – 3,7 selama 8 minggu penyimpanan. Ini dapat disebabkan karena banyaknya kandungan asam pada VCO yang menyebabkan pH dari sediaan menjadi asam. Komponen utama VCO adalah asam lemak jenuh yang terdiri dari ± 53% asam laurat dan sekitar 7% asam kaprilat serta asam lemak tidak jenuh sehingga VCO memiliki pH asam (Wardani, 2007)
Dari data diatas dapat dilihat bahwa pH masing–masing formula sediaan emulsi selama 8 minggu penyimpanan mengalami sedikit penurunan. Penurunan pH ini dapat terjadi karena VCO dalam masing–masing formula terhidrolisis. Ini terjadi karena dalam sediaan emulsi mengandung air yang dapat menyebabkan VCO terhidrolisis sehingga mengeluarkan ion H+ yang lebih banyak dan membuat
pH sediaan semakin menurun. Meskipun terjadi penurunan pH dari masing– masing formula, tetapi sediaan tersebut masih aman digunakan.
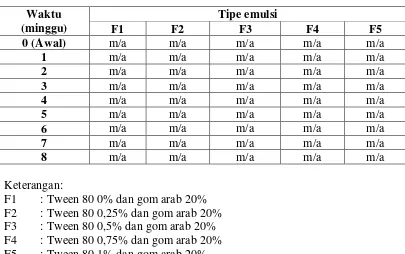
4.3.3 Penentuan tipe emulsi
Hasil untuk uji tipe emulsi dengan menambahkan metilen biru pada emulsi dapat dilihat pada Gambar 4.3 dan Tabel 4.5.
47
Tabel 4.5. Data penentuan tipe emulsi Waktu
Sediaan emulsi VCO yang dibuat mempunyai tipe emulsi m/a karena metilen biru yang ditambahkan pada masing - masing formula terlarut dan berdifusi merata dalam air. Tipe emulsi m/a yang diberikan secara oral memiliki keuntungan mudah dimakan dan ditelan sampai ke lambung (Ansel, 1989). Data diatas menunjukkan bahwa masing-masing formula selama 8 minggu penyimpanan tidak mengalami perubahan tipe emulsi (inversi) dari sediaan yang dibuat yang artinya emulsi stabil.
4.3.4 Pengamatan creaming
48
Gambar 4.3. Pembentukan creaming pada emulsi selama 8 minggu penyimpanan 0 (Awal)
3 minggu
2 minggu 1 minggu
4 minggu 5 minggu
6 minggu 7 minggu
Setelah diredispersi
49
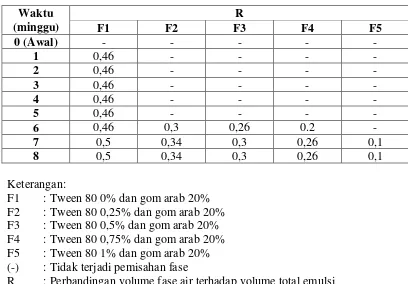
Tabel 4.6. Pembentukan creaming pada emulsi selama 8 minggu penyimpanan Waktu
(-) : Tidak terjadi pemisahan fase
R : Perbandingan volume fase air terhadap volume total emulsi
Dari tabel diatas menunjukkan bahwa formula 1 pada 1 minggu sampai 8 minggu penyimpanan menunjukkan terjadinya pembentukan creaming yang terus mengalami peningkatan seiring bertambahnya umur sediaan sedangkan pada formula 2, 3, 4 dan 5 pembentukan creaming terjadi pada penyimpanan 7 minggu sampai 8 minggu. Perbedaan penggunaan konsentrasi Tween 80 pada gom arab 20% berpengaruh pada peningkatan terjadinya creaming emulsi selama penyimpanan. Apabila semakin kecil konsentrasi Tween 80 yang digunakan maka kemampuannya untuk membentuk lapisan monomelekuler pada fase minyak semakin berkurang, sehingga mengakibatkan mudahnya bergabung antara molekul minyak dengan minyak sehingga terjadi creaming.
50
sehingga kecepatan pembentukan creaming semakin lambat dan emulsi semakin stabil. Formula 5 dengan konsentrasi Tween 80 1% merupakan formula dengan creaming terkecil. Ini berarti formula 5 merupakan formula yang paling stabil karena kecepatan pembentukan creamnya paling kecil. Menurut persamaan Stokes laju pemisahan fase terdispersi dari emulsi dapat dihubungkan dengan faktor-faktor seperti ukuran partikel dari fase terdispersi, perbedaan dalam kerapatan antar fase dan viskositas fase luar.
Penelitian yang dilakukan oleh Syukri (2008), mengunakan emulgator Span 80 dan Tween 40 pada pembuatan emulsi VCO, diperoleh creaming yang semakin tinggi selama 4 minggu penyimpanan.
4.3.5 Pengukuran viskositas
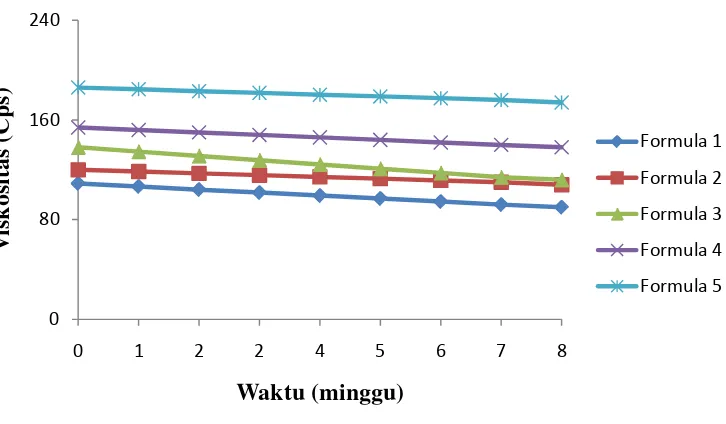
Hasil pengukuran viskositas selama 8 minggu dapat dilihat pada Tabel 4.7. Gambar 4.4, menunjukkan bahwa masing-masing formula mengalami penurunan viskositas selama penyimpanan.
51
Gambar 4.4 Grafik pengukuran viskositas selama 8 minggu penyimpanan Viskositas merupakan nilai yang menunjukkan satuan kekentalan medium pendispersi dari suatu sistem emulsi. Semakin tinggi viskositas suatu emulsi, semakin baik penghambatan agregasi atau penggabungan kembali droplet (Kim, et al., 2003).
Pada sistem emulsi tipe m/a, penambahan Tween 80 akan meningkatkan viskositas sehingga dapat membentuk sistem emulsi yang lebih stabil. Viskositas yang paling besar dimiliki oleh emulsi formula 5 yaitu Tween 80 1%. Pada awal pembuatan emulsi tanpa penambahan Tween 80 memiliki viskositas sebesar 109 cps, sedangkan setelah penambahan Tween 80 viskositas meningkat hingga 120 – 186 cps.
Selama 8 minggu penyimpanan viskositas masing-masing formula emulsi cenderung mengalami penurunan. Penurunan viskositas tersebut diikuti oleh penurunan stabilitas emulsi VCO. Hal ini karena pada viskositas yang rendah, fase terdispersi (droplet) akan mudah bergerak dalam medium pendispersi sehingga peluang terjadinya tabrakan antara sesama droplet semakin tinggi dan
52
droplet akan cenderung bergabung menjadi partikel yang lebih besar dan menggumpal.
Terjadinya penurunan viskositas selama penyimpanan diduga terkait dengan penurunan kemampuan Tween 80 dalam menstabilkan sistem emulsi. Menurut Nawansih dan Nurainy (2007), kestabilan Tween 80 pada penyimpanan sari buah semakin menurun yang disebabkan oleh terputusnya molekul Tween 80 dengan ikatan hidrogen yang mengikat air. Efektivitas Tween 80 dan gom arab dalam proses pengentalan sangat dipengaruhi oleh konsentrasi dan derajat polimerisasi. Dalam kondisi tertentu ikatan glikosida dan hidrokoloid peka terhadap reaksi hidrolisis yang menyebabkan degradasi Tween 80 dan gom arab. Selain itu beberapa mikroba dapat menghasilkan eksoenzim yang juga dapat menyebabkan terjadinya degradasi Tween 80 dan gom arab.
Penelitian yang dilakukan oleh Syukri, et al., (2008), mengunakan emulgator Span 80 dan Tween 40 pada pembuatan emulsi VCO diperoleh viskositas yang menurun perlahan-lahan seiring dengan bertambahnya umur sediaan.
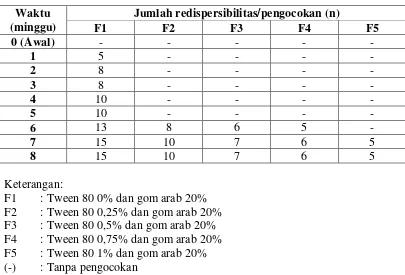
4.3.6 Redispersibilitas
53
Tabel 4.8. Redispersibilitas emulsi selama 8 minggu penyimpanan Waktu
Pembentukan creaming masih diperbolehkan dalam suatu sediaan emulsi oral karena terjadinya creaming bersifat reversibel, artinya dengan pengocokan yang cukup emulsi tersebut dapat kembali homogen. Berbeda dengan koalesensi/breaking (pecahnya sediaan emulsi) yang bersifat irreversibel (Ansel, 1989).
4.3.7 Ukuran partikel dan distribusi partikel terdispersi 4.3.7.1 Ukuran partikel terdispersi
54
50 µm
100 µm 50 µm
50 µm 100 µm
Gambar 4.5a. Ukuran partikel F1 (tanpa Tween 80) perbesaran 40x10 selama 8 minggu
50 µm 100 µm 50 µm
50 µm 100 µm 6 minggu
4 minggu 2 minggu
0 (awal)
0 (awal) 2 minggu 4 minggu
6 minggu
8 minggu
55
Gambar 4.5b. Ukuran partikel F2 (Tween 80 0,25%) perbesaran 40x10 selama 8 minggu
50 µm 100 µm 50 µm
100 µm 50 µm
Gambar 4.5c. Ukuran partikel F3 (Tween 80 0,5%) perbesaran 40x10 selama 8 minggu
25 µm 50 µm 25 µm
50 µm 25 µm
6 minggu
4 minggu 2 minggu
0 (awal)
0 (awal) 4 minggu
6 minggu
2 minggu
56
Gambar 4.5d Ukuran partikel F4 (Tween 80 0,75%) perbesaran 40x10 selama 8 minggu
25 µm 50 µm 25 µm
50 µm
25 µm
Gambar 4.5e. Ukuran partikel F5 (Tween 80 1%) perbesaran 40x10 selama 8 minggu
Dari keseluruhan Gambar 4.4 dapat kita lihat bahwa ukuran partikel terdispersi semakin kecil dengan bertambahnya konsentrasi Tween 80. Pengukuran partikel emulsi bertujuan untuk mengevaluasi adanya koalesensi atau penggabungan globul-globul minyak menjadi lebih besar pada sediaan emulsi selama 8 minggu penyimpanan.
Pengukuran partikel emulsi dapat dilihat pada Tabel 4.9 dan Gambar 4.6 bahwa perbedaan ukuran partikel antara emulsi yang satu dengan yang lainnya serta perbedaan ukuran partikel tiap formula selama 8 minggu penyimpanan jauh berbeda. Data hasil uji dapat dilihat pada Lampiran 8.
6 minggu
4 minggu 2 minggu
0 (awal)
57
Tabel 4.9. Data ukuran rata-rata partikel terdispersi Waktu
(minggu)
Ukuran rata-rata partikel terdispersi (µm)
F1 F2 F3 F4 F5
Gambar 4.6. Grafik ukuran rata-rata partikel terdispersi
58
4.3.7.2 Distribusi partikel terdispersi
Hasil distribusi partikel terdispersi selama 8 minggu dapat dilihat pada Tabel 4.10 dan Gambar 4.7 dibawah ini. Distribusi partikel terdispersi masing– masing formula semakin meningkat sesuai dengan penambahan konsentrasi Tween 80.
59
Tabel 4.10. Data distribusi partikel terdispersi
60
Keterangan : ɸ : diameter partikel n : Jumlah partikel
Gambar 4.7a. Grafik distribusi partikel terdispersi (F1)
Gambar 4.7b. Grafik distribusi partikel terdispersi (F2)
61
Gambar 4.8c. Grafik distribusi partikel terdispersi (F3)
Gambar 4.7d. Grafik distribusi partikel terdispersi (F4)
62
Gambar 4.7e. Grafik distribusi partikel terdispersi (F5)
Gambar 4.7f. Grafik distribusi partikel terdispersi semua formula
Pada keseluruhan Gambar 4.7 dapat dilihat bahwa Formula 5 (Tween 80 1%) lebih stabil dimana jumlah partikel terdispersi paling banyak (400 per lapangan pandang) dan ukuran partikel terdispersi paling kecil (40 µm).
Distribusi partikel terdispersi masing–masing formula selama penyimpanan 8 minggu semakin menurun dimana jumlah partikel terdispersi mengalami penurunan dan ukuran partikel terdispersi semakin besar sehingga menyebabkan emulsi kurang stabil.
0
Ukuran rata-rata partikel terdispersi (µm)
Formula 1
Formula 2
Formula 3
Formula 4
63
BAB V
KESIMPULAN DAN SARAN
4.1 Kesimpulan
Kesimpulan dari penelitian ini adalah:
1. VCO yang dihasilkan dengan menggunakan ragi tempe memiliki kualitas yang memenuhi standart mutu yaitu kadar air 0,03%, bilangan asam 0,1389, bobot jenis 0,9072 dan redemen minyak 40,82%.
2. Gom arab dan Tween 80 dapat digunakan sebagai emulgator untuk membuat formula sediaan emulsi VCO. Keempat formula emulsi VCO dengan variasi jumlah Tween 80 masing-masing 0,25, 0,5, 0,75%, 1% relatif stabil selama penyimpanan. Semakin tinggi konsentrasi Tween 80 emulsi VCO semakin stabil. Formula dengan Tween 80 1% merupakan formula yang paling stabil berdasarkan uji stabilitas.
4.2 Saran
Dari penelitian ini, disarankan bahwa:
1. Dilakukan penelitian lebih lanjut mengenai jenis emulgator lainnya untuk membuat sediaan emulsi VCO.
2. Dilakukan penelitian lebih lanjut menggunakan pemakaian alat untuk membuat emulsi misal dengan ultrasonic atau mixer sehingga ukuran partikelnya lebih seragam.
6 BAB II
TINJAUAN PUSTAKA
2.1 Minyak Kelapa
Minyak kelapa yang dikenal dengan minyak kalentik dan dulu banyak digunakan oleh masyarakat dipedesaan, sekarang jarang sekali ditemukan dipasaran. Minyak kelapa pada umumnya dibagi menjadi dua kategori yaitu minyak kelapa komersial yang telah di Refined, Deodorized, Bleached (RBD) dan minyak kelapa murni. Minyak kelapa komersial terbuat dari kopra (daging kelapa yang dijemur dibawah sinar matahari). Sesuai kondisinya, bahan ini relatif kotor dan mengandung bahan asing yang mempengaruhi hasil akhirnya. Bahan asing ini biasa berupa jamur, tanah, sampah dan kotoran lainnya. Minyak kelapa murni dibuat dari buah kelapa segar diproses dengan pemanasan sekitar 60-700C sehingga menghasilkan minyak yang jernih. Kualitas minyak kelapa sangat dipengaruhi oleh asal dan kualitas bahan baku serta proses pembuatan (Gani, et al., 2005). Komposisi kimia daging buah kelapa pada berbagai tingkat kematangan dapat dilihat dalam Tabel 2.1.
Tabel 2.1 Komposisi kimia daging buah kelapa pada berbagai tingkat kematangan
Analisis (dalam 100 g) Buah muda Buah setengah muda Buah tua
Kalori (kal) 68,0 180,0 359,0
7 2.2 Virgin Coconut Oil
Virgin coconut oil (VCO) atau minyak kelapa murni adalah minyak kelapa yang diperoleh dari kelapa yang sudah tua tanpa pemanasan tinggi, tanpa bahan kimia apapun, diproses dengan cara sederhana sehingga diperoleh minyak kelapa murni yang berkulitas tinggi. Keunggulan dari minyak ini menurut SNI adalah bau kelapa segar, tidak tengik, rasa normal, khas kelapa dan tidak berwarna. Minyak kelapa murni merupakan bentuk olahan daging kelapa yang baru-baru ini banyak diproduksi orang. Di beberapa daerah, VCO lebih terkenal dengan nama minyak perawan, minyak sara, atau minyak kelapa murni (Setiaji dan Prayugo, 2006).
2.3 Komposisi Asam Lemak VCO
VCO mengandung asam lemak rantai sedang yang mudah dicerna dan dioksidasi oleh tubuh sehingga mencegah penimbunan di dalam tubuh. Di samping itu ternyata kandungan antioksidan di dalam VCO pun sangat tinggi seperti tokoferol dan betakaroten. Antioksidan ini berfungsi untuk mencegah penuaan dini dan menjaga vitalitas tubuh (Setiaji dan Prayugo, 2006).
8 Tabel 2.2 Komposisi asam lemak VCO
Asam Lemak Jenuh Asam Lemak Tidak Jenuh Asam Lemak Jumlah ( % ) Asam Lemak Jumlah (%)
2.4 Teknologi Pengolahan VCO
VCO dapat dibuat dengan banyak metode. Beberapa metode tersebut adalah metode fermentasi, pemanasan bertahap, sentrifuse dan pancingan.
a. Fermentasi
Fermentasi merupakan kegiatan mikroba pada bahan pangan sehingga dihasilkan produk yang dikehendaki. Mikroba yang umumnya terlibat dalam fermentasi adalah bakteri, khamir dan kapang. Contoh bakteri yang digunakan dalam fermentasi adalah Acetobacter aceti pada pembuatan nata decoco. Contoh khamir dalam fermentasi adalah Saccharomyces cerevisiae dalam pembuatan alkohol sedangkan contoh kapang adalah Rhizopus oryzae pada pembuatan tempe. Kapang ini mempunyai kemampuan menghasilkan enzim protease dan lipase yang dapat menghidrolisis minyak dengan didukung oleh kadar air yang tinggi (Bawalan, 2011).
9
dengan menambah ragi tempe dengan perbandingan 5:1 (5 bagian krim santan dan 1 bagian ragi tempe). Fermentasi selesai ditandai dengan terbentuknya 3 lapisan yaitu lapisan minyak paling atas, lapisan tengah berupa protein dan lapisan paling bawah berupa air. Pemisahan dilakukan dengan menggunakan kertas saring (Cahyono dan Untari, 2009; Setiaji dan Prayugo, 2006).
Proses fermentasi dalam pembuatan minyak kelapa murni atau virgin coconut oil (VCO) yaitu mikroba dari ragi tempe dalam emulsi menghasilkan enzim, antara lain enzim protease. Enzim protease ini memutus rantai-rantai peptida dari protein berat molekul tinggi menjadi molekul-molekul sederhana dan akhirnya menjadi peptida-peptida dan asam amino yang tidak berperan lagi sebagai emulgator dalam santan kelapa sehingga antara minyak dan air memisah. Dari uraian diatas dapat dimengerti bahwa dengan adanya aktivitas mikroba tersebut dihasilkan asam sehingga akan menurunkan pH. Pada pH tertentu akan dicapai titik isoeletrik dari protein. Protein akan menggumpal sehingga mudah dipisahkan dari minyak (Cahyono dan Untari, 2009).
b. Pemanasan Bertahap
Cara pembuatan dengan metode ini sama dengan cara pembuatan dengan cara tradisional, yang berbeda terletak pada suhu pemanasan. Dimana, pada pemanasan bertahap suhu yang digunakan sekitar 60 - 75⁰ C. Bila suhu mendekati
angka 75⁰ C matikan api dan bila suhu mendekati angka 60⁰C nyalakan lagi api.
10 c. Sentrifugasi
Sentrifugasi merupakan cara pembuatan VCO dengan cara mekanik. Cara pembuatan santan sama dengan yang di atas. Masukkan krim santan kedalam alat sentrifuse. Kemudian nyalakan alat sentrifuse lalu atur pada kecepatan putaran 20.000 rpm dan waktu pada angka 15 menit. Ambil tabung dimana di dalam tabung terbentuk 3 lapisan. Ambil bagian VCO dengan menggunakan pipet tetes (Darmoyuwono, 2006; Setiaji dan Prayugo, 2006).
e. Pancingan
Cara pembuatan santan sama dengan cara diatas. Diamkan santan sampai terbentuk krim dan air. Krim tersebut dicampur dengan minyak pancingan dengan perbandingan 1:3 sambil terus diaduk hingga rata, lalu diamkan 7 – 8 jam sampai terbentuk minyak, blondo dan air. Ambil VCO dengan sendok. (Darmoyuwono, 2006; Sutarmi dan Rozaline, 2005).
2.5 Mutu VCO
VCO mutunya ditentukan oleh beberapa faktor antara lain: kadar air, angka asam, berat jenis.
2.5.1 Kadar air
11
sampel dalam oven T=1050C selama 2 jam lalu didinginkan dalam desikator kemudian ditimbang. Standar kadar air menurut SNI maksimal 0,2%.
Kadar air dapat dihitung dengan menggunakan rumus sebagai berikut:
Kadar air =Berat awal−berat akhir
Berat sampel x 100%
2.5.2 Bilangan asam
Bilangan asam adalah jumlah miligram KOH yang dibutuhkan untuk menetralkan asam-asam lemak bebas yang terdapat dalam 1 gram minyak atau lemak. Bilangan asam dipergunakan untuk mengukur jumlah asam lemak bebas yang terdapat dalam minyak atau lemak. Untuk penetapan bilangan asam dapat dilakukan dengan cara ditimbang 5 gram minyak atau lemak ke dalam erlenmeyer 250 ml. Selanjutnya ditambahkan 50 ml alkohol 95%, kemudian dipanaskan dalam penangas air. Larutan ini kemudian dititrasi dengan KOH 0,1 N dengan menggunakan indikator fenolftalein sampai tepat terlihat warna merah muda (Ketaren, 2005).
Bilangan asam dihitung dengan rumus:
Angka Asam =ml KOH x N KOH x MR KOH Berat Sampel
Keterangan:
12 2.5.3 Berat jenis
Berat jenis adalah suatu besaran yang menyatakan perbandingan antara massa (g) dengan volume (ml) (Bangun, 2013). Cara ini dapat digunakan untuk semua minyak dan lemak yang dicairkan. Alat yang digunakan untuk penentuan ini adalah piknometer. Standar APCC (Asian Pacific Coconut Community) berat jenis yaitu sebesar 0,915 - 0,920. Berat jenis dapat dihitung dengan menggunakan rumus sebagai berikut:
Berat Jenis =(Berat piknometer + minyak)−(berat piknometer) Volume piknometer
2.6 Manfaat VCO
VCO memiliki metabolisme yang berbeda dengan minyak lain. Oleh karena itu minyak kelapa murni bersifat protektif terhadap resiko penyakit jantung koroner (PJK), bersifat menghambat virus, mencegah diabetes dan meningkatkan kualitas air susu ibu.
a. Melindungi Jantung
13
rasio LDL/HDL menurun, mengarah kepada yang menguntungkan dan berarti dapat mengurangi resiko penyakit jantung koroner (Gopala, et al., 2010; Silalahi dan Nurbaya, 2011).
b. Antimikroba dan Antivirus
Sifat antimikroba dari minyak kelapa terutama tergantung pada adanya monogliserida, dan asam lemak bebas. Monogliserida aktif sebagai antimikroba tetapi digliserida dan trigliserida tidak. Asam lemak yang paling aktif adalah asam laurat dibandingkan dengan asam lemak miristat dan kaprilat. Monolaurin mencairkan dan merusak struktur lapisan selaput lipida pada virus dan lipida pada dinding sel bakteri. Monolaurin memperlihatkan efek membunuh virus dengan merusak DNA dan RNA virus yang dilapisi oleh lipida. Monolaurin mampu menghambat virus herpes, influenza (Lieberman, et al., 2006; Wang dan Johnson, 1992).
c. Mencegah Diabetes
14
dapat mencegah diabetes tipe 1 (merangsang produksi insulin) (Gupta, et al., 2010).
d. Meningkatkan Kualitas Air Susu Ibu
Air susu ibu (ASI) biasanya mengandung asam laurat yang rendah sekitar 6%. Ibu yang menyusui mengonsumsi minyak kelapa dapat menaikkan asam laurat sampai tiga kali lipat dan kaprat dua kali lipat di dalam ASI. Asam lemak rantai sedang di dalam ASI lebih mudah dicerna dan diserap walaupun sistem pencernaan bayi yang belum sempurna. Asam lemak rantai sedang di dalam minyak kelapa mudah digunakan sebagai sumber energi yang diperlukan untuk pertumbuhan yang baik, meningkatkan berat bayi yang dilahirkan dengan berat badan yang rendah. Pertambahan berat badan yang lebih cepat bukan karena penimbunan lemak tetapi pertumbuhan fisik (Hegde, 2006).
2.7 Sediaan VCO
2.7.1 VCO dalam bentuk kapsul lunak
15
ekstra untuk menghancurkan kemasan softcapsule sebelum cairan VCO diserap ke dalam tubuh. Kelemahan lainnya adalah harganya yang relatif lebih mahal dibandingkan dengan bentuk cairannya karena produsen harus mengeluarkan investasi tambahan untuk pembelian bahan, peralatan, serta pembayaran royalti dan lisensi paten teknologi pembuatan softcapsule. Meskipun demikian, kemasan VCO dalam bentuk softcapsule juga masih memiliki beberapa kelebihan dibandingkan dengan bentuk cairan, yaitu sebagai berikut:
• Lebih praktis, mudah dibawa ke mana-mana terutama bagi mereka yang
sangat aktif beraktivitas dan bepergian.
• Lebih tahan lama dalam penyimpanan karena terbungkus rapat dalam
kapsul sehingga terhindar dari cahaya dan oksidasi.
• Lebih cocok bagi mereka yang tidak menyukai rasa dan bau minyak
kelapa.
• Tidak mudah dipasulkan.
Sediaan yang ada di pasaran yaitu: Cosvoil (PT. Cocos Coconut), Laurico (PT. Palmanaturasanatco) (Subroto, 2006).
2.7.2 VCO dalam bentuk larutan
Virgin Coconut Oil (VCO) telah banyak diproduksi dan beredar dipasaran dalam bentuk sediaan sirup, namun sediaan yang ada memberikan aroma yang tidak baik dan rasa yang tidak enak. Sediaan yang ada dipasaran yaitu: camBIL (PT. Olah Ragam kokonat), VCO SM (CV. Rumah Obat Alami), AVCOL (PT. Ikot Alfisalam VCO), Naturecon (PT. Kasendra), Extravo 234 (UD. Taman Tirta Sehat) (Subroto, 2006).
16 2.8 Emulsi
2.8.1 Pengertian emulsi
Emulsi adalah suatu sistem yang tidak stabil secara termodinamik yang terdiri atas sedikitnya dua fase cair taktercampurkan, salah satunya terdispersi sebagai globul (fase terdispersi) dalam fase cair lainnya (fase kontinu); emulsi distabilkan dengan adanya bahan pengemulsi (Friberg, 1997; Martin, et al., 2011; Rohman, et al., 2012).
2.8.2 Jenis emulsi
Berdasarkan jenisnya, emulsi dibagi dalam 4 golongan, yaitu emulsi m/a, emulsi a/m, emulsi m/a/m dan emulsi a/m/a (Florence dan Attwood, 2006; Kulshreshtha, et al., 2010; Martin, 2011; Mootoosingh dan Rousseau, 2006). a. Emulsi jenis m/a
Jika fase minyak didispersikan sebagai globul dalam fase kontinu berair, sistem tersebut dikatatan sebagai emulsi minyak dalam (m/a).
b. Emulsi jenis a/m
Jika fase minyak sebagai fase kontinu, emulsi tersebut dikatakan sebagai emulsi air dalam minyak (a/m).
c. Emulsi jenis m/a/m
17
a m m a a m a m a m
(a) (b) (c) (d) Gambar 2.1 Tipe emulsi (a) m/a; (b) a/m; (c) a/m/a; (d) m/a/m
(Florence dan Attwood, 2006; Kulshreshtha, et al., 2010; Mootoosingh dan Rousseau, 2006).
Menentukan jenis emulsi dapat dilakukan dengan beberapa cara, yaitu metode pewarnaan, pengenceran, konduktivitas listrik dan fluoresensi.
a. Metode pewarnaan
Jenis emulsi ditentukan dengan penambahan zat warna yang larut dalam air, seperti metilen biru dapat diteteskan pada permukaan emulsi. Jika air merupakan fase eksternal (m/a), bahan pewarna akan terlarut dan berdifusi merata dalam air. Jika emulsi bertipe a/m, partikel-partikel bahan pewarna akan menggumpal pada permukaan (Martin, et al., 2011).
b. Metode pengenceran fase
Jika emulsi tercampur bebas dengan air, emulsi bertipe m/a, sedangkan bila tidak, jenis emulsi adalah emulsi a/m (Martin, et al., 2011).
c. Metode konduktivitas listrik
18 d. Metode fluoresensi
Minyak dapat berfluoresensi di bawah sinar UV, emulsi m/a menunjukkan pola titik-titik, sedangkan emulsi a/m berfluoresensi seluruhnya (Lachman et al., 1994).
2.8.3 Tujuan emulsi
Tujuan emulsi adalah untuk membuat suatu sediaan yang stabil dan rata dari dua cairan yang tidak dapat bercampur, untuk pemberian obat yang mempunyai rasa lebih enak, serta memudahkan absorpsi obat (Ansel, 1989). 2.8.4 Teori emulsifikasi
Beberapa teori emulsifikasi berikut menjelaskan bagaimana zat pengemulsi bekerja dalam menjaga stabilitas dari dua zat yang tidak saling bercampur:
a. Adsorpsi Monomolekuler
Surfaktan, atau amfifil, mengurangi tegangan antarmuka karena adsorpsinya pada antarmuka minyak-air membentuk selaput monomolekuler. Tetesan terdispersi dilapisi oleh suatu lapisan tunggal koheren yang membantu mencegah penggabungan antara dua tetesan ketika satu sama lain mendekat. Idealnya, lapisan selaput tersebut bersifat fleksibel sehingga mampu membentuk kembali dengan cepat jika pecah atau terganggu (Martin, et al., 2011; Mootoosingh dan Rousseau, 2006).
19
minyak untuk membentuk suatu selaput kompleks pada antarmuka. Tiga campuran bahan pengemulsi pada antarmuka minyak-air digambarkan pada Gambar 2.2. Kombinasi natrium setil sulfat dan kolesterol menyebabkan terbentuknya suatu selaput kompleks Gambar 2.2a, yang menghasilkan emulsi yang sangat baik. Natrium setil sulfat dan oleil alkohol tidak membentuk selaput yang terkondensasi atau tersusun rapat Gambar 2.2b, dan karenanya, kombinasi keduanya menghasilkan emulsi yang tidak baik. Pada Gambar 2.2c, setil alkohol dan natrium oleat menghasilkan selaput yang tersusun rapat, tetapi kompleksasinya terabaikan sehingga juga menghasilkan suatu emulsi yang buruk (Martin, et al., 2011).
20
Atlas – ICI menganjurkan untuk mengkombinasi Tween yang hidrofilik dengan Span yang lipofilik, dengan memvariasikan perbandingannya untuk menghasilkan emulsi m/a atau a/m yang diinginkan. Boyd dkk membahas penggabungan molekular Tween 40 dan Span 80 dalam menstabilkan emulsi. Pada Gambar 2.3, bagian hidrokarbon molekul Span 80 (Sorbitan monoleat) berada dalam globul minyak dan radikal sorbitan berada dalam fase air. Kepala sorbitan yang besar pada molekul Span mencegah ekor-ekor hidrokarbon bergabung rapat dalam fase minyak. Ketika Tween 40 (polioksietilen sorbitan monopalmitat) ditambahkan, senyawa ini mengarah pada antarmuka dengan ekor hidrokarbonnya berada dalam fase minyak, sedangkan sisa rantainya, bersama dengan cincin sorbitan dan rantai polioksietilen, berada dalam fase air. Rantai hidrokarbon molekul Tween 40 teramati berada dalam globul minyak diantara rantai-rantai Span 80, dan orientasi ini menghasilkan tarik-menarik van der Waals yang efektif. Dengan cara ini , selaput antarmuka diperkuat dan stabilitas emulsi m/a ditingkatkan terhadap penggabungan partikel (Martin, et al., 2011; Mootoosingh dan Rousseau, 2006).
21
Tipe emulsi yang dihasilkan, m/a atau a/m, terutama bergantung pada sifat bahan pengemulsi. Karakteristik ini disebut sebagai kesimbangan hidrofil-lipofil (hydrophile-lipophile balance, HLB). Pada kenyataannya, apakah suatu surfaktan merupakan suatu pengemulsi, bahan pembasah, detergen, atau bahan pelarut dapat diperkirakan dari harga HLB (Martin, et al., 2011).
b. Adsorpsi Multimolekuler
Koloid ini dapat dianggap sebagai aktif permukaan karena tampak pada antarmuka minyak-air. Namun, koloid ini berbeda dari bahan aktif permukaan sintetis, yaitu tidak menyebabkan penurunan tegangan antarmuka yang berarti dan zat ini membentuk suatu lapisan multimolekuler dan bukan lapisan monomolekuler pada antarmuka. Kerja koloid ini sebagai bahan pengemulsi terutama disebabkan oleh efek yang kedua karena selaput yang terbentuk kuat dan mencegah penggabungan. Suatu efek pembantu yang meningkatkan stabilitas adalah peningkatkan viskositas medium dispersi yang signifikan. Karena bahan pengemulsi yang membentuk multilapisan di sekitar tetesan selalu hidrofilik, bahan pengemulsi tersebut cenderung menyebakan pembentukan emulsi m/a (Martin, et al., 2011; Mootoosingh dan Rousseau, 2006).
c. Adsorpsi Partikel Padat
22 2.8.5 Penggunaan emulsi
Berdasarkan penggunaannya, emulsi dibagi dalam 2 golongan, yaitu emulsi untuk pemakaian dalam dan emulsi untuk pemakaian luar.
a. Emulsi untuk pemakaian dalam
Emulsi untuk pemakaian dalam meliputi per oral dan injeksi intravena. Suatu emulsi o/w merupakan suatu cara pemberian oral yang baik untuk cairan-cairan yang tidak larut dalam air, terutama jika fase terdispers mempunyai fase yang tidak enak. Senyawa yang larut dalam lemak, seperti vitamin, diabsorpsi lebih sempurna jika diemulsikan daripada jika diberikan per oral dalam suatu larutan berminyak. Penggunaan emulsi intravena telah diteliti sebagai suatu cara untuk merawat pasien lemah yang tidak bisa menerima obat-obat yang diberikan secara oral (Florence dan Attwood, 2006; Kulshreshtha, et al., 2010; Martin, et al., 2011; Mootoosingh dan Rousseau, 2006).
b. Emulsi untuk pemakaian luar
Emulsifikasi banyak digunakan dalam pembuatan produk obat dan kosmetik untuk penggunaan luar, khususnya pada losion dan krim dermatologi dan kosmetik karena produk yang diinginkan adalah produk yang mudah menyebar dan benar-benar menutupi area yang dioleskan. Produk tersebut kini dapat diformulasi menjadi produk yang dapat dibersihkan dengan air dan tidak menimbulkan noda (Florence dan Attwood, 2006; Kulshreshtha, et al., 2010; Martin, et al., 2011; Mootoosingh dan Rousseau, 2006).
2.8.6 Pembuatan emulsi
23 a. Metode Gom Kering
Metode ini juga dikenal sebagai metode 4:2:1 karena untuk tiap 4 bagian minyak, 2 bagian air dan 1 bagian gom ditambahkan untuk membuat emulsi utama atau emulsi awal. Dalam metode ini gom atau zat pengemulsi m/a lainnya dihaluskan dengan minyak dalam mortir porselen dengan sempurna sampai seluruhnya bercampur. Sesudah minyak dan gom dicampur, dua bagian air kemudian ditambahkan sekaligus, dan campuran tersebut digerus dengan segera dan dengan cepat serta terus-menerus sampai emulsi utama terbentuk berwarna putih krim. Umumnya dibutuhkan waktu 3 menit pencampuran untuk menghasilkan emulsi utama seperti itu. Bahan formulatif cair lainnya yang larut dalam fase luar kemudian bisa ditambahkan ke emulsi utama tersebut dengan pengadukan. Zat padat seperti pengawet, penstabil, zat warna, dan bahan pemberi rasa biasanya dilarutkan dalam air dengan volume yang sesuai dan ditambahkan sebagai larutan ke emulsi utama tersebut. Ketimbang menggunakan mortir dan stamper, ahli farmasi umumnya dapat membuat emulsi yang baik sekali dengan menggunakan metode gom kering dan mikser atau blender listrik (Ansel, 1989). b. Metode Gom Basah
24
ditambahkan dan emulsi tersebut dipindahkan ke gelas ukur untuk mencukupkan volumenya dengan air (Ansel, 1989).
c. Metode Botol
Metode ini digunakan untuk membuat emulsi dari minyak-minyak menguap dan mempunyai viskositas rendah. Caranya, serbuk gom arab dimasukkan ke dalam suatu botol kering, ditambahkan dua bagian air kemudian campuran tersebut dikocok dengan kuat dalam wadah tertutup. Suatu volume air yang sama dengan minyak kemudian ditambahkan sedikit demi sedikit sambil terus mengocok campuran tersebut setiap kali ditambahkan air. Jika semua air telah ditambahkan, emulsi utama yang terbentuk bisa diencerkan sampai mencapai volume yang tepat dengan air atau larutan zat formulatif lain dalam air (Ansel, 1989).
2.8.7 Zat Pengemulsi
Pemilihan zat pengemulsi sangat penting dalam menentukan keberhasilan pembuatan suatu emulsi yang stabil. Agar berguna dalam preparat farmasi, zat pengemulsi harus mempunyai kualitas tertentu, diantaranya harus dapat dicampurkan dengan bahan formulatif lainnya, tidak mengganggu stabilitas dari zat terapeutik, tidak toksik dalam jumlah yang digunakan, serta mempunyai bau, rasa, dan warna yang lemah (Ansel, 1989; Gennaro, 1990).
Zat pengemulsi dapat digolongkan berdasarkan sumber sebagai berikut: a. Golongan karbohidrat, seperti gom, tragakan, agar, dan pektin. Bahan-bahan ini
25
b. Golongan protein, seperti gelatin, kuning telur, dan kasein. Zat-zat ini menghasilkan emulsi m/a.
c. Golongan alkohol, seperti stearil alkohol, setil alkohol, gliseril monostearat, kolesterol, dan turunan kolesterol. Bahan-bahan ini digunakan terutama sebagai zat pengental dan penstabil untuk emulsi m/a dari lotio dan salep tertentu yang digunakan sebagai obat luar.
d. Golongan surfaktan (sintetik), bisa yang bersifat anionik, kationik, dan nonionik yang diadsorpsi pada antarmuka minyak-air untuk membentuk selaput monomolekul dan mengurangi tegangan antarmuka.
e. Golongan zat padat terbagi halus, seperti bentonit, magnesium hidroksida, dan alumunium hidroksid yang diadsorpsi pada antarmuka antara dua fase cair taktercampurkan dan membentuk suatu selaput partikel disekitar globul terdispersi (Ansel, 1989; Martin, et al., 2011).
2.8.7.1 Tween 80
Tween 80 adalah ester asam lemak polioksietilen sorbitan, dengan nama kimia polioksietilen 20 sorbitan monooleat. Rumus molekulnya adalah C64H124O26 dan rumus strukturnya pada Gambar 2.3.
26
Pada suhu 25ºC, Tween 80 berwujud cair, berwarna kekuningan dan berminyak, memiliki aroma yang khas, dan berasa pahit. Larut dalam air dan etanol, tidak larut dalam minyak mineral. Tween 80 secara luas digunakan dalam produk kosmetik dan makanan. Kegunaan Tween 80 antara lain sebagai: zat pendispersi, emulgator, dan peningkat kelarutan, pensuspensi dan pembasah (Rowe, et al., 2009).
2.8.7.2 Gom arab
Gum arab dihasilkan dari getah bermacam-macam pohon Acasia sp. di Sudan dan Senegal. Gum arab jauh lebih mudah larut dalam air dibanding hidrokoloid lainnya. Pada olahan pangan yang banyak mengandung gula, gum arab digunakan untuk mendorong pembentukan emulsi lemak yang mantap dan mencegah kristalisasi gula. Gum arab stabil dalam larutan asam. pH alami gum berkisar 4,5 – 5,0. Gum arab dapat meningkatkan stabilitas dengan peningkatan viskositas. Jenis pengental ini juga tahan panas pada proses yang menggunakan panas namun lebih baik jika panasnya dikontrol untuk mempersingkat waktu pemanasan, mengingat gum arab dapat terdegradasi secara perlahan-lahan dan kekurangan efisiensi emulsifikasi dan viskositas. Viskositas akan meningkat sebanding dengan peningkatan konsentrasi (Rowe, et al., 2009).
2.8.8 Sistem HLB
27
dan zat aktif permukaan dapat digolongkan susunan kimianya sebagai keseimbangan hidrofil-lipofil atau HLBnya. Dengan metode ini tiap zat mempunyai harga HLB atau angka yang menunjukkan polaritas dari zat tersebut. Walaupun angka tersebut telah ditentukan sampai kira-kira 40, kisaran lazimnya antara 1 dan 20. Bahan-bahan yang sangat polar atau hidrofilik angkanya lebih besar daripada bahan-bahan yang kurang polar dan lebih lipofilik. Umumnya zat aktif permukaan itu mempunyai harga HLB yang ditetapkan antara 3 sampai 6 dan menghasilkan emulsi air dalam minyak. Sedangkan zat-zat yang mempunyai harga HLB antara 8 sampai 18 menghasilkan emulsi minyak dalam air (Kulshreshtha, et al., 2010). Contoh-contoh dari beberapa harga HLB yang ditetapkan untuk beberapa surfaktan pilihan terlihat dalam Tabel 2.3.
Tabel 2.3 Aktivitas dan harga HLB surfaktan
Aktivitas HLB
Antibusa 1 sampai 3
Pengemulsi (a/m) 3 sampai 6
Zat pembasah 7 sampai 9
Pengemulsi (m/a) 8 sampai 18
Pelarut 15 sampai 20
Detergen 13 sampai 15
(Kulshreshtha, et al., 2010). 2.8.9 Ketidakstabilan emulsi
Beberapa hal yang dapat menyebabkan ketidakstabilan emulsi secara fisika diantaranya, pengkriman (creaming), pemecahan (breaking) dan inversi. a. Pengkriman
Faktor-28
faktor yang penting dalam pengkriman suatu emulsi dihubungkan oleh hukum stokes (Martin, et al., 2011).
Analisa terhadap persamaan tersebut menunjukkan bahwa jika densitas fase terdispersi lebih kecil dari fase kontinu, yang umumnya terjadi pada emulsi m/a, kecepatan sedimentasi menjadi negatif, yaitu terjadi pengkriman ke atas. Jika fase internal lebih berat daripada fase eksternal, globul akan mengendap. Ini merupakan suatu fenomena yang biasa terjadi pada emulsi a/m, yaitu fase internal cair, memiliki densitas lebih besar daripada fase kontinu (minyak). Efek ini dapat disebut sebagai pengkriman ke arah bawah. Semakin besar perbedaan densitas kedua fase, semakin besar globul minyak, dan semakin berkurang kekentalan fase eksternal, semakin tinggi kecepatan pengkriman (Martin, et al., 2011).
b. Pemecahan
Pengkriman harus dianggap berbeda dengan pemecahan (breaking) karena pengkriman merupakan suatu proses reversible, sedangkan pemecahan adalah proses irreversible. Jika emulsi pecah, pencampuran sederhana tidak dapat mensuspensikan globul kembali dalam bentuk emulsi yang stabil karena selaput yang melapisi partikel telah rusak dan minyak cenderung menyatu (Martin, et al., 2011).
c. Inversi
29 2.9 Emulsi Minyak
2.9.1 Emulsi minyak kelapa murni
Penelitian yang dilakukan oleh Syukri, et. al., (2008), menggunakan emulgator Span 80 (20%, 15%, 10%) dan Tween 40 0,1% diperoleh emulsi yang kurang stabil. Volume pemisahan fase pada suhu kamar, suhu 400C dan sentrifugasi selama 4 minggu penyimpanan semakin tinggi sedangkan viskositas menurun perlahan-lahan seiring dengan bertambahnya umur sediaan. Perbedaan konsentrasi Span 80 (20%, 15%, 10%) pada Tween 40 0,1% sebagai emulgator berpengaruh pada stabilitas fisik emulsi minyak kelapa murni.
2.9.2 Emulsi minyak buah merah
Penelitian yang dilakukan oleh Murtiningrum, et. al., (2013), menggunakan CMC, gum arabic, Tween 20 dan Tween 80 dalam pembuatan emulsi minyak buah merah. Penggunaan Tween 20 (0,45%), Tween 80 (0,45%), dan CMC (0,25%) dapat membentuk emulsi minyak buah merah yang stabil selama lima hari. Konsentrasi pengemulsi berpengaruh terhadap rasio minyak dan air untuk menghasilkan kekentalan dan daya alir emulsi minyak buah merah yang baik. CMC menghasilkan kestabilan emulsi minyak buah merah terbaik dengan nilai viskositas tertingi, persentase pemisahan emulsi terendah dan stabil selama penyimpanan.
30
arab 15% merupakan formula yang paling stabil berdasarkan uji stabilitas. Stabilitas fisik yang diuji terhadap beberapa minyak dapat dilihat dalam Tabel 2.4. Tabel 2.4 Stabilitas fisik emulsi Minyak
Bahan (%) Stabilitas Fisik Hasil Literatur
Tween 40 0,1% dalam
Viskositas Viskositas menurun
selama 4 minggu
Pemisahan fase Volume pemisahan
CMC lebih kecil dibanding Tween 20 dan Tween 80 selama 5 hari penyimpanan
(b)
Viskositas Viskositas CMC lebih
tingggi dibanding Tween 20 dan Tween 80 selama 5 hari
Pemisahan fase Volume pemisahan
fase semakin kecil
Viskositas Viskositas semakin
1
BAB I
PENDAHULUAN
1.1 Latar Belakang
Salah satu produk yang dapat dihasilkan dari daging buah kelapa yang sudah tua tetapi masih segar adalah Virgin Coconut Oil (VCO) atau minyak kelapa murni. VCO merupakan salah satu minyak yang memiliki banyak manfaat dalam bidang industri farmasi maupun kesehatan. Dalam dunia industri farmasi VCO digunakan sebagai bahan dasar kosmetik sedangkan di dunia kesehatan sebagai makanan fungsional. Itulah sebabnya saat ini permintaan VCO terus meningkat baik di dalam maupun di luar negeri (Mentawai, 2005; Nevin dan Rajamohan, 2004).
Pada dasarnya cara pembuatan VCO yang banyak dilakukan Indonesia dibedakan menjadi fermentasi, pemanasan bertahap, pemancingan, sentrifugasi. Proses ekstraksi minyak secara fermentasi melibatkan enzim-enzim pemecah emulsi santan. Aktifitas enzim dipengaruhi oleh konsentrasi substrat, enzim, suhu, dan lamanya reaksi enzimatik. Biakan mikroba yang digunakan diharapakan memiliki aktifitas proteolitik, amilolitik yang berperan dalam menghidrolisis protein, karbohidrat (Iswanto, 2001; Darmoyuono, 2006).