1.1 Latar Belakang
Bahan pangan hasil perairan banyak mengandung zat gizi yang diperlukan oleh tubuh. Makanan sehari-hari yang dipilih dengan baik akan memberikan zat gizi yang dibutuhkan untuk fungsi normal tubuh. Bila dikelompokkan, ada tiga fungsi zat gizi dalam tubuh yaitu untuk memberi energi, pertumbuhan dan pemeliharaan jaringan tubuh, dan mengatur proses tubuh (Almatsier 2006).
Salah satu kekerangan yang cukup populer di masyarakat Indonesia yaitu kerang pisau atau lorjuk (Solen spp). Lorjuk merupakan istilah lain dari kerang pisau yang digunakan oleh sebagian besar masyarakat Jawa Timur. Beberapa jenis makanan dan snack berbahan baku lorjuk yang telah dikreasikan oleh masyarakat antara lain kacang goreng lorjuk, soto lorjuk, petis lorjuk, bothok lorjuk dan rengginang lorjuk. Hasil perhitungan Survei Sensus Ekonomi Nasional (SUSENAS) 2009 menunjukkan bahwa penyerapan pasar untuk komoditas kerang/siput di tingkat rumah tangga mencapai 25.450 ton dengan konsumsi rata-rata 0,11 kg/kapita (Ditjen PPHP 2010).
Salah satu kandungan zat gizi yang terdapat pada kerang pisau adalah asam lemak. Beberapa asam lemak bersifat esensial, misalnya asam lemak linolenat dan linoleat (Vaclavik dan Christian 2008). Asam lemak tak jenuh digunakan untuk menjaga bagian-bagian struktural dari membran sel dan mempunyai peran penting dalam perkembangan otak. Komoditas perikanan merupakan sumber asam lemak omega 3 dengan lima hingga enam ikatan rangkap yang terdapat didalamnya (Belitz dan Grosch 1999). EPA dan DHA merupakan Omega 3. Omega 3 memiliki banyak manfaat bagi kesehatan tubuh khususnya jantung dan aliran darah.
gizi bahan pangan, teknik penanganan dan proses selanjutnya. Pertimbangan dalam memilih bahan pangan disamping kandungan gizinya, harus aman untuk dikonsumsi dilihat dari segi zat racun, mikroba patogen atau zat lain yang berbahaya bagi tubuh (Almatsier 2006). Kerang merupakan organisme filter feeder yang menyaring makanannya dari hasil perairan. Lingkungan perairan yang bersih atau tercemar sangat mempengaruhi keamanan pangan dari komoditas kerang. Hal-hal tersebut menjadi alasan dilakukannya penelitian tentang komposisi kimia, asam lemak, kolesterol dan kandungan mineral dan logam berat yang terdapat pada kerang pisau (Solen spp) agar informasi mengenai biota ini dapat dimanfaatkan secara optimal dan berguna dalam meningkatkan pengetahuan akan komposisi gizi kerang pisau yang dapat bermanfaat bagi kesehatan.
1.2 Tujuan
2.1 Deskripsi dan Klasifikasi Kerang Pisau (Solen spp)
Kerang, remis dan kijing merupakan kelas Pelecypoda, filum Mollusca. Kebanyakan hidup di air laut terutama di daerah littoral, beberapa di daerah pasang surut dan air tawar. Beberapa jenis organisme laut hidup pada kedalaman sampai 5000 m. Kerang, remis dan kijing umumnya terdapat di dasar perairan yang berlumpur atau berpasir, beberapa hidup pada substrat yang lebih keras yaitu lempung, kayu atau batu. Tubuh pelecypoda pipih secara lateral dan seluruh tubuh tertutup dua keping cangkang yang berhubungan di bagian dorsal dengan adanya „hinge ligament‟ yaitu semacam pita elastik yang terdiri dari bahan organik seperti zat tanduk (conchiolin) sama dengan periostrakum (lapisan cangkang paling luar). Kedua keping cangkang pada bagian dalamnya juga ditautkan oleh sebuah otot aduktor anterior dan sebuah otot aduktor posterior yang bekerja antagonis dengan hinge ligament (Suwignyo et al. 2005).
Kerang pisau atau lorjuk (Solen spp) merupakan anggota dari famili Solenidae. Kerang pisau memiliki cangkang yang panjang dengan dua sisi paralel, tubuhnya kecil memanjang, salah satu ujung tubuhnya berbentuk runcing seperti mata pisau, menempel dan berdiri tegak di pantai berpasir. Kadang kala lorjuk menarik badannya ke dalam pasir untuk berlindung dari musuh. Lorjuk di beberapa negara dikenal juga dengan sejumlah nama seperti razor clam atau jacknife karena karakteristiknya yang identik dengan pisau (Ditjen PPHP 2010).
Gambar 1 Morfologi kerang pisau (Solen spp)
Habitat kerang pisau berupa pasir berlumpur dengan arus air laut yang lemah. Kerang pisau bersembunyi atau menggali secara vertikal pada substrat berpasir dan sedikit keluar pada saat pasang surut. Kerang pisau banyak ditemukan di sepanjang perairan pantai selatan Pamekasan, Madura dengan ciri pantai yang landai dan datar sehingga jika air laut surut jarak air dengan garis pantai dapat mencapai 200-300 m (Nurjanah et al. 2008).
2.2 Komposisi Kimia Kerang Pisau (Solen spp)
Komposisi kimia kerang sangat beraneka ragam. Hal ini dapat tergantung pada spesies, jenis kelamin, umur, musim, dan habitat. Kandungan gizi kerang pisau dapat dilihat pada Tabel 1.
Tabel 1 Kandungan gizi kerang pisau (Solen spp)
Jenis gizi Basis basah
2.3 Penangkapan, Pengolahan dan Pemasaran Kerang Pisau (Solen spp)
Lorjuk biasanya disajikan dalam bentuk olahan. Proses untuk menghasilkannya sebagai berikut: lorjuk segar hasil tangkapan dicuci bersih, direbus selama 1,5 jam hingga cangkang mengelupas sendiri. Lorjuk setelah itu dijemur selama 4 jam, dikupas dan dagingnya dikeringkan lagi selama 6 jam. Daging yang benar-benar kering dapat diolah lebih lanjut. Lorjuk biasanya digoreng atau diolah menjadi kacang goreng lorjuk, soto lorjuk, petis lorjuk, bothok lorjuk dan rengginang lorjuk (Ditjen PPHP 2010).
Lorjuk memiliki rendemen kecil, namun pedagang tetap tergiur untuk terus mencari lorjuk. Alasan pedagang tetap mencari lorjuk karena nilai jual produknya sangat tinggi. Lorjuk segar hanya senilai Rp. 8000/kg, lorjuk setengah kering Rp. 80.000/kg dan lorjuk kering Rp. 280.000/kg sedangkan lorjuk goreng dipasarkan dengan harga sekitar Rp. 300.000/kg. Kebutuhan pedagang lorjuk sebagian besar hanya bisa dipenuhi oleh nelayan dari lorjuk segar dan setengah kering saja, oleh karena itu keuntungan terbesar berada di tangan para pedagang tersebut. Kemampuan produksi pedagang pun tergantung pada hasil tangkap nelayan (Ditjen PPHP 2010).
2.4 Lemak
Lemak adalah sekelompok senyawa organik yang mempunyai sifat dapat larut dalam zat-zat pelarut tertentu, misalnya petroleum benzene, ether (Sediaoetomo 2008). Senyawa organik ini terdapat dalam semua sel dan berfungsi sebagai sumber energi, komponen struktur sel, sebagai simpanan bahan bakar metabolik, sebagai komponen pelindung dinding sel, dan juga sebagai komponen pelindung kulit vertebrata (Girindra 1987).
Molekul lemak tersusun dari satu hingga tiga asam lemak dan satu gliserol. Gliserol adalah alkohol trihidrat, yaitu mempunyai tiga gugus hidroksil (Gaman dan Sherrington 1992). Jumlah asam lemak yang terdapat pada gugus gliserol menyebabkan adanya pembagian molekul lemak menjadi monogliserida, digliserida, dan trigliserida.
linolenat. Ketiganya mengandung ikatan rangkap (dua atau lebih) termasuk ke dalam kelompok asam lemak tak jenuh majemuk (polyunsaturated fatty acid/PUFA) (Suhardjo dan Kusharto 1987). Komposisi lemak dan strategi penyimpanan moluska, terutama bivalvia dan gastropoda telah dipelajari sejak lipid menjadi bagian utama fraksi dari jaringan moluska (Voogt 1983 diacu dalam Ekin dan Bashan 2010).
2.4.1 Asam Lemak
Asam lemak merupakan senyawa pembangun berbagai lipida, termasuk lipida sederhana, fosfogliserida, glikolipida, sfingolipid, ester kolesterol, lilin dan lain-lain, dan telah diisolasi lebih dari 70 macam asam lemak dari berbagai sel dan jaringan (Girindra 1987). Asam lemak dapat digolongkan berdasarkan tingkat kejenuhan, yaitu asam lemak jenuh (saturated fatty acid/SAFA) dan asam lemak tidak jenuh (unsaturated fatty acid). Pembagian ini penting karena asam lemak jenuh mempunyai titik cair yang lebih tinggi dibandingkan asam lemak tidak jenuh. Asam lemak yang paling umum dijumpai adalah laurat, miristat, palmitat, dan stearat (Suharjo dan Kusharto 1987).
Asam lemak tak jenuh yang mengandung satu ikatan rangkap disebut asam lemak tak jenuh tunggal (monounsaturated fatty acid/MUFA). Asam lemak yang mengandung dua atau lebih ikatan rangkap disebut asam lemak tak jenuh majemuk. Asam lemak tak jenuh umumnya terdapat dalam bentuk cis, sedangkan bentuk trans banyak terdapat pada lemak susu ruminansia pada hewan terestrial dan lemak yang telah dihidrogenasi (Muchtadi et al. 1993). Perbedaan ikatan kimia antar asam lemak jenuh dan asam lemak tak jenuh dapat menyebabkan terjadinya perbedaan sifat kimia dan fisik, diantaranya asam lemak jenuh dapat meningkatkan kadar kolesterol dalam darah. Semakin panjang rantai karbon dan semakin banyak jumlah ikatan rangkapnya, maka semakin besar kecenderungan untuk menurunkan kadar kolesterol dalam darah (Muchtadi et al.1993).
2.4.2 Fungsi Asam Lemak
Asam linolenat merupakan asam lemak esensial, karena dibutuhkan tubuh namun tubuh tidak dapat mensintesisnya. Turunan dari asam linolenat adalah EPA dan DHA. Ikan dapat mengubah asam linolenat menjadi EPA dan DHA, sejalan dengan hal tersebut perubahan asam linolenat menjadi EPA dan DHA terjadi pada manusia namun tidak efisien (Almatsier 2006).
Asam lemak DHA terbukti berpengaruh terhadap retina mata hewan percobaan. Komponen asam lemak pada membran sel otak dan retina berpengaruh terhadap fluiditas dan sifat-sifat yang berhubungan dengan aktivitas penglihatan dan reseptor sel saraf serta inisiasi dan transimisi sel syaraf. Asam lemak esensial dalam tubuh digunakan untuk menjaga bagian-bagian struktural dari membran sel dan untuk membuat bahan-bahan misalnya hormon yang disebut eikosanoid. Eikosanoid membantu mengatur tekanan darah, proses pembekuan darah, lemak dalam darah dan respon imun terhadap luka dan infeksi dan risiko kanker (Haliloglu et al. 2004).
Kandungan EPA berperan dalam mencegah penyakit degeneratif sejak janin dan pada saat dewasa. EPA saat dewasa berfungsi melancarkan pembuluh darah mengatur sirkulasi. Defisiensi omega-3 dapat berisiko menderita penyakit pembuluh darah dan jantung. Adapun fungsi asam lemak esensial yang terdapat dalam tubuh sebagai fosfolipid antara lain memelihara integritas dan fungsi membran seluler dan subseluler, mengatur metabolisme kolesterol, merupakan prekursor dari senyawa yang memiliki fungsi pengatur fisiologis dalam tubuh dan dibutuhkan pertumbuhan dan perkembangan bayi (Muchtadi et al. 1993).
2.5 Kolesterol
manusia disintesis dari dalam tubuh sekitar 60-75% dan sisanya dari luar tubuh yaitu berasal dari makanan yang telah dikonsumsi (Astawan 2008).
Kolesterol diubah dalam mukosa usus dan kulit menjadi 7-dehidro kolesterol yang merupakan prekursor vitamin D. Hormon yang membutuhkan kolesterol sebagai prekursor adalah hormon-hormon kelamin dan hormon adrenokortiko. Kolesterol merupakan bagian yang penting dalam sel dan jaringan tubuh, otak, syaraf, ginjal, limpa, hati dan kulit yang disebut “endogenous cholesterol” sedangkan “exogenous cholesterol” adalah kolesterol yang berasal
dari bahan makanan atau dietary cholesterol. Sumber-sumber kolesterol antara lain kuning telur, ikan, otak, hati dan organ kelenjar kerbau. Konsentrasi total kolesterol dalam plasma darah berkisar 180-250 mg/100 ml (Suhardjo dan Kusharto 1987).
Ada tiga jenis lipoprotein yang dapat mengangkut kolesterol dan trigliserida lain yaitu HDL, LDL dan VLDL. Orang yang terserang jantung koroner umumnya memiliki tingkat LDL/VLDL yang lebih tinggi dan HDL yang lebih rendah. Tingkat LDL dan VLDL yang tinggi akan menyebabkan terjadinya deposisi kolesterol lemak, sisa-sisa sel rusak dan komponen lainnya di sepanjang pembuluh darah sehingga membentuk “kerak“ yang menyebabkan penyempitan pembuluh darah (Freeman dan Junge 2005). Kolesterol bila terdapat terlalu banyak di dalam darah dapat membentuk endapan pada dinding pembuluh darah sehingga menyebabkan penyempitan yang dinamakan aterosklerosis. Bila penyempitan terjadi pada pembuluh darah jantung dapat menyebabkan penyakit jantung koroner dan bila pada pembuluh darah otak penyakit serebrovaskular (Almatsier 2006).
2.6 Mineral
metabolisme, terutama sebagai kofaktor dalam aktivitas enzim-enzim (Almatsier 2006). Kekurangan mineral tertentu dapat menyebabkan gangguan gizi, diantaranya ialah terhambatnya pertumbuhan, anemia, dan penyakit gondok (Buckle et al. 1987).
Bahan makanan sebagian besar yaitu sekitar 96% terdiri dari bahan organik dan air, sisanya sekitar 4% terdiri dari unsur-unsur mineral (Winarno 2008). Sumber mineral paling baik adalah makanan hewani, kecuali magnesium yang lebih banyak terdapat dalam makanan nabati. Hewan memperoleh mineral dari tumbuh-tumbuhan dan menumpuk di dalam jaringan tubuhnya. Mineral yang berasal dari makanan hewani mempunyai ketersediaan biologik lebih tinggi daripada makanan nabati. Makanan hewani mengandung lebih sedikit bahan-bahan pengikat mineral daripada makanan nabati (Almatsier 2006).
2.6.1 Mineral makro
Mineral makro adalah mineral yang diperlukan tubuh dalam jumlah lebih dari 100 mg sehari. Mineral-mineral yang termasuk mineral makro antara lain: natrium, klorida, kalium, kalsium, fosfor, magnesium dan sulfur (Almatsier 2006).
a. Kalsium (Ca)
Kalsium merupakan mineral yang paling banyak terdapat dalam tubuh, yaitu 1,5–2% dari berat badan badan orang dewasa atau kurang lebih sebanyak 1 kg. Berdasarkan jumlah tersebut, 99% berada dalam jaringan keras, yaitu tulang dan gigi terutama dalam bentuk hidroksiapatit dan sisanya tersebar di dalam tubuh (Almatsier 2006). Kalsium berperan dalam proses pembentukan gigi dan tulang, selain itu kalsium yang berada dalam sirkulasi darah dan jaringan berperan dalam transmisi impuls syaraf, kontraksi otot, penggumpalan darah, pengaturan permeabilitas membran sel, serta keaktifan enzim (Winarno 2008). Kalsium juga merupakan salah satu faktor penting dalam pembekuan darah. Kalsium juga diperlukan untuk memelihara otot dan syaraf tubuh agar berfungsi normal (Gaman dan Sherrington 1992).
b. Natrium (Na)
klorida (Gaman dan Sherrington 1992). Natrium berfungsi mengatur tekanan osmotik. Natrium juga berfungsi menjaga keseimbangan asam basa tubuh, transmisi saraf, kontraksi otot, absorpsi glukosa, dan alat angkut zat gizi lain melalui membran (Almatsier 2006).
c. Magnesium (Mg)
Magnesium merupakan kation nomor dua paling banyak setelah natrium dalam cairan ekstraseluler. Kurang lebih 60% dari 20–28 mg magnesium dalam tubuh terdapat pada tulang dan gigi, 26% di dalam otot, dan sisanya di jaringan lunak lainnya serta cairan tubuh (Almatsier 2006). Sebanyak sepertiga magnesium di jaringan keras berada dalam kombinasi dengan fosfat, sisanya melekat secara bebas pada permukaan struktur mineral (Suhardjo dan Kusharto 1987). Magnesium memiliki fungsi sebagai kofaktor untuk beberapa aktivitas enzim (Tayo et al. 2011). Magnesium merupakan aktivator enzim peptidase dan enzim lain yang berfungsi memecah dan memindahkan gugus fosfat (fosfatase) (Winarno 2008). Magnesium juga berperan dalam mencegah kerusakan gigi,
mengendorkan otot, transmisi syaraf, dan berbagai aktivitas enzim (Sizer dan Whitney 2002).
d. Fosfor
Fosfor merupakan mineral kedua terbanyak di dalam tubuh, yaitu 1% dari berat badan. Fosfor berperan dalam kalsifikasi tulang dan gigi, mengatur pengalihan energi, absorpsi dan transportasi zat gizi, bagian dari ikatan tubuh esensial, dan mengatur keseimbangan asam-basa (Almatsier 2006). Sumber fosfor yang utama adalah bahan makanan dengan kadar protein tinggi, diantaranya daging, unggas, ikan, dan telur. Kekurangan fosfor dapat mengakibatkan terhambatnya pertumbuhan, kerusakan gigi, dan kerusakan tulang (Sediaoetama 1987).
e. Kalium (K)
asam piruvat dalam proses metabolisme karbohidrat (Winarno 2008). Kalium terdapat di dalam semua makanan yang berasal dari tumbuh-tumbuhan dan hewan terutama makanan mentah atau segar (Almatsier 2006).
2.6.2 Mineral mikro
Mineral mikro dibutuhkan tubuh dalam jumlah kurang dari 100 mg sehari (Almatsier 2006). Kelompok mineral mikro antara lain: besi (Fe), seng (Zn), iodium (I), dan selenium (se). Mineral mikro terdapat dalam jumlah sangat kecil di dalam tubuh, namun mempunyai peranan esensial untuk kehidupan, kesehatan dan reproduksi (Almatsier 2006).
a. Besi (Fe)
Besi merupakan mineral mikro yang paling banyak terdapat di dalam tubuh manusia dan hewan, yaitu sebanyak 3-5 gram di dalam tubuh manusia. Besi mempunyai beberapa fungsi penting di dalam tubuh, yaitu sebagai alat angkut oksigen dari paru-paru ke jaringan tubuh, sebagai alat angkut elektron di dalam sel dan sebagai bagian terpadu berbagai reaksi enzim di dalam jaringan tubuh. Defisiensi besi dapat menyebabkan anemia. Kekurangan besi pada umumnya menyebabkan pucat, rasa lemah, letih, pusing, kurang nafsu makan, dan menurunnya kekebalan tubuh. Kelebihan besi dapat menyebabkan muntah, diare, sakit kepala, denyut jantung meningkat, dan pingsan (Almatsier 2006).
b. Seng (Zn)
Seng memiliki peranan penting dalam banyak fungsi tubuh, diantaranya dalam berbagai aspek metabolisme, kemampuan untuk sintesis DNA dan RNA, sintesis dan degradasi kolagen, pengembangan fungsi reproduksi laki-laki serta berperan dalam fungsi kekebalan tubuh. Sumber Seng yang paling baik adalah sumber protein hewani, terutama daging, hati, kerang, dan telur. Kekurangan seng dapat menyebabkan fungsi pencernaan terganggu, gangguan pertumbuhan dan kematangan seksual, gangguan sistem saraf dan fungsi otak serta gangguan pada fungsi kekebalan tubuh. Kelebihan seng dapat menurunkan absorpsi tembaga serta mempengaruhi metabolisme kolesterol (Almatsier 2006).
c. Selenium (Se)
yang mencegah terjadinya radikal bebas dengan menurunkan konsentrasi peroksida dalam sel, sedangkan vitamin E menghalangi bekerjanya radikal bebas setelah terbentuk. Konsumsi selenium dalam jumlah cukup menghemat penggunaan vitamin E. Sumber utama selenium adalah makanan laut, organ hati dan ginjal (Almatsier 2006).
2.7 Logam Berat
Logam berat merupakan unsur-unsur metalik yang memiliki sifat berbahaya dengan berat atom lebih dari 40 (Panjaitan 2009). Logam berat cenderung terakumulasi dalam rantai makanan dan terkadang dikonsumsi oleh organisme. Avertebrata bentik dan ikan mengakumulasi logam berat dari air dan sedimen, moluska dan krustasea memiliki konsentrasi yang lebih tinggi dibanding avertebrata lainnya. Bivalvia terkenal akan kemampuannya mengakumulasi logam berat dan telah banyak digunakan sebagai bioindikator untuk pengawasan logam berat pada lingkungan perairan (Kanakaraju et al. 2008).
Logam berat memiliki sifat tidak dapat terurai (non degradable) dan mudah diabsorbsi. Logam di dalam air jarang berbentuk atom, biasanya terikat dengan senyawa lainnya membentuk molekul. Ikatan yang terbentuk dapat berupa garam organik (senyawa metil, etil, fenil) maupun garam anorganik (oksida, klorida, sulfide, karbonat, hidroksida). Bentuk ion dari garam tersebut biasanya banyak ditemukan dalam air kemudian bersenyawa atau diserap dan tertimbun dalam tanaman dan hewan air (Darmono 1995).
Sifat umum kekerangan sebagai filter feeder menyebabkan kualitas kerang sangat dipengaruhi oleh kualitas perairan di suatu lingkungan. Kerang yang hidup dalam lumpur dapat memakan sedimen dan menyaring logam-logam berat (Ditjen PPHP 2010). Unsur-unsur logam berat dapat masuk ke dalam tubuh organisme dengan tiga cara, yaitu melalui rantai makanan, insang, dan difusi melalui permukaan kulit (Siagian 2004).
menyebabkan runoff yang memiliki kemampuan untuk mengaduk beberapa logam berat (Nwabueze 2011). Berdasarkan persyaratan mutu dan keamanan pangan daging kerang beku (SNI 3460.1-2009), persyaratan maksimum kandungan timbal (Pb) yaitu 1 mg/kg, merkuri (Hg) 0,5 mg/kg dan kadmium (Cd) 1 mg/kg (BSN 2009).
2.7.1 Timbal (Pb)
Timbal (Pb) adalah logam lunak kebiruan atau kelabu keperakan yang lazim terdapat dalam kandungan endapan sulfit yang tercampur mineral-mineral lain, terutama seng dan tembaga. Pencemaran Pb dapat terjadi di udara, air, maupun tanah (Panjaitan 2009). Timbal (Pb) dan persenyawaannya dapat berada di dalam badan perairan secara alamiah dan sebagai dampak dari aktivitas manusia diantaranya adalah air buangan (limbah) industri dan dari pertambangan biji timah hitam. Senyawa Pb dalam perairan berada dalam bentuk ion Pb2+ dan Pb4-. Ikan dapat mengadsorbsi Pb dari permukaan tubuh dan makanan yang dikonsumsinya. Kerang dapat mengakumulasi Pb dalam jumlah besar (Siagian 2004). Termakannya senyawa timbal dalam konsentrasi tinggi dapat mengakibatkan gejala keracunan, diantaranya iritasi gastrointestinal akut, rasa logam pada mulut, muntah, sakit perut, dan diare (Darmono 1995).
2.7.2 Kadmium (Cd)
Kadmium (Cd) merupakan logam berwarna putih keperakan menyerupai alumunium. Logam ini banyak bercampur dengan logam lain terutama Zn dan Hg. Kadmium memiliki sifat yang tahan panas sehingga digunakan untuk campuran pembuatan keramik, enamel, dan plastik, serta sangat tahan terhadap korosi sehingga dapat digunakan untuk melapisi pelat baja dan besi. Kadmium (Cd) dalam air laut berbentuk senyawa klorida (CdCl2), sedangkan dalam air tawar berbentuk karbonat (CdCO3). Pada air payau yang biasanya terdapat di muara sungai, kedua senyawa tersebut jumlahnya berimbang (Darmono 1995). Kadmium dilepaskan di udara, tanah dan air oleh aktivitas manusia. Organisme-organisme yang hidup bebas dan dapat dimakan seperti kekerangan, krustase, dan jamur adalah akumulator alami kadmium (IPCS 1992 diacu dalam Codex 1995).
diabsorpsi melalui saluran dinding usus dan diangkut melalui pembuluh darah serta didistribusikan dalam jaringan terutama ginjal dan hati, dimana kurang lebih 50% dari logam tersebut terakumulasikan. Moluska seringkali mengakumulasi Cd pada kelenjar pencernaannya (Laurenco et al. 2009). Keracunan kadmium dapat mengakibatkan efek yang kronis dan akut. Efek akut ditunjukkan dengan gejala diare, kejang perut dan pusing, sedangkan efek kronis biasanya mengakibatkan kerusakan pada ginjal dan kerusakan pada sistem syaraf (Darmono 1995).
2.7.3 Merkuri (Hg)
Merkuri (Hg) merupakan unsur renik pada kerak bumi. Merkuri terdapat di lingkungan sebagai senyawa anorganik dan organik. Logam ini biasanya disebut air raksa, biasanya bersenyawa dengan sulfid membentuk HgS, akan tetapi logam ini tersebar luas dalam bentuk gabungan pada batu dan tanah. Merkuri digolongkan sebagai pencemar paling berbahaya diantara berbagai macam logam berat. Sumber merkuri dapat berasal dari pelapukan batuan dan erosi tanah yang melepas merkuri ke dalam perairan. Berbagai jenis aktivitas manusia dapat meningkatkan kadar merkuri di lingkungan. Aktivitas tersebut antara lain adalah penambangan, peleburan (untuk menghasilkan logam dari bijih tambang sulfidnya), pembakaran bahan bakar fosil, dan produksi baja, semen serta fosfat (Putri 2009).
3.1 Waktu dan Tempat Penelitian
Penelitian ini dilaksanakan pada bulan September hingga Oktober 2011. Preparasi, pengukuran morfometrik dan penghitungan rendemen dilakukan di Laboratorium Karakteristik Bahan Baku, Departemen Teknologi Hasil Perairan, Fakultas Perikanan dan Ilmu Kelautan, Institut Pertanian Bogor. Pengujian proksimat dilakukan di Laboratorium Biokimia Hasil Perairan Fakultas Perikanan dan Ilmu Kelautan, Institut Pertanian Bogor. Analisis asam lemak dilakukan di Laboratorium Terpadu Pascasarjana Baranang Siang, Institut Pertanian Bogor. Analisis kolesterol dilakukan di Laboratorium Terpadu Ilmu Nutrisi dan Teknologi Pakan sedangkan analisis mineral dan logam berat dilakukan di Laboratorium Pengujian Nutrisi Pakan, Departemen Ilmu Nutrisi dan Teknologi Pakan, Fakultas Peternakan, Institut Pertanian Bogor.
3.2 Bahan dan Alat
Bahan baku yang digunakan pada penelitian ini yaitu daging dan jeroan kerang pisau (Solen spp) yang berasal dari Pantai Kejawanan, Cirebon. Bahan yang digunakan untuk analisis proksimat meliputi akuades, HCl 0,1 N, NaOH 40%, katalis selenium, H2SO4, H3BO3 2%, kertas saring, kapas bebas lemak, pelarut heksana, bromcresol green 0,1%, dan methyl red 0,1%. Bahan yang digunakan untuk analisis asam lemak adalah NaOH 0,5 N dalam metanol, BF3, NaCl jenuh, n-heksana, dan Na2SO4 anhidrat. Bahan yang dibutuhkan untuk analisis kolesterol adalah etanol, petroleum benzen, alkohol, acetic anhidrid, dan H2SO4 pekat. Adapun bahan-bahan yang digunakan untuk analisis mineral dan logam berat adalah akuades, H2SO4, HCl, HNO3, dan HClO4.
(metilasi), perangkat kromatografi gas Shimadzu GC 2010+, sedangkan analisis kolesterol menggunakan beberapa alat antara lain: tabung reaksi, vortex, pipet, dan evaporator. Alat-alat yang digunakan untuk analisis mineral dan logam berat adalah timbangan digital, sudip, pipet, bulb, hotplate, corong, labu takar, labu destruksi, kertas Whatman 42, spektrofotometer dan Atomic Absorption Spectrophotometer (AAS) Shimadzu AA-680.
3.3 Metode Penelitian
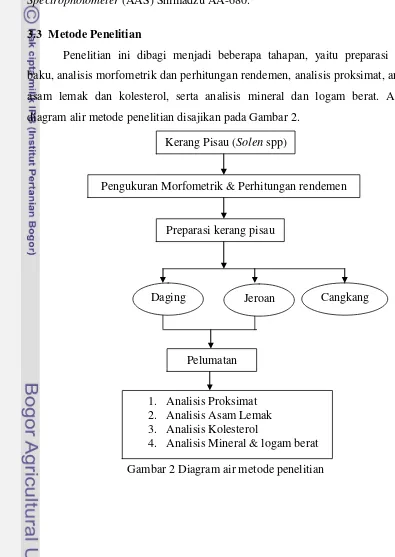
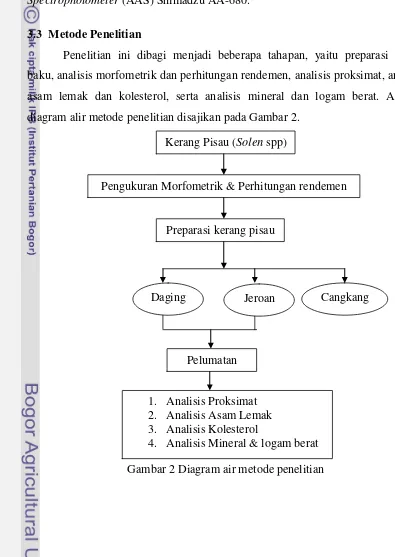
Penelitian ini dibagi menjadi beberapa tahapan, yaitu preparasi bahan baku, analisis morfometrik dan perhitungan rendemen, analisis proksimat, analisis asam lemak dan kolesterol, serta analisis mineral dan logam berat. Adapun diagram alir metode penelitian disajikan pada Gambar 2.
Gambar 2 Diagram air metode penelitian Kerang Pisau (Solen spp)
Pengukuran Morfometrik & Perhitungan rendemen
Preparasi kerang pisau
Daging Jeroan Cangkang
Pelumatan
1. Analisis Proksimat 2. Analisis Asam Lemak 3. Analisis Kolesterol
3.3.1 Preparasi bahan baku dan perhitungan rendemen
Kerang pisau (Solen spp) diperoleh dari Pantai Kejawanan, Cirebon. Bahan baku selanjutnya dianalisis morfometrik yang meliputi berat total, panjang, lebar dan tebal. Bagian daging, jeroan, dan cangkang dipisahkan, kemudian dihitung rendemennya. Rendemen masing-masing bagian dapat dihitung dengan rumus sebagai berikut:
Rendemen (%) = berat sampel (gram )
berat total (gram ) x 100%
3.3.2 Analisis proksimat
Analisis proksimat merupakan suatu analisis yang dilakukan untuk mengetahui komposisi kimia pada suatu bahan. Analisis proksimat meliputi analisis kadar air, kadar abu, protein, lemak dan karbohidrat secara by difference. (a) Analisis kadar air (AOAC 2005)
Analisis kadar air dihitung berdasarkan perbedaan berat contoh sebelum dan setelah dikeringkan. Tahap pertama yang dilakukan pada analisis kadar air adalah mengeringkan cawan porselen dalam oven pada suhu 102-105 °C hingga 1 jam. Cawan tersebut diletakkan ke dalam desikator dan dibiarkan sampai dingin kemudian ditimbang. Kemudian masukkan sampel seberat 5 gram ke dalam cawan. Selanjutnya cawan tersebut dimasukkan ke dalam oven 102-105 °C selama 6 jam. Cawan tersebut dimasukkan ke dalam desikator dan dibiarkan sampai dingin kemudian ditimbang. Perhitungan kadar air pada daging lorjuk:
Keterangan: A = Berat cawan kosong (gram)
B = Berat cawan yang diisi sampel (gram) sebelum dioven C = Berat cawan dengan sampel (gram) setelah dioven
(b) Analisis kadar abu (AOAC 2005)
Analisis kadar abu dilakukan dengan cara mengabukan sampel ke dalam tanur. Cawan abu porselen dipanaskan dalam tungku pengabuan bersuhu sekitar 105 °C selama 1 jam. Cawan abu porselen tersebut didinginkan dalam desikator lalu ditimbang. Sampel sebanyak 5 gram dimasukkan ke dalam cawan abu porselen. Cawan tersebut dimasukkan ke dalam tungku secara bertahap hingga
suhu 600 °C. Proses pengabuan dilakukan sampai abu berwarna putih. Setelah itu, cawan abu porselen didinginkan selama 30 menit di dalam desikator kemudian ditimbang beratnya. Perhitungan kadar abu pada sampel:
Keterangan: A = Berat cawan kosong (gram)
B = Berat cawan yang diisi sampel (gram) sebelum ditanur C = Berat cawan dengan sampel (gram) setelah ditanur
(c) Analisis kadar protein (AOAC 1980)
Prinsip analisis kadar protein yaitu untuk mengetahui kandungan protein kasar (crude protein) pada suatu bahan. Tahap-tahap yang dilakukan dalam analisis kadar protein terdiri dari tiga tahap, yaitu destruksi, destilasi, dan titrasi. (1) Tahap destruksi
Larutan yang telah jernih didinginkan dan ditambahkan 50 ml akuades dan 20 ml NaOH 40%, lalu didestilasi. Hasil destilasi ditampung dalam erlenmeyer 125 ml yang berisi 25 ml asam borat (H3BO3) 2% yang mengandung indikator bromcresol green 0,1% dan methyl red 0,1% dengan perbandingan 2:1. Destilasi dilakukan dengan menambahkan 50 ml larutan NaOH-Na2S2O3 ke dalam alat destilasi hingga tertampung 40 ml destilat di dalam erlenmeyer dengan hasil destilat berwarna hijau kebiruan.
(3) Tahap titrasi
Titrasi dilakukan dengan menggunakan HCl 0,1 N sampai warna larutan pada erlenmeyer berubah warna menjadi merah muda. Perhitungan kadar protein adalah sebagai berikut:
(d) Analisis kadar lemak (AOAC 2005)
Sampel seberat 5 gram dimasukkan ke dalam kertas saring dan dimasukkan ke dalam kertas saring dengan ujung-ujungnya diberi kapas kemudian dimasukkan ke dalam labu lemak yang sudah ditimbang berat konstannya dan disambungkan dengan tabung soxhlet. Selongsong lemak dimasukkan ke dalam ruang ekstraktor tabung soxhlet dan disiram dengan pelarut lemak. Tabung ekstraksi dipasang pada alat destilasi soxhlet dan dipanaskan kemudian dilakukan refluks selama 6 jam. Pelarut lemak yang ada dalam labu lemak didestilasi hingga semua pelarut lemak menguap. Saat destilasi pelarut akan tertampung di ruang ekstraktor, pelarut dikeluarkan sehingga tidak kembali ke dalam labu lemak selanjutnya labu lemak dikeringkan dalam oven pada suhu 105 °C. Kemudian labu didingingkan dalam desikator hingga beratnya konstan. Perhitungan kadar lemak pada sampel:
Keterangan: W1 = Berat sampel (gram)
W2 = Berat labu lemak tanpa lemak (gram)
W3 = Berat labu lemak dengan lemak (gram)
(e) Analisis kadar karbohidrat (AOAC 2005)
Kadar karbohidrat dilakukan secara by difference, yaitu hasil pengurangan dari 100% dengan kadar air, kadar abu, kadar protein dan kadar lemak sehingga kadar karbohidrat tergantung pada faktor pengurangan. Kadar karbohidrat dapat dihitung dengan menggunakan rumus:
Karbohidrat (%): 100% - (% abu + % air + % lemak + % protein)
3.3.3 Analisis asam lemak (AOAC 1999)
Metode analisis yang digunakan memiliki prinsip mengubah asam lemak menjadi turunannya, yaitu metil ester sehingga dapat terdeteksi oleh alat kromatografi. Gas chromatography (GC) memiliki prinsip kerja pemisahan antara gas dan lapisan tipis cairan berdasarkan perbedaan jenis bahan (Fardiaz 1989). Analisis dengan kromatografi gas didasarkan pada partisi komponen-komponen
dari suatu cairan di antara fase gerak berupa gas dan fase diam berupa zat padat atau cairan yang tidak mudah menguap yang melekat pada bahan pendukung inert. Komponen-komponen yang dipisahkan harus mudah menguap pada suhu pemisahan yang dilakukan, sehingga suhu operasi biasanya lebih tinggi dari suhu kamar dan biasanya dilakukan derivatisasi untuk contoh yang sulit menguap.
Dalam hal analisis asam lemak, mula-mula sampel lemak atau minyak dihidrolisis menjadi asam lemak, kemudian ditransformasi menjadi bentuk esternya yang bersifat lebih mudah menguap. Transformasi dilakukan dengan cara metilasi sehingga diperoleh metil ester asam lemak (FAME). Selanjutnya FAME dianalisis dengan alat kromatografi gas. Alat kromatografi gas yang digunakan adalah kromatografi gas Shimadzu GC 2010+.
Hasil analisis akan tertekan dalam suatu lembaran yang terhubung dengan rekorder dan ditunjukkan melalui beberapa puncak pada waktu retensi tertentu sesuai dengan karakter masing-masing asam lemak. Identifikasi tiap komponen asam lemak dilakukan dengan membandingkan waktu retensinya dengan waktu retensi standar pada kondisi analisis yang sama. Waktu retensi dihitung pada kertas rekorder sebagai jarak dari garis pada saat muncul pelarut sampai ke tengah puncak komponen yang dipertimbangkan. Luas puncak dari masing-masing komponen adalah berbanding lurus dengan jumlah komponen tersebut dalam contoh. Analisis asam lemak dilakukan melalui tahap ekstraksi, metilasi, injeksi, dan pembacaan sampel dengan kromatogram.
(a) Ekstraksi
Tahap pertama dilakukan ekstraksi soxhlet untuk memperoleh lemak. Sampel ditimbang sebanyak 20-30 mg lemak untuk dilanjutkan ke tahap metilasi (b) Pembentukan metil ester (metilasi)
Tahap metilasi dimaksudkan untuk membentuk senyawa turunan dari asam lemak menjadi metil esternya. Asam-asam lemak diubah menjadi ester-ester metil atau alkil yang lainnya sebelum disuntikkan ke dalam kromatografi gas (Fardiaz 1989).
bourtiflourid-metanol pada sampel dan dipanaskan pada suhu 80 °C selama 20 menit pada waterbath, diangkat dan dibiarkan dingin. Selanjutnya ditambahkan 2 ml BF3 20% dan dipanaskan lagi selama 20 menit. Kemudian didinginkan, dan ditambahkan 2 ml NaCl jenuh dan 1 ml isooctane dikocok dengan baik. Lapisan isooktan bagian atas larutan dipindahkan dengan bantuan pipet tetes ke dalam tabung reaksi yang berisi 0,1 gram Na2SO4 anhidrat, didiamkan selama 15 menit. Larutan disaring dengan mikrofilter untuk memisahkan fase cairnya sebelum diinjeksikan ke dalam kromatografi gas. Sebanyak 1 μl sampel diinjeksikan ke dalam Gas Chromatography. Asam lemak yang ada dalam metil ester akan diidentifikasi oleh Flame Ionization Detector (FID) atau detektor ionisasi nyala dan respon yang ada akan tercatat melalui kromatogram (peak).
(c) Identifikasi dengan kromatografi gas
Identifikasi asam lemak dilakukan dengan menginjeksikan metil ester pada alat kromatografi gas GC Shimadzu 2010+. Adapun kondisi alat saat analisis adalah sebagai berikut: Kolom: kolom kapiler Cyanopropil methyl sil (merek Quadrex). Dimensi Kolom: p = 60 m, diameter dalam 0,25 mm, tebal lapisan film 0,25 µm. Gas yang digunakan sebagai fase gerak adalah gas nitrogen dengan aliran bertekanan 30 ml/menit. Dalam proses pembakaran FID digunakan gas H2 dengan laju alir 40 ml/menit dan He dengan laju alir 30 ml/menit. Laju alir udara 400 ml/menit. Suhu injektor 220 °C, sedangkan suhu detektor 240 °C. Suhu oven yang digunakan adalah temperatur terprogram dengan laju kenaikan suhu yang tertera pada Tabel 2.
Tabel 2 Laju kenaikan suhu oven
Rate (°C/menit) Temperatur (°C) Hold time (menit)
- 125 5
10 185 5
5 205 10
3 225 7
(d) Perhitungan jumlah asam lemak
Prinsip analisis komposisi asam lemak dengan kromatografi gas adalah dengan mengubah komponen asam lemak pada lemak/minyak menjadi seyawa volatil metil ester asam lemak yang akan dideteksi oleh detektor FID dalam bentuk respon berupa peak kromatogram. Jenis dan jumlah asam lemak yang ada pada contoh dapat diidentifikasi dengan membandingkan peak kromatogram contoh dengan peak kromatogram asam lemak standar yang telah diketahui jenis dan konsentrasinya, kemudian dihitung kadar asam lemaknya. Kadar asam lemak dalam sampel dapat dihitung dengan rumus:
3.3.4 Analisis kolesterol dengan spektrofotometer
Analisis kolesterol dilakukan menggunakan spektrofometer. Sampel kerang pisau sebanyak 0,1 gram sampel dimasukkan ke dalam tabung sentrifuge ditambah 8 ml (etanol:petroleum benzena) dengan perbandingan 3:1 dan diaduk sampai homogen. Pengaduk dibilas dengan 2 ml larutan alkohol:petroleum benzena (3:1) kemudian disentrifuge 4000 rpm selama 10 menit.
Supernatan dituang ke dalam beaker glass 100 ml dan diuapkan di penangas air. Residu dilarutkan dengan kloroform sedikit demi sedikit sambil dituangkan ke dalam tabung berskala (sampai volume 5 ml) dan ditambahkan 2 ml acetic anhidrid ditambahkan juga 0,2 ml H2SO4 pekat atau 2 tetes. Selanjutnya dihomogenkan dengan vortex dan dibiarkan di tempat gelap selama 15 menit. Absorbansinya dibaca pada panjang gelombang 420 nm dengan standar yang digunakan 0,4 mg/ml.
Kadar kolesterol dalam sampel dihitung dengan rumus:
Kadar Kolesterol = Absorbansi contoh Absorbansi standar x
3.3.5 Analisis Mineral dan Logam Berat
(a) Pengujian total mineral (K, Na, Ca, Mg, Se, Zn, Fe)
Sampel yang akan diuji dilakukan proses pengabuan basah. Pada proses pengabuan basah, sebanyak 10 g contoh dimasukkan ke dalam erlenmeyer 150 ml. Selanjutnya ditambahkan 10 ml HNO3 dan dibiarkan selama 1 jam, kemudian dipanaskan di atas hotplate selama 4 jam dan didinginkan. Selanjutnya ditambahkan 0,8 ml H2SO4 pekat dan dipanaskan kembali. Setelah terjadi perubahan warna dari cokelat menjadi kuning bening, sampel ditambahkan campuran HClO4 dan HNO3 (2:1) sebanyak 4 tetes dan dipanaskan kembali 15 menit. Selanjutnya sampel ditambahkan 4 ml akuades dan 1,2 ml HCl pekat dan dipanaskan kembali sampai larut kemudian didinginkan. Setelah larut, sampel diencerkan menjadi 50 ml didalam labu takar dan dilakukan analisis mineral menggunakan Atomic Absorption Spectrophotometer (AAS) Shimadzu AA-680. Kadar mineral pada sampel dihitung dengan memasukkan nilai absorban sampel ke dalam persamaan garis standar y = ax ± b, maka akan diperoleh nilai x yang merupakan konsentrasi sampel. Kadar mineral dalam sampel dapat dihitung dengan menggunakan rumus sebagai berikut:
Kadar mineral (mg/kg bb) = konsentrasi mineral ×FP berat sampel (g)
Keterangan: FP = faktor pengencer
(b) Pengujian fosfor
(c) Pengujian logam Hg
4.1 Karakteristik Kerang Pisau (Solen spp)
Kerang pisau yang digunakan pada penelitian ini berasal dari Pantai Kejawanan, Kelurahan Pegambiran, Kecamatan Lemahwungkuk, Cirebon. Kerang ini memiliki nama lokal antara lain ”lorjuk” untuk daerah Jawa Timur, ”ambal” untuk darah Sarawak dan ”embet” untuk daerah Cirebon. Kerang pisau ini memiliki ciri-ciri simetris bilateral dengan kedua cangkang yang panjang dan tubuhnya kecil memanjang. Salah satu ujung tubuhnya berbentuk runcing seperti mata pisau. Kulit cangkangnya berwarna kuning kehijauan. Bentuk morfologi kerang pisau dapat dilihat pada Gambar 3.
Gambar 3 Morfologi kerang pisau (Solen spp) hasil penelitian
Pengukuran morfometrik kerang pisau dilakukan terhadap 30 sampel. Pengukuran ini terdiri dari pengukuran panjang, lebar, tebal dan berat untuk menentukan rendemen. Hasil rata-rata pengukuran morfometrik dapat dilihat pada Tabel 3.
Tabel 3 Morfometrik kerang pisau (Solen spp)
Parameter Nilai
Panjang (cm) 4,75 ± 0,61
Lebar (cm) 0,83 ± 0,11
Tebal (cm) 0,87 ± 0,15
Bobot utuh (gram) 2,27 ± 0,65
sebelumnya kerang pisau yang menyatakan ukuran panjang kerang pisau antara 3-4 cm dan lebar 0,5-1 cm (Nurjanah et al. 2008).
4.2 Rendemen
Rendemen adalah persentase antara berat suatu bagian yang dapat dimanfaatkan dibandingkan dengan berat bahan utuh. Rendemen paling besar adalah bagian daging yaitu sebesar 41,02%, diikuti bagian cangkang sebesar 35,49%, dan bagian jeroan sebesar 23,49%. Nilai rendemen cangkang ini tidak jauh berbeda dibandingkan dengan hasil penelitian sebelumnya yang menyatakan bahwa rendemen kerang pisau bagian daging 60,79%, cangkang 34,50% dan sisa (air) 4,71% (Nurjanah et al. 2008). Rendemen daging kerang pisau pada penelitian ini lebih besar daripada rendemen kerang hijau yaitu sebesar 27,75% (Sobana 2005) dan simping sebesai 30,91% (Meida 2003). Perbedaan rendemen ini mungkin dipengaruhi oleh beberapa faktor, diantaranya jenis, bentuk tubuh, dan umur (Suzuki 1981).
Bagian yang umumnya dimanfaatkan oleh masyarakat adalah bagian daging kerang pisau sebagai bahan pangan, namun bagian cangkang juga dapat dimanfaatkan karena umumnya cangkang kerang kaya akan kalsium dan fosfor. Jenis-jenis kerang, udang, kerang, cumi-cumi, insekta dan fungi merupakan sumber kitin dan kitosan (Okuzumi dan Fujii 2000).
4.3 Komposisi Kimia
Komposisi kimia pada kerang pisau diperoleh melalui analisis proksimat yang meliputi kadar air, abu, protein, lemak dan karbohidrat (secara by difference). Contoh perhitungan analisis proksimat dapat dilihat pada Lampiran 3. Komposisi kimia daging dan jeroan kerang pisau dapat dilihat pada Tabel 4.
Tabel 4 Komposisi kimia daging dan jeroan kerang pisau (Solen spp) Komposisi
kimia
Terdapat perbedaan antara komposisi kerang pisau hasil penelitian ini dengan penelitian sebelumnya, hal ini dapat dikarenakan perbedaan habitat. Komposisi kimia ikan dapat bervariasi antar spesies, antar individu dalam satu spesies, dan antar bagian dari satu individu ikan. Variasi tersebut dapat disebabkan oleh beberapa faktor, antara lain umur, laju metabolisme, aktivitas pergerakan, makanan, dan kondisi sebelum dan sesudah musim bertelur (Suzuki 1981).
4.3.1 Kadar air
Hasil analisis proksimat untuk uji kadar air daging dan jeroan kerang pisau pada penelitian ini menunjukkan nilai masing-masing sebesar 78,59% dan 75,49%. Nilai ini lebih kecil dibandingkan dengan kadar air kerang pisau yaitu 82,31% (Nurjanah et al. 2008), namun lebih tinggi bila dibandingkan dengan kadar air kerang darah (Anadara granosa) yaitu 74,37% (Nurjanah et al. 2005). Kandungan air pada kerang pisau hasil penelitian ini tidak jauh berbeda bila dibandingkan dengan beberapa jenis kerang lainnya yaitu kandungan air kerang Spisula solidissima sebesar 74,0%, Codacia orbicularis 74,8%, Panope generosa 78,8% dan Protothaca staminea 79,4% (Krzynowek dan Murphy 1987).
Perbedaan kadar air dalam suatu spesies dapat terjadi karena perbedaan habitat, spesies, umur, dan laju metabolisme. Air dalam tubuh berfungsi sebagai pelarut dan alat angkut zat-zat gizi, terutama vitamin larut air dan mineral. Air juga berfungsi sebagai katalisator, pelumas, fasilitator pertumbuhan, pengatur suhu dan peredam benturan (Almatsier 2006). Kadar air yang tinggi pada komoditas hasil perairan menyebabkan mudah mengalami kerusakan (highly perishable).
4.3.2 Kadar abu
Hasil analisis kadar abu pada daging dan jeroan kerang pisau masing-masing adalah 1,45% dan 2,61%. Nilai kadar abu kerang pisau pada penelitian ini sedikit lebih rendah bila dibandingkan dengan hasil penelitian sebelumnya yang
menyatakan bahwa kadar abu kerang pisau adalah sebesar 2,63% (Nurjanah et al. 2008). Kandungan abu kerang pisau hasil penelitian ini juga lebih
Tinggi rendahnya kadar abu dapat disebabkan oleh perbedaan hábitat dan lingkungan hidup yang berbeda. Setiap lingkungan perairan dapat menyediakan asupan mineral yang berbeda-beda bagi organisme akuatik yang hidup di dalamnya. Masing-masing individu organisme juga memiliki kemampuan yang berbeda-beda dalam meregulasi dan mengabsorbsi komponen anorganik, sehingga hal ini nantinya akan memberikan pengaruh pada nilai kadar abu dalam masing-masing bahan (Rusyadi 2006).
4.3.3 Kadar protein
Protein merupakan komponen kedua yang paling banyak terdapat pada kerang pisau setelah air. Hasil pengujian menunjukkan bahwa kadar protein kerang pisau pada penelitian ini adalah 14,59% untuk daging dan 15,60% untuk jeroan. Nilai protein pada penelitian ini lebih tinggi jika dibandingkan dengan kandungan protein kerang pisau hasil penelitian sebelumnya yaitu sebesar 9,79% (Nurjanah et al. 2008). Namun lebih rendah dibandingkan dengan kandungan protein kerang darah (Anadara granosa) yaitu 19,48%. Perbedaan kadar protein ini dapat terjadi karena perbedaan kondisi habitat tempat kerang berasal. Komposisi kimia kerang sangat bervariasi tergantung pada spesies, jenis kelamin, umur, dan habitat (Nurjanah et al. 2005).
4.3.4 Kadar lemak
Hasil uji kadar lemak pada penelitian ini masing-masing adalah sebesar 1,72% pada daging dan 1,95% sebesar pada jeroan. Nilai lemak pada penelitian ini lebih tinggi daripada kandungan lemak kerang pisau hasil penelitian sebelumnya yaitu sebesar 0,32% (Nurjanah et al. 2008), namun lebih rendah bila dibandingkan dengan spesies lain misalnya kerang darah (Anadara granosa) yang memiliki kadar lemak 2,50% (Nurjanah et al. 2005). Perbedaan kandungan lemak antar spesies yang sama dapat terjadi karena perbedaan habitat tempat spesies tersebut berasal dan bergantung bagaimana kondisi hidup, laju metabolisme dan umur.
(Yuliani 2010). Pada tubuh hewan, lemak disimpan di bawah kulit dan di sekitar organ tertentu, misalnya lemak di sekitar ginjal (Gaman dan Sherrington 1992). 4.3.5 Kadar karbohidrat
Kadar karbohidrat pada penelitian ini dihitung berdasarkan metode by difference. Hasil perhitungan menunjukkan nilai karbohidrat pada daging dan jeroan kerang pisau masing-masing sebesar 3,68% dan 4,79%. Karbohidrat pada produk perikanan umumnya terdapat dalam bentuk glikogen. Kandungan glikogen pada produk perikanan sebesar 1% pada ikan, 1% pada krustasea, dan 1-8% pada kekerangan (Okuzumi dan Fujii 2000). Kadar karbohidrat kerang pisau hasil penelitian ini tidak begitu jauh berbeda namun sedikit lebih rendah bila dibandingkan dengan karbohidrat kerang pisau hasil penelitian sebelumnya yaitu 4,95%. Perbedaan kandungan karbohidrat ini dapat terjadi karena perbedaan habitat, jenis kelamin, umur dan laju metabolisme spesies.
4.4 Komposisi Asam Lemak
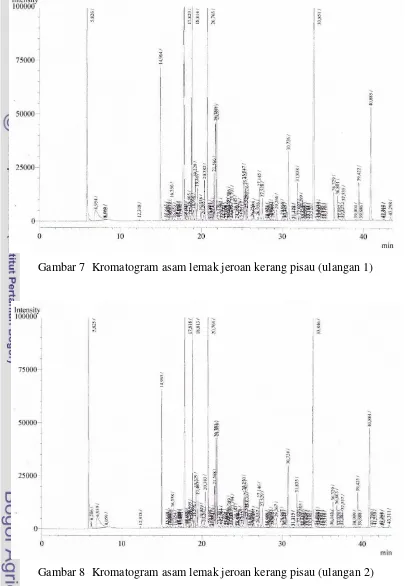
Injeksi asam lemak menghasilkan kromatogram. Masing-masing peak kromatogram menunjukkan jenis asam lemak tertentu. Kromatogram standar asam lemak disajikan pada Gambar 4. Kromatogram sampel kerang pisau disajikan pada Gambar 5-8.
Gambar 5 Kromatogram asam lemak daging kerang pisau (ulangan 1)
Gambar 7 Kromatogram asam lemak jeroan kerang pisau (ulangan 1)
Gambar 8 Kromatogram asam lemak jeroan kerang pisau (ulangan 2)
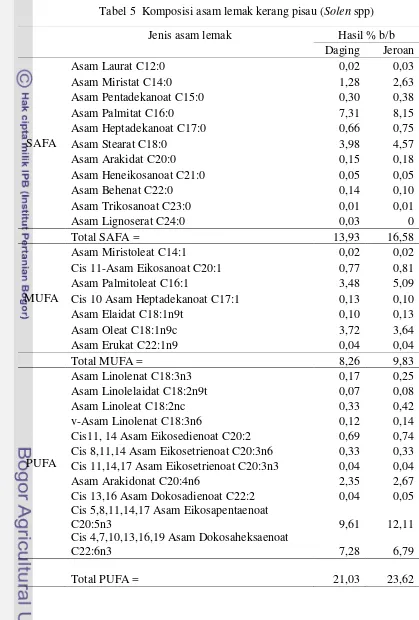
jenuh majemuk (polyunsaturated fatty acid/PUFA). Komposisi asam lemak kerang pisau dapat dilihat pada Tabel 5.
Tabel 5 Komposisi asam lemak kerang pisau (Solen spp)
Jenis asam lemak Hasil % b/b
Daging Jeroan
SAFA
Asam Laurat C12:0 0,02 0,03
Asam Miristat C14:0 1,28 2,63
Asam Pentadekanoat C15:0 0,30 0,38
Asam Palmitat C16:0 7,31 8,15
Asam Heptadekanoat C17:0 0,66 0,75
Asam Stearat C18:0 3,98 4,57
Asam Arakidat C20:0 0,15 0,18
Asam Heneikosanoat C21:0 0,05 0,05
Asam Behenat C22:0 0,14 0,10
Asam Trikosanoat C23:0 0,01 0,01
Asam Lignoserat C24:0 0,03 0
Total SAFA = 13,93 16,58
MUFA
Asam Miristoleat C14:1 0,02 0,02
Cis 11-Asam Eikosanoat C20:1 0,77 0,81
Asam Palmitoleat C16:1 3,48 5,09
Cis 10 Asam Heptadekanoat C17:1 0,13 0,10
Asam Elaidat C18:1n9t 0,10 0,13
Asam Oleat C18:1n9c 3,72 3,64
Asam Erukat C22:1n9 0,04 0,04
Total MUFA = 8,26 9,83
PUFA
Asam Linolenat C18:3n3 0,17 0,25
Asam Linolelaidat C18:2n9t 0,07 0,08
Asam Linoleat C18:2nc 0,33 0,42
v-Asam Linolenat C18:3n6 0,12 0,14
Cis11, 14 Asam Eikosedienoat C20:2 0,69 0,74
Cis 8,11,14 Asam Eikosetrienoat C20:3n6 0,33 0,33 Cis 11,14,17 Asam Eikosetrienoat C20:3n3 0,04 0,04
Asam Arakidonat C20:4n6 2,35 2,67
Cis 13,16 Asam Dokosadienoat C22:2 0,04 0,05
Cis 5,8,11,14,17 Asam Eikosapentaenoat
C20:5n3 9,61 12,11
Cis 4,7,10,13,16,19 Asam Dokosaheksaenoat
C22:6n3 7,28 6,79
Asam lemak jenuh paling tinggi yang terdapat pada kerang pisau adalah palmitat yaitu sebesar 7,31% (pada daging) dan 8,15% (pada jeroan). Asam lemak miristat, palmitat, dan stearat merupakan jenih asam lemak yang paling banyak terdapat di alam (Almatsier 2006). Nilai kandungan asam palmitat pada penelitian ini lebih tinggi dibandingkan dengan nilai palmitat pada kerang baji (Donax cuneatus) yang memiliki kandungan palmitat sebesar 0,35% (Shanmugam et al. 2007). Perbedaan nilai asam palmitat ini dapat disebabkan karena perbedaan kondisi perairan, selain itu dapat pula disebabkan oleh spesies, ketersediaan pakan, umur dan ukuran. Asam palmitat dapat meningkatkan risiko aterosklerosis, kardiovaskular dan stroke. Asam palmitat digunakan sebagai bahan baku shampo, sabun lunak dan krim (Jacquot 1962).
Kandungan asam lemak miristat daging dan jeroan kerang pisau berturut-turut adalah 1,28 % dan 2,63%. Jacquot (1962) menyatakan bahwa asam miristat terdapat dalam jumlah yang sedikit, tidak lebih dari kisaran 1-2%. Jika dibandingkan dengan spesies lain misalnya kerang baji (Donax cuneatus), kandungan asam lemak miristat kerang pisau pada penelitian ini lebih rendah. Shanmugam et al. (2007) menyatakan bahwa kandungan miristat pada kerang baji adalah 7,15%. Keragaman komposisi asam lemak ini dapat dipengaruhi oleh beberapa faktor, yaitu spesies, ketersediaan pakan, umur, habitat dan ukuran (Ozogul dan Ozogul 2005), serta pergantian musim, letak geografis, dan salinitas lingkungan (Ozyurt et al. 2006).
Kandungan asam stearat pada kerang pisau bagian daging dan jeroan masing-masing adalah 3,98% dan 4,57%. Nilai ini agak lebih rendah bila dibandingkan dengan stearat pada kerang baji (Donax cuneatus) yaitu sebesar 15,68% (Shanmugam et al. 2007). Perbedaan nilai asam lemak disebabkan oleh perbedaan komposisi jenis lemak yang dikonsumsi dari lingkungan hidupnya (Leblanc et al. 2008). Asam stearat merupakan asam lemak jenuh dengan berat molekul tertinggi dan terdapat pada biji-bijian serta minyak hewan laut dalam jumlah yang sedikit (Jacquot 1962).
dan 5,09%. Kandungan oleat pada daging dan jeroan kerang pisau adalah 3,72 dan 3,64 %. Asam oleat lebih stabil dibandingkan dengan asam linoleat dan linolenat, terlihat dari peranannya dalam meningkatkan HDL kolesterol yang lebih besar dan menurunkan LDL kolesterol di dalam darah (Muchtadi et al. 1993). Kandungan palmitoleat pada kerang baji (Donax cuneatus) adalah sebesar 12,71% dan kandungan oleatnya sebesar 11,18% (Shanmugam et al. 2007). Nilai ini lebih tinggi dibandingkan dengan nilai asam lemak palmitoleat dan oleat yang terdapat pada kerang pisau. Hal ini diduga karena perbedaan spesies, makanan, dan habitat kerang tersebut.
Kandungan asam lemak tidak jenuh majemuk yang tinggi pada kerang pisau antara lain: EPA, DHA, dan arakhidonat, sedangkan kandungan linoleat dan linolenat lebih sedikit. Kandungan asam lemak linoleat daging dan jeroan kerang pisau masing-masing adalah 0,33% dan 0,42%, sedangkan kandungan linolenat daging dan jeroan kerang pisau masing-masing adalah 0,17% dan 0,25%. Nilai tersebut lebih rendah bila dibandingkan dengan kandungan linoleat kerang baji (Donax cuneatus) sebesar 2,41% dan kandungan linolenatnya sebesar 0,76% (Shanmugam et al. 2007). Perbedaan ini dapat terjadi karena perbedaan spesies, umur, ukuran, habitat, pergantian musim, dan kondisi lingkungan perairan serta makanan.
Kandungan arakidonat pada kerang pisau hasil penelitian adalah 2,35% (pada daging) dan 2,67% (pada jeroan). Nilai asam arakidonat pada kerang pisau ini lebih rendah jika dibandingkan dengan arakidonat pada tubuh remis air tawar Unio elongatulus yaitu sebesar 6,97% (Ekin dan Bashan 2010). Kandungan DHA kerang pisau bagian daging dan jeroan masing-masing adalah 7,28% dan 6,79%. Kandungan EPA kerang pisau bagian daging dan jeroan masing-masing adalah 9,61% dan 12,11%. Nilai EPA pada kerang pisau ini lebih tinggi jika dibandingkan dengan EPA pada tubuh Unio elongatulus yaitu sebesar 7,21%. Kandungan asam lemak moluska dipengaruhi jenis dan habitat. Moluska yang hidup di air laut umumnya kaya akan asam lemak omega-3 (terutama C18:3ω3, C20:5ω3 dan C22:6ω3). Remis air tawar mengandung lebih banyak omega-6 (terutama C18:2 ω6 dan C:20:4ω6) (Ekin dan Bashan 2010).
4.5 Kolesterol
Kerang pisau merupakan salah satu bahan pangan oleh karena itu kolesterol yang berasal dari daging dan jeroan kerang pisau ini tergolong dietary cholesterol atau exogenous cholesterol. Kandungan kolesterol berbagai jenis makanan dan kandungan kolesterol kerang pisau dapat dilihat pada Tabel 6.
Tabel 6 Kandungan kolesterol pada makanan (mg/100g)
Jenis makanan Kolesterol (mg/100g)
Sumber : *) Okuzumi dan Fujii (2000) **) Nurjanah et al. (2008)
tempat kolesterol disintesis dan disimpan serta organ-organ dalam lainnya. Kandungan kolesterol kerang pisau jika dibandingkan dengan kandungan kolesterol pada bahan makanan pada Tabel 6, tergolong rendah untuk bagian daging kerang pisau dan cukup tinggi untuk bagian jeroan. Kandungan kolesterol kerang pisau baik pada bagian daging maupun jeroan pada penelitian ini lebih tinggi dibandingkan hasil penelitian sebelumnya (Nurjanah et al. 2008) yang menyatakan bahwa kandungan kolesterol kerang pisau adalah 21,28 mg/100 g.
Variasi kolesterol berbagai komoditas dipengaruhi oleh beberapa faktor antara lain: spesies, ketersediaan makanan, umur, jenis kelamin, suhu, lokasi geografis, dan musim (Sampaio et al. 2006). Kandungan kolesterol yang rendah pada daging kerang pisau mengindikasikan bahwa komoditas ini dapat dijadikan sebagai diet yang dapat mencegah penyakit jantung koroner. Menurut The National Heart, Lung and Blood Institute (NHLBI) tahun 2005, kadar kolesterol total yang baik bagi tubuh manusia berada di bawah 200 mg/dl, HDL lebih dari 35 mg/dl, LDL kurang dari 130 mg/dl, dan trigliserida kurang dari 250 mg/dl. Kadar kolesterol di atas 200 mg/dl dapat menimbulkan ancaman berbagai penyakit misalnya aterosklerosis, stroke, dan penyakit jantung koroner.
4.6 Mineral
Analisis mineral perlu dilakukan untuk mengetahui kandungan mineral yang terdapat pada suatu bahan. Adapun kandungan mineral yang terdapat pada kerang pisau dapat dilihat pada Tabel 7.
Tabel 7 Kandungan mineral kerang pisau (Solen spp) (mg/kg bb)
4.6.1 Mineral Makro
Mineral makro adalah unsur mineral yang dibutuhkan dalam jumlah besar, yaitu lebih dari 100 mg sehari (Almatsier 2006). Kelompok mineral makro antara lain: kalsium, fosfor, kalium, magnesium, natrium, kalium. Kandungan mineral tertinggi yang terdapat pada kerang pisau adalah natrium diikuti kalium, fosfor, magnesium dan yang terendah adalah kalsium.
a. Kalsium (Ca)
Hasil penelitian menunjukkan bahwa kerang pisau memiliki kadar kalsium 23,12 mg/kg (bb) pada bagian daging dan 58,24 mg/kg (bb) pada bagian jeroan. Nilai ini lebih rendah jika dibandingkan dengan hasil penelitian kerang pisau sebelumnya (Nurjanah et al. 2008) yang menyatakan bahwa kerang pisau memiliki kadar kalsium sebesar 1336,9 mg/kg (bk), namun kandungan kalsium kerang pisau pada penelitian ini lebih tinggi jika dibandingkan dengan siput air
tawar yang memiliki kandungan kalsium antara 0,176-0,198 mg/kg (Tayo et al. 2011). Hal ini diduga karena dipengaruhi oleh beberapa faktor,
diantaranya jenis, habitat, umur, dan ukuran (Okuzumi dan Fujii 2000). Kalsium yang terdapat pada kerang pisau ini dapat dimanfaatkan sebagai sumber mineral bagi asupan tubuh untuk pencegahan defisiensi kalsium, misalnya osteoporosis.
b. Fosfor (P)
Kadar mineral fosfor pada penelitian ini adalah sebesar 748,37 mg/kg (bb) pada daging dan 1143,78 mg/kg (bb) pada jeroan. Kandungan mineral fosfor pada penelitian ini lebih rendah daripada hasil penelitian kerang pisau sebelumnya (Nurjanah et al. 2008) menyatakan bahwa kadar fosfor kerang pisau adalah sebesar 1744,59 mg/kg (bk). Bila dibandingkan dengan moluska air tawar yang memiliki kadar fosfor antara 0,314-0,369 mg/kg (Tayo et al. 2011), kadar fosfor pada penelitian ini jauh lebih tinggi. Perbedaan jumlah kandungan ini diduga karena perbedaan jenis dan habitat. Mineral fosfor yang terkandung dalam kerang pisau ini cukup tinggi. Fosfor merupakan mineral yang bersinergi dengan magnesium dan kalsium dalam pembentukan tulang dan gigi serta kofaktor dalam produksi berbagai jenis enzim, sehingga dengan mengkonsumsi kerang pisau dapat menambah asupan mineral fosfor yang baik bagi tubuh.
Kadar mineral kalium pada penelitian ini adalah sebesar 1894,28 mg/kg (bb) pada daging dan 2152,72 mg/kg (bb) pada jeroan. Hasil
penelitian sebelumnya menyatakan kadar kalium kerang pisau adalah sebesar 2118,4 mg/kg (bk) (Nurjanah et al. 2008). Kandungan kalium pada penelitian ini juga lebih besar dibandingkan kandungan kalium pada moluska air tawar hasil penelitian Tayo et al. (2011) yaitu berkisar antara 0,362-0,418 mg/kg. Kandungan mineral yang berbeda-beda pada suatu organisme dapat disebabkan oleh habitat dan spesies yang berbeda.
d. Magnesium (Mg)
Hasil penelitian menunjukkan bahwa kerang pisau memiliki kadar magnesium 62,62 mg/kg (bb) pada bagian daging dan 109,96 mg/kg (bb) pada bagian jeroan. Kadar magnesium pada penelitian ini lebih rendah bila dibandingkan dengan kadar magnesium kerang pisau (Nurjanah et al. 2008) yang
menyatakan bahwa kerang pisau memiliki kadar magnesium sebesar 472,46 mg/kg (bk), namun kadar magnesium kerang pisau ini lebih tinggi jika
dibandingkan dengan moluska air tawar misalnya siput air tawar (Tayo et al. 2011) yang memiliki kandungan magnesium antara 0,262-0,297
mg/kg. Perbedaan ini dapat terjadi karena perbedaan habitat yaitu komponen-komponen anorganik di lingkungan perairan tempat kerang berasal dan spesies.
e. Natrium (Na)
glukosa dan juga merupakan elemen esensial dari molekul DNA (Tayo et al. 2011)
4.6.2 Mineral Mikro
Mineral mikro adalah unsur mineral yang dibutuhkan dalam jumlah sedikit yaitu kurang dari 100 mg sehari (Almatsier 2006). Kelompok mineral mikro antara lain: besi, seng, tembaga, selenium, iodium, mangan, seng, kobalt, dan fluor (Nabrzyski 2007). Analisis mineral mikro pada penelitian ini meliputi besi, seng dan selenium, namun dalam analisis selenium tidak ditemukan adanya kandungan mineral selenium baik pada daging maupun jeroan.
a. Besi (Fe)
Besi merupakan mineral mikro yang paling tinggi pada penelitian ini. Kandungan besi dalam penelitian ini adalah sebesar 55,43 mg/kg (bb) pada bagian daging dan 484,02 mg/kg (bb) pada bagian jeroan. Nurjanah et al. (2008)
menyatakan bahwa kandungan besi pada kerang pisau adalah sebesar 41,76 mg/kg (bk). Banyak faktor yang dapat mempengaruhi perbedaan kandungan
besi yakni umur, waktu penangkapan, dan habitat (Carvalho et al. 2005).
Kandungan besi pada jeroan lebih tinggi daripada daging kerang pisau. Hal ini diduga karena besi lebih banyak berfungsi di berbagai reaksi enzim di dalam jaringan tubuh dan sebagai alat angkut elektron di dalam sel sehingga banyak terdapat di organ-organ dalam tubuh organisme. Kandungan besi pada kerang pisau cukup tinggi, dengan demikian konsumsi kerang pisau dapat menambah asupan besi bagi tubuh sehingga dapat terhindar dari penyakit-penyakit yang disebabkan karena defisiensi besi.
b. Seng (Zn)
sumber mineral untuk kebutuhan tubuh guna mencegah defisiensi seng sehingga fungsi normal tubuh dapat terjaga.
c. Selenium (Se)
Mineral selenium pada penelitian ini tidak terdeteksi, namun penelitian sebelumnya menunjukkan bahwa kerang pisau memiliki kadar selenium sebesar 480 µg/kg (bk) (Nurjanah et al. 2008). Perbedaan kandungan selenium pada kerang pisau ini dapat terjadi karena perbedaan habitat tempat kerang pisau berasal. Produk perikanan memiliki kadar selenium berkisar antara 0,3-0,4 mg/kg (Okuzumi dan Fujii 2000). Selenium dibutuhkan dalam jumlah sedikit namun penting bagi tubuh. Selenium adalah mineral mikro yang merupakan bagian essensial dari enzim glutation peroksidase (Almatsier 2006).
4.7 Logam Berat
Sifat umum kekerangan sebagai filter feeder menyebabkan kualitas kerang sangat dipengaruhi oleh kualitas perairan di suatu lingkungan. Kerang yang hidup dalam lumpur dapat memakan sedimen dan menyaring logam-logam berat. Logam-logam berat ini dapat berbahaya jika terakumulasi dalam tubuh. Bivalvia terkenal akan kemampuannya mengakumulasi logam berat dan telah banyak digunakan sebagai bioindikator untuk pengawasan logam berat pada lingkungan perairan (Kanakaraju et al. 2008). Hasil analisis logam berat yang terdapat pada kerang pisau (Solen spp) disajikan pada Tabel 8 berikut.
Tabel 8 Kadar logam berat kerang pisau (Solen spp) (mg/kg)
Logam berat Daging Jeroan SNI 3460.1-2009 (mg/kg)
Pb 0,28 ± 0,35 0,67 ± 0,25 1
Cd Tidak terdeteksi 0,13 ± 0,03 1
Hg 0,02 ± 0,00 0,04 ± 0,00 0,5
4.7.1 Timbal (Pb) rendah daripada jeroan, hal ini diduga karena pada jeroan terdapat organ-organ dalam kerang yang langsung bertanggung jawab dalam penyaringan logam berat maupun akumulasi logam berat. Konsentrasi Pb kemungkinan dihasilkan dari sedimen di daerah sekitar yang telah tercemar.
4.7.2 Kadmium (Cd)
5 KESIMPULAN DAN SARAN
5.1 Kesimpulan
Kerang pisau (Solen spp) yang berasal dari pantai Kejawanan, Cirebon memiliki panjang, lebar, tebal, dan bobot utuh rata-rata sebesar 4,75 cm; 0,83 cm; 0,87 cm, dan 2,27 gram. Rendemen terbesar kerang pisau adalah bagian daging, diikuti cangkang dan jeroan. Komposisi kimia yang terdapat pada daging dan jeroan kerang pisau yaitu yaitu kadar air yang terbesar, diikuti protein, karbohidrat, lemak dan abu.
Kandungan asam lemak pada kerang pisau terdiri atas asam lemak jenuh, asam lemak tak jenuh tunggal, serta asam lemak tak jenuh majemuk. Kandungan asam lemak tidak jenuh majemuk tertinggi daging dan jeroan kerang pisau adalah EPA. Kolesterol yang terkandung dalam jeroan kerang pisau lebih tinggi dibandingkan daging kerang pisau. Kolesterol pada daging kerang pisau yaitu 36,16 mg/100 gram, sedangkan kolesterol pada jeroan kerang pisau sebesar 139,43 mg/100 gram.
Mineral makro yang terkandung dalam daging dan jeroan kerang pisau yaitu kalsium, fosfor, kalium, magnesium, dan natrium. Kandungan mineral makro tertinggi adalah natrium. Mineral mikro yang terkandung dalam kerang pisau antara lain: besi dan seng. Kandungan mineral mikro tertinggi pada kerang pisau adalah besi. Logam berat yang terdeteksi pada kerang pisau hasil penelitian ini adalah Pb dan Hg pada daging dan Pb, Cd, Hg pada jeroan. Kandungan logam berat masih berada di bawah batas aman yang diperbolehkan sehingga dapat dikatakan cukup aman untuk dikonsumsi.
5.2 Saran
5 KESIMPULAN DAN SARAN
5.1 Kesimpulan
Kerang pisau (Solen spp) yang berasal dari pantai Kejawanan, Cirebon memiliki panjang, lebar, tebal, dan bobot utuh rata-rata sebesar 4,75 cm; 0,83 cm; 0,87 cm, dan 2,27 gram. Rendemen terbesar kerang pisau adalah bagian daging, diikuti cangkang dan jeroan. Komposisi kimia yang terdapat pada daging dan jeroan kerang pisau yaitu yaitu kadar air yang terbesar, diikuti protein, karbohidrat, lemak dan abu.
Kandungan asam lemak pada kerang pisau terdiri atas asam lemak jenuh, asam lemak tak jenuh tunggal, serta asam lemak tak jenuh majemuk. Kandungan asam lemak tidak jenuh majemuk tertinggi daging dan jeroan kerang pisau adalah EPA. Kolesterol yang terkandung dalam jeroan kerang pisau lebih tinggi dibandingkan daging kerang pisau. Kolesterol pada daging kerang pisau yaitu 36,16 mg/100 gram, sedangkan kolesterol pada jeroan kerang pisau sebesar 139,43 mg/100 gram.
Mineral makro yang terkandung dalam daging dan jeroan kerang pisau yaitu kalsium, fosfor, kalium, magnesium, dan natrium. Kandungan mineral makro tertinggi adalah natrium. Mineral mikro yang terkandung dalam kerang pisau antara lain: besi dan seng. Kandungan mineral mikro tertinggi pada kerang pisau adalah besi. Logam berat yang terdeteksi pada kerang pisau hasil penelitian ini adalah Pb dan Hg pada daging dan Pb, Cd, Hg pada jeroan. Kandungan logam berat masih berada di bawah batas aman yang diperbolehkan sehingga dapat dikatakan cukup aman untuk dikonsumsi.
5.2 Saran
RIANDA GITA FETRISIA
DEPARTEMEN TEKNOLOGI HASIL PERAIRAN
FAKULTAS PERIKANAN DAN ILMU KELAUTAN
INSTITUT PERTANIAN BOGOR
BOGOR
RIANDA GITA FETRISIA C34070035
SKRIPSI
sebagai salah satu syarat untuk memperoleh gelar Sarjana Perikanan di Departemen Teknologi Hasil Perairan, Fakultas Perikanan dan Ilmu
Kelautan,
Institut Pertanian Bogor
DEPARTEMEN TEKNOLOGI HASIL PERAIRAN
FAKULTAS PERIKANAN DAN ILMU KELAUTAN
INSTITUT PERTANIAN BOGOR
BOGOR
RIANDA GITA FETRISIA. C34070035. Komposisi Kimia Kerang Pisau (Solen spp) dari Pantai Kejawanan, Cirebon, Jawa Barat. Dibimbing oleh
NURJANAH dan AGOES M. JACOEB.
Kerang pisau (Solen spp) merupakan salah satu hasil perairan yang bergizi. Kerang pisau merupakan anggota dari kelompok kekerangan yang hidup pada habitat pasir berlumpur dan memiliki bentuk tipis memanjang seperti pisau. Kerang pisau merupakan makanan yang biasa dikonsumsi oleh masyarakat Indonesia dan diolah menjadi berbagai jenis makanan, namun informasi kandungan nutrisi dari kerang pisau masih sedikit di Indonesia, sehingga perlu dilakukan penelitian kandungan nutrisi yang ada pada kerangpisau.
Penelitian ini bertujuan menentukan komposisi asam lemak, kolesterol, mineral dan logam berat kerang pisau. Pengamatan dilakukan terhadap morfometrik (panjang, lebar, tebal dan berat) kerang pisau (Solen spp), rendemen, komposisi kimia (kadar air, abu, lemak, protein dan karbohidrat secara by difference), asam lemak, kolesterol, mineral dan logam berat.
Kerang pisau pada penelitian ini berasal dari Pantai Kejawanan, Cirebon, Jawa Barat. Rendemen daging, jeroan dan cangkang kerang pisau berturut-turut adalah 41,02%, 23,49%, dan 35,49%. Analisis proksimat daging dan jeroan kerang pisau antara lain masing-masing kadar air sebesar 78,59% dan 75,49%, abu 1,53% dan 2,56%, protein 14,48% dan 15,21%, lemak 1,72% dan 1,95%, dan karbohidrat (dihitung by difference) sebesar 3,68% dan 4,79%.
Kandungan asam lemak (daging dan jeroan) kerang pisau masing-masing terdiri asam lemak jenuh dengan kandungan tertinggi yaitu palmitat (7,305% dan 8,15%), dan stearat (3,975% dan 4,57%). Kandungan asam lemak tidak jenuh tunggal (daging dan jeroan) kerang pisau yang tertinggi terdiri atas palmitoleat (3,475% dan 5,085%), dan oleat (3,72% dan 3,64%). Kandungan asam lemak tidak jenuh majemuk (daging dan jeroan) kerang pisau antara lain: linoleat (0,325% dan 0,42%), linolenat (0,17% dan 0,245%), arakhidonat (2,35% dan 2,665%), EPA (9,61% dan 12,11%), serta DHA (7,275% dan 6,785%).
Dengan ini saya menyatakan bahwa skripsi dengan judul “Komposisi Kimia Kerang Pisau (Solen spp) dari Pantai Kejawanan, Cirebon, Jawa
Barat.” adalah karya saya sendiri dan belum diajukan dalam bentuk apapun kepada Perguruan Tinggi manapun. Sumber informasi yang berasal atau dikutip dari karya yang telah diterbitkan dari penulis lain telah disebutkan dalam teks dan dicantumkan dalam Daftar Pustaka di bagian akhir skripsi ini.
Bogor, Desember 2011