BAB II. SPEKTROSKOPI ULTRAVIOLET DAN TAMPAK
2.1. Tujuan Instruksional Khusus
Setelah mempelajari bab ini mahasiswa mampu : a. menjelaskan terjadinya spektra UV
b. menjelaskan klasifikasi transisi elektronik c. memahami terminologi
d. menghitung λmaks suatu senyawaan
2.2. Serapan oleh Senyawa
Serapan cahaya oleh molekul dalam daerah spektrum ultarviolet dan visible tergantung pada struktur elektronik dari molekul. Spektra ultraviolet dan visible dari senyawa-senyawa organik berkaitan erat dengan transisi-transisi di antara tingkat-tingkat tenaga elektronik. Oleh sebab itu serapan radiasi ultraviolet/visible sering dikenal sebagai spektroskopi elektronik.
Dalam praktiknya, spektrometri ultraviolet digunakan terbatas pada sistem-sistem terkonjugasi, namun terdapat keuntungan selektif dari senyawa ultraviolet bahwa gugus-gugus karakteristik dapat dikenal dalam molekul-molekul yang sangat kompleks.
2.3. Terminologi
Sebelum menjelaskan transisi serapan elektronik, maka dipahami beberapa pengertian yang sering digunakan dalam pembicaraan spektra elektronik, yaitu:
a. Kromofor
Kromofor merupakan gugus tidak jenuh kovalen yang dapat menyerap radiasi dalam daerah-daerah ultraviolet dan tampak. Contoh C=C, C=O, dan NO2.
b. Auksokrom
Auksokrom merupakan gugus jenuh yang terikat pada kromofor yang dapat mengubah panjang gelombang dan intensitasnya. Ciri auksokrom adalah heteroatom, contoh: -OCH3, -Cl, -OH, dan –NH2. c. Pergeseran Batokromik
Pergeseran serapan ke arah panjang gelombang yang lebih panjang disebabkan substitusi atau pengaruh pelarut (pergeseran merah). d. Pergeseran Hipsokromik
e. Efek Hiperkromik, kenaikan dalam intensitas serapan. f. Efek hipokromik, penurunan dalam intensitas serapan
2.4. Klasifikasi Transisi
Karena elektron dalam molekul memiliki energi yang tak sama, maka energi yang diserap dalam proses eksitasi dapat mengakibatkan terjadinya satu atau lebih transisi tergantung dari jenis elektron yang terlibat. Transisi-transisi tersebut diklasifikasikan sebagai berikut:
a. Transisi π → σ * → ionisasi
Transisi ini sedikit dipelajari oleh orang-orang organik sebab terjadi dalam ultraviloet jauh, yaitu 180 nm. Daerah ini dikenal sebagai daerah Schuman atau ultraviolet vakum (10-200 nm).
b. Transisi π → π *
Transisi ini paling berguna dan merupakan serapan-serapan karakteristik dari senyawa-senyawa organik dan biasanya dihubungkan dengan tingkat tereksitasi polar. Dalam sistem-sistem yang sederhana transisi ini terjadi dalam ultraviolet jauh. Transisi π →π* ini menunjukkan pergeseran merah dengan adanya substitusi gugus-gugus yang memberi atau menarik elektron dan dengan kenaikan dalam tetapn dielektrik dari pelarut. Dalam kedua keadaan ini menstabilkan tingkat tereksitasi polar.
c. Transisi n → π*
Transisi ini meliputi transisi elektron-elektron heteroatom tak berikatan ke orbital anti ikatan π*. Serapan ini terjadi pada panjang gelombang yang panjang dan intensitasnya rendah. Transisi n →π* menunjukkan pergeseran hipsokromik (biru) dalam pelarut-pelarut yang lebih polar dan substituen-substituen yang bersifat pemberi elektron.
d. Transisi n → σ *
Transisi jenis ini tidak menunjukkan serapan dalam daerah ultraviolet dekat.
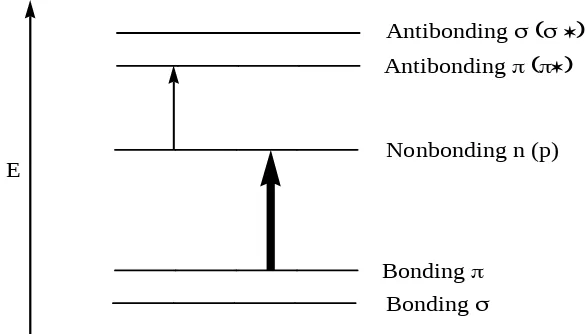
Antibonding Antibonding
Nonbonding n (p)
[image:3.612.173.466.88.255.2]Bonding Bonding E
Gambar 1.1. Macam-Macam Transisi Elektronik
2.5. Kekhasan Serapan dari Senyawa Organik
a. Senyawa yang Hanya Mengandung Elektron σ
Serapan pada hidrokarbon jenuh yang hanya mengandung elektron σ terjadi pada ultraviolet jauh, sehingga dapat digunakan sebagai pelarut.
b. Senyawa Jenuh Mengandung Elektron n
Senyawa jenuh mengandung heteroatom, seperti oksigen, nitrogen, sulfur, atau halogen memiliki memiliki elektron tidak terikat (elektron n atau p) biasanya tidak memiliki serapan pada daerah ultra ungu dekat, sehingga dapat digunakan sebagai pelarut.
c. Senyawa Mengandung Elektron π
Kekhasan serapan dari senyawa yang mengandung elektron π akan dibahas secara jelas sebab serapan ini umumnya terjadi pada daerah ultraviolet. Banyak senyawa yang menunjukkan keteraturan dalam spektra serapannya, sehingga cukup dapat digunakan secara tepat untuk menghitung kedudukan serapan maksimum dari senyawa-senyawa bersangkutan. Perhitungan-perhitungan seperti ini dapat berguna untuk menentukan struktur.
2.6. Perhitungan λmaks
Penentuan rumus empiris dalam menghitung λmax telah ditemukan oleh Woodward-Fieser. Tiga jenis sistem yang akan diketengahkan sebagai berikut:
Diena yang terdapat dalam sistem cincin yang tidak bergabung disebut dengan istilah heteroanular. Aturan dari serapan senyawa jenis ini tersaji dalam Tabel 2.1.
Heteroanular
b. Diena atau poliena dalam sistem cincin yang bergabung
Diena dalam sistem yang bergabung disebut dengan istilah homoanular. Aturan dari serapan jenis ini tersaji dalam Tabel 2.1.
[image:4.612.142.499.458.855.2]Homoanular
Tabel 2.1. Aturan dari Serapan Diena
Contoh :
nm
Harga dasar untuk diena nonsiklik 214
Harga dasar untuk diena heteroanular 214
Harga dasar untuk diena homoanular 214
Pertambahan untuk: Sistem diena homoanular 39
Setiap substituen alkil atau residu lingkar 5
Ikatan rangkap eksosiklik 5
Perpanjangan dengan satu ikatan rangkap 30
Auksokrom: - O-Asil 0
- O-Alkil 6
- S-Alkil 30
- Cl atau –Br 5
- N-(alkil)2 60
kholesta-1,4-diena
1 2
3
λmax 214 (dasar diena heteroanular) 15 (sisa 3 cincin, 1, 2, dan 3)) 5 (1 eksosiklik C=C)
234 nm
c. Enon dan dienon yang terkonjugasi
Woodward telah menurunkan perumusan empiris secara umum terhadap pengaruh substitusi dalam keton-keton α, β- tidak jenuh. Kedudukan jalur serapan yang dihasilkan substitusi dari rumus dasar:
R C
O
C
C
[image:5.612.139.527.575.717.2]Aturan serapannya tersaji pada Tabel 2.2.
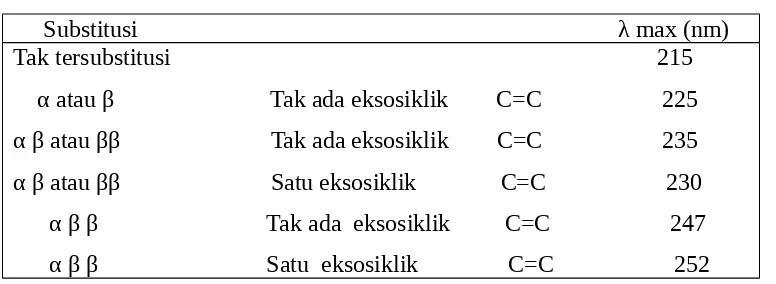
Tabel 2.2. Serapan Maksimum dari Keton Tidak Jenuh –α, β
Substitusi λ max (nm)
Tak tersubstitusi 215
α atau β Tak ada eksosiklik C=C 225
α β atau ββ Tak ada eksosiklik C=C 235
α β atau ββ Satu eksosiklik C=C 230
α β β Tak ada eksosiklik C=C 247
α β β Satu eksosiklik C=C 252
Aturan yang serupa digunakan untuk sistem siklopentanon.
O
* Harga 214 nm dapat dihitung dari:
Harga dasar untuk bentuk enon siklik anggota 5 202 nm Substituen –β 12 nm 214 nm
[image:6.612.135.527.601.906.2]Perumusan lebih terperinci dari serapan enon telah diringkas oleh Fieser dan tersaji pada Tabel 2.3.
Tabel 2.3. Aturan Serapan dienon dan enon (Karbonil Tak Jenuh –α, β dari Keton)
C C C O
dan C C C C O
C
Enon Dienon
Harga Dasar:
nm
Keton asiklik α, β 215
Keton siklik tidak jenuh α, β beranggota 6 215
Keton siklik tidak jenuh α, β beranggota 5 202
Aldehida tidak jenuh α, β 210
Asam karboksilat dan ester tidak jenuh α, β 195
Pertambahan untuk: Ikatan rangkap konjugasi terentang 30
Gugus alkil, sisa cincin α 10
Gugus alkil, sisa cincin β 12
Gugus polar: -OH α 35
β 30
δ 50
-OAc α, β, γ 6
-OMe α 35
β 30
γ 17
δ 31
-OAlk β 85
-Cl α 15
β 12
-Cl α 25
β 30
-NR2 β 95
Ikatan rangkap eksosiklik 5
Bagian homodiena 39 Pembetulan pelarut bervariasi
Contoh:
C
CH3
O
1-asetilsikloheksena
λmax 215 (dasar) 10 (sisipan α) 12 (sisipan β)
237 nm
O
1
2
3 4
5
`
kholesta-1,4-dien-3-on