HUBUNGAN KADAR SERUM LAMI NI N DENGAN
KEPARAHAN SI ROSI S HATI
PENELITIAN POTONG LINTANG DI BAGIAN / SMF ILMU PENYAKIT DALAM
FAKULTAS KEDOKTERAN USU / RSUP H. ADAM MALIK MEDAN
JANUARI 2008 – JUNI 2008
TESI S
OLEH
I MAN RANDAL TARI GAN
PEMBI MBI NG
Dr. MABEL SI HOMBI NG, Sp.PD, KGEH
BAGI AN I LMU PENYAKI T DALAM FAKULTAS KEDOKTERAN
UNI VERSI TAS SUMATERA UTARA
DI AJUKAN DAN DI PERTAHANKAN DI DEPAN
SI DANG LENGKAP DEWAN PENI LAI
DEPARTEMEN I LMU PENYAKI T DALAM
FAKULTAS KEDOKTERAN USU DAN DI TERI MA SEBAGAI SALAH
SATU SYARAT UNTUK MENDAPATKAN KEAHLI AN DALAM BI DANG
PENYAKI T DALAM
Pembimbing Tesis
( Dr. Mabel Sihombing, SpPD- KGEH)
Disahkan Oleh
Kepala Departemen
Ketua Program Studi
DEWAN PENI LAI
1.
Prof. Dr. Sutomo Kasiman, SpPD-SpJP(K)
2.
Dr. Sri Maryuni Sutadi, SpPD-KGEH
3.
Dr. Abdurrahim Rasyid Lubis, SpPD-KGH
4.
Dr. Zulhelmi Bustami, SpPD-KGH
5.
Dr. Dharma Lindarto, SpPD-KEMD
DAFTAR RI WAYAT HI DUP
DATA PRI BADI
Nama : dr. Iman Randal Tarigan
Tempat/Tanggal Lahir : Medan, 24 Oktober 1970
Alamat : Komp. Grand Kasuari Blok B1 No. 10 Medan
RI WAYAT PENDI DI KAN
SD Perguruan Kristen Methodist 1 – Medan : Ijasah tahun 1980
SMP Perguruan Kristen Methodist 1 - Medan : Ijasah tahun 1986
SMA Negeri 4 – Medan : Ijasah tahun 1989
Fakultas Kedokteran Univ. Sumatera Utara – Medan : Ijasah tahun 1997
RI WAYAT PEKERJAAN
1. Dokter PTT di Puskesmas Durian Luncuk Kabupaten Muara Bulian Jambi 1994-1997
2. Mengikuti Pendidikan Keahlian dalam bidang Ilmu Penyakit Dalam FKUSU/RS Dr.
Pirngadi/RS. H. Adam Malik sejak 1 Januari 2002.
KEANGGOTAAN
1. Ikatan Dokter Indonesia (IDI)
KARYA I LMI AH
1. Iman, OK Alfiyen Sjukran, Comparison Small Dense LDL, KOPAPDI. Palembang, 6-9 Juli
2006
2. Iman, Gontar A Siregar, Portal Hypertension Extra Hepatic, KONAS XI PGI, PEGI, PIN XII
PPHI. Batu Malang, 5-7 Juli 2003
PARTI SI PASI DALAM KEGI ATAN I LMI AH
1. Peserta Simposium Pertemuan Ilmiah Tahunan ke III Bagian Ilu Penyakit Dalam. Medan 20
April 2002
2. Peserta Simposium Advance Dyspepsia in general Practice. Medan, 18 May 2002.
3. Peserta Launching Symposium “The Most Potent Antihistamine”. Perhimpunan Alergi
Imunologi Cabang Medan. Medan, 8 Februari 2003.
4. Peserta Simposium Pertemuan Ilmiah Tahunan IV. ”Peningkatan Profesionalisme
Menyambut Era Globalisasi.” Medan, 6-8 Februari 2003.
5. Peserta COXIB Symposium. Re-shaping the treatment paradigm : A COXIB Snapshot.
Medan, 5 April 2003.
6. Peserta Annual Meeting 2003 – Indonesian Society of Nephrology. Palembang, 2-5 Oktober
2003.
7. Peserta Simposium Gastroenteroheptologi update 2003. Medan, 18-19 Oktober 2003.
8. Peserta Simposium The 2nd New Trend in Cardiovascular Management. Medan, 5-6
Desember 2003.
9. Peserta Pertemuan Ilmiah Tahunan V 2004 bagian Ilmu Penyakit Dalam Fakultas
10.Peserta Simposium Putting The Patients First : A New Paradigm in Treatment of Erectile
Dysfunction. Medan, 14 Maret 2004.
11.Peserta Simposium Pathophysiology and Clinical Management of Pain. Medan, 18 Maret
2004.
12.Peserta simposium Psikosomatik dan Gangguan Jantung.Medan, 17 April 2004.
13.Peserta seminar TB 2004 dalam rangka memperingati hari TB sedunia 2004. Medan, 24-25
April 2004.
14.Peserta SAFARI PERALMUNI 2004. Medan, 24 April 2004.
15.Peserta Launching Symposium New Dimension in Management of Hypertension and
Metabolic Syndrome. Medan 15 Mei 2004.
16.Peserta Pendidikan Keterampilan Ultrasonografi Dasar, Unit Pengembangan llmiah
dan Pengabdian Masyarakat ( UPM ) FK USU. Medan, 7-19 Juni 2004.
17.Peserta Symposium Mild Cognitive Impairment Practical Guideline and Treatment
Strategies. Medan, 26 Juni 2004.
18.Peserta Simposium NSAID Gastropathy. Medan, 03 Juli 2004.
19.Peserta simposium Lantus, Upaya mencapai kontrol glikemik optimal pada pasien DM tipe
2. Medan, 10 Juli 2004.
20.Peserta Simposium Infections UpDate 2004. "Strategi Pengendalian Infeksi Menuju
Indonesia Sehat 2010. Medan, 24 Juli 2004.
21.Peserta Safari Nasional PERALMUNI II 2005. Medan, 30 Juli 2004.
22.Peserta dan Pembicara pada Kongres Nasional PETRI X - PERPARI VI- PIT VI PAPDI
25.Peserta simposium Pertemuan Ilmiah Tahunan ke V Imu Penyakit Dalam. Medan 2004.
26.Peserta Pertemuan Ilmiah Tahunan VI Bagian Ilmu Penyakit Dalam FK USU. Medan 3 - 5
Maret 2005.
27.Peserta Simposium The 3rd New Trend Cardiovascular Management. Medan 6 Juni 2005.
28.Peserta Workshop USG. Gastroentero-Hepatologi Update III, Medan 5 Agustus 2005.
29.Peserta 15th Annual Scientific Meeting of The Indonesian Heart Association. Medan, 19-22
KATA PENGANTAR
Puji dan syukur saya ucapkan ke hadirat Tuhan Yang Maha Kuasa yang telah
memberikan berkatNya, sehingga saya dapat menyelesaikan tesis ini dengan judul:
HUBUNGAN KADAR SERUM LAMININ DENGAN KEPARAHAN SIROSIS HATI yang
merupakan persyaratan dalam menyelesaikan pendidikan dokter ahli di bidang Ilmu Penyakit
Dalam pada Fakultas Kedokteran Universitas Sumatera Utara Medan.
Dengan selesainya karya tulis ini maka penulis ingin menyampaikan
terimakasih, hormat serta penghargaan yang setinggi-tingginya kepada:
1. Dr.Salli Roseffi Nasution, SpPD-KGH, selaku Kepala Departemen Ilmu Penyakit Dalam
FK-USU/ RS H.Adam Malik Medan yang telah memberikan kemudahan dan perhatian
yang besar terhadap pendidikan penulis.
2. Dr.Zulhelmi Bustami, SpPD-KGH dan Dr. Dharma Lindarto sebagai Ketua dan
Sekretaris Program Pendidikan Dokter Spesialis Ilmu Penyakit Dalam yang membina
penulis menjadi ahli penyakit dalam yang berilmu dan berbudi luhur.
3. Seluruh staf Depertemen / SMF Ilmu Penyakit Dalam FK USU / RSUD Dr.Pirngadi
Medan; Prof.Harun Rasyid Lubis, Prof Bachtiar Fanani Lubis, Prof Habibah Hanum
Nasution, Prof Pengarapen Tarigan, Prof OK Moehadsjah, Prof Lukman Hakim Zain,
Prof Sutomo Kasiman, Prof Azhar Tanjung, Prof M Yusuf Nasution, Prof Azmi S Kar,
Prof Gonthar A Siregar, Dr Nur Aisjah, Dr A Adin St Bagindo, Dr Sjafii Piliang, Dr Lufti
Latief, Dr Abdurrahim Lubis, Dr Betthin Marpaung, Dr Abiran Nababan, Dr Sri Sutadi, Dr
Sugiarto Gani, Dr Santi Syafril dan Dr Savita Handayani yang merupakan guru saya dan
telah banyak memberikan bimbingan dan petunjuk kepada saya selama mengikuti
pendidikan.
4. Terimakasih juga kepada para guru yang berjasa dalam mendidik saya, Prof Kariman S,
Dr Rusli Pelly (alm), Dr Chairul Bachri (alm) serta Dr OK Alfien Sjukran (alm).
5. Para Dokter Kepala Ruangan: dr Zulhelmi Bustami, Dr A Rahim Lubis, Dr Armon
Rahimi, Dr R Tunggul Ch, Dr Tambar Kembaren, Dr Calvin Damanik, Dr Zuhrial, Dr
Mardianto, Dr Maringan Lumban Gaol, Dr Saut Marpaung, Dr Daud Ginting, Dr Blondina
Marpaung, Dr Dasril, Dr Hariyani Adin, Dr Jerahim Tarigan, Dr Ilhamd. Dr Dairion Gatot,
Dr Sugiarto Gani, Dr Santi Syafril dan Dr Savita Handayani yang telah membimbing
saya selama mengikuti pendidikan.
6. Direktur RSUP H Adam Malik Medan/ RSUD Dr Pirngadi Medan yang telah memberikan
bantuan dan kemudahan serta keizinan dalam menggunakan fasilitas dan sarana
rumah sakit dalam menunjang pendidikan keahlian.
7. Manajer RSU Tarutung yang telah memberikan kesempatan kepada saya selama
ditugaskan sebagai konsultan Ilmu Penyakit Dalam dalam rangka pendidikan ini.
8. Para sejawat peserta PPDS-I Ilmu Penyakit Dalam, perawat, paramedis dan seluruh
karyawan/karyawati di lingkungan SMF / Departemen Ilmu Penyakit Dalam RSUD Dr
Pirngadi Medan /RSUP H.Adam Malik Medan atas kerjasama yang baik selama ini.
9. Para pasien rawat inap dan rawat jalan di SMF / Departemen Ilmu Penyakit Dalam
RSUD Dr Pirngadi Medan / RSUP H Adam Malik Medan, yang tanpa kehadirannya tidak
mungkin penulis dapat menyelesaikan pendidikan ini.
10. Saya mengucapkan terimakasih kepada Rektor Universitas Sumatera Utara dan Dekan
Fakultas Kedokteran Universitas Sumatera Utara yang menerima saya sehingga dapat
11. Laboratorium Prodia Wilayah Sumatera Utara dan Laboratorium Prodia Pusat Jakarta
atas kerjasamanya dalam pengerjaan pemeriksaan laboratorium terhadap sampel
dalam penelitian ini.
12. Khusus mengenai karya tulis ini, penulis mengucapkan terimakasih yang
sebesar-besarnya kepada Dr. Mabel Sihombing, SpPD-KGEH sebagai Pembimbing Penelitian,
atas segala bimbingan bagi penulis selama melaksanakan penelitian hingga selesainya
karya tulis ini.
13. Drs Abd Jalil Amri Amru, MKes yang telah membimbing dalam analisa data statistik
penelitian ini hingga selesai.
Kepada kedua orangtua saya, ayahanda Prof. Pengarapen Tarigan, SpPD,
KGEH yang semangat dan ketabahannya menjadi inspirasi bagi saya, saya berterimakasih dan
akan tetap mengingat ketauladanan beliau. Bagi ibunda R br Ginting yang telah membesarkan
dan senantiasa mendoakan, saya mengucapkan rasa terima kasih yang dalam, kiranya Tuhan
Yang Maha Kuasa senantiasa memberkati.
Kepada istriku tercinta Puri Fitria Kurniati Munthe, SE, MARS, terimakasih atas
segenap kesabaran, pengertian dan dukungannya selama saya menjalani pendidikan ini.
Demikian juga terima kasih untuk putra dan putri saya, Felix Ekarandi Amadeus Tarigan dan
Fidya Dwifina Aurelia Tarigan, yang selalu menjadi pendorong dan penambah semangat serta
pelipur dikala senang dan susah. Terima kasih banyak untuk cinta kalian kepada Papa, dan
Kepada segenap pihak yang telah menolong saya secara langsung dan tidak
langsung, namun tidak mungkin saya sebutkan namanya satu persatu, izinkanlah saya
menghaturkan rasa terimakasih secara menyeluruh.
Medan, Juni 2008
Penulis,
Abstrak
HUBUNGAN KADAR SERUM LAMI NI N DENGAN KEPARAHAN PENYAKI T HATI
Iman Randal Tarigan*, Mabel Sihombing**
Divisi Gastroenterohepatologi Departemen Ilmu Penyakit Dalam FK USU / RSUP H.Adam Malik
Latar Belakang:
Patogenesis fibrosis hati merupakan proses yang sangat kompleks melibatkan hepatic stellate cells (HSC) sebagai sel utama, sel Kupffer, lekosit, bermacam-macam mediator, sitokin, growth factors dan inhibitornya serta berbagai jenis kolagen. Beberapa cara yang digunakan untuk melihat alternative lain dalam menentukan derajat fibrosis hati dengan memeriksakan laminin (LN) serum. Penelitian sebelumnya belumlah menggambarkan keseragaman nilai LN dalam menentukan derajat kerusakan hati.
Tujuan:
Untuk mengetahui peningkatan kadar serum LN pada penderita SH dan untuk membuktikan bahwa peningkatan kadar serum laminin berbanding lurus dengan peningkatan derajat keparahan SH.
Bahan dan Cara:
Penelitian dilakukan secara studi potong lintang dengan pendekatan deskriptif analitik, mulai Januari 2008 - Juni 2008, dan mengikutsertakan pasien laki-laki dan perempuan penderita SH rawat jalan poliklinik dan rawat inap di Divisi Gastroenterohepatologi Departemen Penyakit Dalam RS.H. Adam Malik Medan serta pasien praktek Spesialis Penyakit Dalam-Konsultan Gastroenterohepatologi di Medan. Diagnosis ditegakkan dengan anamnesis, pemeriksaan fisik, USG dan pemeriksaan laboratorium .
Hasil:
Produksi LN terutama di hati dan kadarnya berbanding lurus dengan derajat keparahan hati. Pada penelitian ini didapati kelompok pasien CTP A kadar LN serum 718,30 + 282,22 ng/ml, CTP B kadar LN serum 1241 + 173,80 ng/ml sedangkan pada CTP C kadar LN serum 1732,82 + 411,34 ng/ml. Ada perbedaan yang bermakna antara kadar LN serum pada penderita sirosis hati CTP A dengan CTP B (p=0,0001), B dengan C (p=0,0001) dan juga CTP A dengan C (p=0,0001). Korelasi positif dijumpai antara CTP dengan kadar serum LN. Hubungan ini diperkuat dengan analisa regresi yang menunjukkan kuat hubungan antara CTP dengan kadar serum LN sebesar 65,3%.
Kesimpulan:
Kadar LN dalam serum berbanding lurus dengan beratnya derajat kerusakan hati pada penderita SH dan kadar LN penderita SH lebih tinggi dibanding orang sehat.
Kata Kunci:
fibrosis hati, LN, CTP
* PPDS Ilmu Penyakit Dalam Fakultas Kedokteran Universitas Sumatera Utara / RSUP H. Adam Malik Medan-Indonesia
** Divisi Gastroenterohepatologi Departemen Ilmu Penyakit Dalam Fakultas Kedokteran
Abstract
RELATI ON RATE of SERUM LAMI NI N WI TH CHRONI C LI VER DI SEASE
Iman Randal Tarigan*, Mabel Sihombing**
Gastroenterohepatology Division Departement of Internal Medicine
Faculty of Medicine University of Sumatera Utara/ H.Adam Malik General Hospital
Background:
Patogenesis of liver fibrosis represent the very complex process entangle the hepatic stellate cells (HSC) as primary cell, cell Kupffer, leucocyt, all kinds of mediator, sitokin, growth factors and the inhibitor and also various collagen type. Some other ways used to see the alternative of other in determining degree of fibrosis liver by check the laminin (LN) Serum. Previous research not depicted yet the similiarity assess the LN in determining degree of liver damage.
Aim:
To know the increasing rate of LN serum at liver disease patient and to prove that increasing rate of laminin serum compare diametrical with the increasing of chronic at liver disease.
Material and Method:
This cross sectional study, in the period of Januari 2008 until June 2008, including inpatients and outpatients, male and female gender, chirosis patients admitted to Division of Gastroenterohepatology- Departement of Internal Medicine/ H Adam Malik General Hospital –Medan, and private clinic of the Gastroenterohepatology consultant in Medan. Diagnosis was made by history, physical examination, laboratory examination and USG.
Result:
The production of LN in liver and its compare diametrical with the chronic of liver disease. This research discovered by the group of patient of CTP A of rate of LN serum 718,30 + 282,22 ng / ml, CTP B of rate of LN serum 1241 + 173,80 ng / ml while CTP C of rate of LN serum 1732,82 + 411,34 ng / ml. There had difference between rate of LN serum at patient of cirrhosis liver of CTP A by CTP B ( p=0,0001), B by C ( p=0,0001) as well as CTP A by C ( p=0,0001). Positive correlation shown between CTP with the rate of LN serum. This Relation is strenghtened with the regretin analysis that showing strength relation between CTP with the rate of serum LN of equal to 65,3%.
Conclusion:
The rate of LN in serum, compare diametrical with weighting degree of liver damage at liver disease patients and the rate of LN in liver disease patients compare with the healthy people.
Keyword
Liver fibrosis, LN, CTP
* Internal Medicine Resident, Faculty of Medicine University of Sumatera Utara / H. Adam Malik General Hospital Medan -Indonesia
BAB I
PENDAHULUAN
Pada penyakit hati kronis, dijumpai fibrosis yang disebabkan oleh penumpukan dari
protein matriks ekstraseluler (MES) yang berlebihan dimana fibrosis hati diawali karena adanya
cedera hati kronis yang disebabkan oleh infeksi virus, ketergantungan alkohol, nonalkoholik
steatohepatitis (NASH) dan penyebab lainnya. Penumpukan MES yang berlebihan akan
mengakibatkan gangguan arsitektur hati, dimana pembentukan jaringan ikat akan diikuti
regenerasi dari sel hepatosit. Fibrosis hati merupakan proses yang pasif dan bersifat reversibel
yang disebabkan oleh kolapsnya parenkim hati yang digantikan oleh jaringan ikat. Pada awal
tahun 70an keadaan reversibel ini diduga hanya terjadi pada fibrosis tahap awal, akan tetapi
banyak penelitian pada tahun 90an mendapatkan bahwa pada fibrosis lanjut juga masih
terdapat keadaan yang reversibel.1
Menentukan derajat fibrosis hati melalui pemeriksaan invasiv dan non invasiv. Pemeriksaan
biopsi hati adalah baku emas dalam hal menentukan derajat fibrosis hati, namun mempunyai
beberapa kelemahan, antara lain : 2
1. mortalitas (0,13- 0,33%).
2. menimbulkan rasa nyeri (30%).
3. komplikasi perdarahan non- fatal (0,35-0,5%).
4. tidak semua penderita setuju untuk dilakukan biopsi.
5. memerlukan keahlian khusus.
7. perbedaan tempat pengambilan sampel (lobus kanan / kiri) didapati tingkat kesulitan
lebih tinggi pada lobus kiri.
Di antara beberapa cara yang digunakan untuk melihat alternatif lain dalam
menentukan derajat fibrosis hati digunakan metode yang sederhana dengan memeriksa kadar
Laminin (LN) dalam serum yang merupakan bahan matriks ekstraseluler yang memiliki
korelasi dengan derajat fibrosis walaupun banyak peneliti lain menggabungkannya dengan
komponen bahan pembentukan matriks ekstraseluler lainnya seperti kolagen, fibronektin,
undulin, elastin dan proteoglikans serta hialin.3
Laminin merupakan salah satu pertanda terjadinya fibrosis hati, sehingga dapat
digunakan sebagai pengganti biopsi hati untuk melihat derajat kerusakan hati dan monitoring
perkembangan keparahan hati.
Penelitian tentang LN sehubungan dengan penyakit hati sebelumnya tidaklah banyak
dan tidak menggambarkan keseragaman nilai LN dalam menentukan derajat kerusakan hati,
antara lain:
Collazos dkk mendapatkan peningkatan kadar LN sebesar 62,7% pada penderita Sirosis
Hati (SH) dibandingkan dengan kontrol dan semakin berat keparahan SH (berdasarkan Kriteria
Child-Turcotte-Pugh (CTP)) maka kadar LN akan semakin meningkat.4
Burchardt dkk (2005) mendapatkan bahwa kadar LN meningkat sesuai dengan derajat
fibrosis pada penderita Hepatitis C kronis.5
Cai WM (1995) mendapatkan kadar LN memiliki sensitivitas dan spesifitas yang lebih
rendah dibanding kombinasi pemeriksaan kadar plateletderived growth factor-BB (PDGF-BB) .6
Panomarenko dkk (2002) melaporkan bahwa nilai LN pada orang sehat 15,5 ± 0,52
ng/ml dan pada peminum alkohol dengan fibrosis hati terjadi peningkatan menjadi 47,34
Tao J dkk (2003) melaporkan dari 141 penderita hepatitis kronis yang diperiksa kadar
hyaluronic acid (HA), type III pro-colagen (PCIII), LN dan type IV collagen (C-IV) ternyata
14,16% indeks serum fibrosis hati tidak berhubungan dengan derajat fibrosis hati (berdasar
biopsi) .8
Yong Peng C dkk (2004) mendapatkan bahwa kadar serum LN tidak berhubungan
dengan derajat keparahan penyakit hati atau derajat fibrosis pada penderita hepatitis B kronis
.9
Sedangkan penelitian tentang hal ini dapat dilakukan dengan sederhana dan mungkin
menggambarkan derajat fibrosis hati dan juga dapat digunakan dalam monitoring perjalanan
keparahan SH apapun sebagai penyebabnya.3,10,11 Oleh sebab itu peneliti ingin melihat
BAB I I
TI NJAUAN PUSTAKA
2.1. LAMI NI N ( LN)
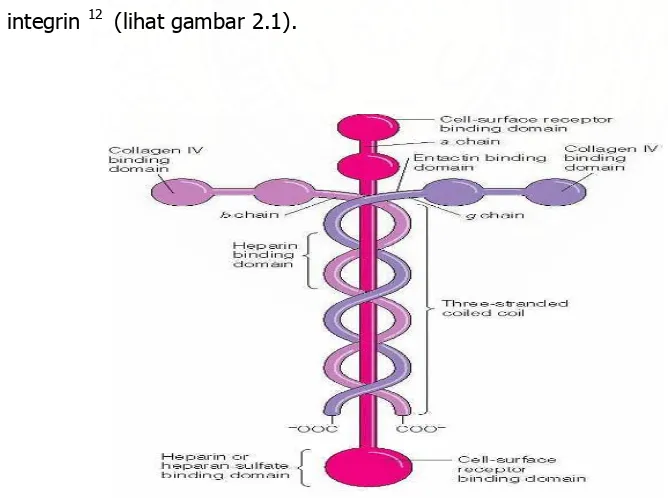
Laminin adalah suatu kompleks glikoprotein ekstrasel dengan berat molekul ± 900 kD.
Peranannya sangat penting pada berbagai aspek biologi sel. Laminin terdiri dari satu rantai A
(400kD), satu rantai B1 (215kD) dan satu rantai B2 (205 kD) kesemuanya diikat dengan ikatan
disulfida.12 Laminin hanya ditemukan dalam jumlah yang bermakna di dalam membran sel;
merupakan matriks ekstrasel tipis yang menyelubungi jaringan epitel, saraf, sel lemak, otot
polos, lurik dan jantung. Laminin tidak hanya penting secara struktural di dalam membran
basalis, tetapi juga memiliki efek pada aktifitas selular yaitu adhesi sel, migrasi sel, dan
diferensiasi sel. Laminin juga memperantarai interaksi matriks sel melaui ikatan dengan
reseptor integrin 12 (lihat gambar 2.1).
LN serum dapat meningkat selama peradagangn cairan sendi seperti reumatik artritis
(RA) disebabkan oleh peningkatkan produksi sendi. Faktor radang yang dapat larut (IL-1, TNF
) akan meningkatkan produksi LN pada sinoval. Pada pasien RA peninggian LN serum dapat
memperlihatkan korelasi dengan keterlibatan sinovial dengan aktivitas penyakit. LN juga
meningkat pada beberapa pasien dengan OA derajat sedang, sklaerosis sistemik yang
progressif atau skeleroferma dan SLE, yang ditandai oleh aktivitas growth faktor dalam jaringan
penyambung dan inflamasi dari sinovial.
Peningkatan LN serum dijumpai pada fibrosis hati dan sirosis sebagai suatu hasil
penurunan penghancuran oleh hati atau peningkatan produksi hepatik selama peradangan hati.
Telah diusulkan bahwa penentuan tingkatan LN serum mungkin berguna dalam perbedaan
bentuk penyakit hati yang kronik dan akut, untuk peningkatan derajat dari fibrosis hati, dan
memonitor fungsi hati pada pasien hepatitis kronbik, sirosis alkoholik, dan primary billiary
sirosis.
Peneliti sebelumnya mendapatkan bahwa kadar serum LN meningkat pada penyakit hati
kronik dan prognosis penyakit tergantung pada beratnya firbosis yang mengakibatkan
terjadinya SH dan kerusakan hati. Walaupun untuk memastikannya dibutuhkan tindakan biopsi
meskipun cara ini juga memiliki tingkat kesulitan seperti yang diterangkan terlebih dahulu di
depan.
Kemungkinan penyebab peningkatan level LN dalam serum atau plasma
1) Peningkatan produksi dari LN
- Inflamasi pada kestrahepatik termasuk seperti sinovium reumatoid
- Penurunan aktivitas sel epitelial sinusoid hepatik (SEC) yang disebabkan oleh fibrosis
atau sirosis.
4) Kombinasi dari faktor : peningkatan produksi, dengan penurunan bersihan
2.1.1. Prinsip dari penilaian LN 12
Pemeriksaan untuk mengukur kadar serum LN adalah dengan menggunakan tekhnik
ELISA. Dengan menggunakan kit dari QuantiMatrix dapat mengukur kadar LN serum pada
tingkat kepekaan 30-70ng, dimana antibodi poliklonal yang terbentuk berikatan dengan LN
yang terdapat pada standard dan sampel dan akan menimbulkan reaksi perubahan warna
menjadi biru, kemudian diteteskan suatu asam untuk menghentikan reaksi dan akan
menimbulkan perubahan warna menjadi kuning; intensitas warna yang terbentuk diukur
dengan ELISA reader
2.2. SI ROSI S HATI
2.2.1. Defenisi
Sirosis hati adalah penyakit hati menahun yang ditandai dengan proses peradangan, nekrosis
sel hati, usaha regenerasi dan penambahan jaringan ikat difus dengan terbentuknya
nodul-nodul yang menganggu susunan lobulus hati.14
2.2.2. I nsidensi
Kejadian sirosis hati di Indonesia banyak berhubungan dengan virus hepatitis B dan C, hal ini
dibuktikan dengan ditemukannya HbsAg positif pada 30-40% pasien sirosis hati dan anti HbC
poistif pda 10-20% pasien sirosis hati. Di Indonesia insidensi sirosis hati belum tercatat secara
nasional, namun Tarigan (Medan) mendapatkan dari 19914 pasien yang dirawat di Bagian
(72.7%). Umumnya di rumah sakit yang besar hanya menunjukkan penderita pria lebih banyak
daripada wanita dengan perbandingan 2:1, usia terbanyak 30-50 tahun.15
2.2.3. Fibrosis pada Sirosis Hati
Fibrosis hati adalah terbentuknya jaringan ikat yang terjadi sebagai respons terhadap
cedera hati kronis tanpa memandang penyebabnya dan bilamana terjadinya fibrosis ini berjalan
secara progresif akan dapat menimbulkan terjadinya SH.
Infeksi virus hepatitis B dan C menimbulkan peradangan sel hati. Peradagangan ini
menyebabkan nekrosis yang meliputi daerah yang luas, terjadi kolaps lobulus hati dan ini
memacu timbulnya jaringan kolagen. Tingkat awal yang terjadi adalah septa yang pasif yang
dibentuk jaringan retikulum penyangga yang mengalami kolaps dan kemudian berubah bentuk
menjadi jaringan paru. Jaringan parut ini dapat menghubungkan daerah porta yang satu
dengan lainnya atau porta dengan sentral (bridging necrosis). Pada tahap berikut, kerusakana
parenkim dan peradagangan yang terjadi pada sel duktulus, sinusoid dan sel-sel
retikuloendotelial di dalam hati akan memacu terjadinya firbogenesis yang akan menimbulkan
septa aktif. Sel limfosit T dan makrofag juga mungkin berperan dengan sekresi limfokin yang
dianggap sebagai mediator dari fibrogenesis.
Septa aktif ini akan menjalar menuju ke dalam parenkim hati dan berakhir di daerah
portal. Pembentukan septa tingkat kedua ini yang sangat menentukan perjalanan progresif SH.
Pada tingkat yang bersamaan nekrosis jaringan perenkim akan memacu pula proses regenrasi
sel-sel hati. Regenerasi yang timbul akan menganggu pula pembentukan susunan jaringan ikat
tadi. Keadaan ini yaitu fibrogenesis sel yang terjadi terus menerus dalam hubungannya dengan
2.2.3.1. Patogenesis Fibrosis Hati
2.2.3.1.1. Sel- Sel Sinusoidal
Hati memiliki sel-sel sinusoidal yang terdiri dari sel-sel endotelial, pit cells, sel Kupffer
dan HSC. Kedua sel yang disebut terakhir berperan penting pada proses fibrogenesis hati.
Sel-sel endotelial membatasi sinusoid-sinosoid dan memiliki fenestra yang memungkinkan
terjadinya pertukaran zat antara hepatosit dan sel endotel. Antara heptosit dan sel endotelial
terdapat ruang Disse (subendotel) yang merupakan tempat HSC.
Sel Kupffer melekat pada sel endotel dan merupakan derivat monosit. Fungsi sel kupffer
ialah fagositosis terhadap hepatosit tua, debris sel, benda asing, sel tumor dan berbagai mikro
organisme. Fagositosis terhadap oxidized low density lipoprotein (LDL) cholesterol dan dibrin
pada keadaan koagulasi intravaskular diseminata juga dilakukan oleh sel ini. Aktivitasi sel ini
antara lain pada keadaan sepsis dan syok serta rangsangan oleh berbagai substansi seperti
endotoksin, lipopolisakarida derivat asam arakidonat, interferon Y dan tumor necrosis faktor
(TNF). Produk dari sel kupffer yang aktif terdiri dari berbagai sitokin, hidrogen peroksida, nitric
oxide (NO), TNF, interleukin (IL),-I, IL-6, IL-10, interferon- dan , transforming growh factor
(TGF) dan berbagai prostanoid.
HSC memiliki sitoplasma yang panjang sampai sinusosid yang bersentuhan denagn
hepatosid sehingga berperan dalam menentukan bersarnya aliran darah hepatik. Pada keadaan
inaktif (quecent) HSC merupakan tempat penyimpanan retinoid sehingga memiliki morfolgi HSC
merupakan tempat penyimpanan retinoid sehingga memiliki morfolgi cytoplasmic lipid droplest.
Pada keadaan aktif akibat terjadinya cedera hati HSC akan kehilangan lipid droplets,
berproliferasi dan kemudian bermigrasi ke zona 3 asinus lalu berubah menjadi sel miofibroblas
memiliki filamen aktin dan miosin. Rangsangan kontraksi utama ialah endotelin-/1 (ET-1) dan
subtansi P. 2,19,20
2.2.3.1.2. Perubahan Matriks Ekstraseluler
Pada jaringan hati normal terdapat MES yang merupakan kompleks terdiri dari 3 group
makromolekul yaitu kalogen, glikoprotein adhesif dan proteoglikan. Makromolekul utama ialah
grup kolagen yang terdiri dari kolagen interstitial atau fibrillar (kolagen tipe I,III) yang
berdensitas tinggi dan kolagen membran basal (kolagen tipe IV) yang berdensitias rendah di
dalam ruang Disse. Kolagen terbanyak pada jaringan hti yang normal ialah kolagen tipe IV.
Pada fibrogenesis terdapat peningkatan jumlah MES sebanyak 3 sampai 8 kali lipat dimana
kolagen tipe I dan III mengganti kolagen tipe IV. Glikoprotein adhensif yang dominan ialah
laminin yang membentuk membran basal dan fibronektin yang berperan dalam perlekatan,
diferensiasi dan migrasi sel. Proteoglikan merupakan protein yang berperan sebagai tulang
punggung MES dalam ikatannya dengan glikosaminoglikan. Pada fibrogenesis terjadi
peningkatan fibronektin, asam hialuronat, proteoglikan dan berbagai glikokonjugat.
Pembentukan jaringan fibrotik terjadi karena sintesis matriks yang berlebihan dan penurunan
penguraian matriks. Penguranain matriks tergantung pada keseimbangan antara enzim-enzim
yang melakukan degrasasi matriks dan inhibitor enzim-enzim tersebut.21,22,23
2.2.3.2. Kematian Sel Hati
Struktur dan fungsi hati normal tergantung pada keseimbangan antara kematian dan
regenersi sel hati. Kematian sel hati dapat melalui 2 proses yaitu nekrosis dan apoptosis. Pada
Mekanisme apoptosis merupakan mekanisme tubuh untuk menyingkirkan sel yang rusak,
berlebihan atau sudah tua (self destruction). Terjadi fragmentasi DNA sedangkan organel sel
tetap variabel. Pada keadaan patologis apoptosis dapat menyebabkan gagal hati fulminan.24
Saat dibutuhkan tambahan hepatosit, sel hati inaktif dirangsang oleh berbagai mediator
termasuk sitokin untuk masuk ke dalam fase G1 dari siklus motosis sel, dimana berbagai faktor
pertumbuhan termasuk nuclear factors seperti NFkB dapat merangsang sintesis DNA dan
kejadian ini disebut sebagai regenerasi. Pada keadaan sirosis hati terjadi regenerasi secara
cepat dan berlebihan sehingga nodul-nodul beregenerasi. Pada kerusakan hati yang luas,
hepatosit dapat dihasilkan oleh sel-sel yang berhubungan dengan duktus biliaris yang disebut
sel oval dan dari stemcells ekstrahepatik seperti sumsum tulang. Pada cedera hati terjadi
kehilangan fenestra endotel dan mikrovili hati serta terjadi kapilarisasi sinusoid yang akhirnya
akan menganggu pertukaran metabolit antara darah dan sel-sel hati. Transomasi sel normal
menjadi sel hati yang fibrotik merupakan proses yang sangat rumit. Terdapat interaksi antara
HSC dengan sel-sel parenkimal, sitokin, growth facor, berbagai protease matriks beserta
Gambar 2.2. Perubahan arsitektur hati pada perjalanan fibrosis hati. 26
Faktor – fakrtor yang berperan dalam terjadinya fibrosis hati dalam :
1. Cedera (injury) dalam hati.
2. Inflamasi yang ditandai dengan :
a. Infiltrasi dan aktivasi berbagai sel seperti : netrofil, limfosit, trombosit dan sel-sel
endotelial temasuk sel kupffer.
3. Aktivasi dan migrasi HSC ke daerah yang mengalami jejas.
4. Perubahan jumlah dan komposisi MES akibat pengaruh HSC serta pengaruh berbagai
sel, mediator dan growth factors.
5. Inaktivasi HSC, apoptosis serta penghambatan apoptosis oleh berbagai komponen yang
terlibat dalam perubahan MES.24,27
Terjadinya fibrosis hati dimulai dari aktivasi HSC yang dibagi dalam beberapa fase yang terdiri
dari beberapa tahap untuk memudahkan dalam mempelajarinya. Pada kenyataan proses ini
terjadi secara simultan dan tumpang tindih. Terdapat beberapa fase aktivtasi HSC. 26
A. Fase inisiasi
Merupakan fase aktivasi HSC menjadi miofibroblas yang bersifat proliferatif, fibrogenik
dan kontraktil. Terjadi induksi cepat terhadap gen HSC akibat rangsang parakrin yang bersla
dari sel-sel inflamasi, hepatosit yang rusak, sel-sel duktur biliarsis serta dari perubahan awal
komposisi MES. Perubahan-perubahan itu menyebabkan HSC responsif terhadap berbagai
sitokin dan stimulus lokal lainnya. Pada fase inisiasi, setelah cedera pada sel hati, terjadi
stimulasi parakrin terhadap HSC oleh sel-sel yang berdekatan dengan HSC seperti sel endotelial
dan hepatosit serta sel kupffer, platelet dan lekosit yang menginfiltrasi lokal cedera hati.
(gambar 1) Stimulasi parakrin tersebut berupa:
1. Inflamasi akibat pelepasan berbagai sitokin seperti : IL-1, IL-4, IL-5, IL-6, IL-13 yang
terutama dihasilkan oleh limfosit SC4 subset TH2, pelepasan berbagai interleukin, faktor –
faktor nekrosis dan interferon oleh sel kupffer.
2. Oksidasi, terutama oleh reactive oxygen (ROS) dan peroksida lipid yang dihasilan oleh
netrofil dan sel kupffer. Oksidan- oksidan tersebut meningkatkan seintesis kolagen oleh
3. Pelepasan dan aktivitas berbagai growth factors seperti TGF- yang terutama dihasilkan
oleh sel kupffer yang teraktivitasi dan oleh sel-sel endotelial lainnya.
4. Pengeluaran proteinase, misalnya matrix metalloproteinase-9 (MMP-9) yang dihasilkan oleh
sel kupffer.
5. Gangguan reseptor HSC. Peroxisome poliferator activated reseptor yang terdapat pada
reseptor HSC terdiri dari reseptor PPAR , dan . Peningkatan PPAR pada penurunan
PPARv menyebabkan aktivasi HSC. Mekanisme ini sering terjadi pada steatosis hati
nonalkoholik. Gangguan reseptor PPRAR juga meningkatkan stres oksidatif.26,28,29
B. Fase “pengkekalan” ( perpetuation phase)
Terjadi respons selular akibat proses inisasi. Pada fase ini terjadi berbagai reaksi yang
menguatkan fenotif sel aktif melalui peningkatan ekspresi berbagai faktor pertumbuhan dan
responsnya yang merupakan hasil rangsang autokrin dan parakrin serta akselerasi remodelling
MES. Fase ini sangat dinamis dan berkesinambungan.
Fase pengkekalan ini juga merupakan hasil stimulasi paraktrin dan autokrin, meliputi
tahap proliferasi, fibrogenesis, peningktan kontraktilitas, pelepsan sitokin proinflamasi,
kemotaksis, retinnoids loss dan defradasi matriks. Uraian mengenai tahapan-tahapan tersebut
ialah sebagai berikut :
a. Tahap proliferasi. Di sini terjadi peningkatan jumlah HSC oleh berbagai rangsangan
mitogenik dan aktivasi reseptor tirosin kinesa HSS. Berbagai rangsangan mitogenik antara
lain adalah PDGF, yang merupakan rangsang utama, oleh ET-1, trombin, fibroblast
growth factor (FGD, VEGF dan insulin-like growth factor (IGF). Ketiga subtansi yang
b. Tahap fibrogenesis dimana terjadi peningkatan produksi MES yang terutama disebabkan
oleh pengaruh TGF 1 yang dihasilakn oleh HSC, sel kupffer dan platelet. Sitokin lain yang
merangsang produksi MES ialah connective tissue growth factor (CTGF). Aktivasi TGF- 1
dipengaruhi leh berbagai subtansi, diantaranya MMP dan tissue plasminogen activators
(tPA). Perlu diketahui interaksi HSC dan MES dijembatani oleh integrin dengan bantuan
enzim focal adhesion kinas (FAK).27,30
c. Tahap kenaikan kontraktilitas HSC disebabkan ET-1 yang mengakibtkan peningkatan
resistensi portal karena adanya konstruksi sinusoid dan kontraksi jaringan hati sirotik.
Meskipun antagonis fisiologik ET-1 yaitu nitricopxide (NO) juga dihasilkan oleh HSC.
d. Tahap pelepasan sitokin proinflamasi dari HSC merupakan tahap pelepasan TFG, PDGF-
1,FGF, hypatofcyte growth factors (HGF), platelet activating factor (AF) dan ET-1.
selanjutnya terjadi pelepasan komoatrakan monosit dan limfosit. Komotraktan tersebut
ialah berbagai colony stimulating, factors, mobocyte chematactic protein-1 (MCP-1) dan
IL-8 dan IL-8, berbagai produk HSC tersebut memperkuat proses inlamasi hati. Meskipun
demikian sitokin anti inflamasi, terutama IL-10, juga dihasilkan oleh HSC.26,30
e. Tahap pembuangan retinoids HSC (retinoids loss) ditandai dengan pengeluaran substansi
tersebut ke ruangan ekstraseluler.
f. Tahap akumulasi ditandai oleh terjadinya pengeluaran HSC pada lokasi radang, baik
dengan migran langsung maupun melalui proses kemotaksis, setelah terjadinya proliferasi
lokal HSC26
Tahap akhir dari perpetuation phase ialah degradasi matriks diatur oleh keseimbangan
antara matrix metalloproteinase (MMP) dan antagonisnya yaitu TIMP (tissue inhibitor
metalloproteinases). Terdapat 2 jenis degradasi MES yaiu degradasi restoratif yang merusak
jaringan parut. Yang menyebabkan degradasi patologik adalah MMP2 dan MMP-9 dimana
kedua enzim ini merusakan kalogen tipe IV, serta membrane type metallopriteinase 1 dan 2
(aktivator MMP-2). Dan stromellisin-1 yang merusak protegoglikan dan glikprotein serta
mengaktivasi kolagenease laten. Kegagalan degradasi restoratif berupa gangguan
penghancuran jaringan parut yang berlebihan terutama disebabkan penurunan jumlah MMP-1
(protease kolagen tipe 1, kolagen utama pada fibrosis hati) dan peningkatan 1 dan
TIMP-2 perlu diketahui bahwa TIMP juga dihasilkan oleh HSC aktif.25,31
C. Fase Resolusi
Pada fase ini jumlah HSC yang aktif berkurang dan integritas jaringan kembali normal. Pada
fase ini terjadi 2 hal, yaitu reversi dimana terjadi perubahan HSC aktif menjadai inaktif (yang
sementara baru dapat diobservasi secara invitro) dan apoptosis. Pada keadaan jejas hati,
apoptosis dihambat oleh berbagai faktor dan komponen matriks yang terlihat dalam pross
infalmasi yang berperan penting menghambat apoptosis ialah TIMO-1 selain itu IGF-1 serta
2.3. FI BROSI S HATI
2.3.1. Diagnosis Fibrosis Hati
Dari defenisi penyakit ini, jelaslah bahwa diperlukan 4 unsur untuk terjadinya fiborsis hati yaitu
:
1. Adanya penyakit dasar sebagai penyebab injury yang mengakibatkan inflamasi kronik.
2. Aktivasi HSC.
3. Terlibat berbagai jenis medaitor, growth factors dan berbagai sel atau subtansi yang
terlihat dalam proses radang kronis hati.
4. Terjadinya fibrogenesis, penumpukkan sel matriks ekstraseluler (mes) dan penguraian
jaringan ikat tersebut.
Dengan demikian diagnosis FH di dasarkan pada :
a. Diagnosis penyakit dasar (misalnya hepatitis virus C).
b. Aktivasi HSC dengan berbagai penandanya diantaranya alpha-smoth muscle action
( -SMA), neural cell adhension molecule dan mestin. Penanda yang lebih baru ialah
prion protein (PrP), suatu sialoglikopretoin yang terutama terdapat pada neuron dan
sel glia pada susunan saraf pusat. Protein ini dikatakan merupakan indikator yang
baik untuk inflamasi aktif dan fibrogenesis. Pemeriksaan-pemeriksaan ini belum
cukup spesifik untuk penyakit fibrosis hati.24,33
c. Pemeriksaan produk degradasi MES dan enzim yang berperan dalam pembentukan
maupun degradasi MES.
d. Adanya fibrosis dan fibrogenesis yang dapat dilihat secara pasti dengan biopsi hati
Berbagai jenis sistim scoring telah dipakai untuk menilai stage dari fiboris hati seprti skir
MTAVIA, skir Ishak (Knodell) dan dianalisis biopsi dengan morfometri komputer menggunakan
pewarnaan jaringan. Yang direkomendasikan saat ini ialah sektor menurut METAVIAR yang
diajukan oleh Poynard dkk, yang terdiri dari 5 stage yaitu :
F0 (tanpa fibrosis)
F1 (fiboris ringan), ekspansi fibrosis sekitar zona portal atau vena sentral
F2 (fiboris moderat), septa yang meluas sampai ke lobus hati.
F3 (fibrosis moderat) disertai bridghing fiborsis (portal-portal, sentral-sentral, poral sentral).
F4 (sirosis) nodulasi parenkimal dikelilingi septa fibortik dan kerusakan arsitektur hati.
Laju fibrosis hati per tahun dapat ditentukan dengan stage fibrosi dalam METAVIR unit (0
sampai 4) dibagi perkiraan lamanya infeksi (tahun). Terjadinya fase akhir fiboris yaitu sirosis
hati dapat dihitung dengan rumus, stage fibrosis (0 sampai 4) dibagi laju fibrosis pertahun.
Penilaian stage dan laju fibrosis dapat digunakan untuk :
- Memperkirakan respons terapi, misalnya pada stage F4 respons terapi interferon- akan
rendah.
- Memberikan terapi sesuai kebutuhan. Jika didapatkan hanya sedikit laku fibrosis pada
interval pengamatan yang relatif lama, maka pengobatan antiviral dapat ditunda sampai
terapi itu diperkirakan dapat lebih efektif dan toleransi
- Memperkirakan waktu terjadinya sirosis hati. Hal ini diperlukan untuk antisipasi perawatan
penderita. Meskipun demikian terjadinya SH tidak serta merta menandakan terjadinya
gagal ganti secara klinis, karena terbukti pada beberapa penelitian bahwa sering gagal
- Menentukan kapan saat yang tepat pemberian terapi anti fibrosis. Saat terbaik pemberian
terapi anti fiboris ialah pada keadaan tidak berlangsung lagi gibrogenesis atau stable
fibrotic stage, dalam waktu relatif panjang.
Sistim scoring memiliki berbagai kelembahan antara lain tingginya kemungkinan
sampling error dan tidak dapat menentukan dinamisitas fibrogenesis. Beberapa peneliti
menyatakan bahwa stage FH menurut Pynard berhubungan secara non-liner dengan akselerasi
dan progreasi fibrosis hati tersebut.26
Pemeriksaan lain dengan menggunakan cara noninvasif seperti pemeriksaan marker serum,
antara lain:
a. Pemeriksaan produk degradasi MES dan enzim yang berperan seperti :
- Glikoprotein, termasuk antibodi terhadap asam hialuronat, laminin atau undulin
(kolagen tipe IV)
- Propeptida yang dihasilkan pada pembelaan MES saat komponen MES masuk ke dalam
jaringan parut, seperti kolagen tipe I, III, IV.
- Enzim yang berperan pada sintesis MES, seperti lysy oxidase, prolyl hydorxylase dan
lysyl hydorxyplase, galactosylglucosyltransferasem, monoamin oxidase danNacetyl
-D-glucoseaminidase.
b. Kombinasi beberapa marker serum
Percobaan multisenter di Eropa sedang berusaha membuat panel marker diagnostifk fiboris
hati. Panel ini terdiri dari pemeriksaan procollagen III N peptide (PIII-NP), kolagen tipe IV,
Kombinasi pemeriksaan klinik dan infeks laboratorium seperti yang dilaporkan oleh Pynard dkk,
dikatakan memiliki korelasi yang baik dengan penyakit fibrosis hati akibat virus hepatitis C.
Indeks laboratorium itu antara lain menggunakan -2 makroglobulin, hepatoglobulin, gama
glutamil transfgerase (GGT), glopbulin, bilirubin total apolipoprotein A.
d. Pemerikasan yang poteinsi dimasa depan
Beberapa pemeriksaan diantaranya positron emision tomography (PET) scanning dan
pencitraan resonansi magnetik diharapkan mempunyai nilai dalam pemeriksaan penentuan
fibrosis.
2.3.2. Perbaikan Fibrosis Hati
Sampai saat ini belum terhadap suatu obat yang diakui secara umum sebagai
antifiborsis hati. Beberapa syarat yang harus dipenuhi sebagai anti fibrosis antara lain obat ini
harus dapat ditoleransi dengan baik dengan kemungkinan pemakaian yang lama, dengan
sasaran yang tepat pada sel hati dan sedikit efek pertamanya yang baik, yang memungkinkan
obat ini untuk lebih fokus pada jaringan hati. Kombinasi beberapa obat mungkin bersifat
sinergis, tetapi belum jelas apakah obat anti fibrosis harus diberikan secara intermiten dan
terus menerus.
Penelitian terhadap obat anti fibrosis sulit dilakukan dengan baik karena tidak mudah dinilai
efikasinya dengan pemeriksaan darah, di samping itu perbaikan yang terjadi mungkin
membutuhkan pemakaian yang lama. Kesulitan ini ditambah lagi dengan belum adanya marker
yang terbaik dalam mengevaluasi hasil terapi sehingga masih diperlukan biopsi untuk hal.26
Secara umum terapi fibrosis hati meliputi :
Idealnya penyakit primer baik itu penyakit hati kronik karena virus, metabolik autoimun
maupun penyakit hati kronik karena obat harus dihilangkan atau diminimalkan, contoh yang
nyata ialah pengobatan hepatitis C dengan kombinasi interferon- dan ribavirin.
B. Penghambatan aktivasi HSC
Ada beberapa jenis obat yang dipakai pada fase ini yaitu :
1. Antioksidan
Obat golongan ini menyebabkan inhibisi stimulasi parakrin terhadap HSC. Contoh obat
golongan ini adalah Vitamin E, yang dapat mencegah terbentuknya berbagai oksidan
seperti asetaldehida serta berbagai spesies oksigen reaktif (ROS) termasuk H2 O2 dan
radikal bebas hidroksil. Disamping itu vitamin E dikatakan dapat menekan fibrogenesis.
Contoh lain ialah silimarin yang dapat menghambat kerusakan hati dan akumulasi kolagen
hati pada fibrosis bilier lanjut, tetapi kurang efektif terhadap penyakit hati alkoholik.
Substratd glutation sinthetase yaitu S-Adenosyl-L-Methionine (SAMe) yang merupakan
donor gugus metil untuk metabolisme beberapa asam amino tubuh, mempunyai efek
hepatoproteksi terhadap hepatitis akibat induksi obat dan toksin. Obat ini juga memperbaiki
parameter laboratorik fungsi hati seperti bilirubin, -giutamil transferase dan alkalin
fosfatase serta mengurangi gejala gatal dan rasa lelah pada penderita dengan kolestasis. Di
samping ini SMAe juga memperpanjang uslivival rate penderita sirosis hati akibat alkohol.
Pentaoksifilin in vitro menghambat pliferasi HSC dan menurunkan produksi TNF- pada
monosit, menurunkan aktivasi NFkB pada HSC. Polyphenilphosphatidycholine (PPC)
2. Sitokin dan grow th factors
Interferon- dan hepatocyte growth factors (HGF) menghambat aktivasi HSC pada hewan
percobaan. Studi besar interferon- pada fibrosis hati akibat infeksi virus hepatitis C sedang
berlangsung.26
3. Obat- obat lain
Peroxisome proliferator activated nuclear receptor (PPAR- dapat menurunkan aktiasi HSc.
Pengobatan menggunakan ramuan tradisional Cina yang berasal dari tumbuh-tumbuhan
seperti xiao caihu tang, Glycyrrhizin (Licorice Extract) dan han-dan-gan-le mungkin efektif.
Obat-obatan tersebut memiliki cara kerja sebagai antioksidan, mengingkatkan kolagenase
interstitial, menurunkan akvitasi pengikut NFkB dan lain-lain. Belum ada suatu studi yang
besar dalam meneliti obat-obat ini, meskipun demikian obat-oba ini jelas membuka
perspektif baru dalam penanganan fibrosis hati.15,19 Interferon- jug mempunyai efek
menghambat aktiivasi HSC. 36,37
C. Usaha untuk mengurangi inflamasi dan respons imun
Pemakaian kortikosteroid sebagai anti inflmasi tidak memiliki efek langsung terhadap
HSC. Deksametason terbukti efek menghambat induksi MCP-1 oleh TNF- dan berbagai
oksidan. Antagonis TNF- mungkin dapat dipergunakan pada penyakit inflamasi hati karena
telah terbukti relatif efektif dan aman pada artritis rematoid dan penyakit Crohn. Asam
ursodeksikolat (UDCA) mempunyai efek yang menguntungkan pada fibrosis hati akibat sirosis
bilier primer karena efek anti inflamasinya. Obat lain yang memiliki efek anti inflamasi dan
dapat mencegah pembentukan kolagen ialah kolokisin, meskipun efikasinya belum dibuktikan
D. Netralisasi respon- respons HSC ( netralisasi respons prliferasi, netralisasi Sifat
fibrogentik, sifat kontraktil, dan penghambat aktivasi sitokin proinflamasi)
1. Netralisasi reseptor TGF- . TGF- memiliki 2 reseptor transmembran serine/theroinen
kinase. Yang minan ialah reseptor tipe 2. Percobaan menggunkan adnevirus (AdCAT
-TR), suatu penghambat resepotor TGF- 2 dapat menurunkan fibrogenesis.
2. Penghambat aktivasi TGF-
salah satu cara aktifasi TGF- ialah melalui reaksi yang diperantarai oleh plasmin.
Plasminogen diubah menjadi plasmin oleh PAF dengan bantuan enzim tissue
transglutamine (tTG) pada permukaan HSC atau MES. Inhibitor tTG seperti fenilefrin,
putrescine atau guanosin 5-0-(3 thiotriphosphate) dapat menghambat aktivasi TGF- .26,29
3. Inhibisi transduksi sinyal (inhibitor tirosinkinase)
Platelet derivate growth factor (PDGF) selain sebagai faktor mitogenik juga berperan
terhadap aktivasi HSC. Aktivasi reseptor PDGF ialah melalui autofosforilasi tirosin yang
dapat dihambat oleh sebuah agen yang disebut SU 5874. Suatu jalur alternatif aktifasi
dari PDGF ialah melalui extraculullar signal regulated kinase (ERK) yang dapat dihambat
oleh PD 98059.
4. Penghambat interaksi matriks
Larutan yang terdiri dari arginin, glusin,a spartat (Arg-Gly-Asp) dapat menghalangi
fosforilasi tirosin dari FAK sehingga menghalangi aktivasi HSC.26
5. Lain-lain
Antagonis terhadap ET-1 (regulator kontraksi HSC) memiliki efek anti fibriotik dan dapat
E. Situmlasi apoptosis HSC
Gliotoksin merupakan obat yang merangsang apoptosis HSC pada hati hewan
percobaan yang mengalami fibrosis akibat klorofrom (CCI4).
F. Meningkat degradasi MES
Degradasi MES dapat ditingkatkan dengan menggunakan antafonis TGF- melalui
penurunan TIMP dan peningkatan aktifitas kolagenase interstitial. Riset penggunaan MMP
mRNA melalui terapi gen telah dimulai.
G. Obat baru
-2 makroglobulin yang menurunkan produksi atuokrin dan parktrin TGF- oleh sel
kupffer dan HSC aktif, dapat menurunkan produksi proteoglikan oleh HSC.26,38 Pengobatan
penderita penyakit hati kronik, baik dengan mengobati penyakit primernya maupun dengan
usaha pengurangan akumulai jaringan parut, hendaknya diusahakan secara optimal meskipun
pada penyakit fiborsis hati yang lanjut, untuk mencapai reversibilits fibrosis hati yang lanjut,
untuk mencapai reversibillitas fibrosis yang maksimal.39
BAB I I I
PENELI TI AN SENDI RI
3.1. Latar Belakang
Sirosis Hati merupakan penyakit hati menahun yang ditandai dengan proses
peradangan, nekrosis, usaha regenerasi dan penambahan jaringan ikat difus, dengan
terbentuknya nodul yang mengganggu susunan lobulus dan fungsi hati.26 Secara patologi
kriteria sirosis hati adalah terbentuknya fibrosis dan regenerasi nodule.
Di Indonesia pria lebih banyak menderita SH dibanding wanita dengan rasio 2-4,5:1, dimana
kelompok usia dekade ke-5 merupakan kelompok yang terbanyak. Dalam kurun waktu 4 tahun,
Tarigan di Medan mendapatkan dari 19.914 pasien yang dirawat di Penyakit Dalam, 1128 (5%)
diantaranya menderita penyakit hati dan penderita SH sebanyak 819 (72,7%). Peneliti lainnya
seperti Hadi dkk (1975) mendapatkan SH sebanyak 5,2% dari seluruh penderita yang dirawat
di Bagian Penyakit Dalam RS. Hasan Sadikin Bandung periode 1966-1974. Julius di RSUP Dr. M
Djamil ( Padang) mendapatkan angka 9,9%. Di negara barat angka kejadian SH didapati
berkisar 2,45 (0,9-5,9%).40
Di antara beberapa cara yang digunakan untuk melihat alternatif lain dalam
menentukan derajat fibrosis hati digunakan metode yang sederhana dengan memeriksa kadar
Laminin (LN) dalam serum yang merupakan bahan matriks ekstraseluler yang memiliki
korelasi dengan derajat fibrosis walaupun banyak peneliti lain menggabungkannya dengan
komponen bahan pembentukan matriks ekstraseluler lainnya seperti kolagen, fibronektin,
Penelitian tentang LN sehubungan dengan penyakit hati sebelumnya tidaklah banyak
dan tidak menggambarkan keseragaman nilai LN dalam menentukan derajat kerusakan hati,
antara lain:
Collazos dkk mendapatkan peningkatan kadar LN sebesar 62,7% pada penderita Sirosis
Hati (SH) dibanding kontrol dan semakin berat keparahan SH (berdasarkan Kriteria
Child-Turcotte-Pugh (CTP)) maka kadar LN akan semakin meningkat.4
Burchardt dkk (2005) mendapatkan bahwa kadar LN meningkat sesuai dengan derajat
fibrosis pada penderita Hepatitis C kronis.5
Cai WM (1995) mendapatkan kadar LN memiliki sensitivitas dan spesifitas yang lebih
rendah dibanding kombinasi pemeriksaan kadar plateletderived growth factor-BB (PDGF-BB) .6
Panomarenko dkk (2002) melaporkan bahwa nilai LN pada orang sehat 15,5 ± 0,52
ng/ml dan pada peminum alkohol dengan fibrosis hati terjadi peningkatan menjadi 47,34
ng/ml .7
Tao J dkk (2003) melaporkan dari 141 penderita hepatitis kronis yang diperiksa kadar
hyaluronic acid (HA), type III pro-colagen (PCIII), LN dan type IV collagen (C-IV) ternyata
14,16% indeks serum fibrosis hati tidak berhubungan dengan derajat fibrosis hati (berdasar
biopsi) .8
Yong Peng C dkk (2004) mendapatkan bahwa kadar serum LN tidak berhubungan
dengan derajat keparahan penyakit hati atau derajat fibrosis pada penderita hepatitis B kronis
.9
Belum ada penelitian tentang hubungan antara kadar LN dengan derajat keparahan penyakit
hati berdasarkan kriteria CTP selama ini di Indonesia sedangkan penelitian tentang hal ini dapat
dilakukan dengan sederhana dan mungkin menggambarkan derajat fibrosis dan juga dapat
sebab itu peneliti ingin melihat bagaimana hubungan kadar LN dengan keparahan penyakit
sirosis hati.
3.2. Perumusan Masalah
1. Apakah didapati peningkatan kadar laminin pada penderita SH bila dibanding
dengan kontrol sehat?
2. Apakah kadar serum laminin berbanding lurus dengan beratnya derajat
keparahan SH berdasarkan kriteria CTP ?
3.3. Hipotesa
1. Kadar serum LN meningkat pada penderita SH dibanding kontrol sehat
2. Kadar serum LN berbanding lurus dengan derajat keparahan SH berdasarkan
kriteria CTP
3.4. Tujuan Penelitian
1.Untuk mengetahui peningkatan kadar serum LN pada penderita SH
2. Untuk membuktikan bahwa peningkatan kadar serum laminin berbanding lurus
dengan peningkatan derajat keparahan SH
3.5. Manfaat Penelitian
1. Dengan mengetahui adanya peningkatan kadar serum LN maka serum LN
3.6. Bahan dan Cara
3.6.1. Desain Penelitian
Penelitian dilakukan secara studi potong lintang dengan pendekatan deskriptif analitik
3.6.2. Waktu dan Tempat Penelitian
Waktu : Januari 2008 s/d Juni 2008
Tempat : RSUP H. Adam Malik, RS Pirngadi Medan , RS Swasta
dan praktek dokter ahli Gastroentero-Hepatologi
3.6.3.Subjek Penelitian
Penderita SH yang rawat jalan ataupun rawat inap, dilakukan pemeriksaan klinis,
laboratorium rutin, kadar serum laminin , masa protrombin, kadar bilirubin, SPE,
USG ; dan sebagai kontrol adalah orang sehat.
3.6.4 Kriteria I nklusi
Penderita SH yang di tegakkan diagnosanya berdasarkan gejala klinis, laboratorium,
USG, tanpa memandang etiologinya, baik wanita ataupun pria, berusia di atas
18 tahun dan bersedia ikut dalam penelitian / inform concern.
3.6.5. Kriteria Eksklusi
Hepatoma, Rematoid Artritis, SLE.
3.6.6. Besar Sampel
Untuk menentukan besarnya jumlah sampel digunakan rumus:
(Z
α
+ Z
β
) S
Dimana :
(X
1– X
2)
Zα = nilai baku normal table Z yang besarnya tergantung pada nilai α yang
Jadi, sampel minimal untuk masing-masing kelompok kasus dan kontrol
sebesar 30 penderita.
3.6.7. Analisa Data
- untuk menjelaskan variable-variabel karakteristik disajikan dalam bentuk tabulasi data
diskriptif
- untuk melihat perbedaan kadar serum LN antara penderita SH dan orang sehat
(kontrol) digunakan uji t independent jika data terdistribusi normal dan jika tidak
digunakan Mann-Whitney
- untuk melihat perbedaan kadar serum LN pada penderita SH (Child-Pugh A,B,C)
digunakan uji Anova jika variansnya sama, jika tidak digunakan uji Kruskal Wallis
3.6.8. Prosedur Penelitian
Seluruh penderita SH yang mengunjungi tempat penelitian setelah ditegakkan
diagnosa berdasarkan pemeriksaan klinis, laboratorium rutin, faal hati, serologi marker
masa protrombin, USG dilakukan pemeriksaan kadar serum laminin setelah diminta
persetujuan tertulis (informed consent).
Untuk menentukan derajat keparahan SH digunakan kriteria CTP yaitu
dikelompokkan ke dalam grade A bila total skor 5-6 (kompensasi), grade B: 7-9
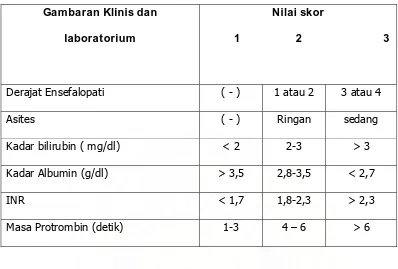
Tabel 3.1. Derajat keparahan SH berdasarkan kriteria Child-Turcotte-Pugh 21
Gambaran Klinis dan
laboratorium
Nilai skor
1 2 3
Derajat Ensefalopati ( - ) 1 atau 2 3 atau 4
Asites ( - ) Ringan sedang
Kadar bilirubin ( mg/dl) < 2 2-3 > 3
Kadar Albumin (g/dl) > 3,5 2,8-3,5 < 2,7
INR < 1,7 1,8-2,3 > 2,3
Masa Protrombin (detik) 1-3 4 – 6 > 6
Untuk mengukur kadar serum LN penderita secara kuantitatif dilakukan dengan metode
ELISA dari Chemicon International, dimana kadar LN dihitung berdasarkan standard kurva yang
dipergunakan. Sampel yang diperiksa ditambahkan free rabbit anti-human laminin yang
berikatan dengan LN . Dengan metode ELISA maka akan terjadi ikatan enzim-antibodi dan
dilihat perubahan warna yang terjadi dan intensitas warna menggambarkan kadar LN.
BAB I V
HASI L PENELI TI AN DAN PEMBAHASAN
4.1. Hasil Penelitian
4.1.1. Karakteristik Responden
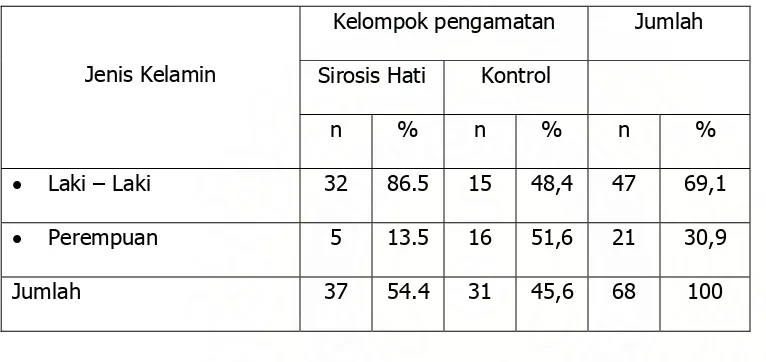
Tabel 4.1. Distribusi Jenis Kelamin Penderita Sirosis Hati dan Kontrol
Kelompok pengamatan Jumlah
Sirosis Hati Kontrol Jenis Kelamin
n % n % n %
• Laki – Laki 32 86.5 15 48,4 47 69,1
• Perempuan 5 13.5 16 51,6 21 30,9
Jumlah 37 54.4 31 45,6 68 100
Dari tabel 4.1. Terlihat bahwa dari 37 responden sirosis hati yang masuk penelitian, terdiri dari
32 (86.5%) orang laki-laki dan 5 (13.5%) orang perempuan dan pada kelompok kontrol dari 31
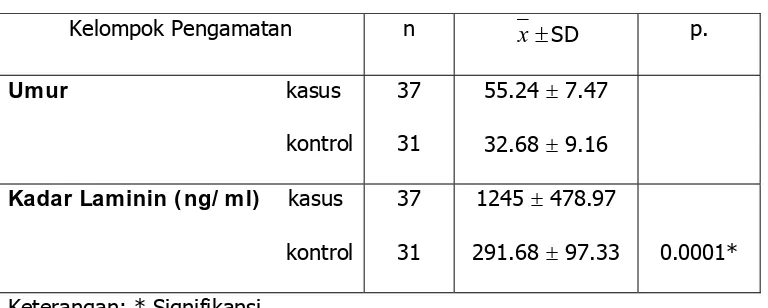
Tabel 4.2. Gambaran LN Penderita Sirosis Hati dan Kontrol
Kelompok Pengamatan n x±SD p.
Umur kasus
kontrol
37
31
55.24 ± 7.47
32.68 ± 9.16
Kadar Laminin ( ng/ ml) kasus
kontrol
37
31
1245 ± 478.97
291.68 ± 97.33 0.0001*
Keterangan: * Signifikansi
Tabel 4.2 menunjukkan rata-rata umur kelompok kasus 55.24 ± 7.47 tahun dimana umur
termuda 45 tahun dan tertua 65 tahun dan rata-rata umur kontrol 32,68 ± 9,163. Dari hasil
diatas, dapat dilihat kadar serum LN antara kelompok kasus dan kontrol terdapat perbedaan
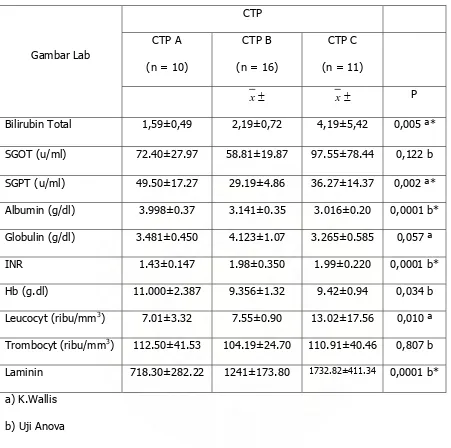
Tabel 4.3. Karateristik data dasar klinik
Bilirubin Total 1,59±0,49 2,19±0,72 4,19±5,42 0,005 ª*
SGOT (u/ml) 72.40±27.97 58.81±19.87 97.55±78.44 0,122 b
SGPT (u/ml) 49.50±17.27 29.19±4.86 36.27±14.37 0,002 ª*
Albumin (g/dl) 3.998±0.37 3.141±0.35 3.016±0.20 0,0001 b*
Globulin (g/dl) 3.481±0.450 4.123±1.07 3.265±0.585 0,057 ª
INR 1.43±0.147 1.98±0.350 1.99±0.220 0,0001 b*
Hb (g.dl) 11.000±2.387 9.356±1.32 9.42±0.94 0,034 b
Leucocyt (ribu/mm3) 7.01±3.32 7.55±0.90 13.02±17.56 0,010 ª
Trombocyt (ribu/mm3) 112.50±41.53 104.19±24.70 110.91±40.46 0,807 b
Laminin 718.30±282.22 1241±173.80 1732.82±411.34 0,0001 b*
a) K.Wallis
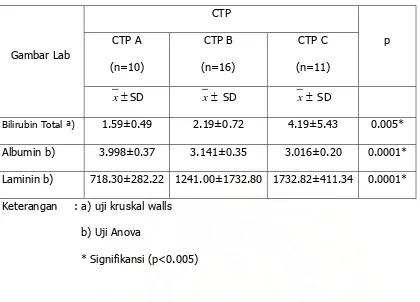
Tabel 4.4. Gambaran Klinis Sirosis Hati Berdasarkan CTP
CTP
CTP A
(n=10)
CTP B
(n=16)
CTP C
(n=11)
p Gambar Lab
±
x SD x± SD x± SD
Bilirubin Total ª) 1.59±0.49 2.19±0.72 4.19±5.43 0.005*
Albumin b) 3.998±0.37 3.141±0.35 3.016±0.20 0.0001*
Laminin b) 718.30±282.22 1241.00±1732.80 1732.82±411.34 0.0001*
Keterangan : a) uji kruskal walls
b) Uji Anova
* Signifikansi (p<0.005)
Dari tabel 4.4 di atas terlihat bahwa rata-rata kadar Bilurubin total, Albumin dan LN antara
Child Pugh A, B da C berbeda bermakna (P<0.05). Dengan kata lain, ada hubungan yang
Tabel 4.5. Gambaran perbedaan nilai rata- rata LN serum berdasarkan CTP
CTP Perbedaan nilai mean LN Signifikansi
CTP A CTP B
Keterangan : * = signifikansi (P.<0.05)
Tabel 4.5. memperlihatkan bahwa rata-rata kadar LN pada CTP A dengan CTP B, CTP A dengan
CTP C dan CPT B dengan CTP C terdapat perbedaan yang bermakna (p<0.05).
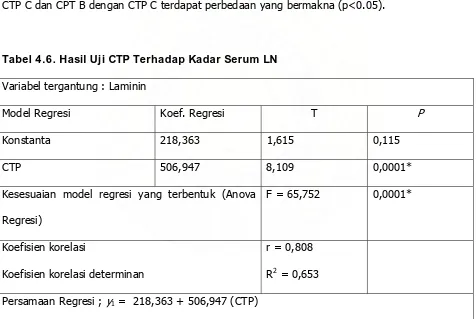
Tabel 4.6. Hasil Uji CTP Terhadap Kadar Serum LN
Variabel tergantung : Laminin
Model Regresi Koef. Regresi T P
Konstanta 218,363 1,615 0,115
CTP 506,947 8,109 0,0001*
Kesesuaian model regresi yang terbentuk (Anova
Regresi)
Pada tabel 4.6 dengan menggunakan uji regresi liner, diperoleh persamaan regresi sebagai
berikut y1 = 218.363 + 506.947 (CTP). Dalam persamaan variabel tergantung adalah kadar
artinya persamaan regresi tersebut sudah sesuai menggambar pengaruh yang sesungguhnya
antara kedua variabel tersebut. Kuat hubungan sebab akibat variabel tersebut didapat dari nilai
koefisien korelasi determinan (R2) yaitu 65,3%.
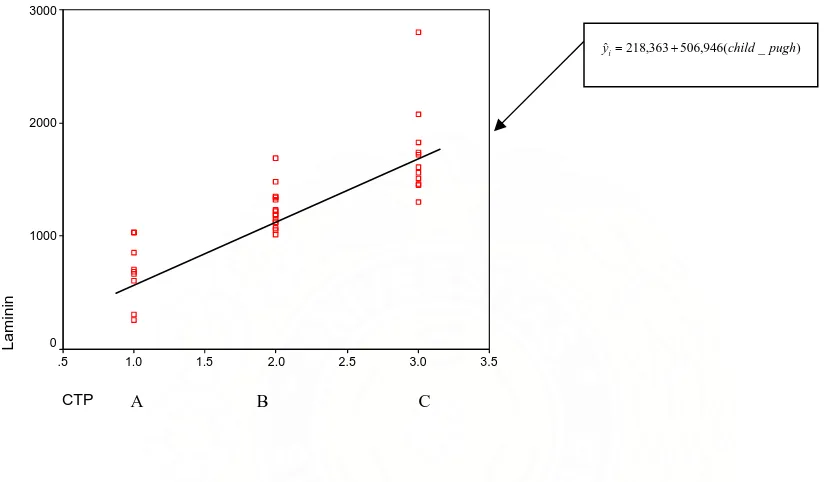
CTP
Gambar 4.1. Hubungan antara beratnya derajat kerusakan hati dengan kadar
rata-rata LN serum
Gambar 4.1. memperlihatkan bahwa semakin berat derajat keparahan kerusakan hati akan
menunjukkan peningkatan kadar LN serum, pada tingkat CTP C (tingkat sirosis hati yang paling
parah) terjadi peningkatan yang berbeda bermakna dibandingkan dengan CTP A, demikian
4.2. PEMBAHASAN
Produksi LN terutama di hati dan kadarnya berbanding lurus dengan derajat keparahan
penyakit hati. Pada penelitian ini didapat kelompok pasien dengan CTP A kadar LN serum
718,30 ± 282,22ng/ml; CTP B kadar LN serum 1241 ± 173,80ng/ml sedangkan pada CTP C
kadar LN serum 1732,82 ± 411,34ng/ml. Ada perbedaan yang bermakna antara kadar LN
serum pada pendeirta sirosis hati CTP A dengan CTP B (p=0,0001) begitu juga antara CPT B
dengan CTP C (p=0,0001) dan CPT A dengan CTP C (p=0,0001). Hal ini menunjukkan ada
hubungan langsung antara kadar LN serum dengan derajat keparahan hati pada pasien SH,
dimana semakin berat keparahan penyakit hati maka akan semakin tinggi nilai LN serum dan
hal ini sesuai dengan penelitian sebelumnya (Collazos, dkk : peningkatan kadar laminin sebesar
62,7% pada penderita SH dibanding kontrol. Semakin berat keparahan SH (berdasarkan CTP)
maka kadar LN akan semakin meningkat)4. Hal ini juga menunjukkan bahwa kadar LN
meningkat dengan derajat fibrosis (Burchardt, dkk 2005).5
Bila dibandingkan dengan kontrol sehat maka pada pasien SH, nilai mean LN serum
lebih tinggi, dimana di dapat 291,68 ± 97,33ng/ml pada kelompok kontrol dan 1245 ± 478,97
ng/ml pada kelompok SH. Hal ini memperlihatkan bahwa ada perbedaan yang bermakna nilai
LN serum penderita SH dan orang sehat.
Bila terjadi gangguan / kerusakan hati yang berat akan mengakibatkan peningkatan
kadar LN serum. Keadaan ini dapat dimengerti karena pada kerusakan hati kronis dibentuk LN
dan kadarnya akan meningkat sesuai dengan derajat kerusakan hati. Percobaan multisenter di
Eropa sedang berusaha membuat panel marker diagnostik fibrosis hati. Panel ini terdiri dari
pemeriksaan prokollagen III N peptide (PIII-NP), kolagen tipe IV, tenascin, laminin P1, asam
hialuronat, TIMP-1, MMP-2 dan kolagen tipe IV. Panel diagnostik ini diharapkan dapat
LN saja dapat dijadikan sebagai marker tejadinya fibrosis dengan nilai 718,30 ± 282,22ng/ml.
nilai ini lebih tinggi bila dibandingkan dengan penelitian tedahulu yang dilakukan di luar negeri
seperti Panomarenko, dkk (2002) mendapatkan kadar LN: 157,5 ± 24,6 pada fibrosis stage IV.
Untuk penelitian selanjutnya perlu dilakukan penilaian dengan membandingkan marker
firbriosis lainnya dan perlu diuji sensitivitas dan spesifisitas tingginya kadar LN serum sebagai
marker dan evaluasi fibriosis yang kiranya dapat menjadi metode evaluasi perkembangan
fibrosis hati dengan cara yang praktis dan dapat digunakan di banyak tempat dengan
keterbatasan tenaga ahli.
Dengan diketahuinya kadar LN meningkat pada penderita SH dan akan semakin tingi
sebanding dengan derajat keparahan penyakit hati maka penelitian ini perlu terus
dikembangkan dengan menggunakan sampel yang lebih banyak dan perlu dibandingkan
dengan marker fibriosis lainnya.
Korelasi positif pada penelitian ini ditemukan antara CTP dengan kadar serum LN. Hal
ini menunjukkan semakin tinggi nilai serum LN maka nilai skor CTP akan semakin besar.
Hubungan ini diperkuat dengan analisa regresi yang menunjukkan kuat hubungan antara
CTPdengan kadar serum LN sebesar 65,3%.
Bila dilihat dari komponen penilaian terhadap skor CTP, pada penelitian ini hasil yang di
dapat nilai yang berbeda bermakna terhadap derajat keparahan SH adalah kadar albumin dan
bilirubin, dimana semakin berat keparahan penyakit hati nilai albumin akan semakin rendah
BAB V
KESI MPULAN DAN SARAN
5.1. KESI MPULAN
5.1.1. Kadar LN dalam serum berbanding lurus dengan beratnya derajat kerusakan hati pada
penderitaan SH.
5.1.2. Kadar LN penderita SH lebih tinggi dibanding orang sehat.
5.2. SARAN
5.2.1. Perlu penelitian lebih lanjut dengan sampel yang lebih banyak untuk menjadikan LN
sebagai pertanda beratnya kerusakan hati.
5.2.2. Perlu diteliti lebih lanjut dengan sampel lebih banyak untuk menilai hubungan kadar LN
sebagai marker fibrosis dengan menentukan spesifisitas dan sensitifitas LN
KEPUSTAKAAN :
1. Bataller R, Brenner DA. Liver Fibrosis.The Journal of Clinical Investigation. 2005;
115:209-18
2. Rosenberg WM,Voelker M, Thiel R et al. Is this end for liver biopsy ? Clinicial Opinion. JR
Coll Physicians Edinb. 2005;35:31-2.
3. Poynard Thierry . Alternatives to Liver Biopsy for Assessing Liver Disease Status in
Patients With Hepatitis C. Busines Briefing: Clinical Virology & Infectious Disease.2004:
57-8.
4. Collazos J, Diaz F, Genolla J. Serum concentrations of laminin in cirrhosis of the liver
(abstract). PubMed – indexed for MEDLINE.
5. Burchardt E, Weist R, Hartmann A, Knoll A, Hellerbrand C. Circulating Serum Markers
Correlate with Liver Fibrosis in Patients with Chronic Hepatitis C. Journal Gastoenterology.
2005;43 (Abstract)
6. Cai WM, Zhang BB, Weng HL, Hu ZR, Zheng M, Liu RH.The diagnostic value of eight
serum indices for liver fibrosis (abstract). PubMed – indexed for MEDLINE
7. Ponomarenko Y, Leo MA, Kroll W, Liebber CS. Effect of alcohol consumption on eight
circulating markers of liver fibrosis. Alcohol & Alcoholism. 2002;Vol 37(3): 252-5
8. Tao J, Peng HQ, Cai WM, Dong FQ, Weng HL, Liu RH. Influence factors of serum fibrosis
markers in liver fibrosis. World J Gastroenterol. 2003; 9(11): 2497-500.
9. Yong-peng Chen, Xiao-rong Feng, Dai Lin, Lian Zhang, Jin-lin Hou. Non-invasive
10. Saltik, Nurten K, Hasan O, Hulya D. Serum HA concentrations in patients with cirrhosis.
Indian Journal of Gastroenterohepatology. 2004.
11. Guechot J, Laudat A, Loria A. et al. Diagnostic accuracy of hyaluronan and type III
procollagen amino-terminal peptide serum assays as markers of liver fibrosis in chronic
viral hepatitis C evaluated by ROC curve analysis. Clinical Chemistry.1996;42(4): 558-61.
12. QuantiMatrix TM Human Laminin ELISA Kit. Chemicon International. Temecula, California
92590.
13. Hui AY, Friedman SL. Extracellular Matrix. In: Dufour JF, Clavien PA. Signaling Pathways
in Liver Disease. Springer. Germany. 2005. p: 65-7
14. Dahlan A, Zubir N, Arsad D, Julius W. Ketepatan diagnosis klinis sirosis hati dibandingkan
dengan ultrasonografi. Naskah lengkap KOPAPDI VIII, Jogyakarta; 1990:145-50.
15. Bonis PA, Friedman SL, Kaplan MM: Is liver fiborisi revensible? N Engl J Med
2001;344:452-54.
16. Sherlock S, Dooley J. The Portal Venous System and Portal Hypertension. In:Disease of
the Liver and Billiary System. 10th Ed. Massachusetts: Blackwell Scientific Pub; 1997.p
135-80.
17. Albanis E, Friedman. Hepatic fibrosis, Patgologesis and principle of therapy. Clin Liver Dis,
2001;5:315-334.
18. HiguchH, Gores GJ. Mechanisms of liver injury. Current biomolecular Medicine,
2003;3:483-90.
19. Skelly MM, James PD, RyderSD. Finding on liver biopsy to invetifate abnormal liver fuction
20. Poynard T, Bedossa P, Opolon P. natural history of liver fibrosis prgoresision in patients
with choronic hepatitis C. the Obsvire, Metabir, Chinirvi and Dosovire group. Lancet
1997;349:825-32.
21. Bemyon D, rthur MJP: Extracelluler matrix degranadation and the role of stellate cells.
Semin Liv Dis 2001, 21:373-84.
22. Kitada T, Seki A, Ikeda K, et al. Cliniocopathological characterization of pron:a novel
mareker for activated human stelalate cells. J hepatol 2000;33:751-7.
23. NN.Fbrosisavaiblefrom.http//:www.fibrosis.com/defferentfromcirrhsois/htm.
24. Wu J, Zen M. Hepatic stellate cells : a targets for the treatment of liver fibrosis. J
Gastroebterol 2000:35:665-72.
25. Friedman SL. Hepatic Fibrosis. In: eugene RS, Michael FS, Willis CM (Eds). Schiff’s
Diseases of the Liver. 8th Ed. Philadelphia: Lippincott Williams & Wilkins; 1996.p.371-85.
26. Friedman SL. Liver fibrosis - from bench to bedside. Journal of Hepatology 2003; 38:
S38-53
27. Marra F. Hepatic stellate cells and the regulation of inflamation. J Hepatol
1999;31:1120-324.
28. Arthur MJ. Metalloproteinase and their inhibitor in the liver fibrosis. Am J Physiol
2000;279:G245-9
29. Szantova M, Kupcopa m. Biochemical markers of fibrogenesis in liver disease. Bratisk Lek
Listy 1999; 100(1):28-35
30. NN. Fibrosisavalablefrom :http://www.fibrosis.com/differentfromcirrhosis/html.