BAB II
TINJAUAN PUSTAKA
2.1 Uraian Tumbuhan
Uraian tumbuhan meliputi daerah tumbuh, sistematika tumbuhan, sinonim tumbuhan, nama daerah, nama asing, morfologi tumbuhan, kandungan kimia dan kegunaan dari tumbuhan.
2.1.1 Jeruk Kesturi
2.1.1.1 Sistematika Tumbuhan
Divisi : Spermatophyta Subdivisi : Angiospermae Kelas : Dicotyledoneae
Ordo : Rutales
Suku : Rutaceae
Genus : Citrus
Spesies : Citrus microcarpa Bunge (Nuraini, 2011). 2.1.1.2 Sinonim Tumbuhan
Sinonim Citrus mitis
Citrus fortunella (Setiadi dan Parimin, 2004). 2.1.1.3 Nama Daerah
Indonesia: Jeruk kesturi, jeruk potong, jeruk peras (Setiadi dan Parimin, 2004).
2.1.1.4 Nama Asing
2.1.1.5 Daerah Tumbuh
Jeruk peras atau jeruk kesturi tumbuh baik di daerah dataran rendah beriklim panas dengan curah hujan rata-rata 1500-2000 mm3/tahun. Tanah tempat tumbuhnya mengandung bahan organik, bisa berupa tanah liat-berlempung, tanah berkapur, atau tanah berpasir. Derajat keasaman (pH) tanah antara 5,5-7,0. Meskipun toleran terhadap kekeringan, jeruk peras tidak begitu tahan terhadap terpaan angin kencang (Setiadi dan Parimin, 2004).
2.1.1.6 Morfologi Tumbuhan
Buah jeruk kesturi berbentuk bulat dan bergaris tengah 4,5 cm. Bagian atas buah memipih atau rata (bulat menggepeng). Kulit buah kuning kehijau-hijauan sampai jingga (buah tua). Bobot buah kurang lebih sama dengan jeruk nipis, yaitu antara 20-30 buah per kg (Setiadi dan Parimin, 2004).
2.1.1.7 Kandungan Kimia
Kulit buah jeruk kesturi memiliki rasa pahit yang disebabkan oleh adanya kandungan naringin. Flavedo mengandung senyawa steroid, sedangkan albedo kaya akan senyawa fenolik (Anonima, 2008).
2.1.1.8 Kegunaan
Kulit buah jeruk kesturi biasanya diolah menjadi manisan, sari buah sirup, selai, dan konsentrat (Anonima, 2008).
2.1.2 Jeruk Lemon
2.1.2.1 Sistematika Tumbuhan
Ordo : Rutales
Suku : Rutaceae
Genus : Citrus
Spesies : Citrus limon (L.) Osbeck (Nuraini, 2011). 2.1.2.2 Sinonim Tumbuhan
Sinonim Citrus medica L. (Nuraini, 2011). 2.1.2.3 Nama Daerah
Indonesia: Jeruk tangan, jeruk honje (Sunda), jeruk sitrun (Jawa), jeruk lemon, dan jeruk sikade (Nuraini, 2011).
2.1.2.4 Nama Asing
Citroen (Belanda) (Nuraini, 2011). 2.1.2.5 Daerah Tumbuh
Tumbuhan ini cocok untuk daerah beriklim kering dengan musim dingin yang relatif hangat. Suhu ideal untuk jeruk lemon agar dapat tumbuh dengan baik adalah antara 15-30оC. Pada tanah yang subur, jeruk lemon dapat berbuah sepanjang tahun. Setelah berumur tiga tahun, jeruk lemon mulai berbuah (Nuraini, 2011; Setiadi dan Parimin, 2004).
2.1.2.6 Morfologi Tumbuhan
2.1.2.7 Kandungan Kimia
Kulit buah jeruk lemon mengandung tangerine yaitu jenis antioksidan kuat yang disebut super-flavonoids, yang bisa mengurangi kadar kolesterol jahat secara signifikan, tanpa menurunkan kadar kolesterol baiknya (Anonimb, 2012).
2.1.2.8 Kegunaan
Kulit buah jeruk lemon digunakan dalam membuat roti, manisan, dan untuk menambah rasa makanan. Selain itu, kulit buah ini juga berfungsi untuk mencegah kanker (Nuraini, 2011).
2.1.3 Jeruk Purut
2.1.3.1 Sistematika Tumbuhan
Divisi : Spermatophyta Subdivisi : Angiospermae Kelas : Dicotyledoneae
Ordo : Rutales
Suku : Rutaceae
Genus : Citrus
Spesies : Citrus hystrix DC. (Nuraini, 2011). 2.1.3.2 Sinonim Tumbuhan
Sinonim Citrus paeda Miq. (Nuraini, 2011). 2.1.3.3 Nama Daerah
2.1.3.4 Nama Asing
Kaffir lime leaf and zest (Inggris), bai magrut, kabuyao, percupin orange, citron combara (Nuraini, 2011).
2.1.3.5 Daerah Tumbuh
Jeruk purut bisa tumbuh pada daerah dengan ketinggian antara 0-1000 dpl. Jeruk tersebut bisa ditanam didaerah sangat basah atau daerah basah (Setiadi dan Parimin, 2004).
2.1.3.6 Morfologi Tumbuhan
Citrus hystrix D.C. termasuk tumbuhan berkayu, merupakan pohon dengan tinggi 5-7,5 m. Batang tegak, bulat, berduri, hijau kotor. Daun tunggal, berseling, lonjong, tepi beringgit, ujung meruncing, pangkal membulat, panjang 4-5,5 cm, lebar 2-2,5 cm. Buah bulat, diameter 4-5 cm, permukaan berkerut, hujau. Biji bulat telur, putih. Daging buah hijau, rasanya sangat asam sangat pahit (Nuraini, 2011).
2.1.3.7 Kandungan Kimia
Kandungan flavonoid pada kulit jeruk purut, terutama naringenin dan hesperidin bersifat sebagai antioksidan (Anonimc, 2012).
2.1.3.8 Kegunaan
Kulit buah jeruk purut dapat digunakan sebagai penyedap masakan dan antiseptik (Nuraini, 2011).
2.1.4 Jeruk Bali
2.1.4.1 Sistematika Tumbuhan
Kelas : Dicotyledoneae
Ordo : Rutales
Suku : Rutaceae
Genus : Citrus
Spesies : Citrus maxima (Burm.) Osbeck (Nuraini, 2011). 2.1.4.2 Sinonim Tumbuhan
Sinonim Citrus Celebia Citrus decumanus L.
Citrus grandis (Nuraini, 2011). 2.1.4.3 Nama Daerah
Indonesia: Jeruk bali, jeruk besar, jeruk cikoneng, jeruk limau makan, jeruk limau besar, dan jeruk pamelo (Nuraini, 2011).
2.1.4.4 Nama Asing
Pomelo (Inggris) (Nuraini, 2011). 2.1.4.5 Daerah Tumbuh
Jeruk ini tumbuh dengan baik di dataran rendah hingga ketinggian 1000 ml dpl (Nuraini, 2011).
2.1.4.6 Morfologi Tumbuhan
daging buah merah muda. Daging buah memiliki tekstur keras sampai lunak, rasa manis sampai sedikit asam, dan berbiji sedikit (Nuraini, 2011).
2.1.4.7 Kandungan Kimia
Kulit buah jeruk bali mengandung likopen yang dapat menghambat proses oksidasi (Nuraini, 2011).
2.1.4.8 Kegunaan
Kulit buah jeruk bali berkhasiat mengobati luka, menghentikan batuk, gangguan pencernaan. Kulit buah jeruk bali dapat dimanfaatkan sebagai manisan (Nuraini, 2011).
2.2 Ekstraksi
Ekstraksi adalah suatu proses pemisahan kandungan senyawa kimia dari jaringan tumbuhan maupun hewan. Sebelum ekstraksi dilakukan biasanya bahan-bahan dikeringkan terlebih dahulu kemudian dihaluskan pada derajat kehalusan tertentu (Harborne, 1987).
Menurut Depkes RI (2000), beberapa metode ekstraksi yang sering digunakan dalam berbagai penelitian antara lain yaitu:
A. Cara dingin 1. Maserasi
dilakukan penyaringan terhadap maserat pertama dan seterusnya disebut remaserasi.
2. Perkolasi
Perkolasi adalah proses penyarian simplisia dengan pelarut yang selalu baru sampai terjadi penyarian sempurna yang umumnya dilakukan pada temperatur kamar. Proses perkolasi terdiri dari tahap pelembaban bahan, tahap perendaman antara, tahap perkolasi sebenarnya (penetesan/penampungan ekstrak) terus-menerus sampai diperoleh perkolat yang jumlahnya 1-5 kali bahan.
B. Cara panas 1. Refluks
Refluks adalah proses penyarian simplisia dengan menggunakan alat pada temperatur titik didihnya, selama waktu tertentu dan jumlah pelarut terbatas yang relatif konstan dengan adanya pendingin balik.
2. Digesti
Digesti adalah proses penyarian dengan pengadukan kontinu pada temperatur lebih tinggi daripada temperatur ruangan, yaitu secara umum dilakukan pada temperatur 40-50°C.
3. Sokletasi
Sokletasi adalah proses penyarian dengan menggunakan pelarut yang selalu baru, dilakukan dengan menggunakan alat soklet sehingga menjadi ekstraksi kontinu dengan pelarut relatif konstan dengan adanya pendingin balik.
4. Infudasi
5. Dekoktasi
Dekoktasi adalah proses penyarian dengan menggunakan pelarut air pada temperatur 90°C selama 30 menit.
2.3 Radikal Bebas
Radikal bebas adalah setiap molekul yang mengandung satu atau lebih elektron yang tidak berpasangan. Radikal bebas sangat reaktif dan dengan mudah menjurus ke reaksi yang tidak terkontrol, menghasilkan ikatan silang pada DNA, protein, lipida, atau kerusakan oksidatif pada gugus fungsional yang penting pada biomolekul ini. Perubahan ini akan menyebabkan proses penuaan. Radikal bebas juga terlibat dan berperan dalam penyebab dari berbagai penyakit degeneratif, yakni kanker, aterosklerosis, jantung koroner, katarak, dan penyakit degenerasi saraf seperti Parkinson (Silalahi, 2006).
Sifat radikal bebas yang tidak stabil menyebabkan reaksi menerima atau memberikan elektron dengan molekul sekitarnya. Kebanyakan molekul ini bukan radikal bebas melainkan makromolekul biologi seperti lipid, protein, asam nukleat, dan karbohidrat. Dengan reaksi ini timbullah reaksi radikal bebas beruntun yaitu terbentuknya radikal bebas baru yang bereaksi lagi dengan makromolekul lain (Kosasih, dkk., 2004).
Secara umum tahapan reaksi pembentukan radikal bebas adalah sebagai
Tahap inisiasi adalah tahap awal terbentuknya radikal bebas. Tahap propagasi adalah tahap perpanjangan radikal berantai, dimana terjadi reaksi antara suatu radikal dengan senyawa lain dan menghasilkan radikal baru. Tahap terminasi adalah tahap akhir, terjadinya pengikatan suatu radikal bebas dengan radikal bebas yang lain sehingga menjadi tidak reaktif lagi. Ketika proses tersebut terjadi maka siklus reaksi radikal telah berakhir (Kumalaningsih, 2006; McMurry, 2008).
2.4 Antioksidan
Antioksidan adalah senyawa yang mempunyai struktur molekul yang dapat memberikan elektronnya kepada molekul radikal bebas tanpa terganggu sama sekali dan dapat memutus reaksi berantai dari radikal bebas (Kumalaningsih, 2006).
Terdapat tiga macam antioksidan yaitu:
b. antioksidan alami yang dapat diperoleh dari tanaman atau hewan, yaitu tokoferol, vitamin C, betakaroten, flavonoid dan senyawa fenolik.
c. antioksidan sintetik, yang dibuat dari bahan-bahan kimia yaitu Butylated Hydroxyanisole (BHA) dan Butylated Hydroxytoluen (BHT) yang ditambahkan dalam makanan untuk mencegah kerusakan lemak (Kumalaningsih, 2006).
Antioksidan dalam tubuh dibedakan atas tiga kelompok, yaitu (1) antioksidan primer yang bekerja dengan cara mencegah terbentuknya radikal bebas yang baru dan mengubah radikal bebas menjadi molekul yang tidak merugikan; (2) antioksidan sekunder yang berfungsi untuk menangkap radikal bebas dan menghalangi terjadinya reaksi berantai dan (3) antioksidan tertier yang bermanfaat untuk memperbaiki kerusakan biomolekuler yang disebabkan oleh radikal bebas (Silalahi, 2006).
2.4.1 Vitamin C
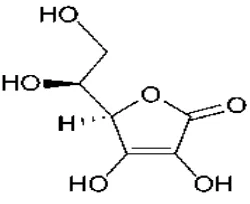
Struktur kimia vitamin C dapat dilihat pada Gambar 2.1 berikut:
Gambar 2.1 Struktur kimia vitamin C
Vitamin C merupakan suatu antioksidan penting yang larut dalam air. Vitamin C mempunyai potensi sebagai antioksidan dengan mendonorkan hidrogen dari gugus hidroksilnya kepada radikal bebas. Vitamin C juga dapat meningkatkan kekebalan tubuh terhadap infeksi dan virus. Aktivitas sistem kekebalan yang optimum memerlukan keseimbangan antara pembentukan radikal bebas dan proteksi antioksidan (Silalahi, 2006).
2.4.2 Flavonoid
Flavonoid memiliki sifat antioksidan. Senyawa ini berperan sebagai penangkap radikal bebas karena mengandung gugus hidroksil. Karena bersifat sebagai reduktor, flavonoid dapat bertindak sebagai donor hidrogen terhadap radikal bebas (Silalahi, 2006).
Kerangka flavonoid dapat dilihat pada Gambar 2.2 berikut:
Gambar 2.2 Kerangka flavonoid
Flavonoid terdapat dalam tumbuhan sebagai campuran dari flavonoid yang berbeda golongan dan jarang sekali dijumpai hanya flavonoid tunggal. Flavonoid pada tumbuhan terdapat dalam berbagai bentuk struktur molekul dengan beberapa bentuk kombinasi glikosida. Untuk menganalisis flavonoid lebih baik memeriksa aglikon yang telah terhidrolisis daripada dalam bentuk glikosida dengan strukturnya yang rumit dan kompleks. Flavonoid dapat berkhasiat sebagai antioksidan, antibakteri dan antiinflamasi (Harborne, 1984).
Struktur dasar dan sistem penomoran untuk turunan flavonoid dapat dilihat pada Gambar 2.3 berikut:
Gambar 2.3 Struktur dasar flavonoid
2.5 Spektrofotometri UV-Visible
elektromagnetik pada panjang gelombang tertentu, yang diserap zat (Depkes RI, 1979).
Berdasarkan panjang gelombang spektrofotometri dibagi dua yaitu spektrofotometri ultraviolet dengan panjang gelombang 200-400 nm, digunakan untuk senyawa yang tidak berwarna dan spektrofotometri visibel (sinar tampak) dengan panjang gelombang 400-750 nm, digunakan untuk senyawa yang berwarna (Rohman, 2007).
2.6Metode Pemerangkapan Radikal 1,1-diphenyl-2-picrylhydrazyl (DPPH) 1,1-diphenyl-2-picrylhydrazil (DPPH) pertama kali ditemukan pada tahun 1922 oleh Goldschmidt dan Renn. DPPH berwarna ungu pekat seperti KMnO4, bersifat tidak larut dalam air (Ionita, 2005).
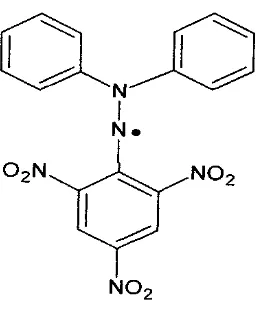
Struktur kimia radikal bebas DPPH dapat dilihat pada Gambar 2.4 berikut ini:
Gambar 2.4 Struktur kimia radikal bebas DPPH
molekul DPPH memberikan serapan maksimum pada panjang gelombang tertentu, berwarna ungu. Warna akan berubah dari ungu menjadi kuning lemah apabila elektron ganjil tersebut berpasangan dengan atom hidrogen yang disumbangkan senyawa antioksidan. Perubahan warna ini berdasarkan reaksi kesetimbangan kimia (Prakash, 2001).
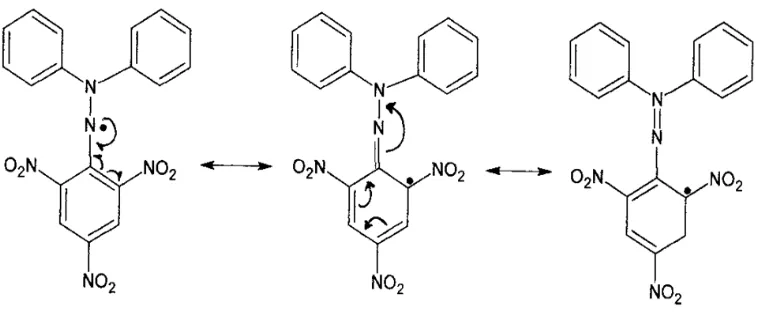
DPPH merupakan radikal bebas yang stabil karena resonansi yang dialaminya. Resonansi juga menyebabkan peningkatan kepekatan warna ungu (Molyneux, 2004).
Resonansi DPPH dapat dilihat pada Gambar 2.5 berikut ini:
Gambar 2.5 Resonansi DPPH
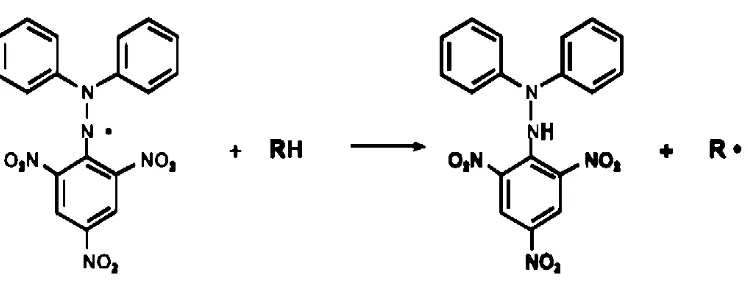
Gambar 2.6 Reaksi antara DPPH dengan atom H dari senyawa antioksidan 2.6.1 Pelarut
Metode pemerangkapan radikal 1,1-diphenyl-2-picrylhydrazyl (DPPH) akan memberi hasil yang baik dengan menggunakan pelarut metanol atau etanol dan kedua pelarut ini tidak mempengaruhi dalam reaksi antara sampel uji sebagai antioksidan dengan DPPH sebagai radikal bebas (Molyneux, 2004).
2.6.2 Pengukuran absorbansi – panjang gelombang
Panjang gelombang maksimum (λmaks) yang digunakan dalam pengukuran sampel uji sangat bervariasi. Menurut beberapa literatur panjang gelombang maksimum untuk DPPH antara lain 515 nm, 516 nm, 517 nm, 518 nm, 519 nm dan 520 nm. Apabila pengukuran menghasilkan tinggi puncak maksimum, maka itulah panjang gelombangnya yaitu sekitar panjang gelombang yang disebutkan di atas. Nilai absorbansi yang mutlak tidaklah penting, karena panjang gelombang dapat diatur untuk memberikan absorbansi maksimum sesuai dengan alat yang digunakan (Molyneux, 2004).
2.6.3 Waktu pengukuran