IDENTIFIKASI DAN PENGUKURAN KONSENTRASI PEWARNA HIJAU DALAM SAMPEL MINUMAN DENGAN ANALISIS POLA SERAPAN DAN INDEKS BIAS MENGGUNAKAN DETEKTOR EMISSION SPECTROMETER
DAN REFRAKTOMETER
SKRIPSI
Diajukan untuk Memenuhi Salah Satu Syarat
Memperoleh Gelar Sarjana Pendidikan
Program Studi Pendidikan Fisika
Oleh :
Edward Arung
NIM: 121424014
PROGRAM STUDI PENDIDIKAN FISIKA
JURUSAN PENDIDIKAN MATEMATIKA DAN ILMU PENGETAHUAN ALAM FAKULTAS KEGURUAN DAN ILMU PENDIDIKAN
UNIVERSITAS SANATA DHARMA YOGYAKARTA
LEMBAR PERSEMBAHAN
Hasil karya dan perjuanganku, kupersembahkan untuk :
Ayahku, Hendrik Arung
Ibuku, Bertha Manik
Adikku, Leonaldi dan Intan Papuana
ABSTRAK
IDENTIFIKASI DAN PENGUKURAN KONSENTRASI PEWARNA HIJAU DALAM SAMPEL MINUMAN DENGAN ANALISIS POLA SERAPAN DAN INDEKS BIAS MENGGUNAKAN DETEKTOR EMISSION SPECTROMETER
DAN REFRAKTOMETER
Telah dilakukan penelitian identifikasi dan penentuan konsentrasi pewarna hijau dalam sampel minuman dengan menggunakan Emission Spectrometer dan Refraktometer. Identifikasi dilakukan dengan membandingkan pola serapan dari larutan sampel dengan pola serapan larutan standar. Pewarna hijau Tartrazin CI 19140 dan Biru Berlian FCF CI 42090 digunakan sebagai larutan standar. Pola serapan diperoleh menggunakan Detektor Emission Spectrometer. Detektor Emission Spectrometer mengukur intensitas dari sumber cahaya pada panjang gelombang 320
– 900 nm dengan interval 1 nm. Penentuan konsentrasi dilakukan dengan analisa indeks bias sampel dengan menggunakan grafik hubungan antara indeks bias terhadap konsentrasi larutan standar. Pengukuran indeks bias dilakukan dengan menggunakan Refraktometer. Hasil penelitian menunjukkan adanya kandungan pewarna standar pada masing – masing sampel S1 sebesar (46,3 ± 2,9) mL/L, sampel S2 sebesar (96,3 ± 6,0) mL/L, sampel S3 sebesar (77,5 ± 4,8) mL/L, dan sampel S4 sebesar (65,0 ± 4,1) mL/L.
ABSTRACT
IDENTIFICATION AND CONCENTRATION MEASUREMENT OF GREEN
DYE IN A DRINK SAMPLE BASED SPECTRUM ABSORBTION AND
REFRACTIVE INDEX USING EMISSION SPECTROMETER AND REFRACTOMETER
The identification and concentration measurement of the green dye in sample using Emission Spectrometer and Refractometer has been invetigated. The identification based on absorbtion spectrum. The sample absorbtion spectrum was compared with standart. The green dye Tartrazin CI 19140 and Briliant Blue FCF CI 42090 spectrum absorbtion is used as a standart. The spectum absorbtion is measured using Emission Spectrometer. The Emission Spectrometer is a portable spectrometer designed to measure the intensity of variety light sources. The Emission Spectrometer can work on 320–900 nm wavelength range with interval 1 nm. The concentration of the green dye in sample can be determinated by analized the refraction index of sample. The refraction index is measured using Refractometer. The result show that sample S1 containing (46,3 ± 2,9) mL/L, sample S2 containing (96,3 ± 6,0) mL/L, sample S3 containing (77,5 ± 4,8) mL/L, and sampel S4 containing (65,0 ± 4,1)mL/L of green dye standart.
KATA PENGANTAR
Puji syukur kepada Tuhan Yesus Kristus atas rahmat dan berkatNya yang begitu melimpah dan cinta yang begitu luar biasa. Berkat kasih-Nya yang luar biasa melimpah, penyusunan skripsi ini dapat terselesaikan dengan baik. Karena cintanya pula skripsi yang berjudul “IDENTIFIKASI DAN PENGUKURAN
KONSENTRASI PEWARNA HIJAU DALAM SAMPEL MINUMAN
DENGAN ANALISIS POLA SERAPAN DAN INDEKS BIAS
MENGGUNAKAN DETEKTOR EMISSION SPECTROMETER DAN
REFRAKTOMETER” dapat berjalan dengan baik dan terselesaikan dengan baik. Penelitian skripsi ini merupakan salah satu syarat guna memperoleh gelar sarjana pendidikan untuk Program Studi Pendidikan Fisika Fakultas Keguruan dan Ilmu pendidikan.
Penulisan dan penelitian ini bisa terselesaikan dengan baik bukan hanya karena penulis saja, melainkan banyak pihak yang senantiasa membantu serta memberi dukungan kepada penulis. Ucapan terimakasih yang begitu dalam diucapkan kepada :
1. Dr. Ign. Edi Santosa, M.S, selaku dosen pembimbing yang senantiasa dengan tulus hati membimbing, meluangkan waktu, memotivasi, mengarahkan, mendengarkan kesulitan yang dialami tentang penelitian ini serta memberikan solusi terbaiknya.
2. Petrus Ngadiono selaku laboran yang selalu membantu dalam pengadaan alat, memberi saran terhadap kesulitan dalam pemilihan alat.
3. Ibu Sri Agustini dan bapak Severinus Domi selaku DPA yang selalu membimbing dan memantau perkembangan skripsi mahasiswanya serta ucapan terimakasih untuk dosen-dosen Pendidikan Fisika atas segala bimbingannya dalam membantu kelancaran penelitian.
4. Dosen-dosen Pendidikan Fisika yang telah membantu saya dalam perkuliahan selama 4 tahun ini.
5. Bapak dan Ibu tercinta di rumah, Hendrik Arung dan Bertha Manik yang selalu mendoakan serta memberikan kasih sayangnya dalam memberikan semangat dan dukungan kepada penulis.
DAFTAR ISI
HALAMAN JUDUL ... i
HALAMAN PERSETUJUAN PEMBIMBING ... ii
HALAMAN PENGESAHAN ... iii
LEMBAR PERSEMBAHAN ... iv
PERNYATAAN KEASLIAN KARYA ... v
LEMBAR PERNYATAAN PERSETUJUAN PUBLIKASI KARYA ILMIAH UNTUK KEPENTINGAN AKADEMIS ... vi
ABSTRAK ... vii
ABSTRACT ... viii
KATA PENGANTAR ... ix
DAFTAR ISI... xi
HALAMAN DAFTAR TABEL ... xiii
HALAMAN DAFTAR GAMBAR DAN GRAFIK ... xiv
BAB IPENDAHULUAN ... 1
F. Sistematika penelitian ... 6
BAB II DASAR TEORI ... 8
A. Teori Atom ... 8
B. Teori Molekul ... 15
C. Emission Spectrometer ... 16
D. Indeks Bias ... 17
E. Pewarna Hijau ... 19
F. Teknik Pengenceran ... 20
A. Persiapan Alat ... 21
B. Persiapan Bahan ... 25
C. Prosedur Percobaan ... 26
D. Analisa Data ... 27
BAB IV HASIL DAN PEMBAHASAN ... 30
A. Hasil Eksperimen ... 30
B. Pembahasan ... 37
BAB V PENUTUP ... 42
A. Kesimpulan ... 42
B. Saran ... 43
HALAMAN DAFTAR TABEL
Tabel 3.1 Sampel minuman berwarna hijau yang didapatkan dari berbagai
tempat ... 26
Tabel 4.2 Nilai indeks bias n untuk berbagai konsentrasi c (mL/L) larutan
standar (Tartrazin CI 19140 dan Biru Berlian FCF CI 42090). ... 33
Tabel 4.3 Nilai indeks bias sampel dan konsentrasi pewarna standar (Tartrazin
HALAMAN DAFTAR GAMBAR DAN GRAFIK
Gambar 2.1 Interaksi inti dan atom ... 3
Gambar 2.2 Peristiwa deeksitasi ... 13
Gambar 2.3 Peristiwa eksitasi ... 14
Gambar 2.4 Sketsa tingkat tenaga molekul: tingkat tenaga elektronik, tingkat
tenaga vibrasi, tingkat tenaga rotasi ... 15
Gambar 2.5 Bagan analisa kualitatif menggunakan detektor Emission
Spectrometer ... 16
Gambar 2.6 Struktur kimia Tartrazin CI 19140 ... 19
Gambar 2.7 Struktur kimia Biru Berlian FCF CI 42090 ... 19
Gambar 3.1 Susunan alat eksperimen untuk mengidentifikasi pewarna hijau
dalam sampel ... 22
Gambar 3.2 Susunan alat eksperimen untuk menentukan konsentrasi pewarna
hijau pada sampel ... 25
Grafik 4.1 Hubungan intensitas terhadap panjang gelombang (nm) larutan
standar (Tartrazin CI 19140 dan Biru Berlian FCF CI 42090), pada konsentrasi 2
Grafik 4.2Hubungan intensitas terhadap panjang gelombang (nm) larutan
pewarna standar (Tartrazin CI 19140 dan Biru Berlian FCF CI 42090) pada
konsentrasi 10 mL/L ... 32
Grafik 4.3 Hubungan indeks bias terhadap konsetrasi (mL/L) pada larutan
standar (Tartrazin Cl 19140 dan Biru Berlian FCF CI 42090) ... 34
Grafik 4.4Hubungan Intensitas terhadap panjang gelombang (nm)larutan
standar Tartrasin CI 19140 dan Biru Berlian FCF CI 42090 pada konsentrasi
10 mL/L, sampel minuman S1 pada konsentrasi 1/5x mL/L ... 35
Grafik 4.5Hubungan Intensitas terhadap panjang gelombang (nm)larutan
standar Tartrasin CI 19140 dan Biru Berlian FCF 42090 pada konsentrasi 10
mL/L (-), sampel minuman S2 pada konsentrasi 1/5x mL/L ... 47
Grafik 4.6 Hubungan Intensitas terhadap panjang gelombang (nm)larutan
standar Tartrasin CI 19140 dan Biru Berlian FCF 42090 pada konsentrasi 10
mL/L (-), sampel minuman S3 pada konsentrasi 1/5x mL/L ( - ) ... 47
Grafik 4.6 Hubungan Intensitas terhadap panjang gelombang (nm)larutan
standar Tartrasin CI 19140 dan Biru Berlian FCF 42090 pada konsentrasi 10
BAB I
PENDAHULUAN
A. Latar belakang
Seperti cabang ilmu Sains lainnya, Fisika didasarkan pada pengamatan
eksperimen dan pengukuran kuantitatif. Tujuan utama fisika adalah untuk
menemukan hukum dasar yang mengatur fenomena alam dan
menggunakannya untuk mengembangkan teori-teori yang dapat memprediksi
hasil dari percobaan berikutnya. Hukum dasar yang digunakan dalam
pengembangan teori disajikan dalam bahasa matematika, alat yang
menyediakan jembatan antara teori dan eksperimen. Fisika merupakan cabang
ilmu Sains yang fundamental dan tidak terlepas dari cabang ilmu sains lainnya
seperti Kimia. Sifat fisis dari zat kimia dapat dijelaskan dengan ilmu Fisika.
Sebagai contoh kandungan molekul dalam suatu minuman dapat ditentukan
dengan mengamati gejala – gejala fisisnya.
Pengukuran adalah kegiatan membandingkan sesuatu yang diukur dengan
alat ukurnya dan kemudian menerakan angka menurut sistem aturan tertentu.
Dalam kehidupan sehari – hari, pengukuran ini menjadi hal penting karena
dapat digunakan untuk melakukan pengecekan, misalnya pengukuran
Minuman sirup atau minuman dalam kemasan sering dijumpai di daerah
pasar ataupun di pinggiran jalan. Berbagai varian rasa dan warnanya menjadi
daya tarik tersendiri bagi masyarakat, khususnya kalangan anak – anak, untuk
membeli minuman tersebut. Untuk menarik minat konsumen, pedagang
biasanya menggunakan tambahan zat pewarna pada minuman. Namun,
terkadang kandungan kadar pewarna pada minuman sering diabaikan. Hal ini
dapat terjadi karena kurangnya pengetahuan mengenai batasan kandungan
pewarna dalam suatu larutan. Adanya kandungan pewarna yang berlebih
dalam suatu minuman dapat menyebabkan dampak negatif bagi kesehatan.
Oleh karena itu, perlu dilakukan penelitian untuk mengetahui jenis dan kadar
pewarna yang ada dalam suatu minuman.
Peraturan Menteri Kesehatan Republik Indonesia telah mengatur tentang
penggunaan bahan tambahan pada makanan. Pewarna sintetik merupakan
salah satu bahan tambahan pada makanan. Kadar maksimal dari pewarna
sintetik dalam suatu minuman sebesar 70 mg/L, untuk pewarna tunggal atau
campuran dengan warna lain, pada produk minuman yang siap konsumsi
[Permenkes RI, 1998]. Kadar ini menjadi acuan sebagai batas aman
penggunaan suatu pewarna pada minuman – minuman siap konsumsi. Salah
satu pewarna yang sering digunakan pada minuman yang dijual di pinggiran
jalan yaitu pewarna hijau. Minuman berwarna hijau didapatkan dengan
dampak buruk bagi kesehatan, seperti asma, kerusakan pada ginjal, dan juga
dapat memicu kanker.
Identifikasi dan penentuan konsentrasi suatu larutan sampel telah
dilakukan sebelumnya, yaitu identifikasi dan pengukuran konsentrasi pewarna
merah dalam suatu larutan sampel dengan menggunakan Emission
Spectrometer dan Colorimeter [Jerry, 2016]. Penelitian ini menggunakan
analisa absorbansi larutan terhadap cahaya dengan panjang gelombang
tertentu. Analisa ini tentu memerlukan pemahaman yang mendalam mengenai
fisika lanjut. Nilai konsentrasi pewarna yang didapatkan juga memiliki ralat
relatif yang cukup tinggi.
Penelitian dalam tulisan ini akan membahas tentang identifikasi dan
penenentuan konsentrasi pewarna hijau dalam beberapa sampel minuman.
Sama seperti penelitian sebelumnya, identifikasi dilakukan dengan
menggunakan alat Emission Spectrometer. Tetapi, dalam menentukan
konsentrasi pewarna pada sampel akan digunakan analisa indeks bias. Materi
mengenai indeks bias tentu sudah tidak asing lagi bagi kalangan pelajar
tingkat SMA ataupun tingkat universitas, sehingga diharapkan dapat
membantu dalam memahami mengenai penentuan konsentrasi suatu larutan
yang ditinjau dari segi Fisika.
Penelitian ini akan menyajikan metode eksperimen yang sederhana
tentang jenis serta kadar pewarna yang ada pada minuman – minuman siap
konsumsi yang banyak dijual di daerah sekitar wilayah Maguwoharjo.
B. Rumusan masalah
1. Bagaimana cara mengidentifikasi keberadaan pewarna hijau dalam larutan
sampel?
2. Bagaimana cara menentukan konsentrasi pewarna hijau dalam larutan
sampel?
3. Berapa konsentrasi pewarna hijau dalam larutan sampel?
C. Batasan masalah
Penelitian ini terbatas pada identifikasi keberadaan dan penentuan
konsentrasi dari pewarna hijau dalam larutan sampel minuman. Pewarna
standar yang digunakan merupakan pewarna hijau yang merupakan kombinasi
dari pewarna kuning Tartrazin Cl 19140 dan Biru Berlian FCF Cl 42090.
Sampel merupakan minuman yang berwarna hijau siap komsumsi yang
D. Tujuan penelitian
1. Mengetahui cara mengidentifikasi keberadaan pewarna hijau dalam
larutan sampel.
2. Mengetahui cara menentukan konsentrasi pewarna hijau dalam larutan
sampel.
3. Dapat menetukan konsentrasi pewarna hijau dalam larutan sampel.
E. Manfaat
Manfaat dari penelitian ini adalah sebagai berikut:
Bagi peneliti,
1. mengetahui cara mengidentifikasi keberadaan pewarna hijau dalam larutan
sampel;
2. mengetahui cara menentukan konsentrasi pewarna hijau dalam larutan
sampel;
3. menunjukkan bahwa konsentrasi suatu larutan tergantung pada niali
indeks bias dari larutan tersebut; dan
4. meningkatkan pengetahuan mengenai metode untuk menentukan
Bagi pembaca,
1. memberi informasi mengenai keterkaitan indeks bias terhadap penentuan
konsentrasi suatu larutan;
2. mengembang metode eksperimen yang dapat diterapkan pada tingkat
SMA ataupun Perguruan Tinggi;
3. meningkatkan pengetahuan mengenai jenis minuman yang mengandung
pewana hijau; dan
4. mengetahui konsentrasi pewarna hijau pada beberapa sampel yang dijual
di pinggiran jalan.
F. Sistematika penelitian
1. Bab I Pendahuluan
Bab I ini akan mengarahkan kita pada latar belakang penelitian, tujuan
penelitian, rumusan masalah, batasan masalah dalam penelitian ini,
manfaat penelitian dan sistematika penelitian.
2. Bab II Dasar Teori
Bab II akan menunjukkan teori yang digunakan dalam penelitian ini.
Dalam hal ini, Bab II berisi teori yang mendukung penelitian yaitu
mengenai medan magnet, Fluks medan magnet, hukum Lenz, dan gerak
magnet di atas konduktor.
Bab III mengarahkan prosedur penelitian yang digunakan serta
bagaimana cara menganalisa data yang telah didapatkan.
4. Bab IV Hasil dan Analisa
Bab IV menyajikan data yang telah didapatkan serta membahas data yang
telah dianalisa sebelumnya yang kemudian dicocokan dengan teori yang
digunakan.
5. Bab V Penutup
BAB II
DASAR TEORI
A. Teori Atom
Atom merupakan bagian terkecil dari suatu materi yang tidak dapat
dibagi lagi. Teori tentang atom mulai berkembang pesat sejak abad ke-19.
Model struktur atom pertama dikemukaan oleh J.J Thomson pada tahun 1897
dengan keberhasilannya mencirikan elektron dan mengukur nisbah muatan
terhadap massa (e/m) elektron. Menurut J.J Thomson elektron bermuatan
negatif dan berada dalam atom, namun secara keseluruhan atom bermuatan
netral. Dia mengusulkan bahwa atom merupakan bola pejal yang terdiri dari
elektron dan materi bermuatan positif tersebar secara merata yang dikenal
sebagai model roti kismis. Model ini disebut model atom plum pudding
[Krane, 1992].
Pada tahun 1911, Rutherford bersama kedua muridnya Hans Geiger dan
Ernest Marsden melakukan eksperimen tentang “Hamburan Sinar Alfa”.
Percobaan hamburan tersebut dilakukan dengan menembakan seberkas
pertikel � menuju selembar emas tipis. Hasil eksperimen menunjukkan
adanya ketidaksesuaian dengan model atom J.J Thomson. Partikel � (
bermuatan positif) tidak bergerak lurus menembus lempeng emas, namun
terhambur dengan berbagai sudut. Rutherford mengoreksi model Thomson
yang terkonsentrasi pada suatu daerah kecil yang disebut inti dan dikelilingi
oleh elektron. Interaksi antara inti dengan elektron dikenal sebagai gaya
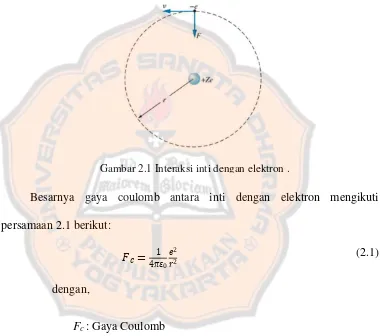
coulomb. Interaksi antara inti dan tiap elektron ditunjukan pada gambar 2.1
berikut [Krane, 1992].
Besarnya gaya coulomb antara inti dengan elektron mengikuti
persamaan 2.1 berikut:
= �� (2.1)
dengan,
Fc : Gaya Coulomb
: muatan listrik
: jarak antara dua muatan yang saling berinteraksi
� : permitivitas ruang hampa
Elektron dapat bergerak mengelilingi inti karena mengalami gaya
sentripetal. Besar gaya sentripetal mengikuti persamaan 2.2 berikut:
= � (2.2)
dengan, : Gaya sentripetal.
: massa elektron.
� : kecepatan elektron.
: jarak antara elektron terhadap inti.
Berdasarkan persamaan 2.1 dan persamaan 2.2 diperoleh persamaan 2.3
sebagai berikut:
� = ��
0 2
(2.3)
Pada tahun 1913, Niels Bohr mengemukakan bahwa atom mirip sistem
planet mini, dengan elektron-elektron beredar mengelilingi inti atom seperti
halnya planet-planet beredar mengelilingi matahari. Bohr mempostulatkan
bahwa elektron hanya dapat bergerak dalam orbit yang diperkenankan. Orbit
stabil ini disebut sebagai keadaan stasioner. Elektron bergerak pada orbit yang
meradiasi tenaga dalam bentuk gelombang elektromagnetik jika elektron
berpindah dari keadaan stasioner ke keadaan stasioner lain yang lebih rendah.
Untuk atom Hidrogen dengan jari-jari orbit r dan massa elektron m,
tenaga total sistem merupakan tenaga kinetik elektron � ditambah tenaga
potensial Coloumb � [Halliday, 1978]. Tenaga total sistem sebesar:
= + (2.4)
dengan tenaga kinetik elektron sebesar:
�= �� (2.5)
tenaga potensial elektron sebesar,
� = − �� (2.6)
sehingga tenaga total elektron menjadi,
= −8��2
0
(2.7)
Bohr menyatakan bahwa momentum sudut orbital elektron bernilai
kelipatan bulat dari ħ. Momentum sudut elektron yang beredar mengelilingi inti atom bernilai bilangan bulat dikalikan konstanta Planck dibagi dengan 2�
yang ditunjukkan dengan persamaan 2.8.
Elektron hanya berada pada orbit yang diperkenankan, dimana jari-jari
orbit menurut Bohr [Krane, 1992]:
= �� ħ = (2.9)
dengan, : jari-jari orbit elektron
ħ : tetapan Planck
: merupakan bilangan bulat 1,2,3, ...
∶ ,
Berdasarkan persamaan 2.9 dan persamaan 2.7 diperoleh
= − �2�024 ħ2 2 (2.10)
Bilangan bulat n merupakan bilangan kuantum utama. Persamaan 2.10
dapat disederhanakan mengikuti persamaan 2.11 berikut.
= − 2,6 eV (2.11)
Elektron dapat berpindah dari suatu orbit ke orbit yang lain. Bila
elektron berpindah dari orbit awal ( tingkat tenaga � ) ke orbit akhir (tingkat
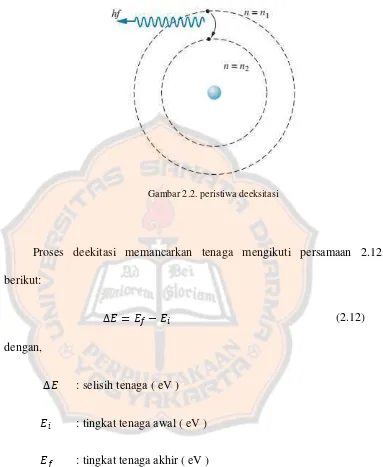
Proses deekitasi memancarkan tenaga mengikuti persamaan 2.12
berikut:
∆ = − � (2.12)
dengan,
∆ : selisih tenaga ( eV )
� : tingkat tenaga awal ( eV )
: tingkat tenaga akhir ( eV )
Tenaga dipancarkan dalam bentuk gelombang elektromagnetik
mengikuti persamaan 2.13 :
ℎ� = − (2.13)
dengan,
h : tetapan Planck sebesar 6,63 x 10-34 J.s
v : frekuensi gelombang elektromagnetik ( Hz )
Sebaliknya, elektron berpindah dari orbit awal ( tingkat tenaga � ) ke orbit
akhir (tingkat tenaga ) dengan �< seperti ditunjukkan pada gambar 2.3.
Proses eksitasi menyerap tenaga mengikuti persamaan 2.14 berikut:
∆ = − � (2.14)
B. Teori Molekul
Molekul dapat menyerap dan memancarkan tenaga seperti pada atom.
Molekul memiliki tiga tingkat tenaga yaitu tenaga elektronik, tenaga rotasi,
dan tenaga vibrasi mengikuti persamaan 2.15 berikut ini [Beiser, 1982]:
= � + �� �+ � (2.15)
Molekul selalu berusaha mencapai keadaan ke tingkat tenaga yang stabil
dengan menyerap dan melepaskan tenaga sebesar [Krane,1992]:
∆ = ℎ� = ℎ� (2.16)
Dengan, ∆ : tenaga yang diserap ( eV )
c : laju cahaya sebesar 3 x 108 m.s-1
� : panjang gelombang ( m )
Karena setiap molekul memiliki tingkat tenaga molekuler yang berbeda,
Gambar 2.4 Sketsa tingkat tenaga molekul : tingkat tenaga elektronik, tingkat tenaga vibrasi, dan tingkat tenaga rotasi
Tingkat tenaga rotasi Tingkat tenaga vibrasi
Tingkat tenaga elektronik keadaan eksitasi
Tingkat tenaga rotasi
Tingkat tenaga vibrasi
dapat dimanfaatkan dalam menentukan molekul yang terkandung dalam suatu
sampel.
C. Emission Spectrometer
Detektor Emission Spectrometer adalah detektor yang dirancang untuk
mengukur intensitas dari berabagai sumber cahaya. Detektor bekerja pada
panjang gelombang mulai dari 320 nm sampai dengan 900 nm dengan interval
1 nm. Detektor Emission Spectrometer digunakan untuk analisa kualitatif.
Analisa kualitatif dilakukan untuk mengetahui senyawa yang terkandung
dalam sampel yang akan diteliti. Analisa kualitatif dilakukan berdasarkan pola
serapan sampel. Analisa kualitatif dilakukan dengan menyusun detektor
Emission Spectrometer [Jerry, 2016] mengikuti gambar 2.6 berikut:
Analisa kualitatif menggunakan Detektor Emission Spectrometer
Setiap molekul memerlukan tenaga untuk melakukan transisi dari
tingkat awal ( �) ke tingkat tenaga akhir ( ) yang lebih tinggi. Tenaga ini
disebut tenaga eksitasi. Sinar datang dari sumber radiasi memiliki berbagai
panjang gelombang. Hal ini menunjukkan tenaga yang dibawa oleh sinar
datang juga bervariasi. Jika tenaga yang dibawa oleh sinar datang sama
Sumber Radiasi
Kuvet Dektektor Perekam dan
penampil data
dengan tenaga yang diperlukan oleh molekul untuk melakukan eksitasi maka
akan terjadi proses penyerapan tenaga. Tenaga yang dibawa oleh sinar
datang akan diserahkan kepada molekul untuk melakukan eksitasi.
Misalnya, untuk transisi molekul memerlukan cahaya dengan panjang
gelombang �, maka cahaya dari sumber dengan panjang gelombang � inilah
yang akan diserap oleh molekul. Hal ini merupakan peristiwa penyerapan
tenaga. Serapan ditunjukkan dengan berkurangnya intensitas pada panjang
gelombang tertentu. Berkurangnya intensitas pada panjang gelombang
cahaya akan menghasilkan pola tertentu. Pola inilah yang disebut sebagai
pola serapan. Pola serapan tergantung molekul penyerapnya. Pola serapan
menjadi dasar untuk mengidentifikasi molekul yang terkandung dalam
sampel. Setelah sampel dipastikan mengandung molekul yang diinginkan,
proses analisa dilanjutkan dengan analisa kuantitatif yaitu menentukan
konsentrasi molekul yang terkandung dalam sampel.
D. Indeks Bias
Indeks bias merupakan perbandingan cepat rambat cahaya pada ruang
hampa dengan cepat rambat cahaya pada medium tertentu. Kecepatan cahaya
dilambangkan dengan c sebesar 2,997 × 108 m/s pada ruang hampa. Pada
medium yang lain, nilainya akan lebih kecil dari nilai tersebut. Indeks bias
menunjukkan seberapa besar kecepatan cahaya yang berkurang pada medium
= � (2.17)
n : indeks bias
c : kecepatan cahaya pada ruang hampa
v : kecepatan cahaya pada suatu medium
Cepat rambat cahaya pada suatu medium tergantung pada medium itu
sendiri, suhu, dan panjang gelombang. Karena kebergantungan terhadap
panjang gelombang maka penelitian sering dilakukan dengan menggunakan
sinar monokromatik. Indeks bias menurut pengertian fisis adalah kemampuan
cahaya merambat dalam suatu zat berdasarkan molekul – molekul penyusun
zat tersebut. Larutan merupakan salah satu medium yang dapat dilalui oleh
cahaya. Kerapatan dari suatu larutan tergantung pada konsentrasi larutan
tersebut. Konsentrasi menunjukkan seberapa besar jumlah zat terlarut dalam
zat pelarut. Nilai konsentrasi ditunjukkan oleh kepekatan dari suatu larutan.
Semakin pekat suatu larutan maka indeks biasnya akan semakin besar
[Hidayanto, 2013; Sarojo, 2011]. Berdasarkan katerkaitan ini maka nilai
konsentrasi suatu larutan dapat ditentukan dengan menganalisa nilai indeks
E. Pewarna Hijau
Pewarna hijau merupakan perpaduan dari pewarna kuning Tartrazin Cl
19140 dan Biru Berlian FCF Cl 42090. Tartrazin merupakan pewarna kuning
sintetis yang umum digunakan sebagai pewarna makanan. Karena
kelarutannya dalam air, tartrazin umum digunakan sebagai bahan pewarna
minuman. Absorbansi maksimal senyawa ini dalam air berada pada panjang
gelombang (427±2) nm [Rajeev Jain,2003]. Tartrazin memiliki rumus empiris
C16H9N4Na3O9S2 dengan struktur kimia seperti pada gambar 2.6. Biru Berlian
adalah bahan pewarna yang dapat diberi pada makanan dan substansi lainnya
untuk mengubah warna. Zat pewarna yang memiliki rumus empiris
C37H34N2Na2O9S3 ini termasuk pewarna golongan trifenil metan, yang
merupakan tepung berwarna ungu perunggu. Bila pewarna ini dilarutkan
dalam air akan menghasilkan warna hijau kebiruan. Struktur kimia dari Biru
berlian seperti pada gambar 2.7.
Gambar 2.6. Struktur kimia Tartrazin Cl 19140
F. Teknik Pengenceran
Pengenceran dilakukan untuk mendapatkan variasi konsentrasi dari
suatu pewarna minuman. Larutan diencerkan dengan menggunakan
persamaan 2.22 berikut [Brady, 1994]:
. � = . � (2.22)
dengan, : konsentrasi larutan induk (mL/L)
� : volume larutan induk yang diambil (mL)
: konsentrasi larutan yang diinginkan (mL/L)
BAB III
METODOLOGI PENELITIAN
Penelitian ini bertujuan untuk mengidentifikasi dan menentukan
konsentrasi pewarna hijau Tartrazin Cl 19140 dan Biru Berlian FCF Cl 42090
pada larutan sampel berwarna hijau. Penelitian ini dilakukan berdasarkan
beberapa tahapan. Tahap pertama adalah persiapan alat dan sampel. Tahap
kedua adalah pengambilan data
A. Persiapan Alat
Alat yang digunakan dalam penelitian ini dibagi menjadi dua bagian.
1. Identifikasi Pewarna Hijau
Alat yang digunakan untuk mengindentifikasi keberadaan pewarna
minuman terdiri dari beberapa komponen, antara lain:
a. Sumber cahaya.
Sumber cahaya yang digunakan merupakan lampu pijar dengan
daya sebesar 40 watt.
b. Kuvet
berinteraksi dengan larutan. Kuvet yang digunakan dapat
menampung sampel dengan ketebalan 10 mm. Kuvet berisi larutan
standar sebagai acuan atau sampel.
c. Detektor
Detektor yang digunakan adalah Emissions Spectrometer buatan
Vernier. Detektor Emissions Spectrometer bekerja pada panjang
gelombang 320 nm sampai 900 nm dengan interval 1 nm.
d. Komputer
Komputer digunakan untuk merekam, menampilkan, dan
menganalisa data. Komputer dilengkapi dengan Software Logger Pro
version 3.12.
Alat dirangkai seperti gambar 3.1 berikut.
A
C
B
PC E
Keterangan gambar
A : sumber cahaya lampu pijar D : Komputer
B : kuvet E : Ruang gelap
C : detekor Emission Spectrometer
Sebuah lampu pijar A dengan daya 40 watt, kuvet B, dan
detektor Emission Spectrometer D disusun seperti pada gambar 3.1.
Ruang gelap E digunakan untuk mengatasi pengaruh cahaya luar.
Sehingga berkas cahaya yang sampai ke detektor merupakan berkas
cahaya dari sumber cahaya. Cahaya dengan panjang gelombang �
memiliki intensitas awal . Berkas cahaya ditembakkan menuju kuvet
yang berisi larutan standar. Setelah melewati larutan, berkas cahaya ini
langsung menuju detektor. Detektor mengukur intensitas cahaya setelah
melewati larutan. Serapan akan ditunjukkan dengan berkurangnya
intensitas cahaya setelah melewati larutan pada panjang gelombang �.
Berkurangnya intensitas cahaya pada panjang gelombang � akan
menghasilkan pola serapan. Pola serapan digunakan untuk
mengidentifikasi keberadaan jenis pewarna hijau dalam sampel. Detektor
dihubungkan ke komputer PC dengan menggunakan kabel penghubung
USB. Untuk pengambilan dan perekaman data digunakan PC yang
2. Penentuan konsentrasi Pewarna Hijau
Alat yang digunakan untuk menentukan konsentrasi pewarna hijau
pada larutan sampel terdiri :
1. Pipet Tetes
Pipet tetes digunakan untuk memindahkan sampel dalam volume yang
kecil.
2. Gelas Ukur
Gelas ukur yang digunakan memiliki resolusi 0,5 mL.
3. Lampu Penerang
Lampu penerang yang digunakan merupakan lampu LED dari
smartphone Hi-Max.
4. Refraktometer
Refraktometer yang digunakan dapat mengukur indeks bias cairan
dengan indeks bias 1,300 – 1,700 dengan ketelitian 0,001 dan
presentase padatan 0 – 95%.
Alat dirangkai seperti pada gambar berikut 3.2.
A
B
Keterangan gambar:
Persiapan bahan dilakukan dengan dua tahap yaitu dengan pengenceran
larutan standar dan persiapan sampel.
1. Larutan Standar
Larutan standar merupakan pewarna hijau yang didapatkan dari
kombinasi pewarna kuning Tartrazin CI 19140 dan biru berlian FCF CI
42090. Larutan standar dibuat dengan konsentrasi yang berbeda yaitu 100
mL/L, 80 mL/L, 60 mL/L, 40 mL/L, dan 20 mL/L. Larutan standar
dengan konsentrasi 80 mL/L sebanyak 10 ml diperoleh dengan cara
mengambil larutan induk dengan konsentrasi 100 mL/L sebanyak 8 ml
yang ditambahkan aquades hingga volume menjadi 10 ml. Larutan
standar dengan konsentrasi 60 mL/L sebanyak 10 ml diperoleh dengan
cara mengambil larutan induk dengan konsentrasi 100 mL/L sebanyak 6
ml kemudian ditambah aquades hingga volume menjadi 10 ml dan
seterusnya. Larutan standar dengan konsentrasi berbeda untuk pewarna
2. Persiapan Sampel
Sampel merupakan minuman siap konsumsi yang didapatkan dari
pedagang di tempat yang berbeda.
Tabel 3.1 sampel minuman berwarna hijau yang didapatkan dari berbagai
tempat.
Sampel Keterangan
S1 Sampel didapatkan dari sekitar Pasar Stan
S2 Sampel didapatkan dari sekitar Jl. Kanigoro
S3 Sampel didapatkan dari daerah di depan Stadion
Maguwoharjo
S4 Sampel didapatkan dari daerah di depan Stadion
Maguwoharjo
S5 Sampel didapatkan dari daerah di Jl. Tasura
C. Prosedur Percobaan
Eksperimen dilaksanakan dalam dua tahap sebagai berikut:
1. Penentuan pola serapan sampel menggunakan Emission Spectrometer
a. Menempatkan larutan standar atau sampel ke dalam kuvet
b. Meletakkan kuvet yang berisi larutan standar atau sampel di antara
sumber cahaya dan detektor Emission Spektrometer.
c. Mengatur posisi lampu pijar, kuvet, dan detektor menjadi satu garis
d. Melakukan perekaman data menggunakan PC yang sudah dilengkapi
dengan software Logger Pro 3.12.
e. Membandingkan pola serapan sampel dengan pola serapan larutan
standar pewarna hijau. Pola serapan ditunjukkan dengan nilai
intensitas yang melewati larutan sampel pada panjang gelombang 320
nm sampai 900 nm dengan interval panjang gelombang 1 nm.
2. Pengukuran indeks bias sampel menggunakan Refraktometer
a. Meneteskan sampel pada plan kaca refraktometer
b. Mengatur posisi lampu penerang sehingga berada di depan
Refraktometer.
c. Mencatat nilai indeks bias yang diukur dengan Refraktometer.
d. Menganalisa nilai konsentrasi pewarna hijau dengan grafik hubungan
antara indeks bias terhadap konsentrasi pewarna hijau.
D. Analisa Data
1. Identifikasi Pewarna Hijau
Identifikasi pewarna hijau dalam larutan sampel dilakukan dengan
analisa kualitatif. Analisa ini dilakukan dengan membandingkan pola
serapan larutan standar dengan pola serapan sampel. Adanya penyerapan
ditandai dengan penurunan intensitas cahaya pada panjang gelombang
menggunakan Emission Spectrometer. Pola serapan larutan standar
didapatkan dengan mengukur intensitas cahaya yang dilewatkan pada
larutan standar. Pola serapan sampel didapatkan dengan mengukur
intensitas cahaya yang dilewatkan pada larutan sampel. Pola serapan
didapatkan dalam bentuk grafik hubungan antara intensitas terhadap
panjang gelombang. Sampel dikatakan mengandung pewarna standar jika
pola serapannya sama atau mengikuti pola serapan yang dihasilkan oleh
larutan standar.
2. Penentuan Konsentrasi Pewarna Hijau
Penentuan konsebtrasi pewarna hijau dalam sampel dilakukan dengan
analisa kuantitatif. Nilai indeks bias larutan standar akan diukur pada
berbagai nilai konsentrasi. Pengukuran dilakukan dengan menggunakan
refraktometer. Hasil pengukuran dibuat dalam bentuk grafik hubungan
antara indeks bias terhadap konsentrasi larutan standar. hubungan antara
indeks bias terhadap konsentrasi pewarna standar mengikuti hubungan
persamaan (3.1) dijadikan dasar perhitungan untuk menentukan nilai
konsentrasi pewarna hijau pada sampel.
Nilai indeks bias untuk setiap sampel akan diukur dengan
refraktometer. Nilai indeks bias kemudian dianalisa dengan persamaan
(3.1). Analisa kuantitatif ini dapat berlaku jika sampel telah teridentifikasi
BAB IV
HASIL DAN PEMBAHASAN
A. Hasil Eksperimen
Pewarna hijau standar yang digunakan dalam penelitian ini yaitu kombinasi
pewarna kuning Tartrazin Cl 19140 dan Biru Berlian FCF Cl 42090.
Penelitian ini dilakukan untuk mengidentifikasi keberadaan pewarna standar
dalam suatu larutan sampel. Setelah dilakukan idenfikasi, penentuan
konsentrasi dapat dilakukan dengan analisa data.
1. Penentuan Pola Serapan Standar Pewarna Hijau
Analisa kualitatif dilakukan berdasarkan pola serapan yang dihasilkan
oleh pewarna hijau standar. Pola serapan ditunjukkan dengan grafik
hubungan antara intensitas cahaya setelah melewati larutan terhadap
panjang gelombang. Pengukuran intensitas cahaya setelah melewati
larutan dilakukan pada panjang gelombang 320 nm sampai dengan 900
nm. Hasil pengukuran intensitas larutan standar pewarna hijau standar
dengan konsentrasi 10 mL/L, 8 mL/L, 6 mL/L, 4 mL/L, dan 2 mL/L
terdapat pada tabel lampiran 1.
Nilai intensitas cahaya pada panjang gelombang 320 nm sampai 900
Grafik 4.1. Hubungan intensitas terhadap panjang gelombang (nm) larutan pewarna
hijau standar pada konsentrasi 2 mL/L (-), 4 mL/L (-), 6 mL/L (-), 8 mL/L (-), dan 10
mL/L (-).
Grafik 4.1 menunjukkan adanya penurunan nilai intensitas pada
rentang panjang gelombang tertentu. Berkurangnya nilai intensitas ini
menunjukkan adanya serapan yang terjadi pada cahaya setelah melalui
pewarna standar. Untuk tiap larutan standar terlihat bahwa terjadi serapan
pada rentang panjang gelombang tertentu. Semakin besar konsentrasi
larutan standar maka rentang panjang gelombang serapannya makin besar.
Adanya wilayah serapan ini yang kemudian disebut sebagai pola serapan.
Salah satu pola serapan dijadikan sebagai pola standar atau acuan
sebagai pembanding untuk menganalisa pola serapan pada sampel. pola
Grafik 4.2. Hubungan intensitas terhadap panjang gelombang (nm) larutan pewarna
hijau standar pada konsentrasi 10 mL/L (-).
Grafik ini merupakan dasar untuk mengidentifikasi sampel. Sampel
dikatakan mengandung jenis pewarna hijau standar jika pola serapannya
mengikuti pola serapan pewarna standar.
2. Pengukuran Indeks Bias Larutan Standar Pewarna Hijau standar
untuk Berbagai Konsentrasi
Pengukuran indeks bias terhadap larutan standar dilakukan dengan
menggunakan Refraktometer. Pengukuran nilai indeks bias untuk berbagai
konsentrasi larutan standar digunakan untuk melihat hubungan antara nilai
indeks bias terhadap konsentrasi larutan standar. Berdasarkan hubungan
Tabel 4.2 Nilai indeks bias n untuk berbagai nilai konsentrasi c (mL/L) larutan pewarna
hijau standar .
Hasil pengukuran nilai indeks bias untuk berbagai konsentrasi sejalan
dengan keterkaitan antara kepekatan larutan dan nilai indeks bias. Tabel
4.2 menunjukkan bahwa semakin besar nilai konsentrasi larutan pewarna
standar maka semakin besar pula nilai indeks biasnya
Dari tabel 4.2 diperoleh grafik hubungan antara indeks bias terhadap
konsentrasi seperti pada grafik 4.2 berikut ini.
No Konsentrasi C ( mL/L ) Indeks Bias n
1 20 1,334
2 40 1,337
3 60 1,340
4 80 1,343
Grafik 4.3. Hubungan indeks bias terhadap konsetrasi (mL/L) pada larutan pewarna hijau
standar .
Persamaan grafik hubungan indeks bias terhadap konsentrasi tersebut
mengikuti persamaan (3.1). Grafik 4.3 digunakan untuk menentukan
konsentrasi pewarna hijau standar dalam larutan sampel. Grafik ini dapat
digunakan pada jangkauan nilai indeks bias antara 1,334 – 1,347. Untuk
nilai ideks bias sampel yang lebih besar atau di luar jangkauan, perlu
dilakukan pengenceran sehingga nilai indeks biasnya berada pada
jangkauan. Nilai konsentrasinya dapat ditentukan dengan persamaan
n = 1,6 × 10-4 c + 1,3306 (4.2)
3. Hasil Pengukuran Sampel
Identifikasi dilakukan dengan membandingkan pola serapan sampel
hasil pengukuran dengan pola serapan standar. Serapan terhadap cahaya
ditunjukkan dengan adanya penurunan nilai intensitas pada pajang
gelombang tertentu setelah melalui larutan. Pengukuran pola serapan
sampel dilakukan menggunakan Emission Spectrometer. Untuk
mendapatkan pola serapan yang mengikuti pola serapan larutan standar,
dilakukian pengenceran terhadap sampel sehingga didapatkan pola
serapan sampel yang sesuai.
Hasil identifikasi pola serapan pada sampel S1 dibandingkan dengan
pola serapan pada larutan standar ditunjukkan pada grafik 4.4.
Grafik 4.4 Hubungan Intensitas terhadap panjang gelombang (nm)larutan pewarna hijau standar pada konsentrasi 10 mL/L (-), sampel minuman S1 pada konsentrasi 1/5x mL/L ( - ).
Pola serapan sampel S1 didapatkan setelah melakukan pengenceran
terhadap sampel S1. Sampel S1 sebanyak 1 mL diencerkan dengan
pelarut aquades sehingga volumenya menjadi 5 mL/L. Pada Grafik 4.4
terlihat pola serapan sampel S1 hasil pengenceran (-) mengikuti pola
menggunakan persamaan (2.22) dapat ditentukan nilai konsentrasi
pewarna hijau standar yang terkandung dalam sampel sebesar 50 mL/L.
Perhitungan ini berlaku jika pola serapan larutan standar berhimpit
dengan pola serapan yang dihasilkan oleh sampel. Dalam penelitian ini,
pengukuran konsentrasi dilakukan dengan analisa indeks bias pada
larutan sampel.
Pengukuran nilai konsentrasi pada larutan sampel dilakukan secara
langsung tanpa melakukan pengenceran. Pengukuran dilakukan dengan
menggunakan refraktometer. Hasil pengukuran nilai indeks bias untuk
sampel minuman S1 adalah 1,338. Berdasarkan hasil perhitungan
menggunakan persamaan (3.1), diperoleh nilai konsentrasi pewarna hijau
standar yang terkandung dalam minuman S1 adalah
c = (46,3 ± 2,9) mL/L
Nilai konsentrasi pewarna hijau standar yang terkandung dalam
sampel dengan menggunakan persamaan (2.22) dan persamaan (3.1)
menunjukkan nilai yang hampir sama. Pola serapan yang dihasilkan oleh
sampel tidak selalu berhimpit dengan pola serapan larutan standar. Untuk
pola serapan yang tidak berhimpit tetapi mengikuti pola larutan standar,
perhitungan konsentrasi didapatkan dengan analisa indeks bias
Pengukuran selanjutnya dilakukan untuk sampel minuman yang
berbeda, masing – masing sampel S2, S3, dan S4 dengan cara yang sama
seperti pengukuran pola serapan dan konsentrasi. Hasil pengukuran pola
serapan dapat dilihat pada lampiran 1. Nilai hasil pengukuran konsentrasi
untuk tiap sampel ditunjukkan dalam tabel 4.3.
Tabel 4.3. Nilai indeks bias dan konsentrasi pewarna hijau standar pada tiap sampel.
No Sampel Indeks Bias (n) Konsentrasi
(mL/L)
1 S1 1,338 (46,3 ± 2,9)
2 S2 1,346 (96,3 ± 6,0)
3 S3 1,343 (77,5 ± 4,8)
4 S4 1,341 (65,0 ± 4,1)
B. Pembahasan
Penelitian ini bertujuan untuk mengidentifikasi dan menentukan
konsentrasi pewarna hijau standar dalam larutan sampel. Analisa yang
digunakan adalah analisa secara kualitatif dan kuantitatif. Analisa kualitatif
dilakukan untuk mengetahui ada tidaknya jenis pewarna hijau standar yang
adalah warna hijau yang dihasilkan dari kombinasi Tartrasin CI 19140 dan
Biru Berlian FCF 42090. Sampel merupakan minuman berwarna hijau siap
konsumsi yang dijual di pinggiran jalan. Warna hijau pada minuman belum
dapat menjamin ada tidaknya pewarna hijau standar dalam larutan sampel.
Analisa kualitatif digunakan untuk memastikan keberadaan pewarna hijau
tersebut. Analisa kuantitatif dilakukan untuk mengetahui konsentrasi pewarna
standar yang terkandung dalam sampel.
Analisa kualitatif dilakukan dengan menggunakan Detektor Emission
Spectrometer. Detektor ini dapat mengukur nilai intensitas setelah melewati
suatu larutan pada panjang gelombang cahaya tertentu. Detektor bekerja
berdasarkan serapan tenaga yang mengikuti persamaan (2.16). Detektor akan
menerima cahaya setelah melewati sampel. Hasilnya merupakan grafik
hubungan antara intensitas cahaya terhadap panjang gelombang.
Berkurangnya intensitas cahaya setelah melewati larutan ini disebabkan
adanya proses serapan tenaga. Proses serapan tenaga dilakukan oleh
molekul-molekul penyusun warna hijau pada sampel untuk melakukan transsisi
mengikuti persamaan (2.16). Hasil pengukuran intensitas cahaya terhadap
panjang gelombang akan membentuk pola tertentu. Pola ini dinamakan
sebagai pola serapan.
Pola serapan digunakan untuk melakukan identifikasi jenis pewarna
yang digunakan sebagai pembanding adalah pola serapan larutan standar pada
konsentrasi 10 mL/L yang ditunjukkan grafik 4.2. Pola inilah yang menjadi
standar sebagai pembanding untuk pola serapan sampel.
Hasil identifikasi pola serapan pada sampel dengan pembanding pola
serapan larutan standar masing – masing ditunjukkan pada garfik 4.3 untuk
sampel S1, grafik 4.4 untuk sampel S2, grafik 4.5 untuk sampel S3, dan grafik
4.6 untuk grafik S4. Untuk mendapatkan pola serapan sampel, dilakukan
pengenceran sehingga didapatkan pola yang paling sesuai dengan pola
serapan standar. Tiap grafik menunjukkan adanya kesesuaian dengan pola
serapan larutan standar sehingga dapat dikatakan terdapat larutan standar pada
sampel minuman.
Analisa kuantitatif dilakukan untuk mengetahui konsentrasi pewarna
standar yang ada di dalam sampel. Analisa kuantitatif dilakukan dengan
mengukur indeks bias dari larutan sampel. Sebelumnya, dilakukan
pengukuran nilai indeks bias untuk berbagai konsentrasi larutan standar. Dari
hasil pengukuran didapatkan adanya hubungan linear antara nilai indeks bias
terhadap konsentrasi pewarna standar yang mengikuti persamaan (4.2).
persamaan (4.2) menjadi dasar untuk perhitungan nilai konsentrasi pewarna
hijau yang terkandung dalam sampel. Pengukuran indeks bias sampel
dilakukan secara langsung tanpa melalui pengenceran. Hasil pengukuran
Grafik ini dapat digunakan untuk menentukan konsentrasi pewarna standar
pada larutan sampel jika indeks bias sampel berada pada nilai 1,334 – 1,347.
Nilai konsentrasi larutan dapat ditentukan dengan memasukkan nilai indeks
bias tiap sampel pada persamaan (4.2).
Pola serapan dari sampel yang ditunjukkan oleh grafik 4.4, 4.5, 4.6,
4.7, mengikuti pola serapan yang dihasilkan pewarna standar. Hal ini berarti
pada sampel S1, S2, S3, dan S4 terdapat kandungan pewarna hijau standar.
Nilai konsentrasi dari pewarna standar pada masing – masing sampel
kemudian dapat ditentukan dengan analisa kuantitatif. Hasil pengukuran
konsentrasi dari masing – masing sampel ditunjukkan oleh tabel 4.3.
Berdasarkan data pada tabel 4.3, diketahui bahwa sampel S1 yang didapatkan
dari dari Pasar Stan dan sampel S4 yang didapatkan dari Jl. Kanigoro
tergolong tidak aman karena melebihi takaran yang sudah ditentukan oleh
pemerintah. Sedamgkan sampel S2 dan S3 yang didapatkan dari sekitar
Stadion Maguwoharjo tergolong aman karena konsentrasinya berada di bawah
batas yang dianjurkan pemerintah.
Nilai konsentrasi pewarna hijau dalam sampel ditunjukkan dalam tabel
4.3. Nilai ini memiliki rata – rata ralat relatif sebesar 6%. Ketidakpastian ini
dapat diminimalkan dengan persamaan garis hubungan antara indeks bias
terhadap konsentrasi yang lebih baik. Artinya, dibutuhkan data konsentrasi
didapatkannya konsentrasi pewarna standar yang makin teliti. Tetapi,
pengukuran indeks bias dengan selisih konsentrasi 10 mL dengan
menggunakan refraktometer yang tersedia belum dapat menunjukkan
perbedaan nilai indeks bias. Hal ini mengakibatkan pengukuran indeks bias
berbagai konsentrasi larutan standar dilakukan untuk setiap kenaikan 20 mL
konsentrasi.
Penelitian ini juga memberikan sumbangan bagi dunia pendidikan.
Penelitian ini menyajikan metode yang sederhana dan masih jarang dilakukan
secara umum. Metode ini diharapkan dapat membantu pelajar untuk dapat
memahami tentang pengukuran konsentrasi yang ditinjau secara optis. Selain
itu, penggunaan perangkat berbasis komputer lebih memudahkan penelitian
sehingga dapat diterapkan untuk pelajar di tingkat SMA. Penggunaan alat
seperti ini diharapkan dapat menarik minat para pelajar dalam mempelajari
BAB V
PENUTUP
A. Kesimpulan
Penelitian ini dilakukan untuk mengidentifikasi dan menentukan konsentrasi
pewarna hijau standar dalam sampel minuman. Penelitian dilakukan dengan
analisa pola serapan menggunakan Detektor Emission Spectrometer dan
analisa indeks bias larutan dengan menggunakan Refraktometer. Berdasarkan
eksperimen dan hasil yang diperoleh diperoleh hasil sebagai berikut :
1. Identifikasi jenis pewarna hijau standar dilakukan dengan cara
membandingkan pola serapan yang dihasilkan sampel dengan pola
serapan yang dihasilkan oleh larutan pewarna standar standar. Pola
serapan dihasilkan oleh detektor Emission Spectrometer.
2. Sampel S1, S2, S3, dan S4, mengandung pewarna hijau standar.
3. Kosentrasi pewarna hijau standar yang digunakan pada sampel dapat
ditentukan dengan menganalisa indeks bias sampel menggunakan
perhitungan berdasarkan persamaan grafik yang diperoleh dengan
mengukur nilai indeks bias pewarna standar untuk berbagai konsentrasi.
maupun pada larutan standar dengan sumber cahaya lampu LED
Smartphone Hi Max.
4. Hasil pengukuran kosentrasi pewarna hijau pada sampel sebagai berikut:
Tabel 4.3. Nilai indeks bias dan konsentrasi pewarna hijau standar pada tiap sampel.
No Sampel Indeks Bias (n) Konsentrasi
(mL/L)
1 S1 1,338 (46,3 ± 2,9)
2 S2 1,346 (96,3 ± 6,0)
3 S3 1,343 (77,5 ± 4,8)
4 S4 1,341 (65,0 ± 4,1)
B. Saran
Beberapa hal dalam penelitian ini yang perlu diperbaiki untuk
kepentingan penelitian selanjutnya sehingga dapat semakin meningkatkan
kualitas penelitian ini. Penulis menyarankan kepada pembaca yang ingin
melanjutkan penelitian selanjutnya untuk :
1. Memperluas wilayah pengambilan sampel dan mencoba
berbeda. Hal ini dapat dilakukan untuk melakukan konfirmasi
terhadap penelitian ini.
2. Dengan adanya penelitian ini, diharapkan dapat membantu siswa
tingkat SMA atau Universitas untuk mempermudah dalam
melakukan pengukuran konsentrasi pewarna minuman. Selain itu,
DAFTAR PUSTAKA
Anggoro, C. Jerry. 2016. Identifikasi dan Pengukuran Konsentrasi Pewarna Merah
dalam Sampel Minuman Menggunakan Emission Spectrometer dan
Colorimeter. Skripsi FMIPA Universitas Sanata Dharma.
Beiser, Arthur. 1982. Konsep Fisika Modern. Jakarta: Erlangga.
Departemen Kesehatan RI. 1998. Permenkes RI No. 722/Menkes/Per/IX/1988
tentang bahan tambahan makanan (BTM).
Doebelin, Ernest O. 1992. Sistem Pengukuran Edisi ketiga (jilid 1). Jakarta: Erlangga.
Halliday dan Resnick. 1978. Fisika jilid 2 diterjemahkan oleh Pantur Silaban dan
Erwin Sucipto. Jakarta : Penerbit Erlangga.
Hidayanto, Eko. 2013. Analisis Korelasi Indeks Bias dengan Konsentrasi Sukrosa
Beberapa Jenis Madu Menggunakan Portable Brix Meter. Youngster Physics
Journal vol.1, no. 5. hal 191 – 198.
Krane, K.S, 1992. Fisika Modern diterjemahkan oleh Hans J. Wospakrik. Jakarta :
Penerbit Universitas Indonesia.
Sasmoko, Y. Hari. 2008. Pengukuran Konsentrasi Carmoizine dalam Sampel
Minuman menggunakan UV-Vis Spektrofotometer SP8-400. Skripsi FST
Universitas Sanata Dharma.
Tipler. Paul A. 2001. Fisika untuk Sains dan Teknik Jilid 2. Jakarta: Erlangga.
Wenninger, John A. Canterbery, Renar C. Ewen, Mc. G. N. Jr. 2000. International
LAMPIRAN
Lampiran 1
Grafik 4.5 Hubungan Intensitas terhadap panjang gelombang (nm)larutan pewarna hijau standar pada konsentrasi 10 mL/L (-), sampel minuman S2 pada konsentrasi 1/5x mL/L ( - ).
Lampiran 2
Lampiran 3
Perhitungan untuk menentukan konsentrasi pewarna hijau standar pada larutan sampel berdasarkan indeks bias sampel yang diukur dengan Refraktometer dengan sumber cahaya LED Smartphone Hi Max.
Untuk data no.1 pada tabel 4.3 besarnya konsentrasi pewarna hijau Tartrazin Cl 19140 dan Biru Berlian FCF Cl dalam larutan sampel
1. Nilai indeks bias pada sampel: 1,338
2. Persamaan garis hubungan antara indeks bias larutan standar terhadap konsentrasi larutan standar
n = (1,6 ± 0,1 ) x 10-4 c + (1,3306 ± 0,0003) 3. Konsentrasi pewarna pada sampel
= , 8− ,, 6 6= , �/�
4. Perhitungan ralat
∆ = , 8− ,, 6 √ ,, 6 + ,, 6 ∆ = ,
5. Konsentrasi pewarna hijau standar dalam sampel
ABSTRAK
IDENTIFIKASI DAN PENGUKURAN KONSENTRASI PEWARNA HIJAU DALAM SAMPEL MINUMAN DENGAN ANALISIS POLA SERAPAN DAN INDEKS BIAS MENGGUNAKAN DETEKTOR EMISSION SPECTROMETER
DAN REFRAKTOMETER
Telah dilakukan penelitian identifikasi dan penentuan konsentrasi pewarna hijau dalam sampel minuman dengan menggunakan Emission Spectrometer dan Refraktometer. Identifikasi dilakukan dengan membandingkan pola serapan dari larutan sampel dengan pola serapan larutan standar. Pewarna hijau Tartrazin CI 19140 dan Biru Berlian FCF CI 42090 digunakan sebagai larutan standar. Pola serapan diperoleh menggunakan Detektor Emission Spectrometer. Detektor Emission Spectrometer mengukur intensitas dari sumber cahaya pada panjang gelombang 320
– 900 nm dengan interval 1 nm. Penentuan konsentrasi dilakukan dengan analisa indeks bias sampel dengan menggunakan grafik hubungan antara indeks bias terhadap konsentrasi larutan standar. Pengukuran indeks bias dilakukan dengan menggunakan Refraktometer. Hasil penelitian menunjukkan adanya kandungan pewarna standar pada masing – masing sampel S1 sebesar (46,3 ± 2,9) mL/L, sampel S2 sebesar (96,3 ± 6,0) mL/L, sampel S3 sebesar (77,5 ± 4,8) mL/L, dan sampel S4 sebesar (65,0 ± 4,1) mL/L.
ABSTRACT
IDENTIFICATION AND CONCENTRATION MEASUREMENT OF GREEN
DYE IN A DRINK SAMPLE BASED SPECTRUM ABSORBTION AND
REFRACTIVE INDEX USING EMISSION SPECTROMETER AND REFRACTOMETER
The identification and concentration measurement of the green dye in sample using Emission Spectrometer and Refractometer has been invetigated. The identification based on absorbtion spectrum. The sample absorbtion spectrum was compared with standart. The green dye Tartrazin CI 19140 and Briliant Blue FCF CI 42090 spectrum absorbtion is used as a standart. The spectum absorbtion is measured using Emission Spectrometer. The Emission Spectrometer is a portable spectrometer designed to measure the intensity of variety light sources. The Emission Spectrometer can work on 320–900 nm wavelength range with interval 1 nm. The concentration of the green dye in sample can be determinated by analized the refraction index of sample. The refraction index is measured using Refractometer. The result show that sample S1 containing (46,3 ± 2,9) mL/L, sample S2 containing (96,3 ± 6,0) mL/L, sample S3 containing (77,5 ± 4,8) mL/L, and sampel S4 containing (65,0 ± 4,1)mL/L of green dye standart.